T 6001:2012
(1)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
目 次
ページ
序文 ··································································································································· 1
1 適用範囲························································································································· 1
2 引用規格························································································································· 1
3 用語及び定義 ··················································································································· 2
4 医療機器のカテゴリ化 ······································································································· 3
4.1 接触様式によるカテゴリ化 ······························································································ 3
4.2 接触期間によるカテゴリ化 ······························································································ 4
5 生物学的評価プロセス ······································································································· 4
5.1 一般 ···························································································································· 4
5.2 試験の選択及び結果の全体評価 ························································································ 4
5.3 試験方法の選択 ············································································································· 5
5.4 試験の種類 ··················································································································· 5
5.5 生体適合性の再評価 ······································································································· 6
6 歯科材料のための試験手順 ································································································· 6
6.1 試料調製のための推奨事項 ······························································································ 6
6.2 寒天拡散試験 ················································································································ 7
6.3 フィルタ拡散試験 ········································································································· 10
6.4 歯髄・象牙質使用模擬試験 ····························································································· 13
6.5 覆髄試験 ····················································································································· 17
6.6 根管充塡使用模擬試験 ··································································································· 19
附属書A(参考)歯科用医療機器の生体適合性の評価を行う上で考慮する試験の種類 ······················· 22
附属書B(参考)象牙質バリア細胞毒性試験············································································· 23
附属書C(参考)急性毒性試験 ······························································································ 30
参考文献 ···························································································································· 31
附属書JA(参考)JISと対応国際規格との対比表 ······································································ 33
T 6001:2012
(2)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
まえがき
この規格は,工業標準化法第14条によって準用する第12条第1項の規定に基づき,日本歯科材料工業
協同組合(JDMA)及び財団法人日本規格協会(JSA)から,工業標準原案を具して日本工業規格を改正す
べきとの申出があり,日本工業標準調査会の審議を経て,厚生労働大臣が改正した日本工業規格である。
これによって,JIS T 6001:2005は改正され,この規格に置き換えられた。
この規格は,著作権法で保護対象となっている著作物である。
この規格の一部が,特許権,出願公開後の特許出願又は実用新案権に抵触する可能性があることに注意
を喚起する。厚生労働大臣及び日本工業標準調査会は,このような特許権,出願公開後の特許出願及び実
用新案権に関わる確認について,責任はもたない。
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
日本工業規格
JIS
T 6001:2012
歯科用医療機器の生体適合性の評価
Evaluation of biocompatibility of medical devices used in dentistry
序文
この規格は,2008年に第2版として発行されたISO 7405を基とし,引用規格の変更などの技術的内容
を変更して作成した日本工業規格である。
なお,この規格で点線の下線を施してある箇所は,対応国際規格を変更している事項である。変更の一
覧表にその説明を付けて,附属書JAに示す。
この規格は,歯科用医療機器(歯科材料を含む。)の生体適合性について規定する。また,この規格は,
JIS T 0993-1及びISO 10993規格群と併せて用いる。また,この規格は,歯科において適用されてきた実
績をもち,歯科用医療機器に固有の特殊性を踏まえた特徴ある試験で,十分にデータが公表されていると
みなされるものについて実施方法の詳細を含む。医療機器としての生体適合性評価のための試験方法は,
JIS T 0993-1及びISO 10993規格群に含まれているので,それらの詳細は,この規格から除外している。
さらに,試験方法を推奨するに当たって,動物の使用を最小限にすることを優先した。他の試験では要
求する評価の結果が得られないという証拠を十分慎重に検討した後に,初めて動物を使う試験の実施を決
定する。試験に要する個体数を最小限にするために,複数の試験(例えば,歯髄・象牙質使用模擬試験及
び覆髄試験)を同じ個体に同時に行うことができる。
なお,医療機器の使用に伴うリスクを評価する試験方法については,詳細には規定していない。
附属書Aは,歯科用医療機器の生体適合性の評価を行う上で考慮する試験の種類を示している。附属書
B及び附属書Cは,歯科用医療機器の生体適合性の評価において,動物の使用を更に少なくするインビト
ロ(in vitro)及びエクスビボ(ex vivo)試験の適用を推奨するためのものである。
1
適用範囲
この規格は,歯科用医療機器の生物学的影響を評価する試験方法について規定する。この規格は,試験
する医療機器の構成要素となっている薬理学的作用をもつ物質の試験も含む。
この規格は,患者の身体に直接的にも間接的にも接触しない材料及び機器の試験には適用しない。
注記 この規格の対応国際規格及びその対応の程度を表す記号を,次に示す。
ISO 7405:2008,Dentistry−Evaluation of biocompatibility of medical devices used in dentistry(MOD)
なお,対応の程度を表す記号“MOD”は,ISO/IEC Guide 21-1に基づき,“修正している”
ことを示す。
なお,平成27年2月28日までJIS T 6001:2005は適用することができる。
2
引用規格
次に掲げる規格は,この規格に引用されることによって,この規格の規定の一部を構成する。これらの
引用規格のうちで,西暦年を付記してあるものは,記載の年の版を適用し,その後の改正版(追補を含む。)
2
T 6001:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
は適用しない。西暦年の付記がない引用規格は,その最新版(追補を含む。)を適用する。
JIS R 6253 耐水研磨紙
JIS T 0993-1 医療機器の生物学的評価−第1部:リスクマネジメントプロセスにおける評価及び試験
注記 対応国際規格:ISO 10993-1:2009,Biological evaluation of medical devices−Part 1: Evaluation
and testing within a risk management process(MOD)
JIS T 14971 医療機器−リスクマネジメントの医療機器への適用
注記 対応国際規格:ISO 14971,Medical devices−Application of risk management to medical devices
(IDT)
ISO 10993-2,Biological evaluation of medical devices−Part 2: Animal welfare requirements
ISO 10993-3,Biological evaluation of medical devices−Part 3: Tests for genotoxicity, carcinogenicity and
reproductive toxicity
ISO 10993-5,Biological evaluation of medical devices−Part 5: Tests for in vitro cytotoxicity
ISO 10993-6,Biological evaluation of medical devices−Part 6: Tests for local effects after implantation
ISO 10993-10,Biological evaluation of medical devices−Part 10: Tests for irritation and skin sensitization
ISO 10993-11,Biological evaluation of medical devices−Part 11: Tests for systemic toxicity
ISO 10993-12:2007,Biological evaluation of medical devices−Part 12: Sample preparation and reference
materials
3
用語及び定義
この規格で用いる主な用語及び定義は,次による。
3.1
医療機器(medical device)
あらゆる器具,器械,装置,ソフトウェア,材料又は他の物品であって,単独使用か組合せ使用かを問
わず,製造販売業者が医療目的で人体への使用を意図し,次の目的で使用するもの。
なお,医療機器の適切な適用に必要なソフトウェアを含むものもある。
− 疾病の診断,予防,モニタリング,治療又は緩和
− 傷害又は障害の診断,モニタリング,治療,緩和又は補償
− 解剖学的構造若しくは生理学的プロセスの検査,置換又は修復
− 受胎調節
なお,体内又は体表で,薬理学的,免疫学的又は代謝的作用を主要な手段としてではなく,補助的手段
として用いるものも含む。
3.2
歯科材料(dental material)
歯科診療及び/又はその関連処置で用いるために,特別に配合,製造された材料及び/又は物質若しく
はそれらの組合せ。
3.3
最終製品(final product)
“使用される状態”にある医療機器。
注記 多くの歯科材料は,練和直後の状態で使用するため,練和直後及び硬化後の両方の状態で材料
評価を考慮することが望ましい。
3
T 6001:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
3.4
陽性対照(positive control)
規定する手順によって試験したとき,再現性のある適切な陽性又は活性反応を試験系に生じて,その手
順の妥当性を示す,十分に特性が明らかな材料及び/又は物質。陽性対照材料(positive control material)
ともいう。
3.5
陰性対照(negative control)
規定する手順によって試験したとき,再現性のある適切な陰性若しくは不活性反応,又は最小限の反応
を試験系に生じて,その手順の妥当性を示す,十分に特性が明らかな材料及び/又は物質。陰性対照材料
(negative control material)ともいう。
注記 実際には,ブランク,担体及び溶媒が陰性対照となる。
3.6
標準材料(reference material)
機器の校正,測定方法の評価又は材料の評価値の決定のための材料及び/又は物質として用いるもので
あって,十分に再現性のある確立された一つ以上の特性値を示すもの。
注記 この規格では,標準材料は,規定した手順で試験したとき,再現性のある予見できる反応を生
じて,その手順の妥当性を示す,十分に特性が明らかな材料及び/又は物質である。その反応
は,陰性又は陽性の場合がある。
4
医療機器のカテゴリ化
4.1
接触様式によるカテゴリ化
4.1.1
一般
この規格を適用する上で,歯科用医療機器をJIS T 0993-1に基づいてカテゴリに分ける。ある機器又は
材料が二つ以上のカテゴリに属し得る場合には,より厳しい試験要求の方を適用しなければならない。人
体との接触が多数回生じる場合に,どのカテゴリに当てはめるかを決めるときには,人体との接触が生じ
る期間に留意して,潜在的な累積効果を考慮しなければならない。
注記 この規格において,“歯科”という用語は,口くう(腔)顎顔面領域を含む。
4.1.2
非接触機器
非接触機器は,患者の体に直接的又は間接的に接触することはなく,JIS T 0993-1の適用外である。
4.1.3
表面接触機器
表面接触機器は,健常又は損傷皮膚の表面に接触するもの,健常又は損傷口くう(腔)粘膜の表面に接
触するもの,及び歯の硬組織(エナメル質,象牙質及びセメント質)の外表面に接触するものをいう。
注記 象牙質及びセメント質は,表面と考えられる場合がある(例えば,歯肉の退縮後の歯根露出面)。
4.1.4
体内と体外とを連結する機器
体内と体外とを連結する機器は,口くう(腔)粘膜,歯の硬組織,歯髄組織若しくは骨,又はこれらの
複合組織を貫通して接触するもので,その一部が口くう(腔)環境にさら(曝)されているものをいう。
注記 修復物の下に用いるあらゆる種類の裏装材及び裏層材もこのカテゴリに含める。
4.1.5
歯科用体内植込み機器
歯科用体内植込み機器は,次のうちの一つ又は複数に,部分的に又は完全に埋め込む,歯科用インプラ
ント及び他の歯科用体内植込み機器をいう。
4
T 6001:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
a) 軟組織(例えば,骨膜下インプラント,皮下インプラント)
b) 骨[例えば,骨内インプラント,骨(代替)補塡材]
c) 歯髄象牙質系(pulpodentinal system)(例えば,歯内療法用材料)
d) これらの組合せ(例えば,骨貫通インプラント)
4.2
接触期間によるカテゴリ化
4.2.1
一般
この規格を適用する上で,機器をJIS T 0993-1及び4.2.2〜4.2.4に規定しているように,次の接触期間に
よってカテゴリに分ける。
4.2.2
一時的接触機器
単回又は複数回使用され,その累積接触期間が,24時間以内の医療機器。
4.2.3
短・中期的接触機器
単回又は複数回使用され,その累積接触期間が,24時間を超えるが30日以内の医療機器。
4.2.4
長期的(永久)接触機器
単回又は複数回使用され,その累積接触期間が,30日を超える医療機器。
注記1 “永久”という表現は,この規格の中だけで使用し,JIS T 0993-1と一致している。
注記2 複数回接触する機器について,その機器をどのカテゴリに当てはめるかを決めるには,この
接触が生じる期間を想定して,起こり得る累積効果を考慮する。
5
生物学的評価プロセス
5.1
一般
歯科用機器はいずれも,リスクマネジメントプロセスの実施の中で,体系化された生物学的な評価プロ
グラムによる評価を受けなければならない(JIS T 0993-1を参照)。このプログラムの実施についての指針
は,JIS T 14971及びJIS T 0993-1に規定されている。生物学的な評価プログラムには,各々の機器の生物
学的性質についてのデータセットが十分そろっているかの精査を含めなければならない。生物学的な評価
プログラムでのデータセットの精査で,一つ又は複数のデータセットが不完全で,更に試験が必要である
ことが示された場合には,JIS T 0993-1及びISO 10993規格群若しくはこの規格,又はその両方に規定し
ている方法の中から,試験を選択することが望ましい。これらの規格に含まれていない試験を選択する場
合には,これらの規格に規定している試験の適用を考慮したことを示すとともに,他の試験を選択したこ
とが妥当である理由を記載しなければならない。
組合せ製品については,適用し得る他の規格と併せて,この規格によって最終製品を評価することが望
ましい。
注記1 この規格では,“組合せ製品”(combination products)とは,次の特性をもつ物質を組み込ん
でいる,又は組み込むことを意図したあらゆる種類の機器である。
a) 個別に使用する場合には,医薬品又は生物学的製品である。
b) 補助的作用によって,患者の身体に影響する。
上記の一例は,生物学的製品である成長因子を含有する骨補塡材及び骨造成材がある。
注記2 組合せ製品については,機器コンポーネントと薬理学的コンポーネントとが別々に包装され
ている場合,機器コンポーネントだけの試験結果は,参考情報になり得る。
5.2
試験の選択及び結果の全体評価
試験の選択及び結果の全体評価は,その医療機器について適切な化学的,物理学的及び生物学的データ
5
T 6001:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
に精通し,使用条件を熟知している専門家が行わなければならない。
5.3
試験方法の選択
試験方法を選択するときは,次のことを考慮しなければならない。
a) 医療機器の意図された用途
b) 医療機器が接触する可能性のある組織
c) 接触期間
選択する試験方法がこの規格に規定されていない場合には,その試験方法の選択が妥当であることを,
個々の医療機器についての報告書に記載しなければならない。また,同じカテゴリの中で複数の試験方法
が推奨されている場合には,選択する試験方法が妥当である理由を示す。
5.4
試験の種類
歯科用機器のカテゴリによって,表A.1に示す試験を用いることを考えなければならない。表A.1は,
どの種類の試験方法を用いるかを考えるためのものであり,必ずしもその種類の試験方法を行うことを強
制するものではない。表A.1に示す種類の試験を行わない場合には,その妥当性を各医療機器の試験報告
書に記載する。表A.1に示す試験の種類は,歯科用機器の生体適合性に対する評価のための枠組みである。
それぞれの種類の試験の大部分について,特定の試験方法を規定しているが,一部の医療機器については,
表A.1に示す以外の方法が適切な場合もある。
試験の種類を便宜上,次の三つのグループに分ける。
a) グループ1 このグループは,細胞毒性のインビトロ(in vitro)試験からなる。インビトロ(in vitro)
細胞毒性試験は,ISO 10993-5に規定する一般指針によらなければならない。歯科用機器に適する,
寒天拡散法及びフィルタ拡散法の詳細な試験プロトコルは,この規格に規定している。インビトロ(in
vitro)細胞毒性試験には,次のものがある。
1) 寒天拡散試験(6.2)
2) フィルタ拡散試験(6.3)
3) ISO 10993-5によって行う直接接触試験又は抽出液試験
4) 象牙質バリア細胞毒性試験(附属書B)
5) 歯スライスモデル
注記1 上記の順序は,ある方法が別の方法に優先することを示すものではない。
注記2 対象となる医療機器について,このリストに記載された全ての細胞毒性試験を実施しな
ければならないということではない。
注記3 象牙質バリア細胞毒性試験を用いることが提案され,この方法が附属書Bに記載されて
いる。もう一つの試験方法は,歯スライスモデルで,この方法について参照資料が参考
文献[22]に収録されている。
b) グループ2 このグループは,ISO 10993規格群による試験からなり,適切である場合には,特定の試
験が示されている。
1) 急性全身毒性−経口投与(ISO 10993-11)
2) 急性全身毒性−吸入投与(ISO 10993-11)
3) 亜急性及び亜慢性全身毒性−経口投与(ISO 10993-11)
4) 皮膚刺激性及び皮内反応(ISO 10993-10)
5) 遅延型過敏症(感作性)(ISO 10993-10)
6) 遺伝毒性(ISO 10993-3)
6
T 6001:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
7) 植込みによる局所的影響(ISO 10993-6)
注記1 引用規格の最新版を利用できるように,引用規格に発行年を付けていない。適切な箇条
及び細分箇条を示すには,発行年を付けた引用による。したがって,この規格を適用す
る場合には,引用規格の適切な箇条番号を調べる必要がある。
注記2 急性毒性試験の情報は,附属書Cに示されている。
注記3 ISO 10993-6によって,石灰化組織を含めて,局所植込み後のインプラント材料を評価す
るには,通常の脱灰切片に加えて非脱灰切片の検査を行うことを推奨する。
c) グループ3 このグループは,JIS T 0993-1及びISO 10993規格群では規定していない,歯科用機器に
特有の,次の試験からなる。
1) 歯髄・象牙質使用模擬試験(pulp and dentine usage test)(6.4)
2) 覆髄試験(pulp capping test)(6.5)
3) 根管充塡使用模擬試験(endodontic usage test)(6.6)
注記 歯科用インプラントシステム使用模擬試験を実施する場合には,ISO/TS 22911によること
が望ましい。
5.5
生体適合性の再評価
成分,品質及び/又は性能仕様の改良又は変更を行うときは,5.4に規定しているように,その機器の生
体適合性の再評価を行わなければならない。
6
歯科材料のための試験手順
6.1
試料調製のための推奨事項
6.1.1
一般
この推奨事項は,インビトロ(in vitro)試験のためのものであるが,他の目的にも用いることができる。
6.1.2
試料調製のための一般的な推奨事項
試料調製について,製品規格及び/又は製造販売業者の説明書を参照し,できる限り厳密にその記載に
従う。製造販売業者の説明書に従わない場合には,それが妥当である理由を説明する。試料調製について
は,試験報告書に詳細に記載しなければならない。機器の最終用途を考えて,次の因子(例えば,環境因
子)を考慮する。
a) 温度
b) 湿度
c) 露光 感光性材料の試料は,環境光によって活性化されない条件下で取り扱うことが望ましい。
d) 試料作製型の材質 試料作製型の材質,及び必要に応じて用いた分離剤が,試料の硬化を妨げないこ
とを確認する。
注記 ポリエチレン,ポリテトラフルオロエチレン(以下,PTFEという。)などの半透明又は白色
のプラスチック材料が適する。
e) 酸素ばく(曝)露 硬化中に酸素による重合阻害層が生じる材料については,硬化中は,試料を適切
に密閉する。
f)
滅菌 必要であり可能である場合には,無菌条件下で試料を作製するか,又は材料に適する方法で試
料を滅菌することが望ましい。滅菌によって材料が影響を受けないようにする(例えば,滅菌によっ
て材料から物質が溶出しない。)。
g) 細胞層又は細胞培養培地と試料接触表面積との比 細胞層又は細胞培養培地に対する試料接触表面
7
T 6001:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
積の比を記録する。試料の形状及び表面積の選択,並びに用いた細胞層又は細胞培養培地に対する試
料接触表面積の比が妥当である理由を説明する。
h) 抽出液 抽出液を必要とする場合には,ISO 10993-12の箇条10によって調製する。
6.1.3
光重合型材料のための推奨事項
光重合型材料の用途を考えて,次の因子を考慮する。
a) 試料作製型の材質 臨床での使用状態を模擬するために,試料作製型に用いる材料の反射率は,象牙
質1)の反射率にできるだけ近いことが望ましい。
注記 ポリエチレン, PTFEなどの半透明又は白色のプラスチック材料が適切である。
注1) “象牙質”は,歯に直接適用する材料の場合を想定している。
b) 光照射 できる限り臨床使用を模擬して,光重合を行うことが望ましい。実際の使用時と同じ重合レ
ベルとなるように,製造販売業者の説明書に従うことが望ましい。多くの場合,片面から重合させる
が,時には,両面からの重合が必要となる。重合方法は,材料及び/又はプロセスに特有である。完
全に重合した試料が試験に必要である場合には,型から取り出した後,試料が均質であることを確か
めることが大切である。
単一構成の材料の場合,目視したときに,空隙,亀裂又は気泡が存在しないことが望ましい。使用
した光源について記載することが望ましい(光強度,照射時間,照射光のスペクトル分布及び光源の
種類を記録することが望ましい。)。光源は,試験する材料に推奨されていること,また,正常に作動
することを確かめなければならない。
c) 酸素の遮断 光重合中に酸素による重合阻害層を生じる材料については,光重合中,透明な酸素遮蔽
材料(例えば,ポリエステルフィルム)で,型の両端を覆うことが望ましい。材料の重合後の表面仕
上げを製造販売業者が推奨している場合には,推奨の臨床的手順を用いて,試料表面を研削・研磨す
ることが望ましい。このような指定がなく,かつ,試験に必要な場合には,透明な酸素遮蔽材料に接
して硬化させた後,JIS R 6253によるP2 000研磨紙を用いて,試料の両面を研磨することが望ましい。
6.1.4
化学的に硬化する材料のための推奨事項
化学的に硬化する材料の用途を考えて,次の因子を考慮する。
a) 練和 試料の作製に当たっては,十分な量の材料を一回で,試料の作製ごとに新たに練和する。製造
販売業者が指定する場合には,それぞれの製品に指定された方法によって練和しなければならない。
b) 酸素の遮断 化学重合中に酸素による重合阻害層を生じる材料については,重合中,酸素遮蔽材料(例
えば,ポリエステルフィルム)で,型の両端を覆うことが望ましい。材料の重合後の表面仕上げを製
造販売業者が推奨する場合には,推奨の臨床的手順を用いて,試料表面を研削・研磨することが望ま
しい。このような指定がなく,かつ,試験に必要な場合には,酸素遮蔽材料に接して硬化させた後,
JIS R 6253によるP2 000研磨紙を用いて,試料の両面を研磨することが望ましい。
6.2
寒天拡散試験
6.2.1
目的
この試験は,寒天又はアガロースを通して拡散した後の試験材料の非特異的細胞毒性を検出するための
ものである。この試験方法は,寒天又はアガロース中に拡散しない溶出物には適さない。
6.2.2
細胞系
入手可能な確立された線維芽細胞系又は上皮細胞系[例えば,American Type Culture Collection(ATCC)
から入手できる(http://www.atcc.org参照)。]2)を用いる。細胞系の識別番号を報告書に明記する。必要な
場合には,用いた細胞系の説明及び呼称,並びにそれを選択した理由も報告書に明記する。
8
T 6001:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
注2) この情報は,この規格の使用者の便宜のために提供するものであって,日本工業規格がこれら
の細胞系を推奨するものではない。同等の細胞系で同じ結果が得られることを示すことができ
る場合には,その細胞系を用いてもよい。
6.2.3
培地,試薬及び器具
選択した細胞系に対して指定された培地を用い,ろ過滅菌する。また,寒天又はアガロース培地を調製
するための2倍濃度の培地を用意し,ろ過滅菌する。3 %寒天又は3 %アガロースの溶液を調製し,オート
クレーブ滅菌する。
使用直前に,0.01 mol/Lりん酸緩衝生理的塩類溶液[例えば,ダルベッコのりん酸緩衝塩類溶液3)]で,
1 %ニュートラルレッド水溶液(供給元を記録する。)の原液を100倍に希釈して,生体染色液を調製する。
ニュートラルレッド溶液は,遮光保存する。組織培養用6穴プレート(直径35 mm)又は組織培養に適す
る呼び径50〜100 mmのシャーレを用いる。
注3) この情報は,この規格の使用者の便宜のために提供するものであって,日本工業規格がこの製
品を推奨するものではない。同等の製品で同じ結果が得られることを示すことができる場合に
は,その製品を用いてもよい。
6.2.4
試料調製
6.1及び次によって試料を調製する。材料の抽出液又は材料そのものについて,ISO 10993-5のガイダン
スによって試験を行う。
a) 固体材料では,寒天重層に十分に接触できるように平らな面をもつ,直径約5 mmの円形試料を調製
する。
b) 硬化する材料では,内径5 mmで高さ2 mmのリング中に練和直後の材料を注入する。リングの材質
を試験報告書に記載する。練和直後の状態で材料を試験する場合には,材料の注入に先立って寒天の
上にリングを置く。種々の硬化時間経過後に試験する場合には,材料の表面がリングの縁と同じ高さ
になるようにリングに材料を充塡し,試験の直前まで温度37±2 ℃及び相対湿度(90±10)%の環境
で硬化するまで放置する。
注記1 リングの材質として,不活性な材料であるガラス又はPTFEが適切である。
c) 液体試料又は抽出液では,寒天の上に置かれた直径5 mmのほうけい酸マイクログラスフィルタのデ
ィスクに,液0.01 mLを吸収させる。
注記2 適切なディスクは,プレフィルタ[例えば,ミリポア社のプレフィルタ4)]から作製でき
る。
注4) “ミリポア社のプレフィルタ”は,製品のシリーズ名である。この情報は,この規格の使用
者の便宜のために提供するものであって,日本工業規格がこの製品を推奨するものではない。
同等の製品で同じ結果が得られることを示すことができる場合には,その製品を用いてもよ
い。
6.2.5
対照
陽性対照,陰性対照及び標準材料を用いる。
6.2.6
試験手順
細胞を対数増殖期の終わりまで培養する。十分な数のシャーレ中に,適切な量(例えば,100 mmのシ
ャーレに10 mL)の細胞懸濁液(2.5×105 個/mL)をピペットで注入し,体積分率5 %の二酸化炭素を加え
た飽和水蒸気の雰囲気中において,37±2 ℃で24時間培養する。別の細胞培養条件を用いた場合には,そ
れが妥当である理由を説明する。

9
T 6001:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
滅菌した寒天又はアガロースを湯浴で100 ℃に加熱した後,48 ℃まで冷却させる。寒天又はアガロー
ス1容を,新たに調製した2倍濃度の培地1容と混合し,48 ℃に加温する。
各シャーレから液体培地を吸引除去し,使用直前に調製した寒天又はアガロース・液体培地混合液10 mL
で置換する。
寒天又はアガロース・液体培地混合液を室温で固化させる(約30分間)。ニュートラルレッド溶液10 mL
を加えて,暗所に15〜20分間保つ。過剰のニュートラルレッド溶液を吸引除去する。
細胞が損傷されるおそれがあるため,ニュートラルレッドが存在するときは,培養物を遮光する。
適切な数の試験材料及び対照試料を,近接する試料の間に十分な距離(可能な場合には20 mm以上)を
空けて,各シャーレに静置する。体積分率5 %の二酸化炭素濃度を加えた飽和水蒸気の雰囲気中において,
37±2 ℃で24時間培養する。試験材料ごとに少なくとも例数4で試験する。
6.2.7
評価のパラメータ
試験材料と対照試料の周囲の脱色域を,目盛板付きの倒立顕微鏡を用いて評価し,表1及び表2に示す
評価基準によって各試料に対する脱色指数及び融解指数を決定する。
表1−脱色指数及び評価基準
脱色指数
評価基準
0
試験体の周囲及び直下のいずれにも脱色域が認められない。
1
脱色域が試験体の直下に限定される。
2
脱色域の広がりが試験体辺縁から5 mm未満
3
脱色域の広がりが試験体辺縁から5 mm以上10 mm以内
4
脱色域の広がりが試験体辺縁から10 mmを超えるが,シャ
ーレ全体には至らない。
5
シャーレ全体が脱色される。
表2−融解指数及び評価基準
融解指数
評価基準
0
細胞毒性が認められない。
1
脱色域の20 %未満の細胞融解
2
脱色域の20 %以上40 %未満の細胞融解
3
脱色域の40 %以上60 %未満の細胞融解
4
脱色域の60 %以上80 %以下の細胞融解
5
脱色域の80 %を超える細胞融解
各試験材料について脱色指数及び融解指数の中央値を求める。試験材料の4連の試験体の指数値が0〜3
の範囲にあり,それらの間で指数の差が2を超える場合には,再試験を行う。ただし,指数値に4又は5
が含まれる場合には,再試験の必要はない。
陰性抽出液を試験する場合には,試験材料だけによる指数を得るために,試験材料を含む抽出溶媒の指
数中央値から,抽出溶媒だけの指数中央値を差し引く。
陰性対照として機能する抽出溶媒に対する指数中央値が1を超える場合には,異なる抽出溶媒を用いて
再試験を行う。
注記 試験が有効な場合には,通常,陰性対照の直下に正常な細胞層が観察できる。

10
T 6001:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
6.2.8
結果の評価
試験結果の評価は,試験で得られた全ての情報,特に試験群と対照群との結果の違いを考慮して行う。
細胞応答は,少なくとも4連の試験による脱色指数及び融解指数の中央値に基づいている。細胞応答は,
表3によって各パラメータについて別個に等級付けしなければならない。
表3−細胞応答a)及び細胞毒性の判定
等級
細胞応答
判定
0
0
細胞毒性なし
1
1
軽度の細胞毒性
2
2〜3
中等度の細胞毒性
3
4〜5
強度の細胞毒性
注a) 脱色指数及び融解指数について別個に等級付ける。
評価の結果は,試験報告書の中に含めなければならない。
注記 細胞培養試験から得られたデータを解釈するには,この試験システムの限界(すなわち,細胞
毒性を示す材料が本質的に不適切なのではなく,特定の用途ごとにデータを解釈する必要があ
る。)を考慮する。
6.2.9
試験報告書
試験報告書には,採用した全ての手順の記録,得られた全ての結果及び結果の評価に必要となる他のデ
ータを含める。試験材料の調製及び適用の方法の詳細を記録し,材料のロット番号がある場合には,それ
も同時に含める。
6.3
フィルタ拡散試験
6.3.1
目的
この試験は,酢酸セルロースフィルタを通して拡散した後の試験材料の非特異的細胞毒性を検出するた
めのものである。
6.3.2
細胞系
入手可能な確立された線維芽細胞系又は上皮細胞系[例えば,American Type Culture Collection(ATCC)
から入手できる(http://www.atcc.org参照)。]2)を用いる。細胞系の識別番号がある場合にはその番号,用
いた細胞系の説明及び呼称,並びにそれを選択した理由を報告書に明記する。
6.3.3
培地,試薬及び器具
培地及び重層として用いるための寒天又はアガロースを,6.2.3によって調製する。こはく酸脱水素酵素
染色用又は非特異的加水分解酵素染色用の溶液を調製する。
こはく酸脱水素酵素染色用に,次の原液を調製する。
a) こはく酸塩溶液 こはく酸ナトリウム13.6 gを0.2 mol/Lのりん酸塩緩衝液に加えて100 mLとし,pH
7.6に調整する。
b) 塩化ニトロブルーテトラゾリウム溶液 塩化ニトロブルーテトラゾリウム100 mgを0.2 mol/Lのりん
酸塩緩衝液に加えて100 mLとし,pH 7.6に調整する。
c) フェナジンメトスルファート溶液 フェナジンメトスルファート4 mgを直前に調製した蒸留水に加
えて10 mLとする。
こはく酸塩溶液1 mL,塩化ニトロブルーテトラゾリウム溶液9 mL及びフェナジンメトスルファート溶
液1 mLを混合して染色液を調製する。
11
T 6001:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
非特異的加水分解酵素染色用に,アセトン1 mL中にフルオレセイン二酢酸5 mgを含むフルオレセイン
二酢酸の原液を調製する。使用時には,原液20 μLをりん酸緩衝生理的塩類溶液[例えば,ダルベッコの
りん酸緩衝塩類溶液3)]100 mLに加える。組織培養に適する直径60 mmのシャーレを用いる。
直径47 mm,ポアサイズ0.45 μmの酢酸セルロース及びニトロセルロースの混合エステルからなるフィ
ルタ[例えば,ミリポアHATF047005)]を用いる。
注5) ミリポアHATF04700は,市場で入手できる適切な製品の例である。この情報は,この規格の使
用者の便宜のために提供するものであって,日本工業規格がこの製品を推奨するものではない。
同等の製品で同じ結果が得られることを示すことができる場合には,その製品を使用してよい。
6.3.4
試料調製
6.1及び次によって試料を調製する。材料の抽出液又は材料そのものについて,ISO 10993-5のガイダン
スによって試験を行う。
a) 固体材料では,フィルタに十分に接触できるように平らな面をもつ,直径約5 mmの円形試料を調製
する。試料の質量は,3.5 g以下でなければならない。
b) 硬化する材料では,内径5 mmで高さ2 mmのリング中に練和直後の材料を注入する。練和直後の状
態で材料を試験する場合には,材料の注入に先立ってフィルタの上にリングを置く。種々の硬化時間
経過後に試験する場合には,材料の表面がリングの縁と同じ高さになるようにリングに材料を充塡し,
試験直前まで温度37±2 ℃及び相対湿度(90±10)%で硬化させる。試料の質量は,3.5 g以下でなけ
ればならない。
注記 リングの材質について,不活性な材料として適しているものには,ガラス又はPTFEがある。
c) 液体試料又は抽出液では,寒天の上に置いた直径5 mmのほうけい酸ミクロガラスフィルタのディス
クに,液0.01 mLを吸収させる。
注記 ディスクとして適切なものは,プレフィルタ4)から作製できる。
6.3.5
対照試料
陽性対照,陰性対照及び標準材料を用いる。
6.3.6
試験手順
試験手順は,次による。
a) 細胞を対数増殖期の終わりまで培養する。
b) 十分な数のシャーレの底に,酢酸セルロースフィルタを置き,細胞懸濁液(2.5×105 個/mL)6 mLを
各シャーレ中にピペットで注入する。体積分率5 %の二酸化炭素を混ぜた飽和湿度の雰囲気中で,37
±2 ℃で24時間培養する。別の細胞培養条件を用いた場合には,それが妥当であることの理由を説明
する。
c) 直前に調製され,48 ℃に保った寒天又はアガロース・液体培地混合液(6.2.6参照)5 mLを十分な数
のシャーレの中にピペットで注入し,室温で固化させる。
d) 酢酸セルロースフィルタが入っているシャーレから過剰の液体培地を吸引除去し,37±2 ℃のりん酸
緩衝生理的塩類溶液[例えば,ダルベッコのりん酸緩衝塩類溶液3)]でフィルタを洗って,細胞の付
着面を下に向けて寒天又はアガロースの上に静置する。
e) 3〜5個の試験試料を各シャーレ中のフィルタの上に載せて,体積分率5 %の二酸化炭素を混ぜた飽和
湿度の雰囲気中で,37±2 ℃で2時間及び24時間培養する。試料がフィルタの面と確実に密着してい
ることを確認する。2時間及び24時間のばく(曝)露後に,細胞毒性の発現を評価しなければならな
い。
12
T 6001:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
f)
各シャーレ中に一つの陽性対照と一つの陰性対照とを加える。そのほかに,試験材料を含まない細胞
単層だけの対照フィルタ,及び細胞を含まない試験材料だけの対照フィルタを用いる。抽出液を試験
する場合には,抽出溶媒だけの対照も用いる。各試験材料は,少なくとも例数4で試験する。
g) 培養後に,試料を取り除き,寒天又はアガロースからフィルタを静かに外す。次の方法A又は方法B
のいずれかの方法によって,細胞酵素活性が低下した面積を細胞化学的に評価する。
1) 方法A Barka及びAnderson [16]の方法によって,こはく酸脱水素酵素(酵素分類1.3.99.1)を検出
する。恒温保持(incubation)時間は,37±2 ℃で3時間とする。測定に先立ってフィルタを蒸留水
中で洗浄し,空気乾燥する。
注記 蒸留水で洗浄する前に,10 %中性ホルマリンで15分間細胞を固定すると,細胞がよりよ
く保持できる。
2) 方法B 4 ℃で30分間,フルオレセイン二酢酸溶液で恒温保持(incubation)することによって,
非特異的加水分解酵素を検出する。フィルタを紫外線で調べる。
6.3.7
細胞損傷の評価
細胞の損傷は,次のいずれかで評価する。
a) 脱色面積を,例えば画像解析システムによって測定する。
b) 表4に定義した等級を用いる。
表4−細胞損傷の評価基準
等級
等級付け評価基準
脱色面積
mm2
0
フィルタ全面で染色強度の差が認められな
い。
0
1
染色強度が低下した領域,又は非染色域の直
径が試料の直径(5 mm)未満
20未満
2
非染色域の直径が5〜7 mm
20〜40
3
非染色域の直径が7 mmを超える。
40を超える
注記 陰性対照試料の下のフィルタ及び細胞だけの対照フィルタは,濃青色(こはく酸脱水素酵素
を用いる場合)又は明緑色(非特異的加水分解酵素を用いる場合)で,いずれも均一に染色
されていることが望ましい。細胞なしの対照フィルタは,フィルタに対する試料の影響の可
能性を判定するために用いる。
6.3.8
結果の評価
試験結果を評価する場合には,試験で得られた全ての情報,特に試験群と対照群との結果の違いを考慮
しなければならない。表5に示すように細胞損傷指数(表4に示す等級に対応する。)によって,試験材
料の毒性を等級付ける。
表5−試験材料の毒性の評価
細胞損傷指数
評価
0
細胞毒性なし
1
軽度の細胞毒性
2
中等度の細胞毒性
3
強度の細胞毒性
13
T 6001:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
これらの評価結果は,試験報告書中に記載する。
注記 細胞培養試験から得たデータを解釈するには,この試験システムの限界(すなわち,細胞毒性
をもつ材料が本質的に不適切なのではなく,特定の用途ごとにデータを解釈する必要がある。)
を考慮する。
6.3.9
試験報告書
試験報告書には,採用した全ての手順の記録,取得した全ての結果及び結果の評価に必要な他のデータ
を含める。試験材料の調製及び適用の方法の詳細を記録し,材料のロット番号がある場合には,それも同
時に含める。
6.4
歯髄・象牙質使用模擬試験
6.4.1
目的
この試験は,歯髄及び象牙質に対する歯科材料の生体適合性を評価するためのものである。評価には,
予定する臨床使用方法に必要な手順を含む。
6.4.2
動物及び動物愛護
動物愛護は,次のいずれかによる。
a) ISO 10993-2
b) 実験動物に対する国の規制
注記1 動物は,ISO 10993-2によって飼育され,餌及び水を自由に摂取できることが望ましい。
根せん(尖)が完成し閉鎖している,健全な永久歯の歯列をもつ年齢の,一種類の非げっ
歯類哺乳動物を用いる。
サル,イヌ,フェレット(シロイタチ)又はミニブタは,適切な動物種である。特別な目的に対しては,
他の動物種が適することもある。選択する動物種の数は,動物愛護を考慮して,科学的な目的を達成する
ために必要な最小数であることが望ましい。動物種の選択について,その理由を記録する。
注記2 サル,イヌ及びミニブタは,M3以外の永久歯が全てほう(萌)出し終わっているものが
適切である。フェレットでは,犬歯だけが使用に適しているので,4本の永久犬歯がほう
(萌)出し終わっているものが適切である。
6.4.3
試験手順
6.4.3.1
動物の準備
各試験期間において,試験材料を充塡した歯を少なくとも7本提供できる数の動物を選ぶ。動物に麻酔
を行い,その後の手順は,6.4.3.2による。
6.4.3.2
歯の処置
歯の処置は,次による。
a) 歯面から歯石,歯こう(垢)などを全て除去する。体積分率3 %の過酸化水素水,続いてポピドンヨ
ード又はクロルへキシジンからなる消毒剤を塗布して,試験に用いる歯の表面を清掃し,消毒する。
十分な注水スプレー下で鋭利なバーを用いて,必要な数の頬側又は唇側のV級か(窩)洞を形成する。
残存象牙質の厚さが1.0 mm未満(好ましくは,0.5 mm未満)で,露髄しないような深さに全てのか
(窩)洞を形成する。試験材料を挿入するときに他の手順が必要でない場合には,か(窩)洞を水洗
し,綿球で乾燥する。
注記1 歯肉に著しい炎症をもつ動物の場合には,か(窩)洞形成の数日前に歯石,歯こう(垢)
などを除去し,歯肉の炎症が鎮静化するまで,更に繰り返す必要がある場合もある。
14
T 6001:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
注記2 あらかじめ校正した根管長測定器などの電気インピーダンス測定器具を用いて,か(窩)
洞形成中に残存象牙質の厚さを推測することができる。
b) 試験材料の調製は,製造販売業者が指定する方法による。試験材料の製造販売業者が,裏装材又はか
(窩)洞処理材(例えば,象牙質接着材)との併用を指定する場合には,これらの手順を追加して用
いる。
c) 各試験期間において,少なくとも7か(窩)洞を試験材料で,4か(窩)洞を陰性対照の材料で,ラ
ンダム割付けに基づいて修復する。必要な場合(注記1参照)には,各試験期間において,陽性対照
の材料で最大で4か(窩)洞を修復する。
注記1 陽性対照の材料に対するデータを既にもっている機関では,陽性反応を確認する場合を除
き,改めて試験を行う必要はない。
選択する動物種の数は,動物愛護を考慮して,科学的な目的を達成するために必要な最小数である
ことが望ましい。動物種の選択について,その理由を記録する。サル,イヌ又はミニブタを用いる場
合には,各試験期間について個体数1が望ましい。フェレットを用いる場合には,各試験期間につい
て少なくとも個体数3が望ましい。
注記2 急速硬化型の酸化亜鉛ユージノール(以下,ZOEという。)セメントは,適切な陰性対照
材料である。長期試験では,ZOEセメントを加水分解から保護することが望ましい。その
ためには,ポリカルボキシレートセメント又は従来型(自己硬化型)グラスアイオノマー
セメントの薄い層でZOEセメントを覆い,次いで酸エッチングしてコンポジットレジンで
覆う。コンポジットレジンをZOEセメントに直接接触させると,コンポジットレジンの重
合阻害が生じることに注意する。従来型グラスアイオノマーセメントを,代替の陰性対照
材料として用いることができる。
注記3 修復材料又は露髄を伴わないか(窩)洞形成であって,中程度から強度の歯髄反応を常に
起こすものは,適切な陽性対照である。
d) 術後は,少なくとも日に一度動物の状態を観察して記録する。摂食行動の変化,炎症又は感染によっ
て生じる苦痛を最小限にするために対策を講じる。術後,必要に応じて,鎮痛剤を投与することがあ
る。
6.4.3.3
スライドの作製
スライドの作製は,次による。
a) 7±2日,28±3日及び70±5日後に,試験材料を充塡した歯を少なくとも7本提供できるだけの数の
動物に麻酔剤を過剰投与,又は他の一般に容認されている物質を投与して,安楽死させる。修復物,
歯及びそれらの支持組織を検査して,全ての異常を詳しく記録する。各処置歯をその周囲の硬組織及
び軟組織とともに一つのブロックとして摘出して,適切な固定剤で固定する。
注記 摘出に先立って,安楽死させるときに固定液による組織の血管かん(灌)流をすると,より
よい固定が得られる。
b) 固定後,適切な試薬(例えば,10 %ぎ酸又はpH 7.4,0.5 mol/Lエチレンジアミン四酢酸)で歯を脱灰
し,歯の長軸方向に各か(窩)洞全長にわたって,厚さ5〜7 μmの連続切片を作製する。連続切片の
スライドを1枚おきにヘマトキシリン−エオシンで染色する。残りのスライドを,適切な細菌染色(例
えば,Brown-Brenn染色),又は細菌の検出に必要な他の染色法で染色する。
6.4.3.4
象牙質及び歯髄の評価
検査対象が試験群又は対照群のいずれであるかの情報を検査者が事前に知らされない状態で,切片を検
15
T 6001:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
査する。各連続切片に対して,か(窩)洞形成に起因する可能性のあるものを含めて,象牙質,歯髄及び
根せん(尖)周囲組織の組織学的特徴を全て詳細に記録する。連続切片から,か(窩)洞全長にわたって
均等に間隔をおいて少なくとも5枚の切片を選択し,個別に,表面組織(象牙芽細胞層,細胞希薄層,細
胞緻密層)及び残りの(より深部の)歯髄組織における炎症性細胞浸潤を,表6によって等級付けする。
表6−歯髄及び象牙質使用試験の等級付け
炎症の等級
炎症の程度
炎症性変化の内容
0
炎症なし
象牙細管によってか(窩)底とつながる,象牙質に隣接す
る歯髄組織の構造が正常である。
1
軽度の炎症
象牙細管によってか(窩)底とつながる,象牙質に隣接す
る歯髄組織内に,炎症性細胞が散在するほかは,歯髄組織
の構造が正常である。
2
中等度の炎症
象牙細管によってか(窩)底とつながる,象牙質に隣接す
る歯髄組織内に,炎症性細胞の限局的な病巣が存在する
が,正常な構造は残存している。
3
強度の炎症
象牙細管によってか(窩)底とつながる,象牙質に隣接す
る歯髄組織において,広範な炎症性細胞浸潤が見られ,正
常な構造が消失している。
4
組織のえ(壊)死
のう(膿)瘍形成,又は象牙細管によってか(窩)底とつ
ながる,象牙質に隣接する歯髄組織だけに限局されない
で,広範な炎症性細胞浸潤が見られる。
等級付けした各切片について,か(窩)底から歯髄−象牙前質界面まで直角に測定した距離及び象牙細
管の走行に沿った距離を測定して,最小残存象牙質厚さとして記録する。後者において,切片の断面が象
牙細管の切断面と一致せず,その結果,当該領域の各象牙細管が,か(窩)底から歯髄−象牙前質界面ま
での全距離を走行していない場合には,象牙細管の一般的な走行方向に沿って測定する。各試験期間につ
いて,個々の等級の総和を観察総数で除することによって,切片の両部位において炎症反応指数を求める。
製造販売業者が指定する場合には,裏装材又はか(窩)洞処理材とともに試験材料で充塡したか(窩)
洞,陰性対照で充塡したか(窩)洞,及び陽性対照で充塡したか(窩)洞について,個別にデータを示す。
陽性対照を充塡したか(窩)洞については,試験条件が同じである過去の実験からのデータを用いても
よい。さらに,試験材料及び陰性・陽性対象について,各試験期間において,か(窩)底又はか(窩)壁
に細菌を含有するか(窩)洞の数を記録する。このようにして,上記の等級に基づき各材料について,各
試験期間における炎症反応指数で表すことができるが,その指数に意味をもたせるためには,最小残存象
牙質厚さの測定値及び細菌の微小漏えい(洩)の観察量を併せて評価する必要がある。
6.4.3.5
象牙芽細胞の生存率分析(補助的評価)
象牙芽細胞生存率の組織形態計測分析のために,か(窩)底全長にわたり均等に間隔をおいて,ヘマト
キシリン−エオシンで染色した切片を少なくとも5枚選び,個々の細胞を識別でき,か(窩)洞下の歯髄
−象牙(前)質界面の全域が視野に入るように拡大して検査する。か(窩)洞下の歯髄−象牙(前)質界
面の全長方向に沿って,目盛付きレンズを用いて象牙(前)質表面の単位長さ当たりの,形態学的に健全
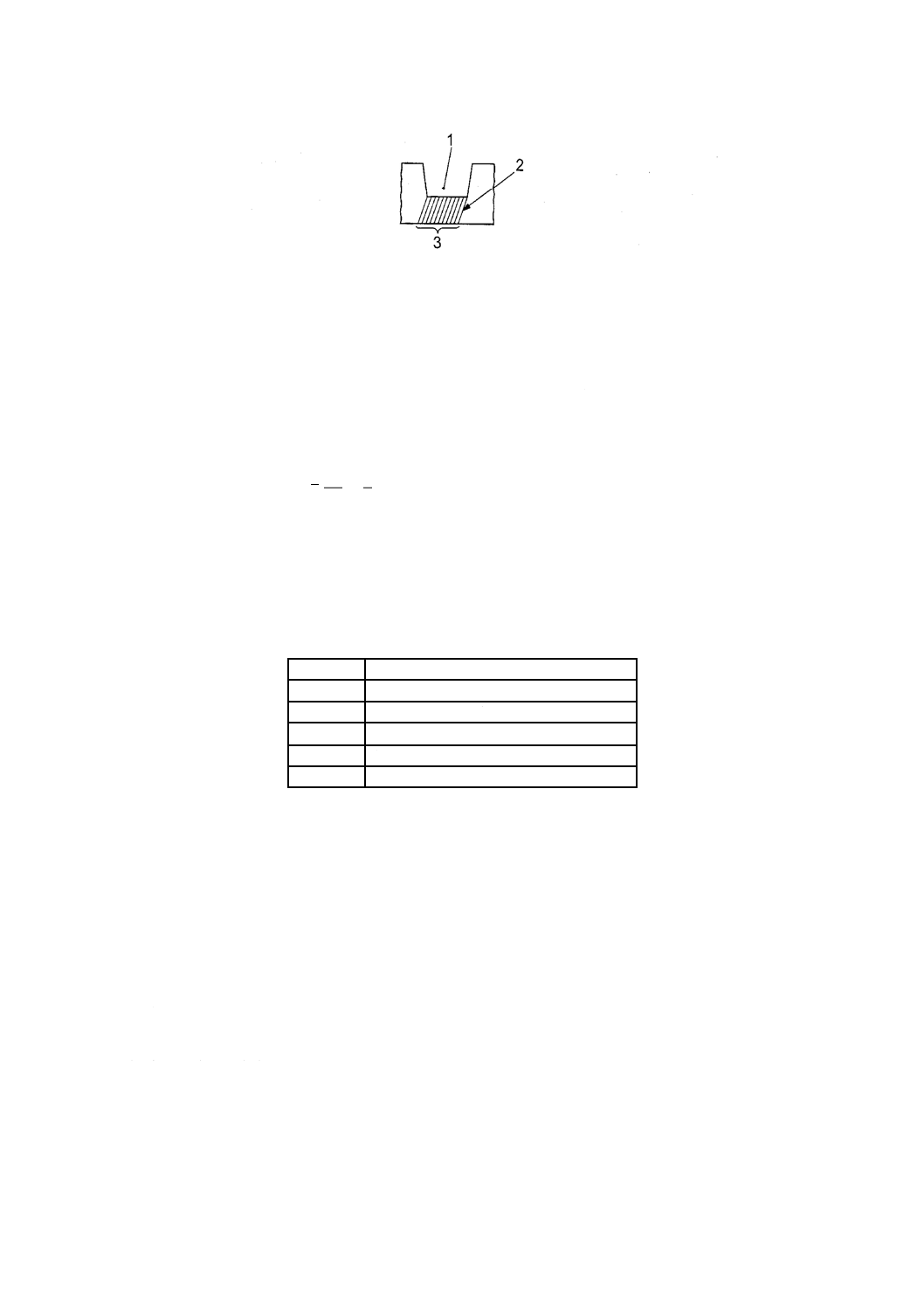
な象牙芽細胞の数を数える。その界面は,図1に示すように象牙細管がか(窩)底とつながる領域とする。
16
T 6001:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
1
か(窩)洞
2
象牙細管
3
象牙芽細胞の計数のための歯髄−象牙(前)質界面領域
図1−象牙芽細胞の計数のための歯髄−象牙(前)質界面領域
各試料から選んだ切片5枚の各々について,か(窩)洞下の歯髄−象牙(前)質界面領域の単位長さ当
たりの象牙芽細胞数を数えて,そのか(窩)洞の平均細胞数を求める。その後,全ての試験材料か(窩)
洞及び陰性対照か(窩)洞について平均細胞数を求める。細胞死の百分率は,次の式によって求める。
100
×
NC
T
NC
CD
−
=
ここに,
CD: 細胞死の百分率(%)
NC: 陰性対照か(窩)洞の細胞数
T: 試験材料か(窩)洞の細胞数
表7に規定する等級で,象牙芽細胞死を等級付けする。
表7−象牙芽細胞死の等級付け
等級
象牙芽細胞死
0
なし
1
細胞死が25 %未満
2
細胞死が25〜50 %
3
細胞死が50 %を超えて75 %以下
4
細胞死が75 %を超える
等級付けした各切片について,6.4.3.4によって最小残存象牙質厚さを記録する。このようにして,表7
に規定する等級に基づいて,各材料について象牙芽細胞生存指数を示すが,評価に影響する因子として,
その材料グループのか(窩)洞について測定した最小残存象牙質厚さを提示する。製造販売業者が推奨す
る場合には,裏装材又はか(窩)洞処理材をも含めて試験材料を充塡したか(窩)洞,及び陽性対照とし
て用いたか(窩)洞について,個別にデータを示す。上記の試験か(窩)洞と同様に,陽性対照のデータ
を陰性対照の百分率として表す。試験条件が現在の試験と同じ場合には,陽性対照のデータを過去の試験
から得てもよい。
6.4.4
結果の評価
試験結果を評価する場合には,試験で得た全ての情報,特に試験群と対照群との結果の違いを考慮する。
評価結果を試験報告書中に記録する。
6.4.5
試験報告書
結果は,試験報告書として作成する。試験報告書には,用いた全ての手順の記録,取得した全ての結果
及び結果の評価に必要となる他の資料を含める。試験材料の調製及び適用方法の詳細も,その材料のロッ
ト番号とともに報告に含める。
17
T 6001:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
6.5
覆髄試験
6.5.1
目的
この試験は,歯髄に対する覆髄材料の生体適合性を評価するために行う。評価方法には,製造販売業者
が指定する臨床使用に必要な手順を含む。
注記1 この試験は,一部を変更して断髄試験に用いることができる。
注記2 歯髄・象牙質使用模擬試験及び覆髄試験は,動物の同一個体の異なる歯を用いて,同時に実
施することができる。
6.5.2
動物及び動物愛護
動物愛護は,6.4.2による。
6.4.2によって,一種類の非げっ歯類哺乳動物を少なくとも個体数2を用いる。
6.5.3
試験手順
6.5.3.1
動物の準備
各試験期間において,試験材料を充塡する歯を少なくとも10本提供できる数の動物を選ぶ。
動物を麻酔して,6.5.3.2の処置を行う。
6.5.3.2
歯の処置
歯の処置は,次による。
a) 歯面から歯石,歯こう(垢)などを全て除去する。使用する歯を隔離するためにラバーダムを装着す
る。歯面及び手術野を清掃し,乾燥する。体積分率3 %の過酸化水素水,続いてポビドンヨード又は
クロルへキシジンからなる消毒剤を塗布して消毒する。十分な注水スプレー下で鋭利なバーを用いて,
歯冠中央部の頬側又は唇側に必要な数のⅤ級か(窩)洞を形成する。形成したか(窩)洞は,そのか
(窩)縁をエナメル質とし,近心面及び遠心面にわたり,かつ,象牙質の厚さの3分の1まで達して
いることが望ましい。質量分率0.9 %の滅菌生理食塩液をスプレーしつつ,歯髄組織内にできる限り
バーを貫通させないように,慎重にか(窩)洞中央部に直径約0.5〜1.0 mm露髄させる。露髄部の直
径は,0.1 mm単位で測定することが望ましい。露髄部の直径は,使用したバーの既知の直径から推定
できる。止血するまで,露髄部を滅菌生理食塩液で十分に洗浄する。滅菌した綿球で乾燥する。
注記 歯肉に著しい炎症がある動物の場合には,か(窩)洞形成の数日前に歯石,歯こう(垢)な
どを除去し,歯肉炎症が治まるまで,更に繰り返す必要がある。
b) 試験材料の調製については,製造販売業者が指定する方法によって行う。製造販売業者が止血又は損
傷歯髄の特定の前処理のために,他の洗浄液又は薬剤の使用を推奨している場合には,それに従う。
c) 各試験期間において,試験材料について少なくとも10か(窩)洞,適切な標準材料について5か(窩)
洞を,ランダムな配置で充塡する。微生物汚染を避けながら,練板(練和紙)上で覆髄材料及び標準
材料を練和する。圧力を加えないようにして露髄部に材料を充塡する。ポリ酸添加型コンポジットレ
ジン又はレジン添加型グラスアイオノマーセメントをか(窩)洞に充塡する。更に接着性コンポジッ
トレジンで修復することが望ましい。
選択する動物種の数は,動物愛護を考慮して,科学的な目的を達成するために必要な最小数である
ことが望ましい。動物種の選択について,その理由を記録する。サル,イヌ又はミニブタを用いる場
合には,各試験期間について,少なくとも個体数1を使用する。フェレットを用いる場合には,犬歯
だけが適合するので,各試験期間について少なくとも個体数4が望ましい。
注記1 質量分率0.9 %の滅菌生理食塩液で練和した直後のパテ状の水酸化カルシウムは,適切な
標準材料である。
18
T 6001:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
注記2 長期試験では,ZOEセメントを加水分解から保護することが望ましい。そのためには,ポ
リカルボキシレートセメント又は従来型(自己硬化型)グラスアイオノマーセメントの薄
い層でZOEセメントを覆い,次いで酸エッチングしてコンポジットレジンで覆う。コンポ
ジットレジンをZOEセメントに直接接触させると,コンポジットレジンの重合阻害が生じ
ることに注意する。
d) 6.4.3.2 d)によって動物を観察する。
6.5.3.3
スライドの作製
スライドの作製は,次による。
a) 7±2日及び70±5日後に,試験材料を充塡した歯を少なくとも10本提供できるだけの数の動物に麻
酔剤の過剰投与,又は他の一般に容認されている物質を投与して,安楽死させる。修復物,歯及びそ
れらの支持組織を検査して,全ての異常を詳しく記録する。各処置歯をその周囲の硬組織及び軟組織
とともに一つのブロックとして摘出して,適切な固定剤で固定する。
注記 摘出に先立って,安楽死させるときに固定液による組織の血管かん(灌)流をすると,より
よい固定が得られる。
b) 固定後,各組織ブロックのX線写真を撮影し,X線画像上の変化が起こっているかどうかを判定した
後,6.4.3.3 b)によって,検査のための切片を作製する。
6.5.3.4
歯髄の評価
6.4.3.4の手順によって切片を調べ,組織学的特徴を記録し,炎症性細胞浸潤を等級付けて炎症反応指数
を求める。表面の歯髄組織は,歯髄を露出させるときに,損傷しているので,評価の対象とせず,表8の
等級を用いて炎症性細胞浸潤についてだけ等級付けする。
表8−覆髄試験の等級付け
炎症の等級
炎症の程度
炎症性変化の内容
0
炎症なし
試料の組織像には炎症性変化を認めない。
1
軽度の炎症
露髄部に隣接する歯髄組織内に,炎症性細胞が
散在
2
中等度の炎症
露髄部に隣接する歯髄組織内に,炎症性細胞の
局所的小集合が存在
3
強度の炎症
露髄部に隣接する歯髄組織に,広範な炎症性細
胞浸潤
4
組織のえ(壊)
死
のう(膿)瘍形成,又は露髄部に隣接する歯髄
組織だけに限局されないで広がった炎症性細胞
浸潤
加えて,バリアとしてのデンティンブリッジの有効性を妨げる可能性がある,トンネル状欠損の存在及
び細胞包含に注意して,デンティンブリッジの形成量,分布及び性状について,十分に記載しなければな
らない。デンティンブリッジが“ない”,“部分的に存在”,“完全封鎖”の等級で,第三象牙質によって露
髄部が塞がれている度合いを等級付けする。デンティンブリッジの組織学的特徴を解釈するためのガイダ
ンスを次に注記として示す。
注記 デンティンブリッジの形成量及び形成範囲については,露髄部を完全に被覆しているか並びに
露髄部における被覆厚さ及び形成範囲について検討する。デンティンブリッジの形成が不完全
な場合には,露出した歯髄を効果的に保護できないが,逆にデンティンブリッジ形成時に無秩
19
T 6001:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
序に多量の修復象牙質が形成されると,歯髄くう(腔)が閉塞し,歯髄の活性が低下する危険
性がある。デンティンブリッジの形成範囲を超えた広範な修復象牙質の形成又は覆髄材料とつ
ながる管状構造が認められる場合には,覆髄材料に対する反応だけではなく,施術時などにお
ける損傷(例えば,外科的損傷)に対する細胞の反応があるとみなしてよい。デンティンブリ
ッジ形成中の形成不全の程度は,デンティンブリッジの象牙細管構造の規則性から知ることが
できる。細管構造の形成がない場合,又は細管構造の形成が僅かである場合には,組織の形成
中に生じた形成障害がより大きかったことを示す。デンティンブリッジ中のトンネル状の欠損
又は細胞包含は,組織形成不全を示しており,デンティンブリッジによってもたらされる正常
な透過性及び封鎖性に影響を与える可能性がある。
6.5.4
結果の評価
結果の評価は,6.4.4による。
6.5.5
試験報告書
試験報告書は,6.4.5による。
6.6
根管充塡使用模擬試験
6.6.1
目的
この試験は,根管充塡用材料と根せん(尖)部残存歯髄組織(残髄)及び根せん(尖)歯周組織との生
体適合性を評価するためのものである。評価方法には,製造販売業者が指定する臨床使用に必要な手順を
含む。
注記 根管充塡使用模擬試験は,根管充塡又は逆根管充塡に用いる歯内療法用生体活性材料,例えば,
根せん(尖)硬組織の形成促進を標榜する材料について適用する。
6.6.2
動物及び動物愛護
動物愛護は,6.4.2による。
6.4.2に規定しているように,根せん(尖)の形成が完成(閉鎖)した健全な永久歯をもつ年齢の,一種
類の非げっ歯類哺乳動物を少なくとも個体数4を用いる。切歯,犬歯及び小臼歯の使用が好ましい。2根
をもつ小臼歯を使用してもよい。
6.6.3
試験手順
6.6.3.1
動物の準備
各試験期間において,試験材料を充塡する歯を少なくとも10本提供できる数の動物を選ぶ。
注記 犬の種類によっては,根せん(尖)形態が複雑で,根管形成が困難な場合がある。
動物を麻酔して,6.6.3.2の処置を行う。
6.6.3.2
歯の処置
歯の処置は,次による。
a) 充塡する全ての歯の根せん(尖)周囲のX線写真を撮影する。6.5.3.2 a)によって歯を清掃し,隔離す
る。
注記 歯肉に著しい炎症がある動物の場合には,か(窩)洞形成の数日前に歯石,歯こう(垢)な
どを除去し,歯肉炎症が治まるまで更に繰り返す必要がある。
根管充塡材を充塡するために,必要な数の歯を用意する。無菌条件下に,鋭利なバーを用いて適切
な髄くう(腔)開拡を行う。質量分率0.9 %の滅菌生理食塩液で露髄部を洗浄し,滅菌綿球で乾燥す
る。抜髄には,新しい滅菌済み根管ファイル又は抜髄針を用い,X線写真を参考にして,根せん(尖)
孔の手前1.0±0.5 mmまで歯髄を切除する。質量分率1.5〜3.5 %の次亜塩素酸ナトリウム溶液で,続
20
T 6001:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
いて質量分率0.9 %の滅菌生理食塩液で,繰り返し根管を洗浄する。
歯髄を切断した位置までの長さに印を付けた滅菌済み根管ファイルを用いて,順次大きなサイズの
ファイルで,充塡に適する大きさになるまで根管を拡大する。象牙質切削くず(屑)が残っていると,
根せん(尖)を塞いで根管充塡材料が根せん(尖)組織に接触するのを妨げる可能性があるから,根
管から象牙質切削くず(屑)をできる限り取り除く。根管拡大処置が完了した後,質量分率1.0〜5.25 %
の次亜塩素酸ナトリウム溶液で,続いて質量分率0.9 %の滅菌生理食塩液で根管を洗浄し,滅菌済み
綿球及び大きな,先の丸い滅菌済みペーパーポイントで,根せん(尖)の残存歯髄に触れないように
して乾かす。
b) 試験材料の調製については,製造販売業者の指示に従う。製造販売業者が上記a)とは異なる歯の形成
方法を推奨する場合には,その指示に従う。
c) 各試験期間について,少なくとも10歯を試験材料で,少なくとも5歯を適切な標準材料で,ランダム
配置に基づいて充塡する。微生物汚染を避けながら,練板(パッド)上で歯内療法材料及び標準材料
を練和する。ガッタパーチャを用いて,歯髄を除去した所まで試験材料又は標準材料で根管を充塡す
る。開拡したか(窩)洞を急速硬化型ZOEセメントで塡塞し,ポリカルボキシレートセメント,従来
型(自己硬化型)グラスアイオノマーセメント又は酸エッチングで維持するコンポジットレジンで覆
う。
コンポジットレジンを用いる場合には,まず従来型(自己硬化型)グラスアイオノマーセメント又
はポリカルボキシレートセメントの薄い層でZOEセメントを覆うことが望ましい。コンポジットレジ
ンがZOEセメントに直接接触すると,コンポジットレジンの重合を阻害する可能性がある。
サル,イヌ,又はミニブタを使う場合には,各試験期間について個体数2を使用することが望まし
い。フェレットを使う場合には,各試験期間について少なくとも個体数4を使用することが望ましい。
注記 単独のZOEセメント又はGrossmanの処方によるシーラのように他の添加剤を含むZOEセメ
ントは,適切な標準材料である。
d) 6.4.3.2 d)によって動物を観察する。
6.6.3.3
スライドの作製
スライドの作製は,次による。
a) 28±3日及び90±5日後に,麻酔剤を過剰投与して,試験材料を充塡した歯を少なくとも10本提供で
きる数の動物を安楽死させる。修復物,歯及び歯の支持組織を検査して,全ての異常を詳しく記録す
る。各処置歯を,その周囲の硬組織及び軟組織とともに一つのブロックとして摘出して,適切な固定
剤で固定する。
注記 摘出に先立って,安楽死させるときに固定液による組織の血管かん(灌)流をすると,より
よい固定が得られる。
b) 固定後,各組織ブロックのX線写真を撮影し,X線画像上の変化の有無を判定する。根管及びその分
岐部を通り,歯の長軸に平行な断面で材料・歯髄組織界面及び隣接する根せん(尖)歯周組織が観察
できるように,6.4.3.3 b)によって組織切片を作製する。
6.6.3.4
組織の評価
検査対象が試験群又は対照群のいずれであるかの情報を検査者が事前に知らされない状態で切片を検査
する。各連続切片に対して,歯髄,根せん(尖)周囲組織,並びに根せん(尖)部の象牙質及びセメント
質の組織学的特徴の全てを詳細に記録する。各試料について,その組織変化を表9によって等級付けする。
考慮すべき組織学的特徴の例を,次の注記に示す。
21
T 6001:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
表9−根管充塡使用模擬試験の等級付け
等級
炎症の程度
所見
0
炎症なし
試料の組織像には炎症性変化を認めない。
1
軽度の炎症
試料の組織像は,炎症性細胞,主に慢性炎症性細胞の散在を示すが,残存歯髄の構造
的特徴は,識別可能な程度に保持されている。
2
中等度の炎症
試料の組織像は,炎症性細胞の局所的な集積を示すが,組織のえ(壊)死はなく,残
存歯髄及び根せん(尖)歯周組織の構造的特徴は,部分的に崩壊している。
3
強度の炎症
残存歯髄又は根せん(尖)歯周組織が,広範囲に炎症性細胞浸潤によって置換されて
いる。
4
組織のえ(壊)死
のう(膿)瘍形成
注記 記録しなければならない組織学的特徴の例は,次による。
a) 根管充塡が根せん(尖)孔の位置との関係において未到達,一致又は突出しているかを判
定する評価:この所見を炎症の存在,根吸収及び骨反応と関連させる。
b) 根管シーラ(セメント)の過剰充塡:根管シーラが根せん(尖)を突き抜けて,周囲の歯
周組織及び骨組織中にいっ(溢)出していないかを判定する。28日後に観察することが多
いが,長期間観察をこの評価から除外しないことが望ましい。
c) え(壊)死した根せん(尖)組織の存在
d) 良好,可又は不良で等級付けする根管充塡材料の適合の度合い
−“良好”な適合とは,一つの切片だけでなく連続した切片で,充塡材料が空隙なく根管壁
に適合していることを意味する。
−“可”の適合とは,幾つかの切片に,空隙,すなわち,充塡材料が根管壁に適合していな
い部分が一部に存在することを意味する。
−“不良”な適合とは,充塡材料が根管壁に適合していない,すなわち,多数の空隙が存在
することを意味する。
e) 表9によって等級付けした炎症(0〜4)について,炎症部位に存在する炎症細胞の種類に
基づく詳細な説明:大多数を占める細胞の種類を調べ,リンパ球,単球,マクロファージ
及び多核巨細胞は,後期に出現するのに対し,急性炎症細胞(好中球)は,初期に出現す
ることに基づき,炎症反応を急性(A),慢性(C)又は混合(M)に分類する。
f)
根吸収の有無
g) 根せん(尖)周囲の骨組織の反応を正常又は炎症状態に等級付けし,更に肉芽腫が存在す
るか否か,及び骨吸収の徴候の有無を判定する。
h) 表9によって等級付けした炎症(0〜3)について,充血の程度を評価する。
6.6.4
結果の評価
結果の評価は,6.4.4による。
6.6.5
試験報告書
試験報告書は,6.4.5による。
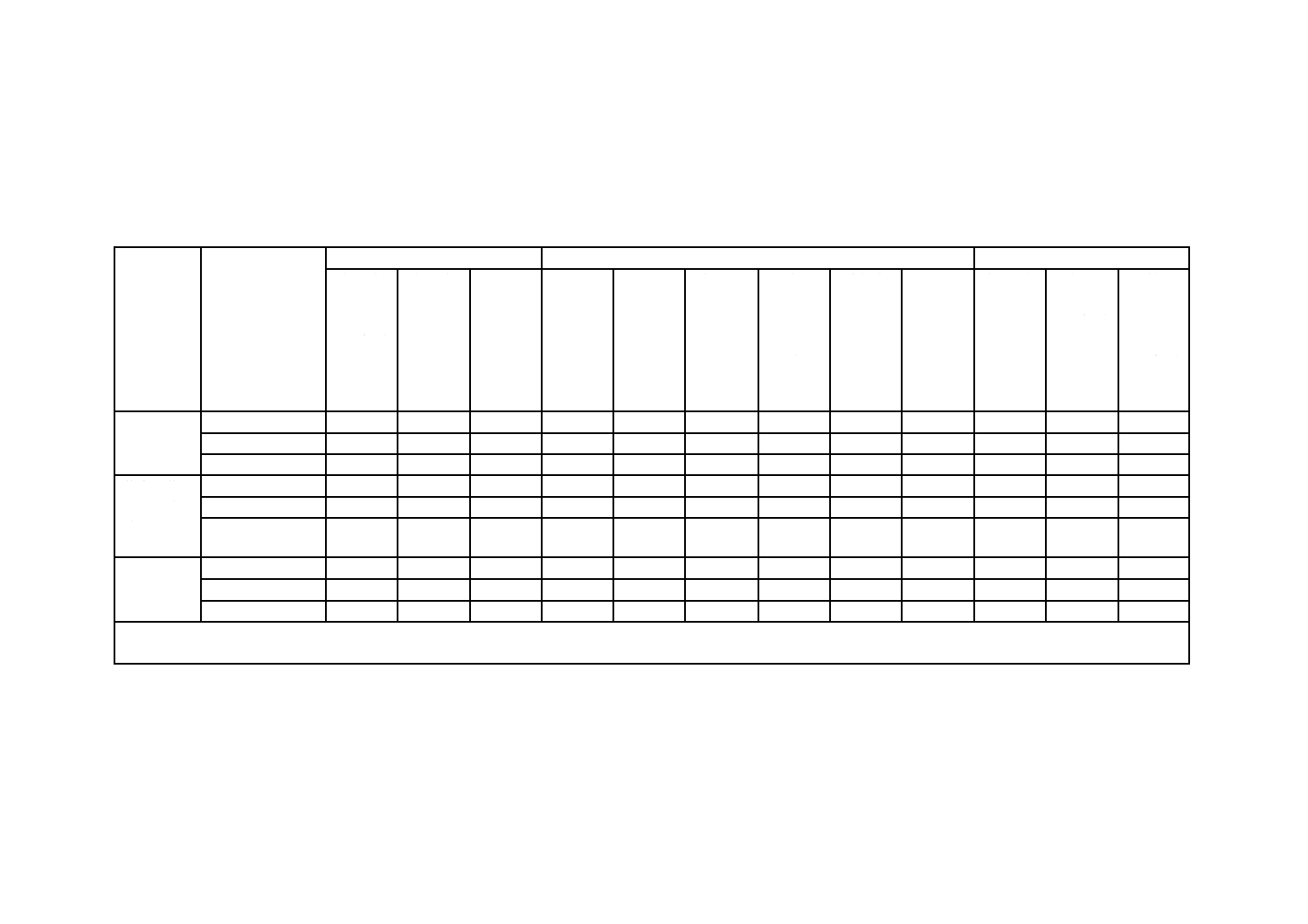
附属書A
(参考)
歯科用医療機器の生体適合性の評価を行う上で考慮する試験の種類
表A.1−歯科用医療機器の生体適合性の評価を行う上で考慮する試験の種類
接触様式
接触期間
A−一時的
(24時間以内)
B−短・中期的
(24時間超〜30
日以内)
C−長期的(永久)
(30日超)
グループ1
グループ2
グループ3
細胞毒
性試験
6.2及び
6.3参照
細胞毒
性試験
ISO
10993-5
細胞毒
性試験
附属書B
参照
遅延型
過敏症
(感作
性)
ISO
10993-10
皮膚刺
激性又
は皮内
反応
ISO
10993-10
急性全
身毒性
ISO
10993-11
亜急性
(又は
亜慢性)
全身毒
性
ISO
10993-11
遺伝毒
性
ISO
10993-3
埋植
ISO
10993-6
歯髄・象
牙質使
用模擬
試験
6.4参照
覆髄試
験
6.5参照
根管充
塡使用
模擬試
験
6.6参照
表面接触
機器
A
○
○
○
○
B
○
○
○
○
C
○
○
○
○
○
○
体内と体
外とを連
結する機
器
A
○
○
○
○
○
○
B
○
○
○
○
○
○
○
○
○
○
C
○
○
○
○
○
○
○
○
○
○
体内植込
み機器
A
○
○
○
○
○
○
B
○
○
○
○
○
○
○
○
○
○
C
○
○
○
○
○
○
○
○
○
○
○は,その試験の実施を考慮することを示す。
注記 この表は,生体適合性評価プログラムの構築のための枠組みであり,チェックリストではない。
2
T
6
0
0
1
:
2
0
1
2
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
23
T 6001:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書B
(参考)
象牙質バリア細胞毒性試験
B.1
目的
この試験は,修復材料が充塡された歯のか(窩)洞の臨床状況を模擬するために,細胞と材料とを象牙
質によって隔てた状態で細胞培養し,歯科用充塡材料の細胞毒性を評価するものである。
B.2
装置及び材料
B.2.1 細胞
入手が容易な[例えば,American Type Culture Collection(ATCC)から入手できる。]2)確立された細胞株,
又は代替品として,SV 40 ラージT抗原遺伝子導入細胞クローン[例えば,こ(仔)ウシの歯乳頭に由来
するもの]を使用できる。それらの細胞を,37±2 ℃で5 %炭酸ガス雰囲気の加湿環境下にある増殖用培
地で培養する。また,象牙芽細胞様の性質,又は歯髄組織の生理機能に類似した性質をもつ,他の確立さ
れた細胞株も使用できる。
B.2.2 培地
ATCC2)が供給する選択した細胞株に規定される培地を用いる。
注記 指針として,http://www.atcc.org を参照。SV 40 ラージT抗原遺伝子導入細胞のための増殖培地
は,20 %ウシ胎児の血清(FBS),150 IU/mL ペニシリン,150 μg/mL ストレプトマイシン,
0.125 μg/mL アンホテリシンB及び0.1 mg/mL ジェネティシンを添加したMEMαからなる。
B.2.3 試薬
B.2.3.1 3-(4,5-ジメチルチアゾール-2-イル)-2,5-ジフェニルテトラゾリウムブロミド(MTT)
B.2.3.2 抗生物質及び防かび剤 ペニシリン,ストレプトマイシン,アンホテリシンBを用いる。ただし,
SV40遺伝子導入細胞クローンを使用する場合には,これに加えてジェネティシンを用いる。
B.2.4 機器
B.2.4.1 プレートインサート 例えば,Millicell6)
注6) Millicellは,ミリポアが供給する製品の商標名である。この情報は,この規格の利用者の便宜
を図って記載するもので,この製品を推奨するものではない。同じ結果が得られる場合には,
これと同等の他のものを使用してもよい。
B.2.4.2 プレート(培養皿) 例えば,6穴のもの
B.2.4.3 ポリアミドメッシュ 直径8 mmのもの。例えば,Sefar7),メッシュ幅150 μm
注7) Sefarは,Sefarが供給する製品の商標名である。この情報は,この規格の利用者の便宜を図っ
て記載するもので,この製品を推奨するものではない。同じ結果が得られる場合には,これと
同等の他のものを使用してもよい。
B.2.4.4 分割チャンバかん(灌)流装置
次に,二つのかん(灌)流チャンバについて記載するが,両方とも適合する。
第一の分割チャンバかん(灌)流装置,Minucells8)(図B.1)は,底部が40 mm×40 mmで,高さが35 mm
のポリカーボネート製のチャンバからなる。この装置において歯髄に該当する部分は,片方が培養液供給
瓶に,他方がペリスタポンプ及び廃液瓶に接続している。試験装置内で,二つのチャンバは,ステンレス
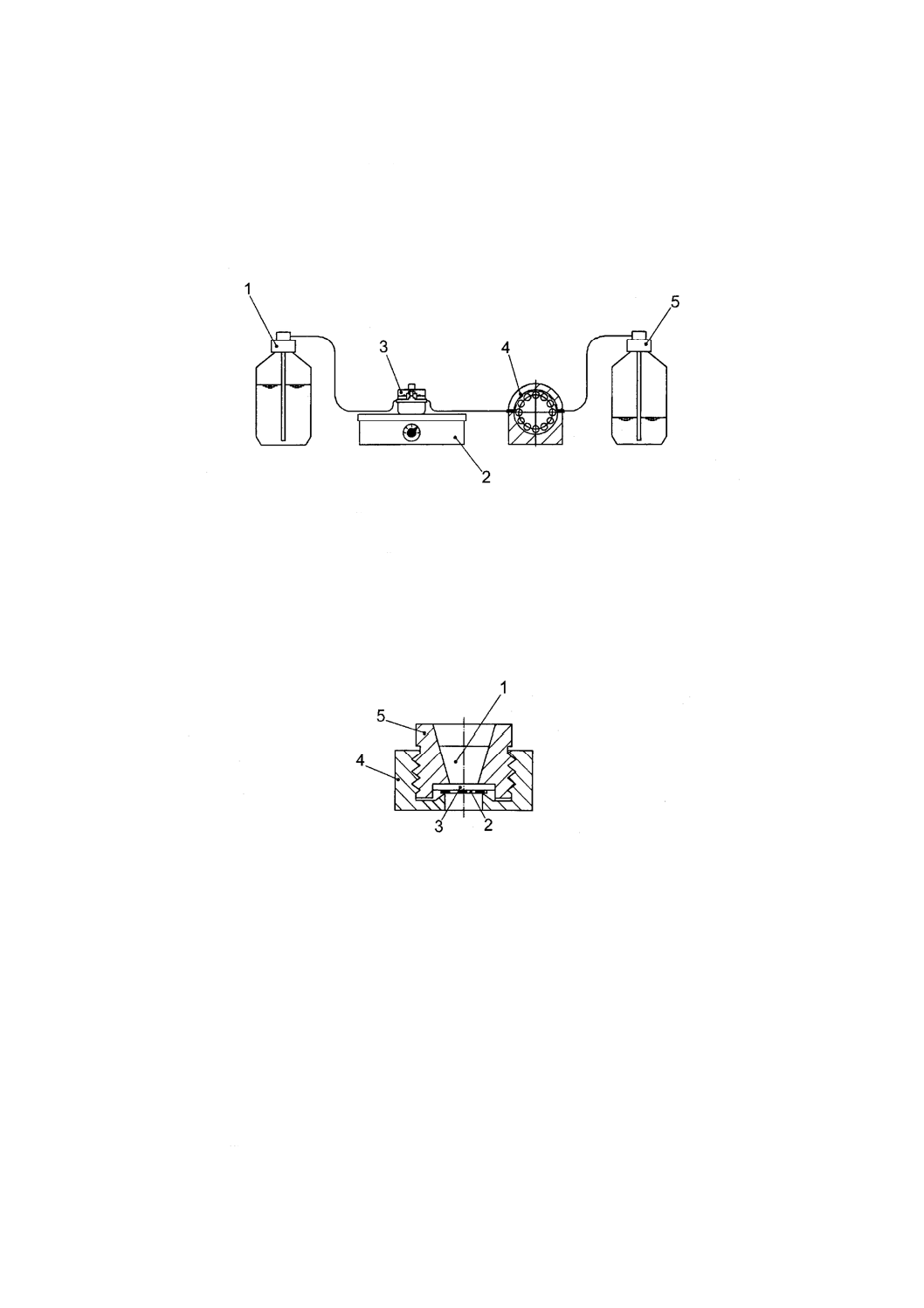
24
T 6001:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
鋼製ホルダ(図B.2)で定位置に保たれる象牙質スライスによって分離されている。
注8) Minucellsは,Minucells & Minutissue GmbHが供給する製品の商標名である。この情報は,この
規格の利用者の便宜を図って記載するもので,この製品を推奨するものではない。同じ結果が
得られる場合には,これと同等の他のものを使用してもよい。
1
培養液供給瓶
2
ホットプレート
3
かん(灌)流チャンバ
4
ポンプ
5
廃液瓶
図B.1−象牙質バリア細胞毒性試験用装置
1
試験材料
2
細胞を増殖させたメッシュ
3
象牙質スライス
4
ステンレス鋼製リング
5
ステンレス鋼製インサート
図B.2−試験装置に象牙質スライス及び培養細胞を固定するステンレス鋼製ホルダ
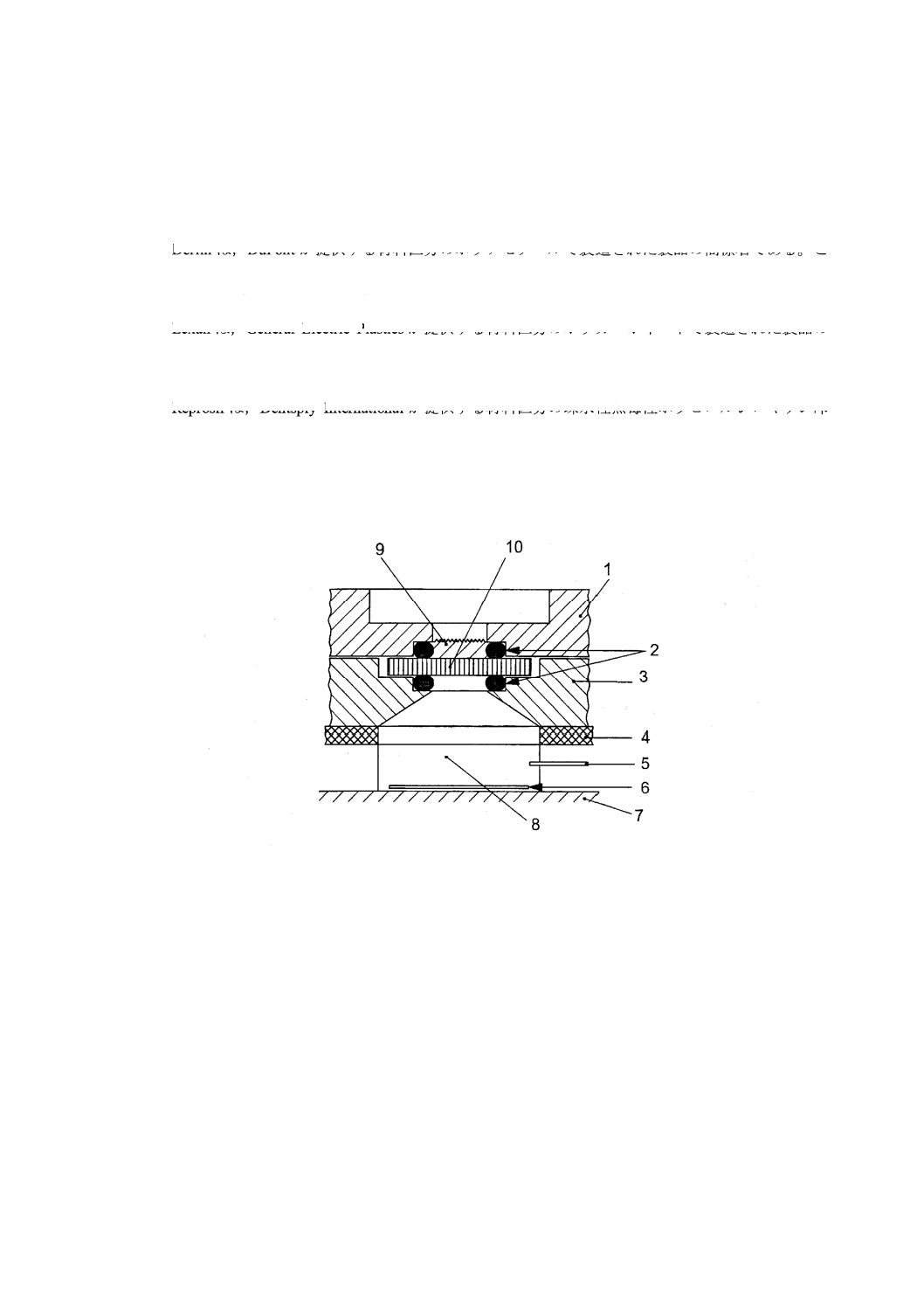
第二の分割チャンバかん(灌)流装置,米国歯科医師会(以下,ADAという。)かん(灌)流チャン
バ9)(図B.3)は,毒性のないDerlin10)又はLexan11)によって作られた透明の壁からなる。流入口及び流出
口弁は毒性のないステンレス鋼製細管である。小さなOリングは,赤色のシリコーン製である(外径15.9
mm,内径12.42 mm)。内径6 mmの,より小さいOリングによって,表面拡散面積が28 mm2になる。こ
のチャンバ部分は,0.5 mLの液を保持する。チャンバを底から,毒性のないポリビニルシロキサン印象材
[例えば,Reprosil12)]で満たすことによって,チャンバ容積が100 μL未満になる。
25
T 6001:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
注9) ADA かん(灌)流チャンバは,Biomedical Engineering, Medical College of Georgiaが提供する製
品の商標名である。この情報は,この規格の利用者の便宜を図って記載するもので,この製品
を推奨するものではない。同じ結果が得られる場合には,これと同等の他のものを使用しても
よい。
10) Derlinは,DuPontが提供する材料区分のポリアセタールで製造された製品の商標名である。こ
の情報は,この規格の利用者の便宜を図って記載するもので,この製品を推奨するものではな
い。同じ結果が得られる場合には,これと同等の他のものを使用してもよい。
11) Lexanは,General Electric Plasticsが提供する材料区分のポリカーボネートで製造された製品の
商標名である。この情報は,この規格の利用者の便宜を図って記載するもので,この製品を推
奨するものではない。同じ結果が得られる場合には,これと同等の他のものを使用してもよい。
12) Reprosilは,Dentsply Internationalが提供する材料区分の疎水性無毒性ポリビニルシロキサン印
象材で製造された製品の商標名である。この情報は,この規格の利用者の便宜を図って記載す
るもので,この製品を推奨するものではない。同じ結果が得られる場合には,これと同等の他
のものを使用してもよい。
1
上部
2
ゴム製Oリング
3
中間部
4
エラストマーシート
5
流入口−流出口
6
カバーグラス
7
底部
8
培養液
9
試験材料
10 ゴム製Oリングで定位置に保たれる象牙質スライス
図B.3−ADAかん(灌)流チャンバ
B.2.4.5 マイクロプレートリーダ 96穴プレート用,波長540 nm,又は適切な他の光度計
B.2.4.6 象牙質スライス ヒト又はウシの象牙質から作製したもの。
26
T 6001:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
注記 ヒト以外の象牙質を使用する場合には,使用に先立って,その象牙質スライスの透過性を測定
して,その透過性が歯髄−象牙質界面に匹敵するレベルで,ヒト象牙質の透過性と同様である
ことを確かめる。このために,キャピラリシステム[例えば,Flodec13)]を用いる。
注13) Flodecは,DeMarco Engineeringが提供する製品の商標名である。この情報は,この規
格の利用者の便宜を図って記載するもので,この製品を推奨するものではない。同じ
結果が得られる場合には,これと同等の他のものを使用してもよい。
B.3
試験手順
B.3.1 細胞培養の準備
B.3.1.1 3次元細胞培養
3次元細胞培養は,Minucells8)かん(灌)流チャンバとともに用いることを推奨する。ポリアミドメッシ
ュを0.1 mol/L酢酸中で30分間加温し,脱イオン水で3回洗浄し,空気乾燥し,フィブロネクチン
(0.03 mg/mL)で被覆し,滅菌条件下で空気乾燥する。プレートインサートを1.25 mLの培養液とともに,
6穴プレートの各穴の中に入れる。メッシュをインサートの上に静置し,4×106 個/mLの細胞懸濁液20 μL
をは(播)種する。37±2 ℃,5 %炭酸ガス雰囲気,相対湿度(90±10)%で48時間培養した後,メッシ
ュを24穴プレートへ移して14±2 日間培養する。培養液を週に3回交換し,第1週の終わりにメッシュ
を新しい24穴プレートへ移す。
B.3.1.2 単層培養
単層培養は,ADAかん(灌)流チャンバとともに用いることが推奨される。入手が容易な[例えば,
ATCC2)から]確立された細胞株を用いて,ISO 10993-5に規定する方法を適用する。
B.3.2 象牙質スライスの作製
B.3.2.1 ヒト象牙質
うしょく(蝕)のない,抜去直後の臼歯を選び,歯石,付着軟組織などを手用器具で除去して,70 %エ
タノール中に少なくとも15分間浸す。歯冠の最大豊隆部において,こう(咬)合面のエナメル質の下,髄
室角の上で,歯軸に垂直に歯を切断することによって,象牙質スライスを作製する。
B.3.2.2 ウシ象牙質
3〜7才のウシの下顎中央の切歯4本の中から,過度にこう(咬)耗していない健全な歯を選ぶ。抜歯し,
歯石,付着軟組織などを手用器具で除去して,使用するまで0.5 %クロラミン又は他の同様な薬剤中に保
存する。歯髄になるべく近接して,歯軸に沿って歯を切断する。試験には,象牙質スライスの歯頚部近傍
を用いる。
B.3.2.3 象牙質スライスの処理
象牙質スライスの“歯髄”側と想定した面を50 %クエン酸で30秒間エッチングし,十分に洗浄して,
0.9 %塩化ナトリウム溶液中でオートクレーブ滅菌(121 ℃,9.6 MPa,25分間)するか,又は70 %エタノ
ール中に15分間浸して滅菌した後,脱イオン水で十分に洗浄する。象牙質スライスは,4±2 ℃の0.9 %
塩化ナトリウム溶液中で3週間までは保存できる。保存した象牙質スライスは,使用前に,各バッチから
サンプリングした試料の微生物培養によって,その無菌状態を確認する。
注記 象牙質スライスの厚さは,その試験が模擬する臨床か(窩)洞の深さに応じて変えることがで
きる。厚さ500±50 μmの象牙質スライスは,中程度の深さとなる臨床か(窩)洞の下の残存
象牙質に相当する。より薄い象牙質スライスは,より深い臨床か(窩)洞の状況を再現するた
めに用いる。
27
T 6001:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
象牙質スライスは,使用するまで,0.9 %塩化ナトリウム溶液中で保存できる。
B.3.2.4 かん(灌)流装置
B.3.2.4.1 Minucells装置
細胞を増殖させたメッシュを試験装置に入れ,象牙質スライスを挿入する。象牙質スライスは,ステン
レス鋼製ホルダによって定位置に保持する。
注記 適合するホルダを,図B.2に示す。
流量0.3 mL/hのアッセイ培地(6 g/L HEPES緩衝液を用いた増殖培地)で,チャンバを24 時間かん(灌)
流する。かん(灌)流を止めて,試験材料を上室内の象牙質スライスの“か(窩)洞”側に直接接触する
ように入れる。
適切な期間(例えば,24時間又は3日)後に,被験細胞の入ったメッシュをチャンバの歯髄部分から取
り出して,あらかじめ温めたMTT溶液(0.5 mg/mL増殖培地溶液)0.5 mLが入っている48穴プレートの
各穴中に入れ,37±2 ℃で2時間インキュベートする。その後,りん酸緩衝生理的塩類溶液[例えば,ダ
ルベッコのりん酸緩衝塩類溶液3)]で2回メッシュを洗う。プレートを30分間室温で振とう(盪)して,
0.25 mLのジメチルスルホキシドで青色ホルマザン沈殿を抽出する。この溶液の200 μLを96穴プレート
へ移して,分光光度法で540 nmの吸光度を測定する。対象の値に対する百分率として,又は吸光度測定
値として結果を表す。
各材料及び対照について,1回の試験で5〜10のチャンバを用い,各試験を少なくとも2回行う。
B.3.2.4.2 ADAかん(灌)流チャンバ装置
かん(灌)流チャンバ装置に象牙質スライスを取り付ける。下室に,適合する細胞培養液(又は他の抽
出用ビヒクル)を満たし,必要に応じて下室を培養液供給瓶及び廃液瓶に接続する。その後,試験材料を
充塡する。所定のばく(曝)露時間後に細胞培養液を除去して,それを通常の単層培養の細胞毒性試験に
用いる。例えば,生物学的評価指標(biological endpoints)としてDNA合成,ミトコンドリア酵素活性(MTT
アッセイ),遺伝子制御の機能発現がある。
B.4
対照
試験される各材料について,陽性対照及び陰性対照を用いる。陽性対照は,24時間のばく(曝)露後に,
細胞生存率を約50 %減少させることが望ましい。陰性対照は,生細胞数に影響しないことが望ましい。陽
性対照材料14)の例を,表B.1に示す。
注14) 次の原材料は,好適な市販製品の例である。この情報は,この規格の使用者の便宜を図って提
供するもので,これらの材料を推奨するものではない。
粒径30±10 μmのガラス粉:Schott, order No. GM35429
ポリアクリル酸:Sigma-Aldrich, order No. 323667
塩化ジフェニルヨードニウム:Sigma, order No. D209082
カンファーキノン:Sigma, order No. 124893
4-ジメチルアミノ安息香酸エチル:Merck, order No. 841086
HEMA (2-hydroxyethyl-methacrylate):Merck, order No. 800588
28
T 6001:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
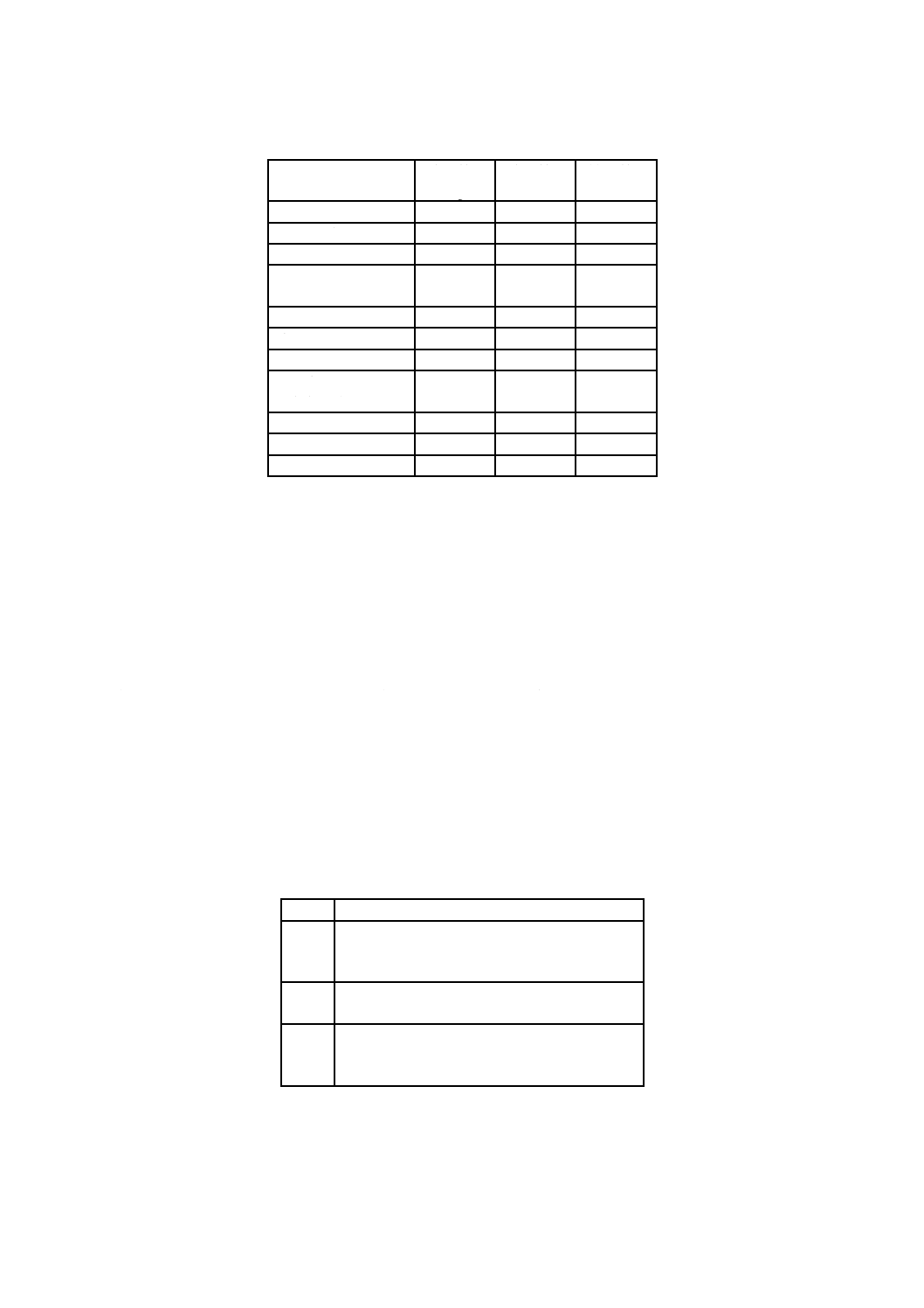
表B.1−陽性対照材料の例
材料
試料質量
mg
試料質量
%
最終質量
%
粉末
ガラス粉
829.000
82.90
66.30
ポリアクリル酸
146.000
14.60
11.70
塩化ジフェニルヨ
ードニウム
25.000
2.50
2.00
計
1 000.00
100.00
80.00
液
カンファーキノン
0.625
0.25
0.05
4-ジメチルアミノ
安息香酸エチル
0.625
0.25
0.05
HEMA
187.500
75.00
15.00
蒸留水
61.250
24.50
4.90
計
250.000
100.00
20.00
注記 陰性対照として,毒性のない疎水性ポリビニルシロキサン印象材が好適である。陽性対照とし
て,表B.1に記載した組成の材料,又は同等の材料を用いることができる。
粉末及び液のそれぞれの成分を別個に混和した後,直ちに粉末1 000 mg,液250 mgの割合で両者を混
ぜ合わせる。一般の光重合用装置によって,混和物を40秒間,700〜800 mW/cm2で硬化させる。
B.5
結果の評価
陰性対照と陽性対照との間に統計的に有意の差が生じない場合には,その試験は棄却する。
ここで得られた評価に加えて,より詳細な情報については,ISO 10993-5を参考にする。Minucells装置
から得られたデータの評価は,各材料について5〜10の独立した試験を基に,試験材料データと陰性及び
陽性対照データとを統計学的(ノンパラメトリック法)に比較して行う。表B.2によって細胞損傷を評価
し,表B.3によって結果を等級付けする。
試験報告書に評価の結果を記載する。
表B.2−細胞損傷の評価
等級
内容
0
陽性対照とは統計的に有意差があり,陰性対照
とは有意差がないか,陰性対照より弱い細胞損
傷しか引き起こさない。
1
陰性対照及び陽性対照のいずれとも,統計的有
意差がある。
2
陰性対照とは統計的に有意差があり,陽性対照
とは有意差がないか,陽性対照よりも強い細胞
損傷を生じている。

29
T 6001:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
表B.3−試験材料の等級付け
等級
内容
0
細胞毒性なし
1
中等度の細胞毒性
2
強度の細胞毒性
B.6
試験報告書
試験報告書には,次の情報を記載しなければならない。
a) 試験に用いた細胞系
b) 試験に用いた培地
c) 試験材料の詳細
d) 試験材料の準備の詳細
e) 陽性対照及び陰性対照の詳細
f)
陰性対照と比較したときの細胞生存率
g) 評価の結果
30
T 6001:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書C
(参考)
急性毒性試験
古典的なLD50法は,動物愛護の見地から,不必要で容認できない方法である。
定量投与法(OECDガイドライン 420[13]),段階投与法(OECDガイドライン 423[14])及び“アップ・
アンド・ダウン”投与法(OECDガイドライン 425[15])を,法規制のための急性毒性試験として用いるこ
とについては,正当性が立証されている。
31
T 6001:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
参考文献
[1] ISO 1942, Dentistry−Vocabulary
[2] ISO 6344-1,Coated abrasives−Grain size analysis−Part 1:Grain size distribution test
[3] ISO 10993-7, Biological evaluation of medical devices−Part 7: Ethylene oxide sterilization residuals
[4] ISO 10993-9, Biological evaluation of medical devices−Part 9: Framework for identification and
quantification of potential degradation products
[5] ISO 10993-13, Biological evaluation of medical devices−Part 13: Identification and quantification of
degradation products from polymeric medical devices
[6] ISO 10993-14, Biological evaluation of medical devices−Part 14: Identification and quantification of
degradation products from ceramics
[7] ISO 10993-15, Biological evaluation of medical devices−Part 15: Identification and quantification of
degradation products from metals and alloys
[8] ISO 10993-16, Biological evaluation of medical devices−Part 16: Toxicokinetic study design for degradation
products and leachables
[9] ISO 10993-17, Biological evaluation of medical devices−Part 17: Establishment of allowable limits for
leachable substances
[10] ISO 10993-18, Biological evaluation of medical devices−Part 18: Chemical characterization of materials
[11] ISO/TS 22911, Dentistry−Preclinical evaluation of dental implant systems−Animal test methods
[12] ANSI/ADA Specification No. 41, Recommended Standard Practices for Biological Evaluation of Dental
Materials
[13] OECD 420: OECD Guidelines for Testing Chemicals−Acute Oral Toxicity. Fixed Dose Procedure,
Organisation for Economic Co-operation and Development, 75775 Paris Cedex 16, France
[14] OECD 423: OECD Guidelines for Testing Chemicals−Acute Oral Toxicity. Acute Toxic Class Method,
Organisation for Economic Co-operation and Development, 75775 Paris Cedex 16, France
[15] OECD 425: OECD Guidelines for Testing Chemicals−Acute Oral Toxicity. Up-and-Down Procedure,
Organisation for Economic Co-operation and Development, 75775 Paris Cedex 16, France
[16] BARKA, T. and ANDERSON, P.J., Histochemistry. Theory, practice and bibliography, Chapter XIII, Hoeber
Medical Division, Harper & Row Publishers, New York, 1963
[17] BERBERT, F.L., LEONARDO, M.R., SILVA, L.A., TANOMARU FILHO, M. and BRAMANTE, C.M.,
Influence of root canal dressings and sealers on repair of apical periodontitis after endodontic treatment, Oral
Surg. Oral Med. Oral Pathol. Oral Radiol. Endod., 93, pp. 184-189, 2002
[18] BROWNE, R.M., Animal tests for biocompatibility of dental materials: relevance, advantages and limitations, J.
Dent., 22, pp. 21-24, 1994
[19] FRANZ, A., KÖNIG, F., SKOLKA, A., SPERR, W., BAUER, P., LUCAS, T., WATTS, D.C. and SCHEDLE, A.,
Cytotoxicity of resin composites as a function of interface area, Dent. Mater., 23, pp. 1438-1446, 2007
[20] HANKS, C.T., DIEHL, M.L., CRAIG, R.G., MAKINEN, P.L. and PASHLEY, D.A., Characterization of the “in
vitro pulp chamber” using the cytotoxicity of phenol, J. Oral Path., 18, pp. 97-107, 1989
[21] MAGLOIRE, H., JOFFRE, A. and BLEICHER, F., An in vitro model of human dental pulp repair. J. Dent. Res.,
75, pp. 1971-1978,1996
32
T 6001:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
[22] MERYON, S.D., The model cavity method incorporating dentine, Int. Endod. J., B, pp. 79-84, 1988
[23] MURRAY, P., HAFEZ, A.A., SMITH, A.J., WINDSOR, L.J. and COX, C.F., Histomorphometric analysis of
odontoblast-like cell numbers and dentine bridge secretory activity following pulp exposure, Int. Endod. J., 36,
pp. 106-116, 2003
[24] MURRAY, P.E., LUMLEY, P.J., ROSS, H.F. and SMITH, A.J., Tooth slice organ culture for cytotoxicity
assessment of dental materials, Biomaterials, 21, pp. 1711-1721, 2000
[25] PAMEIJER, C.H. and STANLEY, H.R., Pulp reaction to a dentin bonding agent, Am. J. Dent., 8, pp. 140-114,
1995
[26] PASCON, E.A., LEONARDO, M.R., SAFAVI, K. and LANGELAND, K., Tissue reaction to endodontic
materials: methods, criteria, assessment, and observations, Oral Surg. Oral Med. Oral Pathol., 72, pp. 222-237,
1991. Erratum in: Oral Surg. Oral Med., 73, p. 347, 1992
[27] SCHMALZ, G., Agar overlay method, Int. Endod. J., 21, pp. 59-66, 1988
[28] SCHMALZ, G., GARHAMMER, P. and SCHWEIKL, H., A commercially available cell culture device for
dentin barrier tests, J. Endod., 22, pp. 249-252, 1996
[29] SCHMALZ, G., HILLER, K.-A. and DÖRTER-ASLAN, F., New developments in the filter test system for
cytotoxicity testing, J. Mat. Sci., Materials in Medicine, 5, pp. 43-51, 1994
[30] SCHMALZ, G. and SCHWEIKL, H., Characterization of an in vitro barrier test using a standard toxicant, J.
Endod., 20, pp. 592-594, 1994
[31] SCHUSTER, U., SCHMALZ, G., THONEMANN, B., MENDEL, N. and METZL, C., Cytotoxicity testing with
three-dimensional cultures of transfected pulp-derived cells, J. Endod., 27, pp. 259-265, 2001
[32] WENNBERG, A., HASSELGREEN, G. and TRONSTAD, L., A method for toxicity screening of biomaterials
using cells cultured on millipore filters, J. Biomed. Mater. Res., 13, pp. 109-120, 1979
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書JA
(参考)
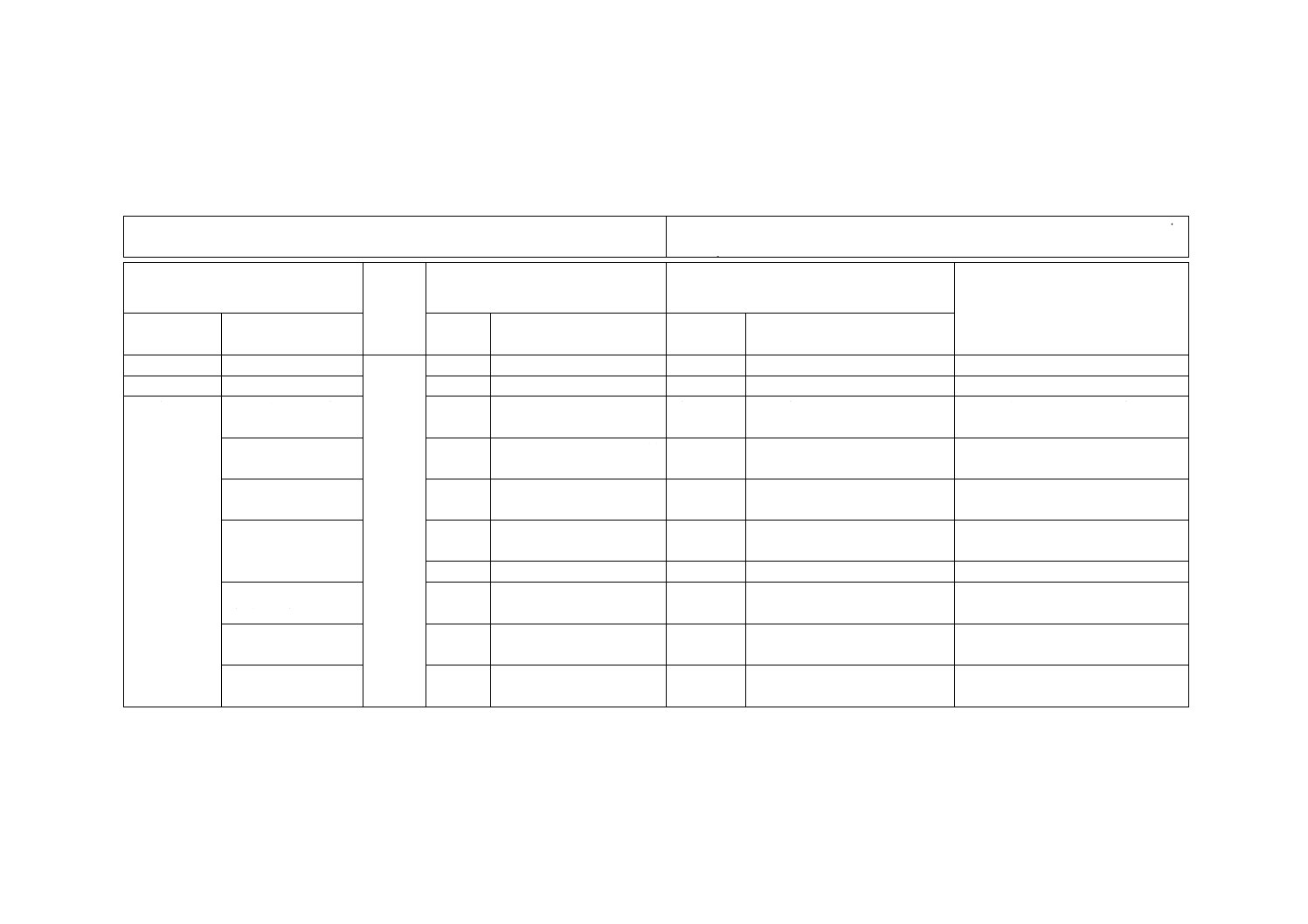
JISと対応国際規格との対比表
JIS T 6001:2012 歯科用医療機器の生体適合性の評価
ISO 7405:2008 Dentistry−Evaluation of biocompatibility of medical devices used in
dentistry
(I)JISの規定
(II)
国際規
格番号
(III)国際規格の規定
(IV)JISと国際規格との技術的差異の箇条ご
との評価及びその内容
(V)JISと国際規格との技術的差異
の理由及び今後の対策
箇条番号及
び題名
内容
箇条番
号
内容
箇条ごと
の評価
技術的差異の内容
2 引用規格
4.1.1 一般
歯科用医療機器
4.1.1
医療機器
変更
歯科用を付けた。
歯科用医療機器として特定した。
6 歯科材料
のための試
験手順
6.1.3 a) 試料作製型
の材質
追加
注を追加した。
分かりやすくするために追加した。
6.1.3 c) 酸素の遮断
6.1.3 c)
ISO 6344-1のP2 000の研
磨紙
変更
JISの研磨紙を採用した。
我が国ではJISの研磨紙が流布し
ている。
6.1.4 b) 酸素の遮断
6.1.4 b)
ISO 6344-1のP2 000の研
磨紙
変更
JISの研磨紙を採用した。
我が国ではJISの研磨紙が流布し
ている。
6.2.4 試料調製
6.2.4
6.2.4に注記を記載
変更
記載箇所を変更した。
適切な箇所に記載した。ISO規格改
正時に提案する。
6.2.4
−
追加
注を追加した。
分かりやすくするために追加した。
6.4.3.4 象牙質及び
歯髄の評価
6.4.3.4
追加
表6の列を追加し,記載内容を
分割し,一部追加した。
分かりやすくするために表を改変
した。
6.5.3.4 歯髄の評価
6.5.3.4
追加
表8の列を追加し,記載内容を
分割し,一部追加した。
分かりやすくするために表を改変
した。
6.6.3.4 組織の評価
6.6.3.4
追加
表9の列を追加し,記載内容を
分割し,一部追加した。
分かりやすくするために表を改変
した。
2
T
6
0
0
1
:
2
0
1
2

JISと国際規格との対応の程度の全体評価:ISO 7405:2008,MOD
注記1 箇条ごとの評価欄の用語の意味は,次による。
− 追加……………… 国際規格にない規定項目又は規定内容を追加している。
− 変更……………… 国際規格の規定内容を変更している。
注記2 JISと国際規格との対応の程度の全体評価欄の記号の意味は,次による。
− MOD…………… 国際規格を修正している。
2
T
6
0
0
1
:
2
0
1
2
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。