3
T 3307:2013
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
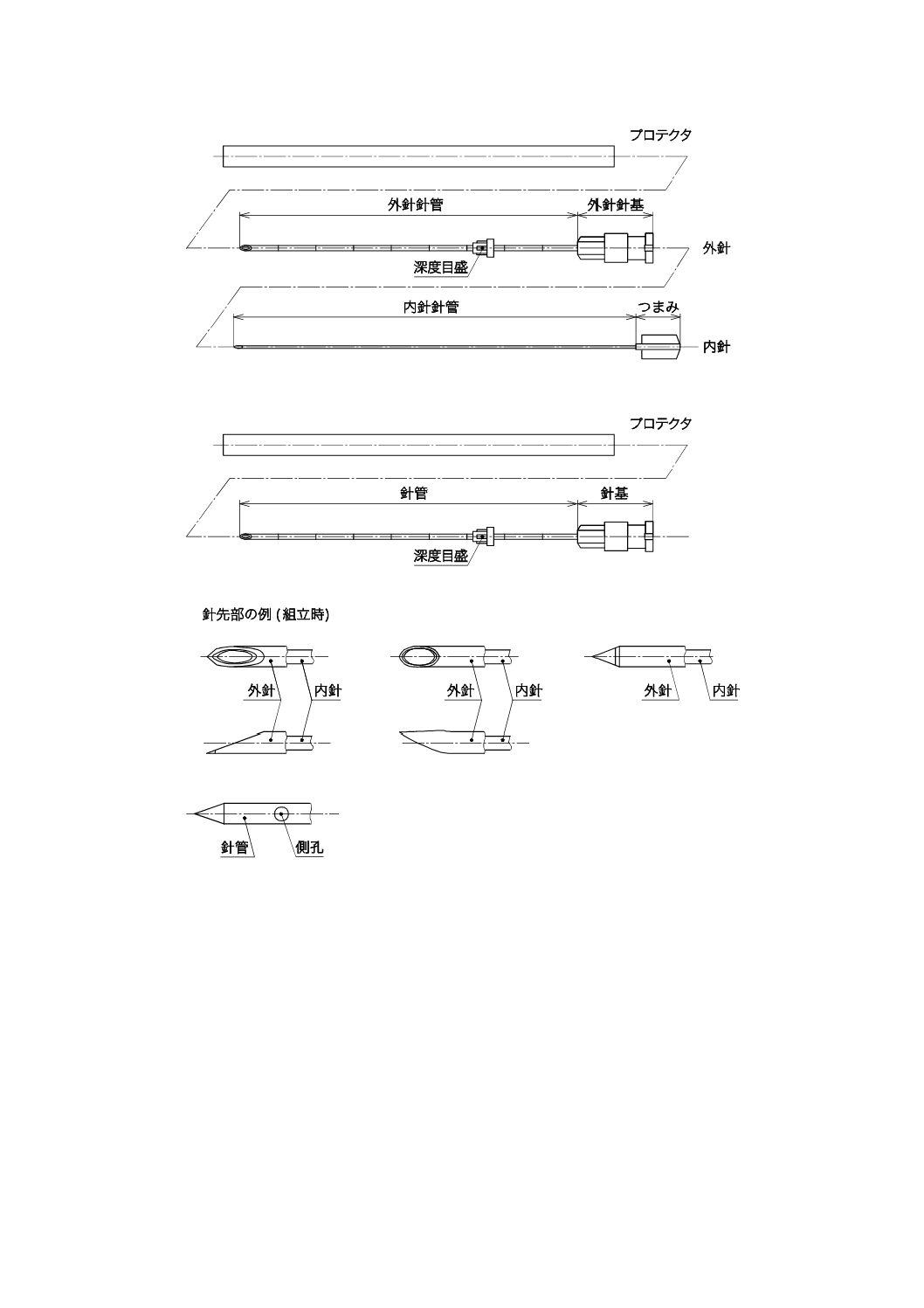
注記1 プロテクタは,使用前後に術者が針管の針先を身体に誤刺しないように保護し,外針針基,深度目盛などに
かん(嵌)合する。
注記2 深度目盛を具備しないものもある。
注記3 針先は様々な形状のものがある。
注記4 内針がないものもある。
図1−胆管造影用針各部名称
T 3307:2013
(1)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
目 次
ページ
序文 ··································································································································· 1
1 適用範囲························································································································· 1
2 引用規格························································································································· 1
3 用語及び定義 ··················································································································· 1
4 構成及び各部の名称 ·········································································································· 2
5 物理的要求事項 ················································································································ 4
5.1 外観及び清浄度 ············································································································· 4
5.2 針先 ···························································································································· 4
5.3 針管の材料 ··················································································································· 4
5.4 潤滑剤 ························································································································· 4
5.5 外針 ···························································································································· 4
5.6 内針 ···························································································································· 6
6 化学的要求事項 ················································································································ 7
6.1 試験液及び空試験液の調製 ······························································································ 7
6.2 pH ······························································································································ 7
6.3 溶出金属物の制限 ·········································································································· 7
7 生物学的安全性 ················································································································ 7
8 無菌性の保証 ··················································································································· 7
9 エンドトキシン ················································································································ 7
10 包装 ····························································································································· 8
10.1 一次包装 ····················································································································· 8
10.2 二次包装 ····················································································································· 8
11 表示 ····························································································································· 8
11.1 一次包装 ····················································································································· 8
11.2 二次包装 ····················································································································· 8
11.3 図記号の使用 ··············································································································· 8
T 3307:2013
(2)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
まえがき
この規格は,工業標準化法第14条によって準用する第12条第1項の規定に基づき,日本医療器材工業
会(JMED)及び一般財団法人日本規格協会(JSA)から,工業標準原案を具して日本工業規格を改正すべ
きとの申出があり,日本工業標準調査会の審議を経て,厚生労働大臣が改正した日本工業規格である。こ
れによって,JIS T 3307:2007は改正され,この規格に置き換えられた。
この規格は,著作権法で保護対象となっている著作物である。
この規格の一部が,特許権,出願公開後の特許出願又は実用新案権に抵触する可能性があることに注意
を喚起する。厚生労働大臣及び日本工業標準調査会は,このような特許権,出願公開後の特許出願及び実
用新案権に関わる確認について,責任はもたない。
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
日本工業規格 JIS
T 3307:2013
滅菌済み胆管造影用針
Sterile percutaneous transhepatic cholangiographic needle
序文
この規格は,2007年に制定され今日に至っている。今回,使用者の利便性のため用語,文書構成などの
内容を変更して改正した日本工業規格である。
なお,対応国際規格は現時点で制定されていない。
1
適用範囲
この規格は,経皮経肝的又は直接,胆管をせん(穿)刺し,胆管造影用の造影剤を胆管に手動で注入す
るために用いる針で,単回使用の滅菌済み胆管造影用針(以下,胆管造影用針という。)について規定する。
ただし,未滅菌品は,箇条8以外について適用する。胆管造影用針は,造影と併せて,薬液注入,排液,
及びガイドワイヤ挿入補助具として使用することもある。この規格は,造影剤注入装置又はシリンジポン
プに接続して用いる針には適用しない。
なお,平成28年8月31日までJIS T 3307:2007は適用することができる。
2
引用規格
次に掲げる規格は,この規格に引用されることによって,この規格の規定の一部を構成する。これらの
引用規格は,記載の年の版を適用し,その後の改正版(追補を含む。)は適用しない。
JIS G 4305:2012 冷間圧延ステンレス鋼板及び鋼帯
JIS T 0307:2004 医療機器−医療機器のラベル,ラベリング及び供給される情報に用いる図記号
JIS T 0993-1:2012 医療機器の生物学的評価−第1部:リスクマネジメントプロセスにおける評価及
び試験
JIS T 3210:2011 滅菌済み注射筒
ISO 594-1:1986,Conical fittings with a 6 % (Luer) taper for syringes,needles and certain other medical
equipment−Part 1: General requirements
ISO 594-2:1998,Conical fittings with 6 % (Luer) taper for syringes,needles and certain other medical
equipment−Part 2: Lock fittings
ISO 9626:1991,Stainless steel needle tubing for the manufacture of medical devices及びAmendment 1:2001
3
用語及び定義
この規格で用いる主な用語及び定義は,次による。
3.1
外針
2
T 3307:2013
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
胆管造影用の造影剤を胆管に注入することを目的に,胆管にせん(穿)刺挿入するように設計された,
単くう(腔)の針。針管表面にせん(穿)刺刺入長の目安として目盛が付されているものもある。
3.2
内針
せん(穿)刺挿入の際,コアリングを防止することを目的として,あらかじめ外針内くう(腔)に挿入
してあり,胆管に達したとき,外針から簡単に引き抜くことができる器具。
3.3
コアリング
胆管造影用針を人体にせん(穿)刺する際にせん(穿)刺部位周辺を削ること。
3.4
公称外径
胆管造影用針の被包又は容器に表示された外針針管の外径の寸法。
3.5
公称長さ
胆管造影用針の被包又は容器に表示された外針針管の長さの寸法。
3.6
精製水
日本薬局方(以下,“日局”という。)の医薬品各条に規定する“精製水”又はこれと同等以上の水。
3.7
エンドトキシン試験用水
日局の医薬品各条に規定する“注射用水”又はその他の方法によって製造した水で,エンドトキシン試
験に用いるライセート(LAL)試薬の検出限界で反応を示さないもの。
3.8
一次包装
胆管造影用針を直接に覆う包装で,胆管造影用針の無菌性を保持するためのもの。さらに,これを二次
包装する場合には,いわゆる“内袋”に該当する。ただし,未滅菌品は,無菌性を保持しない。
3.9
二次包装
一次包装を直接に覆う包装。通常,一次包装した胆管造影用針を複数(例えば,100本)入れた包装。
3.10
ファーストライン
注射筒の外筒の目盛に合わせる押子の,先端の最初のピークのライン。
4
構成及び各部の名称
胆管造影用針は,主として,外針針管と外針針基とからなる外針,及び内針針管とつまみとからなる内
針で構成する。図1に,一般的な胆管造影用針,深度目盛,プロテクタ及び針先部の例を示す。

3
T 3307:2013
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
注記1 プロテクタは,使用前後に術者が針管の針先を身体に誤刺しないように保護し,外針針基,深度目盛などに
かん(嵌)合する。
注記2 深度目盛を具備しないものもある。
注記3 針先は様々な形状のものがある。
注記4 内針がないものもある。
図1−胆管造影用針各部名称
4
T 3307:2013
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
5
物理的要求事項
5.1
外観及び清浄度
外観及び清浄度は,次による。
a) 目視で検査したとき,針管,針基及びつまみの外面(超音波対応処理部を除く。)は,凹凸及びきずが
なく,仕上げ面が滑らかでなければならない。
b) 目視で検査したとき,針管,針基及びつまみの外面(超音波対応処理部を除く。)は,表面に微粒子又
は異物の付着があってはならない。
c) 目視で検査したとき,針管の内面には,有害な酸化物,切り粉などの微粒子又は異物の付着があって
はならない。また,針基の内面には微粒子又は異物の付着があってはならない。
d) 針管に目盛及び深度目盛が付いたものは,目視で検査したとき明確に目盛及び深度目盛が識別できな
ければならない。
e) 目視で検査したとき,針管は真っすぐであり,正常な切断面及び厚さでなければならない。
5.2
針先
針先は,鋭利に研磨してあり,目視で分かる,ばり,ささくれなどがあってはならない。
5.3
針管の材料
針管の材料は,JIS G 4305:2012に規定するSUS304,SUS304L若しくはSUS321,又はISO 9626:1991の
材料の項に適合するステンレス鋼でなければならない。
5.4
潤滑剤
5.4.1
潤滑剤の材料
針管の潤滑剤としてシリコーン油を用いる場合,シリコーン油は,シリコーン油基準又はこれと同等以
上の基準に適合しなければならない。
注記 シリコーン油基準には,厚生労働省が定めたシリコーン油基準がある。
5.4.2
潤滑剤の量
潤滑剤の量は,針管の表面に液滴を認めたり,内面にたまりを認める量であってはならない。
5.5
外針
5.5.1
寸法の許容差
針管の寸法の許容差は,次による。
a) 針管の公称外径に対する許容差は,−3〜+8 %でなければならない。
b) 針管の公称長さに対する許容差は,10 mm以下のものは±20 %,10 mmを超え20 mm未満のものは
±8 %,20 mm以上40 mm未満のものは±7 %,40 mm以上60 mm未満のものは±5 %,60 mm以上
のものは±3 %でなければならない。
5.5.2
テーパの合致
JIS T 3210:2011に適合した注射筒などのテーパに接続することを意図したものにあっては,図2に示す
ISO 594-1:1986で規定するおす・ルアーテーパ検査ゲージ[ISO 594-1:1986の図3参照]へ,針基を5 N
の力でゲージには(嵌)めたとき,針基の接続部のめす・ルアーテーパとゲージのテーパとが合致し,か
つ,針基の先端部は,ゲージの限度内になければならない。また,この検査ゲージを使用できない構造の
ものは,この検査ゲージの要求する寸法に等しい寸法を求めることができるような特別の検査ゲージ,例
えば,ISO 594-2:1998に規定する検査ゲージを用いる。
5
T 3307:2013
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
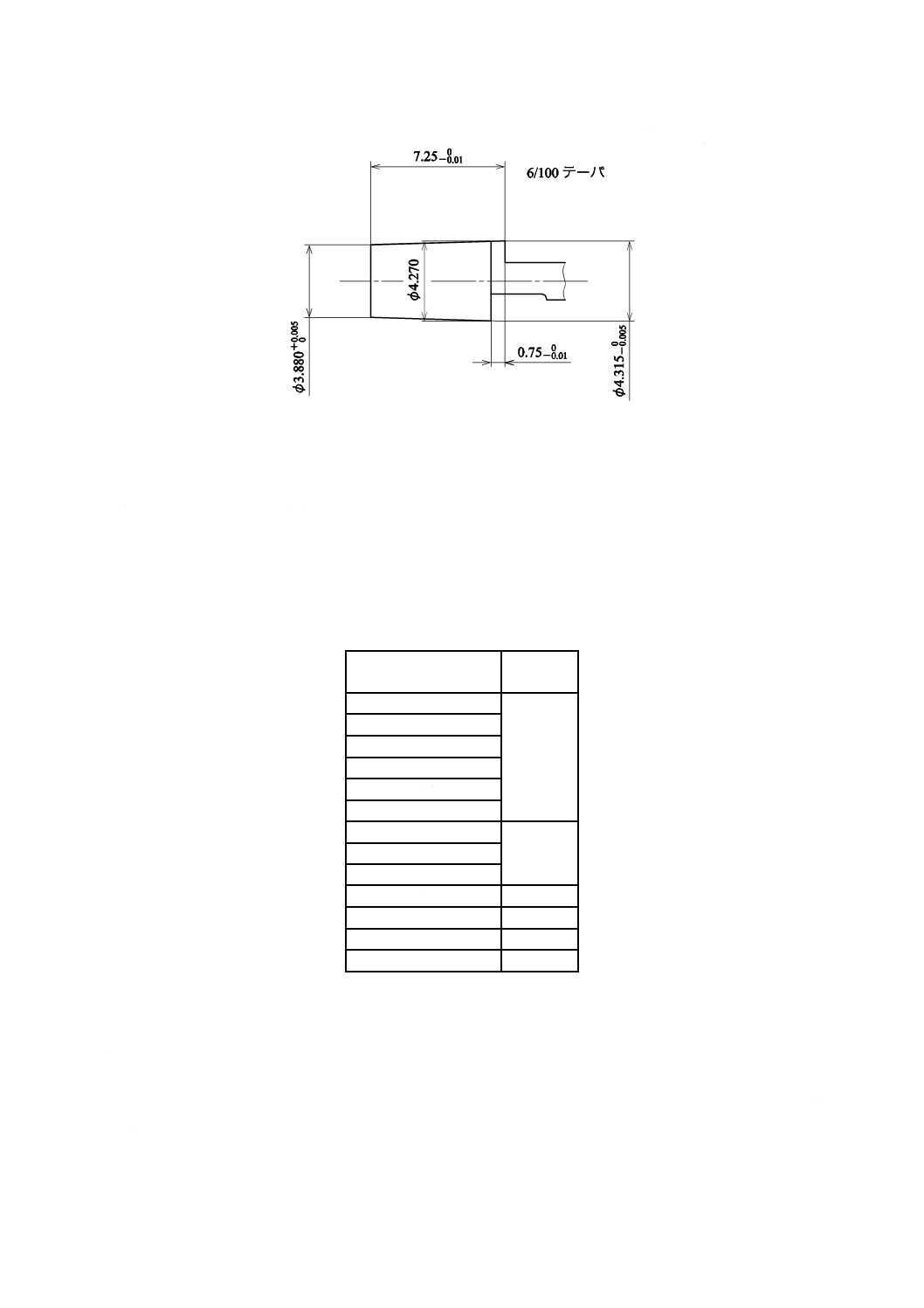
単位 mm
図2−おす・ルアーテーパ検査ゲージ
5.5.3
適用ガイドワイヤ
内くう(腔)にガイドワイヤを挿入するものは,適合するガイドワイヤが内くう(腔)を通過できなけ
ればならない。また,その適合するガイドワイヤの外径を添付文書などで明確に表示する。
5.5.4
引張強さ
外針針管の公称外径に応じて,外針針管の中心軸方向に表1の力を加えたとき,外針針管は外針針基か
ら引き抜けてはならない。
表1−外針の引張強さ
外針針管の公称外径
mm
力
N
0.3
22
0.33
0.36
0.4
0.45
0.5
0.55
34
0.6
0.65
0.7
40
0.8
44
0.9
54
1.1以上
69
5.5.5
漏れ
次のいずれかの試験に適合しなければならない。
a) 第1法 外針をJIS T 3210:2011に適合した注射筒の筒先に27.5 Nの力では(嵌)め合わせる。この
とき,少しねじってもよい。注射筒のファーストラインを5 mLの目盛に合わせ,外針針管の先端に
ゴム栓を刺し,針先から空気が漏れないようにした後,針先から外針針基までを水中に没する。注射
筒のファーストラインを2 mLの目盛まで押し,15秒間観察する。この間,外針針管と外針針基との
接合部,又は外針針基と注射筒の筒先とのは(嵌)め合せ部から連続した気泡の発生を認めてはなら
6
T 3307:2013
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
ない。
b) 第2法 外針針基を,水圧試験装置に取り付けられた,ISO 594-1:1986で規定する漏れ試験用おす(雄)
円すい(錐)かん(嵌)合具(Reference steel male conical fitting)に,27.5 Nの力では(嵌)め合わせ
る。このとき,少しねじってもよい。次に,外針針管の先端にゴム栓を刺し,針先から水が漏れない
ようにした後,0.2 MPaのゲージ圧で水を送り込み,15秒間観察する。この間,外針針管と外針針基
と漏れ試験用おす(雄)円すい(錐)かん(嵌)合具とのは(嵌)め合せ部から,水滴となって落ち
るような水漏れがあってはならない。
5.5.6
弾性
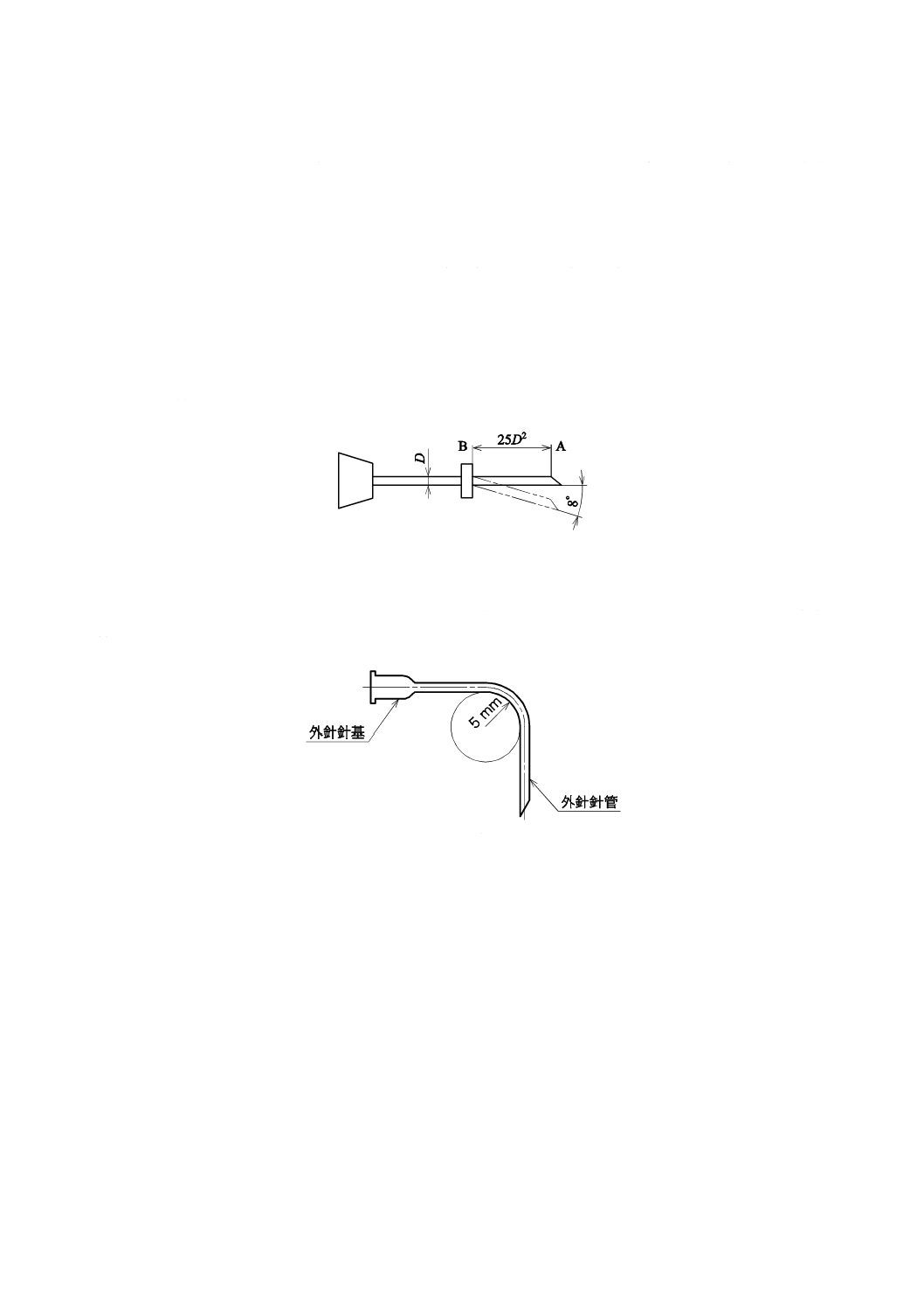
外針針管の公称外径(図3のD)が1.0 mm以下のものは,図3のように,外針針管の先端の一点Aか
ら25D2離れた外針針管上の点Bを固定し,Aに力を加え,8度曲げて1分間保った後,放して目視したと
き,外針針管は,元の位置に復していなければならない。
図3−弾性
5.5.7
曲げ強さ
外針針管の公称外径が1.0 mm以下で,かつ,公称長さが12 mm以上のものは,図4のように,外針針
管を5 mmの曲率半径で90度曲げたとき,折れてはならない。
図4−曲げ強さ
5.6
内針
5.6.1
コアリングの防止
内針刃面が外針刃面と一致するなど,コアリングを防止するようになっていなければならない。
5.6.2
引張強さ
内針針管の実外径に応じて,内針針管の中心軸方向に表2の力を加えたとき,内針針管はつまみから引
き抜けてはならない。

7
T 3307:2013
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
表2−内針の引張強さ
内針針管の実外径
mm
力
N
0.55未満
22
0.55 以上〜0.7未満
34
0.7 以上〜0.8未満
40
0.8 以上〜0.9未満
44
0.9 以上〜1.1未満
54
1.1 以上
69
6
化学的要求事項
6.1
試験液及び空試験液の調製
6.1.1
試験液
胆管造影用針25本を,ほうけい酸ガラスでできた適切な容器に入れ,250 mLの精製水を加え胆管造影
用針を浸せきし(外針針管の内側を含めて,精製水に接触するようにする。),3730
+℃で60±2分間加温し
た後,室温になるまで冷却し,胆管造影用針の内外面から全ての水を容器に戻すようにして胆管造影用針
を取り除き,この液を試験液とする。
6.1.2
空試験液
同時に胆管造影用針を入れない精製水を,同様の方法で操作し空試験液を調製する。
6.2
pH
試験液及び空試験液のpHを,日局の一般試験法のpH測定法で測定したとき,両液のpHの差は1以下
でなければならない。
6.3
溶出金属物の制限
原子吸光光度法又はこれと同等以上の微量分析法によって,試験液及び空試験液を分析し,試験液の測
定値を空試験液の測定値で補正したとき,試験液中の鉛,亜鉛及び鉄の合計は5 mg/L以下で,かつ,試験
液のカドミウム測定値を空試験液のカドミウム測定値で補正したとき,試験液のカドミウム含量は0.1
mg/L以下でなければならない。
7
生物学的安全性
JIS T 0993-1:2012に規定する生物学的安全性の評価を行う。
8
無菌性の保証
無菌性を保証する場合は,滅菌バリデーション基準又はこれと同等以上の基準に基づき,無菌性の担保
を行う。
注記 滅菌バリデーション基準には,厚生労働省が定めた滅菌バリデーション基準がある。
9
エンドトキシン
胆管造影用針10本をとり,硬質ガラスの容器に入れ,エンドトキシン試験用水30 mLを加え,溶封又
は適切な栓で密封してよく振り混ぜた後,室温で1時間放置し,この液を試験液として,日局の一般試験
法のエンドトキシン試験法によって試験をしたとき,0.5 EU/mL未満でなければならない。又はこれと同
等以上の基準に適合しなければならない。
8
T 3307:2013
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
10 包装
10.1 一次包装
一次包装は,微生物の侵入を防止することができ,通常の取扱い,輸送及び保管中に製品を適切に保護
できるものでなければならない。また,一度開封したら,包装は簡単に再シールできず,開封したことが
明確に分かるものでなければならない。
無菌維持を目的としない場合には,一次包装は,通常の取扱い,輸送及び保管中に製品を適切に保護で
きるものでなければならない。
10.2 二次包装
二次包装は,通常の取扱い,輸送及び保管中に製品を保護できる強度をもたなければならない。
11 表示
11.1 一次包装
一次包装には,次の事項を表示する。
a) 外針針管の外径(mm)及び長さ(mm)。また,外径表示に,ゲージを参考で併記してもよい。
注記 ゲージは,Gなどで表記する。
b) 滅菌済みのものにあっては“滅菌済み”の旨
c) 製造番号又は製造記号
d) 一次包装で無菌性を保証していないものは,その旨
11.2 二次包装
二次包装には,次の事項を表示する。ただし,二次包装を用いないで,一次包装を最小販売単位の包装
として用いる場合には,次の事項を一次包装に表示する。
なお,製造番号又は製造記号が滅菌年月を表している場合は,改めて滅菌年月の表示をする必要はない。
また,滅菌年月の代わりに使用期限を表示してもよい。
a) 製造販売業者の氏名又は名称,及び住所
b) 販売名
c) 外針針管の外径(mm)及び長さ(mm)。また,外径表示に,ゲージを参考で併記してもよい。
注記 ゲージは,Gなどで表記する。
d) 数量(入り数)
e) 滅菌済みのものにあっては“滅菌済み”の旨
f)
“再使用禁止”の旨(“ディスポーザブル”の表現は使用しない。)
g) 製造番号又は製造記号
h) 滅菌年月
i)
他の法定表示事項
11.3 図記号の使用
11.1及び11.2は,JIS T 0307:2004に規定する適切な図記号を使用することによって,これに替えてもよ
い。
注記 JIS T 0307:2004に規定する主な図記号の例を,表3に示す。

9
T 3307:2013
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
表3−JIS T 0307に規定する主な図記号の例