T 3264:2018
(1)
目 次
ページ
序文 ··································································································································· 1
1 適用範囲························································································································· 1
2 引用規格························································································································· 1
3 用語及び定義 ··················································································································· 1
4 構成及び各部の名称 ·········································································································· 2
5 要求事項························································································································· 3
5.1 外観及び清浄度 ············································································································· 3
5.2 引張強さ ······················································································································ 3
5.3 気密性 ························································································································· 3
5.4 コネクタ ······················································································································ 3
5.5 経腸栄養三方活栓 ·········································································································· 4
6 無菌性の保証 ··················································································································· 5
7 生物学的安全性 ················································································································ 5
8 包装······························································································································· 5
8.1 一次包装 ······················································································································ 5
8.2 二次包装 ······················································································································ 5
9 表示······························································································································· 5
9.1 一次包装 ······················································································································ 5
9.2 二次包装 ······················································································································ 5
9.3 図記号の使用 ················································································································ 6
T 3264:2018
(2)
まえがき
この規格は,工業標準化法第14条によって準用する第12条第1項の規定に基づき,一般社団法人日本
医療機器テクノロジー協会(MTJAPAN)及び一般財団法人日本規格協会(JSA)から,工業標準原案を具
して日本工業規格を改正すべきとの申出があり,日本工業標準調査会の審議を経て,厚生労働大臣が改正
した日本工業規格である。
これによって,JIS T 3264:2013は改正され,この規格に置き換えられた。
この規格は,著作権法で保護対象となっている著作物である。
この規格の一部が,特許権,出願公開後の特許出願又は実用新案権に抵触する可能性があることに注意
を喚起する。厚生労働大臣及び日本工業標準調査会は,このような特許権,出願公開後の特許出願及び実
用新案権に関わる確認について,責任はもたない。
日本工業規格 JIS
T 3264:2018
経腸栄養延長チューブ
Extension tubes for enteral feeding for single use
序文
この規格は,2007年に制定され,2013年の改正を経て,今日に至っている。その後,この規格で規定し
ているコネクタ規格に関して,新たにISO 80369-3が制定されたため,この規格においても引用規格を追
加するよう改正をした。
1
適用範囲
この規格は,栄養投与又は減圧を目的とした経腸栄養投与セット,経腸栄養カテーテルなどの自然落下
式及びポンプ式のラインを延長するために用いるもので,そのまま直ちに使用でき,かつ,単回使用の経
腸栄養延長チューブについて規定する。ただし,未滅菌品は,箇条6,9.1 a),9.2 d)及び9.2 i)を適用しな
い。
注記 2021年4月30日までJIS T 3264:2013を適用することができる。
2
引用規格
次に掲げる規格は,この規格に引用されることによって,この規格の規定の一部を構成する。これらの
引用規格のうちで,西暦年を付記してあるものは,記載の年の版を適用し,その後の改正版(追補を含む。)
は適用しない。西暦年の付記がない引用規格は,その最新版(追補を含む。)を適用する。
JIS T 0307 医療機器−医療機器のラベル,ラベリング及び供給される情報に用いる図記号
JIS T 0993-1:2012 医療機器の生物学的評価−第1部:リスクマネジメントプロセスにおける評価及
び試験
JIS T 3213:2018 栄養用チューブ及びカテーテル
ISO 80369-3:2016,Small-bore connectors for liquids and gases in healthcare applications−Part 3: Connectors
for enteral applications
3
用語及び定義
この規格で用いる主な用語及び定義は,次による。
3.1
おす(雄)コネクタ
経腸栄養投与セット又は経腸栄養カテーテルに接続する部材。誤接続防止タイプである(図1参照)。
3.2
導管
栄養剤,治療食などを体内に導く流路又は減圧の通路となる管。
2
T 3264:2018
3.3
めす(雌)コネクタ
経腸栄養投与セット又は経腸栄養カテーテルに接続する部材。おす(雄)コネクタと接続できる構造の
もの。
3.4
キャップ
かん(嵌)合部が直接外部に触れることを防ぐためのもの。
3.5
経腸栄養三方活栓
経腸栄養に用いる流路切替可能な機器。接続部は,誤接続防止タイプである(図1参照)。コックを回転
することで流路が切り替わる。
3.6
一次包装
経腸栄養延長チューブ又は各構成品を直接に覆う包装で,経腸栄養延長チューブ又は各構成品の無菌性
を保持するためのもの。さらに,これを二次包装する場合には,いわゆる“内袋”に該当する。ただし,
一次包装で無菌性を保持しないものもあり,その場合は,キャップなどによって経腸栄養延長チューブ又
は各構成品の内部の無菌性を保持している。
3.7
二次包装
一次包装を直接に覆う包装。通常,一次包装した経腸栄養延長チューブ又は各構成品を複数(例えば,
50本)入れた包装。
4
構成及び各部の名称
経腸栄養延長チューブは,主として,おす(雄)コネクタ,導管,めす(雌)コネクタ及びキャップか
らなり,おす(雄)コネクタ及びめす(雌)コネクタをもつ経腸栄養三方活栓を附属するものもある。
一般的な経腸栄養延長チューブの構成及び各部の例を,図1に示す。
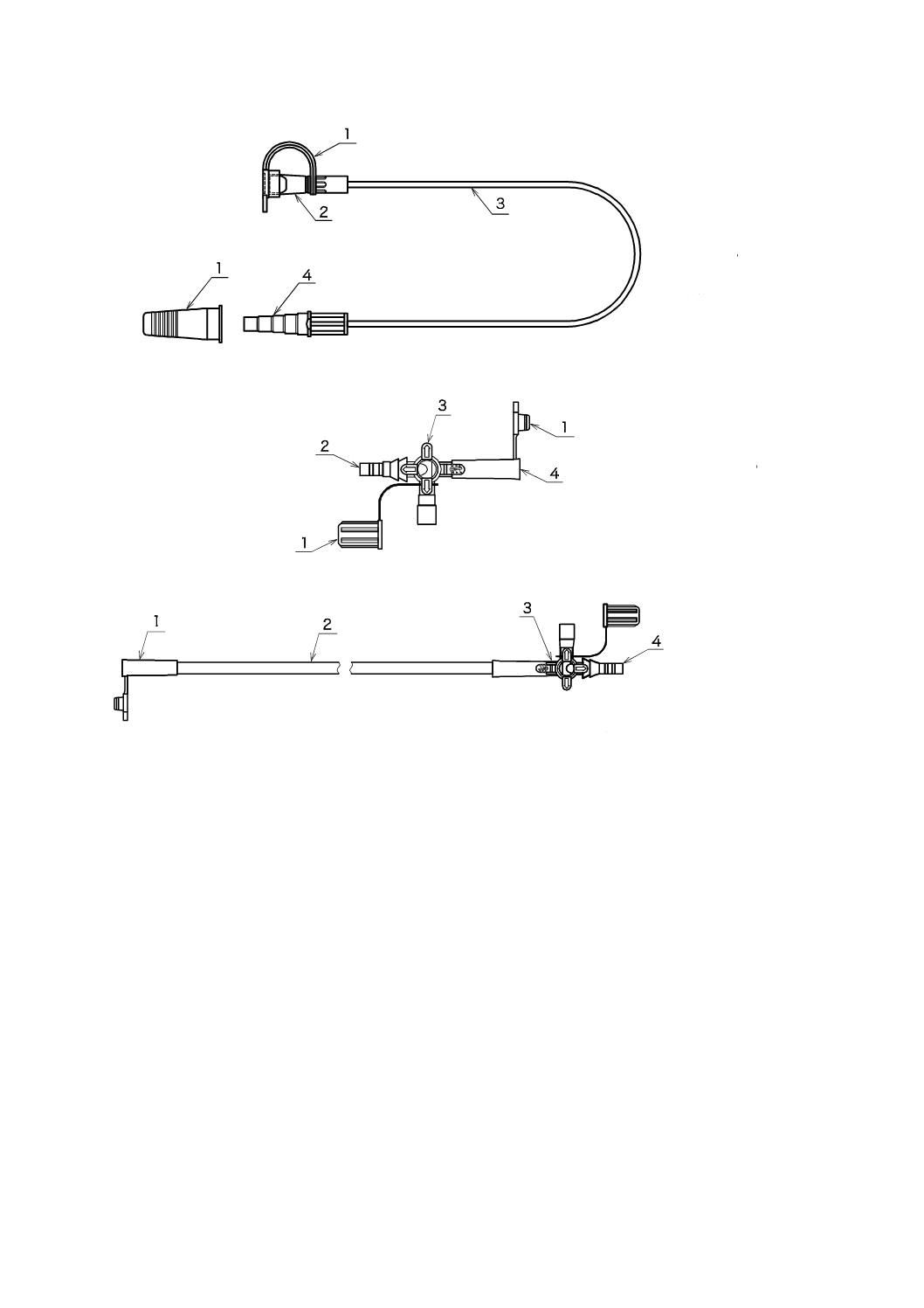
3
T 3264:2018
1 キャップ
2 めす(雌)コネクタ
3 導管
4 おす(雄)コネクタ
a) 一般的な経腸栄養延長チューブ
1 キャップ
2 おす(雄)コネクタ
3 コック
4 めす(雌)コネクタ
b) 一般的な経腸栄養三方活栓
1 めす(雌)コネクタ
2 導管
3 三方活栓
4 おす(雄)コネクタ
c) 一般的な三方活栓付経腸栄養延長チューブ
図1−経腸栄養延長チューブの構成及び各部の名称例
5
要求事項
5.1
外観及び清浄度
目視で試験したとき,内面に異物の付着があってはならない。
5.2
引張強さ
ISO 80369-3に適合するコネクタの接続部を除いた全ての接合部及び接続部は,15 Nの力で15秒間引っ
張ったとき,破断,外れなどが生じてはならない。
5.3
気密性
5.3.1
ポンプ用経腸栄養延長チューブ
ポンプ用経腸栄養延長チューブは,JIS T 3213の4.1.3.1に適合しなければならない。
5.3.2
自然落下式経腸栄養延長チューブ
自然落下式経腸栄養延長チューブは,JIS T 3213の4.1.3.2に適合しなければならない。
5.4
コネクタ
5.4.1
おす(雄)コネクタ
経腸栄養延長チューブ及び経腸栄養三方活栓のおす(雄)コネクタは,ISO 80369-3に適合するもの,
4
T 3264:2018
又は図2の形状に適合するものでなければならず,ISO 80369-7及びJIS T 3201に規定する6 %(ルアー)
テーパをもつ形状であってはならない。さらに,おす(雄)コネクタは,経腸栄養カテーテル又は経腸栄
養投与セットと接続したとき,変形を起こしてはならない。
注記 ISO 80369-3の適用範囲に該当する製品が図2の形状を適用できる期間については,“経腸栄養
分野の小口径コネクタ製品の切替えについて”(平成30年3月16日付け医政安発0316第1号,
薬生薬審発0316第1号,薬生機審発0316第1号,薬生安発0316第1号厚生労働省医政局総務
課医療安全推進室長,医薬・生活衛生局医薬品審査管理課長,同医療機器審査管理課長,同医
薬安全対策課長連名通知)に示されている。
5.4.2
めす(雌)コネクタ
経腸栄養延長チューブ及び経腸栄養三方活栓のめす(雌)コネクタは,ISO 80369-3に適合するもの,
又は図2のコネクタと接続できる構造のものでなければならない。
注記 ISO 80369-3の適用範囲に該当する製品が図2の形状を適用できる期間については,“経腸栄養
分野の小口径コネクタ製品の切替えについて”(平成30年3月16日付け医政安発0316第1号,
薬生薬審発0316第1号,薬生機審発0316第1号,薬生安発0316第1号厚生労働省医政局総務
課医療安全推進室長,医薬・生活衛生局医薬品審査管理課長,同医療機器審査管理課長,同医
薬安全対策課長連名通知)に示されている。
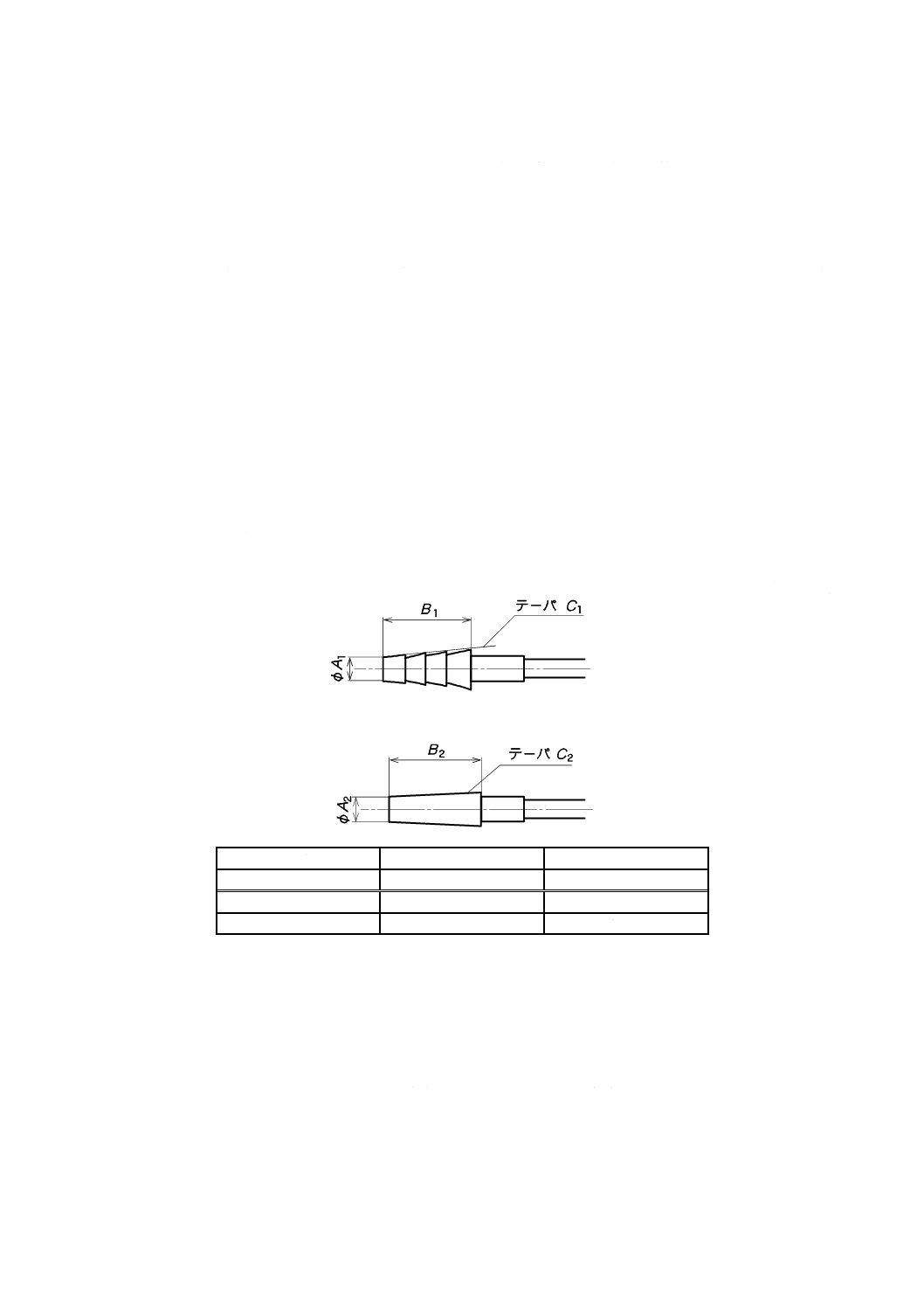
単位 mm
φA1
B1
テーパC1
6.0±0.5
15以上
125±25/1 000
φA2
B2
テーパC2
6.0±0.5
15以上
125±25/1 000
注記 図2の形状は,“医薬発第888号:平成12年8月31日,医療事故を防止するための医療用具に関する基準
の制定等について(注射筒型手動式医薬品注入器基準等)”による。
図2−経腸栄養延長チューブのコネクタ
5.5
経腸栄養三方活栓
経腸栄養三方活栓は,5.1,5.3及び5.4に適合し,かつ,コックの回転軸方向に15 Nの静的な力を15
秒間加えたとき,この力に耐えなければならない。さらに,空気,微生物及び液体が染み通らない気密性
をもち,どのコック位置においても確実に固定していなければならない。経腸栄養三方活栓を滑らすため
に潤滑剤を用いる場合は,潤滑剤はシリコーン油基準又はこれと同等以上の基準に適合しなければならな
5
T 3264:2018
い。
注記 シリコーン油基準には,厚生労働省が定めたシリコーン油基準がある。
6
無菌性の保証
無菌性を保証する場合は,滅菌バリデーション基準又はこれと同等以上の基準に基づき,無菌性の担保
を行う。
注記 滅菌バリデーション基準には,厚生労働省が定めた滅菌バリデーション基準がある。
7
生物学的安全性
JIS T 0993-1に規定する生物学的安全性の評価を行う。
8
包装
8.1
一次包装
一次包装は,微生物の侵入を防止することができ,かつ,通常の取扱い,輸送及び保管中に,内容製品
を適切に保護できるものでなければならない。また,一次包装は,一度開封したならば,簡単に再シール
できず,開封したことが明確に分からなければならない。ただし,一次包装で無菌性を保証しないものは,
キャップなどで内部の無菌性を保持する。
無菌維持を目的としない場合には,一次包装は,通常の取扱い,輸送及び保管中に製品を適切に保護で
きるものでなければならない。
8.2
二次包装
二次包装は,通常の取扱い,輸送及び保管中に内容製品を保護できる強度をもたなければならない。
9
表示
9.1
一次包装
一次包装には,次の事項を表示する。
a) “滅菌済み”の旨
b) 経腸栄養ポンプと併用する経腸栄養延長チューブである場合は,“使用限度圧”又は組合せ使用で安全
を保証しているポンプの機種名
c) “自然落下式”の場合は,“経腸栄養ポンプを使用できない”旨。ただし,添付文書又はその名称から
明らかな場合は,この限りではない。
d) 製造番号又は製造記号
e) 一次包装で無菌性を保証していないものは,その旨
9.2
二次包装
二次包装には,次の事項を表示する。ただし,二次包装を用いないで,一次包装を最小販売単位の包装
として用いる場合には,次の事項を一次包装に表示する。
なお,製造番号又は製造記号が滅菌年月を表している場合には,改めて滅菌年月の表示をする必要はな
い。また,滅菌年月の代わりに使用期限を表示してもよい。
a) 製造販売業者の氏名又は名称,及び住所
b) 販売名
c) 数量(入り数)
6
T 3264:2018
d) “滅菌済み”の旨
e) “再使用禁止”の旨(“ディスポーザブル”の表現は使用しない。)
f)
経腸栄養ポンプと併用する経腸栄養延長チューブである場合は,“使用限度圧”又は組合せ使用で安全
を保証しているポンプの機種名
g) “自然落下式”の場合は,“経腸栄養ポンプを使用できない”旨。ただし,添付文書又はその名称から
明らかな場合は,この限りでない。
h) 製造番号又は製造記号
i)
滅菌年月
j)
他の法定表示事項
k) ISO 80369-3をかん(嵌)合部に用いた場合には,識別表示を行う。識別は,ISO 80369-3の文字又は
ISO 80369-3に適合した製品である旨を表示する。
9.3
図記号の使用
9.1及び9.2は,JIS T 0307に規定する適切な図記号を使用することによってこれに替えてもよい。
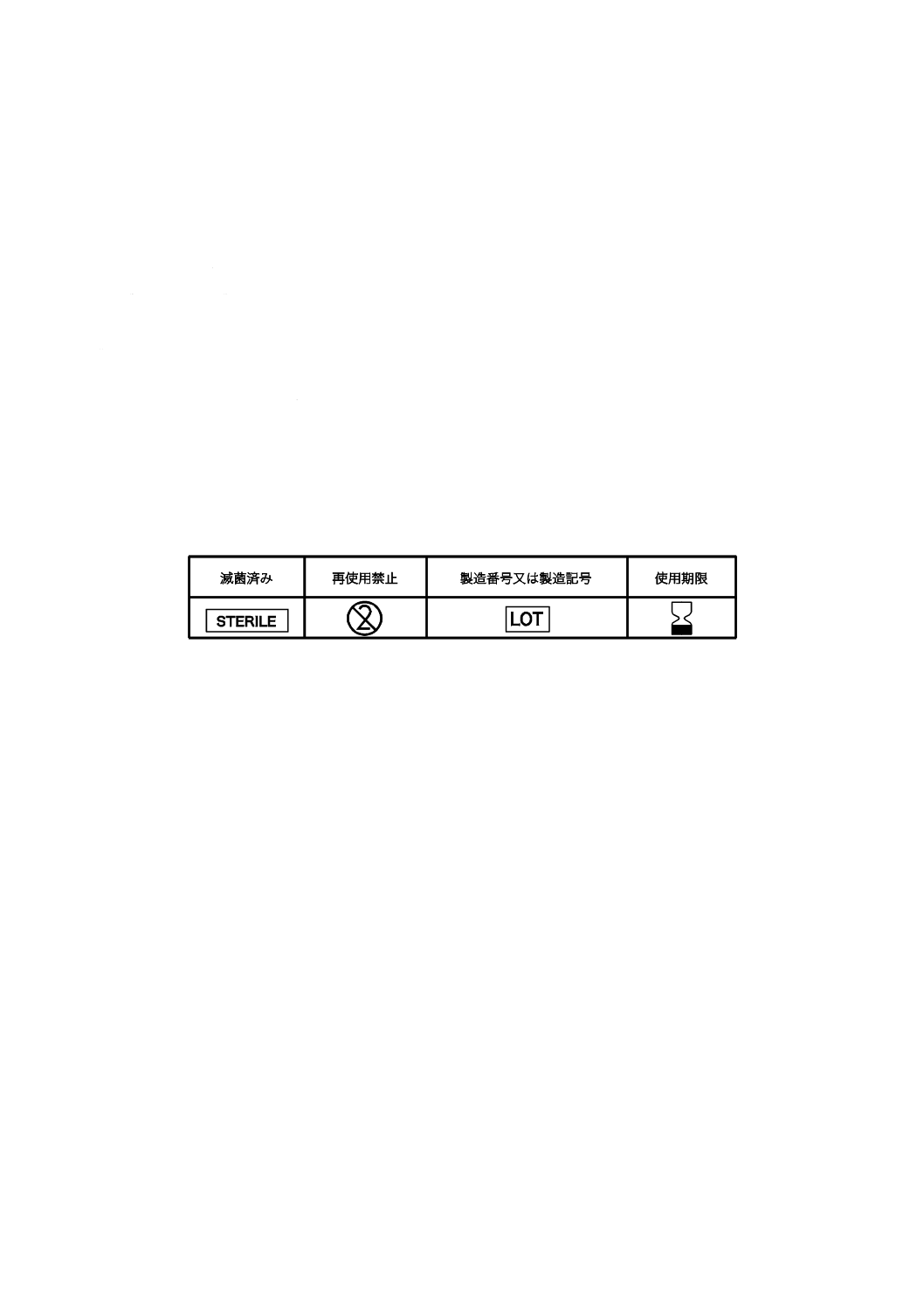
注記 JIS T 0307に規定する主な図記号の例を,表1に示す。
表1−JIS T 0307に規定する主な図記号の例


