T 3236:2011
(1)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
目 次
ページ
序文 ··································································································································· 1
1 適用範囲 ························································································································· 1
2 引用規格 ························································································································· 1
3 用語及び定義 ··················································································································· 1
4 構成及び各部の名称 ·········································································································· 2
4.0 一般 ···························································································································· 2
4.1 シャフト ······················································································································ 2
4.2 吸引孔 ························································································································· 2
5 要求事項 ························································································································· 2
5.1 シャフトの外径 ············································································································· 2
5.2 シャフトの目盛 ············································································································· 2
5.3 引張強さ ······················································································································ 3
5.4 バルーンの機能性試験 ···································································································· 3
5.5 外観及び清浄度 ············································································································· 3
5.6 生物学的安全性 ············································································································· 3
5.7 無菌性の保証 ················································································································ 3
6 包装······························································································································· 3
6.1 一次包装 ······················································································································ 3
6.2 二次包装 ······················································································································ 3
7 表示······························································································································· 3
7.1 一次包装 ······················································································································ 3
7.2 二次包装 ······················································································································ 3
7.3 記号の使用 ··················································································································· 4
附属書A(規定)引張強さ試験 ······························································································· 5
附属書B(規定)機能性試験 ·································································································· 6
T 3236:2011
(2)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
まえがき
この規格は,工業標準化法第14条によって準用する第12条第1項の規定に基づき,日本医療器材工業
会(JMED)及び財団法人日本規格協会(JSA)から,工業標準原案を具して日本工業規格を改正すべきと
の申出があり,日本工業標準調査会の審議を経て,厚生労働大臣が改正した日本工業規格である。
これによって,JIS T 3236:2005は改正され,この規格に置き換えられた。
この規格は,著作権法で保護対象となっている著作物である。
この規格の一部が,特許権,出願公開後の特許出願又は実用新案権に抵触する可能性があることに注意
を喚起する。厚生労働大臣及び日本工業標準調査会は,このような特許権,出願公開後の特許出願及び実
用新案権に関わる確認について,責任はもたない。
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
日本工業規格 JIS
T 3236:2011
胃・食道静脈りゅう(瘤)圧迫止血用チューブ
Styptic balloon
序文
この規格は,2005年に制定されたJIS T 3236の見直しにおいて,使用者の利便性のため,用語,文書構
成などの内容を変更して改正した日本工業規格である。
1
適用範囲
この規格は,胃・食道静脈りゅう(瘤)出血に対して,圧迫止血を行うために用いる胃・食道静脈りゅ
う(瘤)圧迫止血用チューブ(以下,チューブという。)について規定する。
なお,この規格は,金属を用いて一時的(24時間を超えない)に体内に挿入するものには適用しない。
なお,平成26年7月28日までJIS T 3236:2005は適用することができる。
2
引用規格
次に掲げる規格は,この規格に引用されることによって,この規格の規定の一部を構成する。これらの
引用規格は,記載の西暦年の版を適用し,その後の改正版(追補を含む。)は適用しない。
JIS T 0307:2004 医療機器−医療機器のラベル,ラベリング及び供給される情報に用いる図記号
JIS T 0993-1:2005 医療機器の生物学的評価−第1部:評価及び試験
JIS T 3210:2011 滅菌済み注射筒
3
用語及び定義
この規格で用いる主な用語及び定義は,次による。
3.1
胃・食道静脈りゅう(瘤)圧迫止血用チューブ
柔軟性があり,胃・食道静脈りゅう(瘤)破裂による出血を止血する目的で経鼻的に胃又は食道内に挿
入留置する医療機器。
3.2
バルーン
圧迫止血又はチューブの固定を行うために,胃又は食道で膨張させるもの。
3.3
シャフト
主に体内に挿入されるチューブの部分。
3.4
吸引孔
シャフトの側面開口部。
2
T 3236:2011
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
3.5
スタイレット
チューブを挿入するときに,補強のためにチューブ内くう(腔)に挿入するもの。
3.6
吸引用端子
吸引孔から胃又は食道内の内容物を吸引するためのもの。
3.7
シリンジ接続端子
バルーンを膨張させるために用いるシリンジを接続するためのもの。
3.8
マノメータ接続端子
バルーンにかかる圧力を測定する医療機器と接続するためのもの。
3.9
クランプ
バルーンに注入した空気が漏れないようにするためのもの。
4
構成及び各部の名称
4.0
一般
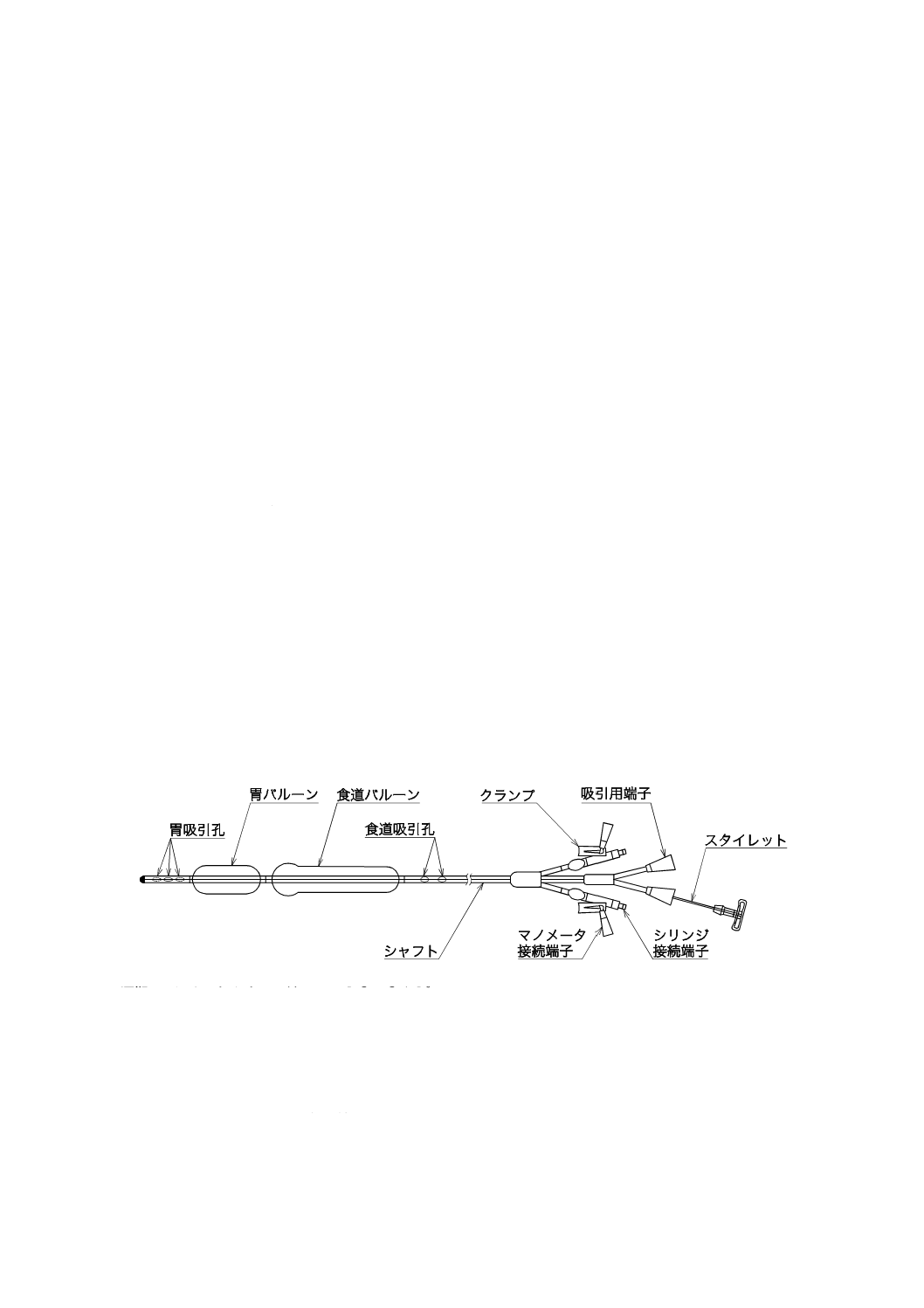
一般的なチューブの構成及び各部の名称を図1に示し,シャフト及び吸引孔は次による。ただし,図1
は,チューブの構成及び各部の名称の例である。
4.1
シャフト
シャフトは,一つ又は複数のバルーンをもつものとする。
4.2
吸引孔
シャフトは,複数個の吸引孔をもつものとする。
注記 スタイレットなどが付いているものもある。
図1−チューブの構成及び各部の名称例
5
要求事項
5.1
シャフトの外径
シャフトの外径は,7.2 d)の表示値の±10 %以内とする。
5.2
シャフトの目盛
シャフトには,挿入の目安となるマーク,目印などが付いていなければならない。
3
T 3236:2011
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
5.3
引張強さ
附属書Aによって試験したとき,シャフトは破断してはならない。
5.4
バルーンの機能性試験
附属書Bによって試験したとき,バルーンの破裂及びバルーンからの空気漏れがあってはならない。
5.5
外観及び清浄度
目視で検査したとき,きず,ばり又は異物の付着があってはならない。
5.6
生物学的安全性
JIS T 0993-1に規定する生物学的安全性の評価を行う。
5.7
無菌性の保証
“滅菌済み”の旨を表示するものは,滅菌バリデーション基準又はこれと同等以上の基準に基づき,無
菌性の担保を行う。
注記 滅菌バリデーション基準には,厚生労働省が定めた滅菌バリデーション基準がある。
6
包装
6.1
一次包装
一次包装は,微生物の侵入を防止することができ,通常の取扱い,輸送及び保管中に,内容製品を適切
に保護できるものでなければならない。一次包装は,一度開封したら,簡単に再シールできず,開封され
たことが明確に分からなければならない。
6.2
二次包装
二次包装は,通常の取扱い,輸送及び保管中に,内容製品を保護できる強度をもつものとする。
7
表示
7.1
一次包装
一次包装には,次の事項を表示する。
なお,製造番号又は製造記号が滅菌年月を表示している場合は,改めて滅菌年月の表示をする必要はな
い。また,滅菌年月の代わりに使用期限を表示してもよい。
a) 製造販売業者の氏名又は名称,及び住所
b) 医療機器の認証番号
c) 販売名
d) シャフトの外径(mm)及び長さ(mm又はcm)。ただし,外径をミリメートル(mm)で示すほか,
フレンチ(シャリエール)又はゲージを参考で併記してもよい。
注記 フレンチ(シャリエール)は,F(Ch)などで表記する。1 mmが3 F(Ch)に相当し,1/3 mm
刻みで表記する。ゲージは,Gなどで表記する。
e) “滅菌済み”の旨
f)
“再使用禁止”の旨(“ディスポーザブル”の表現は使用しない。)
g) “天然ゴム”を使用しているものは,その旨
h) 製造番号又は製造記号
i)
滅菌年月
7.2
二次包装
二次包装には,次の事項を表示する。ただし,二次包装を用いず,一次包装を最小販売単位の包装とし

4
T 3236:2011
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
て用いる場合は,次の事項を一次包装に表示する。
なお,製造番号又は製造記号が滅菌年月を表示している場合は,改めて滅菌年月の表示をする必要はな
い。また,滅菌年月の代わりに使用期限を表示してもよい。
a) 製造販売業者の氏名又は名称,及び住所
b) 医療機器の認証番号
c) 販売名
d) シャフトの外径(mm)及び長さ(mm又はcm)。ただし,外径をミリメートル(mm)で示すほか,
フレンチ(シャリエール)又はゲージを参考で併記してもよい。
注記 フレンチ(シャリエール)は,F(Ch)などで表記する。1 mmが3 F(Ch)に相当し,1/3 mm
刻みで表記する。ゲージは,Gなどで表記する。
e) 数量(入り数)
f)
“滅菌済み”の旨
g) “再使用禁止”の旨(“ディスポーザブル”の表現は使用しない。)
h) “天然ゴム”を使用しているものは,その旨
i)
製造番号又は製造記号
j)
滅菌年月
7.3
記号の使用
7.1及び7.2は,JIS T 0307に規定する適切な記号を使用することによって,これに替えてもよい。
注記 JIS T 0307に規定する主な記号の例を,表1に示す。
表1−JIS T 0307に規定する主な記号の例
5
T 3236:2011
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書A
(規定)
引張強さ試験
A.1 概要
シャフトの試験箇所を選択し,試料の破断の有無を試験する。
A.2 試験装置
試験装置は,9.8 N以上の引張力が負荷できる引張試験機とする。
A.3 試験手順
試験手順は,次による。
a) シャフトから試料を採り,試験を行う。
b) 試料を引張試験機に固定する。
c) 試料に9.8 Nの引張力を加える。
A.4 試験報告書
試験報告書には,次の事項を記載する。
a) 試験に供したチューブの名称,形式,製造番号(又は製造記号)など。
b) 試料の破断の有無及び試料の外径。
6
T 3236:2011
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書B
(規定)
機能性試験
B.1
概要
空気で胃及び食道バルーンを膨張させたとき,バルーンからの空気漏れの有無及びバルーンの破裂の有
無を試験する。
B.2
試験装置
試験装置は,次による。
a) 水槽 バルーンを完全に水没させるのに十分な容積をもつもの。
b) 注射筒 JIS T 3210に適合するもの。
B.3
試験手順
試験手順は,次による。
a) 食道バルーン 食道バルーンを6 kPa(45 mmHg)の圧力になるまで,注射筒を用いて空気を注入す
る。膨張した状態のバルーンを完全に水槽内に水没させ,30秒間保持する。その間,バルーンからの
空気漏れの有無及び破裂の有無を目視によって検査する。
b) 胃バルーン 胃バルーンは,添付文書又は取扱説明書に記載の空気注入量を,注射筒を用いてバルー
ンに注入する。膨張した状態のバルーンを完全に水槽内に水没させ,30秒間保持する。その間,バル
ーンからの空気漏れの有無及び破裂の有無を目視によって検査する。
B.4
試験報告書
試験報告書には,次の事項を記載する。
a) 試験に供したチューブの名称,形式,製造番号(又は製造記号)など。
b) 試験結果として胃及び食道バルーンの空気漏れの有無及び破裂の有無。

