4
T 3220:2011
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
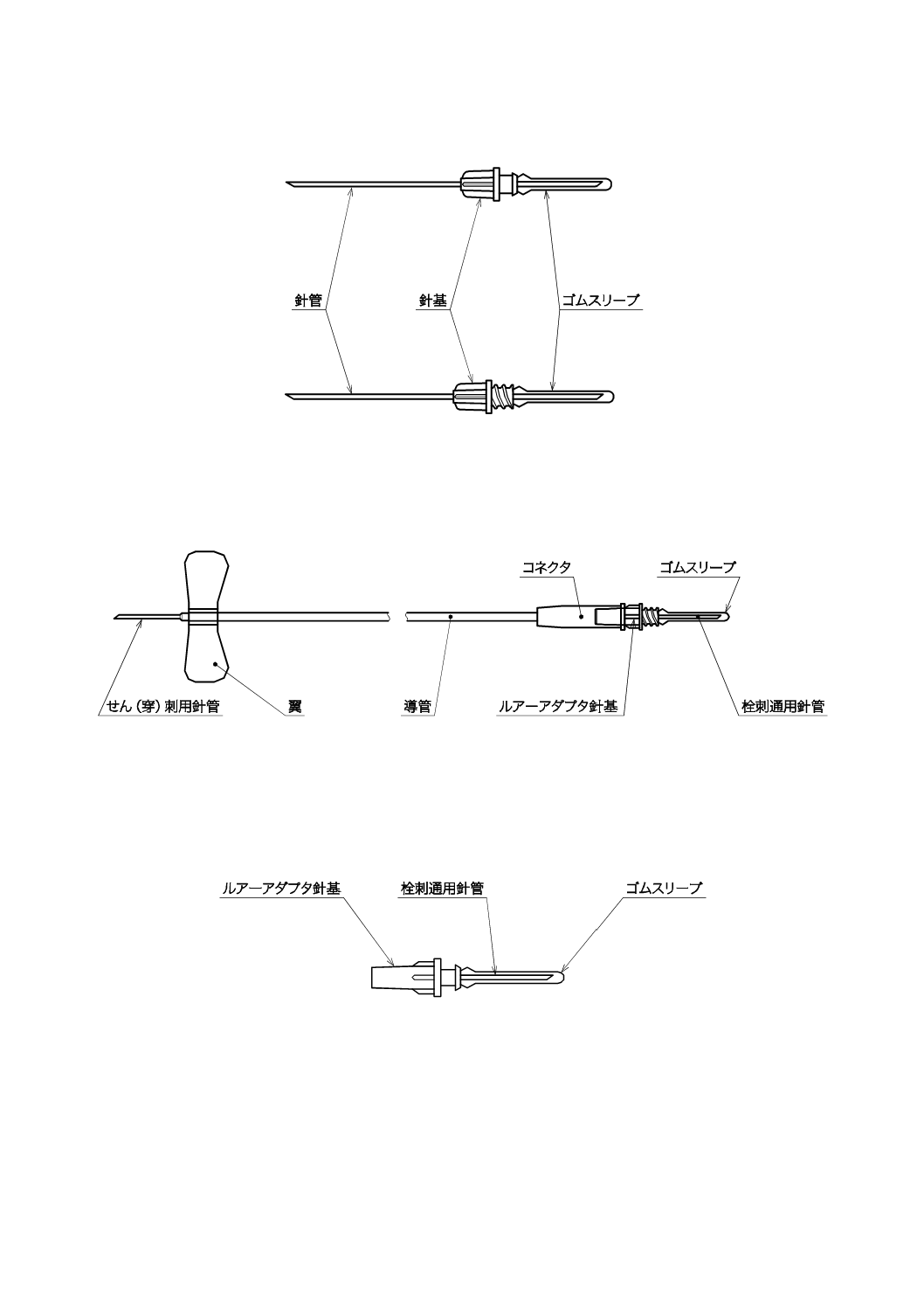
図1−両頭針形の構成及び各部の名称例
図2−翼付針形の構成及び各部の名称例
図3−ルアーアダプタ形の構成及び各部の名称例
T 3220:2011
(1)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
目 次
ページ
序文 ··································································································································· 1
1 適用範囲 ························································································································· 1
2 引用規格 ························································································································· 1
3 用語及び定義 ··················································································································· 1
4 構成及び各部の名称 ·········································································································· 3
5 材料······························································································································· 5
6 物理的要求事項 ················································································································ 5
6.1 針管,せん(穿)刺用針管及び栓刺通用針管 ······································································· 5
6.2 外観及び清浄度 ············································································································· 5
6.3 コネクタ及びルアーアダプタ針基のテーパのはめあい ··························································· 6
6.4 針先 ···························································································································· 7
6.5 性能 ···························································································································· 7
7 化学的要求事項 ················································································································ 9
7.1 溶出物 ························································································································· 9
8 生物学的安全性 ··············································································································· 10
9 無菌性の保証 ·················································································································· 10
10 エンドトキシン ············································································································· 10
10.1 一般 ·························································································································· 10
10.2 両頭針形及びルアーアダプタ形 ······················································································ 10
10.3 翼付針形 ···················································································································· 11
11 包装 ···························································································································· 11
11.1 一次包装 ···················································································································· 11
11.2 二次包装 ···················································································································· 11
12 表示 ···························································································································· 11
12.1 一次包装 ···················································································································· 11
12.2 二次包装 ···················································································································· 11
12.3 記号の使用 ················································································································· 11
附属書A(規定)溶出物試験第二法 ························································································ 13
T 3220:2011
(2)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
まえがき
この規格は,工業標準化法第14条によって準用する第12条第1項の規定に基づき,日本医療器材工業
会(JMED)及び財団法人日本規格協会(JSA)から,工業標準原案を具して日本工業規格を改正すべきと
の申出があり,日本工業標準調査会の審議を経て,厚生労働大臣が改正した日本工業規格である。
これによって,JIS T 3220:2005は改正され,この規格に置き換えられた。
この規格は,著作権法で保護対象となっている著作物である。
この規格の一部が,特許権,出願公開後の特許出願又は実用新案権に抵触する可能性があることに注意
を喚起する。厚生労働大臣及び日本工業標準調査会は,このような特許権,出願公開後の特許出願及び実
用新案権に関わる確認について,責任はもたない。
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
日本工業規格 JIS
T 3220:2011
滅菌済み採血用針
Sterile blood collection needles
序文
この規格は,2005年に制定されたJIS T 3220の見直しにおいて使用者の利便性のため用語,文書構成な
どの内容を変更して改正した日本工業規格である。
1
適用範囲
この規格は,真空採血管と組み合わせて使用し,そのまま直ちに使用でき,複数本の採血管の採血が可
能な,単回使用の滅菌済み採血用針(以下,採血用針という。)について規定する。
なお,平成26年7月28日までJIS T 3220:2005は適用することができる。
2
引用規格
次に掲げる規格は,この規格に引用されることによって,この規格の規定の一部を構成する。これらの
引用規格は,記載の西暦年の版を適用し,その後の改正版(追補を含む。)は適用しない。
JIS G 4305:2005 冷間圧延ステンレス鋼板及び鋼帯
JIS T 0307:2004 医療機器−医療機器のラベル,ラベリング及び供給される情報に用いる図記号
JIS T 0993-1:2005 医療機器の生物学的評価−第1部:評価及び試験
JIS T 3209: 2011 滅菌済み注射針
ISO 594-1:1986,Conical fittings with a 6 % (Luer) taper for syringes, needles and certain other medical
equipment−Part 1: General requirements
ISO 594-2:1998,Conical fittings with 6 % (Luer) taper for syringes, needles and certain other medical
equipment−Part 2: Lock fittings
ISO 9626:1991,Stainless steel needle tubing for the manufacture of medical devices及びAmendment 1:2001
3
用語及び定義
この規格で用いる主な用語及び定義は,次による。
3.1
両頭針形
真空採血管専用の採血用針。針管,針基及びゴムスリーブで構成される。
3.2
翼付針形
翼付針をもった採血用針。せん(穿)刺用針,翼,導管,コネクタ及びルアーアダプタから構成され,
採血後,必要に応じ,翼付針部と輸液の流路とを接続し輸液の流路の一部として用いることができる。
2
T 3220:2011
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
3.3
採血用針(ホルダ付)
あらかじめホルダに採血用針が装着され,ホルダと一体化された採血用針。
3.4
ルアーアダプタ
真空採血管専用の採血針用アダプタ。ルアーアダプタ針基,栓刺通用針管及びゴムスリーブから構成さ
れ,一般の翼付針等を用いて採血するときに使用する器具。
3.5
公称外径
採血用針の被包又は容器に表示された針管又はせん(穿)刺用針管の外径の寸法。
3.6
公称長さ
採血用針の被包又は容器に表示された針管又はせん(穿)刺用針管の静脈せん(穿)刺側長さの寸法。
3.7
精製水
日本薬局方(以下,日局という。)の医薬品各条に規定する“精製水”又はこれと同等以上の水。
3.8
エンドトキシン試験用水
日局の医薬品各条に規定する“注射用水”又はその他の方法によって製造した水で,エンドトキシン試
験に用いるライセート(LAL)試薬の検出限界で反応を示さないもの。
3.9
一次包装
採血用針を直接に覆う包装で,採血用針の無菌性を保持するためのもの。さらに,これが二次包装され
る場合には,いわゆる“内袋”に該当する。
3.10
二次包装
一次包装を直接に覆う包装。通常,複数の一次包装された採血用針,例えば100本を入れた包装。
3.11
針管
一方の針先を血管にせん(穿)刺し,他端の針先を真空採血管に刺し採血を行うため,両端に目的に合
わせた針先をもつ管。
3.12
せん(穿)刺用針管
翼付針の翼に接着された,採血時静脈にせん(穿)刺する針管。
3.13
翼
せん(穿)刺用針管を固定する翼状の針基。
3.14
栓刺通用針管
ルアーアダプタ針基に接着固定し,採血時真空採血管の栓を刺通するための針管。
3
T 3220:2011
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
3.15
ゴムスリーブ
真空採血管刺通側の針管を覆い,真空採血管刺通時以外において針管から血液の流出を防止するゴム部
品。
3.16
針基
針管を接着などで固定し,採血用針を採血用ホルダへ装着固定する部品。
3.17
導管
血液を採血管に導く管。
3.18
コネクタ
導管の針管と反対側に固着し,採血管せん(穿)刺用ルアーアダプタと接続(離脱が可能又は固着)す
る部品。離脱可能なものは6 %のめすテーパをもつ。
3.19
ルアーアダプタ針基
ルアーアダプタをホルダに装着固定する部品。コネクタ又は注射針とルアーアダプタとを接続する機能
ももつ。注射針と接続可能なものは注射針と接続する部分は6 %のおすテーパをもつ。
3.20
ホルダ
採血用針を装着し,採血時真空採血管を保持する器具。
3.21
ゴムスリーブ再シール性
ゴムスリーブを突き刺し真空採血管で採血した後,真空採血管を採血用針から抜いたとき,ゴムスリー
ブが自身のゴム弾性によって戻り,血液がホルダ内へ流出することを防止する性質。
4
構成及び各部の名称
採血用針は,両頭針形のものは針管,針基及びゴムスリーブ,翼付針形のものは,せん(穿)刺用針管,
翼,導管,コネクタ,ルアーアダプタ針基,栓刺通用針管及びゴムスリーブ,ルアーアダプタ形のものは
ルアーアダプタ針基,栓刺通用針管及びゴムスリーブで構成する。また,これらにあらかじめホルダが付
きそのまま採血に使用できるもの,及び針刺し事故防止装置が付いているものもある。
なお,採血用針はホルダに取り付け,形式によっては注射針を付け,真空採血管を付けて静脈血検体を
採血するとき,静脈内と真空採血管との流路として用いる。
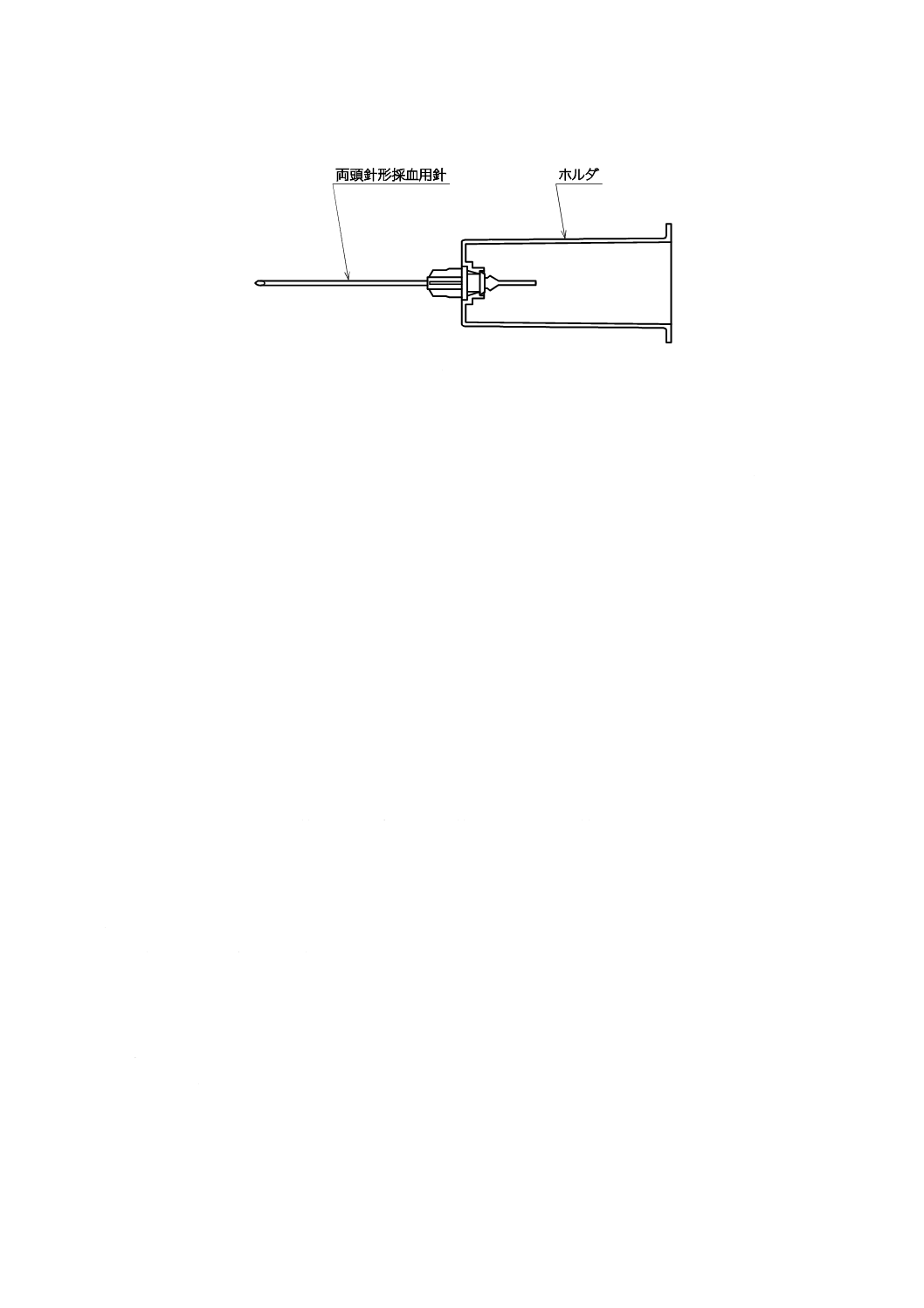
一般的な両頭針形の例を図1に,一般的な翼付針形の例を図2に,一般的なルアーアダプタ形の例を図
3に,及び一般的なホルダ付の例を図4に示す。

4
T 3220:2011
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
図1−両頭針形の構成及び各部の名称例
図2−翼付針形の構成及び各部の名称例
図3−ルアーアダプタ形の構成及び各部の名称例
5
T 3220:2011
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
図4−採血用針(ホルダ付)の構成及び各部の名称例
5
材料
針管,せん(穿)刺用針管及び栓刺通用針管の材料は,JIS G 4305に規定するSUS304,SUS304L若し
くはSUS321に適合するステンレス鋼又はISO 9626の材料に適合するステンレス鋼とする。針管の潤滑剤
としてシリコーン油を用いる場合,シリコーン油は,シリコーン油基準又はこれと同等以上の基準に適合
しなければならない。
注記 シリコーン油基準には,厚生労働省が定めたシリコーン油基準がある。
6
物理的要求事項
6.1
針管,せん(穿)刺用針管及び栓刺通用針管
6.1.1
外観及び清浄度
外観及び清浄度は,次による。
a) 目視で検査したとき,針管及びせん(穿)刺用針管の外面は,凹凸及びきずがなく,仕上げ面が滑ら
かで表面に微粒子又は異物の付着があってはならない。
b) 目視で検査したとき,針管,せん(穿)刺用針管及び栓刺通用針管の内面には,有害な酸化物,切り
粉などの微粒子又は異物の付着があってはならない。
c) 目視で検査したとき,針管,せん(穿)刺用針管及び栓刺通用針管はまっすぐであり,正常な刃断面
及び厚さをもたなければならない。
6.1.2
寸法の許容差
寸法の許容差は,次による。
a) 針管及びせん(穿)刺用針管の外径の公称外径に対する許容差は,−3 %〜+8 %とする。
b) 針管及びせん(穿)刺用針管長さの公称長さに対する許容差は,10 mm以下のものにあっては±20 %,
10 mmを超え20 mm未満のものにあっては±8 %,20 mm以上のものにあっては±7 %とする。
6.1.3
潤滑剤の量
人体へせん(穿)刺する針管及びせん(穿)刺用針管表面の潤滑剤の量は,針管の外面に液滴を認めた
り,内面にたまりを認める量であってはならない。
6.2
外観及び清浄度
目視で検査したとき,採血用針の導管,コネクタ及びルアーアダプタ針基の内面に微粒子又は異物の付
着があってはならない。
6
T 3220:2011
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
6.3
コネクタ及びルアーアダプタ針基のテーパのはめあい
6.3.1
コネクタ
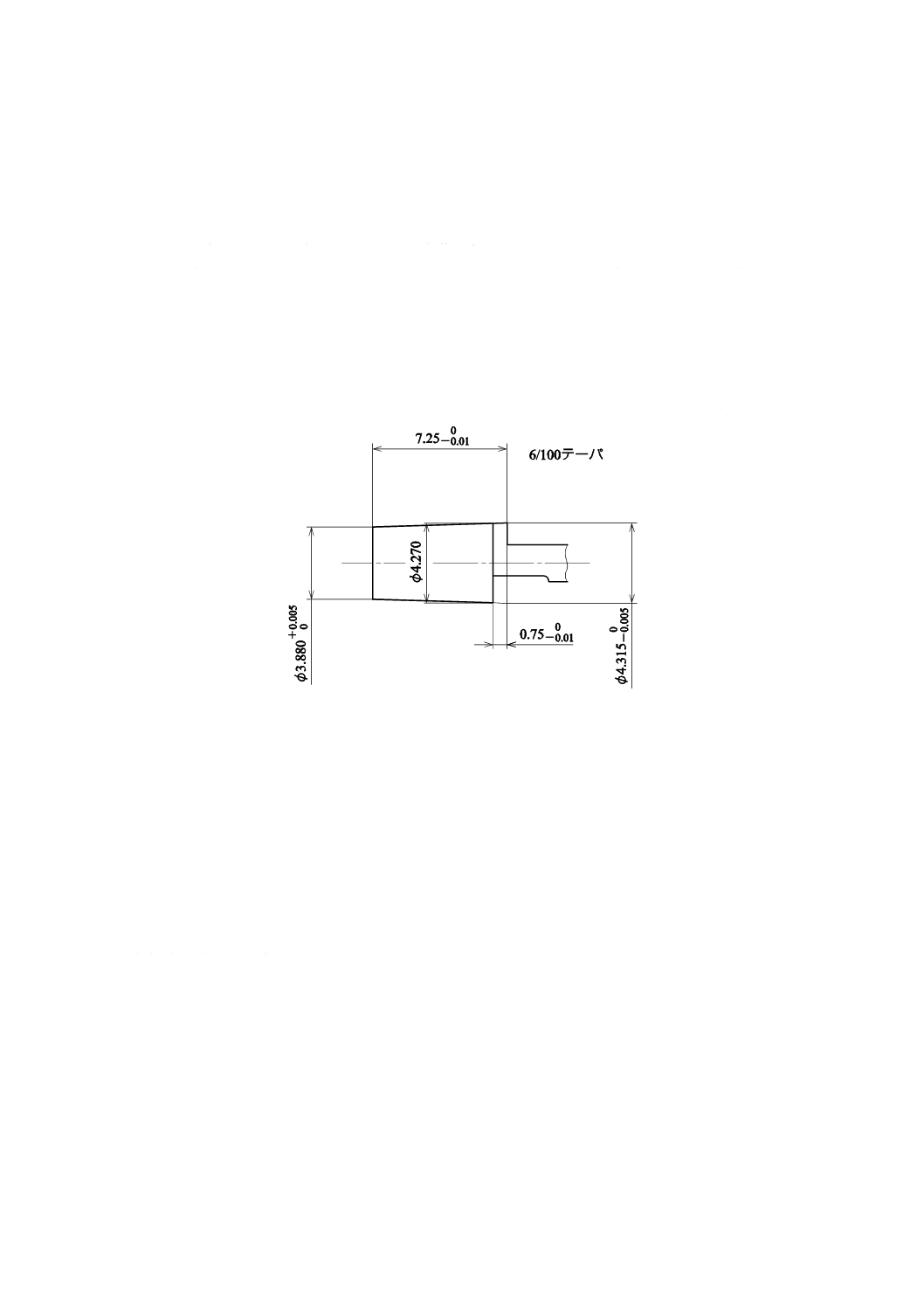
一般的に存在する注射筒などのテーパのはめあいに接続することを意図したものは,図5に示すISO
594-1で規定するおす・ルアーテーパ検査ゲージ[ISO 594-1のFigure 3−Gauges for testing 6 % (Luer) conical
fittings c) Gauge for testing female conical fittings of all materials参照]へコネクタを5 Nの力でゲージには(嵌)
めたとき,コネクタの接続部のめす・ルアーテーパとゲージのテーパとが合致し,かつ,コネクタの先端
部は,ゲージの限度内になければならない。また,この検査ゲージを使用できない構造のものは,この検
査ゲージの要求する寸法に等しい寸法を求めることができるような特別の検査ゲージ,例えば,ISO 594-2
に規定する検査ゲージを用いる。
単位 mm
図5−おす・ルアーテーパ検査ゲージ
6.3.2
ルアーアダプタ針基
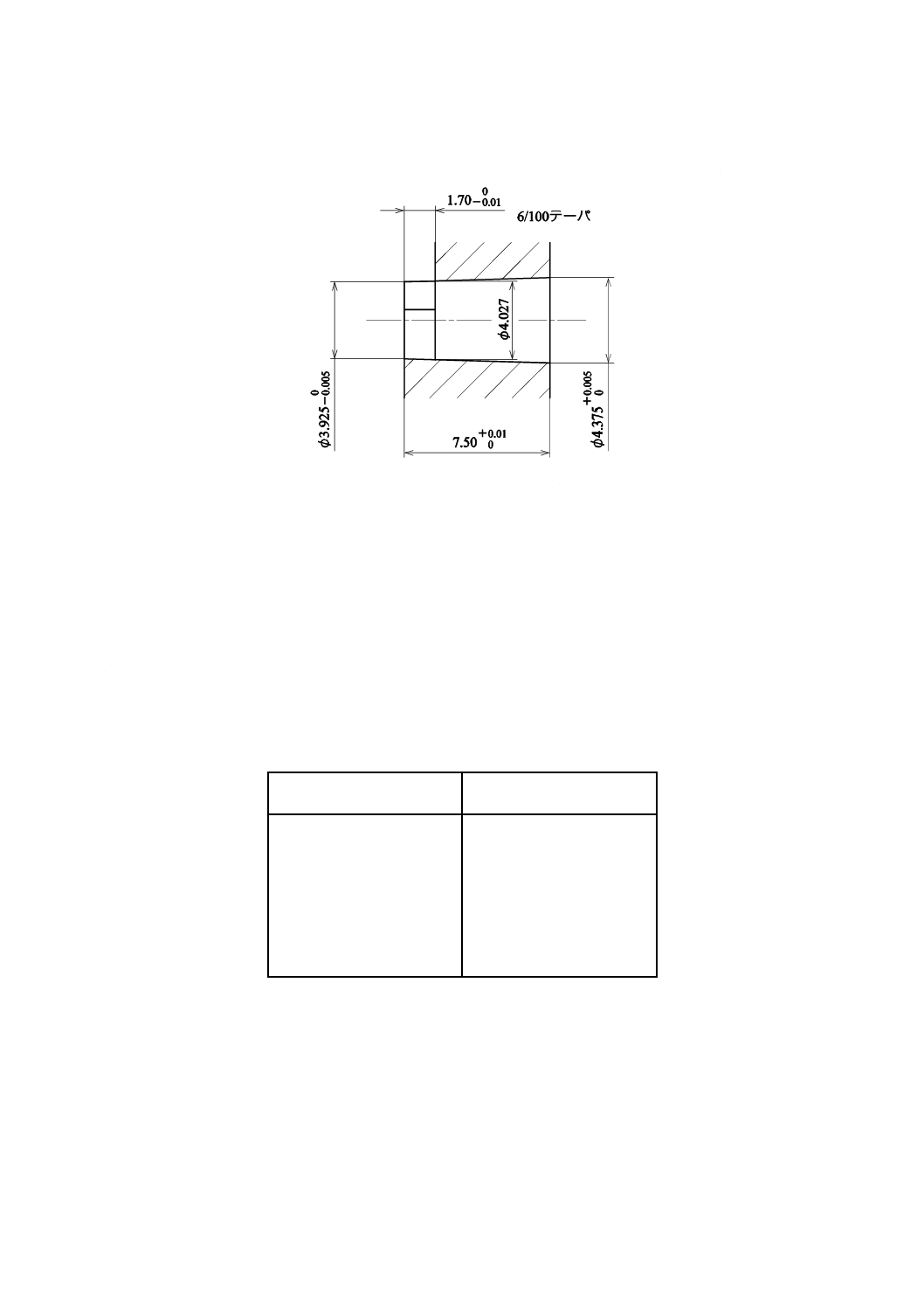
一般に存在する注射針などのテーパのはめあいに接続することを意図したものは,図6に示すISO 594-1
で規定する,めす・ルアーテーパ検査ゲージ[ISO 594-1のFigure 3−b) Gauge for testing semi-rigid male
conical fittings参照]へルアーアダプタ針基のおす・ルアーテーパ接続部を5 Nの力でゲージには(嵌)め
たとき,ルアーアダプタ針基のおす・ルアーテーパとゲージのテーパが合致し,かつ,ルアーアダプタ針
基のおす・ルアーテーパ接続部の先端は,ゲージの限度内になければならない。また,この検査ゲージを
使用できない構造のものは,この検査ゲージの要求する寸法に等しい寸法を求めることができるような特
別の検査ゲージ,例えば,ISO 594-2に規定する検査ゲージを用いる。
7
T 3220:2011
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
単位 mm
図6−めす・ルアーテーパ検査ゲージ
6.4
針先
人体に刺通する針先は,鋭利に研磨してあり,目視で分かるばり,ささくれなどがあってはならない。
6.5
性能
6.5.1
引抜強さ
引抜き強度は,次のいずれかによる。
a) 両頭針形 針管の公称外径に応じ,針管の中心軸方向に表1の引抜荷重を加えたとき,針管は針基か
ら引き抜けてはならない。
表1−両頭針形の引抜荷重
針管の公称外径
mm
力
N
0.55
0.6
0.65
0.7
0.8
0.9
1.1
1.2以上
34
34
34
40
44
54
69
69
b) 翼付針形及びルアーアダプタ形 針管の中心軸方向に15 Nの引抜荷重を加えたとき,せん(穿)刺用
針管及び栓刺通用針管は針基から引き抜けてはならない。
注記 両頭針形と異なり,採血時人体に向けて真空採血管の栓を刺通するための力が加わらない構
造となっている。
6.5.2
弾性
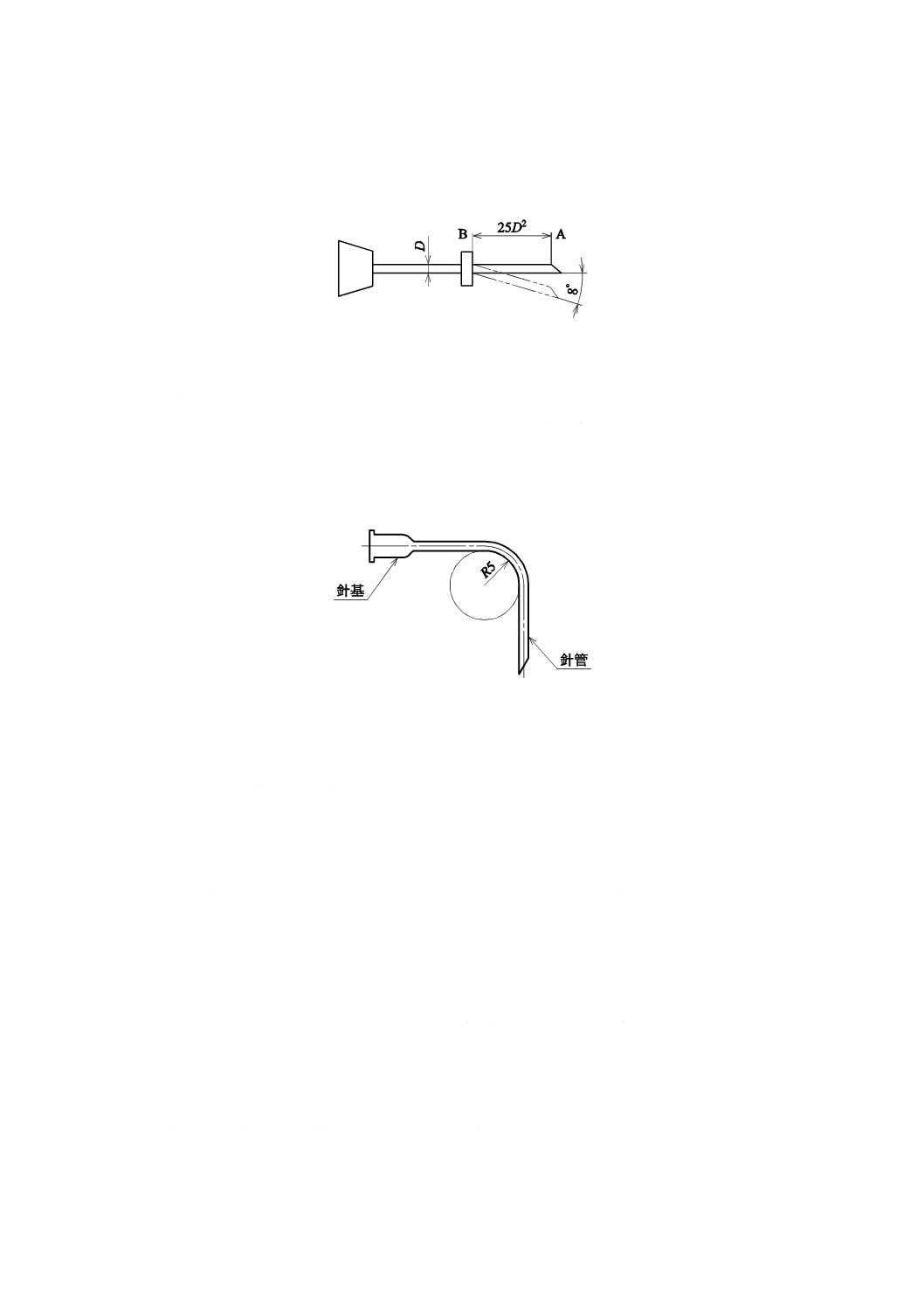
針管及びせん(穿)刺用針管の公称外径(図7のD)が1.0 mm以下のものは,図7のように針管の先
8
T 3220:2011
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
端の一点Aから25 D2離れた針管上の点Bを固定し,Aに荷重を加え,8度曲げて1分間保った後放して
目視したとき,針管は,元の位置に戻らなければならない。
図7−弾性
6.5.3
曲げ強さ
針管及びせん(穿)刺用針管の公称外径が1.0 mm以下で,公称長さが12 mm以上のものは,図8のよ
うに針管を5 mmの曲率半径で90度曲げたとき,折れてはならない。
単位 mm
図8−曲げ強さ
6.5.4
気密性(翼付針形だけに適用し,他の形には適用しない)
翼付針形は,せん(穿)刺用針管の先端を閉じた後,20〜30 ℃の水中に入れ,ルアーアダプタ部を外し
コネクタの先端から内圧150 kPaで15分間空気を送り込んだとき,空気漏れがあってはならない。ゴムス
リーブ再シール性については,6.5.7に規定する方法に従う。
6.5.5
引張強さ(翼付針形だけに適用し,他の形には適用しない)
翼付針形は,各接続部は,15 N以上の引張荷重を15秒間かけたとき,緩みがあってはならない。
6.5.6
導管(翼付針形だけに適用し,他の形には適用しない)
翼付針形の導管は,透明又は気泡が検知できる程度に透明でなければならない。
6.5.7
ゴムスリーブの耐圧性
製造販売業者が推奨する真空採血管を用いて連続して10本採血(水又は牛血など)し,採血用針に13 kPa
の圧力を1分間かけたとき,採血用針のゴムスリーブ自体及びゴムスリーブと採血針との接合部からホル
ダの血液汚染につながるような連続的な血液漏れがあってはならない。
6.5.8
ホルダ
ホルダは,次による。
a) ホルダは,採血管及び採血管内の血液が見える程度に透明でなければならない。
b) ホルダは,製造販売業者が指定する採血用針と組み合わせて,針管の中心軸方向に34 Nの荷重で引っ
9
T 3220:2011
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
張ったとき,採血用針はホルダから外れてはならない。
c) ホルダは,製造販売業者が指定する採血用針と組み合わせたとき,採血管を押し込む力に耐え,採血
に支障が出るようながた又は緩みがあってはならない。また,製造販売業者は,組み合わせて使用す
る採血用針及びホルダの情報を添付文書に記載しなければならない。
d) 製造販売業者は,ホルダと組み合わせて使用できる採血管に関する情報を添付文書に記載しなければ
ならない。
e) ホルダが単回使用の場合は,その旨を,添付文書に記載しなければならない。また,ホルダを消毒し
て再使用可能とする場合は,消毒耐久性について評価を行い,消毒方法及び使用回数の限度を,添付
文書に記載しなければならない。
6.5.9
採血用針のカラーコード
カラーコードは,JIS T 3209の滅菌済み注射針に規定するカラーコードとする。
7
化学的要求事項
7.1
溶出物
7.1.1
一般
7.1.2又は7.1.3の試験を行うか,又はこれと同等以上の試験を行ったとき適合しなければならない。
7.1.2
両頭針形及びルアーアダプタ形
両頭針形及びルアーアダプタ形は,次による。
a) 試験液及び空試験液の調製
1) 試験液 ゴムスリーブを取り除いた採血用針25本を,ほうけい酸ガラスでできた適切な容器に入
れ,250 mLの精製水を加え採血用針を完全に浸せきし(針管の内側を含めて,精製水に接触するよ
うにする。),
30
37+ ℃で60±2分間加温した後,室温になるまで冷却し,採血用針の内外面から全
ての水を容器に戻すようにして採血用針を取り除きこの液を試験液とする。
2) 空試験液 同時に採血用針を入れない精製水を同様の方法で操作し空試験液を調製する。
b) pH 試験液及び空試験液のpHを日局の一般試験法のpH測定法で測定したとき,両液のpHの差は1
以下でなければならない。
c) 溶出金属の制限 原子吸光光度法又は同等以上の微量分析法によって試験液及び空試験液を分析し,
試験液の測定値を空試験液の測定値で補正したとき,試験液中の鉛,亜鉛,鉄の合計は5 mg/L以下で,
かつ,試験液のカドミウム測定値を空試験液のカドミウム測定値で補正したとき,試験液のカドミウ
ム含量は0.1 mg/L以下でなければならない。
7.1.3
翼付針形
翼付針形は,次のいずれかによって試験する。
a) 第一法
1) 試験液及び空試験液の調製
1.1) 試験液 プラスチック製の材料各々10 gずつとり(ゴムスリーブは除く。)細片とし,ほうけい酸
ガラスでできた適切な容器に入れ,100 mLの精製水を加え材料を浸せきし ℃で60±2分間
加温した後,室温になるまで冷却し,材料を取り除きこの液を試験液とする。
1.2) 空試験液 同時に材料を入れない精製水を同様の方法で操作し空試験液を調製する。
2) pH 試験液及び空試験液20 mLずつをとり,これに塩化カリウム1.0 gを精製水に溶かして1 000 mL
とした液1.0 mLずつを加え,日局の一般試験法のpH測定法で測定したとき,両液のpHの差は,
30
37+
10
T 3220:2011
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
2.0以下でなければならない。
3) 重金属 試験液10 mLをとり,日局の一般試験法の重金属試験法の第1法で試験をしたとき試験液
の呈する色は比較液の呈する色より濃くてはならない。比較液には空試験液10 mL及び日局の一般
試験法の標準液で規定する鉛標準液2.0 mLを加える(2.0 ppm以下)。
4) 過マンガン酸カリウム還元性物質 試験液10 mLを共栓三角フラスコにとり,0.002 mol/L過マンガ
ン酸カリウム液20.0 mL及び日局の一般試験法の試薬・試液で規定する希硫酸1 mLを加え,3分間
煮沸し,冷後,これによう化カリウム0.10 g加えて密栓し,振り混ぜて10分間放置した後,0.01 mol/L
チオ硫酸ナトリウム液で滴定する(指示薬:日局の一般試験法の試薬・試液で規定するでんぷん試
液5滴)。別に空試験液10 mLを用い,同様に操作する。試験液及び空試験液の0.002 mol/L過マン
ガン酸カリウム液消費量の差は2.0 mL以下でなければならない。
5) 蒸発残留物 試験液10 mLを水浴上で蒸発乾固し,残留物を105 ℃で1時間乾燥したとき,残留物
の質量は1.0 mg以下でなければならない。
b) 第二法 第一法と同様に操作した試験液について,次の試験をする。
1) 酸性又はアルカリ性 A.1によって試験したとき,容量分析用標準液が1 mL未満で色が灰色になら
なければならない。
2) 金属イオン 原子吸光光度法又は同等以上の微量分析法によって試験液及び空試験液を分析し,試
験液の測定値を空試験液の測定値で補正したとき,試験液中のバリウム,クロム,銅,鉛及びすず
の合計が1 μg/mL以下であり,かつ,カドミウムは0.1 μg/mL以下でなければならない。又はA.2
によって試験をしたとき,試験液の呈する色は,比較液[濃度ρ (Pb2+)=1 μg/mL]の呈する色より
濃くてはならない。
3) 過マンガン酸カリウム還元性物質 A.3によって試験したとき,0.002 mol/L過マンガン酸カリウム
溶液消費量は2.0 mL以下でなければならない。
4) 蒸発残留物 A.4によって試験したとき,残留物は5 mg以下でなければならない。
5) 紫外吸収スペクトル A.5によって試験したとき,試験液の吸光度は,0.1以下でなければならない。
8
生物学的安全性
JIS T 0993-1に規定する生物学的安全性の評価を行う。
9
無菌性の保証
無菌性の保証は,滅菌バリデーション基準又はこれと同等以上の基準に基づき,無菌性の担保を行う。
注記 滅菌バリデーション基準には,厚生労働省が定めた滅菌バリデーション基準がある。
10 エンドトキシン
10.1 一般
次の試験を行うか,又はこれと同等以上の試験を行ったとき,次の規定に適合しなければならない。
10.2 両頭針形及びルアーアダプタ形
採血用針10本をとりゴムスリーブを外した後,硬質ガラスの容器に入れ,エンドトキシン試験用水30
mLを加え,溶封又は適切な栓で密封してよく振り混ぜた後,室温で60分間放置し,この液を試験液とす
る。日局の一般試験法のエンドトキシン試験法によって試験したとき,0.5 EU/mL未満でなければならな
い。
11
T 3220:2011
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
10.3 翼付針形
ゴムスリーブを外した翼付針形10セットをとり,各セットの管内にエンドトキシン試験用水40 mLを1
分間約10 mLの速さで流し,その液で針管をよく洗い,洗液を合わせて試験液とし,日局の一般試験法の
エンドトキシン試験法によって試験したとき,0.5 EU/mL未満でなければならない。
11 包装
11.1 一次包装
一次包装は,使用前に容易に破れるおそれがなく,微生物の侵入を防止することができ,通常の取扱い,
輸送及び保管中に,内容製品を適切に保護できるものでなければならない。また,一度開封したら,包装
は簡単に再シールできず,開封されたことが明確に分かるものでなければならない。
11.2 二次包装
二次包装は,通常の取扱い,輸送及び保管中に,内容製品を保護できる強度をもたなければならない。
12 表示
12.1 一次包装
一次包装には,次の事項を表示する。
a) 針管の外径(mm)及び長さ(mm)
b) “滅菌済み”の旨
c) 製造番号又は製造記号
12.2 二次包装
二次包装には,次の事項を表示する。ただし,二次包装を用いないで,一次包装を最小販売単位の包装
として用いる場合には,次の事項を一次包装に表示する。
なお,製造番号又は製造記号が滅菌年月を表している場合は,改めて滅菌年月の表示をする必要はない。
また,滅菌年月の代わりに使用期限を表示してもよい。
a) 製造販売業者の氏名又は名称,及び住所
b) 医療機器の認証番号
c) 販売名
d) 針管の外径(mm)及び長さ(mm)
e) 数量(入り数)
f)
“滅菌済み”の旨
g) “再使用禁止”の旨(“ディスポーザブル”の表現は使用しない。)
h) 製造番号又は製造記号
i)
滅菌年月
12.3 記号の使用
12.1及び12.2は,JIS T 0307に規定する適切な記号を使用することによってこれに替えてもよい。
注記 JIS T 0307に規定する主な記号の例を,表2に示す。

12
T 3220:2011
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
表2−JIS T 0307に規定する記号の例
13
T 3220:2011
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書A
(規定)
溶出物試験第二法
A.1 酸性又はアルカリ性
滴定フラスコに入れた試験液20 mLにタシロ指示薬0.1 mLを加える。色が紫色の場合は水酸化ナトリ
ウム溶液(0.01 mol/L)を,緑色の場合は塩酸(0.01 mol/L)を灰色が現れるまで加える。
注記 タシロ指示薬(Tashiro's indicator):95 %(V/V)エタノールへ,メチルレッド0.2 g及びメチレ
ンブルー0.1 gを溶解し100 mLとしたもの。
A.2 金属イオン
10 mLの試験液を用いて日局によって金属イオンの試験を行う。呈色度を調べる。
A.3 過マンガン酸カリウム還元性物質
10 mLの試験液に0.002 mol/Lの過マンガン酸カリウム液10 mLと1 mol/Lの硫酸液1 mLとを加え,か
くはんし,室温で15分間反応させる。よう化カリウム0.1 gを加え,0.005 mol/Lのチオ硫酸ナトリウム液
で薄茶色になるまで滴定した後に,5滴のでんぷん溶液を加え,青色が消えるまで滴定する。空試験液に
ついても同様に行う。0.002 mol/L過マンガン酸カリウム液消費量(mL)を空試験液との差によって計算
する。
A.4 蒸発残留物
50 mLの試験液を,質量を量った蒸発皿に入れ,沸点近くの温度で蒸発乾固する。105 ℃で質量が一定
となるまで乾燥させる。50 mLの空試験液についても同様な操作を行う。試験液と空試験液の蒸発残留物
との差をmgで表す。
A.5 紫外吸収スペクトル
試験液を0.45 μmのメンブランフィルタでろ過する。5時間以内に空試験液を入れたセルを対照として,
1 cmの石英セルに入れた液を走査紫外分光光度計にかけ,波長250〜320 nmまでのスペクトルを記録する。
結果を,波長に対する吸光度を図示したスペクトルとして報告する。