T 0601-2-16:2014
(1)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
目 次
ページ
序文 ··································································································································· 1
201.1 適用範囲,目的及び関連規格 ························································································ 1
201.1.1 適用範囲 ················································································································· 1
201.1.2 目的 ······················································································································· 2
201.1.3 副通則 ···················································································································· 2
201.1.4 個別規格 ················································································································· 2
201.2 引用規格 ··················································································································· 3
201.3 用語及び定義 ············································································································· 4
201.4 一般要求事項 ············································································································· 7
201.4.3 *基本性能 ················································································································ 7
201.4.7 ME機器の単一故障状態 ···························································································· 11
201.5 ME機器の試験に対する一般要求事項 ············································································ 11
201.6 ME機器及びMEシステムの分類 ·················································································· 11
201.7 ME機器の標識,表示及び文書 ····················································································· 11
201.8 ME機器の電気的ハザードに関する保護 ········································································· 14
201.8.3 *装着部の分類 ········································································································· 15
201.9 ME機器及びMEシステムの機械的ハザードに関する保護 ················································· 15
201.10 不要又は過度の放射のハザードに関する保護 ································································· 16
201.11 過度の温度及び他のハザードに関する保護 ···································································· 16
201.11.8 *ME機器への電源供給又は電源(商用)の中断 ··························································· 16
201.12 *制御及び計器の精度並びに危険な出力に対する保護 ······················································· 17
201.13 危険状態及び故障状態 ······························································································· 26
201.14 プログラマブル電気医用システム(PEMS) ·································································· 26
201.14.13 *ネットワーク・データ結合によるPEMSの他の機器への接続 ······································ 26
201.15 ME機器の構造 ········································································································ 26
201.16 *MEシステム ·········································································································· 27
201.16.1 MEシステムに対する一般要求事項 ··········································································· 27
201.16.2 MEシステムの附属文書 ·························································································· 27
201.17 ME機器及びMEシステムの電磁両立性 ······································································· 28
202 電磁両立性−要求事項及び試験 ······················································································· 28
202.3.18 生命維持用医用電気機器又は医用電気システム ···························································· 28
208 医用電気機器及び医用電気システムのアラームシステムに関する一般要求事項,
試験方法及び適用指針 ···································································································· 28
208.4 *一般要求事項 ··········································································································· 28
208.6.3 アラーム信号の発生 ································································································· 29
T 0601-2-16:2014 目次
(2)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
ページ
210 生理的閉ループ制御器の開発に関するプロセス要求事項 ······················································ 30
211 *ホームヘルスケア環境で使用する医用電気機器及び医用電気システムに対する要求事項 ··········· 30
211.6 ME機器及びMEシステムの分類 ·················································································· 30
附属書G(規定)可燃性麻酔剤の発火を引き起こすハザードに関する保護 ····································· 31
附属書AA(参考)特定の指針及び理論的根拠 ·········································································· 32
附属書BB(参考)人工腎臓装置におけるハザード,予想される一連の事象及び危険状態の例 ············ 51
参考文献 ···························································································································· 58
この個別規格で使用される定義の索引 ····················································································· 59
附属書JA(参考)JISと対応国際規格との対比表 ······································································ 62
T 0601-2-16:2014
(3)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
まえがき
この規格は,工業標準化法第14条によって準用する第12条第1項の規定に基づき,一般社団法人日本
医療機器テクノロジー協会(MTJAPAN)及び一般財団法人日本規格協会(JSA)から,工業標準原案を具
して日本工業規格を改正すべきとの申出があり,日本工業標準調査会の審議を経て,厚生労働大臣が改正
した日本工業規格である。
これによって,JIS T 0601-2-16:2008は改正され,この規格に置き換えられた。
この規格は,著作権法で保護対象となっている著作物である。
この規格の一部が,特許権,出願公開後の特許出願又は実用新案権に抵触する可能性があることに注意
を喚起する。厚生労働大臣及び日本工業標準調査会は,このような特許権,出願公開後の特許出願及び実
用新案権に関わる確認について,責任はもたない。
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
日本工業規格 JIS
T 0601-2-16:2014
医用電気機器−第2-16部:人工腎臓装置の
基礎安全及び基本性能に関する個別要求事項
Medical electrical equipment-Part 2-16: Particular requirements for the
basic safety and essential performance of haemodialysis, haemodiafiltration
and haemofiltration equipment
序文
この規格は,2012年に第4版として発行されたIEC 60601-2-16を基とし,我が国で流通している日本独
自の医療機器についても規定する必要があるため,技術的内容を変更して作成した日本工業規格である。
なお,この規格で点線の下線を施してある箇所は,対応国際規格を変更している事項である。変更の一
覧表にその説明を付けて,附属書JAに示す。
この規格で箇条,細分箇条などにアスタリスク(*)がある箇所は,その根拠についての説明を附属書
AAに記載している。
この規格は,通則規格であるJIS T 0601-1:2012(医用電気機器−第1部:基礎安全及び基本性能に関す
る一般要求事項)(以下,通則という。)及び関連する副通則規格(以下,副通則という。)と併読する規格
である。
この規格の箇条などの番号は,通則に対応している。また,本文中の“置換え”,“追加”及び“修正”
の意味は,201.1.4を参照する。
この規格において人工腎臓装置とは,個人用透析装置,多人数用透析液供給装置,透析用監視装置,血
液透析ろ(濾)過用装置,血液ろ過用装置及び多用途透析装置を指す(以下,人工腎臓装置という。)。
この規格は,長時間にわたって持続的及び緩徐に血液透析,血液透析ろ過及び/又は血液ろ過を行うの
に必要な機能を備えた装置についても適用可能な箇条がある。ただし,適用する箇条及びその試験条件に
ついては製造販売業者が指定する必要がある。
201.1
適用範囲,目的及び関連規格
次を除き,通則の箇条1を適用する。
201.1.1
適用範囲
追加
この規格は,201.3.210.1〜201.3.210.6で定義した人工腎臓装置の基礎安全及び基本性能について規定す
る。
この規格は,透析液を再生して使用する人工腎臓装置の透析液制御システムを考慮していない。しかし,
電気的安全性及び患者の安全性の見地から,そのような装置の特定の安全要求事項は考慮に入れる。
この規格は,人工腎臓装置のための最小限度の安全要求事項を規定している。これらの装置は,医療ス
2
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
タッフによる使用又は患者若しくは医学専門家の監督の下で他の訓練された者による使用を意図してい
る。
この規格は,血液透析,血液透析ろ過及び血液ろ過の治療を腎不全患者に提供することを意図する全て
のME機器を含む。
この規格の個別要求事項は,次のものには適用しない。
− 体外循環回路
− ダイアライザ
− 透析液原液
− 水処理装置
− 腹膜透析を実施するために使用する機器(JIS T 0601-2-39参照)
ある箇条又は細分箇条がME機器だけか又はMEシステムだけに限定して適用することを意図している
場合は,それらの表題及び内容にその旨を記載している。その記載がない場合には,その箇条又は細分箇
条は,ME機器及びMEシステムの両方に適用する。
この規格が適用するME機器又はMEシステムの意図する生理学的機能に関係するハザードは,通則の
7.2.13及び8.4.1を除いて,取り扱わない。
注記1 通則の4.2も参照。
注記2 この規格の対応国際規格及びその対応の程度を表す記号を,次に示す。
IEC 60601-2-16:2012,Medical electrical equipment−Part 2-16: Particular requirements for the basic
safety and essential performance of haemodialysis, haemodiafiltration and haemofiltration
equipment(MOD)
なお,対応の程度を表す記号“MOD”は,ISO/IEC Guide 21-1に基づき,“修正している”
ことを示す。
なお,旧規格(JIS T 0601-2-16:2008)は平成29年2月28日まで適用することができる。
201.1.2
目的
置換え
この個別規格の目的は,人工腎臓装置のための基礎安全及び基本性能についての要求事項を確立するこ
とである。
201.1.3
副通則
追加
この個別規格は,通則の箇条2で記載する適用可能な副通則及びこの個別規格の箇条201.2を引用する。
IEC 60601-1-2,JIS T 60601-1-8,IEC 60601-1-10及びIEC 60601-1-11は,箇条202,箇条208,箇条210
及び箇条211でそれぞれ変更され,適用される。JIS T 0601-1-3は適用されない。JIS T 0601-1規格群にお
いて他の全ての発行された副通則が,適用される。
201.1.4
個別規格
置換え
JIS T 0601規格群において,個別規格は,検討中の特定のME機器のために必要に応じてこの通則及び
副通則を変更,置換え又は削除してもよく,かつ,他の基礎安全及び基本性能の要求事項を加えてもよい。
個別規格の要求事項は,通則に優先する。
簡潔にするため,通則は,この個別規格において通則という表現で引用する。副通則は,規格番号で引
用する。
3
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
この個別規格の箇条及び細分箇条の番号は,通則の番号に接頭語“201”を付与する(例えば,この規格
の201.1は,通則の箇条1の内容を扱う。)。また,副通則の場合には,接頭語“20x”を付与する。ここで
xは,副通則の最後の数字である(例えば,この個別規格の202.4は,IEC 60601-1-2の箇条4の内容を,
203.4は,JIS T 0601-1-3の箇条4の内容を扱う。)。通則の条文の変更は,次の用語を用いて規定する。
“置換え”は,通則又は適用する副通則の箇条又は細分箇条を,この個別規格の規定に全て置き換える
ことを意味する。
“追加”は,通則又は適用する副通則の該当する要求事項に,この個別規格の規定を追加することを意
味する。
“修正”は,通則又は適用する副通則の箇条又は細分箇条を,この個別規格の規定に修正することを意
味する。
通則に追加する細分箇条,図又は表には,201.101から始まる番号を付ける。しかし,通則は3.1〜3.139
の細分箇条番号で定義している。この個別規格では,201.3.201から始まる細分箇条で定義する。追加した
附属書は,附属書AA,附属書BBなどと記載し,追加項目はaa),bb)などと記載する。
各副通則に追加する細分箇条,図又は表は,“20x”から始まる番号を付ける。ここでxは,副通則の番
号である。例えば,202はIEC 60601-1-2,203はJIS T 0601-1-3を示す。
以下,“この規格”という用語は,通則,あらゆる適用できる副通則及びこの個別規格を同時に適用して
引用することを示す。
この個別規格に対応する箇条又は細分箇条がない場合,通則又は適用できる副通則の箇条又は細分箇条
を修正することなく適用する。また,通則又は適用できる副通則の一部が,たとえ何らかの関連があって
も適用してはならないことを意図するときは,その趣旨の説明をこの個別規格に示す。
201.2
引用規格
注記 末尾に参考文献を列記した。
次を除き,通則の箇条2を適用する。
修正
IEC 60601-1-2:2007,Medical electrical equipment−Part 1-2: General requirements for basic safety and
essential performance−Collateral standard: Electromagnetic compatibility−Requirements and tests
注記1 現行の対応日本工業規格“JIS T 0601-1-2:2012 医用電気機器−第1-2部:安全に関する一
般的要求事項−電磁両立性−要求事項及び試験”は,IEC 60601-1-2:2001及びAmendment
1:2004に対応している。
注記2 諸外国では現時点,IEC 60601-1-2 Ed2.1:2004,及び同内容でIEC 60601-1:2005の構成に対
応したIEC 60601-1-2 Ed3:2007 が用いられている。
IEC 60601-1-6:2010,Medical electrical equipment−Part 1-6: General requirements for basic safety and
essential performance−Collateral standard: Usability
注記 対応する国際規格としてIEC 62366を適用してもよい。
JIS T 60601-1-8:2012 医用電気機器−第1-8部:基礎安全及び基本性能に関する一般要求事項−副通
則:医用電気機器及び医用電気システムのアラームシステムに関する一般要求事項,試験方法及
び適用指針
注記 対応国際規格:IEC 60601-1-8:2006,Medical electrical equipment−Part 1-8: General requirements
for basic safety and essential performance−Collateral standard: General requirements, tests and
4
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
guidance for alarm systems in medical electrical equipment and medical electrical systems(IDT)
追加
IEC 60601-1-10:2007,Medical electrical equipment−Part 1-10: General requirements for basic safety and
essential performance−Collateral Standard: Requirements for the development of physiologic closed-loop
controllers
IEC 60601-1-11:2010,Medical electrical equipment−Part 1-11: General requirements for basic safety and
essential performance−Collateral standard: Requirements for medical electrical equipment and medical
electrical systems used in the home healthcare environment
IEC 62366:2007,Medical devices−Application of usability engineering to medical devices
ISO 594-2,Conical fittings with 6 % (Luer) taper for syringes, needles and certain other medical equipment−
Part 2: Lock fittings
JIS Z 8733 音響−音圧法による騒音源の音響パワーレベルの測定方法−反射面上の準自由音場にお
ける実用測定方法
注記 対応国際規格:ISO 3744,Acoustics−Determination of sound power levels of noise sources using
sound pressure−Engineering method in an essentially free field over a reflecting plane(MOD)
JIS T 3248 透析用血液回路
注記 対応国際規格:ISO 8638,Cardiovascular implants and artificial organs−Extracorporeal blood
circuit for haemodialysers, haemodiafilters and haemofilters(MOD)
201.3
用語及び定義
この個別規格で用いる主な用語及び定義は,通則及びIEC 60601-1-10によるほか,次による。
注記 定義された用語のインデックスは,“この個別規格で使用される定義の索引”を参照。
201.3.8
*装着部(APPLIED PART)
置換え
体外循環回路及び体外循環回路に恒常的,かつ,電気的に接続されている全ての部品(例えば,透析液
回路)。
注記1 図AA.1参照。
201.3.78
患者接続部(PATIENT CONNECTION)
追加
注記1 患者血液回路接続部は,正常状態又は単一故障状態で電流が患者と個人用透析装置,透析用
監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置との間を流れることが
できる装着部上の個々の部分である。
追加
201.3.201
動脈圧(ARTERIAL PRESSURE)
体外循環回路の血液取り出しラインで測定した圧力。
注記1 血液ポンプの上流側の前ポンプ圧と血液ポンプの下流側の後ポンプ圧との間には,圧力差が
ある。
5
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
201.3.202
*漏血(BLOOD LEAK)
ダイアライザの血液側から透析液側への血液の漏れ。
注記1 HFを行う場合は,ろ液部を意味する。
201.3.203
セントラル透析液送液システム(CENTRAL DIALYSIS FLUID DELIVERY SYSTEM)
透析用水,及び透析液原液又は粉末用剤から透析液を調製し,個々の透析用監視装置,血液透析ろ過用
装置,血液ろ過用装置及び多用途透析装置へ透析液を送液するシステム。
201.3.204
ダイアライザ(DIALYSER)
この規格においてダイアライザは,血液透析器,血液ろ過器及び血液透析ろ過器の総称として用いる。
201.3.204.1
血液透析器(HAEMODIALYSER)
血液透析を目的とする機器。
201.3.204.2
血液ろ過器(HAEMOFILTER)
血液ろ過を目的とする機器。
201.3.204.3
血液透析ろ過器(HAEMODIAFILTER)
血液透析ろ過を目的とする機器。
201.3.205
透析液(DIALYSIS FLUID, DIALYSATE, DIALYSIS SOLUTION, DIALYSING FLUID)
HD又はHDF中に,血液中の溶質及び/又は水と交換するための溶液。
201.3.206
透析液原液(DIALYSIS FLUID CONCENTRATE)
透析用水で適切に希釈又は溶解するとき,透析液となる物質。
201.3.207
体外循環回路(EXTRACORPOREAL CIRCUIT)
血液回路及びそれに組み込まれた附属品。
201.3.208
血液透析ろ過,HDF(HAEMODIAFILTRATION,HDF)
HD及びHFの同時組合せによって,腎不全患者の血液中の水溶性物質の濃度及び患者の過剰な体液を
是正するプロセス。
201.3.209
血液透析,HD(HAEMODIALYSIS,HD)
透析液と血液を分離する半透膜を介した双方向の拡散移動及び限外ろ過によって,腎不全患者の血液中
の水溶性物質の濃度及び患者の過剰な体液を是正するプロセス。
注記1 通常,このプロセスは,ろ過による除水を伴う。また,通常,このプロセスは透析液から血
液への物質拡散も伴う。
6
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
201.3.210
*血液透析装置(HAEMODIALYSIS EQUIPMENT)
血液透析,血液透析ろ過及び/又は血液ろ過を行うために使用されるME機器又はMEシステム。
注記1 ME機器という用語が表題に使用されるときは,それは人工腎臓装置と同等である。ME機
器という用語が文中に使用されるときは,それは一般的なME機器を指す。
201.3.210.1
個人用透析装置
1人の患者の透析治療を行うのに必要な機能を備えた装置。
201.3.210.2
多人数用透析液供給装置
透析治療を行うための透析液を作製し,2人以上の患者に供給する装置。
201.3.210.3
透析用監視装置
透析治療を行うときに透析液流量,温度,静脈圧などをモニタする装置。
201.3.210.4
血液透析ろ過用装置(HAEMODIAFILTRATION EQUIPMENT)
血液透析ろ過を行うのに必要な機能を備えた装置。
201.3.210.5
血液ろ過用装置(HAEMOFILTRATION EQUIPMENT)
血液ろ過を行うのに必要な機能を備えた装置。
201.3.210.6
多用途透析装置
血液透析,血液透析ろ過及び/又は血液ろ過を行うことができる透析用監視装置又は個人用透析装置。
201.3.211
血液ろ過,HF(HAEMOFILTRATION,HF)
半透膜を介して血液の一部を膜の反対側に移動(ろ過)させることによって,腎不全患者の溶質濃度レ
ベル及び過剰水分の是正を図る治療。限外ろ過と同時に,血液とほぼ等張な補充液を用いて液置換が行わ
れるが,この場合,限外ろ過速度から補充液流量を差し引いたものが過剰体液の除去速度に相当する。
201.3.212
正味の体液除去(除水)(NET FLUID REMOVAL)
患者からの体液(水及び物質)を除去(除水)すること。
注記1 歴史的にはこの用語は“体重減少”であった。
201.3.213
*オンラインHDF(ONLINE HDF)
血液透析ろ過用装置及び多用途透析装置が透析液をもとにHDF治療のための注入に適した補充液を調
製する血液透析ろ過の手段。
201.3.214
*オンラインHF(ONLINE HF)
血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置が透析液をもとにHF治療のための注入に適
した補充液を調製する血液ろ過の手段。
7
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
201.3.215
*保護システム(PROTECTIVE SYSTEM)
発生する可能性のある危険状態に対して,患者を保護するために特別に設計された,自動システム又は
構造的特徴。
注記 “危険状態”は,対応国際規格では“ハザード”であるが,これは明らかな誤りである。リス
クマネジメントの考え方を示した重要な部分であり,単純な誤りではないので,あえて点線の
下線で修正した。この個別規格を通して同様の誤りが多々あるので,それらにも点線の下線を
施したが,注記は省いた。
201.3.216
補充液(SUBSTITUTION FLUID)
HF又はHDFにおいて,体外循環回路を介して患者に投与される液体。
注記 “補充液”は,“補液”,“置換液”又は“希釈液”ということがある。
201.3.217
膜間圧力差,TMP(TRANSMEMBRANE PRESSURE,TMP)
半透膜を介して生じる液体圧力差。
注記1 一般的に平均TMPが使用される。実際には,表示される膜間圧力差は,通常それぞれ一か
所で測定された体外循環回路の圧力と測定された透析液圧とから推定される。
201.3.218
*限外ろ過(ULTRAFILTRATION)
ダイアライザを介して,患者の血液から体液を取り除くプロセス。
201.3.219
静脈圧(VENOUS PRESSURE)
体外循環回路の返血ラインで測定した圧力。
201.3.220
ダイアライザ血液入口圧(INLET PRESSURE AT BLOOD SIDE OF THE DIALYSER)
体外循環回路(動脈側)の血液ポンプの下流側からダイアライザ入口の間で測定した圧力。
201.4
一般要求事項
次を除き,通則の箇条4を適用する。
201.4.3
*基本性能
追加
201.4.3.101
*追加の基本性能要求事項
人工腎臓装置の基本性能は,表201.101に規定している細分箇条の機能を含むが,これに限定されない。
これに該当する場合,正常状態において製造販売業者が指定する許容値に適合しなければならない。
8
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
表201.101−基本性能要求事項
要求事項
細分箇条
血流量
201.4.3.102
透析液流量
201.4.3.103
正味の体液除去(除水)
201.4.3.104
補充液流量
201.4.3.105
透析(運転)時間
201.4.3.106
透析液の組成
201.4.3.107
透析液温度
201.4.3.108
補充液温度
201.4.3.109
注記 表201.101に規定の幾つかの基本性能は,使用されるディスポーザブル製品の特性に依存する
[例えば,回転式ぜん(蠕)動ポンプにおける血流量は,ポンプセグメントの内径に依存する。]。
201.4.3.102
血流量
個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置に適用し,
次による。
a) 血流量は,製造販売業者が指定しなければならない。
注記1 血流量が設定値より低い場合だけ,治療効率を低下させるとみなされる。このため,試験の
目的は,最も治療効率を低下させる血流量の誤差を見つけることである。
(試験)
b) 適合性は,典型的なぜん動ポンプを次の試験条件下で確認する。
− 適用装置にポンプセグメントを取り付け,かつ,少なくとも30分間運転する。
− 体外循環回路に37 ℃の液体(例えば,水)を注入する。
− 適用装置の血流量を400 mL/min,又は不可能な場合は設定可能な最高の血流量に設定する。
− 動脈圧を−200 mmHgに設定する。
− 血流量を測定する。
測定された血流量の値が,製造販売業者の取扱説明書で記載した許容値以内でなければならない。
注記2 ポンプセグメントの疲労は,血流量を減少させる。
注記3 ぜん動ポンプの吸込側が陰圧の場合は,血流量に影響する。
201.4.3.103
透析液流量
個人用透析装置,透析用監視装置,血液透析ろ過用装置及び多用途透析装置に適用し,次による。
a) 適用装置の透析液流量は,製造販売業者が指定しなければならない。
注記 透析液流量が設定値より低い場合だけ,治療効率を低下させるとみなされる。
(試験)
b) 適合性は,次の試験条件下で確認する。
− 適用装置を製造販売業者が指定する血液透析モードに設定する。
− 適用装置を最大の透析液流量に設定する。
− 透析液流量を30分間計測する。
− 適用装置を最小の透析液流量に設定する。
− 透析液流量を30分間計測する。
透析液流量の値が,製造販売業者の取扱説明書で記載した許容範囲内でなければならない。
9
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
201.4.3.104
正味の体液除去(除水)
個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置に適用し,
次による。
a) 適用装置の正味の体液除去(除水)は,製造販売業者が指定しなければならない。
(試験)
b) 適合性は,次の試験条件下で確認する。
適用装置のバランス部だけについての試験1
− 設定可能な場合,製造販売業者の推奨するダイアライザを装着し,適用装置を血液透析モードに設
定する。
− 体外循環回路に液体(例えば,水)を注入する。
− 設定可能な場合,最大の透析液流量に設定する。
− 設定可能な場合,透析液温度を37 ℃に設定する。
− 正味の体液除去(除水)の速度を0 mL/h又は設定可能な最小の値に設定する。
− 血液出口圧を製造販売業者が指定した最高圧より50 mmHg低くする。
− 正味の体液除去(除水)を適切な時間間隔で測定する。
続いて試験2
− 正味の体液除去(除水)の速度を最大に設定する。
− 適切な時間間隔で,正味の体液除去(除水)を測定する。
続いて試験3
− 血液出口圧を製造販売業者が指定した最低圧より20 mmHg高くする。
− 適切な時間区間での正味の体液除去(除水)を測定する。
正味の体液除去(除水)の値が,製造販売業者の取扱説明書で記載した許容範囲内でなければならない。
201.4.3.105
補充液流量
血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置に適用し,次による。
a) 適用装置の補充液流量は,製造販売業者が指定しなければならない。
注記 補充液流量が設定値より低い場合だけ,治療効率を低下させるとみなされる。
(試験)
b) 適合性は,次の試験条件下で確認する。
適用装置のバランス部及び治療に関連する補充液流量のための試験1
− 製造販売業者の推奨するダイアライザを装着し,適用装置をHDFモード又はHFモードに設定する。
− 体外循環回路に液体(例えば,水)を注入する。
− 正味の体液除去(除水)の流量を0 mL/h又は不可能な場合は最小に設定する。
− 最大の補充液流量に設定する。
− 設定可能な場合,補充液温度を37 ℃に設定する。
− 補充液流量及び正味の体液除去(除水)を測定する。
続いて試験2
− 最小の補充液流量に設定する。
− 補充液流量及び正味の体液除去(除水)を測定する。
補充液流量及び正味の体液除去(除水)の値が,製造販売業者の取扱説明書で記載した許容範囲内でな
ければならない。
10
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
201.4.3.106
透析(運転)時間
個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置に適用し,
次による。
a) 適用装置のための透析(運転)時間の精度は,製造販売業者が指定しなければならない。
(試験)
b) 適合性は,製造販売業者が指定した透析(運転)時間の定義にあてはまる機能測定によって確認する。
201.4.3.107
*透析液の組成
試験方法は,製造販売業者が指定する。
201.4.3.108
透析液温度
個人用透析装置,透析用監視装置,血液透析ろ過用装置及び多用途透析装置に適用し,次による。
a) 適用装置の透析液温度は,製造販売業者が指定しなければならない。
注記 この試験は,透析液用ヒータを搭載している適用装置にだけ適用する。
(試験)
b) 適合性は,次の試験条件下で確認する。
− 熱的に安定な状態になるまで,適用装置を運転する。
− 周囲温度は20 ℃〜25 ℃以内とする。
− 設定可能な場合,透析液温度を37 ℃に設定する。
− 最大の透析液流量に設定する。
− ダイアライザの入口で温度を測定する。
− 30分間,温度を記録する。
− 最小の透析液流量に設定する。
− ダイアライザの入口で温度を測定する。
− 30分間,温度を記録する。
透析液温度の値が,製造販売業者の取扱説明書で記載した許容範囲内でなければならない。
201.4.3.109
補充液温度
血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置に適用し,次による。
a) 適用装置の補充液温度の許容値は,製造販売業者が指定しなければならない。
注記 この試験は,補充液用ヒータを搭載している適用装置にだけ適用する。
(試験)
b) 適合性は,次の試験条件下で確認する。
− 熱的に安定な状態になるまで,適用装置を運転する。
− 周囲温度は20 ℃〜25 ℃以内とする。
− 設定可能な場合,補充液温度を37 ℃に設定する。
− 最大の補充液流量に設定する。
− 補充液ラインの血液ラインへの接続箇所で補充液温度を測定する。
− 30分以上,温度を記録する。
− 最小の補充液流量に設定する。
− 補充液ラインの血液ラインへの接続箇所で補充液温度を測定する。
− 30分以上,温度を記録する。
補充液温度の値が,製造販売業者の取扱説明書で記載した許容値以内でなければならない。
11
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
201.4.7
ME機器の単一故障状態
追加
単一故障状態の例は,保護システム(201.12.4.4.101,201.12.4.4.102,201.12.4.4.103,201.12.4.4.104及び
201.12.4.4.105を参照)の故障である。
注記 製造販売業者が意図するように個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液
ろ過用装置及び多用途透析装置が使用されるとき,体外循環回路に恒常的にエアがある場合は,
エアは単一故障状態とはみなされず正常状態である。
201.5
ME機器の試験に対する一般要求事項
通則の箇条5を適用する。
201.6
ME機器及びMEシステムの分類
通則の箇条6を適用する。
201.7
ME機器の標識,表示及び文書
次を除き,通則の箇条7を適用する。
201.7.4.3
計測の単位
追加
mmHgは,人工腎臓装置の生体に関するあらゆる部分の圧力測定に使用してもよい。
201.7.9.2
取扱説明書
201.7.9.2.2
警告及び安全上の注意
追加
該当する場合,取扱説明書は,更に次の事項を含めなければならない。
− 患者間のいかなる交さ(叉)感染をも防ぐために必要な予防措置に対し,操作者が注意を払うことを
記述した声明。
− 患者への接続及び切り離しに関連する危険状態に操作者が注意を払うことを記述した声明。
− 体外循環回路の不適切な接続から起こるあらゆる危険状態を含むハザードに操作者が注意を払うこと
を記述した声明。
− 透析液原液の誤った選択に関連する危険状態についての記述。
− 単一故障状態における保護システムのアラーム設定値について,透析液の各組成がとる可能性がある
逸脱に関する定量的記述。
− *ダイアライザの透析液側から血液側への不要物質の移動の可能性に関連する危険状態についての記
述。
− 201.12.4.4.104.1 a) 注記1に従って用いられた保護システムには,
・ この保護システムによってリスクをある程度減らすことができるが,残る可能性があるリスクを説
明した警告。
・ リスクを減らすための更なる対策の記述。
− 根本的な問題を解決せず警報が繰返し解除された場合の,警報及び危険状態に対する操作者の適切な
行動についての説明。
− *体外循環回路内のあらゆる狭い通路(血液ラインのねじれ又は極細のカニューレのような)が,溶血
12
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
を引き起こす可能性があること及びこの危険状態が保護システムでは検出できない可能性があること
を明記した警告。
− 201.12.4.4.105 a) 注記1に従って保護システムが適用される場合は,凝血又は超音波ゲルの塗布によ
って超音波気泡検出器の機能不全を引き起こす可能性があることを記した声明。
− 気泡検出器の下流に位置する接続部において,陰圧が生じた場合,そこからエアが入る可能性がある
ことを記載した警告。これはシングルニードル又は中心静脈カテーテル使用のような場合に起こる可
能性がある。
− オンラインHDF及びオンラインHFに対しては,
・ 製造販売業者によって定義され,かつ,妥当性を確認された消毒手順だけが,オンラインHDF及
びオンラインHFのために使用されてもよいことを記した警告。
・ 使用される水及び透析液原液に要求される品質についての情報。
・ 交換が望まれる消耗品(例えば,フィルタ)の交換間隔。
− ポンプ前の動脈圧が極端に陰圧になると,実際に流れる血流量が低下し,それによって治療効率が低
下する可能性があるという内容の警告かつポンプの正確な流量範囲及び精度,並びに精度を維持する
入口及び出口の圧力範囲についての記載。
− CF形装着部以外の装着部をもつ個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過
用装置及び多用途透析装置に関し,操作者及び責任部門の両方に,心房部位での中心静脈カテーテル
を使用している患者環境では,CF形装着部に要求される接触電流及び患者漏れ電流の制限値を超え
る電気機器(非ME機器及びME機器)を使用しないことを確実にするようにという警告。
注記 附属書AAの201.8.3参照。
201.7.9.2.5
ME機器の説明
追加
該当する場合,取扱説明書には,更に次の事項を含めなければならない。
− 製造販売業者が201.3.217に述べられた定義と異なったものを用いた場合,その膜間圧力差の定義。
− 透析液原液のコネクタの色マーキングの説明。
− シングルニードル治療での有効な血液の送出量に関する情報。
− シングルニードル治療での体外循環回路における血液の再循環に関する情報。
− 電源供給の遮断後に警報音が作動する遅延時間。
− 生理的閉ループ制御器の機能には,
a) 技術的な動作原理。
b) 測定される患者パラメータ及び制御される生体パラメータ。
c) 臨床テスト(clinical testing)で記録された有効性及び副作用を含んだ,これらフィードバック制御
モードを評価した方法。
副通則IEC 60601-1-10も参照。
− *人工腎臓装置によって表示又は指示され,かつ,治療の処方の変更又は治療の有効性を評価若しくは
確認する上で利用してもよいあらゆるデータに関して,
a) 技術的な動作原理。
b) 測定が間接的である場合は,精度及び可能性のある影響要因に関する記述。
c) 標準的治療を想定し,その技術的動作原理を評価する方法。
− CF形装着部以外の装着部をもつ個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過
13
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
用装置及び多用途透析装置には,これらの装置が心房部位での中心静脈カテーテルと同時使用できる
かについての声明。また,これらの装置が心房部位での中心静脈カテーテルの使用に適さない場合は,
危険状態が列挙されなければならない。
201.7.9.2.6
設置
追加
該当する場合,取扱説明書には,更に次の事項を含めなければならない。
− 水及び他の関連する液体の質に関する適切な規則及び勧告を遵守して設置され,かつ,使用されるこ
とが,人工腎臓装置に不可欠であることの声明。
− クラスIの人工腎臓装置には,電気設備における保護接地の重要性の記述。
− 等電位化導線の使用が望ましい適用についての記述。
− 給水及びセントラル透析液送液システムに要求される温度,流量及び圧力の許容範囲。
− 個人用透析装置,多人数用透析液供給装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装
置を給水から分離すること,飲用水源への逆流を防ぐこと,及びあらゆる下水管への接続から人工腎
臓装置の排液接続を介した汚染を防ぐことに関する全ての地域の規則を遵守することの重要性を強調
した注記。
− 視覚的警報の色識別の異なる仕組みが構成可能である場合は,責任部門はそこでの環境での混乱を最
小にする色識別の仕組みを選択することが望ましいことの記述。
− 操作パラメータ又は保護システムの設定が構成可能である場合は,責任部門は構成を選択するか,又
はしっかりと初期設定を確認することが望ましいことの記述。
201.7.9.2.12 清掃,消毒及び滅菌
追加
該当する場合,取扱説明書には,更に次の事項を含めなければならない。
− 浄化又は消毒が達成される方法の記述。
− *浄化又は消毒の効果が検証された試験手順が要求によって利用可能であることの声明。
− 人工腎臓装置を消毒するために製造販売業者の取扱説明書に従うことの警告。他の手順が用いられた
場合は,消毒手順の効果及び安全性を検証することは責任部門に責任があること。この警告は,他の
手順を用いた結果によって起こる可能性がある故障モードを含む危険状態を具体的に記載しなければ
ならない。
− あらゆる送液システム(例えば,個人用透析装置,多人数用透析液供給装置,血液透析ろ過用装置,
血液ろ過用装置及び多用途透析装置への接続ポイントからの液体ラインを含む給水システム,セント
ラル透析液送液システム並びに人工腎臓装置に接続する機器)の衛生的品質に責任部門が責任をもつ
ことの警告。
201.7.9.2.14 附属品,組合せ機器及び使用材料
追加
該当する場合,取扱説明書には,更に次の事項を含めなければならない。
− 人工腎臓装置と一緒に使用することを意図した透析液原液,ダイアライザ及び血液回路の情報。
(試験)
適合性は,取扱説明書の検査によって確認する。
201.7.9.3
技術解説
201.7.9.3.1
一般
14
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
追加
該当する場合,技術解説は,更に次の事項を含めなければならない。
•
設置
− 人工腎臓装置を設置又は使用し始めるとき,とるべき特別の手段又は観察すべき条件の記述。これ
らは,実行すべきテストの種類及び回数の基準を含めなければならない。
− 人工腎臓装置の排液において,起こる可能性がある最大温度。
− *エネルギー消費量,周囲へのエネルギー放出,並びに通常運転条件下及び給水温度の関数としての
排液へのエネルギー放出についての情報。
− *通常運転条件での水及び透析液原液の消費量についての情報。
•
装置仕様
− *抗凝固剤ポンプを備えた個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装
置及び多用途透析装置の場合には,ポンプの種類,流量の範囲及び精度並びにその精度を維持する
のに必要な圧力。
− 停電の場合に対して製造販売業者によって予見されるあらゆる追加対策。
− 201.12.4.4.101(透析液の組成)によって要求される保護システムの種類,測定精度及びアラーム設
定値の値又は範囲。
− 201.12.4.4.102(透析液及び補充液の温度)によって要求される保護システムの種類,測定精度及び
アラーム設定値の値又は範囲。
− 201.12.4.4.103[正味の体液除去(除水)]によって要求される保護システムの種類,測定精度及びア
ラーム設定値の値又は範囲。
− 201.12.4.4.104.1(周囲への体外循環血液の損失)によって要求される保護システムの種類,測定精
度及びアラーム設定値の値又は範囲。
− *201.12.4.4.104.2(透析液への漏血)によって要求される保護システムの種類及び測定精度,並びに
漏血検出器を通過する流量が最小時及び最大時の保護システムのアラーム設定値。
− 201.12.4.4.104.3(凝固による体外循環血液の損失)によって要求される保護システムの種類及びア
ラーム設定値。
− 201.12.4.4.105(気泡混入)によって要求される保護システムのために採用された方法及び製造販売
業者が指定した試験条件下での感度。
− あらゆる保護システムに対するオーバライド時間。
− 聴覚アラームのアラーム音中断期間。
− あらゆる調整可能な聴覚アラーム源の音圧レベルの範囲。
− 水,透析液及び透析液原液と接触することを意図する全ての材料の開示。
− オンラインHDF及びオンラインHFに関し,補充液の準備の方法,補充液フィルタの自動的な完全
性試験の方法(該当する場合)及びこれらの試験の精度。
(試験)
適合性は,技術解説の検査によって確認する。
201.8
ME機器の電気的ハザードに関する保護
次を除き,通則の箇条8を適用する。
15
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
201.8.3
*装着部の分類
追加
CF形装着部への要求事項に適合する漏れ電流の個人用透析装置,透析用監視装置,血液透析ろ過用装
置,血液ろ過用装置及び多用途透析装置は,心房部位での中心静脈カテーテルの併用に適しているとみな
される。
CF形装着部以外の装着部をもつ個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用
装置及び多用途透析装置が,心房部位での中心静脈カテーテルを用いた患者の治療を意図する場合は,次
の事項に適合しなければならない。
aa) 正常状態において,患者漏れ電流及び接触電流はCF形装着部の限界値以内でなければならない。
bb) 単一故障状態において,患者漏れ電流,接触電流及び接地漏れ電流はCF形装着部の限界値以内でな
ければならない。
個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置がbb)の
項目に適合しない場合は,単一故障状態において患者漏れ電流がCF形装着部の限界値以内であることを
維持するために,製造販売業者のリスクマネジメントプロセスによって正当化される外部の対策を施さな
ければならない。
(試験)
適合性は,検査によって確認する。
201.8.7.4.7
患者漏れ電流の測定
追加
*aa) 測定装置は,患者に接続される両方の体外循環血液回路の部位に接続されなければならない。試験の
期間中は,25 ℃で温度補償された選択可能な最高の電導度であり,かつ,選択可能な最高の透析液
温度の試験溶液を透析液回路内及び体外循環回路内に流さなければならない。個人用透析装置,透析
用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置は,警報の発生なしに最大血
流量及び代表的な治療モードで運転されなければならない。実用性をもたせるために,測定装置は透
析液コネクタに接続してもよい。
注記101 上記に記載された患者漏れ電流の測定は,B形装着部をもつ個人用透析装置,透析用監
視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置のための通則の
8.7.4.7.b)(装着部に適用する電圧)に基づく測定を含んでいない。
注記102 最大の血流量は,静脈側ドリップチャンバ内のエア層で最低の電気抵抗を生じる。
201.8.11.2 *マルチタップ
追加
人工腎臓装置にマルチタップが備えられて,かつ,他のマルチタップとの相互互換又は互換によって危
険状態を引き起こす場合は,マルチタップはそのような互換を防ぐタイプでなければならない。
(試験)
適合性は,検査及び機能試験によって確認する。
注記 機械的に互換性のないソケットなどによって防止する。
201.9
ME機器及びMEシステムの機械的ハザードに関する保護
通則の箇条9を適用する。
16
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
201.10 不要又は過度の放射のハザードに関する保護
通則の箇条10を適用する。
201.11 過度の温度及び他のハザードに関する保護
次を除き,通則の箇条11を適用する。
201.11.6.3 ME機器及びMEシステムへのこぼれ
追加
(試験)
適合性は,JIS C 0920のコードIPX1に基づいて確認する。
201.11.6.6 *ME機器及びMEシステムの清掃及び消毒
追加
単回使用ではない透析液回路をもつ人工腎臓装置は,そのような透析液回路の消毒を行う手段をもたな
ければならない。
消毒手順は,危険状態となる可能性がある内部の部品又は外部の附属品(例えば透析液フィルタ)の悪
化をもたらしてはならない。
(試験)
適合性は,附属文書並びに人工腎臓装置の検査によって確認する。
201.11.8 *ME機器への電源供給又は電源(商用)の中断
追加
a) 内部電源をもたない個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多
用途透析装置
これらの装置への電源供給の中断時又は電源(商用)の中断時の安全な状態は,次による。
− 聴覚アラーム信号が1分間以上作動する。
− 製造販売業者のリスクマネジメントプロセスの判断から,追加対策が必要としてもよい。
− 製造販売業者のリスクマネジメントプロセスの判断から,患者に対し,いかなる受容できないリス
クも生じない場合に限り,これらの装置は,電源供給の回復で自動的に再起動してもよい。
(試験)
適合性は,リスクマネジメントファイルの検査及び機能試験によって確認する。
b) 内部電源をもつ個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途
透析装置
これらの装置への電源供給の中断時又は電源(商用)の中断時の安全な状態は,次による。
− 視覚アラーム信号が作動する。
− 製造販売業者が指定した時間間隔後に,聴覚アラーム信号が作動する。
− 製造販売業者のリスクマネジメントプロセスの判断から,追加対策が必要としてもよい。
− 電源供給の中断時に,これらの装置の機能が停止される場合は,製造販売業者のリスクマネジメント
プロセスの判断から,患者に対し,いかなる受容できないリスクも生じない場合に限り,これらの装
置は,電源供給の回復で自動的に再起動してもよい。
− 内部電源が中断又は放電される場合は,これらの装置は,201.11.8 a)に記載の要求事項に適合しなけ
ればならない。
(試験)
17
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
適合性は,リスクマネジメントファイルの検査及び機能試験によって確認する。
201.12 *制御及び計器の精度並びに危険な出力に対する保護
次を除き,通則の箇条12を適用する。
201.12.4.4 不正確な出力
追加
次の箇条にある試験手順は,人工腎臓装置の妥当性確認のための最低限度の要求事項の要旨を示してい
る。全ての詳細が各試験手順に含まれているとは限らず,かつ,特定の人工腎臓装置並びに製造販売業者
のリスクマネジメントプロセスに基づいたこれらの詳細を扱うことは,試験実施部門の責務である。
201.12.4.4.101 *透析液の組成
個人用透析装置,多人数用透析液供給装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置
に適用し,次による。
a) 適用装置は,いかなる透析液の調製制御システムから独立した,危険状態を引き起こすような組成の
透析液が,ダイアライザに流れるのを防ぐ保護システムを備えなければならない。
透析液の危険な組成を防ぐ保護システムの設計は,透析液の調製のあらゆる局面における潜在的な故障
を考慮しなければならない。
保護システムによって,次の安全な状態を達成しなければならない。
− 聴覚及び視覚アラーム信号(208.6.3.1,208.6.3.3.2及び208.6.3.3.101参照)が作動する。聴覚アラー
ムは,208.6.3.3.101 b)で規定されたように遅延してもよい。
− 透析液のダイアライザへの流れを停止する。
− オンラインHDF又はオンラインHFモードにおいて,体外循環回路への補充液の流れを停止する。
b) 電導度プロファイル及び生理的閉ループ制御器
あらかじめプログラムされた時間で透析液の組成が変化する場合又は患者の生理学的パラメータを測定
することによって透析液の組成のフィードバック制御を行う場合,適用装置はその制御システムから独立
した,危険状態を引き起こすような制御システムでのいかなる意図しない変化をも防ぐ保護システムを備
えなければならない。
保護システムによって,次の安全な状態を達成しなければならない。
− 聴覚及び視覚アラーム信号(208.6.3.1,208.6.3.3.2及び208.6.3.3.101参照)が作動する。
− 製造販売業者のリスクマネジメントプロセスによって定義される場合は,他の対策とする。
c) 適用装置が原液のボーラス投与機能を備えている場合は,適用装置は,その制御システムから独立し
た,患者への危険状態を引き起こすような原液のボーラス投与動作を防ぐ保護システムを備えなけれ
ばならない。
保護システムによって,次の安全な状態を達成しなければならない。
− 聴覚及び視覚アラーム信号(208.6.3.1,208.6.3.3.2及び208.6.3.3.101参照)が作動する。
− 原液のボーラス投与を中断する。
(試験)
適合性は,機能試験及び次のテストによって確認する。
・ アラーム設定値を決定する試験1
− 試験用装置を,アラーム信号が出ない状態での最低及び最高の透析液の組成にそれぞれ設定する。
− 保護システムがアラーム信号を発するまで透析液の組成をゆっくりと変更する。
18
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
− 正常状態及び警報直後にダイアライザ入口でサンプルを採取する。
− 正常状態及び警報直後に採取したサンプルの透析液の組成の違いを測定する(例えば,炎光光度法
によって)。
・ 警報反応時間に関する試験2
− 試験用装置を,設定可能な最高の透析液流量に設定する。
− 各透析液原液の供給を一つずつ模擬的に遮断する。
− 正常状態及び警報直後にダイアライザ入口でサンプルを採取する。
− 正常状態及び警報直後に採取したサンプルの透析液の組成の違いを測定する(例えば,炎光光度法
によって)。
・ 予見できる誤使用に関する試験3
− 可能な場合は,透析液原液を入れ替える(例えば,A原液,B原液を入れ替える)。
− 警報の作動を判定する。
201.12.4.4.102 *透析液及び補充液の温度
個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置に適用し,
次による。
a) 製造販売業者のリスクマネジメントプロセスによって正当化されない限り,透析液及び補充液の温度
の設定範囲は,33 ℃から42 ℃の範囲外であってはならない。
b) 適用装置は,透析液がダイアライザに流れるとき及び/又は補充液が体外循環回路に流れるとき,そ
れぞれの出口部において33 ℃未満又は42 ℃を超える透析液及び/又は補充液が流れることを未然
に防ぐ保護システムを,いかなる温度制御システムとは独立した形で備えなければならない。
c) 短時間であれば,温度の46 ℃までの上昇及び33 ℃未満の状態が発生しても容認される。ただし,そ
の許容される時間及び温度は,製造販売業者のリスクマネジメントプロセスで正当化されなければな
らない。
d) 保護システムによって,次の安全な状態を達成しなければならない。
− 聴覚及び視覚アラーム信号(208.6.3.1,208.6.3.3.2及び208.6.3.3.101参照)が作動する。聴覚アラー
ムは,208.6.3.3.101 b)で規定されたように遅延されてもよい。
− ダイアライザへの透析液の流れ及び/又は補充液の体外循環回路への流れを停止する。
(試験)
適合性は,機能試験及び次のテストによって確認する。
・ 透析液に関する試験1
− 試験用装置を,設定が可能な場合は,最高の透析液流量に設定する。
試験は,透析液温度の上側及び下側について,それぞれ確認する。
− 上側の確認の場合,最高の透析液温度に設定する。下側の確認の場合,最低の透析液温度に設定す
る。
− ダイアライザ入口での温度が安定するのを待つ。
− 上側の確認の場合,保護システムがアラーム信号を発するまで透析液の温度をゆっくり上げる。下
側の確認の場合,保護システムがアラーム信号を発するまで透析液の温度をゆっくり下げる。
− 上側の確認の場合,ダイアライザ入口で連続的に温度を測定し,かつ,最高の温度を計測する。下
側の確認の場合,ダイアライザ入口で連続的に温度を測定し,かつ,最低の温度を計測する。
・ 補充液に関する試験2
19
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
− 試験用装置を,設定が可能な場合は,最高の補充液流量に設定する。
試験は,透析液温度又は補充液温度の上側及び下側について,それぞれ確認する。
− 上側の確認の場合,最高の透析液温度又は補充液温度に設定する。下側の確認の場合,最低の透析
液温度又は補充液温度に設定する。
− 体外循環回路への入口での温度が安定するのを待つ。
− 上側の確認の場合,保護システムがアラーム信号を発するまで透析液又は補充液の温度をゆっくり
上げる。下側の確認の場合,保護システムがアラーム信号を発するまで透析液又は補充液の温度を
ゆっくり下げる。
− 上側の確認の場合,体外循環回路への入口で連続して補充液温度を測定し,かつ,最高の温度を計
測する。下側の確認の場合,体外循環回路への入口で連続して補充液温度を測定し,かつ,最低の
温度を計測する。
201.12.4.4.103 *正味の体液除去(除水)
個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置に適用し,
次による。
a) 適用装置は,正味の体液除去(除水)に関して,限外ろ過制御(除水制御)システムとは独立した,
危険状態を引き起こすような制御パラメータの設定値からの変動を防ぐ保護システムを備えなければ
ならない。
HDF及びHFの場合,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置は,いかなる補充液の
制御システムとは独立した,危険状態を引き起こすような補充液の不適切な投与を防ぐ保護システムを備
えなければならない。
保護システムによって,次の安全な状態を達成しなければならない。
− 聴覚及び視覚アラーム信号(208.6.3.1,208.6.3.3.2及び208.6.3.3.101参照)が作動する。
− 液体のバランスエラーの継続を防止する。
b) 限外ろ過プログラム(除水プログラム)及び生理的閉ループ制御器
あらかじめ,限外ろ過速度(除水速度)を経時的に変化させる限外ろ過プログラム及び患者の生理学的
パラメータを監視装置によって測定し,その値によって限外ろ過速度を制御する限外ろ過の場合,適用装
置は,その制御システムとは独立した,危険状態を引き起こすような制御システムのいかなる意図しない
変化を防ぐ保護システムを備えなければならない。
保護システムによって,次の安全な状態を達成しなければならない。
− 聴覚及び視覚アラーム信号(208.6.3.1,208.6.3.3.2及び208.6.3.3.101参照)が作動する。
− 製造販売業者のリスクマネジメントプロセスによって定義される場合は,他の対策とする。
c) 適用装置が液体のボーラス投与機能を備えている場合は,適用装置は,その制御システムから独立し
た,患者への危険状態を引き起こすような液体のボーラス投与機能を防ぐ保護システムを備えなけれ
ばならない。
保護システムによって,次の安全な状態を達成しなければならない。
− 聴覚及び視覚アラーム信号(208.6.3.1,208.6.3.3.2及び208.6.3.3.101参照)が作動する。
− 液体のボーラス投与を中断する。
(試験)
適合性は,次のテストを含む機能試験及び故障模擬によって確認する。
・ 正味の体液除去(除水)速度の誤差を検証する試験
20
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
− 試験用装置を最高の透析液流量に設定する。
− 可能な場合は,最高の補充液流量に設定する。
− 該当する場合,透析液温度を37 ℃に設定する。
− 限外ろ過速度を最低及び最高に(一つずつ)設定する。
− 保護システムがアラーム信号を発するまで,正味の体液除去(除水)の速度に影響を与えるそれぞ
れのポンプ制御システムの低い側及び高い側の故障(透析液流量を低くする故障,補充液流量を低
くする故障,限外ろ過速度を高くする故障及び限外ろ過速度を低くする故障を一つずつ)を模擬す
る。
− 理論値との量の差を計測する。
201.12.4.4.104 体外循環血液の損失
201.12.4.4.104.1 体外循環血液の周囲への損失
個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置に適用し,
次による。
*a) 適用装置は,危険状態を引き起こすような体外循環血液の周囲への損失から患者を守る保護システム
を備えなければならない。
注記1 今日,周囲への血液の損失を検出する全面的に信頼できるシステムは開発されていない。
次の勧告は,周囲への血液の損失を検出する最も知られたシステムである。
保護システムが静脈圧の測定を利用している場合は,操作者は少なくとも下限のアラーム設定値を手動
で現在の測定値にできる限り近づけることが望ましい。また,シングルニードル治療モードでは追加手段
が必要である。
b) 適用装置は,周囲への血液の損失を防ぐ本質的な安全設計がなされていないかぎり,過大な圧力によ
る体外循環回路における破裂又は離断によって起こる体外循環血液の周囲への損失から患者を守る保
護システムを備えなければならない。
注記2 これは患者接続部又はアクセスニードルの離断に関係するものではなく,体外循環回路に
おける回路の破裂又はジョイントの離断を引き起こすようなポンプによって発生する可能
性がある潜在的な圧力に関係するものである。
*c) 保護システムによって,次の安全な状態を達成しなければならない。
− 聴覚及び視覚アラーム信号(208.6.3.1,208.6.3.3.2及び208.6.3.3.101参照)が作動する。
− 単一故障状態下においても,適用装置による周囲への血液の流れを停止する。
− 血液ろ過又は血液透析ろ過の場合は,補充液の流れを停止する。
(試験)
適合性は,機能試験及び次のテストによって確認する。
・ 静脈圧測定を用いる保護システムに関する試験
− 試験用装置の血流量を中程度に設定する。
− 静脈圧を中程度の値に調整する。
− アラーム信号を発するまで静脈圧を低くする。
− 警報点と基準値との差を測定する。
201.12.4.4.104.2 *透析液への漏血
個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置に適用し,
次による。
21
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
a) 適用装置は,危険状態を引き起こすような漏血から患者を守る保護システムを備えなければならない。
b) 保護システムによって,次の安全な状態を達成しなければならない。
− 聴覚及び視覚アラーム信号(208.6.3.1,208.6.3.3.2及び208.6.3.3.101参照)が作動する。
− 透析液への更なる血液損失を防止する。
(試験)
適合性は,機能試験及び次のテストによって確認する。
•
アラーム設定値の決定に関する試験
− 漏血検出器への流れが最大となるようにする(最高の透析液流量,最高の限外ろ過速度,関係する
場合は,最高の補充液流量も)。
− 漏血検出器を通過する流れが,製造販売業者が指定した漏血アラーム設定値に相当するように,透
析液へ牛血(Hct 32 %)を加える。
201.12.4.4.104.3 *凝固による体外循環血液の損失
個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置に適用し,
次による。
a) 適用装置は,危険状態を引き起こすような血液の流れを中断した結果発生する,凝固による血液の損
失から患者を守る保護システムを備えなければならない。
注記 この要求事項に適合する方法は,例えば,意図的又は不注意に,血液ポンプが長時間停止し
た場合に作動する保護システムである。
b) 保護システムによって,聴覚及び視覚アラーム信号(208.6.3.1,208.6.3.3.2及び208.6.3.3.101参照)が
作動しなければならない。
c) 例えば,抗凝固剤ポンプの停止若しくは開始忘れ,又は後希釈HDFの場合の過剰な補充液の流量に
よる凝固に伴う血液損失の対策は,製造販売業者のリスクマネジメントプロセスの一環として取り扱
われなければならない。
(試験)
適合性は,機能試験及び故障模擬によって確認する。
201.12.4.4.105 *気泡混入
個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置に適用し,
次による。
a) 適用装置は,単一故障状態下においても,危険状態を引き起こすような気泡混入から患者を守る保護
システムを備えなければならない。
注記1 この要求事項に適合する方法は,例えば,溶存していないエアを検出できる気泡検出器(例
えば,超音波)を用いた保護システムである。
b) 保護システムによって,次の安全な状態を達成しなければならない。
− 聴覚及び視覚アラーム信号(208.6.3.1,208.6.3.3.2及び208.6.3.3.101参照)が作動する。
− 単一故障状態下において,動脈側及び静脈側血液回路を介しての更なる気泡混入を防止する。
注記2 更なる気泡混入の防止は,一般的に血液ポンプの停止及び静脈側血液回路の閉塞によっ
て達成できる。
(試験)
適合性は,次のテストの原理を考慮した機能試験によって確認する。
注記3 試験の中の数値は,例である。製造販売業者はリスクマネジメントプロセスで値を決定しな
22
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
ければならない。
注記4 原理として,気泡混入をモニタリングする方法が二つある。
a) エアトラップ(例えば,静脈側ドリップチャンバ)では,気泡に浮力が働くため,水面
位置を正しく設定することによってエアトラップから気泡が出て行くのを防ぐ。ここで
使用される気泡の監視方法は,レベルを監視する方法である。
b) 血液回路(気泡が液体の流れの中にある)で直接監視。この場合,エアの量は流速から
測定できる。
注記4の気泡の監視方法に関係なく,二つの異なる試験手順がある。
•
連続的な気泡混入
− 標準型中空糸ダイアライザ(例えば表面積1 m2〜1.5 m2),推奨の体外循環回路及びカ
ニューレ(例えば16ゲージ)を適用装置にセットする。
− プライミング後に透析液ラインを閉塞又は閉じる。
注記5 これは最悪条件である。脱気された透析液が流れると,ダイアライザで気体が除去されるで
あろう。
− ヘパリン化された血液(ヘマトクリット0.25〜0.35,人血,牛血,豚血)又は適切な試
験液を用いて体外循環回路を作動する。
注記6 適切な試験液は,37 ℃で粘度3.5 mPa・s,かつ,気泡を破砕する界面活性剤を含むものであ
る。
− 試験液の貯蔵容器は,例えば床から100 cm(±20 cm)の高さに置く。
− 試験液の回収容器は,例えば床から100 cm(±20 cm)の高さに置く又は試験液を貯蔵
容器へ再循環する。
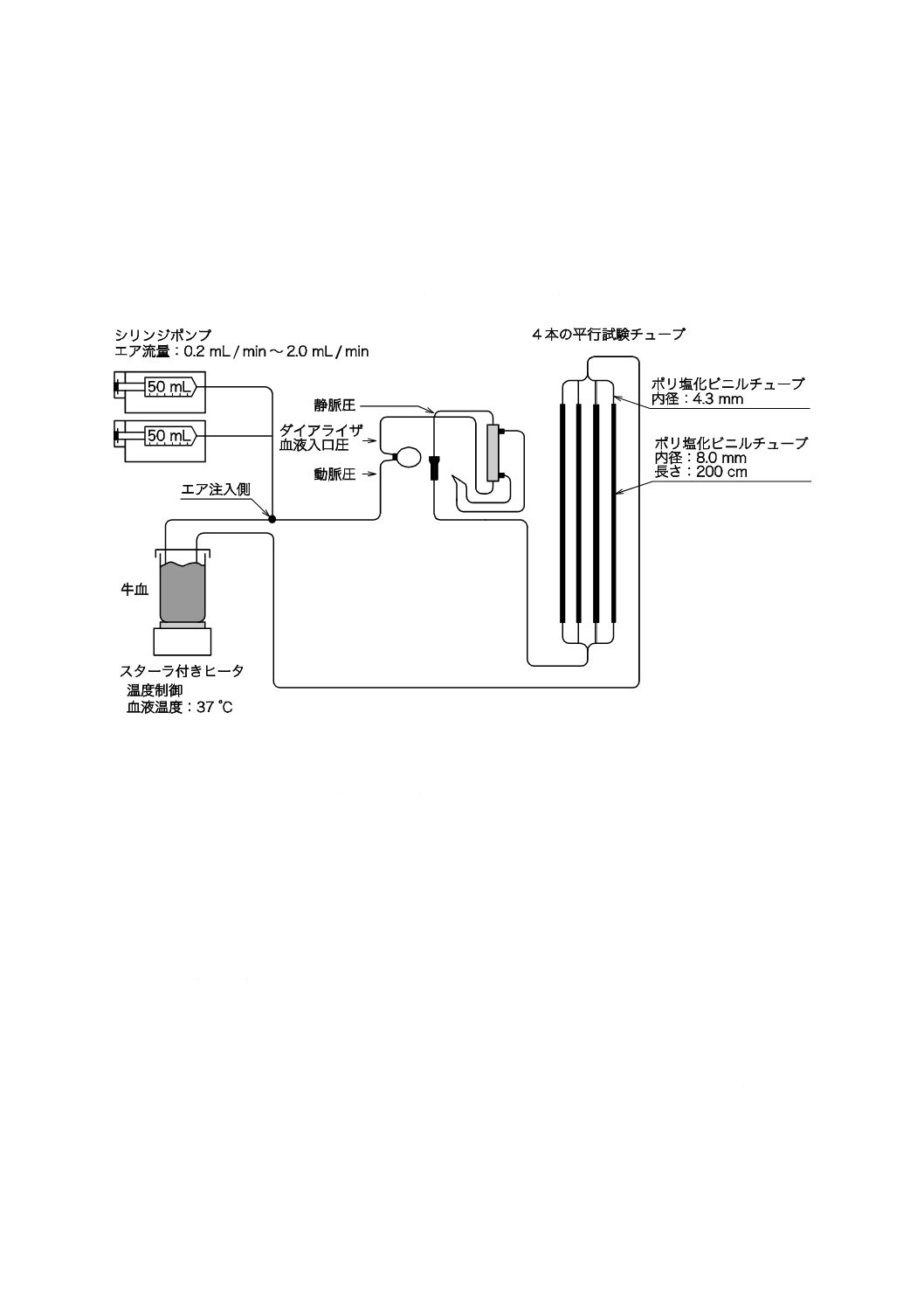
− 少なくとも一つの垂直に配置された直径約8 mm及び長さが約2.0 mの試験チューブを,
より細い直径の第2チューブに沿って,患者コネクタと回収容器との間で静脈側回路の
静脈側患者コネクタに直接付ける(図201.101を例として参照)。
− カニューレ(例えば22ゲージ)を動脈側(脱血)カニューレへの接続の近くの負圧部分
の動脈側血液回路に挿入し,かつ,負圧の条件下でエアの注入制御ができるポンプにそ
れを接続する。
注記7 可能な方法は,小さな逆回転可能なぜん動ポンプの使用である。このポンプは,血液ポンプ
が動き出したときにエアの制御できない注入を避けるように,はじめは逆回転モードで運転
されて試験液で充塡される。針とポンプとの間の逆止弁が使用可能である。
− ポンプ前の負圧が定められた値(例えば−200〜−250 mmHg)になるように,血液ポン
プの速度を調整する。
− 気泡検出器が警報を発するまで,製造販売業者が指定したように速度をゆっくりと増加
してエアを注入する。
注記8 この試験の論理的根拠は,透析液回路が閉じているとエアは体外循環回路から逃げ出せず,
かつ,結局はポンプで注入された速度で回収容器に送り込まれることになるという仮定に基
づいている。
− 気泡検出器の警報が出たら直ちに,試験チューブの両端を閉塞する。
− 例えば15分後に,より細い直径の試験チューブの上部に発生しているエアの量を測定す
23
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
る。
− 血液の流速,試験チューブの体積及び測定されたエアの量からエアの流速を計算する。
•
適用装置がダイアライザの血液の流れ方向を上向き及び下向きの両方を容認している
場合は,それぞれの流れ方向での試験を行わなければならない。
•
リスク分析で,血液ポンプの後でのエアの注入経路(例えば,レベル調整ポンプによ
って)が明らかになった場合は,試験は体外循環回路の同ポイントへ指定された速さ
でエアを送ることによって繰り返されなければならない。
図201.101−空気連続注入試験の寸法例付き構成
・ ボーラス気泡混入
− 標準的な中空糸ダイアライザ(例えば表面積1〜1.5 m2),推奨の体外循環回路及びカニ
ューレ(例えば16ゲージ)を適用装置にセットする。
− プライミング後に透析液回路を閉塞又は閉じる。
注記9 これは最悪条件である。脱気された透析液が流れると,ダイアライザで気体が除去されるで
あろう。
− ヘパリン化された血液(ヘマトクリット0.25〜0.35,人血,牛血,豚血)又は適切な試
験液を用いて体外循環回路を作動する。
注記10 適切な試験液は,37 ℃で粘度3.5 mPa・s,かつ,気泡を破砕する界面活性剤を含むものであ
る。
− 試験液の貯蔵容器は,例えば100 cm(±20 cm)に置く。
− 試験液の回収容器は,例えば100 cm(±20 cm)に置く又は液を貯蔵容器へ再循環する。
− 返血(静脈側)カニューレを通して送り込まれるような,いかなるエアも集められるよ
うに目盛付き測定シリンダ又は前の試験と同じ試験チューブを置く。
− ルアーコネクタ付きのT管を血液回路と動脈側(脱血)カニューレとの間に挿入する。
− T管にルアーコネクタ付きのチューブ片(例えば長さ5 cm)を接続する。
24
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
− 体外循環回路及び前述のチューブ片をプライミングし,チューブ片を閉塞する。
− ポンプ前の負圧が定められた値(例えば0〜−250 mmHg)になるように血液ポンプの速
度を調整し,かつ,クランプを開いても警報が発生しないこと。
− チューブ片のクランプを開き,かつ,気泡検出器によってアラーム信号が作動するまで
待つ。
− 目盛付き測定シリンダ又は試験チューブに集められたエアの量をチェックする。その量
は,指定されたボーラスの限界より少なければならない。
•
適用装置がダイアライザの血液の流れ方向を上向き及び下向きの両方を容認している
場合は,それぞれの流れ方向での試験を行わなければならない。
•
リスク分析で,血液ポンプの後でのエアの注入経路(例えば,レベル調整ポンプによ
って)が明らかになった場合は,体外循環回路の同ポイントへ最大の速さでエアを送
る試験も実施しなければならない。
*201.12.4.4.106
警報オーバライドモード
個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置に適用し,
次による。
a) 治療中は,全ての保護システムが作動しなければならない。
注記1 例外として,次の項目b)を参照。
注記2 この細分箇条の意味する範囲において,治療は患者の血液が体外循環回路から患者に初め
て戻る時に開始したとみなされ,静脈側せん(穿)刺針が外された時に終了したとみなさ
れる。
b) 透析液の組成及び温度の保護システムは,ダイアライザにおいて血液に透析液が最初に接する以前に
作動しなければならない。
c) アラーム状態の間,漏血監視(201.12.4.4.104.2参照)の保護システムには,個別に一時的オーバライ
ドモードを適用してもよい。
d) オーバライドモードの時間は3分を超えてはならない。しかしある臨床条件下では,期限を限定せず
に漏血検出器を完全に又は部分的に無効にしてもよい。
e) オーバライドモードの作動は,保護システムがオーバライドされているという視覚的表示を維持しな
ければならない。
f)
特定の保護システム[項目c)参照]のオーバライドは,次に起こるいかなるアラーム状態にも影響を
与えてはならない。次に起こるアラーム状態は,規定された安全な状態を達成しなければならない。
残留するアラーム状態は,オーバライド時間経過後には再び規定された安全な状態を達成しなければ
ならない。
注記3 この細分箇条の意味する範囲において,オーバライドとは,操作者が意図して保護システ
ムを一時的に無効にすることを選択する場合は,アラーム状態下においても適用装置が機
能できるようにする手段である。治療開始の遅れによる変更は,それによって危険状態を
起こさない場合は,適用装置のオーバライドとはみなされない。
(試験)
適合性は,附属文書の検査及び機能試験によって確認する。
201.12.4.4.107 保護システム
人工腎臓装置に適用し,次による。
25
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
a) 201.12.4.4によって要求される保護システムの故障は,次の期限内に操作者に明らかにされなければな
らない。
b) 201.12.4.4.105(気泡混入)を除く全ての保護システム
− 少なくとも1日1回又はそれが不可能であれば,製造販売業者のリスクマネジメントプロセスでの
決定による。
注記 この要求事項に適合する許容可能な方法は,例えば,
•
操作者によって起動され,かつ,制御される保護システムの定期的な機能チェック。
•
操作者によって起動され,かつ,適用装置によって制御される保護システムの定期的
な機能チェック。
•
適用装置による自己診断のある保護システムの冗長性。
•
適用装置によって起動され,かつ,制御される保護システムの定期的な機能チェック。
ただし,保護システムの定期的な機能チェックは,単一故障によって保護システムと
同時に故障しないように設計されていなければならない。
c) 201.12.4.4.105(気泡混入)によって要求される保護システム
− 気泡検出器の(最初の)故障の結果として,危険状態を引き起こすような量のエアが患者に混入す
る可能性がある場合は,この故障の検出に要する最大時間が,故障耐容時間として計算される。
•
気泡検出器と静脈側カニューレの間の体外循環回路の容積を最大の血流量で除したもの。
− 他の場合は,全てb)が適用される。
(試験)
適合性は,機能試験及び故障模擬によって確認する。
201.12.4.4.108 薬品による汚染の防止
a) 個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置が,洗
浄,滅菌又は消毒モードである間は,患者を治療できてはならない。通則の4.7及び11.8を適用する。
b) 薬品(例えば,水,透析液,消毒剤又は透析液原液)は,単一故障状態下でさえも人工腎臓装置から
いかなる供給ラインへも流れてはならない。
(試験)
適合性は,機能試験及び故障模擬によって確認する。
201.12.4.4.109 *血液ポンプ及び/又は補充液ポンプの逆転
危険状態を引き起こすような治療中の血液ポンプ及び/又は補充液ポンプの意図しない逆転を防ぐ手段
を組み込まなければならない。
適用される危険状態(例えば,動脈側血液回路を介しての気泡混入)は,製造販売業者のリスクマネジ
メントプロセスによって決定されなければならない。ヒューマンエラーも技術的故障と同様に考慮されな
ければならない。
(試験)
適合性は,検査及び機能試験によって確認する。
201.12.4.4.110 運転モードの選択及び変更
運転モードの故意でない選択及び変更は,回避されなければならない。そのとき,ヒューマンエラーも
技術的故障と同様に考慮されなければならない。
(試験)
適合性は,検査及び機能試験によって確認する。
26
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
201.12.4.4.111 オンラインHDF及びオンラインHF
血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置が,オンライン血液ろ過(オンラインHF)
又はオンライン血液透析ろ過(オンラインHDF)を意図している場合は,製造販売業者の取扱説明書に従
ったときに,これらの装置がオンライン補充液の要求事項(例えば,微生物学的)に適合する補充液を作
り出すことができることを製造販売業者は確かにしなければならない。この要求事項は,単一故障状態下
においても適合しなければならない。
(試験)
適合性は,検査及び機能試験によって確認する。
201.13 危険状態及び故障状態
次を除き,通則の箇条13を適用する。
201.13.2.6 *液体の漏れ
追加
人工腎臓装置の送液部分は,通常の動作圧力下で漏れた液体が,例えば,沿面距離の短絡などによって
患者を危険状態にさらすことのないように,電気部品に対して遮蔽されていなければならない。
(試験)
適合性は,次の試験によって確認する。
a) 可動部分は,動かしておくか,又は止めておくかいずれか好ましくない状態にしておき,継手,密閉
部分及び破裂する可能性がある配管にピペットを用いて水道水をかける。
かつ,試験a)で疑いがある場合には,
b) 可動部分は,動かしておくか,又は止めておくかいずれか好ましくない状態にしておき,継手,密閉
部分及び破裂する可能性がある配管からシリンジを用いて,人工腎臓装置のその部分に適切な液体を
噴射させる。
これらの処理の後,人工腎臓装置は,絶縁されていない電気部品又は水道水若しくは選択された液体に
よって悪影響を受けやすい絶縁物にぬ(濡)れた痕跡がないことを示さなければならない。疑わしい場合,
人工腎臓装置は,通則の8.8.3に規定される耐電圧試験を受けなければならない。
他の危険状態の決定は,人工腎臓装置の検査によって確認する。
201.14 プログラマブル電気医用システム(PEMS)
次を除き,通則の箇条14を適用する。
201.14.13
*ネットワーク・データ結合によるPEMSの他の機器への接続
追加
ネットワーク・データ結合と人工腎臓装置との間でのデータ転送は,単一故障状態で患者に危険状態を
引き起こしてはならない。
201.15 ME機器の構造
次を除き,通則の箇条15を適用する。
201.15.4.1 コネクタの構造
追加
27
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
201.15.4.1.101 *透析液原液のコネクタ
個人用透析装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置に適用し,次による。
a) 複数の透析液原液供給容器及び洗浄剤は,適用装置の透析液原液コネクタと機械的接続によって区別
されるか又は恒久的なカラーマークがされてもよい(ISO 13958参照)。
適用装置は,さらに,コネクタの機械的区別によって又はコネクタの色識別によって,患者に危険状態
を引き起こすような複数の透析液原液と洗浄剤の混合を防がなければならない。
注記1 複数の透析液原液を使用する場合,透析液原液ラインの誤接続によって患者に危険状態を引
き起こすような問題が,発生する可能性がある。コネクタの設計及び色識別は,このリスク
を最小限にする方法として認識されている。製造販売業者の取扱説明書に従わない操作によ
って,危険状態を引き起こす可能性があることは常に考えられる。
製造販売業者は,透析液原液の接続において,起こる可能性がある混乱を最小にする取り組みをするこ
とが望ましい。
次の色を透析液原液のコネクタに用いなければならない。
− アセテート用コネクタは,白色でなければならない。
− バイカーボネイト透析のA原液コネクタは,赤色でなければならない。
− バイカーボネイト透析のB原液コネクタは,青色でなければならない。
− 一つのコネクタを異なる透析液原液に使用する場合は,適用装置のコネクタにそれぞれの色表示を貼
らなければならない。例えば,アセテート及びA原液共通コネクタには,白及び赤の表示でなければ
ならない。
(試験)
適合性は,検査によって確認する。
注記2 ISO 13958は,透析液原液の容器の色識別に関する要求事項を提示している。
201.15.4.1.102 *血液圧力トランスデューサ用のコネクタ
JIS T 3248によって規定されるように,血液回路と血液圧力トランスデューサとの間の接続は,ISO
594-2と同等の安全性をもたなければならない。
気泡混入,交さ(叉)感染及び血液損失のような患者へのあらゆるハザードを製造販売業者のリスクマ
ネジメントプロセスにおいて考慮しなければならない。
(試験)
適合性は,機能試験及びリスクマネジメントファイルの検査によって確認する。
201.16 *MEシステム
次を除き,通則の箇条16を適用する。
201.16.1 MEシステムに対する一般要求事項
追加
この個別規格において,MEシステムは透析の全領域に関して,いまだに包括的には試験されていない。
一つの透析施設において,ある特定の製造販売業者による完璧なMEシステムを明確に確認することは,
しばしば困難であるため,人工腎臓装置の製造販売業者には,MEシステムを考慮したリスクマネジメン
トの適用が推奨される(通則のA.4,4.2及び16.1参照)。
201.16.2 MEシステムの附属文書
d) 責任部門への次の助言
28
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
追加
− 人工腎臓装置をセントラル透析液送液システム又は他の送液システムに接続する場合のリスク及び
対策の一覧表作成。例えば,漏れ電流の増加などがある。
(試験)
適合性は,附属文書の検査によって確認する。
201.16.6.3 患者漏れ電流
追加
注記 患者漏れ電流の低減が可能な方法としては,給水システムにおいて導電性の部品を利用するか,
又は透析室の全ての接続ポイントを等電位にし,かつ,保護接地するのが望ましい(ISO 11197
参照)。
201.16.9.1 *接続端子及びコネクタ
追加
− 色識別は,操作者が透析液原液を適切に色識別された透析液原液容器に容易に割り当てることができ
るように貼付されなければならない(201.15.4.1.101参照)。
(試験)
適合性は,検査及び試験によって確認する。
201.17 ME機器及びMEシステムの電磁両立性
通則の箇条17を適用する。
202
電磁両立性−要求事項及び試験
次を除き,IEC 60601-1-2を適用する。
202.3.18 生命維持用医用電気機器又は医用電気システム
追加
注記 透析治療の途中終了は,患者に重大な障害又は死をもたらすことはないため,人工腎臓装置は,
IEC 60601-1-2の3.18で定義される生命維持用装置又はシステムとはみなされない。
208 医用電気機器及び医用電気システムのアラームシステムに関する一般要求事項,試験方法及び適用指
針
次を除き,JIS T 60601-1-8を適用する。
208.4
*一般要求事項
追加
個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置の意図す
る使用に集中治療室又は手術室環境が含まれている場合は,JIS T 60601-1-8の次の細分箇条と異なる追加
のアラームシステムとすることが許される。
•
6.1.2 アラーム状態の優先度
•
6.3.2.2 視覚アラーム信号の特性
•
6.3.3.1 聴覚アラーム信号の特性
JIS T 60601-1-8と異なる追加のアラームシステムとした場合は,
29
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
a) JIS T 60601-1-8に従うアラームシステムを工場出荷時の設定としなければならない。
b) 責任部門だけが,アラームシステムを変更できるようにしなければならない。
(試験)
適合性は,機能試験で確認する。
注記1 附属書AAの表AA.1に個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過
用装置及び多用途透析装置の要求に適合するJIS T 60601-1-8の6.1.2に従う可能なアラーム
状態の優先度を示す。
個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置の意図す
る使用に集中治療室又は手術室環境が含まれていない場合は,JIS T 60601-1-8の次の箇条は強制ではない。
•
6.1.2 アラーム状態の優先度
•
6.3.2.2 視覚アラーム信号の特性
•
6.3.3.1 聴覚アラーム信号の特性
注記2 通則の7.8.1(表示光の色)が適用されるが,操作者応答の緊急性が患者を中心とする要因よ
り優先できる。
208.5.2.1
取扱説明書
追加
注記101 可能性のある全てのアラーム状態の記載及び説明の中で,人工腎臓装置の安全な状態に加
えて,製造販売業者のリスクマネジメントプロセスにおける残留リスクを記載する必要が
ある。
208.6.3
アラーム信号の発生
208.6.3.1
*一般
追加
この個別規格によって規定されない限り,アラーム信号は,視覚的及び聴覚的の両方で発せられなけれ
ばならない。聴覚アラームは,208.6.3.3.101 b)に規定される時間の間,中断することは認められている一
方で,視覚アラームはアラーム状態の時間中,作動したままでなければならない。
(試験)
適合性は,機能試験で確認する。
208.6.3.3.2
*聴覚的なアラーム信号及び情報信号の音量
追加
製造販売業者による初期設定において,個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液
ろ過用装置及び多用途透析装置は,距離1 mで少なくとも音圧レベル65 dB(A)を発生しなければならない。
(試験)
適合性は,JIS C 1509-1のクラス1の測定器のための要求事項に一致する測定器及びJIS Z 8733で指定
される自由音場で,A特性音圧レベルを測定することによって確認する。
208.6.3.3.101
*血液透析装置に関する聴覚アラーム信号の特性
聴覚アラーム信号は,次の要求事項に適合しなければならない。
a) 個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置が,操
作者に聴覚アラーム音量をより低く設定することを許す場合は,その最低限度の値を定義しなければ
ならない。この最低限度の値は,責任部門によってだけ変更されてもよい。責任部門が聴覚アラーム
音量をゼロに減らすことができる場合は,単一故障状態下であることを操作者に気づかせる他の手段
30
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
がなければならない。
b) 聴覚アラーム信号を中断する場合,警報のアラーム音中断の時間は,3分を超えてはならない。
例外は,次による。
201.12.4.4.101(透析液の組成)又は201.12.4.4.102(透析液及び補充液の温度)に記述されたアラー
ム信号に関しては,警報のアラーム音中断の時間は,10分を超えてはならない。
c) アラーム音中断期間中に,あらゆる危険状態を防ぐために,操作者による迅速な対応を要求する他の
警報が引き起こされた場合は,アラーム音中断期間は,中断されなければならない。
(試験)
適合性は,機能試験によって確認する。
210
生理的閉ループ制御器の開発に関するプロセス要求事項
次を除き,IEC 60601-1-10を適用する。
附属書A 一般指針及び理論的根拠
A.2 特定の箇条及び細分箇条の理論的根拠
定義 210.3.20 生理的閉ループ制御器
追加
生体パラメータは,例えば,血液の温度,血圧,脈拍及びヘマトクリットなどである。制御回路のコン
トローラは,生体パラメータを基準値と比較し,かつ,その差を用いて限外ろ過速度(除水速度),電導
度及び温度のような変量に効力を発する制御信号を変更する。
211
*ホームヘルスケア環境で使用する医用電気機器及び医用電気システムに対する要求事項
次を除き,IEC 60601-1-11を適用する。
211.6
ME機器及びMEシステムの分類
追加
電源(商用)への永久設置形接続に加えて,ホームヘルスケア環境では通常使用されない固有の電源プ
ラグのような,非接地コンセントへの接続を防ぐ他の手段を使用することができる。
附属書
次を除き,通則の附属書を適用する。
31
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書G
(規定)
可燃性麻酔剤の発火を引き起こすハザードに関する保護
通則の附属書Gを適用しない。
32
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書AA
(参考)
特定の指針及び理論的根拠
AA.1 一般指針
通則の箇条A.1を適用する。
AA.2 特定の箇条及び細分箇条に関する理論的根拠
次は,この個別規格の特定の箇条及び細分箇条に関する理論的根拠であり,本文の箇条及び細分箇条の
番号と一致する。
注記 次の箇条又は細分箇条番号に付した“†”印(ダガーマーク)は,対応する要求事項に対する
根拠であることを示し,かつ,要求事項の文章でないことを容易に識別できるようにしたもの
である。
201.3.8†
装着部
患者は,血液と透析液を介して個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装
置及び多用途透析装置並びにMEシステムと直接接触する。患者漏れ電流を測定するためには,操作者を
通して,MEシステム又は非MEシステムの部分が患者と直接又は間接に接触することを考慮することも
重要である。
201.3.202† 漏血
血液側から透析液側への圧力勾配があり,かつ,ダイアライザの半透膜の破損があるときだけ,血液が
透析液側に混入する。
漏血は,逆ろ過によって起こる汚染も伴う。
漏血検出器のアラーム設定値以上の血液量が透析液に入ったときだけ,漏血検出器は,半透膜の破損を
見つける。
201.3.210† 血液透析装置
HD,HDF及びHFタイプの機器は,透析液を調製する又は調製しない,個人用透析装置,透析用監視
装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置に分類される。透析液を調製する個人用
透析装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置は,常に水処理システム(ROシス
テム)を必要とする。
HDFタイプの血液透析ろ過用装置及び多用途透析装置は,HD又はHF治療にも使用される。そのため
治療法は,附属品及び設定されたパラメータによって決まる。
201.3.213†及び201.3.214†
オンラインHDF及びオンラインHF
最新の技術によれば,補充液は血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置によって透析
液から作り出される。そのプロセスは,微生物学的ろ過及び体外循環回路への補充液の送液から成り立っ
ている。
33
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
201.3.215† 保護システム
Polaschegg HD, Levin N. Hemodialysis machines and monitors. Winchester J, Koch R, Lindsay R, Ronco C, Horl
W, editors. Replacement of Renal Function by Dialysis, 5th Edition. Kluwer Academic Publishers, 2004: pp.325-449
(page 342) を参照。血液透析装置は,制御システムに加えて,冗長システム(予備若しくは補完システム)
又は保護システムから構成されることを執筆者らは指摘する。患者への危険状態は,制御システム及び保
護システムの両方が故障した場合だけである。これらシステムのいずれかにおける故障の可能性は,1回
の治療当たり10-4以下であり,結果として両システムの故障の可能性は,1回の治療(4〜6時間)当たり
10-8以下である。この観察結果は,最初の執筆者によって1980年代の中頃に3 000台の血液透析装置から
の品質フィードバックデータに基づいて作られ,かつ,FDAによって出版されるアクシデントレポートに
おいて,米国での血液透析装置の故障を原因とする重大な事故が少ないことで裏付けられた。
201.3.218† 限外ろ過
HF又はHDF治療においては,限外ろ過は患者の体重減少[正味の体液除去(除水)]と混同しないこ
とが望ましい。なぜならばこの治療では,補充液流量に相当する量もダイアライザ膜を介して流入するか
らである。
限外ろ過速度=正味の体液除去(除水)速度+補充液流量
201.4.3†
基本性能
基本性能項目の試験手順の定義のために,次の一般的な原則が適用された。
試験手順を定義するに当たり,人工腎臓装置の安全規格は,次のような試験実施部門の一般的な知識を
繰り返して記載しないことが望ましい。
− 測定の適切な方法の選択(例えば,流量メータ又は量及び時間による流量測定)
− 十分な精度をもつ測定器の使用
− 校正された測定器の使用
このため,試験手順は人工腎臓装置を試験するのに必要な基本情報だけを含む。
201.4.3.101† 追加の基本性能要求事項
人工腎臓装置の基本性能は,次の観点が考慮に入れられ決定された。一方では,治療の効果に関して要
求される全てのパラメータを含むことが望ましく,他方では,電磁両立性−EMCイミュニティ試験の照射
条件下でさえ,基本性能は適合しなければならないので,必要以上に多くのパラメータの定義は避けるこ
とが望ましい。基本性能についての非常に多くの観察及び文書化は,EMC試験の非現実的な時間及び高コ
ストの浪費の原因となるであろう。ここで定義された基本性能のリストは,これら二つの相反する観点間
の折衷案である(IEC 60601-1-2参照)。
規格は,典型的な透析手順に一部変更又は拡大することによって行われる特殊な手順全てを記載するこ
とはできないので,この箇条では,標準的な人工腎臓装置だけを記載する。治療の有効性向上のための特
殊な手順がさらなるパラメータを要したり,又はこの規格の基本性能として定義されたパラメータが不要
となるような場合,製造販売業者が示した人工腎臓装置の基本性能項目のリストに追加又は削除して修正
することが望ましい。製造販売業者は,基本性能項目のリスト及びその理論的根拠を示すことが望ましい。
次は,注記へのコメントである。
ぜん動ポンプを使用し,かつ,吸込側における陰圧が大きい場合,血流量はかなり減少する可能性があ
34
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
る。
201.4.3.107† 透析液の組成
透析液の組成を測定するのは複雑であるため,全ての種類の個人用透析装置,多人数用透析液供給装置,
血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置に実用的かつ簡単な方法は今まで見つかってい
ない。透析液の組成を測定する考えは,
− イオン感受性電極による測定。しかしながら,血液分析に用いられている標準的な検査方法は,透析
液中の絶対値を測定するには,精度が不十分である。
− 透析液原液に染料を加えることによる希釈の測定。吸着量は,混合の前後を測定することで分かる。
− 透析液原液の既知の組成に基づいた電導度の理論的な計算。設定の系統的なマトリックスを作成する。
例えば,
•
最も低い注入量設定のバイカーボネイトで最も高い注入量設定のナトリウム
•
最も高い注入量設定のバイカーボネイトで最も低い注入量設定のナトリウム
•
最高のバイカーボネイトで最高のナトリウム
•
最も低い注入量設定のバイカーボネイトで最も低い注入量設定のナトリウム
− 測定値と理論値とを比較する又はマトリックスの成分間での相対的差異若しくは相対比率を比較する。
− バイカーボネイトからナトリウムを分離するために電導度及びpHの測定。
201.7.9.2.2†
警告及び安全上の注意(6番目の“−”)
ダイアライザでの対向流のため,ローフラックスのダイアライザ[限外ろ過率<10 mL/(h・mmHg)]でさ
え,少なくともダイアライザの一部において透析液の逆ろ過が起こる。ハイフラックスダイアライザが使
用される場合は,仮に患者からの体液除去のために許容される高限外ろ過速度がかかった状態であっても,
ダイアライザにおける逆ろ過は生じる。
リークのないダイアライザ膜での逆ろ過による透析液側から血液側への大分子物質の移動は,限定的で
ある。逆ろ過の影響は,透析液から血液への大分子の移動の増加だけである。透析液は,意図的にはその
ような物質を含んでいない。細菌汚染がある場合,透析液は,エンドトキシン及び他の細菌細胞残せつ(屑)
を含んでいる。分解されていない,もともとのエンドトキシン分子が膜を通過することは考えにくいが,
エンドトキシンはより小さな物質へ分解される。発熱反応を引き起こす主要因子であるリピドAの分子量
は,2 000以下であり,これらはローフラックス膜でさえ拡散によって容易に通過することになる。血液中
で細胞の拒絶反応を引き起こす他の分子は,更に低い分子量である。
好ましくない条件でハイフラックス膜を使用した場合でさえ,逆ろ過の影響は50 %未満にすぎない。細
菌及びエンドトキシン汚染が,指数関数で測定されていることを考えると,二つの要因(ダイアライザで
の対向流及びハイフラックス膜)は問題にならない。TMP又は限外ろ過の増加によって逆ろ過を“避ける”
ことは,移動を防ぐ十分な対策としてみなすことはできない。そのため,適切な対策によって細菌による
透析液の汚染を避けることが必要である。
ダイアライザの構造上の漏れによる逆ろ過の影響は,通常,漏血検出器によって検出できない程度の量
に制限される。ぜん動血液ポンプによって作り出される脈流のため,逆及び正の限外ろ過は,ダイアライ
ザで交互に起きることになる。逆ろ過のフェイズの間,細菌は検出されないで血流へ入る可能性がある。
逆流が1 mL/min(漏血検出器の典型的な検出感度より3倍以上大きい)であると仮定すると,透析用水又
は透析液がそれぞれ“日本透析医学会制定の透析液水質基準2008”に従っている場合は,血液の仮想の汚
35
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
染は0.1 CFU/min〜100 CFU/minである。ダイアライザにおいて,漏血検出器の検出限界以下の小さな漏れ
が継続することは,極めて起こりそうもないことである。小さな漏れは,通常数分以内に凝固によってな
くなる。
注記 欧州局方又はAAMIガイドラインでは,血液の仮想の汚染は100 CFU/min〜200 CFU/minであ
る。
201.7.9.2.2†
警告及び安全上の注意(9番目の“−”)
溶血は,高血流量で狭い流路を通過する場合,特に乱流域の過大なせん(剪)断力によって引き起こさ
れる可能性がある。静圧(−600 mmHg〜+1 000 mmHg)は,溶血を引き起こさない。体外循環回路で測
定される圧力上昇は,無症状の溶血を引き起こす可能性がある流体抵抗の増加を示している。急性の溶血
は,血液ポンプの下流から圧力モニタの上流までの血液回路システムにおける障害によって引き起こされ
ると報告されている。そのような障害は,静脈圧モニタでは見つけられない。アクシデントレポートのレ
ビューには次を参照。
Polaschegg HD, Levin N. Hemodialysis machines and monitors. Winchester J, Koch R, Lindsay R, Ronco C, Horl
W, editors. Replacement of Renal Function by Dialysis, 5th Edition. Kluwer Academic Publishers, 2004: 323-447
(pp 328-332)
201.7.9.2.5†
ME機器の説明[7番目の“−”の細別c)]
Kt/Vの適用規格は,例えば,K/DOQIガイドライン及びEuropean Best Practice Guidelines for Haemodialysis
である。
201.7.9.2.12† 清掃,消毒及び滅菌(2番目の“−”)
試験手順には,少なくとも次の記述を含むことが望ましい。
− 推奨される消毒剤のタイプ
− 容器中の消毒剤に要求される濃度
− 人工腎臓装置の配管内の希釈後の消毒剤濃度
− 要求される消毒フェイズの最小時間(人工腎臓装置によって自動的に設定されない場合)
− 要求される洗浄フェイズの最小時間(人工腎臓装置によって自動的に設定されない場合)
201.7.9.3.1†
一般(3番目及び4番目の“−”)
様々な機能を比較するための個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置
及び多用途透析装置での慢性HD治療の典型的な運転条件の提案は,次による。
− 透析時間:4 h+準備時間及び治療後の運転
− 透析液流量:500 mL/min
− 血流量:300 mL/min
− 限外ろ過流量:0.5 L/h
− 透析液温度:37 ℃
− 製造販売業者の指定に従った薬液消毒及び/又は熱消毒
36
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
201.7.9.3.1†
一般(5番目の“−”)
抗凝固剤溶液を送液する機器を備えたシステムは,システム又は保護システムが故障した場合に,次の
危険状態が生じる可能性を考慮することが望ましい。
− 血液を送液する機器が作動していない状態での動脈側の患者接続部から体外循環回路の血流の停止
− 抗凝固剤溶液の不適切な投薬によって引き起こされる危険状態
− 抗凝固剤ポンプが血液ポンプの上流で投薬することによる,動脈側患者接続部を通しての気泡混入(抗
凝固剤ポンプの誤った送液速度又は血液ポンプが作動していない間の抗凝固剤ポンプの送液)
201.7.9.3.1†
一般(11番目の“−”)
漏血検出器を流れる流量は,治療の種類に依存する。HD及びオンラインHDFでは,透析液流量+限外
ろ過流量である。ECUM及びHFでは,限外ろ過流量である。
注記 限外ろ過速度=正味の体液除去(除水)速度+補充液流量(201.3.218 限外ろ過)
201.8.3†
装着部の分類
継続的に水及び/又はセントラル透析液送液システムへ接続された,個人用透析装置,透析用監視装置,
血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置のCF形装着部の要求事項への適合は,高い技
術費用をかけないと達成できない。そのような理由で,心房部位での中心静脈カテーテルのある患者への
B形装着部をもつ個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透
析装置の使用のための例外規則が,確立された。
例外規則の目標は,CF形装着部をもつ個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液
ろ過用装置及び多用途透析装置と同じ有効性で,正常状態及び単一故障状態下で漏れ電流から患者を守る
ことである。漏れ電流の二つの源は,区別されなければならない。
1) 個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置を起源
とする漏れ電流
これらの漏れ電流は,心房部位での中心静脈カテーテルから患者の心臓を介して,接地された患者
ベッド,チェア又はその他へ流れる。正常状態下では,これらの漏れ電流は個人用透析装置,透析用
監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置の保護接地線を介して大地へ流
れる。単一故障状態下(これらの装置の保護接地線の断線)では,漏れ電流を他の対策で最小限にす
る必要がある。
ME機器が,これら特別な漏れ電流制限値に正常状態では適合するが,単一故障状態(すなわち,
保護接地線が断線)では適合しない場合,漏れ電流を必要な低レベルまで減らすために外部に等電位
化導線を使用してもよい。外部の等電位化導線は,不注意による断線(不注意によるプラグの抜け)
が,防止されていなければならない。意図的に工具の使用なしにプラグを抜くこともできる。
2) 患者環境に据え付けられた他の電気機器及びME機器を起源とする漏れ電流
これらの漏れ電流は,心臓及び心房部位での中心静脈カテーテルを介して,患者の体から個人用透
析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置を介して大地へ
流れる。正常状態下では,これらの漏れ電流は外部の機器の保護接地線を介して大地へ流れる。
単一故障状態下(外部の機器の保護接地線が断線)で,かつ,個人用透析装置,透析用監視装置,
血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置がCF形装着部を備えている場合は,装着
部と残りのこれらの装置との間の絶縁障壁は,これらの漏れ電流が患者に到達するのを防ぐであろう。
37
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置がB
形装着部を備えている場合は,これらの漏れ電流を他の対策によって最小限にする必要がある。
個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置以外
に適用しなければならない対策は,この個別規格の適用範囲ではないため,この個別規格で規定する
要求事項は,操作者(201.7.9.2.5の8番目の“−”及び201.7.9.2.2の14番目の“−”)のための附属
文書及び責任部門(201.7.9.2.6の3番目の“−”及び201.7.9.2.2の14番目の“−”)のための附属文
書に記載しなければならない情報である。
中心静脈カテーテルの使用のための備考
•
カテーテル漏れ電流によるミクロショックは,除外できない仮想リスクである。そのようなショック
が発生する可能性は限定される。
•
先端が右心房の中にある中心静脈カテーテルだけが関係する。
•
このことは,リスクのあるカテーテルを上肢[けい(頸)静脈又は鎖骨下静脈]から挿入されるカフ
型カテーテルに限定する。カフ型でない又は大たい(腿)静脈からのカテーテルの先端は通常,心房
に留置されない。
•
また,カテーテル静脈側の側孔は,電流を心臓以外の体にも送る(Jonsson P, Stegmayr B, Polaschegg HD.
Central dialysis catheter leakage current distribution. Nephrol Dial Transplant 2007;22:vi519)。最も,今日,
ほとんどのカテーテルには,返血(静脈)側管こう(腔)に側孔はない。
•
脱血(動脈)側管腔は,電気的に絶縁されているか又は単に高抵抗で接地されている(Jonsson P,
Stegmayr BG. Current leakage in hemodialysis machines may be a safety risk for patients. Artif Organs
2000;24:977-81)。
•
カテーテル先端がカフ型カテーテルとして右心房内に留置される場合は,カテーテルは心房壁には接
触しない。なぜならば,接触すると流れ上の問題が発生する可能性があるからである。ミクロショッ
クによるリスクに基づくCF形への要求事項は,心房に直接に接触する金属電極を使用しての測定を
基礎として作成された。
•
心筋に直接に接触していないカテーテルでは,電流が広い表面積に分布するので,心筋表面の電流密
度は非常に僅かなものとなる。Starmerらは(Starmer CF, McIntosh HD, Whalen RE. Electrical hazards and
cardiovascular function. N Engl J Med 1971;284:181-6)直径2.5 mmの円形表面に流して細動を起こすた
めには,交流500 μAが必要だと報告している。表面積を直径2.5 cmまで増やしたときには,細動に
必要な電流は3 000 μA以上に増加した。
•
深刻な危険状態を引き起こすには,
− カテーテルの先端は右心房の中に留置されなければならない,かつ
− 心房壁に接触(誤って)
− 及び患者が電流源に接触しなければならない。
201.8.7.4.7 aa)†
患者漏れ電流の測定
“警報の発生がない代表的な治療モード”とは,例えば,測定中はヒータがオンであることを意味する。
弁がヒータと患者との間の電流経路を遮断できる場合は,これらの弁は開の状態が望ましい。
201.8.11.2†
マルチタップ
一例は,マルチタップをもつ人工腎臓装置である。一つのソケットは,温度アラーム状態になったとき,
38
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
人工腎臓装置によって電源遮断される外部ヒータ用である。他のソケットは読書灯用であり,かつ,アラ
ーム状態でも遮断されないものである。ヒータを無意識に読書灯用のソケットに接続した場合は,危険状
態となる可能性がある。このようなことは,例えば機械的に互換性のないソケットなどによって防止する
必要がある。
201.11.6.6†
ME機器及びMEシステムの清掃及び消毒
人工腎臓装置の表面は,表面の消毒後に,表面に微生物が残留する可能性がある隙間及び角部がないよ
うな方法で設計されることが望ましい。
次の事項は,どのように消毒の効果及び残留消毒剤が試験できるかの例である。
a) 消毒効果の試験
1) 薬品消毒
消毒の効果試験は,次のステップから成る。
(1) 消毒フェイズにおいて,人工腎臓装置の中の液体が,本当に意図した消毒剤の濃度に達するこ
とを示さなければならない。この試験の目標は,消毒プロセスにおいて,配管部品及びソフト
ウエアが正しく機能することを検証することである。試験は,人工腎臓装置の透析液回路の異
なる場所から液体のサンプルを採取して,かつ,これらサンプルの消毒剤濃度を測定する。
(2) 人工腎臓装置において,消毒剤の接触時間が意図したとおりであることを示さなければならな
い。消毒剤の代わりに色の付いた試験液を用いて,接触時間が期待したとおりであることを,
液体の経路の各場所で視覚的検査によって確認する。
(3) 消毒プロセスにおいて,全ての内部配管が含まれることを示さなければならない。これは本物
の消毒剤の代わりに色の付いた試験液を使用して,通常の消毒を実行することによって示され
る。それから消毒フェイズにおいて,液体システムの全ての部品が色つき液体で満たされてい
ることを視覚的検査によって確認する。一部だけが満たされた又はかなり薄い色の液で満たさ
れたようなチューブ又は容器がないことが,望まれる。そのような試験液は,例えば,“メチレ
ンブルー”又は“フルオレセイン”である。一つの代替方法としては,導電性液体の電導度測
定がある。
(4) 取扱説明書に従った受容可能な最悪条件(低い濃度,最短の時間)において,消毒剤の濃度及
び消毒時間が必要な程度まで微生物を非活性化することを,“定量的懸濁試験”によって示さな
ければならない。この試験は,何種類かの微生物を含む。
次の微生物の組合せは,人工腎臓装置における代表的な薬品消毒法をカバーしているとみな
せる。特定の薬品消毒の方法の妥当性を確認するには,関連する部分組合せ(少なくとも四つ)
を選ぶ。
− 緑のう(膿)菌
− 黄色ブドウ球菌
− 枯草菌胞子
− カンジタ菌
− 黒色アスペルギルス
− 腸内連鎖球菌
ATCC菌株が推奨される。
このステップ4は,次の三つの方法のうちの一つで実施できる。
39
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
a) 1 mL当たりの微生物の数が既知である液体を注入しておき,人工腎臓装置を消毒し,かつ,
必要な程度まで微生物の数が減少したかを確認する。必要な程度とは,関連する規格によ
って決定する。例えば,バクテリアの105(EN 1040)及び酵母菌の104(EN 1275)。試験
は,微生物の個々のタイプごとに,又は幾つかの微生物のタイプを混ぜてのいずれかで行
うことができる。上記に表示された中で関連する部分組合せを使用する(少なくとも四つ)。
b) 人工腎臓装置と同じような条件(消毒剤濃度,温度及び時間)で,かつ,微生物の上記の
全てのタイプを含めて,検査室検査(試験管で)を実施する。
c) 文献によって,例えば,消毒剤の妥当性確認のデータ
2) 熱消毒
製造販売業者は,関連する微生物のどれが最も熱抵抗性があるかを識別する。
熱抵抗性の高い微生物として,枯草菌胞子が使用できる。
上記に示された中の少なくとも四つの微生物を含む液に識別された微生物が加えられ,かつ,人
工腎臓装置の熱消毒を実施する。
熱消毒フェイズにおいて,人工腎臓装置の液体が,本当に必要な時間の間,意図した温度に到達
していることが示されなければならない。この試験の目的は,消毒プロセスにおいて,含まれる部
品及びソフトウエアが正確に機能することを検証することである。この試験は,消毒プロセス時間
中,人工腎臓装置の透析液回路の異なった場所での温度を測定することによって実施する。
3) 薬品及び熱消毒の組合せ
消毒手順の時間中の人工腎臓装置の配管内の温度並びに濃度分布を検証する。
b) 残留消毒剤の試験
消毒の後の洗浄プロセスが,許容レベルまで消毒剤の濃度を減らすことを示さなければならない。
基準としては,参考限界として,“致死量”(致死量50 %未満)が使用されることが望まれる。この試
験は,次の方法で実施する。
消毒剤の代わりに色の付いた試験液(例えば,メチレンブルー又はフルオレセイン)を使用し,通
常の消毒及び洗浄を実施する。まず,洗浄フェイズにおいて,液体システムの全ての部品が色の付い
た液体で満たされたかを確認する。部分的にしか液体で満たされない,又はかなり薄い色の液体で満
たされたような配管又は容器がないことが,望まれる。
洗浄後,液体システムの部品は,色の付いた液体の痕跡を示さないことが望まれる。色の付いた液
体の残留濃度は,光度測定の手段で測定することができる。
色の付いた試験液を使用することは,本物の消毒剤を使用するよりも測定が高感度になるが,プラ
スチックへの消毒剤の浸潤の影響まで考慮できない。
代用の方法は,次のような電導度測定である。液体内の電導度レベルを増加させ,かつ,分析のた
めに人工腎臓装置の最も重要な部分からサンプルを採取する。
201.11.8†
ME機器への電源供給又は電源(商用)の中断
次の項目は,必要の可能性がある追加対策の例である。
− ダイアライザへの透析液の流れを停止する。
− あらゆる補充液の流れを中断する。
− 最小値に限外ろ過を減らす。
− 静脈側血液回路を閉塞する。
40
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
201.12† 制御及び計器の精度並びに危険な出力に対する保護
この個別規格の前のJIS T 0601-2-16:2008では,通常,保護システムの必要なアラーム設定値に対する
いかなる明確な値をも特定していなかった。保護システムによって検出され,かつ,製造販売業者のリス
クマネジメントプロセスにおいて正当化されなければならない危険状態を引き起こす値からの差を定義
することは,製造販売業者の責務であった。
この個別規格のJIS T 0601-2-16:2014の目的は,全てのシステムに適用できるリスクマネジメントプロ
セスのその部分に関して,製造販売業者及び他の利害関係のある組織との間で同意に到達することであり,
かつ,結果を現規格に記載することである。製造販売業者におけるいかなる不要な重複する仕事をも避け,
かつ,テストエージェンシーによる統一された評価を確立することを意図している。
この個別規格を準備するに当たり,原則として急性又は慢性の腎不全に対する治療のための“代表的な”
人工腎臓装置を取り上げた。人工腎臓装置の特性が“代表的な”値から逸脱している場合は,製造販売業
者はリスクマネジメントプロセスにおいて,アラーム設定値を定義及び正当化することが望ましい。
201.12.4.4.101†
透析液の組成
保護システムに関する要求事項は,ヒューマンエラー(例えば透析液原液の取り違え)にも適用し,か
つ,箇条15(ME機器の構造)及び箇条16(MEシステム)にも適用する。
アセテート治療では,次の限度からの逸脱を防止するように保護システムが設計されている場合は,適
切であると考えられる。
− 最終透析液の電導率が12 mS/cm〜16 mS/cm
− 透析液中のナトリウムが設定値から±5 %
バイカーボネイト治療では,さらに次の条件を追加する。
− 透析液中の重炭酸が設定値から±25 %
他の電解質を個別に追加することができる場合は,さらに次の条件を追加する。
− 透析液中のその他の電解質が設定値から±20 %
無緩衝血液透析ろ過(緩衝剤が透析液の一部としてではなく,補充液の一部として患者に投与される特
殊な形態のHDF)及び他の特殊な方法の場合には,技術的安全性の要求事項を製造販売業者のリスクマネ
ジメントプロセスの範囲の中で定めることが望ましい。
201.12.4.4.102†
透析液及び補充液の温度
透析液の温度が体温よりも高い状態が長期間継続すると,熱エネルギーが患者側に移行することになり,
生理的反応が生じる。体温上昇によって皮膚の血流が増加し,かつ,その結果,頻繁に臨床的に関連のあ
る血圧低下を引き起こす。温度が46 ℃を超えると,溶血を引き起こす。
体温が低下すると,不快感及び震えを引き起こす。身体の許容低下温度は,1.0 ℃未満である。
短時間で42 ℃超まで温度を上げることは,例えば,温度測定を利用した再循環の測定のためであれば,
許容される。短時間の上昇であれば,身体のエネルギーバランスの変動を来たさないので,重視する必要
はない。
血液に対する危害(熱による溶血)は,長時間,血液が46 ℃を超えて加熱されたときに起こる。温熱
41
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
治療では,体外循環回路の血液を46 ℃まで加熱している。温度が低い場合は,血液に悪影響はない。
歴史を振り返ると,血液透析では透析液温度を5 ℃で実施してきた。
ダイアライザは,極めて効率的な熱交換器であり,かつ,温度勾配があれば患者の熱エネルギーバラン
スが変わる。熱エネルギーが患者側へ移行する状態が長時間継続すると,血圧低下を引き起こすことが知
られており,熱エネルギーが透析液側に大きく移行する状態が長時間継続すると,患者を不快にし,かつ,
震えが生じる。
血圧低下を引き起こすおそれのある大きなエネルギーが,患者側へ移行する状態を避けるには,透析液
の最高温度を42 ℃以下に設定する。
透析液の温度が低い場合の有害作用としては,患者の不快感以外は知られていない。大量(>5 L)の低
温(4 ℃)の血液を短時間で注入したところ,心臓の温度が33 ℃を下回り,心室細動を来たしたとの報
告がある。血流量が多く,透析液温度が低く(10 ℃),かつ,体重が軽い(50 kg)場合を仮定しても,血
液透析で33 ℃に達するには15分以上かかる。
201.12.4.4.103†
正味の体液除去(除水)
除水バランスの誤差は,その値の正負が重要である。維持透析の場合,除水が不十分であっても患者が
透析から離脱する前にそれを発見し,かつ,是正すれば大きな問題とはならない。一方,過剰な除水は,
危険を伴う。液の補充に伴う水分過剰も危険を伴う可能性があり,かつ,それは治療前の状況に左右され
る。
4時間の透析には,通常,保護システムによって次の限度を監視することが適切であると考えられる。
a) 正味の体液除去(除水)が設定値±0.1 L/hの範囲にあり,かつ,
b) 治療中は常に正味の体液除去(除水)の目標値を±400 mLの範囲に保つこと。
許容できる正味の体液除去(除水)の誤差の安全な限度を生理学的データから導き出すことはできない
が,医療工業会には体液のバランスシステムに関する長年の経験がある。201.12.4.4.103に掲げた限度は,
この経験から得られたものである。
ハイフラックスダイアライザを使用する場合,TMP監視は体液バランスエラー検出に対して,有効な手
段とならない(しかし,TMP監視は,例えば,蛋白の膜付着,透析間で蓄積された尿毒症性物質,漏血検
出器で検知されない程度の膜リーク又はヘパリン不足に伴う凝血によるダイアライザ交換の回避など安全
性及び性能面で重要なモニタリングとなる可能性がある。)。
例えば,接続部での漏れ(補充液を含む),バランスシステム(流量計,バランスチャンバー)での故障
など正味の体液除去(除水)のバランスエラーの原因となる可能性のあるものは,保護システムによって
補完することが望ましい。
201.12.4.4.104.1 a)† 体外循環血液の周囲への損失
静脈圧の監視は,静脈側せん(穿)刺カニューレが抜けたときに直ちに血液の損失を検出するには,必
ずしも適していない。静脈圧は,主に静脈側せん(穿)刺カニューレの流体力学的抵抗によって決まる。
今日,使用される最高500 mL/分に達する高血流量では,特にこれが当てはまる。したがって,静脈圧ア
ラームシステムでせん(穿)刺カニューレが抜けたかどうかが必ずしも検出できるわけではない。
血液ポンプを1台だけ使用するシングルニードル法(“シングルニードル・シングルポンプ”,“SN
click-clack”)で透析を実施する場合は,静脈圧の測定が制御システムの不可欠な部分である。この制御シ
ステムにエラー(例えば圧力センサの値が低値に固着)が生じると,いつまでも静脈圧の上部切替点に到
42
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
達しないということが起こる可能性がある。その結果,圧力が高くなりすぎ,血液回路が破裂して,かつ,
患者の血液が大量に失われる可能性がある。このため,制御システムから独立した保護システム,例えば
独立したマイクロプロセッサによる工程の継続時間の監視を必要としてもよい。
本質的に安全な設計にするには,例えば,ポンプのロータが滑らかなばね式になっていれば回路が破裂
する可能性はない。しかし,この場合は溶血が生じる可能性がある。
このほか,過剰圧力を防止する手段としては,ねじれが生じる可能性を十分に低下させた体外循環回路
ライン及びダイアライザの保持具が挙げられる。
体外循環回路での切断又は欠陥に起因する周囲への血液損失は,いかなる保護システムをもってしても
防ぐことができない。保護システムは,血液の損失を検知し,血液の大量損失を防ぐように設計されるこ
とが望まれる。報告によれば,致命的な血液の損失のほとんどは,カニューレがバスキュラーアクセスか
ら抜けることが原因である。これは個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用
装置及び多用途透析装置によって防止することはできない。従来,静脈圧監視は血液の周囲への損失を防
止するために使用されてきた。このようなセンサは,戻りの血液ラインでの圧力の低下を検知するもので
ある。血液ラインが破裂したり,又は血液ラインがバスキュラーアクセスデバイス(カニューレ又は中心
静脈カテーテル)から外れた場合,バスキュラーアクセスデバイスの中の流体抵抗が高いため,相当な圧
力低下が起こる。静脈側カニューレが内シャントから抜けた場合には,圧力変化が小さすぎるため静脈圧
監視装置には検知されない。圧力低下の程度は内シャント圧の高さ分にすぎず,通常5 mmHg〜20 mmHg
である。患者の体動によって頻繁に警報が出る煩わしさを避けるため,静脈圧の実測値と下限アラーム設
定値との差は,通常10 mmHg〜20 mmHgに設定される。
圧力パルス又は他のパラメータを利用する監視機器は,より感度が高い可能性があるが,それでも欠陥
を検知して,かつ,血液ポンプのスイッチを切るまでに最長で1分かかる可能性がある。この場合,高血
流量では血液の損失が500 mLになる可能性があるが,成人には通常致命的ではない。
出血の影響は,次に記載されている。
GUYTON AC. Circulatory Shock and Physiology of Its Treatment. Guyton AC, editor, Textbook of Medical
Physiology, Eight Edition. W.B. Saunders Company,1991: pp 263-71
201.12.4.4.104.1 c)† 体外循環血液の周囲への損失
警報発生時の動作としては,閉塞した血液ポンプを停止させれば十分であると考えられる。破裂は圧力
が最も高い箇所,すなわち,通常は血液ポンプとダイアライザとの間で起こる可能性が高いため,さらに
安全クランプを閉めても僅かな効果しかない。この場合,静脈側血液ラインからの“逆方向”の血液の損
失は,動脈側血液ラインからの直接的な血液の損失と比べれば,無視できる程度である。
スタッフがいない場合(例えば在宅患者)又は静脈側せん(穿)刺カニューレが抜けたときにスタッフ
が来るのが大きく遅れた場合は,静脈側アクセス(逆方向)からの血液の損失が患者にとって危険となる
可能性がある。
201.12.4.4.104.2† 透析液への漏血
この要求事項に適合する方法は,例えば,漏血検出器を利用した保護システムがある。
漏血が0.35 mL/分(Hct 32 %)以下の場合は,危険状態は生じないと考えられる。
従来,漏血に対する感度は,透析液1リットル当たりのヘモグロビンのミリグラム値(mgHb/L)で特定
されてきた。これはおそらく,ヘモグロビン測定のための分光光度分析法が確立しているためと思われる。
43
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
しかし,mgHbは,臨床医が知りたいパラメータである血液喪失量の推算に必要となる。限界値55 mgHb/L
は,血液の0.35 mL/minに相当することが明らかとなっている。
計算では,正常な被験者における血液100 mL中のヘモグロビン量を14グラム,正常な被験者のヘマト
クリットを46 %(0.46),典型的な血液透析患者のヘマトクリットが取る可能性がある最低値を25 %(0.25),
かつ,透析液流量を500 mL/分と仮定している。
201.12.4.4.104.3† 凝固による体外循環血液の損失
この場合,危害の程度が体外循環回路での血液の損失に限られるため,独立した保護システムは必要な
い。
この規格の作成時点では,体外循環の停止時間と血液凝固の関係に関する学術文献はない。警報遅延時
間の最大値は,3分間が適切であることが経験的に証明されている。
201.12.4.4.105†
気泡混入
この規格の作成時点では,この規格に適する安全なアラーム設定値を規定するには科学論文が少なすぎ
る。“Replacement of renal function by dialysis, 5th ed.”第14章でPolaschegg及びLevinは,0.03 mL/(kg・min)
以下のエアの持続注入及び0.1 mL/kgの大量瞬時注入は,危険状態ではないと判断している。
意図するとおりに使用すれば,血液回路システムの中にエアが存在しない個人用透析装置,透析用監視
装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置において,エアが存在する場合には,既
に第1の故障であり,かつ,同一の治療中にこれとは無関係な第2の故障(例えば気泡検出器の故障)が
生じる可能性はないであろう。この場合,気泡検出器は単一故障安全を備えている必要はない。この点は
リスクマネジメントプロセスによって決定しなければならない。
個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置を意図す
るとおりに使用しても血液回路システムの中に恒常的にエアが存在する場合,例えば部分的に充塡したド
リップチャンバを使用する場合には,システム中のエアの存在は正常状態(第1の故障ではない)である。
正常な操作方法(技術的エラーがない状態)で患者に気泡が注入される可能性がある場合には,気泡検出
器は単一故障安全を備えていなければならない。
気泡検出器が単一故障安全を備えているとされるのは,例えば次の条件を満たすときである。
a) 2チャンネルを備えた設計であり,かつ,治療のたびに各チャンネルの治療前検査を実施する。又は
b) 1チャンネルを備えた設計であり,かつ,治療中に定期検査を実施する。検査の間隔は,故障許容時
間よりも短くしなければならない。故障許容時間は,気泡が気泡検出器から患者接続部に移動するの
に要する最短時間である。
患者への血流を停止させるための単一故障安全を備えた方法は,例えば次のとおりである。
a) 完全な2チャンネル設計であり(例えばポンプの停止及びクランプの閉鎖),かつ,いずれのチャンネ
ルも検査を実施する。又は
b) 血液ポンプ及び患者の方向に送り出す全てのポンプは,二つのチャンネルを介して停止するようにな
っており,かつ,機械的破損(例えばロータのばねの破損)が起きても閉塞による損失が生じ得ない。
気泡検出器の警報によって血液ポンプが停止しても,体外循環回路に蓄積したエアが膨張によって患者
に到達する場合は,患者に対する気泡混入を防ぐためにクランプを追加するものとする。
このことは,通常,気泡検出器がダイアライザよりも下流にある場合にあてはまる。
気泡検出器が血液ポンプからは下流であるがダイアライザよりも上流に位置している場合であって,か
44
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
つ,体外循環回路の陰圧の流路区間での漏れがエア進入の唯一の経路である場合には,クランプの追加は
通常必要ない。
電動エアポンプでドリップチャンバのレベルを上昇又は下降できる個人用透析装置,透析用監視装置,
血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置の場合には,このエアポンプの機能不全によっ
て血液回路システムの中にエアが混入するおそれがある。このエアポンプが,静脈側クランプの閉塞圧力
よりも高い圧力を発生させる可能性がある場合には,静脈側クランプは,もはや安全な回路閉塞クランプ
とはいえない。この場合,単一故障安全を備えた機構によってエアポンプのスイッチも切らなければなら
ない。さらに,血流が停止した場合(例えば警報によって),エアポンプが動脈側血液ラインを介して患
者にエアを押し込む可能性があり,かつ,このエアが気泡検出器に検知されない可能性があることに留意
することが望まれる。
シングルニードル法では,システム内に圧縮エアが存在するため,実際の血流量が設定血流量よりも一
時的に高くなる可能性があることに留意することが望まれる。気泡検出器の走査間隔及び故障許容時間を
決定する場合には,この点を考慮することが望まれる。
また,電源が故障した場合には,体外循環回路の中の加圧されたエアが,静脈側及び/又は動脈側の患
者接続部の方向に流れを発生させる可能性がある。この場合には,エアが患者に到達することを防がなけ
ればならない。
リスク分析では,潜在的なエアの発生源として少なくとも次のものを考慮することが望まれる。
− ドリップチャンバ内のエア
− 血液ライン内の残留エア
− ダイアライザ内の残留エア
− 圧力トランスデューサにつながる監視ライン内のエア
− シングルニードル治療の再循環経路でシステムに入り込んでくるエア
− 体外循環回路に入り込んでくるエア
溶解していないエアは,大きなかたまり及び異なったサイズの泡の形をとることができる。
リスク分析では,気泡検出器に使用されている全ての物理学的原則及び電気的遅延又は不感時間を考慮
することが望まれる。現代では,体外循環回路内のエアの検知には,ほぼ例外なく超音波気泡検出器が使
用されている。このような気泡検出器の中には,部分的にエアで満たされた静脈側ドリップチャンバに設
置されているものもある。そのような検知器は,通常,液面検出器として設計されており,液面が低下し
たり,又はドリップチャンバが気泡で満たされたりしたときに警報を発する仕組みになっている。
このほか,血液回路に直接設置される気泡検出器もあり,かつ,それらは通常,危険状態が生じると思
われる体積よりもさらに小さな体積の気泡を個別に検知することが可能である。気泡検出器の重要なパラ
メータは,このような個々の気泡の累積体積である。警報の煩わしさを避けるため,検知された気泡の数
は,時間関数によって積分される。
201.12.4.4.106†
警報オーバライドモード
不注意で漏血検出器を無効にすることができないことが望ましい。考えられる解決法としては,例えば
操作者側で二つの独立した動作を必要とするようにすること,かつ,治療を開始する度に再起動するよう
にすることが挙げられる。漏血検出器の無効化によって血液損失のリスクが必要以上に増大することがな
いようにすることが望まれる。適切な方法は,漏血検出器のスイッチを完全に切るだけではなく,感度を
下げることもでき,かつ,次回治療を開始するときに,この感度低減が自動的に解除されるように検出器
45
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
を設計することである。
201.12.4.4.109†
血液ポンプ及び/又は補充液ポンプの逆転
ヒューマンエラーに起因する危険状態の例
透析装置の主電源が故障した場合,スタッフのストレスが高まっている可能性が極めて高く,したがっ
てヒューマンエラーが比較的起こりやすい。このような状況で血液ポンプの方向を間違え,動脈側ライン
からの気泡混入の危険状態(該当する場合)を避けるには,例えば次の方法がある。
a) 手動でクランクを回すときに,回転方向の間違いを防止するには,
− 一方向性のクラッチ機構を採用する。若しくは,
− ポンプにはっきりと分かる矢印を付ける。又は,
b) 電池からの給電で血流を継続させることによって手動クランク操作を避ける。
技術的な欠陥に起因する危険状態の例
技術的な欠陥によって,血液ポンプ及び/又は補充液ポンプが間違った方向に回転する可能性がある。
これを避けるには,例えば次の方法がある。
a) 任意のいかなる機械の故障が発生しても電流の方向が逆転することがないように,DCモータに電気
機械的な整流装置を取り付ける。又は,
b) モータ制御システムから独立し,方向が間違っている場合には,モータを停止させる保護システムを
稼動させる。
201.13.2.6† 液体の漏れ
この検査は,液体が通常運転圧力下で流出する可能性を検討するものである。その実行及び再現は難し
いが,この個別規格で規定されているこの検査は,この種の装置には適していると考えられる。
201.14.13† ネットワーク・データ結合によるPEMSの他の機器への接続
人工腎臓装置の設定値をネットワーク経由で伝達するときのリスクを減少させる方法は,人工腎臓装置
において,その設定値を有効にする前に操作者がデータ転送を実際に実行して確認するような明確な試験
を行うことである。
201.15.4.1.101†
透析液原液のコネクタ
透析液原液は,液体の形で使用される。液体の透析液原液は容器から取るが,これらは構造上の特徴に
よる誤用防止が施されていない。
リスクマネジメントプロセスでは,少なくとも次の種類の透析液原液を考慮に入れることが望まれる。
− アセテート透析液原液
− 塩化ナトリウムを含まないB原液とともに用いるA原液
注記1 35倍,36.83倍,45倍に希釈して用いる。
− 塩化ナトリウムを含むB原液とともに用いるA原液
注記2 35倍,36.83倍,45倍に希釈して用いる。
− 塩化ナトリウムを含まないB原液
注記3 液体の形で供給される。
− 塩化ナトリウムを含むB原液
46
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
− 塩化ナトリウム
注記4 液体の形で供給される。
− ナトリウム及びバイカーボネイトを補完する濃縮物
注記5 ナトリウム及びバイカーボネイトの濃縮物を別々に供給する混合システムに用いる。
注記6 液体の形で供給される。
201.15.4.1.102†
血液圧力トランスデューサ用のコネクタ
個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置の汚染を
防止する一つの方法は,内部圧力トランスデューサと外部トランスデューサプロテクタへの接続部との間
に内部トランスデューサプロテクタを設置することである。
201.16†
MEシステム
透析のMEシステムは,1台又はそれ以上の人工腎臓装置並びに次のものを一つ又はそれ以上で構成さ
れる。
− 水処理システム
− 排液装置(配水管)
− データ伝達システム
− セントラル透析液送液システム
− スタッフ呼出しシステム
注記 患者環境には,他の装置の接触電流が存在するため(例えば透析チェア),このような装置には
等電位化導線が必要となる場合もある。
水処理システムは,通常,個人用透析装置,多人数用透析液供給装置,血液透析ろ過用装置,血液ろ過
用装置及び多用途透析装置から離れた場所に設置され,かつ,マルチタップを介して接続することはでき
ない。設置のときに,供給ラインに例えば個人用透析装置,多人数用透析液供給装置,血液透析ろ過用装
置,血液ろ過用装置及び多用途透析装置と同じ電圧をかけることによって,生じるリスクを受容できるレ
ベルに低減することが必要である。
47
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
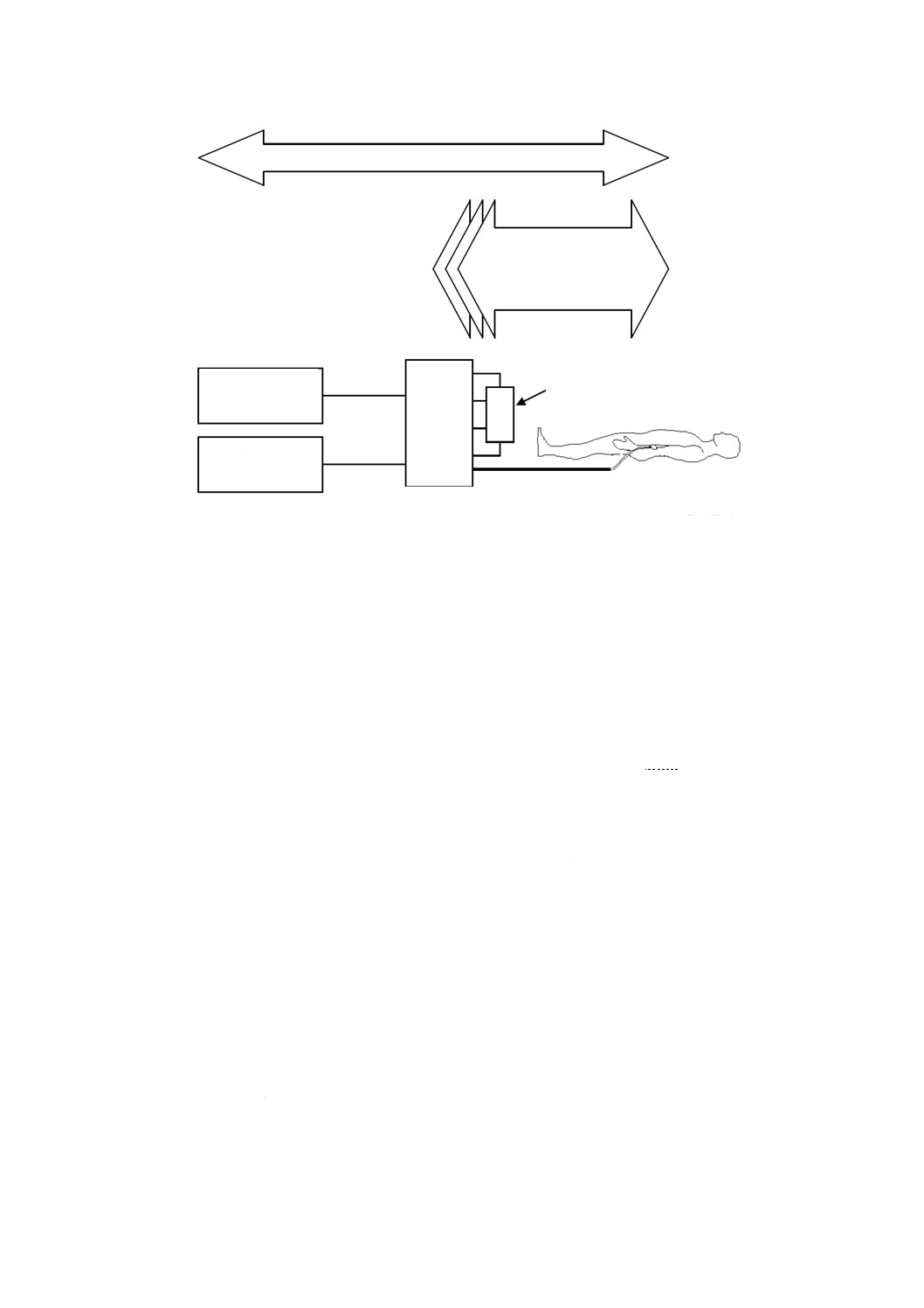
図AA.1−血液透析用MEシステムの例
CF形装着部を含む個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用
途透析装置では,次の項目を考慮することが望まれる。
体外循環回路の血液ラインは,絶縁されていないと考えられる。回路の中及び周りの導電性溶液が,患
者との電気な接触を確立すると想定することが望まれる。
体外循環回路又は透析液回路は,次の条件を満たすときに絶縁していると判断される。
a) その物質が電気的に絶縁されている,かつ,
b) 破裂の可能性が十分に低くなるようにその回路が作られている。
ポイントa)は,0.9 %塩化ナトリウム溶液を充塡した回路の関連部分に交流1 000 Vを印加することで検
査する。回路の周りに,長さ10 cmにわたって導電性フォイルを巻く。最低でも1分間はフォイルと液体
との間に漏れがないことが望まれる。
ポイントb)は,個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透
析装置と回路とのインターフェース及び製造工程を含むリスクマネジメントによって,回路を製造した製
造販売業者が証明する。
201.16.9.1† 接続端子及びコネクタ
現在の技術では,“透析液の組成”に関する保護システムは,電導度の測定又は混合液の容積計量に基
づいている。運転モード(アセテート,バイカーボネイト)中の不適切な透析液原液は,しばしばこの電
導度の測定又は混合液の容積計量によって検知される。
期待された範囲内の電導度でできている透析液原液であるものの,その組成に関係する治療のタイプに
おいて危険状態となる場合(例えば,アセテート透析用に45倍希釈比率のA原液),色識別のほかに追加
の対策が,リスクマネジメントによって要求されてもよい。
そのような場合,責任部門は,アセテート透析運転モードを無効化するか又は個人用透析装置,多人数
用透析液供給装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置と透析液原液の容器を機械
MEシステム
ダイアライザ
装着部又は
同様に使用される部分
血液透析装置
水供給システム
透析液原液
供給システム
48
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
的に符合させるような,適切な運転モードをもたらす色識別に同等な適切な対策を着手することが望まれ
る。
208.4† 一般要求事項
JIS T 60601-1-8は,集中治療又は手術といった環境での観点から記載されており,かつ,まさに患者中
心の観点からのアラーム状態の原因への対処の失敗から起こりそうな結果を6.1.2アラーム状態の優先度
に追加した。個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装
置は,主に慢性患者の通院という形で使用される。患者は,通常,生命を脅かされるような状況にはなく,
アラーム状態はほとんどが技術的な原因で起こり,かつ,大部分の問題において安全な状態へ移行するこ
とができる。これは,患者及び操作者にとっては時間のロスとなるだけであるが,次に続く治療シフトが
時間的に厳密に計画されている場合は,非常に重大な問題の一つとなる。通常,患者環境で個人用透析装
置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置以外のME機器が継続的
に使用されることはない。
この外来通院という環境においては,アラーム分類は,患者が生命を脅かされ,かつ,治療が生命を維
持しているという環境とは,全く異なる優先度を必要とする。6.1.2アラーム状態の優先度の表1は,外来
通院環境で要求される優先度を反映していない。
個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置は,救命
救急治療環境でさえ,生命維持としての目的ではなく,ほとんどの警報状況は,患者及び操作者への危険
状態となっていない。したがって,その警報優先度は低い。場合によって,慢性血液透析の操作者が,集
中治療環境にある個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透
析装置を運転する。
集中治療環境で使用されない個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置
及び多用途透析装置において,実際に使用され,かつ,長年にわたって操作性が最適化されたアラームシ
ステムが,JIS T 60601-1-8適用によって改悪されないことが望ましい。
この理由から,この規格では,集中治療環境での使用が意図する使用である個人用透析装置,透析用監
視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置の場合にだけ,JIS T 60601-1-8の完全
な実施を要求する。この環境に関して,JIS T 60601-1-8に従うアラーム状態の優先度をいかに個人用透析
装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置のニーズに適用できる
かを表AA.1に示す。個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用
途透析装置が,両方の環境での使用を意図する場合は,JIS T 60601-1-8に従うアラームシステムを実施し,
かつ,責任部門によって選択可能になっていることが望ましいが,6.1.2アラーム状態の優先度,6.3.2.2視
覚アラーム信号の特性及び6.3.3.1聴覚アラーム信号の特性,とは異なるアラームシステムを追加対応する
ことは差し支えない。
この個別規格は,画面から独立した表示灯で視覚アラームを表示する画面を備えた個人用透析装置,透
析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置では,要件ではない。これは,
画面上にアラームを表示するかどうかを定めたアプリケーションがあると考えられるためである。大規模
な血液透析室では,表示灯を上方の位置に設置して,かつ,遠い場所からも見えるようにして,個人用透
析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置にアラーム信号を作
動させたほうがよい場合がある。
49
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
表AA.1−個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液ろ過用装置及び多用途透析装置の
ニーズに適用されるJIS T 60601-1-8:2012に従う可能なアラーム状態優先度
アラーム状態
アラーム状態の優先度
様々な理由(例 圧力,技術的故障)
血液システムを停止に導く理由
低優先度,黄色
体外循環システムでの凝固による血液損失
上記警報の拡大としての血液ポンプ停止警報(201.12.4.4.104.3) 中優先度,黄色の点滅
商用電源の停止−電池運転システム,電池機能低下前
偶発的なせん(穿)刺針又はカテーテルの外れに伴う,せん(穿)刺針又はカテーテルで起こる可能性がある血液
損失
低い静脈圧で検出可能
高優先度,赤の点滅
他の規格で規定していない場合は,生体アラーム状態
生体警報,例えば,非侵襲血圧限界警報
高優先度,赤の点滅
二つの異なる限界点による段階化可
治療からの逸脱,処方への影響
例えば,バランス警報,透析液の長時間バイパス
低優先度,黄色
技術情報
血液が流れている状態(血液の送液システムは作動中)での技術
的な故障。例えば,透析液の短時間のバイパス
情報信号として,例えば,緑の点滅
代替えとして,低優先度,黄色
体外循環血液の周囲への損失があった場合に発せられるアラーム信号(201.12.4.4.104.1を参照)は,操
作者の即座の応対を必要とする高優先度のアラーム信号の一例である。血流が長時間停止する場合
(201.12.4.4.104.3),これは中優先度のアラーム信号の一例である。それ以外のほとんどのアラーム状態で
は,少なくとも一時的には保護システムが個人用透析装置,透析用監視装置,血液透析ろ過用装置,血液
ろ過用装置及び多用途透析装置を患者にとって安全な状態にし,かつ,そのようなアラーム信号は低優先
度のアラーム信号として示される。その他のアラーム信号は,製造販売業者のリスクマネジメントプロセ
スで決めることが望ましい。
208.6.3.1† 一般
操作者が画面の内容を設定することを許されている場合は,製造販売業者は警報があらゆる状況でも表
示できるような構成方法(かつ取扱説明書には注記しない)とする必要がある。
208.6.3.3.2† 聴覚的なアラーム信号及び情報信号の音量
この種の消音機能は自動的には終了しないので,操作者が警報を止めようとして音量調節機能の誤った
使用をしないようにということを意図している。それでも,責任部門は警報音を現場の騒音レベルに見合
う適正な値に調整できることが望まれる。
208.6.3.3.101† 血液透析装置に関する聴覚アラーム信号の特性
警報が3分以上中断しても危険状態とはならないような場合に,警報の原因の排除に3分以上かかる場
合がある。それは,例えば,透析液原液容器が空になった場合の濃度警報などである。この場合,警報の
アラーム音中断であってもバイパスモードで運転中であれば,患者の状態をそれ以上悪化させることはな
い。
50
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
211†
ホームヘルスケア環境で使用する医用電気機器及び医用電気システムに対する要求事項
電源(商用)への永久設置形接続に加えて,通常のホームヘルスケア環境では使用されない固有の電源
プラグのような非接地コンセントへの接続を防ぐ他の手段を使用することができる。このことは,患者操
作者に,不適切な保護接地接続をもつ他の電源(商用)ソケットに接続してしまうという問題を起こすこ
となく,装置を取り外すことを可能にする。固有の電源(商用)ソケットが使用される場合は,電源(商
用)ソケットは,責任部門によって設置され,かつ,テストする必要がある。
51
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書BB
(参考)
人工腎臓装置におけるハザード,予想される一連の事象及び危険状態の例
表BB.1は完全なリスク分析であることを意図しておらず,かつ,部分的及び単なる例として提示している。挙げられている危害のレベルは全ての
患者群に適用されるものではない。リスクアセスメントは各製造販売業者の責任である。
表BB.1−JIS T 14971:2012,附属書Eによるハザード状況リスト
ハザード
予想される一連の事象
危険状態
危害
参照規格
多数のハ
ザードの
可能性
静脈側せん(穿)刺針がバスキュラーアクセ
スに穴をあける。
体外循環血液が静脈側せん(穿)
刺針を通じて組織内に入る。
血腫
ヘパリンの注入速度又は注入量が多すぎる。 血液のヘパリン濃度が高すぎる。 過剰な出血
− JIS T 0601-2-16(この規格): 201.11.8
血流が長時間にわたって停止
体外循環血液の凝固
血液の損失
− JIS T 0601-2-16: 201.7.9.2.5,201.7.9.3.1,201.11.8,
201.12.4.4.104.3
− JIS T 0601-1:2012,7.9.2.4
電源の中断が長すぎる。
− JIS T 0601-2-16: 201.11.8,201.7.9.3.1,
201.12.4.4.104.3
血流に比して限外ろ過速度が高すぎる。
ヘマットクリットの上昇でダイ
アライザの中空糸が詰まる可能
性あり。
− JIS T 0601-2-16: 201.12.4.4.104.3
静脈側せん(穿)刺針が抜ける。
体外循環血液が周囲に流れ出す。
− JIS T 0601-2-16: 201.7.9.2.2の7番目の“−”,
201.7.9.3.1の2番目の“・”の6番目の“−”,
201.12.4.4.104.1
動脈側血液ポンプ後の消耗品のコネクタが開
放する又は漏れる。
− JIS T 0601-2-16: 201.7.9.2.2の3番目の“−”,
201.12.4.4.104.1
破裂を導くような消耗品の耐圧以上の圧力
− JIS T 0601-2-16: 201.12.4.4.104.1
血液ポンプ後のヘパリンポンプシリンジプラ
ンジャーが抜け落ちる。
− JIS T 0601-2-16: 201.12.4.4.104.1
ダイアライザの膜又は中空糸の破れ
血液が透析液中に漏れる。
− JIS T 0601-2-16: 201.7.9.3.1の2番目の“・”の7
番目の“−”,201.12.4.4.104.2
2
T
0
6
0
1
-2
-1
6
:
2
0
1
4
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
52
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
表BB.1−JIS T 14971:2012,附属書Eによるハザード状況リスト(続き)
ハザード
予想される一連の事象
危険状態
危害
参照規格
多数のハ
ザードの
可能性
意図しない血液の逆流及びシステム内のエア 動脈側分岐からの気泡混入
気泡混入
− JIS T 0601-2-16: 201.7.9.3.1の2番目の“・”の2
番目の“−”,201.12.4.4.109
レベル(液面)調整ポンプが動脈側血液ポン
プ前の動脈圧モニタへエアを送り込む。
− JIS T 0601-2-16: 201.7.9.3.1の2番目の“・”の2
番目の“−”,201.12.4.4.109
血液ポンプ前で血液側にエアを吸い込む(部
材損傷又は注入口の不慮の開口)。
静脈側分岐からの空気混入
− JIS T 0601-2-16: 201.7.9.2.2の8番目の“−”,
201.7.9.3.1の2番目の“・”の2番目の“−”,
201.12.4.4.105,201.12.4.4.106,201.12.4.4.107
レベル(液面)調整ポンプが動脈側血液ポン
プ後の動脈及び/又は静脈圧力モニタへエア
を送り込む。
− JIS T 0601-2-16: 201.7.9.3.1の2番目の“・”の2
番目の“−”,201.12.4.4.105,201.12.4.4.106,
201.12.4.4.107
補充液ポンプが静脈側分岐にエアを送り込
む。
− JIS T 0601-2-16: 201.7.9.3.1の2番目の“・”の2
番目の“−”,201.12.4.4.105,201.12.4.4.106,
201.12.4.4.107
凝血又は超音波ゲルによる超音波気泡検出器
の機能不全
− JIS T 0601-2-16: 201.7.9.2.2の10番目の“−”
シングルニードル治療での再循環経路へのエ
ア進入
− JIS T 0601-2-16: 201.7.9.2.2の11番目の“−”
血液回路のねじれ(特にダイアライザの入口) 赤血球への高せん(剪)断力の印
加
溶血
− JIS T 0601-2-16: 201.7.9.2.2の9番目の“−”
ポンプ前の動脈圧の強い陰圧による血流量低
下
透析効率の低下
処方透析量の
未達
− JIS T 0601-2-16: 201.7.9.2.2の13番目の“−”
透析液の脱気不足
新鮮透析液の流量不足
− JIS T 0601-2-16: 201.7.9.3.1の2番目の“・”の4
番目の“−”
技術上の問題による血流量の過度の低下
− JIS T 0601-2-16: 201.4.3.101
透析液がダイアライザをバイパス
− JIS T 0601-2-16: 201.4.3.101
技術上の問題による有効透析(運転)時間の
過度の不足
− JIS T 0601-2-16: 201.4.3.101
技術上の問題による補充液流量の過度の低下
− JIS T 0601-2-16: 201.4.3.101
2
T
0
6
0
1
-2
-1
6
:
2
0
1
4
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
53
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
表BB.1−JIS T 14971:2012,附属書Eによるハザード状況リスト(続き)
ハザード
予想される一連の事象
危険状態
危害
参照規格
生物学的
前の患者の血液の装置受圧口への流れ込み。 パイロジェン,エンドトキシン,
バクテリア又はウイルスが血液
に直接感染[交さ(叉)感染]す
る可能性あり。
ウイルス,バク
テリア感染又
はパイロジェ
ン反応
− JIS T 0601-2-16: 201.15.4.1.102
装置の内部及び外部の消毒手順がウイルス汚
染を除去するには不十分。
− JIS T 0601-1:2012: 7.9.2.12,11.6.6
− JIS T 0601-2-16: 201.7.9.2.12の1番目,2番目及び
3番目の“−”,201.11.6.6
オンラインHDF又はオンラインHFシステム
の透析液側から血液への汚染透析液の注入
パイロジェン,エンドトキシン又
はバクテリアが血液に直接感染
する可能性あり。
− JIS T 0601-2-16: 201.7.9.3.1の2番目の“・”の14
番目の“−”,201.12.4.4.111
外装表面の汚染
バクテリアによる皮膚汚染
バクテリア汚
染
− JIS T 0601-2-16: 201.7.9.2.2の1番目の“−”
化学的
装置の消毒モード運転中の患者治療
血液の毒素汚染
中毒又はアレ
ルギー
− JIS T 0601-2-16: 201.12.4.4.108
透析液回路の消毒後の洗浄不足
− JIS T 0601-2-16: 201.11.6.6
操作者がB原液若しくはA原液又はアセテー
ト透析液原液容器の替わりに消毒液容器を使
用。
− JIS T 0601-1:2012: 15.4.1
− JIS T 0601-2-16: 201.15.4.1.101
有害物質の透析液への接触
− JIS T 0601-1:2012: 11.7
− JIS T 0601-2-16: 201.7.9.3.1の2番目の“・”の13
番目の“−”
生物学的
水への液戻り
血液の毒素汚染
中毒又はアレ
ルギー
− JIS T 0601-2-16: 201.12.4.4.108
多数のハ
ザードの
可能性
透析液又は補充液の温度が過度に低い。
血液が直接(注入)又はダイアラ
イザを介して冷やされる。
心停止に至る
までの冷却
− JIS T 0601-1:2012: 12.4.3
− JIS T 0601-2-16: 201.7.9.3.1の2番目の“・”の4
番目の“−”,201.12.4.4.102,201.11.8
透析液又は補充液の温度が過度に高い。
血液が直接(注入)又はダイアラ
イザを介して加熱される。
溶血
− JIS T 0601-1:2012: 12.4.3
− JIS T 0601-2-16: 201.7.9.2.6の4番目の“−”,
201.7.9.3.1の2番目の“・”の4番目の“−”,
201.12.4.4.102,201.11.8
透析液組成が処方より低い。
血液が低濃度(NaCl)の透析液
で透析又は注入(オンライン
HDF)される。
低ナトリウム
血症
− JIS T 0601-1:2012: 12.4.3
− JIS T 0601-2-16: 201.4.3.101,201.7.9.3.1の2番目
の“・”の3番目の“−”
透析液組成が120 m mol/Lより低い。
溶血
− JIS T 0601-1:2012: 12.4.3
− JIS T 0601-2-16: 201.12.4.4.101
2
T
0
6
0
1
-2
-1
6
:
2
0
1
4
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
54
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
表BB.1−JIS T 14971:2012,附属書Eによるハザード状況リスト(続き)
ハザード
予想される一連の事象
危険状態
危害
参照規格
多数のハ
ザードの
可能性
透析液組成が処方より高い。
血液が高濃度(NaCl)の透析液
で透析又は注入(オンライン
HDF)される。
高ナトリウム
血症
− JIS T 0601-1:2012: 12.4.3
− JIS T 0601-2-16: 201.4.3.101,201.7.9.3.1の2番目
の“・”の3番目の“−”
透析液組成が160 m mol/Lより高い。
− JIS T 0601-1:2012: 12.4.3
− JIS T 0601-2-16: 201.12.4.4.101
バイカーボネイト濃度が低すぎる透析液
血液が低濃度(バイカーボネイ
ト)の透析液で透析又は注入(オ
ンラインHDF)される。
アシドーシス
− JIS T 0601-1:2012: 12.4.3
− JIS T 0601-2-16: 201.12.4.4.101
アセテート透析が選択されているときに,ア
セテート原液の代わりにA原液を使用。
− JIS T 0601-2-16: 201.7.9.2.5の2番目の“−”,
201.12.4.4.101,201.15.4.1.101,201.16.9.1
バイカーボネイト透析が選択されているとき
に,B原液の代わりにA原液を使用。
− JIS T 0601-2-16: 201.7.9.2.5の2番目の“−”,
201.12.4.4.101,201.15.4.1.101,201.16.9.1
バイカーボネイト透析が選択されているとき
に,B原液の代わりにアセテート原液を使用。
− JIS T 0601-2-16: 201.7.9.2.5の2番目の“−”,
201.12.4.4.101,201.15.4.1.101,201.16.9.1
バイカーボネイト透析に代わりにアセテート
透析
高酢酸血症
− JIS T 0601-2-16: 201.12.4.4.110
バイカーボネイト濃度が高すぎる透析液
血液が高濃度(バイカーボネイ
ト)透析液で透析又は注入(オン
ラインHDF)される。
アルカローシ
ス
− JIS T 0601-1:2012: 12.4.3
− JIS T 0601-2-16: 201.12.4.4.101
バイカーボネイト透析が選択されているとき
に,A原液の代わりにアセテート原液を使用。
− JIS T 0601-2-16: 201.7.9.2.5の2番目の“−”,
201.12.4.4.101,201.15.4.1.101,201.16.9.1
補充液ボーラス量が多すぎる。
血液量の増加
細胞外液量の
変化
− JIS T 0601-1:2012: 12.4.3
− JIS T 0601-2-16: 201.12.4.4.103
技術的故障によってプライミング量又は返血
量が多すぎる。
− JIS T 0601-1:2012: 12.4.3
− JIS T 0601-2-16: 201.12.4.4.103
ダイアライザへの透析液流入量が流出量より
も多い。
− JIS T 0601-2-16: 201.12.4.4.103,201.7.9.2.2,
201.7.9.2.5,201.7.9.3.1
補充液量が限外ろ過量より多い。
− JIS T 0601-1:2012:12.4.3
− JIS T 0601-2-16: 201.12.4.4.103
ドライウェイトの未達
血中水分の除去不足
透析中水分過
剰
− JIS T 0601-1:2012: 12.4.3
− JIS T 0601-2-16: 201.12.4.4.103
2
T
0
6
0
1
-2
-1
6
:
2
0
1
4
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
55
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
表BB.1−JIS T 14971:2012,附属書Eによるハザード状況リスト(続き)
ハザード
予想される一連の事象
危険状態
危害
参照規格
多数のハ
ザードの
可能性
補充液ボーラス量が少なすぎる。
患者血液量の増加不足
細胞外液量の
変化
− JIS T 0601-1:2012: 12.4.3
限外ろ過量が多すぎる。
血中水分の過剰除去
− JIS T 0601-1:2012: 12.4.3
− JIS T 0601-2-16: 201.12.4.4.103
限外ろ過速度が設定速度より高い。
− IEC 60601-1-10:2007:箇条4
− JIS T 0601-2-16: 201.12.4.4.103,201.7.9.2.2,
201.7.9.2.5,201.7.9.3.1,201.11.8
バランスシステムからの透析液の喪失
− JIS T 0601-2-16: 201.12.4.4.103
限外ろ過量が補充液量より多い。
− JIS T 0601-2-16: 201.12.4.4.103
操作上
電源中断によるデータ又は指示の復元間違い 誤った治療
多種の危害の
可能性がある。
− JIS T 0601-2-16: 201.11.8
患者カード又はネットワークからの誤った治
療データ又は指示
− JIS T 0601-1:2012: 14.13
− JIS T 0601-2-16: 201.14.13
ネットワークから画面上への誤った治療指示
− JIS T 0601-1:2012: 14.13
− JIS T 0601-2-16: 201.14.13
情報
定期的保守が実施されていない。
− JIS T 0601-1:2012: 7.9.2.13
予想耐用期間が経過
− JIS T 0601-1:2012: 4.4
表示又はユーザ情報がないか又は誤ってい
る。
− JIS T 0601-1:2012:7.1,7.2,7.4,7.5,7.6,7.9.2
− JIS T 60601-1-8:2012,5.2,6.1,6.2
− IEC 60601-1-10:2007,5.1,5.2
− JIS T 0601-2-16: 201.7.9.2.2
サービス情報がないか又は誤っている。
− JIS T 0601-1:2012: 7.3,7.7,7.9.2.13,7.9.3
− JIS T 0601-2-16: 201.7.9.2.6
操作者応答がないか又は誤っている。(使用ミ
ス)
− JIS T 0601-1:2012: 7.8,7.9.2.8,7.9.2.9,7.9.2.10,
7.9.2.11,7.9.2.14,9.2.3.1,12.1,12.2,12.4.2
− JIS T 60601-1-8:2012,6.1.2,6.3.1,6.3.2.1
− IEC 60601-1-10:2007,6.1,6.2,6.3,6.4
− JIS T 0601-2-16: 201.7.9.2.2,201.7.9.2.6,
201.7.9.2.14,201.7.9.3.1,208.4,208.6.3.1,
208.6.3.3.2,201.12.4.4.110
操作上
警報オーバライド
− JIS T 0601-2-16: 201.12.4.4.106
保護システムの故障
− JIS T 0601-2-16: 201.12.4.4.107
2
T
0
6
0
1
-2
-1
6
:
2
0
1
4
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
56
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
表BB.1−JIS T 14971:2012,附属書Eによるハザード状況リスト(続き)
ハザード
予想される一連の事象
危険状態
危害
参照規格
電気的
絶縁不良
漏れ電流
電気ショック
− JIS T 0601-1:2012:8.5,8.6,8.7,8.8,13.1.3,13.2.2
− JIS T 0601-2-16: 201.8.3,201.8.7.4.7,201.11.6.3
沿面距離及び空間距離の減少
− JIS T 0601-1:2012: 8.9,13.2.6
− JIS T 0601-2-16: 201.13.2.6
沿面距離及び空間距離を減少させる内部又は
外部の液漏れ
− JIS T 0601-1:2012: 8.9
絶縁の急速劣化
− JIS T 0601-1:2012: 11.1,11.6.6
接触可能部分への接触
− JIS T 0601-1:2012: 4.8,4.9,5.9.2,7.9.2.7,8.4,
8.5,8.10,8.11,9.2.2.4
− JIS T 0601-2-16: 201.7.9.2.6,201.8.11.2
装置内への液体の浸入
− JIS T 0601-1:2012: 11.6
− JIS T 0601-2-16: 201.11.6.3
規定された定格電流以外での部品の使用
− JIS T 0601-1:2012: 13.2.3
部品交換
− JIS T 0601-1:2012: 15.2
きょう(筐)体の機械的部品
− JIS T 0601-1:2012: 15.3
トランスの加熱
− JIS T 0601-1:2012: 15.5
給水システムへの排液の接続
− JIS T 0601-1:2012: 15.4.1
給水システムへの原液の接続
− JIS T 0601-1:2012:15.4
患者環境内又は患者環境外のMEシステム
− JIS T 0601-1:2012: 16.1,16.2,16.3,16.4,16.5,
16.6,16.9
− JIS T 0601-2-16: 201.16.2,201.16.6.3
B形装置による心房カテーテルを用いた治療 患者漏れ電流
電気ショック
− JIS T 0601-1:2012: 8.7
− JIS T 0601-2-16: 201.7.9.2.5,201.8.3
他の機器及び電源からの電磁界干渉による正
常動作の混乱
誤った治療
多種の危害
− IEC 60601-1-2:2007
− JIS T 0601-2-16: 202.3.18
他の機器及び電源への電磁界干渉による正常
動作の混乱
患者及び他へ
の多種の危害
− IEC 60601-1-2:2007
化学的
化学物質の漏出
化学薬品への接触
身体への危害
− JIS T 0601-1:2012: 7.9.2.4,11.6.4
高圧液の噴出
− JIS T 0601-1:2012: 9.7
熱的
外部又は内部の高温部品
高温液への接触
身体への危害
− JIS T 0601-1:2012: 11.1,11.6.4,11.6.6
高圧液の噴出
− JIS T 0601-1:2012: 9.7
2
T
0
6
0
1
-2
-1
6
:
2
0
1
4
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
57
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
表BB.1−JIS T 14971:2012,附属書Eによるハザード状況リスト(続き)
ハザード
予想される一連の事象
危険状態
危害
参照規格
機械的
ローラーポンプへの指の挟み込み
押しつぶす,せん(剪)断又は四
肢の破断
打撲,捻挫,切
断又は骨折
− JIS T 0601-1:2012:5.9.2,9.2.2.4.4
動く部分間にある手足
− JIS T 0601-1:2012: 9.2.2.2,16.7
ベース下にある足
斜面上にある機器
− JIS T 0601-1:2012: 9.4
機器の移動
とが(尖)った部分
切断
身体への危害
− JIS T 0601-1:2012: 9.3
可動部の陰になる部分をもつきょう(筐)体
の全体
− JIS T 0601-1:2012: 5.9.2
熱的
規定された定格電流以外での部品の使用
火災
患者及び他へ
の多種の危害
− JIS T 0601-1:2012: 4.8,4.9,13.1.2,13.2.3,13.2.13
液体浸入による短絡電流
− JIS T 0601-1:2012: 11.6
− JIS T 0601-2-16: 201.11.6.3
ヒータの制御不良
− JIS T 0601-1:2012: 13.2.4,13.2.5,13.2.13,15.4.2
冷却装置の故障
− JIS T 0601-1:2012: 13.2.7
モータ用コンデンサの遮断及び短絡
− JIS T 0601-1:2012: 13.2.9
バッテリ不良
− JIS T 0601-1:2012: 15.4.3.1
バッテリ接続における極性の間違い
− JIS T 0601-1:2012: 15.4.3.2
バッテリ過充電
− JIS T 0601-1:2012: 15.4.3.3
バッテリからの過電流
− JIS T 0601-1:2012: 15.4.3.5
トランスの加熱
− JIS T 0601-1:2012: 15.5
2
T
0
6
0
1
-2
-1
6
:
2
0
1
4
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
58
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
参考文献
JIS T 0601-2-16:2008 医用電気機器−第2-16部:人工じん(腎)臓装置の安全に関する個別要求事項
注記 JIS T 0601-2-16:2014によって,取消し及び置換えとなる。
IEC 60601-2-39,Medical electrical equipment−Part 2-39: Particular requirements for basic safety and essential
performance of peritoneal dialysis equipment
ISO 11197,Medical supply units
ISO 13958,Concentrates for haemodialysis and related therapies
EN 1040,Chemical disinfectants and antiseptics−Quantitative suspension test for the evaluation of basic
bactericidal activity of chemical disinfectants and antiseptics−Test method and requirements (phase 1)
EN 1275,Chemical disinfectants and antiseptics−Quantitative suspension test for the evaluation of basic
fungicidal or basic yeasticidal activity of chemical disinfectants and antiseptics−Test method and
requirements (phase 1)
Polaschegg HD, Levin N. Hemodialysis machines and monitors. Winchester, J, Koch, R, Lindsay, R, Ronco, C,
Horl, W, Editors. Replacement of Renal Function by Dialysis, 5th Edition. Kluwer Academic Publishers,
2004, pp. 323-447
GUYTON, AC. Circulatory Shock and Physiology of Its Treatment. Guyton AC, editor, Textbook of Medical
Physiology, Eight Edition. W.B. Saunders Company,1991:pp263-71
59
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
この個別規格で使用される定義の索引
接触可能部分(ACCESSIBLE PART) ··························································· JIS T 0601-1:2012,3.2
附属品(ACCESSORY) ············································································· JIS T 0601-1:2012,3.3
附属文書(ACCOMPANYING DOCUMENT) ················································· JIS T 0601-1:2012,3.4
アラーム状態(ALARM CONDITION) ····················································· JIS T 60601-1-8:2012,3.1
アラーム設定値(ALARM LIMIT) ·························································· JIS T 60601-1-8:2012,3.3
アラーム信号(ALARM SIGNAL) ··························································· JIS T 60601-1-8:2012,3.9
アラームシステム(ALARM SYSTEM) ··················································· JIS T 60601-1-8:2012,3.11
装着部(APPLIED PART) ·········································································· JIS T 0601-1:2012,3.8
動脈圧(ARTERIAL PRESSURE) ·················································································· 201.3.201
アラーム音中断(AUDIO PAUSED) ······················································· JIS T 60601-1-8:2012,3.13
基礎安全(BASIC SAFETY) ····································································· JIS T 0601-1:2012,3.10
漏血(BLOOD LEAK) ································································································ 201.3.202
セントラル透析液送液システム(CENTRAL DIALYSIS FLUID DELIVERY SYSTEM) ·············· 201.3.203
クラスI(CLASS I) ················································································ JIS T 0601-1:2012,3.13
沿面距離(CREEPAGE DISTANCE) ···························································· JIS T 0601-1:2012,3.19
ダイアライザ(DIALYSER) ························································································· 201.3.204
透析液(DIALYSIS FLUID) ························································································· 201.3.205
透析液原液(DIALYSIS FLUID CONCENTRATE) ····························································· 201.3.206
接地漏れ電流(EARTH LEAKAGE CURRENT) ············································· JIS T 0601-1:2012,3.25
基本性能(ESSENTIAL PERFORMANCE)···················································· JIS T 0601-1:2012,3.27
体外循環回路(EXTRACORPOREAL CIRCUIT) ······························································· 201.3.207
ハザード(HAZARD) ·············································································· JIS T 0601-1:2012,3.39
危険状態(HAZARDOUS SITUATION) ······················································· JIS T 0601-1:2012,3.40
血液透析ろ過,HDF[HAEMODIAFILTRATION(HDF)] ·················································· 201.3.208
血液透析,HD[HAEMODIALYSIS(HD)] ····································································· 201.3.209
血液透析装置(HAEMODIALYSIS EQUIPMENT) ····························································· 201.3.210
血液ろ過,HF[HAEMOFILTRATION(HF)] ·································································· 201.3.211
高優先度(HIGH PRIORITY) ································································ JIS T 60601-1-8:2012,3.22
情報信号(INFORMATION SIGNAL) ······················································ JIS T 60601-1-8:2012,3.23
ダイアライザ血液入口圧(INLET PRESSURE AT BLOOD SIDE OF THE DIALYSER) ··············· 201.3.220
意図する使用(INTENDED USE) ······························································· JIS T 0601-1:2012,3.44
内部電源(INTERNAL ELECTRICAL POWER SOURCE) ································· JIS T 0601-1:2012,3.45
漏れ電流(LEAKAGE CURRENT) ····························································· JIS T 0601-1:2012,3.47
生命維持用医用電気機器又は医用電気システム
(LIFE-SUPPORTING ME EQUIPMENT or ME SYSTEM) ························· IEC 60601-1-2:2007,3.18
低優先度(LOW PRIORITY) ································································· JIS T 60601-1-8:2012,3.27
電源プラグ(MAINS PLUG) ····································································· JIS T 0601-1:2012,3.50
60
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
製造販売業者(製造業者)[MANUFACTURER] ··········································· JIS T 0601-1:2012,3.55
機械的ハザード(MECHANICAL HAZARD) ················································ JIS T 0601-1:2012,3.61
医用電気機器(ME機器)
[MEDICAL ELECTRICAL EQUIPMENT (ME EQUIPMENT)] ······················ JIS T 0601-1:2012,3.63
医用電気システム(MEシステム)
[MEDICAL ELECTRICAL SYSTEM (ME SYSTEM)] ································· JIS T 0601-1:2012,3.64
中優先度(MEDIUM PRIORITY) ··························································· JIS T 60601-1-8:2012,3.28
マルチタップ(MULTIPLE SOCKET-OUTLET) ············································· JIS T 0601-1:2012,3.67
正味の体液除去(除水)(NET FLUID REMOVAL) ··························································· 201.3.212
ネットワーク・データ結合(NETWORK/DATA COUPLING) ··························· JIS T 0601-1:2012,3.68
正常状態(NORMAL CONDITION) ···························································· JIS T 0601-1:2012,3.70
オンラインHDF(ONLINE HDF) ················································································· 201.3.213
オンラインHF(ONLINE HF)······················································································ 201.3.214
操作者(OPERATOR) ·············································································· JIS T 0601-1:2012,3.73
患者(PATIENT) ···················································································· JIS T 0601-1:2012,3.76
患者接続部(PATIENT CONNECTION) ······················································· JIS T 0601-1:2012,3.78
患者環境(PATIENT ENVIRONMENT) ························································ JIS T 0601-1:2012,3.79
患者漏れ電流(PATIENT LEAKAGE CURRENT) ··········································· JIS T 0601-1:2012,3.80
生理的閉ループ制御器(PHYSIOLOGIC CLOSED-LOOP CONTROLLER) ······· IEC 60601-1-10:2007,3.20
生体アラーム状態(PHYSIOLOGICAL ALARM CONDITION) ······················ JIS T 60601-1-8:2012,3.31
等電位化導線(POTENTIAL EQUALIZATION CONDUCTOR) ·························· JIS T 0601-1:2012,3.86
プロセス(PROCESS) ············································································· JIS T 0601-1:2012,3.89
プログラマブル電気医用システム(PEMS)
[PROGRAMMABLE ELECTRICAL MEDICAL SYSTEM (PEMS)] ················ JIS T 0601-1:2012,3.90
保護接地線(PROTECTIVE EARTH CONDUCTOR) ······································· JIS T 0601-1:2012,3.93
保護接地接続(PROTECTIVE EARTH CONNECTION) ··································· JIS T 0601-1:2012,3.94
保護接地する(した)(PROTECTIVELY EARTHED) ····································· JIS T 0601-1:2012,3.96
保護システム(PROTECTIVE SYSTEM) ········································································ 201.3.215
責任部門(RESPONSIBLE ORGANIZATION) ············································· JIS T 0601-1:2012,3.101
リスク(RISK) ···················································································· JIS T 0601-1:2012,3.102
リスク分析(RISK ANALYSIS) ······························································· JIS T 0601-1:2012,3.103
リスクマネジメント(RISK MANAGEMENT) ············································ JIS T 0601-1:2012,3.107
リスクマネジメントファイル(RISK MANAGEMENT FILE) ························· JIS T 0601-1:2012,3.108
単一故障状態(SINGLE FAULT CONDITION) ············································ JIS T 0601-1:2012,3.116
単一故障安全(SINGLE FAULT SAFE) ······················································ JIS T 0601-1:2012,3.117
補充液(SUBSTITUTION FLUID) ················································································· 201.3.216
電源(商用)(SUPPLY MAINS) ······························································· JIS T 0601-1:2012,3.120
工具(TOOL) ······················································································ JIS T 0601-1:2012,3.127
接触電流(TOUCH CURRENT) ······························································· JIS T 0601-1:2012,3.129
膜間圧力差,TMP[TRANSMEMBRANE PRESSURE(TMP)] ··········································· 201.3.217
61
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
B形装着部(TYPE B APPLIED PART) ······················································ JIS T 0601-1:2012,3.132
CF形装着部(TYPE CF APPLIED PART) ··················································· JIS T 0601-1:2012,3.134
限外ろ過(ULTRAFILTRATION) ·················································································· 201.3.218
使用ミス(USE ERROR) ············································································ IEC 62366:2007,3.21
静脈圧(VENOUS PRESSURE) ···················································································· 201.3.219
62
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書JA
(参考)
JISと対応国際規格との対比表
JIS T 0601-2-16:2014 医用電気機器−第2-16部:人工腎臓装置の基礎安全及び
基本性能に関する個別要求事項
IEC 60601-2-16:2012 Medical electrical equipment−Part 2-16: Particular requirements
for the basic safety and essential performance of haemodialysis, haemodiafiltration and
haemofiltration equipment
(I)JISの規定
(II)
国際
規格
番号
(III)国際規格の規定
(IV)JISと国際規格との技術的差異の箇条ごとの
評価及びその内容
(V)JISと国際規格との技
術的差異の理由及び今後の
対策
箇条番号
及び題名
内容
箇条番号
内容
箇条ごと
の評価
技術的差異の内容
201.1 適用範
囲,目的及び
関連規格
201.1.1
201.1.2
201.1.1
201.1.2
血液透析装置
変更
人工腎臓装置を適用範囲とした。呼称
は,JMDNにおける一般的名称に準じ
た。
技術的差異はない。
我が国の透析医療の実情を
反映させた。
201.3 用語及
び定義
201.3.78
201.3.203
201.3.204
201.3.78
201.3.203
201.3.204
血液透析装置
変更
JIS T 3250又はJMDNにおける一般的
名称に準じ,追加又は変更した。
規格を理解しやすくするた
めに追加又は変更した。
なお,用語であるので実質
的な差異はない。
201.3.204.1〜
201.3.204.3
−
−
追加
201.3.210
201.3.210
血液透析装置
変更
人工腎臓装置を適用範囲とした。呼称
は,JMDNにおける一般的名称に準じ
た。
我が国の透析医療の実情を
反映させた。
201.3.210.1〜
201.3.210.6
−
−
追加
JMDNにおける一般的名称に準じ,追
加又は変更した。
我が国の透析医療の実情を
反映させた。
201.3.213
201.3.214
201.3.213
201.3.214
血液透析装置
変更
201.3.215
201.3.215
ハザード
変更
対応国際規格では,“ハザードに対す
る保護”であるが誤りであるので“危
険状態”に修正した。
技術的差異はない。
国際規格の次回改正時,提
案を検討する。
201.3.216
201.3.216
−
追加
我が国の使用している用語を追加し
た。
規格を理解しやすくするた
めに追加した。
なお,用語であるので実質
的な差異はない。
201.3.220
−
−
追加
2
T
0
6
0
1
-2
-1
6
:
2
0
1
4
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
63
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
(I)JISの規定
(II)
国際
規格
番号
(III)国際規格の規定
(IV)JISと国際規格との技術的差異の箇条ごとの
評価及びその内容
(V)JISと国際規格との技
術的差異の理由及び今後の
対策
箇条番号
及び題名
内容
箇条番号
内容
箇条ごと
の評価
技術的差異の内容
201.4 一般要
求事項
201.4.3.101〜
201.4.3.106
201.4.3.108
201.4.3.109
201.4.7
201.4.3.101〜
201.4.3.106
201.4.3.108
201.4.3.109
201.4.7
血液透析装置
変更
細分箇条ごとに人工腎臓装置,個人用
透析装置,多人数用透析液供給装置,
透析用監視装置,血液透析ろ過用装
置,血液ろ過用装置及び/又は多用途
透析装置を適用範囲とした。呼称は,
JMDNにおける一般的名称に準じた。
技術的差異はない。
我が国の透析医療の実情を
反映させた。
201.7 ME機器
の標識,表示
及び文書
201.7.4.3
201.7.4.3
mmHgの使用可能箇所
は,あらゆる部分の圧
力測定。
変更
mmHgの使用可能箇所を生体に関す
るあらゆる部分の圧力測定とした。
mmHg使用可能箇所を計量
法で認められている箇所に
限定した。
201.7.9.2.2
201.7.9.2.5
201.7.9.2.6
201.7.9.2.12
201.7.9.2.14
201.7.9.3.1
201.7.9.2.2
201.7.9.2.5
201.7.9.2.6
201.7.9.2.12
201.7.9.2.14
201.7.9.3.1
血液透析装置
変更
細分箇条ごとに人工腎臓装置,個人用
透析装置,多人数用透析液供給装置,
透析用監視装置,血液透析ろ過用装
置,血液ろ過用装置及び/又は多用途
透析装置を適用範囲とした。呼称は,
JMDNにおける一般的名称に準じた。
技術的差異はない。
我が国の透析医療の実情を
反映させた。
201.8 ME機器
の電気的ハザ
ードに関する
保護
201.8.3
201.8.7.4.7
201.8.11.2
201.8.3
201.8.7.4.7
201.8.11.2
血液透析装置
変更
細分箇条ごとに人工腎臓装置,個人用
透析装置,透析用監視装置,血液透析
ろ過用装置,血液ろ過用装置及び/又
は多用途透析装置を適用範囲とした。
呼称は,JMDNにおける一般的名称に
準じた。
技術的差異はない。
我が国の透析医療の実情を
反映させた。
201.8.11.2
201.8.11.2
−
追加
要求内容の具体例を注記として追加
した。
技術的差異はない。
国際規格の次回改正時,提
案を検討する。
201.11 過度
の温度及び他
のハザードに
関する保護
201.11.6.6
201.11.8
201.11.6.6
201.11.8
血液透析装置
変更
細分箇条ごとに人工腎臓装置,個人用
透析装置,透析用監視装置,血液透析
ろ過用装置,血液ろ過用装置及び/又
は多用途透析装置を適用範囲とした。
呼称は,JMDNにおける一般的名称に
準じた。
技術的差異はない。
我が国の透析医療の実情を
反映させた。
2
T
0
6
0
1
-2
-1
6
:
2
0
1
4
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
64
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
(I)JISの規定
(II)
国際
規格
番号
(III)国際規格の規定
(IV)JISと国際規格との技術的差異の箇条ごとの
評価及びその内容
(V)JISと国際規格との技
術的差異の理由及び今後の
対策
箇条番号
及び題名
内容
箇条番号
内容
箇条ごと
の評価
技術的差異の内容
201.12 制御
及び計器の精
度並びに危険
な出力に対す
る保護
201.12.4.4
201.12.4.4.101〜
201.12.4.4.103
201.12.4.4.104.1〜
201.12.4.4.104.3
201.12.4.4.105〜
201.12.4.4.108
201.12.4.4.111
201.12.4.4
201.12.4.4.101〜
201.12.4.4.103
201.12.4.4.104.1〜
201.12.4.4.104.3
201.12.4.4.105〜
201.12.4.4.108
201.12.4.4.111
血液透析装置
変更
細分箇条ごとに人工腎臓装置,個人用
透析装置,多人数用透析液供給装置,
透析用監視装置,血液透析ろ過用装
置,血液ろ過用装置及び/又は多用途
透析装置を適用範囲とした。呼称は,
JMDNにおける一般的名称に準じた。
技術的差異はない。
我が国の透析医療の実情を
反映させた。
201.12.4.4.102
201.12.4.4.103
201.12.4.4.102
201.12.4.4.103
JISと同じ
変更
試験方法を分かりやすい表現にした。 技術的差異はない。
201.13 危険
状態及び故障
状態
201.13.2.6
201.13.2.6
血液透析装置
変更
人工腎臓装置を適用範囲とした。呼称
は,JMDNにおける一般的名称に準じ
た。
技術的差異はない。
我が国の透析医療の実情を
反映させた。
201.14 プロ
グラマブル電
気医用システ
ム(PEMS)
201.14.13
201.14.13
血液透析装置
変更
人工腎臓装置を適用範囲とした。呼称
は,JMDNにおける一般的名称に準じ
た。
技術的差異はない。
我が国の透析医療の実情を
反映させた。
201.15 ME機
器の構造
201.15.4.1.101
201.15.4.1.101
血液透析装置
変更
個人用透析装置,血液透析ろ過用装
置,血液ろ過用装置及び多用途透析装
置を適用範囲とした。呼称は,JMDN
における一般的名称に準じた。
技術的差異はない。
我が国の透析医療の実情を
反映させた。
201.16 MEシ
ステム
201.16.1
201.16.2
201.16.1
201.16.2
血液透析装置
変更
人工腎臓装置を適用範囲とした。呼称
は,JMDNにおける一般的名称に準じ
た。
技術的差異はない。
我が国の透析医療の実情を
反映させた。
201.16.9.1
201.16.9.1
色識別された透析液原
液容器又はセントラル
送液システム
変更
透析液原液容器を適用範囲とした。
我が国の透析医療の実情を
反映させた。
202 電磁両立
性−要求事項
及び試験
202.3.18
202.3.18
血液透析装置
変更
人工腎臓装置を適用範囲とした。呼称
は,JMDNにおける一般的名称に準じ
た。
技術的差異はない。
我が国の透析医療の実情を
反映させた。
2
T
0
6
0
1
-2
-1
6
:
2
0
1
4
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
65
T 0601-2-16:2014
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
(I)JISの規定
(II)
国際
規格
番号
(III)国際規格の規定
(IV)JISと国際規格との技術的差異の箇条ごとの
評価及びその内容
(V)JISと国際規格との技
術的差異の理由及び今後の
対策
箇条番号
及び題名
内容
箇条番号
内容
箇条ごと
の評価
技術的差異の内容
208 医用電気
機器及び医用
電気システム
のアラームシ
ステムに関す
る一般要求事
項,試験方法
及び適用指針
208.4
208.5.2.1
208.6.3.3.2
208.6.3.3.101
208.4
208.6.3.3.2
208.6.3.3.101
血液透析装置
変更
細分箇条ごとに人工腎臓装置,個人用
透析装置,透析用監視装置,血液透析
ろ過用装置,血液ろ過用装置及び/又
は多用途透析装置を適用範囲とした。
呼称は,JMDNにおける一般的名称に
準じた。
技術的差異はない。
我が国の透析医療の実情を
反映させた。
附属書AA
(参考)
附属書BB
(参考)
JISと国際規格との対応の程度の全体評価:IEC 60601-2-16:2012,MOD
関連する法規
薬事法
注記1 箇条ごとの評価欄の用語の意味は,次による。
− 追加 ················ 国際規格にない規定項目又は規定内容を追加している。
− 変更 ················ 国際規格の規定内容を変更している。
注記2 JISと国際規格との対応の程度の全体評価欄の記号の意味は,次による。
− MOD ··············· 国際規格を修正している。
2
T
0
6
0
1
-2
-1
6
:
2
0
1
4
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。