T 0404:2019
(1)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
目 次
ページ
1 適用範囲························································································································· 1
2 用語及び定義 ··················································································································· 1
3 試験回路························································································································· 2
3.1 試験回路の構成 ············································································································· 2
3.2 試験回路に用いる器材及びその役割··················································································· 2
3.3 試験回路に設置する装置 ································································································· 3
3.4 その他の装置及び器具 ···································································································· 3
3.5 試験回路の確認 ············································································································· 3
4 血液調製························································································································· 3
5 試料······························································································································· 3
5.1 試験試料 ······················································································································ 3
5.2 対照試料 ······················································································································ 3
6 試験手順························································································································· 4
7 試験報告書 ······················································································································ 4
附属書A(参考)試験回路の情報 ···························································································· 6
参考文献 ····························································································································· 7
T 0404:2019
(2)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
まえがき
この規格は,工業標準化法第12条第1項の規定に基づき,一般社団法人日本医療機器テクノロジー協会
(MTJAPAN)及び一般財団法人日本規格協会(JSA)から,工業標準原案を具して日本工業規格を制定す
べきとの申出があり,日本工業標準調査会の審議を経て,厚生労働大臣が制定した日本工業規格である。
この規格は,著作権法で保護対象となっている著作物である。
この規格に従うことは,次の者の有する特許権等の使用に該当するおそれがあるので,留意する。
− 学校法人早稲田大学
住所:東京都新宿区戸塚町1丁目104
− 特開2016-123711 2016年7月11日 血液浄化器の循環試験装置及び試験評価方法
上記の,特許権等の権利者は,非差別的かつ合理的な条件でいかなる者に対しても当該特許権等の実施
の許諾等をする意思のあることを表明している。ただし,この規格に関連する他の特許権等の権利者に対
しては,同様の条件でその実施が許諾されることを条件としている。
この規格に従うことが,必ずしも,特許権の無償公開を意味するものではないことに注意する必要があ
る。
この規格の一部が,上記に示す以外の特許権等に抵触する可能性がある。厚生労働大臣及び日本工業標
準調査会は,このような特許権等に関わる確認について,責任はもたない。
なお,ここで“特許権等”とは,特許権,出願公開後の特許出願又は実用新案権をいう。
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
日本工業規格 JIS
T 0404:2019
持続的血液ろ(濾)過器のインビトロ(in vitro)
血栓性試験方法
Method for in vitro thrombogenicity testing for continuous haemofilters
1
適用範囲
この規格は,持続的血液ろ(濾)過器の血栓性を,インビトロ(in vitro)で試験する方法について規定
する。この規格は,使用環境を模擬した血液循環回路を使用して,第一に血液接触後のろ過器入口圧の測
定による回路循環時間(ライフタイム)の評価,及び第二にろ過器への血栓の付着状態を評価するための
試験方法を規定する。
2
用語及び定義
この規格で用いる主な用語及び定義は,次による。
2.1
持続的血液ろ過(continuous haemofiltration)
体外に取り出した血液を血液ろ過器に通過させて,持続的にろ過を行う治療法。主に循環動態の不安定
な症例に対する腎機能代替療法の一つとして施行される。
2.2
血液ろ過器(haemofilters)
半透膜素材でできた中空糸束等を内蔵した血液処理を行う医療機器。中空糸を介して血液から余分な水,
毒素,老廃物をろ過(除去)するために使用する医療機器。
2.3
血液ポンプ(blood pump)
血液ろ過器に血液を送り,試験回路内を循環させるポンプ。
2.4
ろ過ポンプ(filtration pump)
血液ろ過器を通過する血液から中空糸束等を介してろ液を抽出する,血液ろ過器のろ液ポートに接続さ
れたチューブに設置されたポンプ。
2.5
付着血栓(adhered thrombus)
試験後に試験回路を生理食塩液又はりん酸緩衝生理食塩液で洗浄し,試験試料壁に残った血栓。
2.6
回路循環時間(ライフタイム)(lifetime)
あらかじめ設定したろ過器入口圧に上昇するまでの時間。
2
T 0404:2019
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
3
試験回路
3.1
試験回路の構成
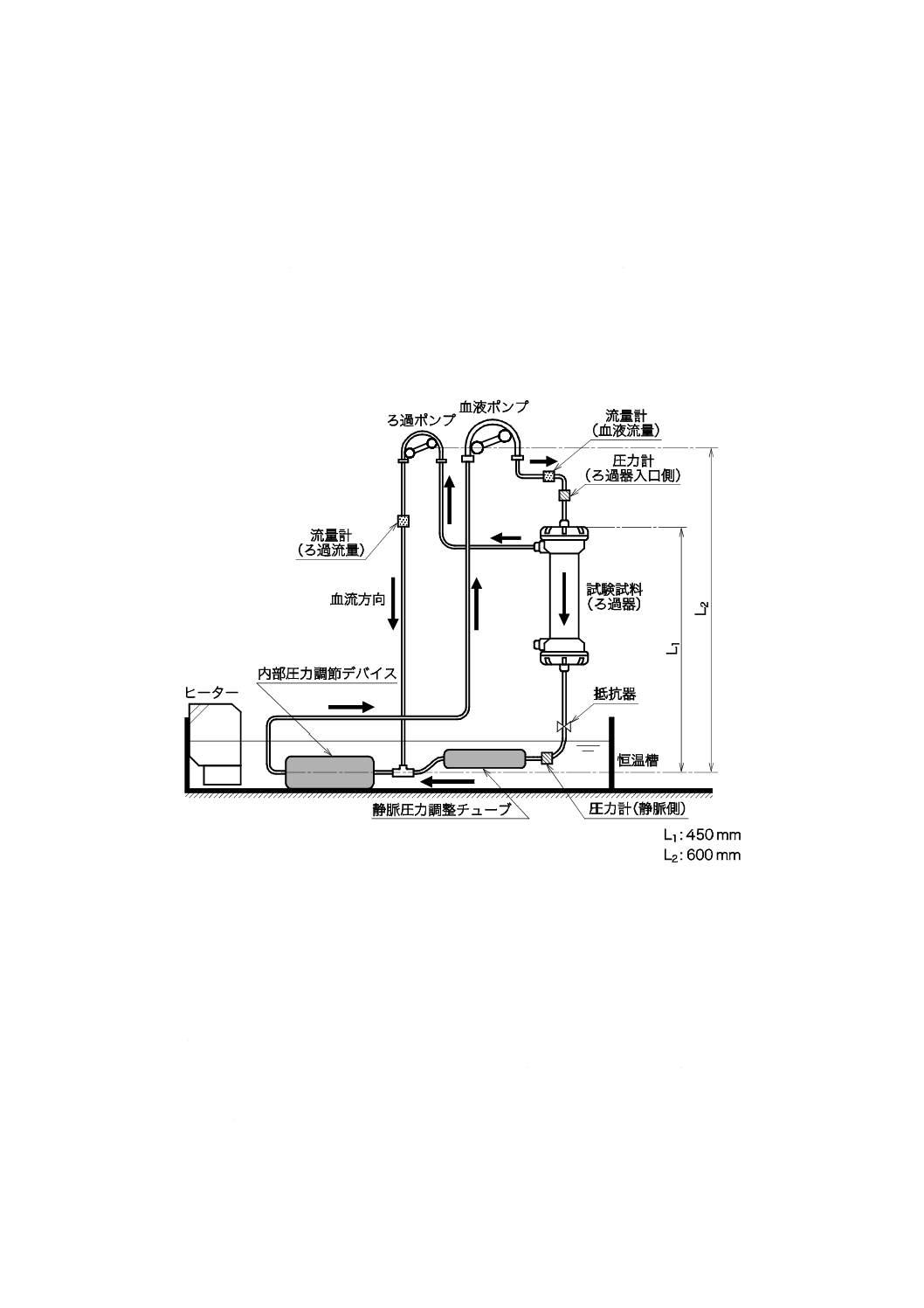
試験対象となる血液ろ過器(試験試料),ろ過器に血液を送る血液ポンプ,血液をろ過しろ液を送るろ過
ポンプ,静脈圧力調整チューブ(リザーバ)及び内部圧力調節デバイスで構成する。ろ過器の血液流量及
びろ過流量を計測する流量計並びにろ過器の入口圧及び静脈圧を計測する圧力計を設置する。試験開始時
のろ過器入口圧を設定値に合わせるための抵抗器をろ過器出口部のチューブに設置する。試験中に血液を
サンプリングしない場合には,必ずしも内部圧力調節デバイスを使用する必要はない。図1に試験回路及
び試験回路に設置する装置の一例を示す。試験実施時に,恒温槽内に試験回路の一部を設置し,37±2 ℃
で試験を行う。
図1−試験回路及び試験回路に設置する装置の一例
3.2
試験回路に用いる器材及びその役割
試験回路に用いる器材及びその役割は,次による。試験試料を除く試験回路に血栓が生じないように,
必要に応じて次の器材の血液接触面を抗凝固処理する。
a) 持続的血液ろ過器 市販又は試験試料の取扱説明書などで規定される持続的血液ろ過器を使用する。
b) チューブ 血液回路に用いるチューブを使用する。
c) 静脈圧力調整チューブ(リザーバ) 静脈圧力を目標値に合わせるとともに,一定量の血液を貯留する
ために使用する。
d) 内部圧力調節デバイス 採血時に試験回路の圧力を調節するために,弾性チューブを設置する(附属
書A参照)。
3
T 0404:2019
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
注記 セグメント化ポリウレタン,シリコーンのチューブなどを使用することができる。
e) 抵抗器 血液ろ過器の入口圧力を調節するため,血液ろ過器の出口側に抵抗器を設ける。
3.3
試験回路に設置する装置
試験回路に設置する主な装置及びその機能は,次による。
a) 血液ポンプ 血液ろ過器に血液を送出し試験回路内を循環させることができるもの。
b) ろ過ポンプ 血液ろ過器の中空糸膜を介して血液をろ過し,ろ液を送り出すことができるもの。
3.4
その他の装置及び器具
試験回路に設置するその他の装置,器具及びその機能は,次による。
a) 流量計 超音波血流計若しくは電磁流量計,又はこれと同等の精度をもつ流量計を用いる。
b) 圧力計 圧力トランスデューサなどを用いる。
c) 恒温槽 37±2 ℃で血液を保温できるもの。
3.5
試験回路の確認
試験に使用する回路は,試験実施前に生理食塩液などを使用し,次によって確認する。
a) 試験回路の各接合部から漏れがない。
b) 試験回路の容量
c) 血液ポンプで通液させたとき,血液ポンプ・ろ過ポンプの回転数及び抵抗器を操作して,計画した平
均血液流量及び平均ろ過流量,並びに目標のろ過器入口圧及び静脈圧の条件を設定できるもの。
4
血液調製
試験に使用する血液の調製は,次による。
a) ヘパリンなどを添加した血液を使用し,活性化全血凝固時間(Activated clotting time, ACT)を所望の
設定値(例 150〜180秒)に調整する。その他の抗凝固剤の使用が規定されている血液ろ過器につい
ては,当該抗凝固剤を使用して試験を行う。
b) 試験試料及び対照試料の試験回路に必要な血液量を同一個体から採取する。
注記 試験に必要な血液量を得るために,ブタなどの大型動物の血液を使用することが望ましい。
c) 採血開始から試験に使用するまで空気接触を極力避け,可能な限り採血開始から4時間以内までを目
安に試験に使用する。4時間を超える場合には,採血後の試験に供されるまでの経過時間が試験結果
に及ぼす影響を十分に検討する必要がある。
5
試料
5.1
試験試料
最終製品又は設計管理された血液ろ過器の機能をもつ試験試料を使用する。
5.2
対照試料
対照試料を設定する。同一個体から採取した血液を使用して,試験試料との比較試験を行う。対照試料
を使用した回路についても,3.5を確認する。試験回路は試験試料(対照試料)を除き同じ構成にすること
が望ましい。
注記 一般的には,血栓形成リスクが低い既知の対照試料を設定し,この結果と比較することで,試
験試料使用時の血栓症のリスクを評価する。
4
T 0404:2019
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
6
試験手順
試験手順は,次による。
a) 試験回路を取扱説明書などで規定する方法に従って生理食塩液などで洗浄・充塡(プライミング)す
る。
b) 箇条4で規定した血液で試験回路内を充塡する。
注記1 試験回路内に空気(気泡)が残らないよう注意する。
c) 3.1で規定した試験回路を恒温槽(37±2 ℃)に設置する。
d) 血液ポンプ及びろ過ポンプを稼働させて計画した平均血液流量及び平均ろ過流量に調整し,血液循環
を開始する。
注記2 試験における一般的な平均血液流量,平均ろ過流量,血液循環開始時のろ過器入口圧及び
静脈圧の目標値を表1に示す。
表1−一般的な試験条件の例
平均血液流量
平均ろ過流量
ろ過器入口圧
(目標値)
静脈圧(目標値)
100 ml/min
10 ml/min
70 mmHg(9.3 kPa)
7 mmHg(0.93 kPa)
[脈圧3 mmHg(0.40 kPa)以下]
e) ろ過器入口圧を目標値に設定して,ろ過器入口圧を経時的に記録し,試験前に設定したろ過器入口圧
に到達するまでの時間を回路循環時間(ライフタイム)とする。
f)
試験回路内を一定量の生理食塩液又はりん酸緩衝生理食塩液で洗浄後,ろ過器の流入部,流出部及び
中空糸束に残った血栓の有無の観察を行い,写真を撮影する。
g) 必要に応じてろ過器の血液流入部から流出部に向けて,上,中,下(又は,上,下)に分割された部
分から中空糸を採取し,走査電子顕微鏡による観察を行い,写真を撮影する。
h) 試験前後の血液の血算(赤血球数,白血球数,血小板数,ヘマトクリット値),総タンパク値及び血し
ょう(漿)遊離ヘモグロビン量を記録する。
7
試験報告書
7.1
試験報告書には,次の事項を記載する。
a) ろ過器入口圧の経時変化
b) 回路循環時間(ライフタイム)
c) ろ過器に形成された血栓の写真
例
状態
凝集塊等の分布
付着部位
血液流入部,血液流出部,ろ過器の中空糸束の上中下部位
d) 中空糸内の付着血栓の走査電子顕微鏡による写真観察結果(付着状態,付着部位など)
例
状態
中空糸内の血栓の付着の有無,付着血栓の多少,付着血栓の様子
付着部位
血液流入口付近,血液流入口と流出口との中間付近,血液流出口付近
5
T 0404:2019
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
7.2
試験報告書には,次の試験条件についても,記載する。
a) 試験を実施した機関の名称,住所,試験責任者の氏名,試験開始日及び試験終了日
b) 試験試料及び対照試料を特定する要素(名称,製造業者名,製造番号,原材料名など)
c) 試験回路の構成(回路図,各装置を特定する要素)及び試験回路の容量
d) 使用した血液(動物種,採血量,使用した抗凝固剤及び量,ACT,採血してから血液循環開始までの
時間,試験前後の血小板数,試験前後の血しょう遊離ヘモグロビン量など)
e) 使用したACTの測定装置
f)
血液循環前に行う洗浄・充塡(プライミング)の方法
g) 血液循環条件(平均血液流量,平均ろ過流量及び血液循環開始時のろ過器入口圧・静脈圧)
h) 試験後の血液ろ過器の洗浄時及びグルタールアルデヒド溶液で固定処理時の循環方法
i)
血栓の観察方法(外観観察,走査電子顕微鏡観察など)
6
T 0404:2019
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書A
(参考)
試験回路の情報
A.1 内部圧力調節デバイスの機能
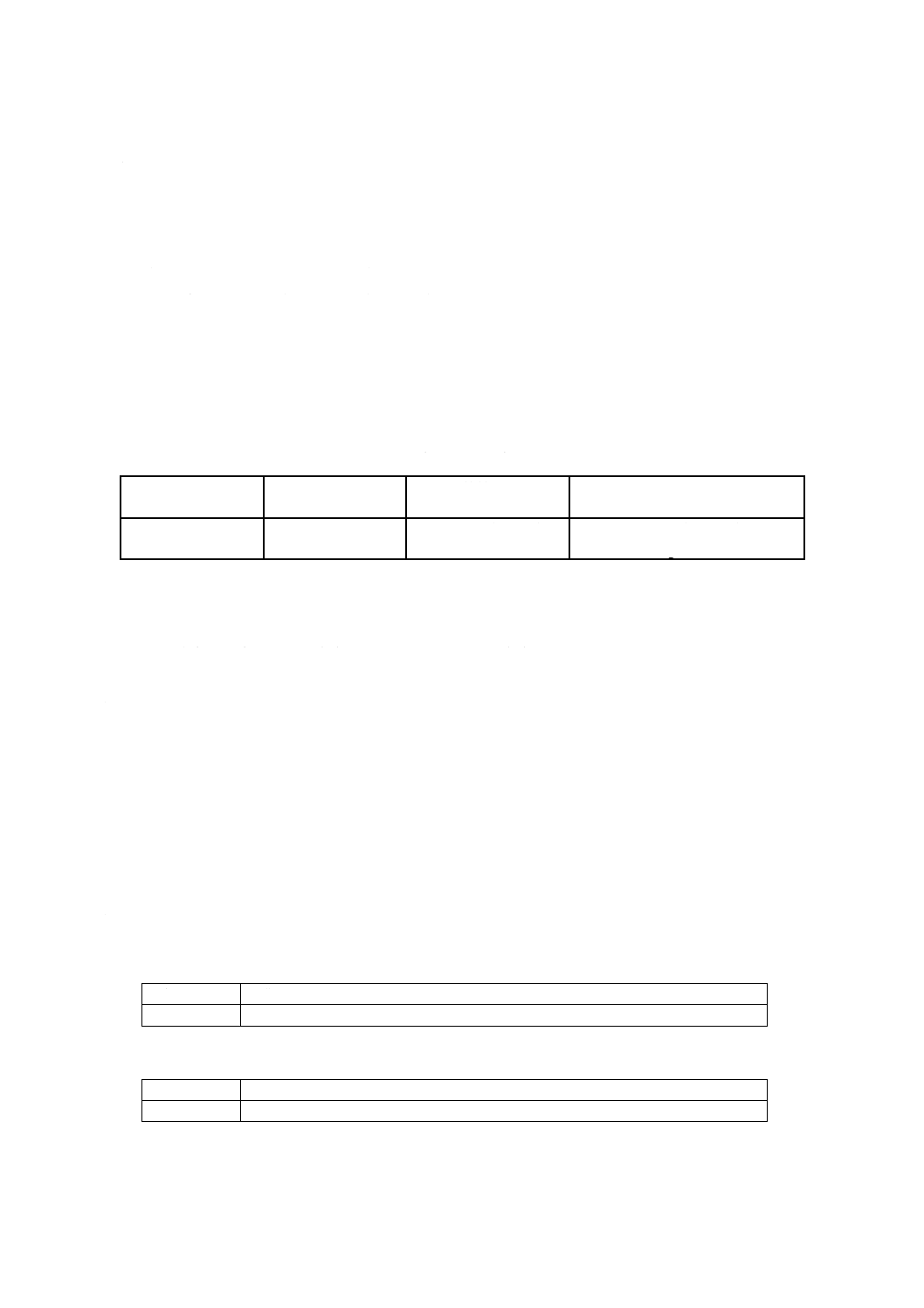
循環血液を採血する際に,閉鎖系の回路内の圧力は減少する。採血する血液と同量の非圧縮性溶液を循
環回路の内部圧力調節デバイスの弾性チューブ外側に入れ,循環血液の圧力を採血前と同様にする。
A.2 内部圧力調節デバイスの材質及び形状
内部圧力調節デバイスの材質及び形状は,次による。また,形状例を図A.1に示す。
− 材質 セグメント化ポリウレタン
− 直径 12 mm
− 長さ 250 mm
− 形状 円筒チューブ状
図A.1−内部圧力調節デバイスの形状例
7
T 0404:2019
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
参考文献
[1] JIS T 3250 血液透析器,血液透析ろ(濾)過器,血液ろ(濾)過器及び血液濃縮器
[2] ISO 10993-4,Biological evaluation of medical devices−Part 4: Selection of tests for interactions with blood
[3] 平田麻由紀,岩﨑清隆,松橋祐輝,高橋東,永井美玲,梅津光生,持続緩徐式血液濾過器の抗血栓性
評価項目の提案,第27回バイオエンジニアリング講演会,第27回バイオエンジニアリング講演会講
演論文集,pp.141-142,新潟,2015年1月9日


