K 6955:2017
(1)
目 次
ページ
序文 ··································································································································· 1
1 適用範囲························································································································· 1
2 引用規格························································································································· 2
3 用語及び定義 ··················································································································· 2
4 原理······························································································································· 4
5 試験環境························································································································· 4
6 試薬······························································································································· 4
7 装置······························································································································· 4
8 操作······························································································································· 5
8.1 試験材料の調製 ············································································································· 5
8.2 対照材料の調製 ············································································································· 5
8.3 試験土壌の調製 ············································································································· 6
8.4 試験の準備及び実施 ······································································································· 7
9 計算及び結果の表示 ·········································································································· 9
9.1 計算 ···························································································································· 9
9.2 結果の表示及び解釈 ······································································································ 10
10 結果の正当性 ················································································································ 10
11 試験報告 ······················································································································ 10
附属書A(参考)圧力測定型閉鎖呼吸計の原理 ········································································· 12
附属書B(参考)発生した二酸化炭素の量を測定する装置の例 ····················································· 13
附属書C(参考)発生した二酸化炭素の量を求める方法の例························································ 14
附属書D(参考)理論的酸素要求量(ThOD) ·········································································· 16
附属書E(参考)生分解性試験の終わりに,水に不溶性のプラスチック材料の残存量及びその分子量を測
定する例 ······················································································································ 17
附属書F(参考)長期試験の例 ······························································································· 18
附属書G(参考)ラウンドロビン試験 ····················································································· 21
附属書JA(参考)JISと対応国際規格との対比表 ······································································ 26
K 6955:2017
(2)
まえがき
この規格は,工業標準化法第14条によって準用する第12条第1項の規定に基づき,日本プラスチック
工業連盟(JPIF),日本バイオプラスチック協会(JBPA),国立研究開発法人産業技術総合研究所(AIST)
及び一般財団法人日本規格協会(JSA)から,工業標準原案を具して日本工業規格を改正すべきとの申出
があり,日本工業標準調査会の審議を経て,経済産業大臣が改正した日本工業規格である。これによって,
JIS K 6955:2006は改正され,この規格に置き換えられた。
この規格は,著作権法で保護対象となっている著作物である。
この規格の一部が,特許権,出願公開後の特許出願又は実用新案権に抵触する可能性があることに注意
を喚起する。経済産業大臣及び日本工業標準調査会は,このような特許権,出願公開後の特許出願及び実
用新案権に関わる確認について,責任はもたない。
日本工業規格 JIS
K 6955:2017
プラスチック−呼吸計を用いた酸素消費量又は
発生した二酸化炭素量の測定による土壌中での
プラスチックの好気的究極生分解度の求め方
Plastics-Determination of the ultimate aerobic biodegradability of plastic
materials in soil by measuring the oxygen demand in a respirometer or the
amount of carbon dioxide evolved
序文
この規格は,2012年に第2版として発行されたISO 17556:2012を基とし,技術的内容を変更して作成し
た日本工業規格である。
なお,この規格で点線の下線を施してある箇所は,対応国際規格を変更している事項である。変更の一
覧表にその説明を付けて,附属書JAに示す。
1
適用範囲
この規格は,閉鎖呼吸計を用いた酸素の消費量又は発生した二酸化炭素量の測定によって,プラスチッ
ク材料の土壌中での好気的究極生分解度を求める方法について規定する。この方法は,至適な生分解度を
得るため,土壌の水分量を調整するのがよい。
植種源として非じゅん(馴)化土壌を用いる場合には,この試験は,自然環境下での土壌中の生分解過
程を模擬し,混合又は予暴露土壌を用いる場合は,試験材料の潜在的な生分解性の可能性を検討する方法
である。
この方法が適用される物質は,次による。
− 天然及び/又は合成ポリマー,共重合体,又はこれらの混合物
− 可塑剤,着色剤のような添加物を含むプラスチック材料
− 水溶性ポリマー
試験条件下で,土壌中に存在する微生物の活性に阻害的な材料には必ずしも適用できるわけではない。
阻害性効果は,阻害対照を使用するか又は他の適切な方法(例えば,ISO 8192参照)によって決定できる。
試験材料が,土壌中の微生物に阻害的である場合は,低い試験材料濃度,別の土壌,又は予暴露土壌を用
いることができる。
注記 この規格の対応国際規格及びその対応の程度を表す記号を,次に示す。
ISO 17556:2012,Plastics−Determination of the ultimate aerobic biodegradability of plastic materials
in soil by measuring the oxygen demand in a respirometer or the amount of carbon dioxide evolved
(MOD)
なお,対応の程度を表す記号“MOD”は,ISO/IEC Guide 21-1に基づき,“修正している”
2
K 6955:2017
ことを示す。
警告 土壌は,潜在的に病原性生物を含む可能性があるので,取り扱うときは,適切な予防措置を講
じる必要がある。有毒又は性質の未知な物質を扱う場合は,各自の責任において,安全及び健
康に対する適切な措置を取らなければならない。
2
引用規格
次に掲げる規格は,この規格に引用されることによって,この規格の規定の一部を構成する。これらの
引用規格は,その最新版(追補を含む。)を適用する。
JIS K 6953-2 プラスチック−制御されたコンポスト条件下の好気的究極生分解度の求め方−発生二
酸化炭素量の測定による方法−第2部:実験室規模における発生二酸化炭素の質量測定方法
JIS Z 8802 pH測定方法
ISO 10381-6,Soil quality−Sampling−Part 6: Guidance on the collection, handling and storage of soil for the
assessment of aerobic microbial processes in the laboratory
ISO 10390,Soil quality−Determination of pH
ISO 10634,Water quality−Guidance for the preparation and treatment of poorly water-soluble organic
compounds for the subsequent evaluation of their biodegradability in an aqueous medium
ISO 10694,Soil quality−Determination of organic and total carbon after dry combustion (elementary analysis)
ISO 11274,Soil quality−Determination of the water-retention characteristic−Laboratory methods
3
用語及び定義
この規格で用いる主な用語及び定義は,次による。
3.1
好気的究極生分解(ultimate aerobic biodegradation)
微生物によって,酸素の存在下での,有機物の二酸化炭素,水及び存在する他の元素の無機塩(無機質
化)並びに新しいバイオマスへの分解。
3.2
生物化学的酸素要求量,BOD(biochemical oxygen demand)
化学物質又は有機物が,特定条件下で,好気的生物酸化によって消費された溶存酸素の質量濃度。
注記 試験土壌1 kg当たりの消費酸素量(mg)として表す。
3.3
溶存有機炭素量,DOC(dissolved organic carbon)
特定の相分離によって除去不可能な水中の有機炭素部分。
注記1 試験材料100 mg当たりの炭素量(mg)として表す。
注記2 分離法の例は,15分間,40 000 m・s−2の遠心分離,又は直径0.2 μm〜0.45 μmの孔をもつ膜
を用いる膜ろ過。
3.4
理論的酸素要求量,ThOD(theoretical oxygen demand)
化学物質が,完全に酸化されるために必要な,分子式から計算する最大理論酸素要求量。
注記 試験材料1 mg又は1 g当たりの要求酸素量(mg)として表す。
3
K 6955:2017
3.5
理論的二酸化炭素発生量,ThCO2(theoretical amount of evolved carbon dioxide)
化学物質が,完全に酸化されるときに発生する二酸化炭素の最大理論量又は分子式から計算した理論値。
注記 試験材料1 mg又は1 g当たり発生する二酸化炭素量(mg)として表す。
3.6
誘導期(lag phase)
試験の開始から,分解微生物のじゅん(馴)化及び選択が始まり,化学物質又は有機物の生分解度が,
理論最大分解度の約10 %に到達するまでの期間(日数)。
3.7
生分解期(biodegradation phase)
試験の誘導期終了時から生分解の最大レベルの約90 %に到達するまでの期間(日数)。
3.8
生分解の最大レベル(maximum level of biodegradation)
化学物質又は有機物が試験中に到達する最大分解度で百分率で表示される。これ以上生分解は起こらな
い。
3.9
定常期(plateau phase)
生分解期の最後(生分解の最大レベル)から試験終了までの期間(日数)。
3.10
予調整(pre-conditioning)
試験条件での微生物のじゅん(馴)化によって試験性能の向上を目的とする試験対象化学物質又は有機
物の存在しない条件下での土壌の前培養。
3.11
予暴露(pre-exposure)
微生物のじゅん(馴)化及び選択によって試験材料を分解する土壌の能力向上を目的とする試験対象化
学物質又は有機物の存在下での土壌の前培養。
3.12
水分含量(water content)
土壌が105 ℃で恒量に達したとき,土壌から蒸発した水の質量を土壌の乾燥質量で除した値(土壌サン
プル中の水の質量と土壌粒子の質量との比)。
3.13
容水量(water-holding capacity)
土壌が105 ℃で恒量に達したとき,水で飽和された土壌から蒸発した水の質量を土壌の乾燥質量で除し
た値。
3.14
全有機炭素量,TOC(total organic carbon)
有機化合物中の炭素の量。
注記 化合物100 mg当たりの炭素量(mg)として表す。
4
K 6955:2017
4
原理
この方法は,土壌の水分量を調整することによって,試験土壌中におけるプラスチック材料の最適な生
分解速度を与え,さらに,材料の究極生分解度を求めるために設計されたものである。
プラスチック材料は,唯一の炭素源(エネルギー源)として土壌と混合する。混合物は,酸素の消費量
(BOD)又は二酸化炭素の発生量が検出される期間中フラスコ内に保持する。BODは,例えば,呼吸計フ
ラスコの気体体積を一定に保つのに要する酸素量を測定するか,体積及び/又は圧力を自動又は手動で測
定する。適切な呼吸計の例を,附属書Aに示す。二酸化炭素発生量は,試験材料の生分解挙動に合わせた
一定の間隔で,土壌に二酸化炭素を含まない空気を通し,適切な方法で空気中の二酸化炭素量を決定する
ことによって,測定する。適切な方法の例を,附属書B及び附属書Cに示す。
生分解度は,BODと理論的酸素要求量(ThOD)との比として,又は発生した二酸化炭素量と理論発生
量(ThCO2)との比として計算し,パーセントで表す。BODに対する硝化反応の影響は考慮しなければな
らない。試験は,生分解が定常状態に到達するか,長くとも2年1) を経過したとき,終了する。
各種の有機物に対して用いられるISO 11266と違って,この規格は,プラスチック材料の生分解度を測
定するために特別に設計されたものである。
注1) 対応国際規格には,“長くとも6か月”と記載されているが,これは誤りである。
5
試験環境
培養は,密閉系の暗所又は散乱光下,微生物に有害な種々の蒸気から遮断された囲いの中で行う。培養
温度は,20〜28 ℃の範囲から選び,望ましくは25 ℃とする。設定温度±2 ℃の一定温度に保つ。
6
試薬
試薬は次による。
6.1
蒸留水,脱イオン水 DOC 2 mg/L以上を含まないもの。
6.2
二酸化炭素吸収剤 ソーダ石灰を用いるのがよい。
7
装置
装置は,次による。
なお,全てのガラス器具は,完全に洗浄し,特に有機物又は有害な物質が付着していてはならない。
7.1
圧力測定型閉鎖呼吸計 試験用フラスコなどの器具を含むもの。恒温室又は定温装置(例えば,恒
温水槽)の中に設置する。例として,附属書Aに示す。
注記 十分な精度で生物化学的酸素要求量を測定できる呼吸計でもよいが,酸素消費量を検知し,自
動的にその酸素を補給する装置を用いるのがよい。これによって分解過程における酸素不足及
び微生物活性の阻害が生じない。
7.2
発生二酸化炭素量を測定するための装置
7.2.1
試験フラスコ ガス漏れのない,二酸化炭素を透過させない管を備えたガラス容器(例えば,500 ml
程度の三角フラスコ又は瓶)。恒温室又は定温装置(例えば,恒温水槽)の中に設置する。
7.2.2
二酸化炭素を含まない空気の供給装置 各試験フラスコに二酸化炭素を含まない空気を数ml/min
±10 %の範囲で一定量供給できるもの(試験フラスコと供給装置とを組み合わせた例は,附属書B参照)。
ASTM D5988に示されている培養槽を選択してもよい。
7.2.3
二酸化炭素測定装置 代表的なものは,二酸化炭素赤外分析計,溶存無機炭素(DIC)分析計,塩
5
K 6955:2017
基性溶液に完全に吸収した後,滴定法で測定する装置(附属書C参照)及びJIS K 6953-2に規定する重量
法で測定する装置。
7.3
分析用はかり
0.1 mg単位まで測定可能な化学天びん(秤)。
7.4
pHメータ
JIS Z 8802に規定するpH計。
8
操作
8.1
試験材料の調製
試験材料は,質量が既知で,試験に用いる分析装置で測定可能なBOD量,又は二酸化炭素発生量を生
じる十分な量の炭素を含んでいなければならない。全有機炭素量(TOC)を化学式から計算するか,又は,
適切な分析手段(例えば,元素分析,ISO 8245による測定)によって決定し,ThOD又はThCO2を計算す
る(附属書C及び附属書D参照)。
注記 高分子化合物に対する元素分析は,低分子化合物に対するよりも精度は劣るが,ThOD又は
ThCO2を計算する目的には,通常十分な精度である。
試験材料の量は,試験材料が入っていない試験土壌だけによる酸素消費量又は二酸化炭素発生量よりも
十分に大きくなる量でなければならない。100 mg〜300 mgの試験材料を100 g〜300 gの土壌に対して用い
るのが通常適切である。土壌が非常に大量の有機物を含んでいない場合は,200 mgの試験材料と200 gの
土壌とを使用するとよい。
二酸化炭素発生測定による試験の場合は,試験材料の二酸化炭素発生量と空試験の二酸化炭素発生量と
の差を大きくするために,試験材料を多めに使用できる(例えば,200 gの土壌に対して2 500 mg)。追加
で,最終マスバランスを求める場合には,更に多くの試験材料が必要になる(附属書E参照)。
フラスコにおける土壌呼吸への影響を低減するためには,必要に応じて,試験材料をあらかじめ通気し
ておくか,又は不活性物質を添加することが望ましい。
試験材料は,粉体を用いることが望ましいが,フィルム,断片又は成形品を用いてもよい。
試験試料は,低温で粉体にしてもよい。
試験材料の形状は,究極生分解度には,ほとんど影響しないことが実験によって示されている。しかし,
生分解速度は,試験材料の形状の影響を受ける。したがって,同じ試験期間で異なるタイプのプラスチッ
ク間で比較を行う場合は,同一形状の試験材料を用いることが望ましい。粉体を試験材料とする場合は,
粒度分布が分かっている細かい粒子形状のものの使用が望ましい。最大直径は,250 μmの粒度が望ましい。
試験材料が粉体でない場合は,材料の大きさが5 mm×5 mmを超えてはならない。また,試験材料の形状
によって使用する試験装置の大きさが決まる。装置の構造によって機械的な異常が発生しないことを確か
めておくことが望ましい。通常は,試験材料を加工する場合は,試験材料の分解挙動に影響しないように
する(例えば,混合物の場合は,粉体を使用する。)。
試験材料の水素,酸素,窒素,りん,硫黄含量及び分子量(例えば,サイズ排除クロマトグラフ法によ
る。)を測定することが望ましい。試験材料中に,添加剤が含まれている場合,プラスチック材料の正確な
生分解度を求めるためには,添加剤の生分解度を求めなければならない。
水に貧溶解性の物質の詳細な取扱いは,ISO 10634による。
8.2
対照材料の調製
既知の生分解性ポリマー(例えば,微結晶セルロース粉体,灰分のないセルロースろ紙,又はポリ-β -

6
K 6955:2017
ヒドロキシ酪酸)を対照材料とする。対照材料の形状及び大きさは試験材料と同じにするとよい。陰性対
象として,形状及び大きさが試験材料と同じ非生分解ポリマー(例えば,ポリエチレン)を使用してもよ
い。
8.3
試験土壌の調製
8.3.1
土壌の採集及びふるい分け
畑地,森林などの表層から採集した天然の土壌を用いる。土壌は,5 mm以下,望ましくは2 mm以下の
大きさにふるい分けし,さらに,植物材料,小石,その他不活性物を取り除く。
わら(藁)などの有機物固体は,試験中に分解されて結果に影響する可能性があるため,できるだけ取
り除かなければならない。
土壌は,予調整を行ってよいが,通常は予暴露した土壌は使用しない。特に,自然環境下での生分解挙
動を模擬する場合の土壌は,予暴露しない。試験の目的に応じて予暴露を行った土壌を用いることができ
る。試験材料の潜在的生分解度を評価する場合には,採取した土壌は,試験材料に予暴露した土壌を使用
する。この場合,試験報告書には,予暴露した土壌を用いたこと及び予暴露の詳細な方法を明記する(例
えば,予暴露した土壌での生分解度=x %)。予暴露した土壌は,種々の条件下で行っている適切な実験室
内生分解試験又は関連した環境条件が存在する場所(例えば,有機物を含む場所又は工業的処理プラント)
から採取することができる。
土壌を採集した場所,位置,植物の存在又は以前に栽培した作物,採集した日付,採集した深さ,また,
可能であれば,肥料及び殺虫剤使用履歴を記録する。
8.3.2
基準土壌の調製
8.3.1に規定する天然土壌の代わりに,基準土壌を使用してもよい。塩類を添加する前の基準土壌の成分
は表1に示す。基準土壌の使用によって,土壌の取扱い及びその通気の問題が減少するので,かさばった
土壌(ローム土壌又は粘土質土壌)の条件下でのプラスチック材料の生分解性を決定するのに非常に有効
となる。
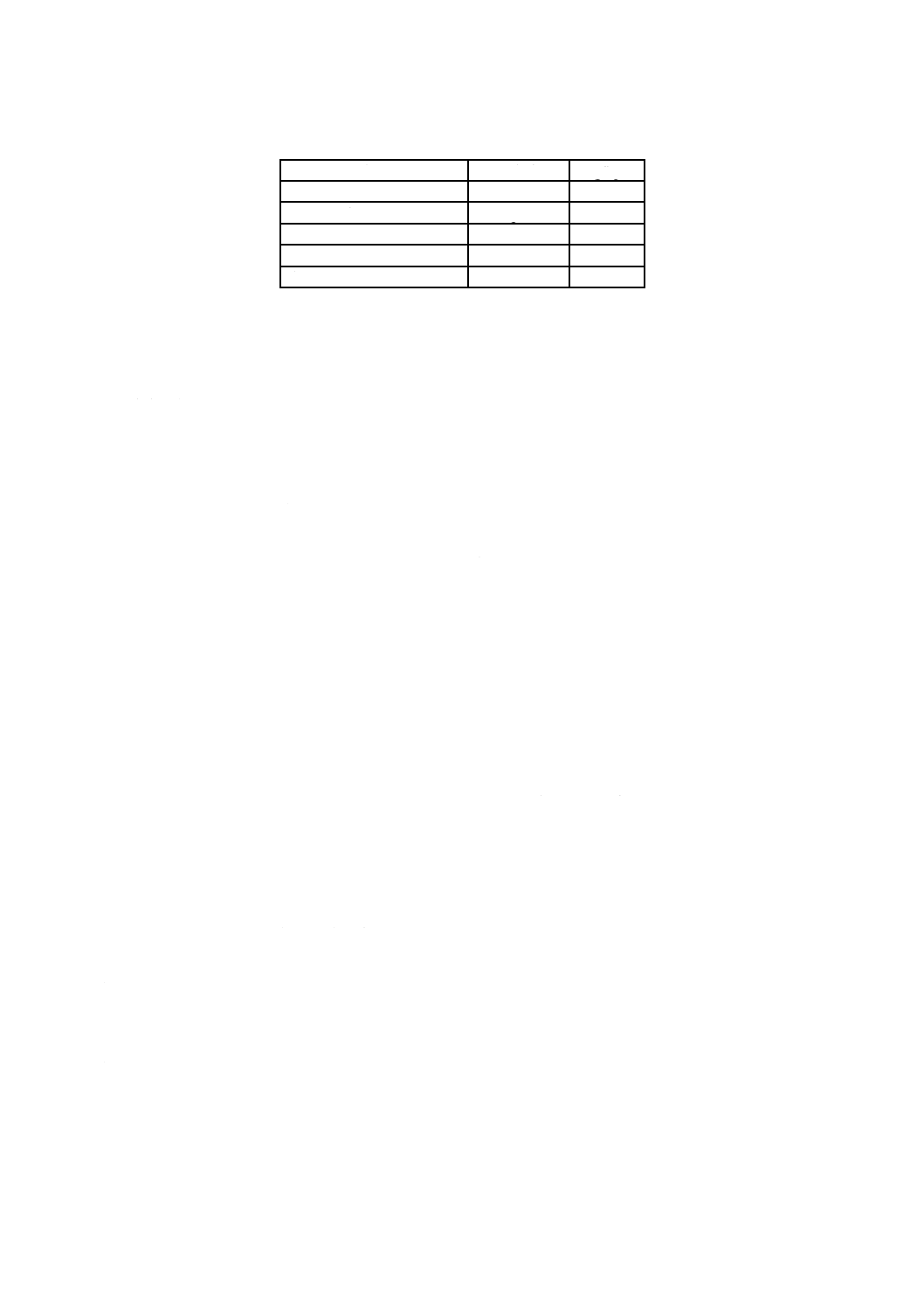
表1−塩類を加える前の基準土壌の成分
組成
説明
乾燥質量による
配合率(%)
工業用けい砂
直径0.05 mm〜0.2 mmの粒子を50 %以上含む細砂
70
粘土
カオリナイト粘土(少なくとも30 %のオリナイトを含んでいる。)
又はカルシウムベントナイト
10
天然土壌
8.3.1参照
16
熟成堆肥
好気的堆肥化プラントの十分に通気されていた堆肥を使用する。
基準土壌の微生物活性を安定させるために,少なくとも1年間成
熟した堆肥を使用するか,又は使用の前に数箇月の間老化を待つ
のがよい。
使用する堆肥は,ガラス,石又は金属片のような大きい不活性物
質のない,均一な堆肥でなければならない。手作業で不活性物質
を取り除いて,次に2 cm〜5 cmのふるい(篩)で堆肥を選別する。
4
表1で規定する土壌に,表2で示す塩類を添加して,基準土壌として使用する。水分調整の際に,塩類
を蒸留水又は脱イオン水に溶解して加えるとよい(8.3.4参照)。
7
K 6955:2017
表2−表1の土壌に添加する塩類の成分
化合物名
化学式
g/kg
リン酸二水素カリウム
KH2PO4
0.2
硫酸マグネシウム
MgSO4
0.1
硝酸ナトリウム
NaNO3
0.4
尿素
CH4N2O
0.2
塩化アンモニウム
NH4Cl
0.4
基準土壌の妥当性は,ラウンドロビン試験によって検証された(附属書G参照)。
8.3.3
土壌特性の測定
試験結果を十分に解釈するため,土壌特性に関する知見を求める。選択した土壌について,少なくとも
次の検査を行うとよい。
a) 最大容水量 ISO 11274による。
b) 土壌のpH ISO 10390による。
c) 有機物含量 ISO 10694による。
8.3.4
土壌の水分含量及びpHの調整
土壌に適切量の蒸留水又は脱イオン水を添加,又は直射日光の当たらない場所で風乾後適切量の蒸留水
又は脱イオン水を添加することによって,土壌の水分含量を試験材料に適した値に調整する。土壌のpH
が,6.0〜8.0の間に入っていない場合は,この範囲に調整する。
注記 試験土壌の最適な水分含量は,試験材料によって異なる。通常は,最大容水量の40 %〜60 %で
ある。
適切な生分解状態を得るためには,試験材料,又は対照材料中の有機炭素と土壌中の窒素との比率(C:
N比)において,C:N=40:1よりも窒素が少ない場合は,このレベルに調整するとよい。C:N比の調
整は,窒素源として,例えば,塩化アンモニウム水溶液を添加する,又は,表2に示す窒素化合物の水溶
液を使用することによって行われる。
8.3.5
土壌の取扱い及び保存
土壌は,試験に使用するまで密閉容器に入れ4 ℃±2 ℃で保存する。土壌中の微生物活性が低下しない
ように,採取した水分量を保つ。
ISO 10381-6に従い,サンプリングによって土壌微生物の活性が影響を受けないようにする。
8.4
試験の準備及び実施
次の数のフラスコを用意する。
a) 試験材料用フラスコ(略号FT)3個
b) 空試験用フラスコ(略号FB)3個
c) 対照材料を用いて土壌の活性を調べるためのフラスコ(略号FC)3個
必要に応じて,次のフラスコを用意する。
d) 試験材料の非生物的変化又は非微生物的分解を調べるためのフラスコ(略号FS)1個
e) 試験材料の阻害効果可能性を調べるためのフラスコ(略号FI)1個
それぞれのフラスコの底に土壌(8.3参照)を置き,表3に示されているように試験材料(8.1参照)又
は対照材料(8.2参照)を土壌に加える。試験混合物を含む,それぞれのフラスコの質量を記録する。試験
材料用,空試験用及び対照材料用のフラスコ数が2個の試験条件で行った場合は,これを報告書に記載す
る。
8
K 6955:2017
試験材料と土壌中の微生物とをよく接触させるために,粉体の場合は,土壌と均一に混合する。また,
フィルムの場合は,できるだけ土壌に広く分散させる。また,試験材料と土壌中の微生物との接触をよく
するために,試験混合物の表面をスパチュラで圧縮することが望ましい。
非生物的な分解を検証する場合には,試験の開始に当たって微生物の活性を阻害し,さらに,試験中無
菌状態を持続した手順の細部を報告に記載する。
これらの試験フラスコを恒温環境(箇条5)に置いて,所定の温度になるまで放置する。呼吸計又は二
酸化炭素を含まない空気製造装置と必要な接続を確認し,培養を開始する。
酸素消費量測定の場合,圧力計の目盛を読み取る(手動装置の場合)又は酸素消費量の記録計が正常に
作動しているかを確認する(自動測定呼吸計の場合)(附属書A参照)。
二酸化炭素発生量測定の場合,二酸化炭素発生速度に応じた時間間隔で各フラスコから発生する二酸化
炭素量を適切な方法で測定する(附属書B及び附属書C参照)。
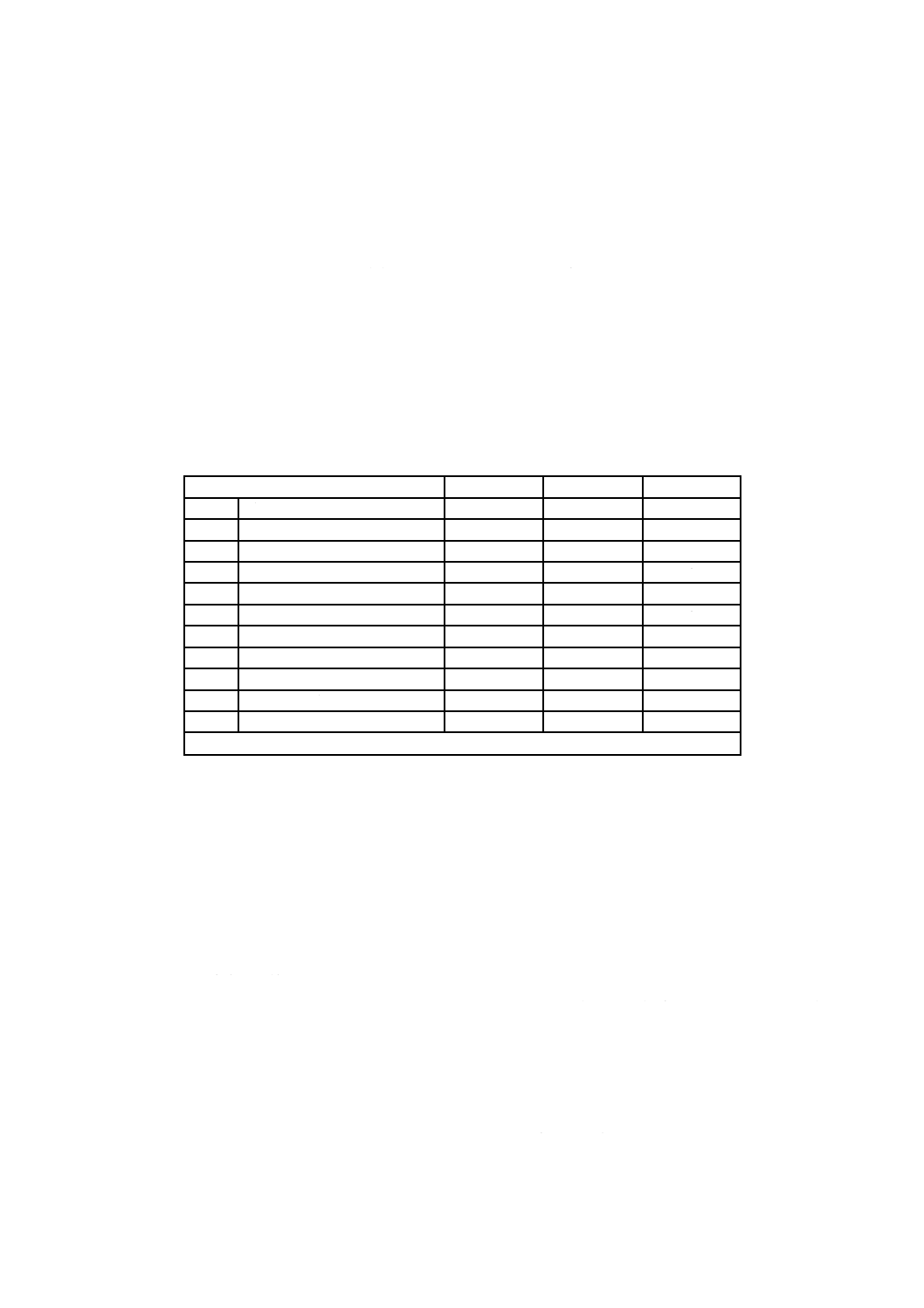
表3−試験材料及び対照材料の構成
フラスコ
試験材料
対照材料
試験土壌
FT
試験
+
−
+
FT
試験
+
−
+
FT
試験
+
−
+
FB
空試験
−
−
+
FB
空試験
−
−
+
FB
空試験
−
−
+
FC
土壌活性確認
−
+
+
FC
土壌活性確認
−
+
+
FC
土壌活性確認
−
+
+
FS
非生物的分解確認(任意)
+
−
−
FI
阻害確認(任意)
+
+
+
注記 +:あり −:なし
試験の途中で試験土壌の乾燥によって生分解速度が低下したと考えられる場合は,測定を停止してフラ
スコを呼吸計,又は二酸化炭素を含まない空気の製造装置から取り外す。フラスコの質量を測定し,水分
含量が試験開始時の値になるように適切量の蒸留水又は脱イオン水を添加する。フラスコを試験装置に再
び接続して酸素消費量の測定,又は二酸化炭素発生量の測定を再開する。これらの操作は,土壌微生物の
活性を阻害しないようにし,かつ,酸素消費量又は二酸化炭素発生量の測定に影響しないようにする。ま
た,実際に行った作業を,試験報告書に明記する。
BOD値,又は二酸化炭素発生が一定レベルに至り(定常期になる。),それ以上は分解が進まないと考え
られるときに,試験は,終了したとみなす。
試験期間は6か月を超えないことが望ましい。しかしながら,生分解がまだ観察されて,かつ,生分解
が定常期に到達しない場合は,その試験は延長してもよい(附属書F参照)。ただし,2年を超えない方が
よい。試験期間が6か月より長い場合は,定期的に可能性のある箇所のガス漏れを調べる。試験の延長及
び特別措置,例えば微生物を再接種したり,又は十分な栄養素を供給したりした場合には,試験報告に詳
述する。
試験終了後に,フラスコを取り出して質量を測定し,試験土壌の水分含量の減少を確認する。可能であ
るならば,残留する試験材料を適切な溶媒で土壌から抽出して質量測定をすることが望ましい。
9
K 6955:2017
9
計算及び結果の表示
9.1
計算
9.1.1
酸素消費量からの生分解度百分率
適切なタイプの呼吸計に対して,製造業者から与えられた方法を使用して,それぞれのフラスコごとに
酸素消費量を測定する。生分解度百分率Dtは,式(1)によって算出する。
d
T
Bt
t
t
O
B
B
D
×
−
=ρ
············································································ (1)
ここに,
Dt: 時間tの生分解度百分率(%)
Bt: 時間tの試験材料を含むフラスコFTの試験土壌1キログ
ラム当たりのBOD値(mg/kg)。酸素消費量測定値(mg)
を試験土壌量(kg)で除することによって計算する
BBt: 時間tの試験土壌1キログラム当たりの空試験FBのBOD
値(mg/kg)
ρT: フラスコFTの試験材料の濃度。試験土壌1キログラム当
たりの試験材料の質量(g/kg)
Od: 試験材料1グラム当たりのThOD値(mg/g)
同様な方法で対照材料FCの生分解度百分率を算出する。非生物的分解確認フラスコFS,及び阻害確認
フラスコFIの試験をしているときは生分解していないことを確認する。ThODの計算は,附属書Dを参照。
9.1.2
二酸化炭素発生量からの生分解度百分率
9.1.2.1
試験材料の理論的二酸化炭素発生量
ミリグラムで表された理論的二酸化炭素発生量ThCO2は,式(2)によって算出する。
12
44
C
CO2
×
×
=
w
m
T
······································································ (2)
ここに,
2
CO
T
: 試験材料の理論的二酸化炭素発生量ThCO2(mg)
m: 試験系中に導かれた試験材料の質量(mg)
wC: 化学式から求める,又は元素分析から計算される試験
材料の炭素含有量。質量分率として表される
44及び12: それぞれ二酸化炭素の分子量及び炭素の原子量
同じ方法で対照材料の理論的二酸化炭素発生量並びにフラスコFI中の試験材料及び対照材料の混合物の
理論的二酸化炭素発生量を計算する。
9.1.2.2
生分解度百分率
それぞれの測定間隔ごとに,発生した二酸化炭素量から試験フラスコFTに対する生分解度百分率Dtは,
式(3)によって算出する。
100
2
CO
B
T
t
×
Σ
−
Σ
=
T
m
m
D
································································· (3)
ここに,
Dt: 試験のスタートから時間tの生分解度百分率(%)
ΣmT: 試験のスタートから時間tの間に試験フラスコFT中に発
生した二酸化炭素の質量(mg)
ΣmB: 試験のスタートから時間tの間に空試験フラスコFB中に
発生した二酸化炭素の質量(mg)
2
CO
T
: 試験材料の理論的二酸化炭素発生量ThCO2(mg)
同様に,土壌活性確認フラスコFC中の対照材料の生分解度百分率を算出する。
10
K 6955:2017
9.2
結果の表示及び解釈
測定したBOD値又は二酸化炭素発生量,及び生分解度百分率は,測定した時間ごとに表を作って表示
する。それぞれのフラスコごとに,時間の関数としたBOD曲線又は二酸化炭素発生量曲線,及び時間の
関数とした生分解度百分率曲線をプロットする。3個2) のフラスコ間で結果が類似している場合には,平
均曲線をプロットしてもよい。
生分解度曲線の定常期の平均値から測定した最大の生分解度は,その試験材料の生分解度の特性を表す。
試験材料のぬれ能力及び形状は,得られた結果に影響を及ぼす可能性がある。異なる試験材料の結果と
比較する場合,このことを考慮に入れることが望ましい。
低い生分解性を示す試験結果を解釈するために,試験材料の毒性に関する情報を得ておくのがよい。
注2) 対応国際規格では“2個”と記載されているが,これは誤りである。
10
結果の正当性
試験は,以下のa) 及びb) の条件を満たす場合に適合とみなす。
a) 対照材料の生分解度百分率が,定常期又は試験終了時に60 %以上である。
b) 定常期又は試験終了時に,3個のブランクのBOD値又は二酸化炭素発生量を求める。この平均値と3
個のブランクのそれぞれの値との差が20 %以内である。
これらの判定基準が満たされない場合は,他の予調整又は予暴露された土壌を用いて再試験する。
11
試験報告
試験報告には,次の事項を含まなければならない。
a) この規格の番号
b) 試験材料及び対照材料を同定するのに必要な全ての情報:名前,化学組成,化学式(分かる範囲で),
ThOD,ThCO2(計算方法を含む。),形状,外観,試験に使用したサンプルの量及び濃度並びに添加剤
濃度(分かる範囲で)を含む。
c) 試験材料の履歴[未使用か(顆)粒,加工最終プラスチック製品又は古い試料],前処理が行われたら,
前処理の条件の詳細。
d) 土壌に関する完全な情報:出所,採取日,特性,試験に使用した量,貯蔵条件,予暴露の操作及び詳
細を含む。
e) 主な試験条件:使用した試験材料の量,培養温度及び培養期間を含む。
f)
使用した分析技術:呼吸計の原理及び二酸化炭素量の測定方法を含む。
g) 他の実施した操作の全て:試験中の試験混合物への水分添加,試験材料の分析結果及び試験終了時の
水分含量を含む試験混合物の分析結果を含む。
h) 試験材料及び対照材料に関して得られた全ての試験結果(表及びグラフ形式で):測定された累積BOD
又は二酸化炭素発生量,生分解度百分率及び時間に対するこれらの変数の曲線を含む。
i)
誘導期,分解期,分解の最高レベルの期間及び全体の試験期間。
さらに,任意の試験として実施,又は測定した場合の試験報告には,次のことを記載する。
j)
試験材料の残留量又は残留量から計算される生分解度百分率。
k) 土壌中の微生物のコロニー形成単位(cfu/g)。
l)
試験期間の延長中に微生物を再接種又は栄養不足を回避するために用いた方法の詳細。
m) 入手可能な試験材料の全ての情報及び毒性作用を避けるために試験試料濃度を減らした場合の使用
11
K 6955:2017
量。
n) 他の関連データの全て(例えば,試料の初期分子量,未分解プラスチック材料の分子量)。
o) 指定された試験方法からのあらゆる逸脱。
12
K 6955:2017
附属書A
(参考)
圧力測定型閉鎖呼吸計の原理
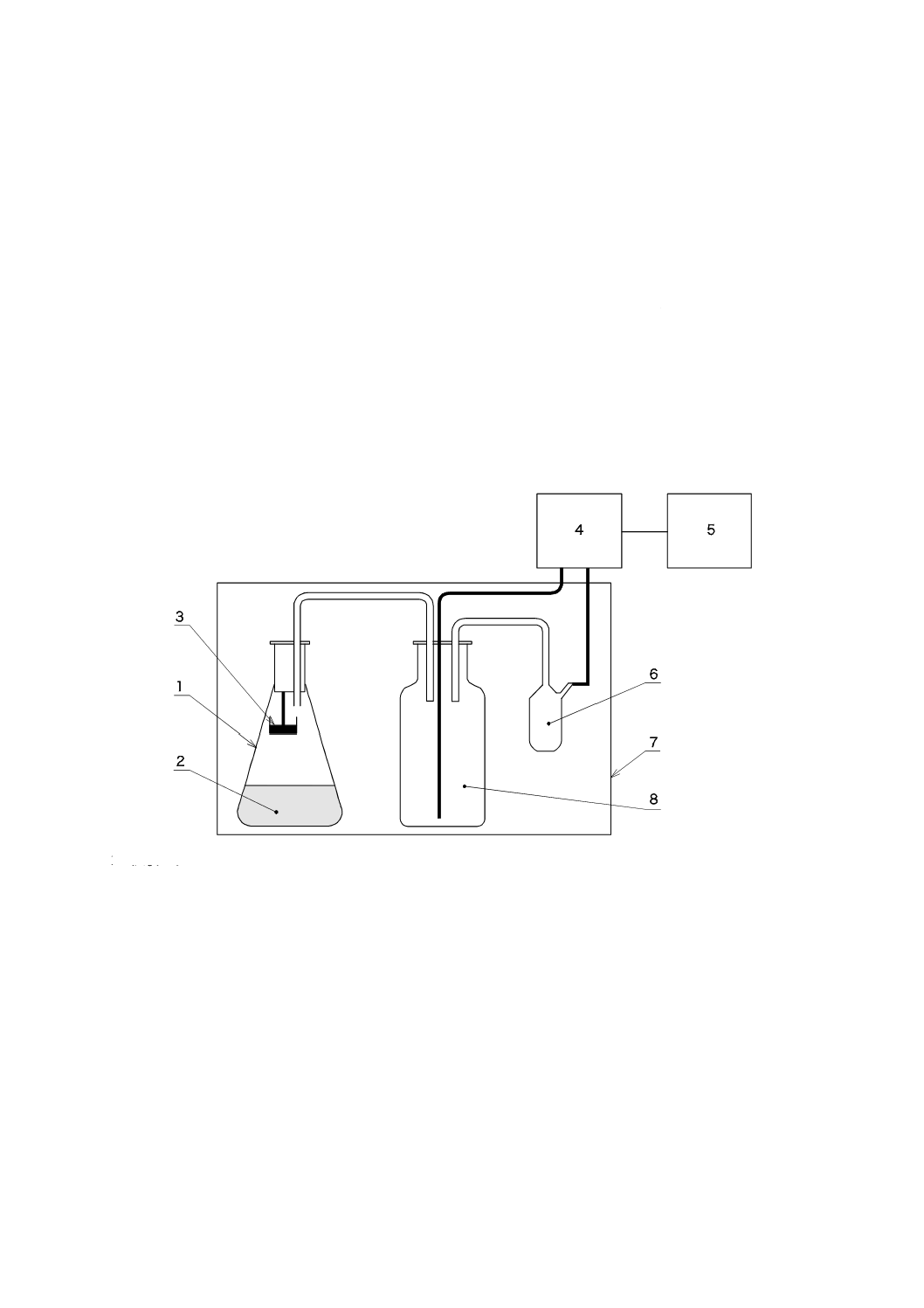
上部空間に二酸化炭素吸収剤を装備した試験フラスコ(図A.1の1),電気分解形の酸素発生装置(図
A.1の8),圧力計(図A.1の6),外部のモニタ(図A.1の4)及び記録装置(図A.1の5)(プリンタ,プ
ロッタ又はコンピュータ)で構成する圧力測定型閉鎖呼吸計(図A.1)を,温度管理した環境(例えば,
湯せんなどを用いて)に設置する。試験フラスコには,容器容量のほぼ1/3まで試験混合物を入れる。生
分解が起こると,微生物は,酸素を消費し二酸化炭素を発生する。この二酸化炭素は,全て二酸化炭素吸
収剤に吸収され,試験フラスコ内の圧力が低下する。圧力低下は,圧力計によって検知され,その度に電
気分解形の酸素生成が開始される。初期圧力に回復すると電気分解が停止する。酸素消費量に比例して使
用された電気量は,連続測定され,記録計にmg/Lの単位でBODが,酸素消費量として記録される。
1 試験フラスコ
2 試験混合物
3 二酸化炭素吸収剤
4 モニタ
5 プリンタ,プロッタ又はコンピュータ
6 圧力計
7 温度自動調節された囲い
8 酸素発生装置
図A.1−圧力測定型閉鎖呼吸計の概要図
13
K 6955:2017
附属書B
(参考)
発生した二酸化炭素の量を測定する装置の例
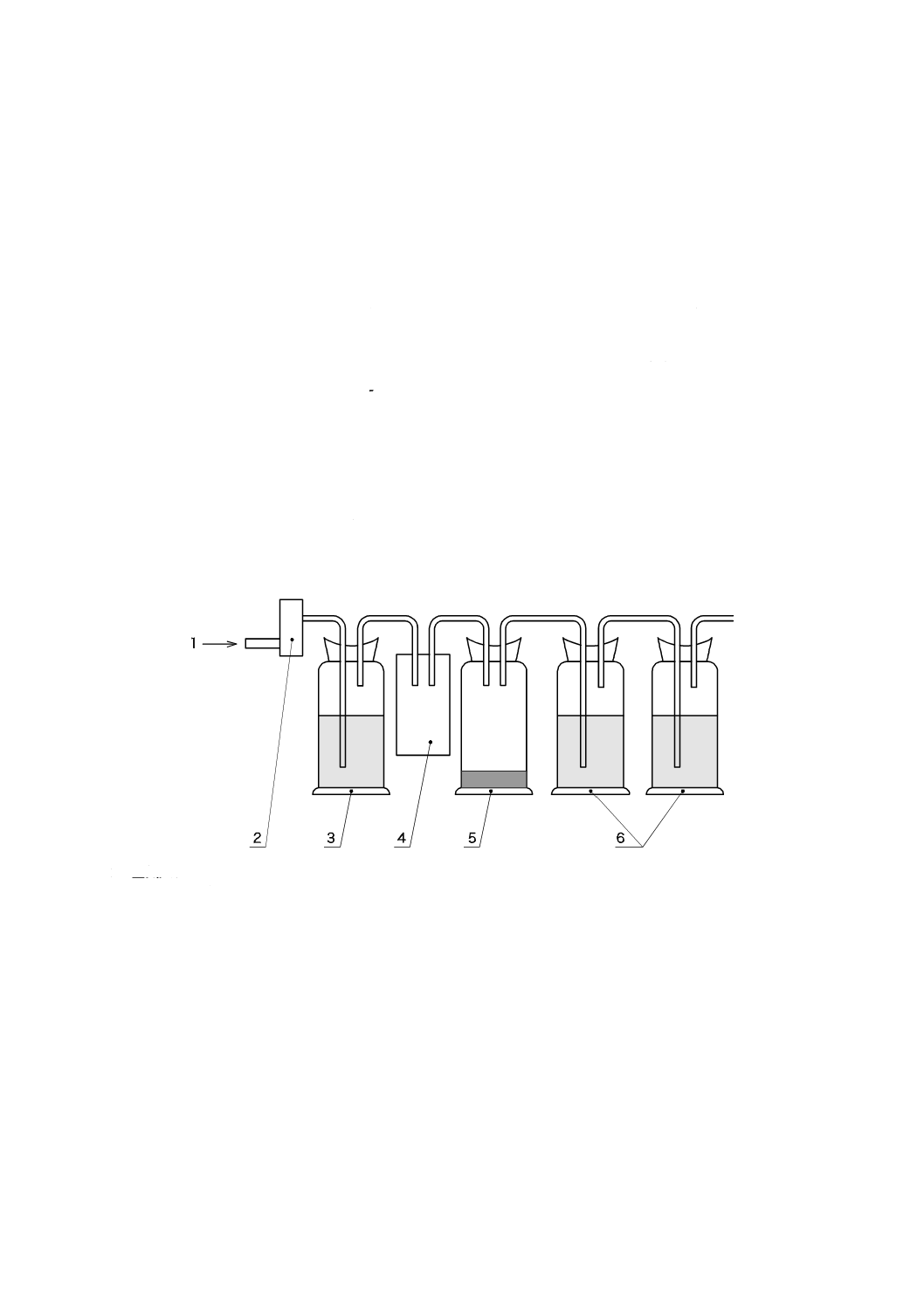
試験装置の各容器は,図B.1に示すように,ガスを透過しない管によって直列につなぐ。一定の低圧で
二酸化炭素を除去した空気で試験装置を数ml/minで通気する。空気流量を調べるために,空気量を泡の数
で判断するか,又は適切なガス流量調節計(図B.1の2)を使用する。二酸化炭素を含まない合成空気,
又は圧縮した空気を使用する。後者の場合,空気を乾燥ソーダ石灰の入った瓶(図B.1の3)に通すか,
又は少なくとも2本の例えば,10 mol/Lの水酸化カリウム水溶液500 mlのガス洗浄瓶を通すことによって
二酸化炭素を除去する。例えば,0.012 5 mol/Lの水酸化バリウム100 mlが入った追加の瓶及び空瓶は,濁
りによって空気中の二酸化炭素を確認するため又は,試験フラスコへの液体の流入を防ぐために使用する
ことができる。必要ならば,試験土壌からの水分蒸発を避ける目的で空気を加湿するために試験フラスコ
(図B.1の5)の前へ加湿器(図B.1の4)を挿入してもよい。例えば,飽和したりん酸ナトリウム水溶液
のような一定加湿水溶液に,空気をバブリングすることでできる。附属書Cに記載するように,生分解が
起これば,試験フラスコ内で二酸化炭素が発生し,次の吸収瓶(図B.1の6)で吸収される。
試験土壌(試験フラスコ図B.1の5)の湿度,好気条件,及び空気流量の調整を保持する必要がある。
1 空気入口
2 ガス流量調節計
3 空気中二酸化炭素吸収瓶
4 加湿器
5 試験フラスコ
6 発生二酸化炭素吸収瓶
図B.1−発生二酸化炭素量を測定する装置の概略図
14
K 6955:2017
附属書C
(参考)
発生した二酸化炭素の量を求める方法の例
C.1 DIC測定による二酸化炭素定量
発生した二酸化炭素は,水酸化ナトリウム水溶液に吸収され,灰化することなしにDOC分析機器など
を用いて,溶存無機炭素(DIC)として定量する。
蒸留水又は脱イオン水を用いて0.05 mol/Lの水酸化ナトリウム水溶液を調製する。二酸化炭素発生量を
計算するとき,この溶液のDIC測定値を空試験の値とする。試験フラスコに,各々100 mlの水酸化ナトリ
ウム水溶液が入った2本の二酸化炭素吸収瓶を直列につなぐ。空気中の二酸化炭素が水酸化ナトリウム水
溶液に入らないように,最後の二酸化炭素吸収瓶の出口には小さなサイフォンをセットする。二酸化炭素
測定日には,試験フラスコの次にある二酸化炭素吸収瓶を取り外し,DIC測定のために十分なサンプルを
採取する。その瓶を第二の二酸化炭素吸収瓶と取り替え,新たに調製した水酸化ナトリウム水溶液の入っ
た二酸化炭素吸収瓶を追加する。最終日には,試験溶液を酸性化後,両方の二酸化炭素吸収瓶のDICを測
定する。
発生した二酸化炭素は,式(C.1)によって算出する。
10
67
.3
)
(
)
CO
(
B
T
T
2
×
−
=
D
D
························································· (C.1)
ここに,
(CO2)T: 二酸化炭素発生量(mg)
DT: 試験の水酸化ナトリウム水溶液のDIC測定値(mg/L)
DB: 空試験の水酸化ナトリウム水溶液のDIC測定値(mg/L)
3.67: 二酸化炭素(44)分子量と炭素(12)原子量との比
10: 100 mlの水酸化ナトリウム水溶液に対する補正係数
C.2 水酸化バリウム溶液を用いる滴定方法
発生した二酸化炭素は,水酸化バリウム[Ba(OH)2]と反応し炭酸バリウム(BaCO3)として沈殿する[式
(C.2)参照]。発生した二酸化炭素量は,残存する水酸化バリウム量を塩酸(HCl)で滴定することによって
決定する[式(C.3)参照]。
CO2+Ba(OH)2 → BaCO3+H2O ··········································· (C.2)
Ba(OH)2+2HCl → BaCl2+2H2O ··········································· (C.3)
Ba(OH)2・8H2Oの4.0 gを蒸留水又は脱イオン水に溶解し,1 000 mlとすることによって0.012 5 mol/L水
溶液を得る。試験期間中同一試薬を用いることができるよう,十分な量(例えば,5 L)を調製することが
望ましい。固形物をフィルタでろ過し,標準塩酸溶液を用いて適定し,正確な濃度を決定しておく。空気
中の二酸化炭素の吸収を防ぎ,透明な溶液としておくためにシールして保管する。指示薬としてフェノー
ルフタレインを用いるか又は自動滴定装置で終点を決定する。
1 mol/Lの塩酸(36.5 g/L)の50 mlを蒸留水又は脱イオン水で1 000 mlとし,0.05 mol/L溶液を得る。
試験開始時,3本の吸収瓶それぞれに水酸化バリウム水溶液100 mlを正確に分け入れる。試験材料の性
質と量とに応じて,吸収させる液量は変更する。滴定のため定期的に試験フラスコに最も近い瓶を取り外
す。この操作は,例えば,最初の吸収瓶が濁り,かつ,2番目の吸収瓶には炭酸バリウムの沈殿が観察さ
れる前に,必要に応じて取り替える。滴定は,試験開始時は1日おきに行い,それから定常期に達したと
15
K 6955:2017
きは5日ごとに行う。吸収瓶を取り外した後は,空気中の二酸化炭素が入るのを防ぐために,速やかに栓
で封鎖する。残りの二つの瓶を一つずつ試験フラスコ側に近づけ,一連の装置の最後には新鮮な水酸化バ
リウム溶液で満たした新しい吸収瓶を設置する。特に試験期間が長い場合には,その溶液の正確な濃度を
決定しておく。試験材料,対照材料,空試験,阻害対照及び植種源だけの対照を含む全てのフラスコは,
正確に同じ方法で取り扱う。
吸収瓶を取り外した後は,水酸化バリウム溶液を2〜3本に分けて塩酸で滴定する。使用した塩酸の量を
記録しておく。
吸収瓶に捕集された二酸化炭素量は,式(C.4)によって算出する。
22
2
A
Bz
Bt
A
A
0
B
B
×
×
×
−
×
=
c
V
V
V
c
V
c
m
·············································· (C.4)
ここに,
m: 吸収瓶に捕集された二酸化炭素量(mg)
cA: 塩酸の正確な濃度(mol/L)
cB: 水酸化バリウム水溶液の正確な濃度(mol/L)
VB0: 試験開始時における水酸化バリウム水溶液の体積(ml)
VBt: 時間t時点での,滴定前の水酸化バリウム水溶液の体積
(ml)
VBz: 滴定に使用した水酸化バリウム水溶液の体積(ml)
VA: 滴定に使用した塩酸の体積(ml)
22: 二酸化炭素の分子量の半分の値
次の条件が満たされる場合には,式(C.5)を用いる。
− 水酸化バリウム水溶液の体積は,吸収前後で正確に100 mlである。
− 全ての溶液を滴定に使用(VB0=VBt=VBz)
− 水酸化バリウム水溶液の濃度cBは正確に0.012 5 mol/L
− 塩酸の濃度cAは,正確に0.05 mol/L
)
50
(
1.1
A
V
m
−
×
=
···································································· (C.5)

16
K 6955:2017
附属書D
(参考)
理論的酸素要求量(ThOD)
D.1 ThODの計算
ユニット分子量Mrをもつ物質CcHhClclNnSsPpNanaOoの理論的酸素要求量は,元素組成が既知か,又は元
素分析によって決定することができれば,次の式によって算出することができる。
この計算は,炭素は二酸化炭素に,水素は水に,りんはP2O5に,硫黄は六価の酸化状態に,さらに,塩
素は塩化水素になることを暗に示している。N,P及びSの酸化は,分析によって確認する必要がある。
この計算では,窒素はアンモニウムとして放出される。
ThODは,試験材料1 g又は1 mg当たりのmg-酸素量として表示する。
[
]
r
M
o
na
p
s
n
cl
h
c
−
+
+
+
−
−
+
=
5.0
5.2
3
)
3
(
5.0
2
16
ThOD
D.2 例 ポリ-β -ヒドロキシ酪酸(PHB)
化学式1) C4H6O2 c=4,h=6,o=2,ユニット分子量Mr:86
86
)2
6
5.0
4
2(
16
ThOD
−
×
+
×
×
=
ThOD=1.674 4 mg/mg PHB=1 674.4 mg/g PHB
注1)
PHBは,β -ヒドロキシ酪酸モノマーからなる高分子である。重合(エステル形成)のために水
が除去される。したがって,PHBの最終的な分子式は,モノマーから(化学反応によって外れ
る)水1分子を差し引いたものに等しい。
D.3 例 ポリエチレン/でんぷん/グリセロールブレンド物
組成
化学式
ThOD
(mg/g)
組成量
ThOD
(mg/フラスコ)
(%)
(mg/フラスコ)
ポリエチレン
(C2H4)n
3 400
50
500
1 700
でんぷん
(C6H10O5)n
1 190
40
400
476
グリセロール
C3H8O3
1 200
10
100
120
ブレンド計
100
1 000
2 296
17
K 6955:2017
附属書E
(参考)
生分解性試験の終わりに,水に不溶性のプラスチック材料の残存量及び
その分子量を測定する例
生分解度試験の終わりに残っているプラスチック材料の量及び分子量を測定することが有効な場合があ
る。水と混和しない有機溶剤に可溶で,水に不溶なプラスチック材料を分析する場合には,次のような方
法又は他の適切な方法が使える。
a) 分液漏斗に試験混合物を移し,適切な有機溶剤を加え,生分解されないで残ったプラスチック材料を
抽出するために10〜20分間振とうする。水層から有機溶媒層を分離する。新しい溶媒を加え,この手
順を繰り返す。
b) 有機抽出物を混合して,乾燥するまで溶媒を蒸発させる。その固体サンプルは,適正な容量の適切な
溶媒に溶解する。
c) マイクロシリンジを使用して,サイズ排除のクロマトグラフ法のゲルを詰めたカラムを使った高速液
体クロマトグラフ(HPLC)に適正量を注入する。分析を開始し,クロマトグラムを記録する。
d) 検量線を使ってプラスチック材料の量を測定する。
e) 検量線を作成するには,同じプラスチック材料,又は類似の構造をもつ分子量が既知のプラスチック
材料を使用して,保持時間と分子量との関係(検量線)がクロマトグラムから得られる。これらの関
係を使って分子量を計算する。
試験後の残存プラスチック材料の絶対分子量は,Low Angle Laser Light Scattering(LALLS)及び
Differential Refractive Index(示差屈折率)を組み合わせた検知器をもったHPLCによっても測定すること
ができる。
18
K 6955:2017
附属書F
(参考)
長期試験の例
F.1
セルロース,小麦グルテン,亜麻繊維及びエニシダ繊維の土壌における生分解評価
参考文献[5]に記載の長期試験の例を,次に示す。
植種源:農業用土壌(500 g,<2 mm)
試験材料:セルロース(5 g),小麦グルテン(5 g),亜麻繊維(2 g),エニシダ繊維(2 g)
試験期間:セルロース:2年,小麦グルテン,亜麻繊維,エニシダ繊維:1年
試験温度:20 ℃±2 ℃
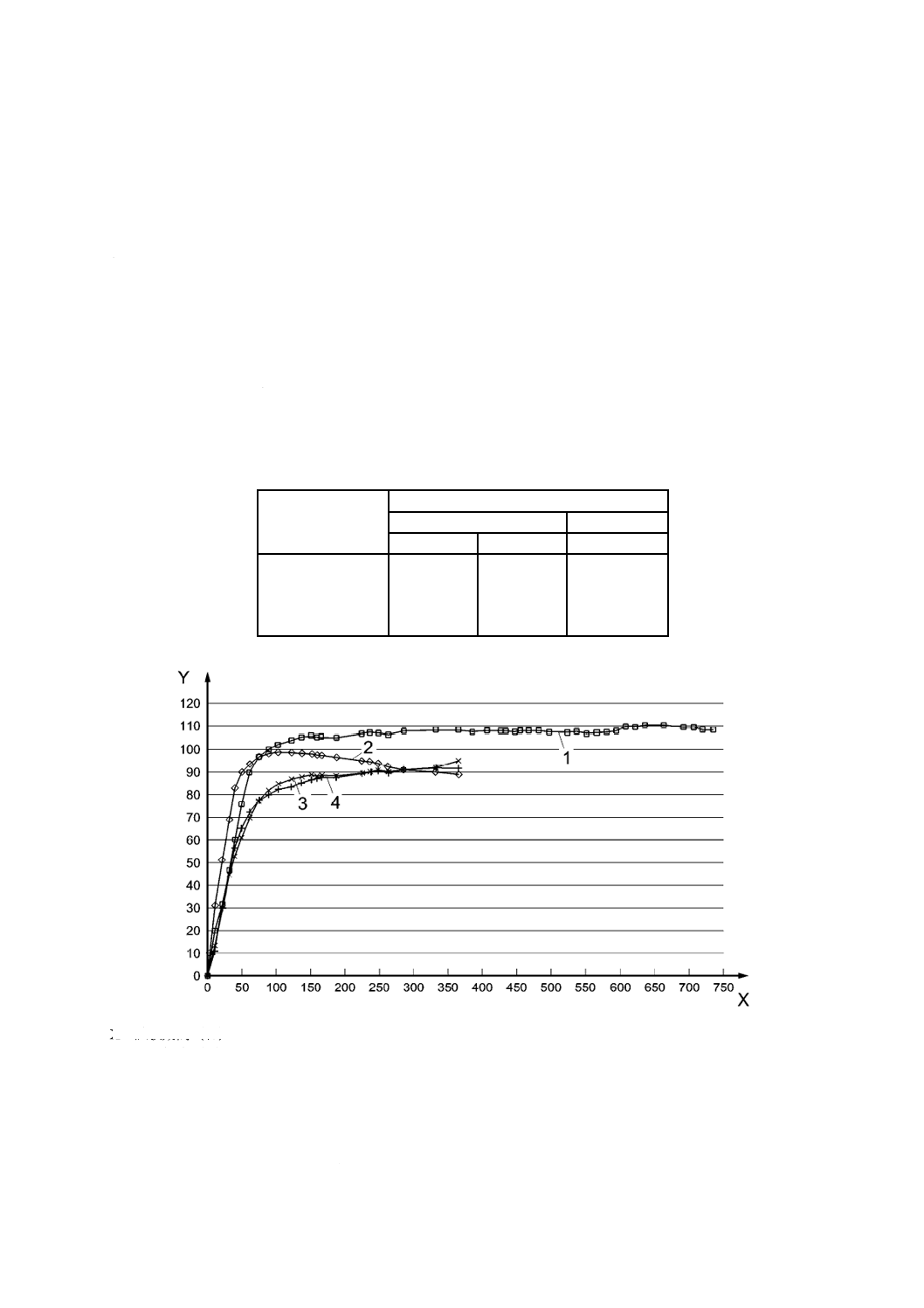
結果:(試験数2):表F.1及び図F.1を参照
表F.1−生分解度(試験例1)
試験項目
生分解度(%)
1年
2年
平均値
標準偏差
試験数1
セルロース
108.3
2.8
108.5
小麦グルテン
89.2
2.6
−
亜麻繊維
94.8
6.8
−
エニシダ繊維
91.8
5.6
−
X 試験期間(日)
Y 生分解度(%)
1 セルロース
2 小麦グルテン
3 亜麻繊維
4 エニシダ繊維
図F.1−セルロース,小麦グルテン,亜麻繊維及びエニシダ繊維の土壌における生分解評価
19
K 6955:2017
F.2
セルロース,カバ(樺)の葉,カシ(樫)の葉及び松葉の土壌中の生分解評価
参考文献[6]に記載の長期試験の例を,次に示す。
植種源:農業用土壌(500 g,<2 mm)
試料:セルロース(1 g),カバ(樺)の葉(1 g),カシ(樫)の葉(1 g),松葉(1 g)
測定期間:1年
測定温度:20 ℃±2 ℃
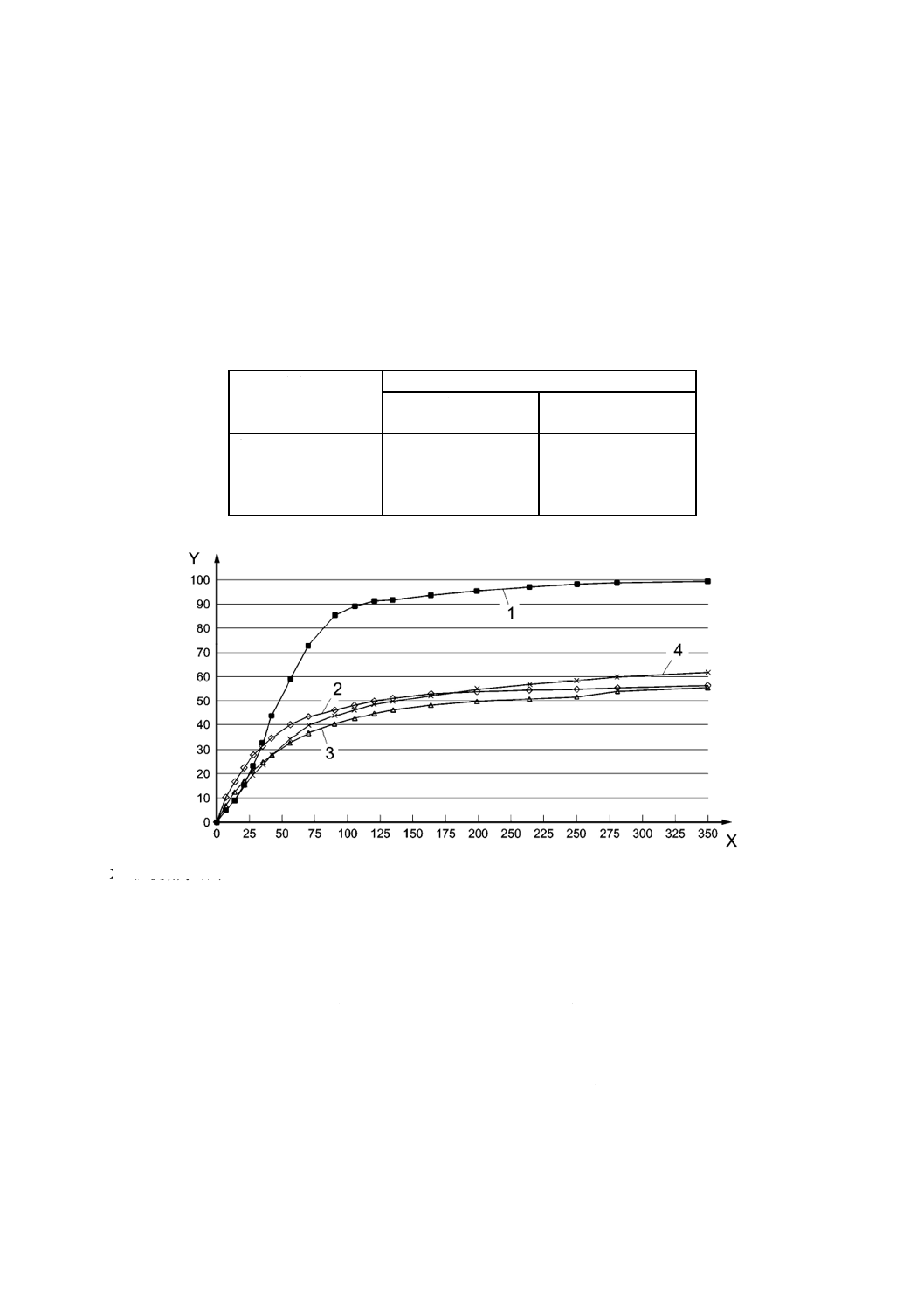
結果:表F.2及び図F.2を参照
表F.2−1年後の生分解度(試験例2)
試験項目
生分解度(%)
絶対値
セルロースに対する
相対値
セルロース
99.7
100.0
カバ(樺)の葉
56.2
56.4
カシ(樫)の葉
55.8
56.0
松葉
61.9
62.1
X 試験期間(日)
Y 生分解度(%)
1 セルロース
2 カバ(樺)の葉
3 カシ(樫)の葉
4 松葉
図F.2−セルロース,カバ(樺)の葉,カシ(樫)の葉及び松葉の土壌中の生分解評価
F.3
セルロース及びわらの土壌中の生分解評価
植種源:農業用土壌1容に対して森林の土壌2容の混合物(500 g,<2 mm)
試験試料:セルロース(1 g),わら(1 g)
試験期間:270日
測定温度:20 ℃±2 ℃
20
K 6955:2017
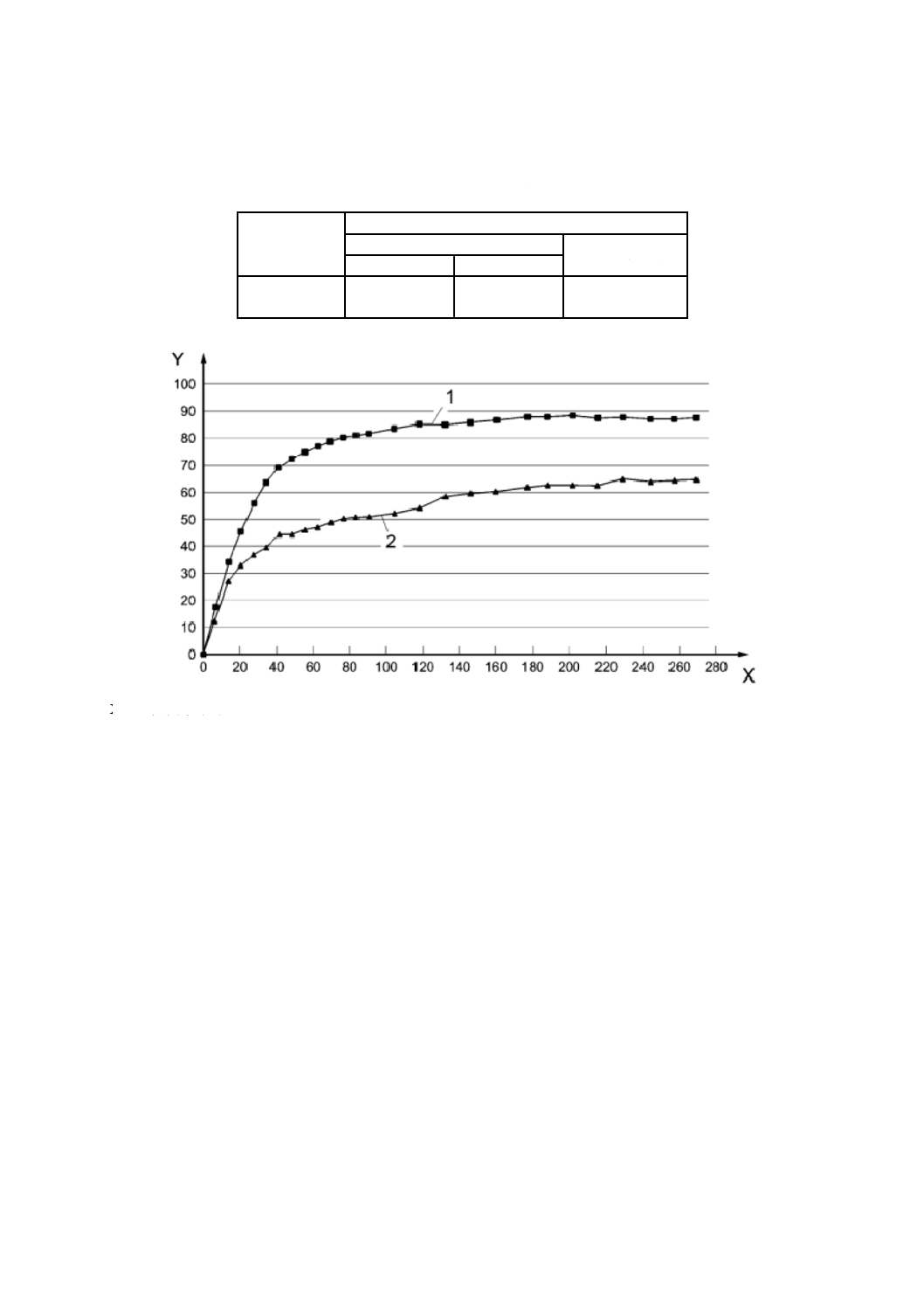
結果:(試験数2):表F.3及び図F.3参照
表F.3−生分解度(試験例3)
試験項目
生分解度(%)
絶対値
セルロースに
対する相対値
平均値
標準偏差
セルロース
89.8
1.9
100.0
わら
66.4
0.0
74.0
X 試験期間(日)
Y 生分解度(%)
1 セルロース
2 わら
図F.3−セルロース及びわらの生分解度の評価
21
K 6955:2017
附属書G
(参考)
ラウンドロビン試験
天然土壌の代わりに基準土壌使用の可能性を検証するため,ラウンドロビン試験が2009年に実施された。
その基準土壌の組成を8.3.2に示す。この基準土壌中の砂及び粘土は土壌に土性を与え,天然土壌は微生
物を提供し,さらに,完熟堆肥は有機物と追加の微生物とを提供する。六つの異なる試験機関が,ラウン
ドロビン試験に参加した。それぞれの試験機関は,“天然土壌”として使用するため,また,“基準土壌”
の植種源として,個々に土壌を収集した。試験材料は,微結晶セルロースの対照材料(RM)とでん(澱)
粉/ポリブチレンアジペート−ブチレンテレフタレート共重合体とのコンパウンド試験材料(TM)とした。
ラウンドロビン試験を実施するため,試験機関は市販土壌,天然土壌又は異なる土壌の混合物(例えば,
森林の土壌,牧草地の土壌及び庭の土壌の混合物)を使用することが認められた。
高濃度の試験材料(湿った土壌800 g当たり10 g)を使用するとき,表2に示される塩類を混合して,
天然土壌は,肥沃に調整された。
全ての試験機関は,赤外分析計,中和滴定,及びJIS K 6953-2に従った二酸化炭素の重量測定のいずれ
かで,発生二酸化炭素の量を測定して,土壌中の生分解性を測定した。温度は,20 ℃〜28 ℃の間とした。
二つの試験機関は,2種類又は3種類の土壌の混合物を使用した。二つの試験機関は,畑から集めた土壌
を使用した。他の二つの試験機関は,市販土壌を使用した。
最終の生分解度百分率値を,表G.1に示す。
22
K 6955:2017
表G.1−ラウンドロビン試験の結果
参加者
植種源
装置
試験
日数
TMの生分
解度(%)
標準偏差
RMの生分
解度(%)
標準偏差
TMの相対的
生分度(%)a)
1
天然土壌 CO2を含まない
空気の供給装置
120
33.0 b)
2.16
70.3
0.31
47.0
1
基準土壌 CO2を含まない
空気の供給装置
120
11.8
1.17
59.0
0.5
20.1
2
天然土壌 ASTM D5988-03
の7.2.2参照
120
16.9 b)
2.9
63.8 b)
1.4
26.5
2
基準土壌 ASTM D5988-03
の7.2.2参照
120
23.8 b)
0.9
70.4 b)
3.4
33.8
2
天然土壌 CO2を含まない
空気の供給装置
120
21.9 b)
0.9
69.9 b)
1.6
31.3
2
天然土壌 ASTM D5988-03
の7.2.2参照
120
18.8 b)
0.2
61.1 b)
0.8
30.8
2
天然土壌 ASTM D5988-03
の7.2.2参照
120
19.9 b)
1.1
81.6 b)
2.8
24.4
3
天然土壌 CO2を含まない
空気の供給装置
182
61
1
72 c)
3.5
83.6
3
基準土壌 CO2を含まない
空気の供給装置
182
26
4
46
4.5
56.5
4
天然土壌 CO2を含まない
空気の供給装置
134
59.3
2.3
60.9
1.9
97.3
4
基準土壌 CO2を含まない
空気の供給装置
134
70.8
1.78
70.1
0.0
101.0
4
天然土壌 CO2を含まない
空気の供給装置
115
31.1
4.5
56.6
4.3
54.9
4
基準土壌 CO2を含まない
空気の供給装置
115
37.2
6.9
64.5
5.1
57.7
5
天然土壌 CO2を含まない
空気の供給装置
70
92.6
3.2
86.5
9.0
107.1
5
基準土壌 CO2を含まない
空気の供給装置
60
74.1 b)
0.5
77.0 b)
6.6
96.2
6
天然土壌 CO2を含まない
空気の供給装置
118
21.5 b)
4.9
104 b)
2.6
20.7
6
基準土壌 CO2を含まない
空気の供給装置
118
26 b)
4.2
107 b)
1.4
24.3
注a) TMの相対的生分解度=(TMの生分解度/RMの生分解度)×100
b) まだ定常期に到達しない段階
c) まだ高いCO2発生段階
異なる試験機関で得られた天然土壌と基準土壌との生分解度値の平均を,表G.2に示す。6番目の試験
機関は,対照材料の生分解度が共に100 %を超え,また,定常期に到達していないので除外した。
23
K 6955:2017
表G.2−平均生分解度
単位 %
試料
天然土壌
基準土壌
試験材料(TM)
39.39±26.03
40.62±25.96
対照材料(RM)
69.19±9.91
64.50±10.91
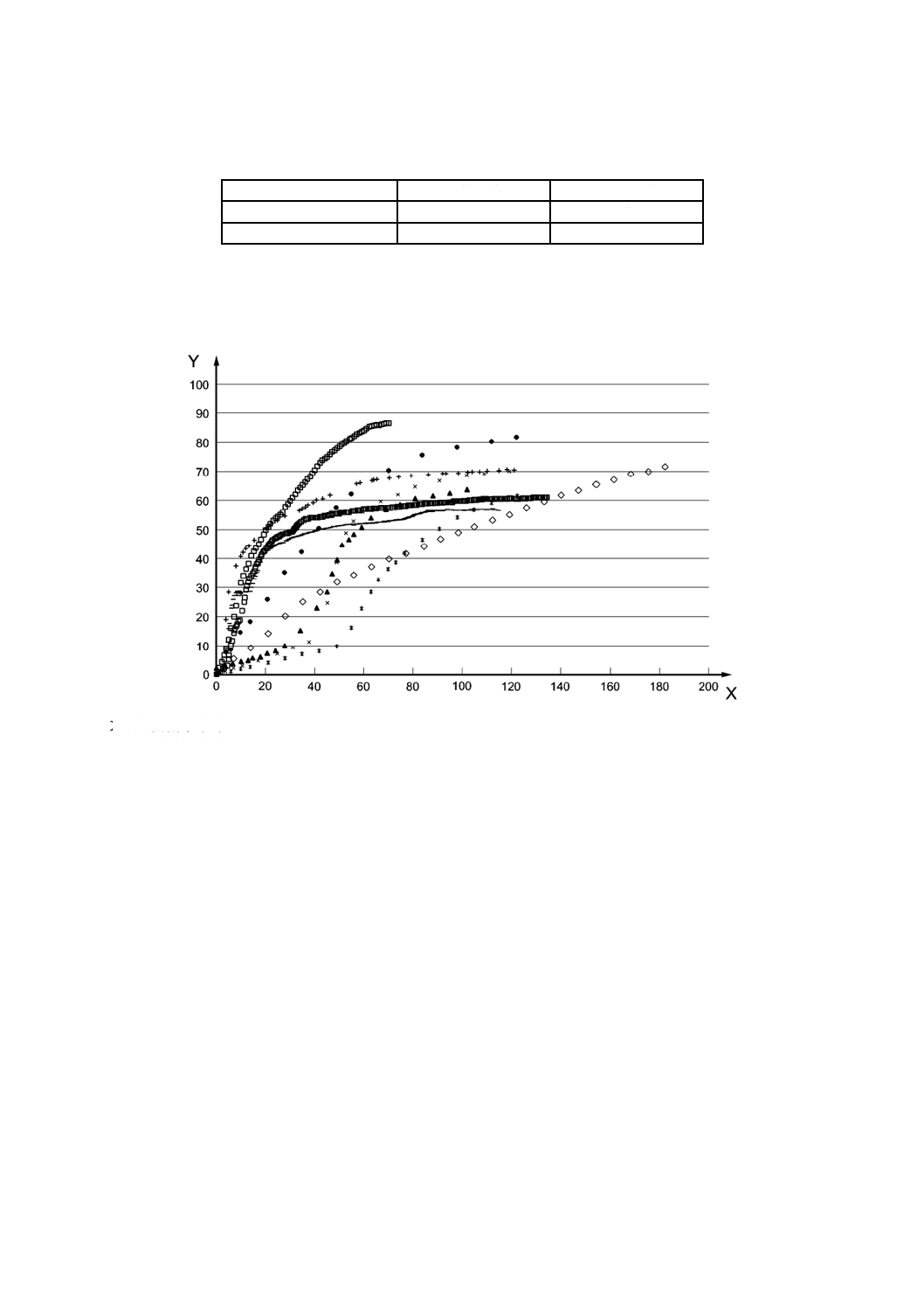
図G.1及び図G.2は,幾つかの試験機関による,天然土壌と基準土壌中との対照材料の生分解度曲線を
示す。
X 試験期間(日)
Y 生分解度(%)
図G.1−天然土壌における微結晶セルロースの生分解度の評価
24
K 6955:2017
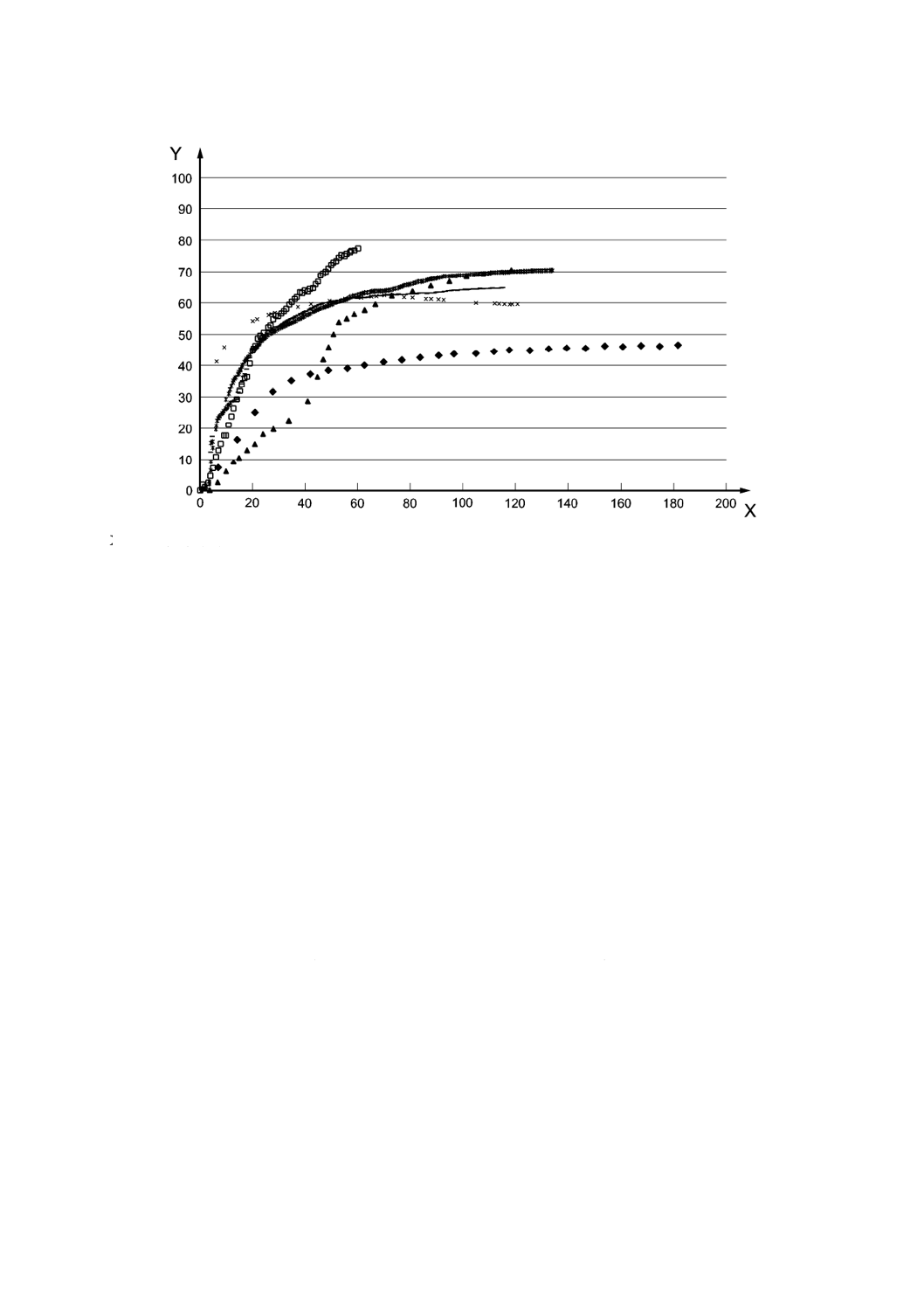
X 試験期間(日)
Y 生分解度(%)
図G.2−基準土壌における微結晶セルロースの生分解度の評価
天然土壌における対照材料(微結晶セルロース)の生分解度の試験機関間の変動は,大きくない。セル
ロースは,試験条件によって生分解性が大きく影響される材料ではないと思われる。一方,試験材料は大
きな変動を示していることから,試験条件に対してもっと敏感であることが考えられる。このことは,異
なる土壌を使用しているからなのか,又は他の主要な原因,例えば各試験機関における試験条件(温度,
通期速度,試料濃度などの差異)のばらつきが影響しているかは,原因の究明が困難である。
表G.2に示す生分解度の標準偏差から,天然土壌で接種された基準土壌の調製は,試験機関のばらつき
には影響を与えていないと考えられる。
基準土壌の生分解度の平均値は,天然土壌の生分解度とは,本質的に異ならない。この天然土壌が基準
土壌の成分として使用される場合には,天然土壌の生物学的因子(微生物の母集団)が,重要な要因と考
えられる。
附属書Eで示すように,最終の物質収支を定量するために,試験の終了時に試験化合物を取り出すため
には,大量の試験材料で試験を始めることが必要である。
一般的に,標準的な土性と粒度とをもつ基質を使用する場合は,基準土壌が試験手順の標準化に役立つ。
特に,大量の土壌を使用する場合は,都合がよい。
25
K 6955:2017
参考文献 [1] ISO 8192,Water quality−Test for inhibition of oxygen consumption by activated sludge
[2] ISO 8245,Water quality−Guidelines for the determination of total organic carbon (TOC) and
dissolved organic carbon (DOC)
[3] ISO 11266,Soil quality−Guidance on laboratory testing for biodegradation of organic chemicals
in soil under aerobic conditions
[4] ASTM D5988-03,Standard Test Method for Determining Aerobic Biodegradation in Soil of Plastic
Materials or Residual Plastic Materials After Composting
[5] EU project FAIR-CT98-3919,New functional biopolymer-natural fibre-composites from
agricultural resources
[6] EU project AIR2-CT93-1099,Biodegradability of bioplastics: prenormative research, biorecycling
and ecological impacts
26
K 6955:2017
附属書JA
(参考)
JISと対応国際規格との対比表
JIS K 6955:2017 プラスチック−呼吸計を用いた酸素消費量又は発生した二酸
化炭素量の測定による土壌中でのプラスチックの好気的究極生分解度の求め方
ISO 17556:2012,Plastics−Determination of the ultimate aerobic biodegradability of
plastic materials in soil by measuring the oxygen demand in a respiormeter or the amount
of carbon dioxide evolved
(I)JISの規定
(II)
国際規
格番号
(III)国際規格の規定
(IV)JISと国際規格との技術的差異の
箇条ごとの評価及びその内容
(V)JISと国際規格との技術的差異の理由
及び今後の対策
箇条番号
及び題名
内容
箇条
番号
内容
箇条ごと
の評価
技術的差異の内容
2
JIS Z 8802
2
記載なし。
追加
技術的差異はない。
7.4における説明の引用規格。
対応国際規格を改正するときに盛り込む。
3.2
“試験材料1 mg又
は1 g”を“試験土
壌1 kg”に変更した。
3.2
“試験材料1 mg又は
1 g”と記載されている。
変更
技術的差異がある。
ISOに修正を申し出る。
4
試験期間を“長くと
も2年”に変更した。
4
試験は,生分解が定常状
態に到達するか,長くと
も6か月を経過したと
き,終了する。
変更
技術的差異がある。
対応国際規格作成時に,本来2年とすべき
ところ誤って6か月とした。
ISOに修正を申し出る。
7.2.1
例えば,500 ml程度
の三角フラスコ又
は瓶
7.2.1
例えば,フラスコ又は瓶 追加
技術的差異はない。
使用するフラスコや瓶の大きさの情報を
提示し,使用者の利便性を図った。
対応国際規格を改正するときに盛り込む。
7.3
0.1 mg単位まで測定
可能な化学天びん
(秤)。
7.3
説明文なし。
追加
技術的差異はない。
利用者の利便性を図るため,情報を提示し
た。
対応国際規格を改正するときに盛り込む。
7.4
JIS Z 8802に従い,
測定を行う。
7.4
説明文なし。
追加
技術的差異はない。
利用者の利便性を図るため,情報を提示し
た。
対応国際規格を改正するときに盛り込む。
8.3.2
表2 塩類の成分の
化合物名と化学式
を併記した。
8.3.2
表2 化合物名と化学式
が混在。
追加
技術的差異はない。
利用者にとって分かりやすくするため。
対応国際規格を改正するときに盛り込む。
3
K
6
9
5
5
:
2
0
1
7
27
K 6955:2017
(I)JISの規定
(II)
国際規
格番号
(III)国際規格の規定
(IV)JISと国際規格との技術的差異の
箇条ごとの評価及びその内容
(V)JISと国際規格との技術的差異の理由
及び今後の対策
箇条番号
及び題名
内容
箇条
番号
内容
箇条ごと
の評価
技術的差異の内容
9.1.1
生分解度百分率を
求める二つの式を
一つの式にまとめ
た。
9.1.1
(1)式,(2)式を用いてい
る。
変更
技術的差異はない。
利用者にとって分かりやすくするため。
対応国際規格を改正するときに盛り込む。
9.2
3個のフラスコ
9.2
2個のフラスコ
変更
技術的差異がある。
対応国際規格作成時に,本来“3個”とす
べきところを誤って“2個”とした。
ISOに修正を申し出る。
JISと国際規格との対応の程度の全体評価:ISO 17556:2012,MOD
注記1 箇条ごとの評価欄の用語の意味は,次による。
− 追加 ················ 国際規格にない規定項目又は規定内容を追加している。
− 変更 ················ 国際規格の規定内容を変更している。
注記2 JISと国際規格との対応の程度の全体評価欄の記号の意味は,次による。
− MOD ··············· 国際規格を修正している。
3
K
6
9
5
5
:
2
0
1
7













