K 3810-1:2003
(1)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
まえがき
この規格は,工業標準化法第14条によって準用する第12条第1項の規定に基づき,財団法人バイオイ
ンダストリー協会 (JBA)/財団法人日本規格協会 (JSA) から,工業標準原案を具して日本工業規格を改正
すべきとの申出があり,日本工業標準調査会の審議を経て,経済産業大臣が改正した日本工業規格である。
これによって,JIS K 3810-1 : 1997は改正され,この規格に置き換えられる。
JIS K 3810の規格群には,次に示す部編成がある。
JIS K 3810-1 第1部:培養による直接検出法
JIS K 3810-2 第2部:DNA蛍光染色による間接検出法
JIS K 3810-3 第3部:二段階PCRによる検出法
K 3810-1:2003
(2)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
目 次
ページ
1. 適用範囲 ························································································································ 1
2. 引用規格 ························································································································ 1
3. 定義 ······························································································································ 1
4. 陽性対照マイコプラズマ ··································································································· 1
5. 試験方法 ························································································································ 1
5.1 試薬 ···························································································································· 1
5.2 装置及び器具 ················································································································ 2
5.3 完全培地の調製 ············································································································· 2
5.4 検体試料の調製法 ·········································································································· 3
5.5 マイコプラズマの接種及び培養方法 ··················································································· 3
5.6 マイコプラズマの判定 ···································································································· 3
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
日本工業規格 JIS
K 3810-1:2003
マイコプラズマの検出法−
第1部:培養による直接検出法
Mycoplasma detection methods-
Part 1: Microbiological cultivation assay
1. 適用範囲 この規格は,細胞培養及び細胞培養に用いられる試薬類並びに細胞培養によって生産され
た製品からマイコプラズマを分離培養して検出する方法について規定する。
2. 引用規格 次に掲げる規格は,この規格に引用されることによって,この規格の規定の一部を構成す
る。これらの引用規格は,その最新版(追補を含む。)を適用する。
JIS K 0950 プラスチック製滅菌シャーレ
JIS K 3600 バイオテクノロジー用語
JIS K 3604 組織培養用培地(最小必須培地)
JIS K 3605 高圧蒸気滅菌操作通則
JIS Z 8802 pH測定方法
3. 定義 この規格で用いる主な用語の定義は,JIS K 3600によるほか,次による。
a) 蒸留水 JIS K 3604に規定する純水。
b) マイコプラズマ 無細胞培地で発育可能な無細胞壁原核生物。DNAをゲノムとしてもつ。
c) コロニー形成単位 [Colony Forming Unit (CFU) ] 寒天培地上で1個のコロニーを形成する試料1 ml
中のマイコプラズマの量。
d) PPLO寒天粉末 マイコプラズマの古い呼称であるPleuropneumonia-like Organismに由来するPPLOを
培養するための基礎培地成分。寒天を含まないものはPPLO粉末と呼ばれ,ウシ心臓抽出物,ペプト
ン,塩化ナトリウムなどを含む。
4. 陽性対照マイコプラズマ 陽性対照として用いる,Mycoplasma hyorhinis(ATCC 29052又はIFO 14858)
及びMycoplasma arginini(ATCC 23838又はIFO 14476)。
5. 試験方法
5.1
試薬
5.1.1
イースト・エキストラクト (25 %) マイコプラズマ培養のためには自家調製したものが最も優れ
ている。これとほぼ同等の性能をもつ市販イースト抽出液を用いてもよい。粉末のイースト抽出物を用い
たものは培養性能が多少劣るので,初代分離培養のときの陰性結果の判定を複雑にする場合がある。

2
K 3810-1:2003
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
イースト・エキストラクト (25 %) の自家調整は,次の方法による。
a) 蒸留水1 Lに製パン用ドライイースト250 gを溶かす。
b) 沸騰水中で30分間浸出し,水冷する。
c) 冷却後,14 000×g(実効回転半径12 cmの遠心機で10 000 rpm),30分間遠心し,上澄み液を採取す
る。
d) 水酸化ナトリウム溶液 (0.5 mol/L) でJIS Z 8802に規定するpH計を用いてpH7.8に調節する。
e) 孔径0.2 μm又は0.45 μmフィルタを取り付けたろ過器で除菌する。
f)
ろ過液は使用時まで−20 ℃以下で保存する。
5.1.2
酢酸タリウム溶液 (2.5 %) 純度95 %以上の酢酸タリウム25 gを蒸留水1 Lに溶かし,JIS K 3605
に規定する高圧蒸気滅菌装置を用いて120 ℃,15分間滅菌後,室温に保存する。
警告 酢酸タリウムは潮解性無色結晶の劇物のため取り扱いには注意をようする。
5.1.3
ペニシリン ペニシリンGカリウムを蒸留水で10万単位/mlに調製し,孔径0.2 μm又は0.45 μm
のメンブランフィルタを用いてろ過除菌後,凍結保存する。
警告 ペニシリンは安易に耐性菌を生み出さないよう使い方には注意をようする。
5.1.4
ウマ血清 市販の非加熱ウマ血清を用いる。
5.2
装置及び器具
5.2.1
培地容器 寒天培地では,JIS K 0950に規定する直径4.5 cmのプラスチック製滅菌シャーレを用
いる。二層培地では,直径8×100 mmの滅菌したプラスチック製密栓付試験管を用いる。
a) インキュベータ 温度37±0.5 ℃に調節できるもの。
b) ろ過滅菌器 孔径0.45 μmでろ過し,更に孔径0.2 μmのメンブランフィルタでろ過できる構造をもつ
もの。
c) 高圧蒸気滅菌器 JIS K 3605に規定するもの。
d) 倒立顕微鏡 10〜100倍に拡大できるもの。
e) クリーンベンチ JIS K 3604に規定するもの。
5.3
完全培地の調製
5.3.1
完全マイコプラズマ寒天培地 培地組成を表1に示す。
表 1 完全マイコプラズマ寒天培地
成分
添加量
(A)
PPLO寒天粉末 (1)
蒸留水
2.4 g
70 ml
(B)
ウマ血清(非加熱)
25 %イースト・エキストラクト
酢酸タリウム溶液 (25 g/L)
10万単位/mlペニシリンGカリウム
20 ml
10 ml
1 ml
1 ml
注(1) PPLO寒天粉末に蒸留水を加え,121 ℃で15分間煮沸し,寒天を溶かす。
55 ℃に冷却後,(B) を無菌的に加える。
PPLO寒天培地は乾燥を防ぐため,ポリ塩化ビニル袋,缶などに入れて冷蔵庫に
保存する。
5.3.2
完全マイコプラズマ液体培地 培地組成を表2に示す。
なお,蒸留水は,121 ℃で15分間滅菌後,放冷してから表2の組成を無菌的に加える。
3
K 3810-1:2003
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
表 2 完全マイコプラズマ液体培地
成分
添加量
PPLO粉末 (2)(クリスタルバイオレットを含まない。)
蒸留水
ウマ血清(非加熱)
25 %イースト・エキストラクト
酢酸タリウム溶液 (25 g/L)
10万単位/mlペニシリンGカリウム
L-アルギニン塩酸塩 (100 g/L)
D (+)-グルコース (100 g/L)
フェノールレッド (10 g/L)
2.1 g
61 ml
20 ml
10 ml
1 ml
1 ml
2 ml (2) (0.2 %)
5 ml (2) (0.5 %)
0.2 ml (2) (0.002 %)
注(2) PPLO粉末に蒸留水61 mlを加え,121 ℃で15分間高圧滅菌する。室温に冷却後,
残りの成分を無菌的に加え,全量を100 mlにする。
5.3.3
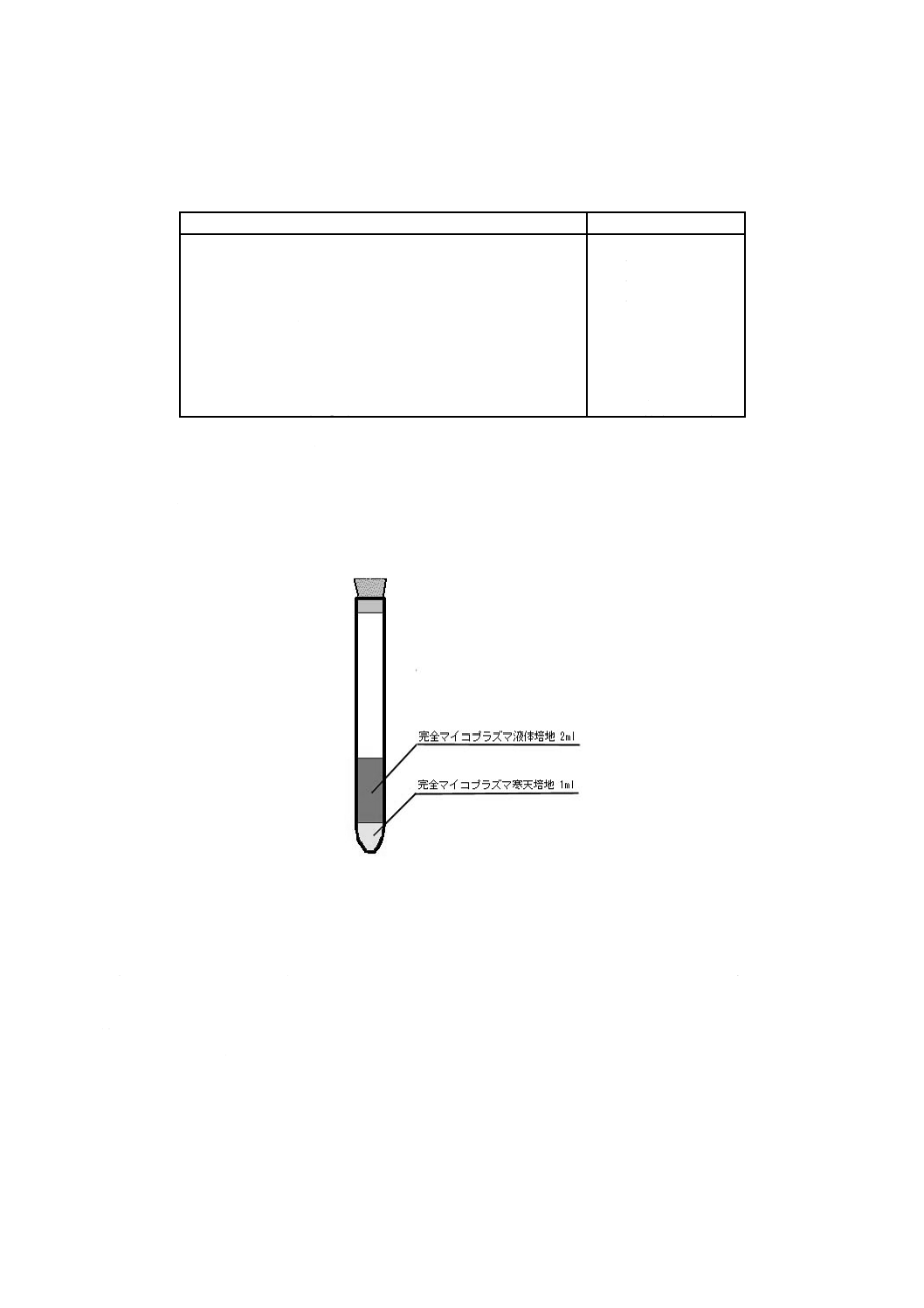
二層培地 二層培地を図1に示す。
a) 小試験管に完全マイコプラズマ寒天培地1 mlを入れて固める。
b) 完全マイコプラズマ液体培地2 mlを重層する。
図 1 二層培地
5.4
検体試料の調製法 検体が液体又はサスペンジョンの場合はそのまま,若しくはマイコプラズマ液
体培地によって2倍段階希釈を行い,それぞれの希釈段階のものを接種材料とする。また,検体が固体の
場合は,マイコプラズマ液体培地とともにホモゲナイズしてから,サスペンジョンと同じ取扱いをする。
5.5
マイコプラズマの接種及び培養方法 マイコプラズマの培養は,寒天培地及び二層培地に同時に接
種する。
a) 寒天培地 直径4.5 cmのプラスチック製滅菌シャーレに対し,ピペットを用いて検体0.1 mlを接種す
る。密閉できるプラスチック製又は金属製の箱に入れ,蒸留水を含ませた脱脂綿を小容器に入れ接種
培地とともに箱内に入れて湿度を保った状態で,37±1 ℃で3〜20日間培養する。
b) 二層培地 二層培地に検体0.1 mlを接種し,37±1 ℃で培養する。接種後7日目及び14日目に液層
から0.1 mlをとって寒天培地に接種する。寒天培地を用いた培養法と同様に14日間培養する。
4
K 3810-1:2003
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
5.6
マイコプラズマの判定 マイコプラズマの判定は,次による。
a) 寒天培地 接種の3〜20日後に20〜40倍の倒立顕微鏡下でコロニーの有無を観察する。マイコプラズ
マのコロニーは,コロニーの中心にニプルを形成し,全体として直径0.1〜0.5 mm,目玉焼き状の形
態を示す。
b) 二層培地 接種の14日後に,培地の混濁の有無,マイクロコロニーの出現の有無及び培地のpHの変
化による色調の変化を観察する。
c) 二層培地の液層 0.1 mlを接種した寒天培地は,接種した14日後にコロニーを確認する。

