K 3704:2008
(1)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
まえがき
この規格は,工業標準化法第12条第1項の規定に基づき,財団法人バイオインダストリー協会(JBA)及
び財団法人日本規格協会(JSA)から,工業標準原案を具して日本工業規格を制定すべきとの申出があり,日
本工業標準調査会の審議を経て,経済産業大臣が制定した日本工業規格である。
この規格は,著作権法で保護対象となっている著作物である。
この規格の一部が,特許権,出願公開後の特許出願,実用新案権又は出願公開後の実用新案登録出願に
抵触する可能性があることに注意を喚起する。経済産業大臣及び日本工業標準調査会は,このような特許
権,出願公開後の特許出願,実用新案権又は出願公開後の実用新案登録出願に係る確認について,責任は
もたない。
K 3704:2008
(2)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
目 次
ページ
序文 ··································································································································· 1
1. 適用範囲 ························································································································ 1
2. 引用規格 ························································································································ 1
3. 定義 ······························································································································ 2
4. 一般原則 ························································································································ 2
5. 培地,試薬及び抗血清 ······································································································ 2
5.1 増菌培地(ノボビオシン添加変法トリプトソイブロス培地) ·················································· 2
5.2 第一選択分離培地(セフィキシム−亜テルル酸−ソルビトール添加マッコンキー寒天培地) ········ 3
5.3 第二選択分離培地 ·········································································································· 4
5.4 普通寒天培地 ················································································································ 4
5.5 トリプトン−トリプトファン培地······················································································ 5
5.6 コバックのインドール試薬······························································································· 5
5.7 抗大腸菌O157免疫磁気ビーズ ························································································· 5
5.8 洗浄用緩衝液(変法りん酸緩衝液) ··················································································· 5
5.9 生理的食塩水 ················································································································ 6
5.10 大腸菌O157抗血清 ······································································································· 6
6. 装置及びガラス器具 ········································································································· 6
6.1 オーブン及びオートクレーブ···························································································· 6
6.2 乾燥器又はインキュベータ(25〜50 °C) ········································································· 6
6.3 インキュベータ(37±1 °C) ···························································································· 6
6.4 インキュベータ(41.5±1 °C) ·························································································· 6
6.5 水浴 ···························································································································· 6
6.6 pH計··························································································································· 6
6.7 試験管,フラスコ及び瓶 ································································································· 6
6.8 メスシリンダー ············································································································· 6
6.9 吐出式メスピペット ······································································································· 6
6.10 白金耳及び白金線 ········································································································· 6
6.11 ピペッター ·················································································································· 6
6.12 磁石付ラックを備えた磁気分離装置 ················································································· 6
6.13 エッペンドルフ形プラスチックチューブ ··········································································· 6
6.14 ロータリ−ミキサー(風車形の血液試料用ミキサー) ························································· 6
6.15 シャーレ ····················································································································· 6
6.16 かき混ぜ機(ボルテックスミキサー) ·············································································· 6
7. 試料の採取 ····················································································································· 6
8. 試料の調製 ····················································································································· 7
K 3704:2008 目次
(3)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
ページ
9. 実施手順 ························································································································ 7
9.1 試料及び試料懸濁液(1次希釈試料液) ············································································· 7
9.2 増菌 ···························································································································· 7
9.3 免疫磁気分離法(IMS) ·································································································· 7
9.4 選択分離培地への接種と大腸菌O157コロニーの同定 ··························································· 7
9.5 確定 ···························································································································· 8
9.6 追加解析 ······················································································································ 8
10. 精度評価 ······················································································································ 8
10.1 精度評価用菌株 ············································································································ 8
10.2 培養方法 ····················································································································· 9
11. 結果の表記···················································································································· 9
12. 試験報告書 ··················································································································· 9
附属書A(規定)実施手順説明図 ··························································································· 10
附属書1(参考)JISと対応する国際規格との対比表 ·································································· 12
K 3704:2008
(4)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
白 紙
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
日本工業規格 JIS
K 3704:2008
培地の試験方法−大腸菌用検出培地
Culture media-Detection of Escherichia coli O 157
序文 この規格は,2001年に第1版として発行されたISO 16654:2001,Microbiology of food and animal
feeding stuffs−Horizontal method for the detection of Escherichia coli O157を翻訳し,技術的内容を変更して作
成した日本工業規格である。
なお,この規格で点線の下線を施してある箇所は,原国際規格を変更している事項である。変更の一覧
表をその説明を付けて,附属書1(参考)に示す。
警告 大腸菌O157は,生命を脅かす重とく(篤)な疾患を引き起こすおそれがあり,少量で感染する。
試験室内感染も報告されている。試験担当者の健康を守るために,この検出方法はすべて,習熟
した担当者だけがGLP[good laboratory practice(動物実験実施基準)]に準拠して実施すること
が必す(須)であり,かつ,封じ込め施設内で実施することが望ましい。さらに,関連する健康
及び安全に関する国内法規を遵守し,あらゆる感染性物質の処分は慎重に行う。
1. 適用範囲 この規格は,大腸菌O157の検出を目的とする培地試験の方法について規定する。
備考 この規格の対応国際規格を,次に示す。
なお,対応の程度を表す記号は,ISO/IEC Guide 21に基づき,IDT(一致している),MOD
(修正している),NEQ(同等でない)とする。
ISO 16654:2001,Microbiology of food and animal feeding stuffs−Horizontal method for the detection
of Escherichia coli O157 (MOD)
2. 引用規格 次に掲げる規格は,この規格に引用されることによって,この規格の規定の一部を構成す
る。これらの引用規格は,その最新版(追補を含む。)を適用する。
JIS K 3701 培地の試験方法−通則
備考 ISO 7218:1996,Microbiology of food and animal feeding stuffs−General rules for microbiological
examinations及びAMENDMENT 1:2001からの引用事項は,この規格の該当事項と同等であ
る。
JIS K 3702 培地の試験方法−試料懸濁液及び希釈系列の調製方法
備考 ISO 6887-1 Microbiology of food and animal feeding stuffs−Preparation of test samples, initial
suspension and decimal dilutions for microbiological examination−Part 1: General rules for the
preparation of the initial suspension and decimal dilutionsからの引用事項は,この規格の該当事
項と同等である。
JIS K 8008 生化学試薬通則

2
K 3704:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
JIS K 8121 塩化カリウム(試薬)
JIS K 8150 塩化ナトリウム(試薬)
JIS K 8180 塩酸(試薬)
JIS K 8263 寒天(試薬)
JIS K 8294 クリスタルバイオレット(試薬)
JIS K 8496 p−ジメチルアミノベンズアルデヒド(試薬)
JIS K 8676 L−トリプトファン(試薬)
JIS K 8824 D(+)−グルコース(試薬)
JIS K 9007 りん酸二水素カリウム(試薬)
JIS K 9017 りん酸水素二カリウム(試薬)
JIS K 9020 りん酸水素二ナトリウム(試薬)
JIS Z 8802 pH測定方法
3. 定義 この規格で用いる主な用語の定義は,次による。
3.1
大腸菌O157(E. coli O157) この規格で用いる接種培地上に定形コロニーを形成し,かつ,インド
ール産生能をもち,大腸菌O157抗原の抗血清に対し特異的凝集反応を示す微生物。
備考 大腸菌O157のソルビトール陽性株は,セフィキシム−亜テルル酸−ソルビトール添加マッコ
ンキー寒天培地(5.2)では検出されない。インドール陰性変異株も存在する。
3.2
精製水 JIS K 8008の3.2(水)に規定するA2の水。
備考 これを超える精製度のものを使用することに関して制限はしない。
3.3
塩酸 JIS K 8180に規定するもの。
4. 一般原則 大腸菌O157の検出には,連続する4段階の操作が必要である(附属書A参照)。
a) 増菌 試料をホモジナイザーで均一化して,ノボビオシンを添加した変法トリプトソイブロス培地に
加え,41.5±1 ℃で6時間培養し,更に12〜18時間培養して増菌する。
b) 分離及び濃縮 大腸菌O157に対する抗体を固定化した免疫磁気ビーズを用いて,菌を分離及び濃縮
する。
c) 単離 菌が接着した免疫磁気ビーズを,セフィキシム−亜テルル酸−ソルビトール添加マッコンキー
寒天培地及びその他の選択分離寒天培地上で培養し,菌を単離する。
d) 確定 セフィキシム−亜テルル酸−ソルビトール添加マッコンキー寒天培地上に出現したソルビトー
ル陰性のコロニー及びこのほかに用いた選択分離培地上に発育した大腸菌O157定形コロニーについ
て,インドール産生反応及び大腸菌O157抗血清を用いた凝集反応で確定する。
備考 陽性菌株のより詳細な解析が必要であれば指定試験施設に転送する。
5. 培地,試薬及び抗血清 (JIS K 3701参照)
5.1
増菌培地(ノボビオシン添加変法トリプトソイブロス培地)(参考文献1.参照)
5.1.1
変法トリプトソイブロス培地

3
K 3704:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
5.1.1.1
組成
表 1 変法トリプトソイブロス培地の組成
カゼインペプトン
17.0 g
ソイペプトン
3.0 g
D(+)−グルコース (JIS K 8824)
2.5 g
胆汁酸塩
1.5 g
塩化ナトリウム (JIS K 8150)
5.0 g
りん酸水素二カリウム(K2HPO4) (JIS K 9017)
4.0 g
精製水
1 000 mL
5.1.1.2
調製 各成分又は粉末培地を精製水に溶かす。必要に応じて加熱して溶かし,滅菌後25 ℃でpH
7.4 ± 0.2になるように滅菌前にpH調節を行う。フラスコ又は瓶(6.7)に適量ずつ培地をはかりとる。オ
ートクレーブ(6.1)を用いて121 ℃で15分間加熱し,滅菌する。
5.1.2
ノボビオシン溶液
5.1.2.1
組成
表 2 ノボビオシン溶液の組成
ノボビオシン
0.45 g
精製水
100 mL
5.1.2.2
調製 ノボビオシンを精製水に溶かし,メンブレンフィルターを用いてろ過し滅菌する。使用時
に調製する。
5.1.2.3
最終使用培地の調製 使用直前に,ノボビオシン溶液(5.1.2)1 mL又は4 mLを,冷却した変法
トリプトソイブロス培地(5.1.1)225 mL又は900 mLに加える。変法トリプトソイブロス培地に含まれる
ノボビオシンの最終濃度は20 mg/Lとする。
5.2
第一選択分離培地(セフィキシム−亜テルル酸−ソルビトール添加マッコンキー寒天培地)(参考文
献2.参照)
5.2.1
基礎培地
5.2.1.1
組成
表 3 基礎培地の組成
カゼインペプトン
17.0 g
ミートペプトン
3.0 g
ソルビトール
10.0 g
胆汁酸塩
1.5 g
塩化ナトリウム (JIS K 8150)
5.0 g
ニュートラルレッド
0.03 g
クリスタルバイオレット (JIS K 8294)
0.001 g
寒天 (JIS K 8263)
9〜18 g (1)
精製水
1 000 mL
注(1) 寒天のゲル強度による。
5.2.1.2
調製 各基礎成分及び粉末培地を精製水に加え,煮沸して溶かす。必要であれば,滅菌後,25 ℃
でpH 7.0±0.2になるように滅菌前にpH調節を行う。オートクレーブ(6.1)を用いて121 ℃で15分間加
熱し,滅菌する。
5.2.2
亜テルル酸カリウム溶液

4
K 3704:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
5.2.2.1
組成
表 4 亜テルル酸カリウム溶液の組成
亜テルル酸カリウム
0.25 g
精製水
100 mL
5.2.2.2
調製 亜テルル酸カリウムを精製水に溶かし,メンブレンフィルターを用いてろ過し滅菌する。
備考 この溶液は室温で1か月間保存できるが,白い沈殿物が生じた場合には廃棄する。
5.2.3
セフィキシム溶液
5.2.3.1
組成
表 5 セフィキシム溶液の組成
セフィキシム
5 mg
精製水
100 mL
5.2.3.2
調製 セフィキシムを精製水(2)に溶かし,メンブレンフィルターを用いてろ過し滅菌する。
注(2) セフィキシムをエタノールに溶解する場合もある。
備考 この溶液は,3±2 ℃で1週間保存できる。
5.2.4
最終使用培地
5.2.4.1
組成
表 6 最終使用培地の組成
基礎培地(5.2.1)
1 000 mL
亜テルル酸カリウム溶液(5.2.2)
1.0 mL
セフィキシム溶液(5.2.3)
1.0 mL
5.2.4.2
調製 滅菌した基礎培地(5.2.1)を44〜47 ℃(6.5)まで冷却する。滅菌後に冷却して固化した
基礎培地を蒸気で加熱して溶かし,その後44〜47 ℃まで冷却してもよい。基礎培地1 000 mLに,亜テル
ル酸溶液1 mLとセフィキシム溶液1 mLとを加え,混和する。滅菌済みシャーレ(6.15)に約15 mLずつ
加え,固化する。亜テルル酸及びセフィキシムの最終濃度はそれぞれ2.5 mg/L及び0.05 mg/Lとなる。
寒天平板培地は,25〜50 ℃(6.2)で,ふたを外して寒天表面を下向きにし,培地表面から液滴が消え
るまで乾燥させる。クリーンベンチ(JIS B 9922を参照)中で,ふたを半分ずらした状態で30分間,又は
ふたをした状態で一夜放置して乾燥してもよい。
備考 乾燥前の寒天平板培地は,袋又は湿気が保てる容器に入れて3 ℃±2 ℃で冷蔵すれば,遮光下
で2週間保存できる。
5.3
第二選択分離培地 試験所の判断によってセフィキシム−亜テルル酸−ソルビトール添加マッコン
キー寒天培地を補完するものとして大腸菌O157の分離に特に適した培地を,第二選択分離培地として用
いる。寒天平板培地の調製は,5.2.4.2による。
5.4
普通寒天培地
5.4.1
組成
表 7 普通寒天培地の組成
肉エキス
3.0 g
ペプトン
5.0 g
寒天
9〜18 g (*)
精製水
1 000 mL
注(*) 寒天のゲル強度による。
5
K 3704:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
5.4.2
調製 各成分又は粉末培地を精製水で溶かす。必要に応じて,加熱し溶解する。必要であれば,滅
菌後25 ℃でpH 7.0±0.2になるように滅菌前にpH調整を行う。適切な容量のフラスコ又は瓶(6.7)に培
地を移しオートクレーブ(6.1)を用いて121 ℃で15分間加熱し,滅菌する。
5.4.3
普通寒天平板培地の作製 溶解した培地(5.4.2)を50〜70 ℃(6.5)まで冷却し,シャーレ(6.15)
に移し,固化させる。寒天平板培地の使用方法は,5.2.4.2による。
5.5
トリプトン−トリプトファン培地
5.5.1
組成
表 8 トリプトン−トリプトファン培地の組成
トリプトン
10.0 g
塩化ナトリウム (JIS K 8150)
5.0 g
トリプトファン(JIS K 8676)
1.0 g
精製水
1 000 mL
5.5.2
調製 各成分を精製水に溶かす。必要に応じて,煮沸して溶かす。必要であれば,滅菌後25 ℃で
pH 7.0±0.2になるように滅菌前にpH調節を行う。適切な容量の試験管又は瓶(6.7)に5 mLずつ加え,
オートクレーブ(6.1)を用いて121 ℃で15分間加熱し,滅菌する。
5.6
コバックのインドール試薬
5.6.1
組成
表 9 コバックのインドール試薬の組成
p-ジメチルアミノベンズアルデヒド (JIS K 8496)
5.0 g
2-メチルブタン-1-オール又はペンタン-1-オール
75.0 mL
濃塩酸(3.3) (JIS K 8150)
25.0 mL
5.6.2
調製 p-ジメチルアミノベンズアルデヒドを2-メチルブタン-1-オール又はペンタン-1-オールに溶
解する。必要であれば、44〜47 ℃の水浴 (6.5) 中で加熱する。室温まで冷却し,塩酸を加える。褐色ガラ
ス瓶に入れて遮光し,3℃±2℃で冷蔵保存する。
備考 この試薬の色は淡黄色又は淡褐色で,沈殿物がないものとする。
5.7
抗大腸菌O157免疫磁気ビーズ 抗体を固定化した免疫磁気ビーズ及び磁気分離装置を用いて大腸
菌O157を濃縮及び分離する。
備考 免疫補そく(捉)法を用いて大腸菌O157を特異的に濃縮する市販キットを用いる場合には,
製造業者の取扱説明書に従って調製及び操作をする。
5.8
洗浄用緩衝液(変法りん酸緩衝液)
5.8.1
組成
表 10 変法りん酸緩衝液の組成
塩化ナトリウム (JIS K 8150)
8.0 g
塩化カリウム (JIS K 8121)
0.2 g
りん酸水素二ナトリウム(無水物) (JIS K 9020)
1.44 g
りん酸二水素カリウム(無水物) (JIS K 9007)
0.24 g
ポリ(オキシエチレン)ソルビタンモノラウラート
0.2 mL
精製水
1 000 mL
5.8.2
調製 各成分を精製水に溶かす。必要であれば,滅菌後,25 ℃でpH 7.0±0.2になるように滅菌前
にpH調節を行う。適切な容量のフラスコ又は瓶(6.7)に分注し,オートクレーブ(6.1)を用いて121 ℃
で15分間加熱し,滅菌する。成分及び性能が同等の市販品を用いてもよい。

6
K 3704:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
備考 溶液が濁ることがあるが,静置すると透明になる。成分及び性能が同等の市販品を用いてもよ
い。
5.9
生理的食塩水
5.9.1
組成
表 11 生理的食塩水の組成
塩化ナトリウム (JIS K 8150)
8.5 g
精製水
1 000 mL
5.9.2
調製 塩化ナトリウムを精製水に溶かす。適切な容量のフラスコ又は瓶(6.7)に加え,オートク
レーブ(6.1)を用いて121 ℃で15分間加熱し,滅菌する。
5.10 大腸菌O157抗血清 専門の試験所から入手するか又は分離した体細胞O157として市販品を入手で
きる。未知の分離菌株に用いる前に,陽性及び陰性対照で試験する。
6. 装置及びガラス器具 微生物試験用の装置及びガラス器具(JIS K 3701参照)及び次に示すものを用
いる。
6.1
オーブン及びオートクレーブ JIS K 3701(5.10及び5.5)参照。
6.2
乾燥器又はインキュベータ(25〜50 °C) 温度範囲25〜50 ℃で,±1 ℃に維持できるもの。
6.3
インキュベータ(37±1 °C) 37 ℃±1 ℃に維持できるもの。
6.4
インキュベータ(41.5±1 °C) 41.5 ℃±1 ℃に維持できるもの。
6.5
水浴 44〜47 ℃に維持できるもの。
6.6
pH計 JIS Z 8802に規定するpH計の形式Ⅲによる。
6.7
試験管,フラスコ及び瓶 培地の滅菌及び保存,並びに液体培地の培養に用いる。適切な容量のも
の。
6.8
メスシリンダー 希釈液及び培地の調製に用いる。適切な体積のもの。
6.9
吐出式メスピペット 体積1 mL及び10 mLで,それぞれ0.1 mL及び0.5 mLの目盛付きのもの。
6.10 白金耳及び白金線 白金イリジウム又はニッケルクロム製とする。パスツールピペット又は使い捨
て白金耳を用いてもよい。
6.11 ピペッター 滅菌済みで,容量範囲20〜200 μLで10 μLの目盛付のもの。
6.12 磁石付ラックを備えた磁気分離装置 免疫磁気ビーズを用いて細菌を濃縮するもの。エッペンドル
フ形プラスチックチューブ(6.13)と共に用いる。
6.13 エッペンドルフ形プラスチックチューブ スクリューキャップ付きで滅菌済み及び使い捨ての遠心
分離用プラスチックチューブ。磁気ラックに適合する1.5 mLの容量のもので,開栓時にエアロゾルの発生
を防止できるもの。
6.14 ロータリ−ミキサー(風車形の血液試料用ミキサー) 15〜20 rpmで回転できるもの。
6.15 シャーレ 直径90 mm又は140 mmのもの。
6.16 かき混ぜ機(ボルテックスミキサー)
7. 試料の採取 試験対象を真に代表する試料で,輸送中及び保存中に損傷及び変化を受けていないもの
を試験室で受け入れる。試料は迅速に冷却して保存する。
試料の採取方法は,この規格では規定しない。当該試料について個別の規格が存在しない場合,当事者
7
K 3704:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
間で採取方法について合意を得ることが望ましい。
8.
試料の調製 試料の調製は,当該試料の個別の規格による。個別の規格がない場合は,当事者間で合
意することが望ましい。
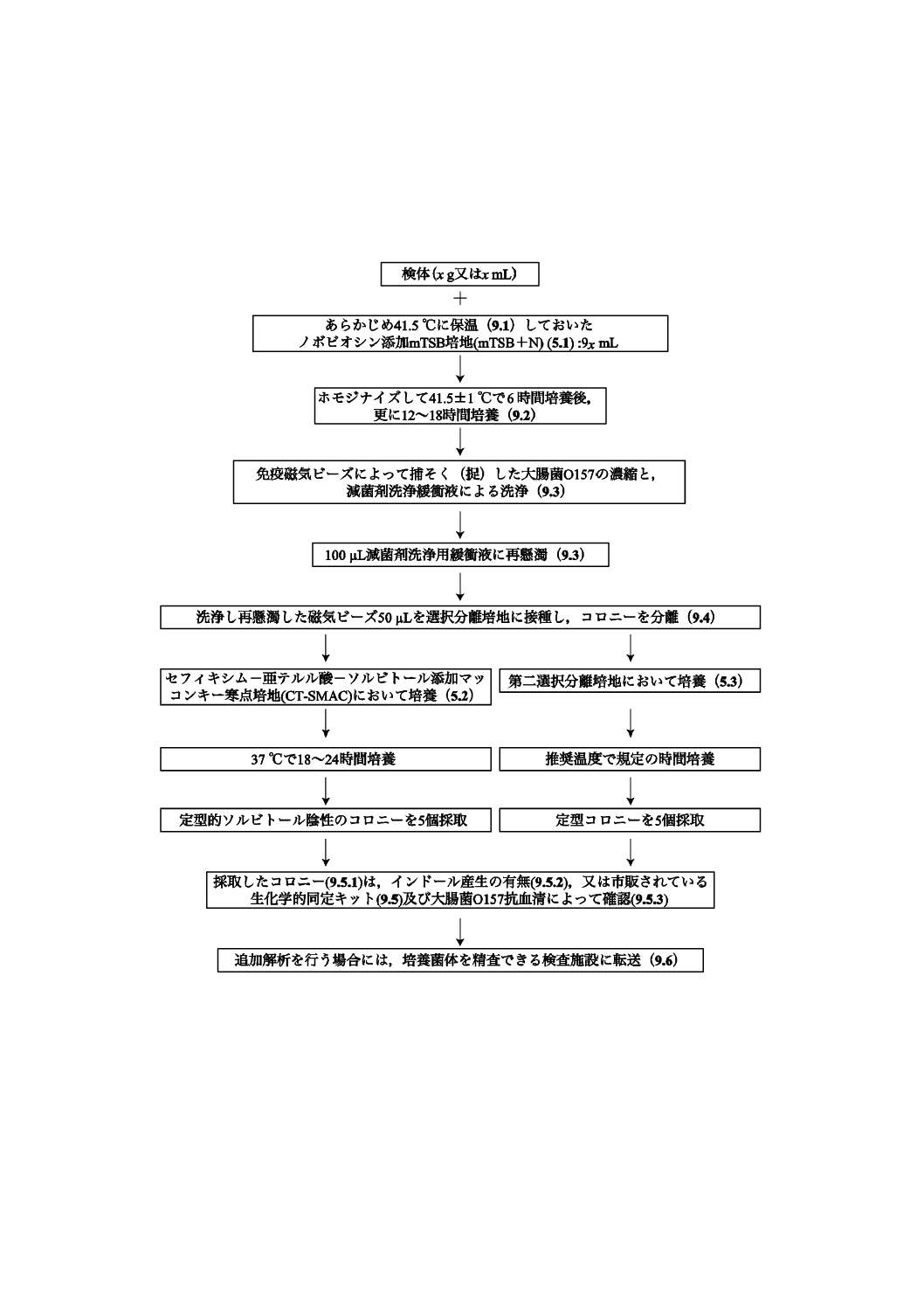
9. 実施手順 (附属書A参照)
9.1
試料及び試料懸濁液(1次希釈試料液)(JIS K 3702参照) 通常,試料懸濁液は,ノボビオシン添
加変法トリプトソイブロス培地(mTSB+N)(5.1)に対する試料の割合が10分の1となるように調製する。
試料x(g)又はx(mL)を,あらかじめインキュベータ(6.4)内で41.5 ℃に保温した変法トリプトソイ
ブロス培地の9x(mL)又は9x(g)に加える。メッシュフィルター付きのストマッカー用袋を用いて,試
料粒子が免疫磁気分離法(9.3)に及ぼす影響を減少させることが望ましい。
9.2
増菌 試料懸濁液(9.1)をインキュベータ(6.4)で培養する。41.5 ℃で6時間培養後,更に12〜
18時間培養する。
備考 6時間培養後,免疫磁気分離し,選択分離培地へ接種すると,一時的に陽性を示すが,更に18
時間培養すると陰性を示す可能性がある。
9.3
免疫磁気分離法(IMS)
9.3.1
概要 免疫磁気分離は6時間の培養後に実施する。必要であれば,12〜18時間培養後に再び実施
する。免疫磁気分離法に用いるキットと必要な器具の使用方法及び操作手順は,製造業者の取扱説明書に
従う。
9.3.2
免疫捕そく(捉)
警告 無菌的に操作し,外部汚染及びエアロゾルの発生を防止する。この操作は,手袋を着用し,封じ
込め設備である安全キャビネット内で実施する。
磁気分離装置(6.12)及び抗体を固定化した免疫磁気ビーズ(5.7)を用い,捕そく(捉)及び分離を行
う。増菌(9.2)した培養液をかき混ぜ,粗い粒子を沈澱させる。粒子又は脂肪性物質ができるだけ混入し
ないように増菌培養液から上澄み液1 mLを採取し,室温で免疫磁気ビーズ(5.7)20 μLを加えたエッペ
ンドルフ形プラスチックチューブ(6.13)に移す。12〜20 rpmに設定したロータリ−ミキサー(6.14)で,
試料懸濁液を10分間かき混ぜる。
9.3.3
分離 エッペンドルフ形プラスチックチューブ(9.3.2)を磁石付きラック(6.12)に取り付け,磁
石付きラックを穏やかに180°振って,磁石に磁気ビーズを集める。チューブ壁面に付着したビーズを動
かさないよう注意深くキャップを開ける。チューブを磁石付きラックにセットしたまま,試料液ごとに新
しい滅菌済みピペッター(6.11)を用いて試料液をチューブの底から静かに吸い取り,除く。滅菌済みの
洗浄用緩衝液(5.8)1 mLを加え,キャップを閉める。磁石をラックから取りはずした後,ラックを穏や
かに180°振ってチューブの中身を混和し,磁石をラックに戻す。緩衝液を加える際の交差汚染を防止す
る。洗浄用緩衝液を取り除く際は,試料液ごとに新しいピペッターを用いる。洗浄操作を幾度か繰り返す。
磁気分離装置からチューブを取り出し,滅菌済みの洗浄用緩衝液(5.8)100 μLを加え,磁気ビーズを再度
懸濁させる。
9.4
選択分離培地への接種と大腸菌O157コロニーの同定
9.4.1
接種 ピペッター(6.11)を用い,洗浄後に再懸濁した磁気ビーズ(9.3.3)を50 μLずつ,セフィ
キシム−亜テルル酸−ソルビトール添加マッコンキー寒天培地(5.2)及び第二選択分離培地(5.3)に移す。
滅菌済み白金耳(6.10)を用いてビーズを画線塗抹し,単一コロニーを寒天平板上に数多く発生させる。
8
K 3704:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
インキュベータ(6.3)内で,セフィキシム−亜テルル酸−ソルビトール添加マッコンキー寒天培地(5.2)
は,37 ℃で18〜24時間培養し,第二選択分離培地は,推奨温度で規定時間だけ培養する。
備考 試料及び細菌そう(叢)の種類によっては,増菌用ブロスで20〜24時間培養すると選択寒天培
地上に他の細菌が大量に増殖し,大腸菌O157のコロニーの確定が困難になることがある。免
疫磁気分離法で調製した試料懸濁液の希釈液,又は1平板当たり50 μL未満を選択寒天培地に
接種すれば,大腸菌O157のコロニーが得られやすくなるが,希釈液の量が少なくなるので検
出される可能性は低下する。
9.4.2
大腸菌O157の定形コロニーの識別 セフィキシム−亜テルル酸−ソルビトール添加マッコンキー
寒天培地上で定形コロニーの有無を確定する。
備考 セフィキシム−亜テルル酸−ソルビトール添加マッコンキー寒天培地上では,定形コロニーが
透明である。色調は,ほとんど無色に近い淡黄褐色で,直径は約1 mmである。
第二選択分離培地については,製造業者の取扱説明書に従って定形コロニーを識別する。
9.5
確定
9.5.1
コロニーの選択 9.4に従って,各平板から定形的コロニー5個を選択する。寒天平板培地上の定
形コロニーが5個未満の場合には,すべてのコロニーを試験する。選択した各コロニーを普通寒天平板培
地(5.4)上に画線塗抹し,インキュベータ(6.3)内で, 37 ℃で18〜24時間培養する。生育したコロニ
ーの中で単独コロニーだけを用いて9.5.2及び9.5.3の試験を行う。
9.5.2
生化学的確定(インドール産生反応) 普通寒天平板培地上の独立したコロニー1個を釣菌(9.5.1)
し,トリプトン−トリプトファン培地(5.5)の入った試験管に接種する。インキュベータ(6.3)内で,37 ℃
で24時間培養する。コバック試薬(5.6)1 mLを加え,室温で10分間静置する。赤を呈した場合は陽性
とし,黄色又は褐色を呈した場合は陰性とする。
9.5.3
血清学的同定
9.5.3.1
概要 大腸菌O157抗血清を用いる血清学的反応は,インドール陽性のコロニーだけを試験する。
9.5.3.2
自発凝集性を示す分離菌株の排除 生理的食塩水(5.9)1滴を,洗浄済みスライドガラスに滴加
する。白金耳(6.10)を用いて,この1滴に普通寒天平板培地上のコロニー1個(9.5.1)を混和し,均一の
懸濁液とする。スライドガラスを30〜60秒間穏やかに振った後,背景を暗くして観察する。必要であれば,
拡大レンズを用いる。懸濁液が目に見える凝集塊を形成した場合,この菌株を自発凝集性とする。この場
合,特定の抗血清による凝集反応は,識別できないので,それ以上の試験は行わない。
9.5.3.3
大腸菌O157抗血清による凝集反応 普通寒天平板培地上に形成された独立したコロニー1個を
釣菌し(9.5.1),滴下した生理的食塩水1滴に懸濁(9.5.3.2)して大腸菌O157抗血清(5.10)を少量添加
する。凝集反応が,1分間以内に起きれば陽性とする。
9.5.3.4
陽性菌株の同定 インドール陽性で,かつ,大腸菌O157抗血清又は入手可能であれば大腸菌
O157:H7抗血清で凝集反応を起こす分離菌株を陽性とする。
9.6
追加解析 陽性のコロニーについて,べん(鞭)毛抗原の検出及び病原性特性などの追加解析は,
培養菌体が精査できる試験施設で行う。
10. 精度評価
10.1 精度評価用菌株 精度評価用菌株は,この規格では規定しない。
備考 病原性をもたない大腸菌O157を用いる精度評価は,高度の技術が必要であるため専門家が安
全性の高い施設で実施する。
9
K 3704:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
10.2 培養方法 培養方法は,この規格では規定しない。
備考 病原性をもたない大腸菌O157を用いる精度評価は,高度の技術が必要であるため専門家が安
全性の高い施設で実施する。
11. 結果の表記 試験結果に基づき,試験試料中の大腸菌O157の有無を報告する。試験試料の質量(g)
又は体積(mL)を明記する。
12. 試験報告書 試験報告書には,次の事項を明記する。
a) 試験試料を完全に特定するために必要な全情報
b) 使用した試験試料の採取方法(判明している場合)
c) 使用した試験方法
d) 採用した培養温度
e) この規格で規定していないあらゆる操作又は任意としたあらゆる操作についての詳細,及び試験結果
に影響を及ぼす可能性のある全事象についての詳細
f)
得られた試験結果
試験報告書には,精査できる試験施設が追加試験を実施予定であるか否かも記載する。実施済みであ
れば,その結果を記載する。
10
K 3704:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書A(規定)実施手順説明図
実施手順説明図
11
K 3704:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
参考文献
1. Doyle M.P. and Schoeni J.L. Appl. Environ. Microbiol., 53, 1987, pp. 2394-2396.
2. Zadik P.M., Chapman P.A. and Siddons C.A. J.Med. Microbiol., 39, 1993, pp. 155-158.
3. ISO 6887-2, Microbiology of food and animal feeding stuffs−Preparation of test samples, initial suspension
and decimal dilutions for microbiological examination−Part2: Specific rules for the preparation of the test
samples and initial suspension of meat and meat products.
4. ISO 6887-3, Microbiology of food and animal feeding stuffs−Preparation of test samples, initial suspension
and decimal dilutions for microbiological examination−Part3: Specific rules for the preparation of the test
samples and initial suspension of milk and milk products.
5. ISO 6887-4, Microbiology of food and animal feeding stuffs−Preparation of test samples, initial suspension
and decimal dilutions for microbiological examination−Part4: Specific rules for the preparation of the test
samples and initial suspension of fish products.
6. ISO 6887-5, Microbiology of food and animal feeding stuffs−Preparation of test samples, initial suspension
and decimal dilutions for microbiological examination−Part5: Specific rules for the preparation of the test
samples and initial suspension of products other than milk and milk products, meat and meat products and fish
products.
1
2
K
3
7
0
4
:
2
0
0
8
1
2
K
3
7
0
4
:
2
0
0
8
附属書1(参考)JISと対応する国際規格との対比表
JIS K 3704:2008 培地の試験方法−大腸菌用検出培地
ISO 16654:2001 食品及び動物用飼料の微生物試験−大腸菌O157検出法
(Ⅰ) JISの規定
(Ⅱ) 国際
規格番号
(Ⅲ) 国際規格の規定
(Ⅳ) JISと国際規格との技術的差異
の項目ごとの評価及びその内容
表示箇所:本体
表示方法:点線の下線
(Ⅴ) JISと国際規格との技術的差異の理由
及び今後の対策
項目
番号
内容
項目
番号
内容
項目ごと
の評価
技術的差異の内容
1.適用範
囲
大腸菌O157の検出を目的
とする培地の試験方法につ
いて規定。
ISO
16654
1
JISとほぼ同じ。
MOD/削
除
培地試験に限定。
工業標準化法の対象とならない試験を
削除。
2.引用規
格
JIS K 3701
JIS K 3702
2
ISO 7218
ISO 6887-1
IDT
JISからの引用事項
は,ISO規格の該当事
項と同等である。
―
JIS K 8008,他12規格
−
MOD/追
加
追加した用語を規定するため。
3.定義
用語の定義を規定。
3
JISとほぼ同じ。
MOD/追
加
2用語(精製水及び塩
酸)を追加。
JISとして必要な用語を規定。
4.一般原
則
大腸菌O157の検出のため
の段階操作を規定。
4
JISと同じ。
IDT
―
―
5. 培地,
試薬及び
抗血清
培地,試薬及び抗血精(増
菌培地,第一選択分離培地,
第二選択分離培地,普通寒
天培地,トリプトン−トリ
プトファン培地,コバック
のインドール試薬,抗大腸
菌O157免疫磁気ビーズ,
洗浄用緩衝液,生理的食塩
水及び大腸菌O157抗血清)
について規定。
5
JISとほぼ同じ。
MOD/変
更
5.1(増菌培地)の表1
及び5.2(第一選択分離
培地)表3に記載の一
部の物質名で,酸素分
解物となっているのを
ペプトン表記に変更。
また,必要なJISを追
加。
国内の表記法と異なるため。
技術的差異はない。
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
1
3
K
3
7
0
4
:
2
0
0
8
1
3
K
3
7
0
4
:
2
0
0
8
(Ⅰ) JISの規定
(Ⅱ) 国際
規格番号
(Ⅲ) 国際規格の規定
(Ⅳ) JISと国際規格との技術的差異
の項目ごとの評価及びその内容
表示箇所:本体
表示方法:点線の下線
(Ⅴ) JISと国際規格との技術的差異の理由
及び今後の対策
項目
番号
内容
項目
番号
内容
項目ごと
の評価
技術的差異の内容
6.装置及
びガラス
器具
微生物試験用の装置及びガ
ラス器具(乾燥機及び高圧
蒸気減菌器など)について
規定。
6
JISとほぼ同じ。
MOD/追
加
必要なJISを追加。
―
7.試料の
採取
試料採取は,この規格では
規定しない。
7
JISと同じ。
IDT
―
―
8.試料の
調製
試料調製は,この規格では
規定しない。
8
JISと同じ。
IDT
―
―
9.実施手
順
実施手順(試料及び試料懸
濁液,増菌,免疫磁気分離
法,選択分離培地への接種
と大腸菌O157コロニーの
同定,確定及び追加解析)
について規定。
9
JISとほぼ同じ。
MOD/削
除
MOD/追
加
9.5(確定)にある備考
を削除。
10.2(培養方法)で備
考を追加。
備考に記載の内容が,専門家が実施すべ
き試験となっているため。。
10.精度
評価
精度評価(精度評価用菌株
及び培養方法)について規
定。
10
JISとほぼ同じ。
MOD/削
除
病原性をもたない大腸
菌O157を用いる評価
を削除。
高度の技術が必要であるため。
11.結果
の表記
試験試料中の大腸菌O157
の有無及び試験試料の質量
又は体積の明記を規定。
11
JISと同じ。
IDT
―
―
12.試験
報告書
試験報告書に明記すべき項
目を規定。
12
JISと同じ。
IDT
―
―
附属書A
(規定)
(規定)実施手順説明図
附属書A
(規定)
JISと同じ。
IDT
―
―
JISと国際規格との対応の程度の全体評価:MOD
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
1
4
K
3
7
0
4
:
2
0
0
8
1
4
K
3
7
0
4
:
2
0
0
8
備考1. 項目ごとの評価欄の記号の意味は,次のとおりである。
― IDT……………… 技術的差異がない。
― MOD/削除……… 国際規格の規定項目又は規定内容を削除している。
― MOD/追加……… 国際規格にない規定項目又は規定内容を追加している。
― MOD/変更……… 国際規格の規定内容を変更している。
2. JISと国際規格との対応の程度の全体評価欄の記号の意味は,次のとおりである。
― MOD…………… 国際規格を修正している。
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。