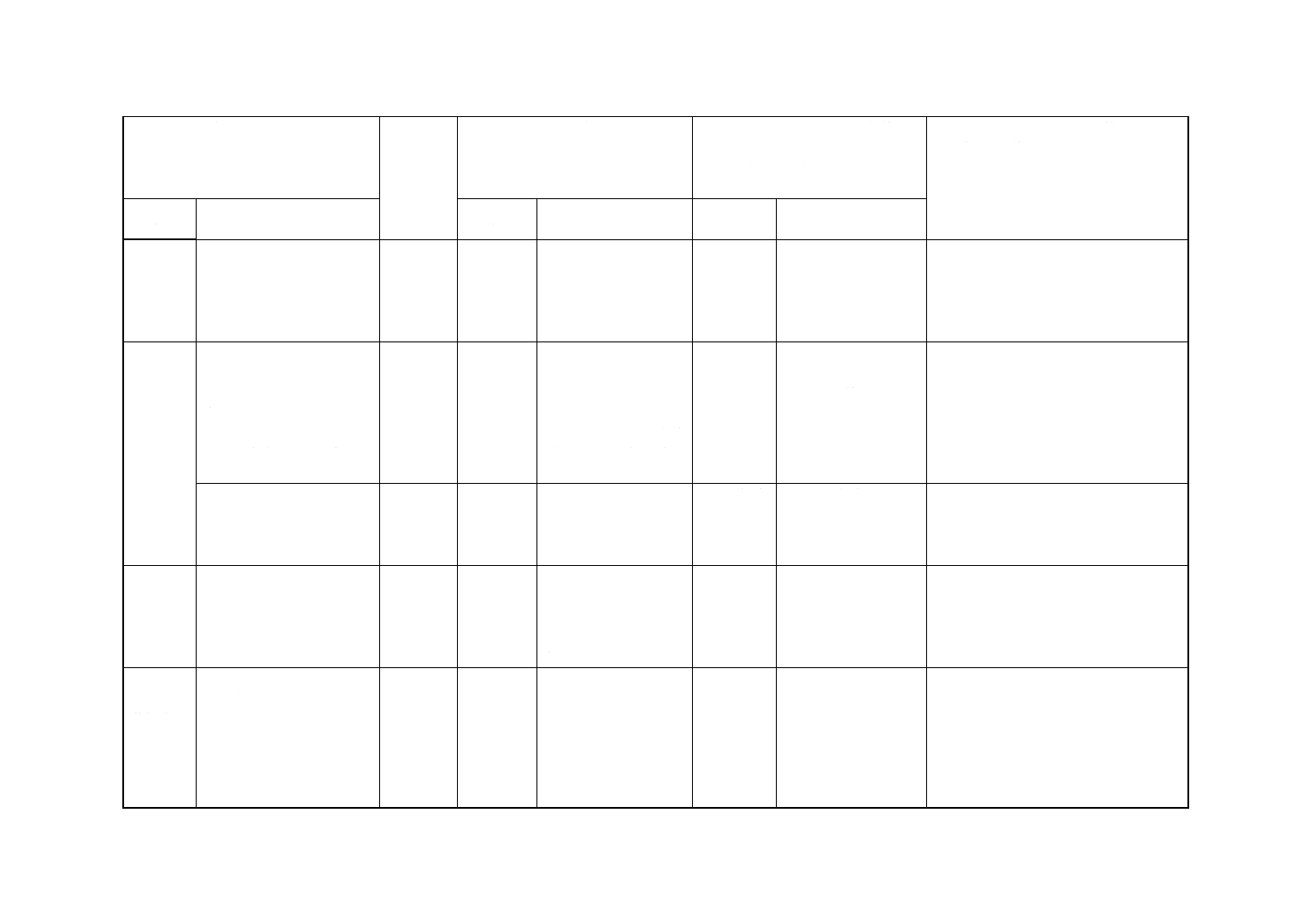K 0350-50-10:2006
(1)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
まえがき
この規格は,工業標準化法第12条第1項の規定に基づき,社団法人日本工業用水協会(JIWA)/財団法人
日本規格協会(JSA)から,工業標準原案を具して日本工業規格を制定すべきとの申出があり,日本工業標準
調査会の審議を経て,経済産業大臣が制定した日本工業規格である。
制定に当たっては,日本工業規格と国際規格との対比,国際規格に一致した日本工業規格の作成及び日
本工業規格を基礎にした国際規格原案の提案を容易にするために,ISO 11731:1998,Water quality−Detection
and enumeration of Legionellaを基礎として用いた。
この規格の一部が,技術的性質をもつ特許権,出願公開後の特許出願,実用新案権,又は出願公開後の
実用新案登録出願に抵触する可能性があることに注意を喚起する。経済産業大臣及び日本工業標準調査会
は,このような技術的性質をもつ特許権,出願公開後の特許出願,実用新案権,又は出願公開後の実用新
案登録出願にかかわる確認について,責任はもたない。
JIS K 0350-50-10には,次に示す附属書がある。
附属書1(規定)グラム染色法
附属書2(参考)JISと対応する国際規格との対比表
JIS K 0350の規格群には,次に示す部編成がある。
JIS K 0350-10-10 用水・排水中の一般細菌試験方法
JIS K 0350-20-10 用水・排水中の大腸菌群試験方法
JIS K 0350-30-10 用水・排水中の従属栄養細菌試験方法
JIS K 0350-40-10 用水・排水中の全細菌試験方法
JIS K 0350-50-10 工業用水・工場排水中のレジオネラ試験方法
JIS K 0350-60-10 工業用水中の硫酸塩還元菌試験方法
JIS K 0350-70-10 工業用水中のスフェロチルス試験方法
JIS K 0350-80-10 工業用水中の鉄細菌試験方法
JIS K 0350-90-10 工業用水中の硫黄細菌試験方法
K 0350-50-10:2006
(2)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
目 次
ページ
序文 ··································································································································· 1
1. 適用範囲 ························································································································ 1
2. 引用規格 ························································································································ 1
3. 定義 ······························································································································ 1
4. 共通事項 ························································································································ 1
4.1 通則 ···························································································································· 1
4.2 水 ······························································································································· 1
4.3 試薬 ···························································································································· 1
4.4 ガラス器具類 ················································································································ 2
4.5 器具などの滅菌及び除菌操作 ··························································································· 2
4.6 消毒操作 ······················································································································ 2
5. 試料 ······························································································································ 2
5.1 試料の採取 ··················································································································· 2
5.2 試料の取扱い ················································································································ 3
6. 試験方法 ························································································································ 3
6.1 試薬 ···························································································································· 4
6.2 器具及び装置 ················································································································ 6
6.3 器具などの滅菌操作 ······································································································· 7
6.4 消毒操作 ······················································································································ 7
6.5 試料の前処理 ················································································································ 7
6.6 推定試験 ······················································································································ 9
6.7 確定試験 ······················································································································ 9
7. 結果の表示 ···················································································································· 10
附属書1(規定)グラム染色法 ······························································································· 13
附属書2(参考)JISと対応する国際規格との対比表 ·································································· 15
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
日本工業規格 JIS
K 0350-50-10:2006
工業用水・工場排水中のレジオネラ試験方法
Testing method for detection and enumeration of Legionella in industrial
water and wastewater
序文 この規格は,1998年に第1版として発行されたISO 11731,Water quality−Detection and enumeration
of Legionellaを翻訳し,技術的内容を変更して作成した日本工業規格である。
なお,この規格で側線又は点線の下線を施してある箇所は,原国際規格を変更している事項である。変
更の一覧表をその説明を付けて,附属書(参考)に示す。
1. 適用範囲 この規格は,工業用水及び工場排水中のレジオネラの試験方法について規定する。
備考 この規格の対応国際規格を,次に示す。
なお,対応の程度を表す記号は,ISO/IEC Guide 21に基づき,IDT(一致している),MOD
(修正している),NEQ(同等でない)とする。
ISO 11731:1998,Water quality−Detection and enumeration of Legionella (MOD)
2. 引用規格 付表1に示す規格は,この規格に引用されることによって,この規格の規定の一部を構成
する。これらの引用規格は,その最新版(追補を含む。)を適用する。
3. 定義 この規格で用いる主な用語の定義は,JIS K 0101,JIS K 0102,JIS K 0550及びJIS K 0211に
よるほか,次による。
3.1
レジオネラ レジオネラ属に属するグラム陰性の無芽胞のかん(桿)菌で,GVPCα寒天培地,WYO
α寒天培地などの選択培地で36±1 ℃,5〜7日間培養したとき,青白から灰白の定型的集落を形成し,
L-システインを必す(須)に要求するもの。代表種はレジオネラ ニューモフィラ(Legionella pneumophila)で
ある。
備考 レジオネラは病原細菌であり,これを吸入することで感染する。したがって,レジオネラの試
験は病原細菌の取扱いに十分な知識及び技術をもった者が行うとともに,試験操作に伴いレジ
オネラ症発症の原因となるエーロゾルの発生及び吸入を極力避ける。
4. 共通事項 共通事項は,次による。
4.1
通則 化学分析に共通する一般事項は,JIS K 0050による。
4.2
水 JIS K 0557に規定するA2又はA3(1)の水。
注(1) 石英ガラス又はほうけい酸ガラス-1製の蒸留器で精製したもの。
4.3
試薬 試薬は,次による。
a) 試薬は,日本工業規格(以下,JISという。)に規定されているものの最上級の品質のものを用い,JIS
2
K 0350-50-10:2006
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
に規定されているものがない場合には,試験に支障のないものを用いる。
b) 試薬類の溶液の濃度は,特に断らない限り質量濃度はg/L又はmg/L,モル濃度はmol/Lで示す。
なお,化合物については無水物としての質量を用いる。
c) 試薬類の溶液名称の後に括弧で示されている濃度は,概略の濃度であることを意味する。
d) 試薬類の名称は,国際純正及び応用化学連合(IUPAC)の無機化学命名法及び有機化学命名法を基にし
て,社団法人日本化学会が定めた化合物命名法及びJIS試薬の名称ともできるだけ整合させている。
e) 試薬類,廃液などの取扱いについては,関係法令などに従い,十分に注意する。
4.4
ガラス器具類 ガラス器具類は,一般にJIS R 3503及びJIS R 3505に規定するものを使用する。た
だし,特殊な器具を必要とする場合には,それぞれの項目に,その一例を図示又は説明する。また,加熱
操作を伴う場合には,JIS R 3503に規定するほうけい酸ガラス-1を用いる。
4.5
器具などの滅菌及び除菌操作 器具などの滅菌及び除菌操作は,次による。
a) 乾熱滅菌 ガラス製及び金属製器具類の滅菌に用いる。滅菌する器具類は,硫酸紙,アルミニウムは
くなどで包むか,滅菌用の金属箱などに収めた後,乾熱滅菌器内に入れ,器内の温度が約170 ℃に到
達した後,約1時間加熱する。
b) 高圧蒸気滅菌 培地,希釈水,試料容器,使用済み培地などの滅菌に用いる。また,比較的構造の複
雑なガラス器具,肉厚のガラス瓶などで乾熱滅菌では破損しやすいものの滅菌にも用いる。
なお,大きなガラス瓶,フラスコなどを高圧蒸気滅菌する場合には,その内部に少量の水を入れて
おく。滅菌時間は高圧蒸気滅菌器の内部の温度が121 ℃に到達した後,15〜20 分間とする。
c) 火炎滅菌 白金線又はニクロム線,移植操作時のフラスコの口部などの滅菌に用いる。試料採取時の
給水栓などの滅菌にも用いる。
d) ろ過除菌 水又は溶液の除菌に用いる。ろ過材に孔径0.2 μmのメンブレンフィルタ(2)(例えば,直径
47 mm)を用い,ろ過することによって除菌する。
注(2) 使用するメンブレンフィルタは,あらかじめ,アルミニウムはく(又は硫酸紙など)に包み,ガラ
ス製ペトリ皿に入れて高圧蒸気滅菌を行う。又は滅菌済みの市販品を用いてもよい。メンブレ
ンフィルタの取扱いには,ピンセットを用いる。
4.6
消毒操作 消毒操作は,次による。
a) 試験操作の前後には,手指及び実験台を消毒する。手指の消毒にはクレゾール石けん液(10 g/L),陽性
石けん液(1〜10 g/L),消毒用エタノール(日本薬局方に規定するもの)又はエタノール(体積分率80 %)
[JIS K 8102に規定するエタノール(95)を用いて調製する。]を用いる。
実験台は,陽性石けん液(10 g/L),消毒用エタノール又はエタノール(体積分率80 %)などを噴霧する
か,これらを含ませた布でぬぐって消毒する。
b) 使用済みのピペット,試料容器,採水器などの器具は,クレゾール石けん液(30〜50 g/L)などの消毒液
中に1日間浸した後(又は高圧蒸気滅菌した後),消毒液が完全に除去されるまで,水でよくすすぐ。
5. 試料
5.1
試料の採取 試料は,試料容器又は採水器を用いて採取する。
5.1.1 器具 器具は,次による。
a) 試料容器 共栓ガラス瓶100〜1 000 ml。試料容器は,あらかじめ水で洗浄した後,栓部と首部とをア
ルミニウムはく(又は硫酸紙など)に包み,乾熱滅菌又は高圧蒸気滅菌を行う(3)。又は滅菌済みの細菌
試験用のポリエチレン瓶を用いてもよい。試料採取時まで汚染を受けないように注意する。

3
K 0350-50-10:2006
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
注(3) 残留塩素などの酸化性物質を含む試料を採取する場合には,試料容器にJIS K 8637に規定する
チオ硫酸ナトリウム五水和物(粉末にしたもの。)20〜30 mgを入れ,高圧蒸気滅菌などにより滅
菌をしておく。市販の滅菌済みの細菌試験用ポリエチレン瓶でチオ硫酸ナトリウムの入ってい
るものを用いてもよい。
b) 採水器 ハイロート採水器。採水器は,携帯箱に収めて乾熱滅菌を行う。図 1に一例を示す。
A:ガラス製試料容器(100〜1 000 ml)
B:栓
C:鎖
D:開栓用鎖
E:瓶の保持板の止め金具用鎖
F:瓶の保持板
G:携帯箱
H:携帯箱のふた
I:おもり
図 1 ハイロート採水器及び携帯箱の一例
5.1.2
操作 試料の採取は,次による。
a) 表層水の採取 湖沼,河川,水路,排水口,貯水槽などの表層水で,直接採取できる場合は,試料容
器で試料を採取する。この際,手指に触れた水は採取しない。直接採取できない場合は,採水器を用
いて採取する(3)。
b) 各深度の水の採取 一定の深さの水は,採水器を用いて採取する(4)。
注(4) ハイロート採水器による採取が困難な場合には,バンドーン採水器を用いて採取し,試料容器
に移す。
c) 給水栓からの採取 給水栓の材質が火炎滅菌に耐えるものである場合は,あらかじめ,火炎滅菌に準
じて給水栓口を滅菌し,栓を開き,配管中の水を十分に放出した後,試料容器に採取する。
火炎滅菌ができない場合は,あらかじめ,給水栓口の周辺及び内部の汚れを除去し,エタノール(体
積分率80 %)などで消毒し,栓を開き,配管中の水を十分に放出した後,試料容器に採取する。
d) 配管,装置からの採取 c)と同様に操作して採取する。
5.2
試料の取扱い 試験は試料採取後,直ちに行う。直ちに試験ができない場合には,0〜5 ℃(凍結さ
せない。)の暗所に保存する。
6. 試験方法 試料中のレジオネラをメンブレンフィルタによるろ過又は遠心分離によって濃縮し,低pH
処理又は高温処理を行った後,選択培地に塗抹し,36±1 ℃で5〜7日間培養し,集落を形成させる。その
中に湿潤性の青白又は灰白の集落が認められれば推定レジオネラとして判定し,計数する。
推定レジオネラとして判定した集落の一部又は全部をBCYEα寒天平板培地及びL-システインを含まな
い寒天平板培地に画線し,36±1 ℃で少なくとも2日間以上,通常,5〜7日間まで培養し,集落を形成さ
せる。
L-システインを含まない寒天平板培地では集落を形成せず,BCYEα寒天平板培地だけに集落を形成し
4
K 0350-50-10:2006
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
たものを確定レジオネラとする。確定試験で陽性と判定された集落数を求め,この値をもとに試料中のレ
ジオネラの菌数を算出する。
備考 3.の備考による。
6.1
試薬 試薬は,次による。
a) 塩酸(0.2 mol/L) JIS K 8180に規定する塩酸20 mlに水を加えて1 Lとする。
b) 塩化カリウム溶液(0.2 mol/L) JIS K 8121に規定する塩化カリウム14.91 gを水に溶かして1 Lとする。
c) 塩酸-塩化カリウム混合溶液(pH2.2) 塩酸(0.2 mol/L)3.9 mlと塩化カリウム溶液(0.2 mol/L)25 mlとを混
合し,水酸化カリウム溶液(1 mol/L)(JIS K 8574に規定する水酸化カリウム56.1 gを水に溶かして1 L
とする。)を用いてpHを2.2±0.2に調節する。ガラス容器に移し,密栓して暗所で保存し,1か月間
以内に使用する。
d) L-システイン溶液(36 g/L) JIS K 8470に規定するL-システイン塩酸塩一水和物4.0 gを水に溶かして
100 mlとした後,ろ過除菌したもの(5)。
注(5) この溶液は,滅菌済み容器に入れて−20±3 ℃で3か月間保存できる。使用時は室温で解凍す
る。
e) 二りん酸鉄(Ⅲ)溶液(25 g/L) 二りん酸鉄(Ⅲ)(可溶性)2.5 gを水に溶かして100 mlとした後,ろ過除菌
したもの(5)。
f)
ポリミキシン溶液 ポリミキシンB硫酸塩を水に溶かして10 000国際単位(i.u.)/ml(6)となるように調
製した後,ろ過除菌したもの(5)。
注(6) 国際単位(i.u.)(International unit)は,質量単位(SI単位)ではなく,一定量もつ効力を国際的に統
一した単位として表したもので,入手したポリミキシンB硫酸塩(試薬)に表示されている単
位をもとに調製する。
g) バンコマイシン溶液(1 g/L) バンコマイシン塩酸塩を水に溶かして1 mg/mlとなるように調製した後,
ろ過除菌したもの(5)。
h) シクロヘキシミド溶液(20 g/L) シクロヘキシミド(7)を水に溶かして20 mg/mlとなるように調製した
後,ろ過除菌したもの(5)。
注(7) シクロヘキシミドは肝臓毒性があるので,粉末試薬を扱う際は手袋及び防じんマスクを着用す
る。
i)
アムホテシリンB溶液(20 g/L) アムホテシリンBをスルフィニルビスメタン[ジメチルスルホキシド
(DMSO)]に溶かして20 mg/mlとなるように調製した後,ろ過除菌したもの(5)。
j)
BCYEα寒天平板培地 BCYEα寒天平板培地の調製は,次による(8)。
1) N-(アセトアミド)-2-アミノエタンスルホン酸(ACES)10.0 gを水500 mlに加え,水浴(45〜50 ℃)中で
加熱しながら溶かす。水酸化カリウム溶液(5.83 g/L)(JIS K 8574に規定する水酸化カリウム2.9 gを
水に溶かして500 mlとする。) 480 mlを加えてかき混ぜる。
2) 1)の溶液に粉末活性炭2.0 gを加えてかき混ぜ,酵母エキス(粉末)10.0 gと2-オキソペンタン二酸水
素カリウム(α-ケトグルタル酸カリウム)1.0 gとをこの順に加えて溶かす。滅菌後のpHが6.9 ± 0.2
となるように,水酸化カリウム溶液(0.1 mol/L)(JIS K 8574に規定する水酸化カリウム5.6 gを水に溶
かして1 Lとする。)又は硫酸(0.05 mol/L)(JIS K 8951に規定する硫酸2.7 mlを水1 Lに注意しなが
ら加えて調製する。)を用いて調節し,JIS K 8263に規定する寒天(粉末)15.0 gを加えて混ぜ合わせ
た後,高圧蒸気滅菌を約15 分間行い,滅菌後,速やかに約50 ℃に冷却する。
3) これにL-システイン溶液(36 g/L)10 mlと二りん酸鉄(Ⅲ)溶液(25 g/L)10 mlを無菌的に加えてよくか
5
K 0350-50-10:2006
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
き混ぜる。
4) 粉末活性炭が沈降しないように常にかき混ぜながらこの溶液約15 mlをペトリ皿にそれぞれ分注し,
平板に固める(9)。保存する場合は,ポリエチレン製の袋などに入れて0〜10 ℃(凍結しないように
して)の暗所に保存し,4 週間以内に使用する。
注(8) 市販の調製済み寒天培地又は市販の粉末培地を用いて調製してもよい。
(9) ペトリ皿を逆さにして少し開けて培養器内におき,内部の水蒸気及び凝縮水を蒸発させて平板
表面を乾かす。この際,JIS B 9920に規定する清浄度クラス3 以上の環境(例えば,クリーンベ
ンチ内)で行えば,ペトリ皿のふたを大きく開けて水蒸気及び凝縮水を迅速に蒸発させることが
できる。
k) 選択培地 選択培地にはGVPCα寒天培地又はWYOα寒天培地を用いる。これらの培地は,BCYEα
寒天培地にレジオネラ以外の微生物の増殖を抑制するための3種類の抗生物質及びグリシンを加えた
もので,平板の選択培地の調製は,次による(8)。
1) GVPCα寒天平板培地 GVPCα寒天平板培地の調製は,次による(8)。
1.1) j) 1)による。
1.2) 1.1)の溶液に粉末活性炭2.0 gを加えて混ぜ合わせ,酵母エキス(粉末)10.0 g,2-オキソペンタン二
酸水素カリウム(α-ケトグルタル酸カリウム)1.0 g,JIS K 8291に規定するグリシン3.0 gをこの順
に加えて溶かす。滅菌後のpHが6.9 ± 0.1となるように,水酸化カリウム溶液(0.1 mol/L)又は硫
酸(0.05 mol/L)を用いて調節し,JIS K 8263に規定する寒天(粉末)15.0 gを加えて混ぜ合わせた後,
高圧蒸気滅菌を約15 分間行い,滅菌後,速やかに約50 ℃に冷却する。
1.3) これにL-システイン溶液(36 g/L)10 ml及び二りん酸鉄(Ⅲ)溶液(25 g/L)10 mlを無菌的に加えてよく
振り混ぜる。さらにポリミキシンB溶液8 ml,バンコマイシン溶液(1 g/L)1 ml及びシクロヘキシ
ミド溶液(20 g/L)4 mlを無菌的に加えてよく振り混ぜる。
1.4) j) 4)による。
2) WYOα寒天平板培地 WYOα寒天平板培地の調製は,次による(8)。
2.1) j) 1)による。
2.2) j) 2)による。
2.3) これにL-システイン溶液(36 g/L)10 ml及び二りん酸鉄(Ⅲ)溶液(25 g/L)10 mlを無菌的に加えてよく振
り混ぜる。さらにポリミキシンB溶液10 ml,バンコマイシン溶液(1 g/L)5 ml及びアムホテリシンB
溶液(20 g/L)4 mlを無菌的に加えてよく振り混ぜる。
2.4) j) 4)による。
l)
L-システインを含まない寒天平板培地 j) 3)のL-システイン溶液(36 g/L)の添加を除いて,j)の操作に
よって調製する(8)。
備考 L-システインを含まない寒天平板培地として,血液寒天平板培地*を用いてもよい。血液寒天平
板培地の調製は,次による。
肉エキス10.0 g, ペプトン10.0 g,JIS K 8150に規定する塩化ナトリウム5 g及びJIS K 8263
に規定する寒天(粉末)15.0 gを水1 Lに加え,加熱して溶かした後,滅菌後のpHが7.5 ± 0.1
となるように,水酸化ナトリウム溶液(1 mol/L)(JIS K 8576に規定する水酸化ナトリウム40 gを
水に溶かして1 Lとする。)又は塩酸(1 mol/L)(JIS K 8180に規定する塩酸を用いて調製する。)
を用いて調節した後,高圧蒸気滅菌を約15 分間行う。滅菌後,速やかに約50 ℃に冷却し,羊
又は馬の血液50 mlを泡立てないように加えてよく混合し,約15 mlずつをペトリ皿に分注し,
6
K 0350-50-10:2006
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
平板に固める**。保存する場合は,ポリエチレン製袋などに入れて0〜10 ℃(凍結しないように
して)の暗所に保存する。
注*
注(8)による。
**
注(9)による。
参考 肉エキスは,Lab-Lemco社製のものを用いるとよい。Lab-Lemco社製の肉エキスは,この規格
使用者の便宜のために,一般に入手できるものとして掲げたが,これを推奨するわけではない。
同じ効果を得られることを証明することができれば,これと同等の他のものを用いてもよい。
6.2
器具及び装置 器具及び装置は,次による。
a) メスピペット 1〜10 ml。ピペット滅菌箱に先端を先にして入れるか,アルミニウムはく又は硫酸紙
に包んで乾熱滅菌をしておく。
b) 駒込ピペット 1〜2 ml。ピペット滅菌箱に先端を先にして入れるか,アルミニウムはく又は硫酸紙に
包んで乾熱滅菌をしておく。
c) ピンセット 先端が平らで滑らかなもの。使用直前に火炎滅菌を行う。
d) ねじ口三角フラスコ 合成樹脂製のねじふた付きの容量100 mlのもの(10)。ねじふたをゆるめて,高
圧蒸気滅菌をした後,密栓をしておく。
注(10) ふたの材質は,高圧蒸気滅菌に耐えるもの。
e) メンブレンフィルタ 孔径0.2 μm,直径約25〜47 mmのメンブレンフィルタ。アルミニウムはく,硫
酸紙などに包んでペトリ皿に入れて高圧蒸気滅菌を行う,又は滅菌済みの市販品を用いてもよい。メ
ンブレンフィルタの取扱いには,ピンセットを用いる。
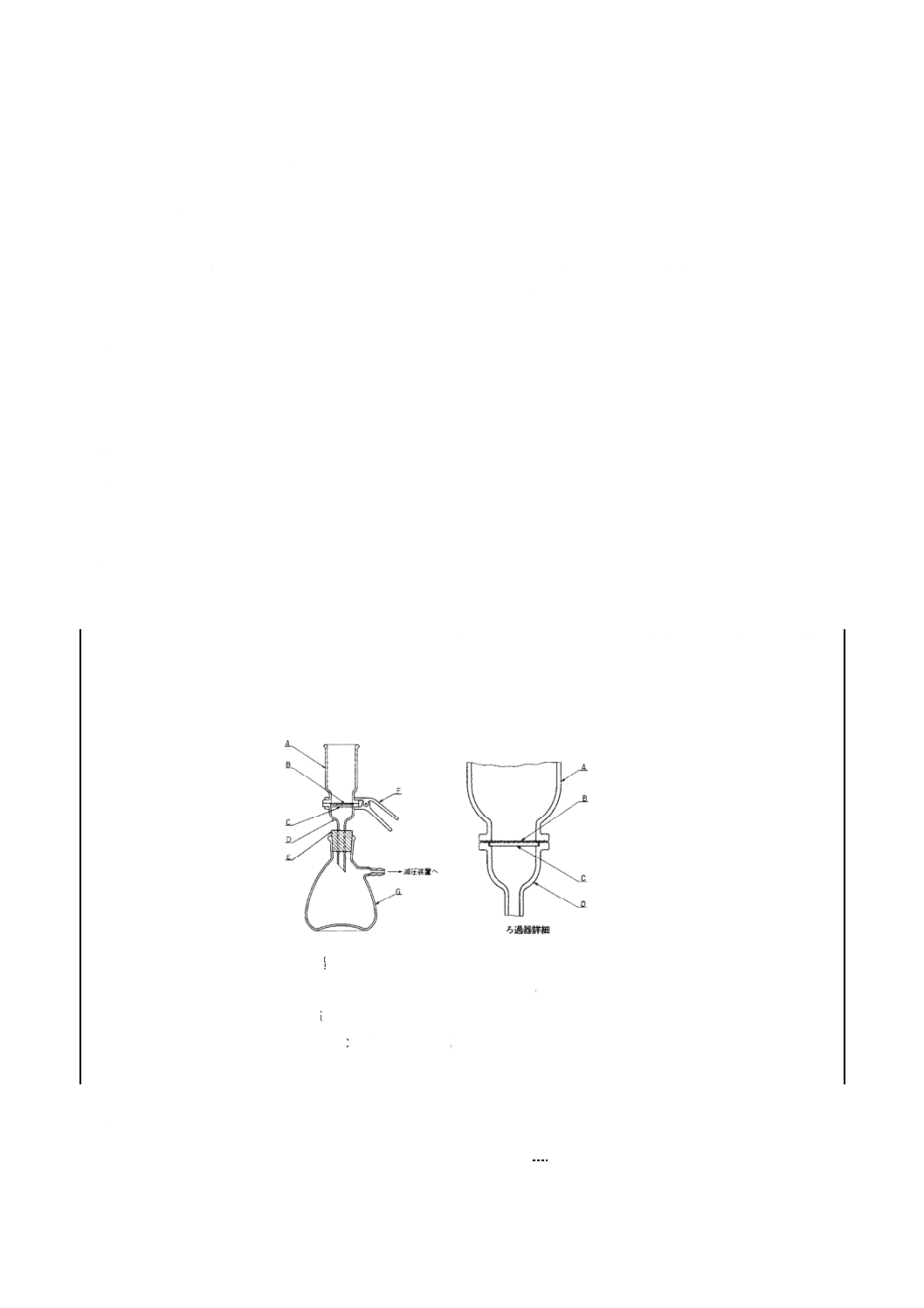
f)
ろ過器(分離形) 図 2に一例を示す。ろ過器の各部をアルミニウムはく,硫酸紙などに包んで材質に
適した滅菌をしておく。
A:上部ろ過管 B:メンブレンフィルタ
C:メンブレンフィルタの支持台(スクリーン)
D:下部ろ過管 E:ゴム栓(シリコーン)
F:金属製クランプ G:吸引瓶
図 2 ろ過器(分離形)の一例
g) ペトリ皿 ガラス製の直径約90 mm,高さ約15 mmのもの。ペトリ皿滅菌箱に入れるか,アルミニウ
ムはく又は硫酸紙に包んで乾熱滅菌をしておく,又はJIS K 0950に規定するプラスチック製滅菌シャ
7
K 0350-50-10:2006
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
ーレ90B。
h) コンラージ棒(塗抹棒) 直径約4 mm,長さ約25 cmのガラス棒で,一端を底辺3〜4 cmの二等辺三角
形状に曲げたもの。ペトリ皿滅菌箱に入れるか,アルミニウムはく又は硫酸紙に包んで乾熱滅菌をし
ておく(11)。
注(11) 市販の滅菌済みの合成樹脂製のものを用いてもよい。
i)
スライドガラス JIS R 3703に規定するもの。大きさは,76.0×26.0 mmのもの。
j)
拡大鏡 1.5〜2 倍に拡大できるもの。
k) 光学顕微鏡及びその附属品 光学顕微鏡は,総合倍率100〜1 000 倍が得られるもので,次のものから
成る。
1) 光学顕微鏡 JIS B 7132に規定する液浸系レンズ用生物顕微鏡。
2) 対物レンズ 液浸系レンズで,呼び倍率90 以上のもの。
3) 接眼レンズ 呼び倍率5〜15 のもの。
4) 十字標本移動器(メカニカルステージ) 光学顕微鏡に取り付け,スライドガラスを前後左右に移動
できるもの。
l)
集落計数器 1.5〜2倍の拡大鏡を備えたもの。
m) 培養器 JIS T 1702に規定するふ卵器。36±1 ℃に調節できるもの。
n) 乾熱滅菌器 160〜200 ℃に調節できるもの。
o) 高圧蒸気滅菌器 JIS T 7322又はJIS T 7324に規定するもので,121 ℃で加熱でき,器内圧力198 kPa
で使用できるもの。
p) 遠心管 ねじふたつきのガラス製の容量50 ml以上のもの。あらかじめ乾熱滅菌又は高圧蒸気滅菌し
て使用する。市販の滅菌済みのポリエチレン製のものを用いてもよい。
q) 遠心機 JIS T 1701に規定するもの。遠心力30 000〜60 000 m/s2{3 000〜6 000 g}で4〜25 ℃に自動温
度制御できるもの。
r) 試験管ミキサー
s)
白金線 直径約0.8 mmの白金線又はニクロム線を約80 mmに切断したもの。白金線ホルダーに取り
付けて使用する。使用の直前に火炎滅菌をし,菌の移植に支障のない程度に冷えてから使用する(11)。
6.3
器具などの滅菌操作 器具などの滅菌操作は,4.5による。
6.4
消毒操作 消毒操作は,4.6による。
6.5 試料の前処理 試料中のレジオネラをメンブレンフィルタによるろ過又は遠心分離によって濃縮し,
続いて低pH処理又は高温処理のいずれかを行う。
備考 レジオネラの菌数が非常に多い(10 000 個/100 ml以上)と予想される試料については,6.5.1の濃
縮操作を行わずに,直接ねじ口三角フラスコに試料を5 ml採取し,6.5.2の低pH処理又は高温
処理のいずれかを行う。
6.5.1
濃縮 メンブレンフィルタによるろ過又は遠心分離によって濃縮する。
a) メンブレンフィルタによる濃縮 メンブレンフィルタによる濃縮は,次による。
1) ろ過器下部のメンブレンフィルタの支持台(スクリーン)上に水(12)2,3滴を滴加(13)した後,ピンセ
ットを用いてメンブレンフィルタを置き,ろ過器に固定する。
2) よく振り混ぜて均一にした5.1の試料の適量(14)を,ろ過器に注ぎ入れ,吸引ろ過する(15)。ろ過後,
水(12)20〜30 mlを用いて上部ろ過管内壁を洗浄し,更に吸引ろ過する。この洗浄操作を2,3回繰り
返す。
8
K 0350-50-10:2006
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
3) ろ過が終了した後,ピンセットを用いてメンブレンフィルタをメンブレンフィルタの支持台から取
り外し,直ちにねじ口三角フラスコに入れる(16)。
4) メスピペットを用いて水(12)5 mlを加え,試験管ミキサーを用いて約1 分間激しく振り混ぜ,フィ
ルタ上の懸濁物をはく離させて均一な懸濁液にする。
注(12) 4.2の水について,高圧蒸気滅菌を約20分間行ったもの。
(13) あらかじめ水2,3滴を滴加しておくと,気泡が入りにくくなる。
(14) 試料は,100〜1 000 mlの一定量とする。試料中に存在すると予想されるレジオネラの菌数,懸
濁物,濁度などの試料の状況によって100〜1 000 mlの範囲で適量を用い調製する。
(15) 目詰まりをおこしやすい試料の場合は,試料の一定量をビーカーにとり,よく振り混ぜて少量
をろ過し,ろ過され終わる直前に再び少量を追加し,ろ過速度が遅くなったら追加を止める。
ビーカー中の残量から試料の量を求める。
(16) メンブレンフィルタに捕そく(捉)した懸濁物が,ピンセット及びフラスコの内壁に触れないよう
に注意する。
b) 遠心分離による濃縮 遠心分離による濃縮は,次による。
1) よく振り混ぜて均一にした5.1の試料の適量(14)を,複数の遠心管にとり,遠心機を用いて, 15〜
25 ℃の温度を維持しながら,遠心力60 000 m/s2{6 000 g}で10分間又は遠心力30 000 m/s2{3 000 g}
で30分間遠心分離する。
なお,遠心分離を停止する際には,沈殿物の巻き上げがないようにブレーキを使用せず自然に減
速する。
2) 沈殿物を巻き上げないように注意して上澄み液を駒込ピペットで吸引除去し,沈殿物を含めて残り
の体積を約5 mlにする。試験管ミキサーで沈殿物を溶液中に再懸濁させ,全量を菌体の捕集用に1
本の遠心管に合わせる。空になった遠心管は水(12)1〜2 mlで内部を洗浄し,この洗液も先の遠心管
に合わせる。
試料を入れたすべての遠心管についてこの操作を行い,再懸濁させた溶液及び洗液をすべて1 本
の菌体集積用の遠心管に集める。
3) 菌体の捕集用の遠心管を1)と同様に遠心分離する。沈殿物を巻き上げないように注意して上澄み液
を駒込ピペットで吸引除去し,沈殿物を含め残りの体積を4 mlにする。試験管ミキサーで沈殿物を
溶液中に再懸濁させ,全量をねじ口三角フラスコに移す。遠心管の内部を水(12)1 mlで洗浄し,この
洗液も,ねじ口三角フラスコに合わせる。
6.5.2
低pH処理又は高温処理 低pH処理又は高温処理は,次による。
a) 低pH処理
1) 6.5.1 a) 4)又は6.5.1 b) 3)のねじ口三角フラスコに塩酸-塩化カリウム混合溶液(pH2.2)5 mlを加え,試
験管ミキサーで約1 分間激しく振り混ぜた後,2〜4 分間放置し(17),試験用溶液とする。
注(17) 塩酸-塩化カリウム混合溶液(pH2.2)による処理時間が5 分間を超えるとレジオネラの回収率が
低下するので,1 分間の振り混ぜ後の放置時間は4 分間を超えないようにし,処理後,試験用
溶液は直ちに培地へ接種する。
b) 高温処理
1) 6.5.1 a) 4)又は6.5.1 b) 3)のねじ口三角フラスコを50±1 ℃の水浴中で30±1 分間加熱する。
2) 加熱後,直ちに冷水で冷却し,メスピペットで水(12)5 mlを加え,試験管ミキサーで約1 分間激し
く振り混ぜ,試験用溶液とする。
9
K 0350-50-10:2006
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
6.6
推定試験 推定試験は,次による。
a) 6.5.2で調製した試験用溶液の一定量(0.1〜0.25 ml)を,メスピペットを用いて,選択培地の寒天平板表
面の中央部に載せる。次いで,コンラージ棒を用い,試験用溶液が寒天平板培地に吸収されるまで平
板全面に均一に広げ,塗抹平板とする(18)。この操作を選択培地の寒天平板5〜10 枚について繰り返
す(19)。
注(18) 試験用溶液を塗抹する前に,培養器の中で選択平板培地のペトリ皿を逆さにしてふたを少し開
き,15 分間程度放置して寒天平板の表面をあらかじめ乾燥させておくと試験用溶液が速やかに
吸収される。また,JIS B 9920に規定する清浄度クラス3以上の環境(例えば,クリーンベンチ
内)で行えば,ペトリ皿のふたを大きく開けて水蒸気及び凝縮水を迅速に蒸発させることができ
る。
(19) レジオネラの集落数は1 枚当たり20〜100(個)がよい。
レジオネラの集落数が多いと予想される場合は,平板に接種する試験用溶液の量を少なくす
るか,6.5の備考によって濃縮操作を行わない低pH処理又は高温処理して調製した試験用溶液
を用いるか,若しくはJIS K 0350-10-10の6.5(試料の希釈)の操作によって希釈した試験用溶液
を用いて,6.6 a)と同時に培養する。
b) それぞれの塗抹平板に試験用溶液が残っていないことを確認した後,直ちにふたをし,逆さにして培
養器に入れ,36±1 ℃で5〜7日間培養する(20)(21)。
注(20) レジオネラは,ほかの細菌,かび(黴)などよりも増殖が遅いので,培養後,2日間目からは1〜2
日間おきに寒天平板を観察し,レジオネラと推定される集落の数を観察し,その都度記録する。
ほかの細菌及びかびの増殖によって推定レジオネラの集落の計数に支障が出るおそれがあると
判断された場合は,その時点で培養を中止し,推定レジオネラの集落数と培養日数とを記録す
る。
(21) 培養後2日間目以前に集落が出現した場合は,その集落の外観が推定レジオネラの集落に類似
していても,レジオネラ以外の細菌である可能性が高い。そのためそれ以後に出現してきた推
定レジオネラの集落とは明確に区別して記録する。
c) 培養後,塗抹平板上に形成された湿潤性の青白及び灰白の集落を推定レジオネラと判定し,その数を
記録する(20)。レジオネラと判定された集落すべて又は一部について確定試験を行う(22)。
注(22) 寒天平板1 枚に出現した推定レジオネラの集落数が10 個以下の場合は,すべての集落につい
て確定試験を行う。10 個を超える場合は集落の外観を考慮して代表的な集落10 個について確
定試験を行う。
備考 培養後の使用済み培地は,必ずペトリ皿のまま,高圧蒸気滅菌をしてから廃棄する。
6.7
確定試験 確定試験は,次による。
a) 6.6でレジオネラと推定された集落のすべて又は一部(22)について,白金線で集落から菌体をごく少量
とり,BCYEα寒天平板培地に,それぞれ画線塗抹する(23)。直ちにふたをし,逆さにして培養器に入
れ,36±1 ℃で2〜7 日間培養する(21)(24)。
注(23) 白金線は,次の集落を操作する前に必ず火炎滅菌を行うか,集落ごとに新たな白金線を用いる。
また,画線する際に寒天培地平板の表面をきずつけないように注意する。
(24) 2 日間以上培養し,BCYEα寒天平板培地にレジオネラの集落が形成されれば,7 日間まで培養
しなくてもその時点で培養をうち切ってよい。
b) 培養後,それぞれの平板上に形成された単独の集落から白金線で菌体をごく少量とり,L-システイン
10
K 0350-50-10:2006
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
を含まない寒天平板培地及びBCYEα寒天平板培地に,それぞれ平板塗抹法によって画線塗抹する
(23)(25)。直ちにふたをし,逆さにして培養器に入れ,36±1 ℃で2〜7 日間培養する(21)(24)。
注(25) L-システインを含まない寒天平板培地とBCYEα寒天平板培地に画線塗抹する際は,L-システ
インを含まない寒天平板培地へのL-システインの持ち込みを防ぐため,必ずL-システインを含
まない寒天平板培地から先に画線する。
c) 培養後,L-システインを含まない寒天平板培地では集落を形成せず,BCYEα寒天平板培地だけで集
落を形成したものについて,グラム染色を行う(26)。
注(26) グラム染色の操作は,附属書1による。
d) グラム染色によってグラム陰性のかん(桿)菌と確認されたものについて,レジオネラと確定し,式(1)
によって試料中の菌数を算出する。
V
P
C
v
v
v
V
p
p
p
N
n
n
100
)
(
)
(
c
c
2
1
1
2
1
×
×
+
+
×
+
+
=
Λ
Λ
··············································· (1)
ここに,
N: 確定レジオネラ数(個/100 ml)
p1,p2,…pn: 選択培地の平板培地各々に出現した推定レジオネラの集
落数
v1,v2,…vn: 平板培地の各々に塗抹した試験用溶液(ml)
V: 濃縮に用いた試料(ml)(27)
Pc: 確定試験に供した推定レジオネラの集落の数
Cc: 確定試験でレジオネラと確定された集落の数
V1: 6.5.2で調製した試験用溶液(ml)
注(27) 試料の濃縮を行わずに試料を直接低pH処理又は高温処理した場合は5 ml。
備考 6.6の備考による。
7. 結果の表示 6.7で得られたレジオネラ数(個/100 ml)は,有効数字2けたに数値を丸める。
結果には,試料の採取場所,採取日時,試験日時,用いた培地及び式(2)によって求めた検出下限値を付
記する。
V
v
v
v
V
Dl
n
100
)
(
2
1
1
×
+
+
=
Λ
······················································ (2)
ここに,
Dl: 検出下限値(個/100 ml)
v1,v2,…vn: 平板培地の各々に塗抹した試験用溶液(ml)
V: 濃縮に用いた試料(ml)(27)
V1: 6.5.2で調製した試験用溶液(ml)
11
K 0350-50-10:2006
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
付表1 引用規格
JIS B 7132 生物顕微鏡
JIS B 9920 クリーンルーム中の空気清浄度の評価方法
JIS K 0050 化学分析方法通則
JIS K 0101 工業用水試験方法
JIS K 0102 工場排水試験方法
JIS K 0211 分析化学用語(基礎部門)
JIS K 0350-10-10 用水・排水中の一般細菌試験方法
JIS K 0550 超純水中の細菌数試験方法
JIS K 0557 用水・排水の試験に用いる水
JIS K 0950 プラスチック製滅菌シャーレ
JIS K 8101 エタノール(99.5)(試薬)
JIS K 8102 エタノール(95)(試薬)
JIS K 8121 塩化カリウム(試薬)
JIS K 8150 塩化ナトリウム(試薬)
JIS K 8180 塩酸(試薬)
JIS K 8263 寒天(試薬)
JIS K 8291 グリシン(試薬)
JIS K 8294 クリスタルバイオレット(試薬)
JIS K 8470 L-システイン塩酸塩一水和物(試薬)
JIS K 8521 しゅう酸アンモニウム一水和物(試薬)
JIS K 8574 水酸化カリウム(試薬)
JIS K 8576 水酸化ナトリウム(試薬)
JIS K 8637 チオ硫酸ナトリウム五水和物(試薬)
JIS K 8913 よう化カリウム(試薬)
JIS K 8920 よう素(試薬)
JIS K 8951 硫酸(試薬)
JIS R 3503 化学分析用ガラス器具
JIS R 3505 ガラス体積計
JIS R 3703 顕微鏡用スライドガラス
JIS T 1701 医療用遠心機
JIS T 1702 ふ(孵)卵器
JIS T 7322 医療用高圧蒸気滅菌装置
JIS T 7324 医療用小形高圧蒸気滅菌器

2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書1(規定)グラム染色法
序文 この規格は,本体6.7確定試験において,レジオネラ菌であることをグラム染色によって確定する
ための方法を規定したものである。
グラム染色法 この方法は,本体6.6推定試験でレジオネラと推定された集落から,BCYEα寒天平板培地
だけで集落を形成したものを対象として,クリスタルバイオレット溶液,よう素溶液及びサフラニン溶液
を用いて染色し,グラム陰性のかん(桿)菌を判定する方法である。
a) 試薬 試薬は,次による(1)。
注(1)
市販の染色セットを用いてもよい。
1) エタノール(99.5) JIS K 8101に規定するもの。
2) クリスタルバイオレット溶液 JIS K 8294に規定するクリスタルバイオレット約11 gを乳鉢で細か
くすりつぶし,その10 .0gをとり,JIS K 8101に規定するエタノール(99.5)100 mlを少量ずつ加えて
溶かした後,ろ紙5種Bでろ過する。この溶液20 mlとしゅう酸アンモニウム溶液(JIS K 8521に規
定するしゅう酸アンモニウム一水和物0.8 gを水80 mlに溶かす。)80 mlとを混合する。褐色瓶に入
れて保存する。
3) よう素溶液(3.33g/L) JIS K 8913に規定するよう化カリウム2.0 gを水約50 mlに溶かし,この溶液
にJIS K 8920に規定するよう素1.0gを加えて溶かした後,水を加えて300 mlとする。
4) サフラニン溶液 サフラニンT(3,7-ジアミノ-2,8-ジメチル-5-フェニルフェナジニウムクロリド)2.5
gをエタノール(99.5)100 mlに少量ずつ加え溶かす。これをろ紙5種Bでろ過して褐色瓶に入れ,室
温で保存する。使用時に水で10 倍に薄める。
b) 操作 操作は,次による。
1) 清浄なスライドガラスに水(2)1 滴を滴加し,白金線でBCYEα寒天平板培地だけに発育した集落か
らごく少量の菌体をとる。これをスライドガラスの上の水(2)とよく混ぜながら薄く均一に塗り広げ,
自然乾燥する。このとき塗抹面がかなり薄い白に見える程度にする。次に,塗抹面を上にして弱い
火炎中をゆっくり3 回通して固定する(3)。
2) クリスタルバイオレット溶液を塗抹面の全体に滴加し,ゆっくり動かしながら約1 分間染色する。
染色後,塗抹面を下にしたスライドガラスに流水を静かにそそぎ,色素をよく洗い流す。
3) よう素溶液(3.33 g/L)を繰り返し滴加して約1 分間染色する。染色後,塗抹面を下にしたスライドガ
ラスに流水を静かにそそぎ,色素をよく洗い流す。
4) エタノール(99.5)を繰り返しそそぎながら,約30 秒間脱色する。軽く水洗してよく水切りする。
5) サフラニン溶液を塗抹面に滴加して約1 分間染色する。染色後,塗抹面を下にしたスライドガラス
に流水を静かにそそぎ,色素をよく洗い流した後,スライドガラスを横に立てて自然乾燥する。
6) スライドガラスの塗抹面に顕微鏡用オイルを1 滴を滴加し,液浸系対物レンズ(×100)を用いて検鏡
する。
7) 淡紅に染色されているものをグラム陰性菌,濃紫に染色されたものをグラム陽性菌と判定し,球状
のものを球菌,かん(桿)状のものをかん(桿)菌と判定する(4)。
注(2)
本体注(12)による。
14
K 0350-50-10:2006
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
(3)
固定が不完全であると,塗抹面が水洗操作中にはく離してしまう。
(4)
グラム陰性のかん(桿)菌の対照として大腸菌(Escherichia coli)及びグラム陽性の球菌の対照
として腸球菌(Entercoccus faecalis,Entercoccus faecium など)を用い,試料と同時に染色して
比較すると判定が容易である。
15
K 0350-50-10:2006
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
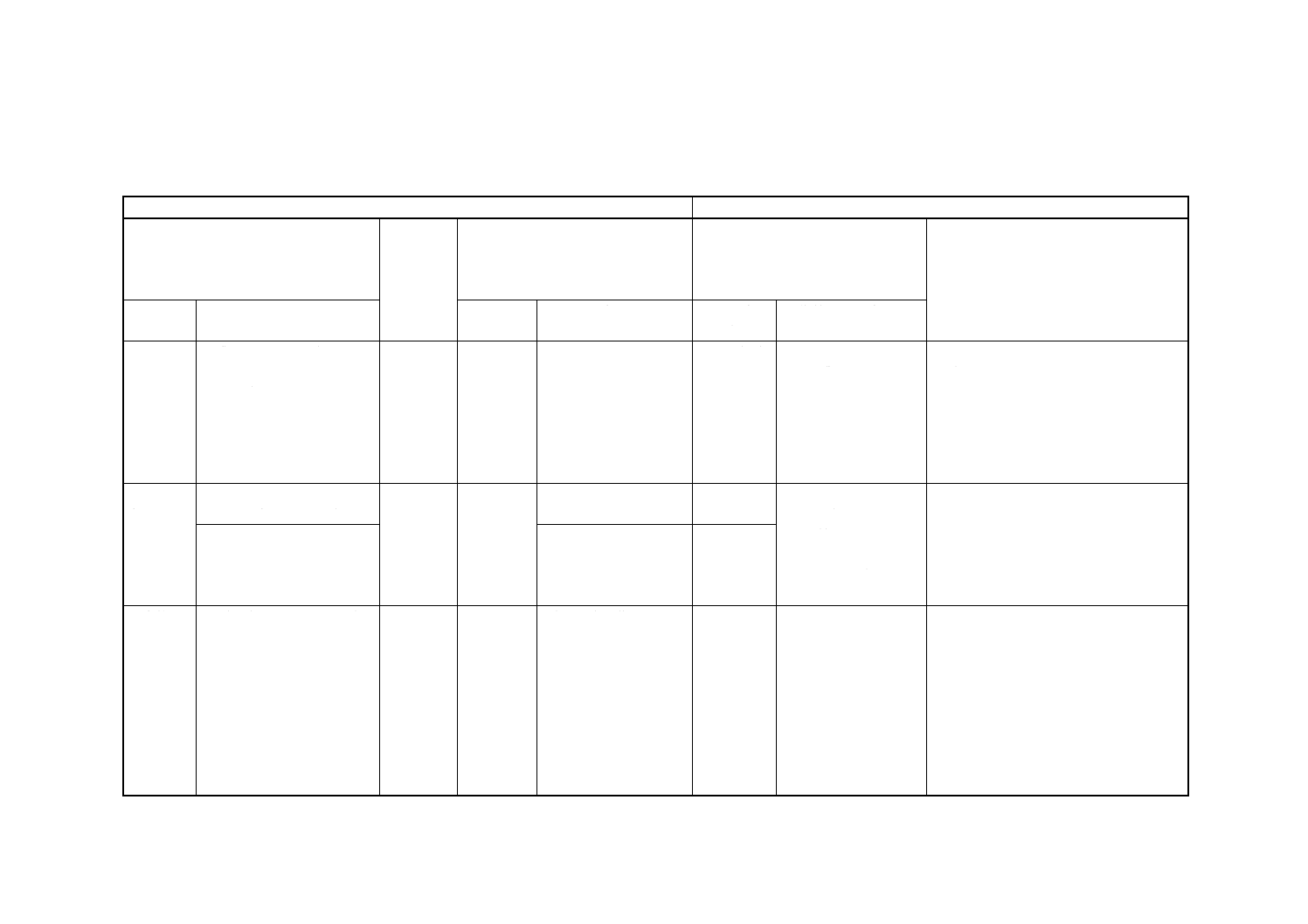
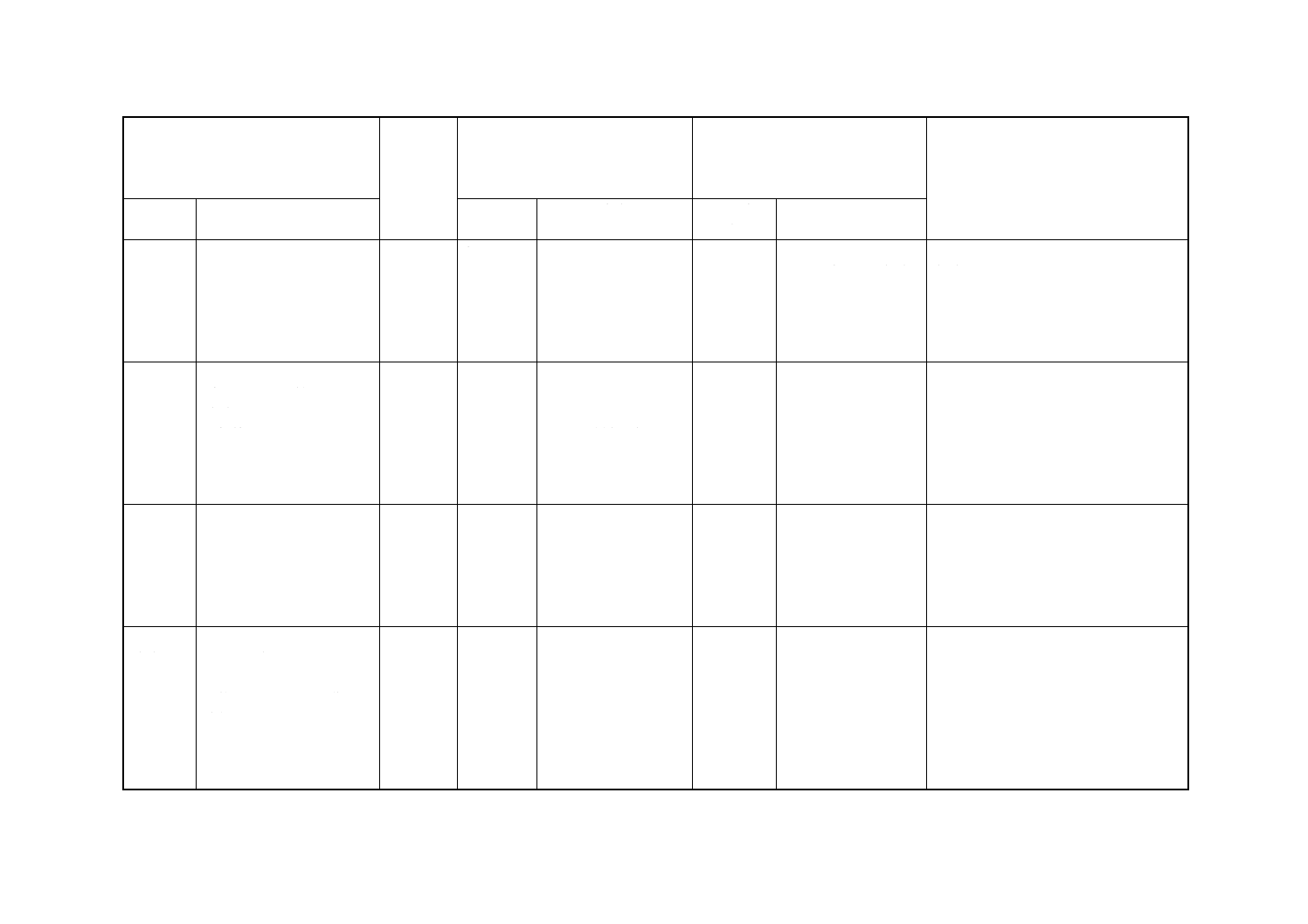
附属書2(参考)JISと対応する国際規格との対比表
JIS K 0350-50-10:9999 工業用水・工場排水中のレジオネラ試験方法
ISO 11731:1998,水質−レジオネラの検出と計数
(Ⅰ) JISの規定
(Ⅱ) 国際
規格番号
(Ⅲ) 国際規格の規定
(Ⅳ) JISと国際規格との技術的差異
の項目ごとの評価及びその内容
表示箇所:本体
表示方法:側線又は点線の下線
(Ⅴ) JISと国際規格との技術的差異の理由
及び今後の対策
項目
番号
内容
項目
番号
内容
項目ごと
の評価
技術的差異の内容
1.適用範
囲
工業用水及び工場排水中の
レジオネラの試験方法につ
いて規定。
ISO 11731 1
水道水,工業用水及び
自然水並びにこれらに
付随する底質,沈殿物,
スライムなどの環境試
料中のレジオネラの検
出及び計数のための培
養法を規定。
MOD/削除
JISは,環境試料とし
て,工業用水及び工場
排水に限定。
JISは,工業標準化法の対象に限定して
規定。
4.以降の試験方法の規定についても,
ISO規格と差異がある箇所もあるが,こ
れらについては今後更に整合化を検討
する。
2.引用規
格
JIS 32規格(付表1に記載)
を引用規格として規定。
2
−
MOD/追加
試薬などについて,
ISO規格は分析用水
の水質だけを引用規
格で規定。JISは,分
析用水に限定せず規
定。
試験方法として,試薬などの仕様を規定
することが必要なため。
−
ISO 3696
MOD/削除
3.定義
レジオネラ属に属するグラ
ム陰性かん(桿)菌で選択
培地で培養したときに,青
白から灰白の集落を形成,
L-システインを要求するも
の。
備考に危険性を提示。
3
4
グラム陰性菌に属し,
L-システイン及び鉄を
含む培地で,白,青,
ライムグリーン色の集
落を形成。
レジオネラの危険性を
提示。
MOD/変更
表現は異なるが,内容
は同じ。
−
1
5
K
0
3
5
0
-5
0
-1
0
:
2
0
0
6
16
K 0350-50-10:2006
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
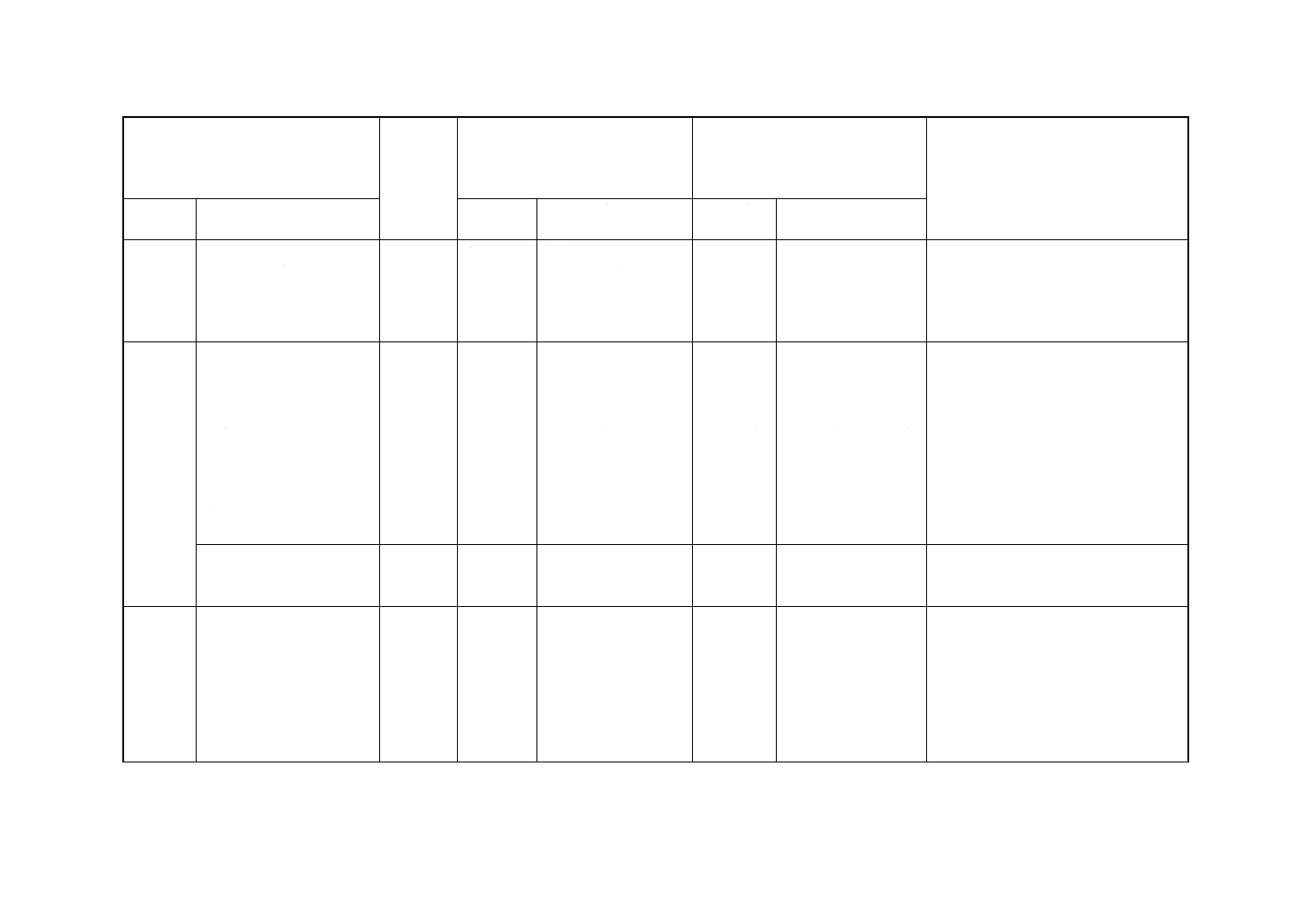
(Ⅰ) JISの規定
(Ⅱ) 国際
規格番号
(Ⅲ) 国際規格の規定
(Ⅳ) JISと国際規格との技術的差異
の項目ごとの評価及びその内容
表示箇所:本体
表示方法:側線又は点線の下線
(Ⅴ) JISと国際規格との技術的差異の理由
及び今後の対策
項目
番号
内容
項目
番号
内容
項目ごと
の評価
技術的差異の内容
4.共通事
項
共通事項として,化学分析
通則,水,試薬,ガラス器
具,器具などの滅菌及び除
菌操作並びに消毒について
規定
6
7
試薬,器具などは,本
文中で記述している
が,共通事項としての
取扱いではない。
MOD/追加
JISは共通事項として
一般的な概要を記載
し,かつ,器具類の消
毒方法を記載。
JISの規定に従い共通事項を記載。
5.試料
5.1試料
の採取
試料容器は,共栓ガラス瓶
を乾燥若しくは高圧蒸気滅
菌したもの又は滅菌済みの
細菌試験用ポリエチレン瓶
を使用。
採水器は,表層,各深度,
給水栓からの採取としてハ
イロート,バンドーン採水
器を用いる。
8
8.1
ガラス瓶,ポリエチレ
ン又は同様な容器を高
圧滅菌したものを採取
容器とする。高圧滅菌
できない容器は低温殺
菌する。小さな滅菌容
器は,スライム,底質
採取に用い,広口容器
でスクリューキャップ
で栓をする。
MOD/削除
MOD/追加
JISは,滅菌後の共栓
ガラス瓶又は細菌試
験用のポリエチレン
瓶に限定。
JISは,採水器及び採
取場所による採水法
を追加。
JIS適用外のスライム,底質などの採取
容器を削除。
採水器及び採取場所による採水法をJIS
K 0094を参考に追加規定した。
残留塩素など酸化性物質が
あるときは,還元剤を入れ
た容器に採取する。
8.2
JISと同じ。
IDT
−
−
5.2試料
の取扱い
試験は採取後直ちに行う。
できない場合は,0〜5 ℃の
暗所に保存。
8.3
試料は6 ℃以上18 ℃
以下で光,熱を避け輸
送。できる限り早く試
験を行う。
MOD/変更
MOD/削除
ISO規格は,運搬の条
件を詳細に示し,試験
室に搬入してからの
保存法を規定してい
ない。
JIS K 0094を参考として規定した。
1
6
K
0
3
5
0
-5
0
-1
0
:
2
0
0
6
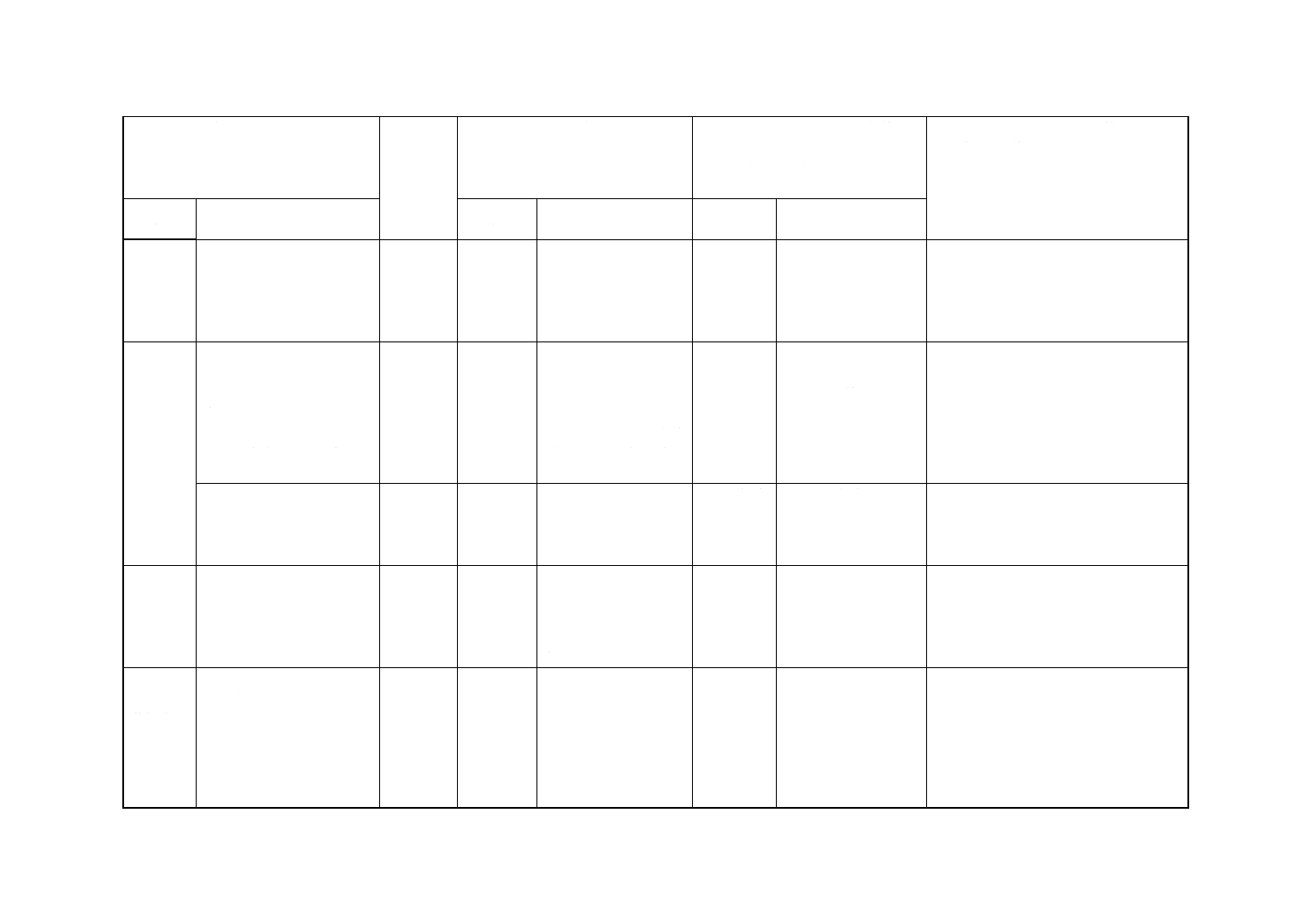
17
K 0350-50-10:2006
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
(Ⅰ) JISの規定
(Ⅱ) 国際
規格番号
(Ⅲ) 国際規格の規定
(Ⅳ) JISと国際規格との技術的差異
の項目ごとの評価及びその内容
表示箇所:本体
表示方法:側線又は点線の下線
(Ⅴ) JISと国際規格との技術的差異の理由
及び今後の対策
項目
番号
内容
項目
番号
内容
項目ごと
の評価
技術的差異の内容
6.試験方
法
試料中のレジオネラをフィ
ルタ又は遠心分離にによっ
て濃縮し,酸又は加熱処理
後選択培地で培養し,集落
を判定し計数する。
5
JISと同じ。
IDT
−
−
6.1試薬
培養培地(確認用)用選択
培地としてのGVPCα又は
WYOα寒天培地,BCYEα
寒天平板培地,L-システイ
ンを含まないBCYEα培地
及び関連試薬類を規定。
6
選択培地としてGVPC
培地を培養培地とし
て,BCYEα寒天培地
L-システインを含まな
いBCYEα培地,血清
試薬及び関連の試薬
類。
MOD/選択
ISO規格の選択培地
のほかに,WYOα寒
天培地の使用も可と
した。
我が国で繁用されている選択培地を追
加。レジオネラの検出能力には差がな
い。
WYOα培地をISOに提案することを検
討する。
−
6.2.4
培地成分変質変動を見
るために血清形1の3
日間の培養で増殖する
か確認する。
MOD/削除
JISは,血清形による
免疫学的な手法を採
用していない。
工業用水中のレジオネラを血清形で同
定する必要性は認められないため削除。
今後採用するか検討する。
6.2器具
及び装置
使用ガラス器具,メンブレ
ンフィルタ,ろ過器,顕微
鏡,培養器,医療用遠心機
及び関連部品などを規定。
7
使用ガラス器具,メン
ブレンフィルタ,ろ過
器,顕微鏡,培養器,
医療用遠心機及び関連
部品など。
MOD/削除
JISは,ISO規格の蛍
光顕微鏡を削除。
免疫学的手法を採用しないために,削
除。
今後採用するか検討する。
6.3器具
などの滅
菌操作
6.4消毒
操作
4.共通事項に記載し引用し
ている。
−
−
MOD/追加
JISは,器具,使用済
器具について消毒操
作を規定。
器具などの滅菌は必す(須)のものであ
り,試験方法に追加。
ISOに提案することを検討する。
1
7
K
0
3
5
0
-5
0
-1
0
:
2
0
0
6
18
K 0350-50-10:2006
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
(Ⅰ) JISの規定
(Ⅱ) 国際
規格番号
(Ⅲ) 国際規格の規定
(Ⅳ) JISと国際規格との技術的差異
の項目ごとの評価及びその内容
表示箇所:本体
表示方法:側線又は点線の下線
(Ⅴ) JISと国際規格との技術的差異の理由
及び今後の対策
項目
番号
内容
項目
番号
内容
項目ごと
の評価
技術的差異の内容
6.5試料
の前処理
6.5.1
濃
縮
水試料をメンブレンフィル
タによるろ過又は遠心分離
によって濃縮。
9
9.1
水試料をメンブレンフ
ィルタによるろ過又は
遠心分離によって濃
縮。底質,スライム及
び沈殿物については希
釈して直接培養。
MOD/削除
JISは,底質,スライ
ム及び沈殿物を削除。
水試料以外はJISの適用範囲外であり
削除。
JISとして規格外であるので対応できな
い。
6.5.2
低
pH処理
又は高温
処理
試料をpH2.2で1分振り混
ぜ後2〜4分間放置。
試料を50±1 ℃で30±1分
間加熱。
9.2
9.2.1
9.2.3
9.2.2
試料を酸・熱処理に分
ける。
pH2.2酸緩衝液で5±
0.5分間放置
50±1 ℃で30±2分間
加熱。
MOD/変更
低pH処理,高温処理
については操作内容
はほぼ一致している。
−
6.6推定
試験
試料を選択培地の寒天培地
には(播)種し,36±1 ℃,
5〜7日間培養する。平板上
の青白及び灰白の集落をレ
ジオネラと推定。
9.2.4
9.2.5
試料をGVPC寒天培地
は(播)種し,36±1 ℃,
10日間以上培養する。
レジオネラの集落は白
−灰色−青−紫色を呈
する。
MOD/変更
培養日数が異なる
培養日数は最大7日で判定できるため。
今後採用するか、さらに検討する。
6.7確定
試験
推定した集落の菌体を
BCYEα寒天培地には(播)
種し,36±1 ℃で2〜7日間
培養する。平板上の集落の
菌体を,BCYEα寒天培地
及びL-システイン不含寒
天培地には(播)種し,36±
1 ℃で2〜7日間培養する。
9.3
JISと同じ。
IDT
−
−
1
8
K
0
3
5
0
-5
0
-1
0
:
2
0
0
6
19
K 0350-50-10:2006
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
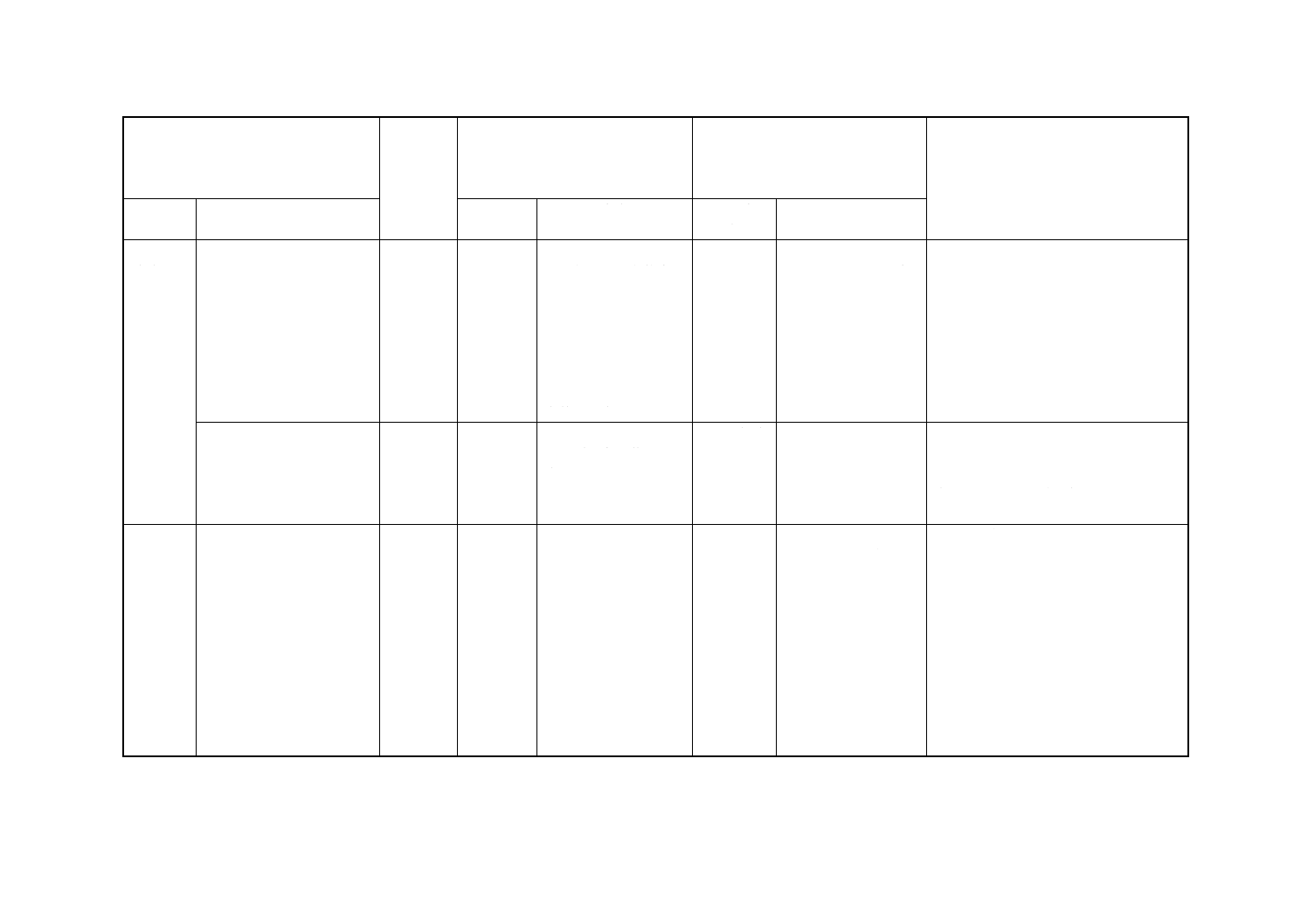
(Ⅰ) JISの規定
(Ⅱ) 国際
規格番号
(Ⅲ) 国際規格の規定
(Ⅳ) JISと国際規格との技術的差異
の項目ごとの評価及びその内容
表示箇所:本体
表示方法:側線又は点線の下線
(Ⅴ) JISと国際規格との技術的差異の理由
及び今後の対策
項目
番号
内容
項目
番号
内容
項目ごと
の評価
技術的差異の内容
6.7確定
試験
(続き)
L-システインを含まない寒
天培地で集落を形成せず,
BCYEα寒天培地だけで集
落を形成したものをグラム
染色しグラム陰性のかん菌
をレジオネラと確定し菌数
を算出する。
9.3
ノート:BCYE-Cys培
地の代わりに栄養寒天
培地,血液寒天培地も
使用できる。
BCYE-Cys培地で集落
を形成せず,BCYEα
寒天培地だけで集落を
形成したものを,血清
学的に同定する。
MOD/変更
培養結果の判定後の
確認は,JISではグラ
ム染色によって,ISO
規格では血清学的に
判定する。
用水・排水中のレジオネラについて,水
質の評価,管理を目的とする検査では血
清学的な判定は不要であり,この手法は
専門的な臨床検査技術及び経験が必要
であり,JISでは不採用。
今後必要があれば、採用を検討する。
−
9.3.2
AnnexCの方法によっ
てレジオネラ菌種の同
定を行う。
MOD/削除
−
免疫蛍光法は参考法であり,ISO規格の
レジオネラの定義にこの手法はふれら
れていない。
今後必要があれば参考法として採用を
検討する。
7.結果の
表示
レジオネラ数(個/100 ml)
は,有効数字2けたに数値
を丸める。結果には,採取
場所,日時,試験日時,用
いた培地及び検出下限値を
付記する。
10
11
レジオネラ集落数
(CFU)の推定は3枚の
平板から集落を同定し
た最大個数とする。
報告書には,規格の引
用,採取場所・採取法・
試料の性状,試験試料
量,採取日時・試験室
受取日時・試験日時,
必要と思われる情報を
記載する。
MOD/変更
JISは,試料100 ml
中の個数を計算式に
よって算出,ISO規格
は,具体的な算出法を
規定していない。
具体的な算出法をJISとして採用。
ISOに提案することを検討する。
1
9
K
0
3
5
0
-5
0
-1
0
:
2
0
0
6
20
K 0350-50-10:2006
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
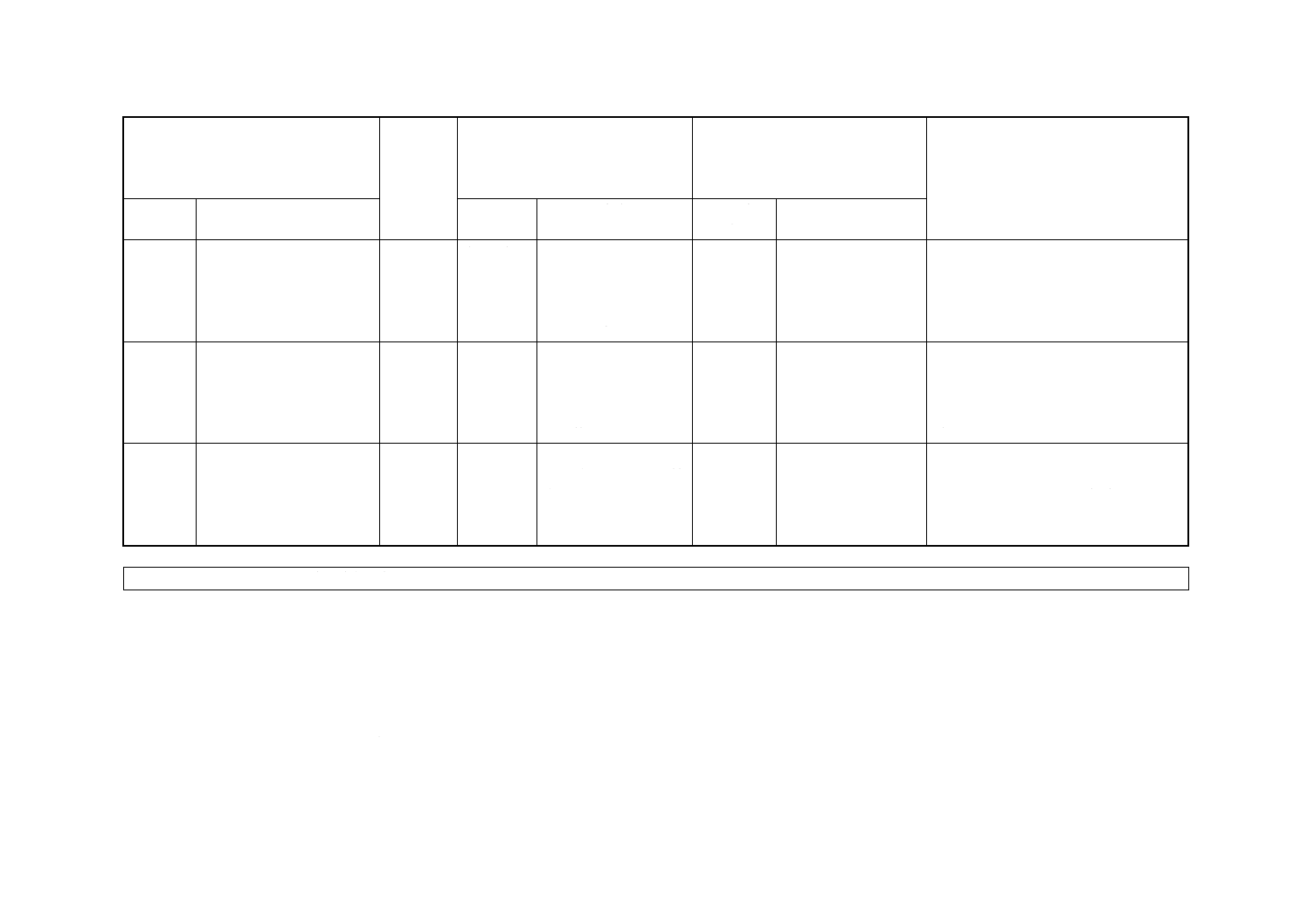
(Ⅰ) JISの規定
(Ⅱ) 国際
規格番号
(Ⅲ) 国際規格の規定
(Ⅳ) JISと国際規格との技術的差異
の項目ごとの評価及びその内容
表示箇所:本体
表示方法:側線又は点線の下線
(Ⅴ) JISと国際規格との技術的差異の理由
及び今後の対策
項目
番号
内容
項目
番号
内容
項目ごと
の評価
技術的差異の内容
−
−
AnnexA
(参考)
メンブレンフィルタか
らの細菌のかきとり
法,試料を通したフィ
ルタを滅菌セルスクラ
パーでかきとる。
MOD/削除
−
参考法であり規格ではないので削除
今後必要があれば参考法として採用を
検討する。
−
−
AnnexB
(参考)
BCYE-Cysの集落確認
血液寒天培地及び栄養
寒天培地もレジオネラ
のシステイン要求性確
認に使用できる。
MOD/削除
−
JIS,ISO規格本体の培地で十分確認で
きる。
規格ではないため削除
今後必要があれば参考法として採用を
検討する。
−
−
AnnexC
(参考)
レジオネラニューモフ
ィラ確認のための間接
免疫蛍光法。
MOD/削除
−
免疫蛍光法は参考法であり,ISO規格の
レジオネラの定義にこの手法はふれて
いない。このためJISは削除。
今後必要があれば参考法として採用を
検討する。
JISと国際規格との対応の程度の全体評価:MOD
備考1. 項目ごとの評価欄の記号の意味は,次のとおりである。
― IDT………国際規格と一致している。
― MOD/削除……… 国際規格の規定項目又は規定内容を削除している。
― MOD/追加……… 国際規格にない規定項目又は規定内容を追加している。
― MOD/変更……… 国際規格の規定内容を変更している。
― MOD/選択……… 国際規格の規定内容と別の選択肢がある。
2.
JISと国際規格との対応の程度の全体評価欄の記号の意味は,次のとおりである。
― MOD…………… 国際規格を修正している。
2
0
K
0
3
5
0
-5
0
-1
0
:
2
0
0
6