B 8223:2015
(1)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
目 次
ページ
序文 ··································································································································· 1
1 適用範囲························································································································· 1
2 引用規格························································································································· 1
3 用語及び定義 ··················································································································· 1
4 水処理方式 ······················································································································ 4
5 給水及びボイラ水の水質に関する一般事項 ············································································ 4
5.1 給水の水質 ··················································································································· 4
5.2 ボイラ水の水質 ············································································································· 4
5.3 補給水の水質 ················································································································ 5
5.4 水質管理項目の測定値が管理値を逸脱した場合 ···································································· 5
5.5 起動時及び停止中の場合 ································································································· 5
6 丸ボイラの水質 ················································································································ 5
6.1 丸ボイラの給水の水質 ···································································································· 5
6.2 丸ボイラのボイラ水の水質 ······························································································ 6
7 特殊循環ボイラの水質 ······································································································· 7
7.1 単管式特殊循環ボイラの水質 ··························································································· 7
7.2 多管式特殊循環ボイラの水質 ··························································································· 9
8 水管ボイラ,循環ボイラの水質 ·························································································· 11
8.1 産業用水管ボイラの水質(軟化水を使用する場合) ····························································· 11
8.2 産業用水管ボイラの水質(イオン交換水を使用する場合) ···················································· 13
8.3 電力事業用循環ボイラの水質 ·························································································· 20
9 電力事業用排熱回収ボイラの水質 ······················································································· 22
9.1 一般 ··························································································································· 22
9.2 給水の水質 ·················································································································· 23
9.3 ボイラ水の水質 ············································································································ 23
10 貫流ボイラの水質 ·········································································································· 24
10.1 水質の管理項目及び管理値 ···························································································· 24
10.2 水質に関する留意事項 ·································································································· 24
11 蒸気の質 ······················································································································ 32
11.1 蒸気の質の管理項目及び管理値 ······················································································ 32
11.2 蒸気の質に関する留意事項 ···························································································· 32
12 試験 ···························································································································· 33
附属書A(参考)ボイラ水の水処理方式 ·················································································· 34
附属書B(参考)ボイラの給水及びボイラ水の水質の管理項目 ····················································· 69
附属書C(参考)補給水の水質 ······························································································ 81
B 8223:2015 目次
(2)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
ページ
附属書D(参考)水質管理項目が管理値を逸脱した場合の一般的対処方法 ······································ 83
参考文献 ···························································································································· 87
B 8223:2015
(3)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
まえがき
この規格は,工業標準化法第14条によって準用する第12条第1項の規定に基づき,一般社団法人火力
原子力発電技術協会(TENPES)及び一般財団法人日本規格協会(JSA)から,工業標準原案を具して日本
工業規格を改正すべきとの申出があり,日本工業標準調査会の審議を経て,経済産業大臣が改正した日本
工業規格である。
これによって,JIS B 8223:2006は改正され,この規格に置き換えられた。
この規格は,著作権法で保護対象となっている著作物である。
この規格の一部が,特許権,出願公開後の特許出願又は実用新案権に抵触する可能性があることに注意
を喚起する。経済産業大臣及び日本工業標準調査会は,このような特許権,出願公開後の特許出願及び実
用新案権に関わる確認について,責任はもたない。
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
日本工業規格 JIS
B 8223:2015
ボイラの給水及びボイラ水の水質
Water conditioning for boiler feed water and boiler water
序文
この規格は,1961年に制定され,その後6回の改正を経て今日に至っている。前回の改正は2006年に
行われたが,その後のボイラ水処理の運用実績及び技術の進展に対応するために改正した。
なお,対応国際規格は現時点で制定されていない。
1
適用範囲
この規格は,陸用ボイラ及び船用蒸気ボイラの給水及びボイラ水の水質について規定する。
2
引用規格
次に掲げる規格は,この規格に引用されることによって,この規格の規定の一部を構成する。これらの
引用規格は,その最新版(追補を含む。)を適用する。
JIS B 0126 火力発電用語−ボイラ及び附属装置
JIS B 0127 火力発電用語−蒸気タービン及び附属装置並びに地熱発電設備
JIS B 8224 ボイラの給水及びボイラ水−試験方法
JIS K 0556 超純水中の陰イオン試験方法
3
用語及び定義
この規格で用いる主な用語及び定義は,JIS B 0126,JIS B 0127及びJIS B 8224によるほか,次による。
3.1
常用使用圧力
実運用上の最高圧力。
3.2
伝熱面蒸発率
単位蒸発面積について1時間当たりの蒸発量[kg/(m2・h)]。
3.3
陸用ボイラの用語
3.3.1
水管ボイラ,循環ボイラ
伝熱面が水管で構成されており,自然循環又は強制循環するボイラ及び貫流ボイラ。
3.3.2
丸ボイラ
2
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
胴を主体とし,その内部に炉筒,火室,煙管などを設けたボイラ。立てボイラ,炉筒ボイラ,煙管ボイ
ラ,炉筒煙管ボイラなどがある。
3.3.3
単管式特殊循環ボイラ
単一又は数本の管をら旋状に巻いた構成で,強制流動式に一端から押し込まれた水を加熱蒸発させて他
端から汽水混合蒸気を取り出し,汽水分離器によって飽和蒸気と飽和水とを分離し,分離された飽和水が
大気に開放された脱気タンクに戻り,補給水と混合され,再び加熱水管に供給される貫流ボイラ。
3.3.4
多管式特殊循環ボイラ
管が全て上昇管である2本以上の加熱管及び管寄せによって構成され,一端から水を送り込み,他端か
ら汽水混合物を取り出し,汽水分離器で分離後,加熱管へ戻る熱水の量が汽水混合物の50 %以下となる水
管ボイラ。
3.3.5
産業用水管ボイラ
電力事業用以外の事業に供する水管ボイラ。産業用循環ボイラともいう。
3.3.6
電力事業用循環ボイラ
主に発電用蒸気タービン及び発電所施設に供給する蒸気を発生させる循環ボイラ。電力事業用水管ボイ
ラともいう。
3.3.7
廃熱ボイラ
炉,その他の排ガスの余熱を回収して蒸気を発生させるボイラ。
3.3.8
排熱回収ボイラ
ガスタービンの排気及びプロセスガスからの熱を回収して蒸気を発生させるボイラ。
3.3.9
電力事業用排熱回収ボイラ
発電用ガスタービンの排熱を回収ボイラの熱源とし,複数圧ドラムと多数の加熱水管とで構成され,水
管内で発生した蒸気を主に発電用蒸気タービン及び発電所施設に供給するボイラ。
3.3.10
貫流ボイラ
給水を管の一端からポンプで押し込み,管の他端から蒸気を取り出すボイラ。
3.4
船用ボイラの用語
3.4.1
船用主ボイラ
主機関を駆動させるために必要な蒸気を作るボイラ。蒸気タービン船に搭載する。
3.4.2
船用補助ボイラ
主機関駆動以外の補機の駆動,油タンク加熱,船内空調設備などに必要な蒸気を作るボイラ。ディーゼ
3
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
ル船に搭載される。
3.5
用水の種類の用語
3.5.1
原水
河川水,地下水,水道水,工業用水などの,まだ給水処理をしていない水。
3.5.2
補給水
ボイラへ補給する水。軟化水,イオン交換水,蒸留水などがある。
3.5.3
軟化水
水道水,工業用水,地下水,河川水,湖沼水などの原水を,陽イオン交換樹脂を充塡した軟化装置で処
理した硬度CaCO3: 1 mg/L以下の水。
3.5.4
イオン交換水
陽イオン交換樹脂と陰イオン交換樹脂とを用いたイオン交換装置で精製した水。
3.5.5
復水
ボイラから発生した蒸気の使用箇所(蒸気タービンなど)以降の系統で凝縮した水で,サイクル内に戻
る水。
3.5.6
給水
給水ポンプによってボイラ入口[エコノマイザ(節炭器)がある場合は,エコノマイザ入口]に供給さ
れる復水と補給水との混合水。
3.5.7
ボイラ水
ボイラの内部で濃縮された水。一般には,ドラム内の水とする。
3.5.8
蒸気の過熱低減器スプレー水
蒸気の過熱を抑制・防止するために注入する冷却用の水。ボイラ給水を利用する場合が多い。
3.6
ボイラの水処理方式の種類の用語
3.6.1
アルカリ処理
ボイラ水のpHを主として水酸化ナトリウムで調節し,りん酸イオンの濃度をりん酸塩(主としてナト
リウム塩)で調節する処理方法。
3.6.2
りん酸塩処理
ボイラ水のpH及びりん酸イオンの濃度をりん酸ナトリウム塩で調節する処理方法。
4
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
3.6.3
揮発性物質処理
給水だけ又は給水及びボイラ水のpHの調節にアンモニア又は揮発性のアミンを用い,溶存酸素の除去
にはヒドラジンを用い,揮発性物質だけで処理する方法。ヒドラジンなどの脱酸素剤の使用の有無,酸化
還元雰囲気の程度によって次の3種類の処理方式に区分される。
a) 還元形[AVT(R): All-volatile Treatment (Reducing)] ヒドラジンなどの脱酸素剤を添加し,積極的に還
元雰囲気とする給水処理。
b) 低酸化形[AVT(LO): All-volatile Treatment (Low Oxidizing)] ヒドラジンなどの脱酸素剤が無添加の給
水処理で,溶存酸素濃度5 μg/L未満のもの。
c) 酸化形[AVT(O): All-volatile Treatment (Oxidizing)] ヒドラジンなどの脱酸素剤が無添加の給水処理で,
溶存酸素濃度5 μg/L以上20 μg/L未満のもの。
3.6.4
酸素処理,OT(Oxygenated Treatment)
高純度水中に,酸素及びアンモニアなどのアルカリ薬品を添加し,腐食抑制を図る水処理方法。複合水
処理(CWT: Combined Water Treatment)と呼ぶこともある。
なお,高純度水中に,酸素だけを添加する水処理方法は,中性水処理(NWT: Neutral Water Treatment)
と呼ばれており,アルカリ薬品が使用できないなどの特殊な条件下だけで使用する。
3.6.5
低濃度水酸化ナトリウム処理
ボイラ水のpHを微量の水酸化ナトリウムで調節する処理方法。
4
水処理方式
ボイラ水の水処理方式は,ボイラの使用目的,構造,温度及び圧力条件に応じて選定する。具体的な水
処理方法については,附属書Aに示す。
5
給水及びボイラ水の水質に関する一般事項
5.1
給水の水質
給水の水質に関する一般事項は,次による。
a) 油脂類(ヘキサン抽出物質でJIS B 8224を参照。)は,ボイラ水のホーミング(Foaming:泡立ち)及
びスケール付着を防止するために,ボイラに油脂類が混入しないように留意するという観点から低く
保つことが望ましい。
b) 給水配管又はドレン回収配管(復水配管)に亜鉛めっき鋼管(通称:白ガス管)を使用した場合,亜
鉛が溶出し給水中に含まれることがある。通常,亜鉛は,鉄に対し犠牲電極及び沈殿皮膜となり防食
作用を示すが,ボイラ内では亜鉛系スケールの原因となるため低く保つことが望ましい。
c) 給水の水質管理項目については,附属書Bに示す。
5.2
ボイラ水の水質
ボイラ水の水質に関する一般事項は,次による。
a) 原水又は軟化水を補給水とする場合は,ボイラ水中のシリカの濃度が高くなるため,シリカの含有率
の高いスケールが生成する傾向にある。ボイラ内でのシリカによるスケール化を防止するためには,
硬度成分を共存させないようにするとともに,ボイラ水中のシリカの濃度を制限し,ボイラ水の酸消

5
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
費量(pH 8.3)を,この値の上限値に1/1.7を乗じた値[シリカをメタけい酸イオンの形態にするため
に必要な酸消費量(pH 8.3)対応量]を超えないようにブローによって管理する(B.14を参照)。シリ
カを高濃度で維持する場合には,シリカの析出を防止する酸消費量(pH 8.3)を維持し,硬度成分流
入によるけい酸塩スケールに注意する。給水中のシリカ濃度が高い場合には,ボイラ水のpHが上が
りにくくなるため,ブローの調整又は清缶剤を併用したり,逆浸透膜装置などのシリカを除去したり
できる水処理装置などを併用する。タービンに送気する場合には,タービンでのシリカスケールによ
るタービン効率低下を防ぐために,シリカ濃度を低く保つことが望ましい。
b) 硫酸イオンは腐食促進作用があるため,なるべく低濃度に維持することが望ましい。
c) ボイラ水中の鉄,銅及び亜鉛は,スケール,ボイラ内でのスラッジの堆積,伝熱面の汚染防止及び酸
素濃淡電池による二次腐食を防止する目的で低く保つことが望ましい。
d) ボイラ水の水質管理項目については,附属書Bに示す。
5.3
補給水の水質
補給水の水質に関する一般事項については,附属書Cに示す。
5.4
水質管理項目の測定値が管理値を逸脱した場合
水質管理項目の測定値が管理値を逸脱した場合の一般的対処方法は,附属書Dによって実施するのが望
ましい。
5.5
起動時及び停止中の場合
ボイラの起動時及び停止中の水質管理は,腐食を抑制するために,通常運転中とは異なる処置が必要で
ある。
6
丸ボイラの水質
6.1
丸ボイラの給水の水質
6.1.1
水質の管理項目及び管理値
丸ボイラの給水の水質は,常用使用圧力,伝熱面蒸発率及び補給水の種類によって区分し,表1による
ほか,次による。
a) 丸ボイラの補給水にイオン交換水を用いる場合には,表8の2 MPa以下の圧力区分の水質を適用する。
b) 船用に用いる場合には,表4の該当する圧力区分の補給水に軟化水又はイオン交換水を用いる場合の
水質を適用する。
c) 2 MPaを超える圧力で使用する炉筒煙管ボイラの場合は,表8の該当する圧力区分の給水の水質を適
用する。
表1−丸ボイラの給水の水質の管理項目及び管理値
区
分
常用使用圧力
MPa
1以下
1を超え2以下
伝熱面蒸発率
kg/(m2・h)
30以下a)
30を超えるもの
−
補給水の種類
原水
軟化水
給
水
pH(25 ℃における)
5.8〜9.0
硬度
CaCO3: mg/L
60以下
1以下
注a) 鋳鉄製ボイラで,室内加湿,食品加工,フィルム製造,病院などで直接蒸気を使用し,常時補給水
を使用する場合に適用する。
6.1.2
水質に関する留意事項
丸ボイラの給水の水質については,次の事項について留意することが望ましい。

6
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
a) 原水又は軟化水を給水として用い,ドレン(復水)を回収する場合には,給水温度の上昇が,給水系
統の腐食増大の一因となることから腐食抑制のために,アンモニア,アミンなどを添加することによ
ってpHを7以上に高めに管理する。
b) 一般に,腐食は電気化学的な反応であり,給水のpHが中性又はアルカリ性であっても水中に溶存酸
素が存在すると腐食が生じる(B.7を参照)。また,丸ボイラでは給水系統に脱気器がほとんど設置さ
れていないために,給水中の溶存酸素の濃度は一般的に高い。したがって,給水タンクなどの開放部
において給水温度を上昇させたり,膜式脱気装置などによって溶存酸素をできるだけ給水から除去す
る。
6.2
丸ボイラのボイラ水の水質
6.2.1
水質の管理項目及び管理値
丸ボイラのボイラ水の水質は,アルカリ処理方式とし,常用使用圧力,伝熱面蒸発率及び補給水の種類
によって区分し,表2によるほか,次による。
a) 丸ボイラの補給水にイオン交換水を用いる場合には,表9の2 MPa以下の圧力区分の水質を適用する。
b) 船用に用いる場合には,表5の該当する圧力区分の補給水に軟化水又はイオン交換水を用いる場合の
水質を適用する。
c) 2 MPaを超える圧力で使用する炉筒煙管ボイラの場合は,表9の該当する圧力区分のボイラ水の水質
を適用する。
表2−丸ボイラのボイラ水の水質の管理項目及び管理値
区
分
常用使用圧力
MPa
1以下
1を超え2以下
伝熱面蒸発率
kg/(m2・h)
30以下a)
30を超え60以下
60を超えるもの
−
補給水の種類
原水
軟化水
処理方式
アルカリ処理
ボ
イ
ラ
水
pH(25 ℃における)
11.0〜11.8
酸消費量(pH 4.8)
CaCO3: mg/L
100〜800
600以下
酸消費量(pH 8.3)
CaCO3: mg/L
80〜600
500以下
電気伝導率(25 ℃における) mS/m
600以下
450以下
400以下
350以下
(μS/cm)(6 000以下)
(4 500以下)
(4 000以下)
(3 500以下)
塩化物イオン
Cl: mg/L
600以下
500以下
400以下
350以下
りん酸イオンb)
PO4: mg/L
20〜40
亜硫酸イオンc)
SO3: mg/L
10以上
ヒドラジンd)
N2H4: mg/L
0.1〜1.0
注a) 鋳鉄製ボイラで,室内加湿,食品加工,フィルム製造,病院などで直接蒸気を使用し,常時補給水を使用す
る場合に適用する。
b) りん酸塩を添加する場合に適用する。
c) 亜硫酸塩を脱酸素剤として添加する場合に適用する。亜硫酸イオンの上限は規定しないが,ボイラ水の電気
伝導率が規定値の上限を超えない範囲とする。
d) ヒドラジンを脱酸素剤として給水に添加する場合に適用する。
6.2.2
水質に関する留意事項
丸ボイラのボイラ水の水質については,次の事項について留意することが望ましい。
a) 原水又は軟化水を補給水とするボイラでは,硬度成分及びシリカによるスケール化を防止するために,
ボイラ水中のりん酸イオンの濃度を十分に高く保持し,かつ,pHを11以上で管理する。また,軟化
水を給水とする丸ボイラでは,不測の硬度成分の漏えいによるカルシウム及びマグネシウムに注意す
7
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
る。
b) ボイラ水のりん酸イオンは,不測の硬度成分の漏れ及び原水を補給水とする場合に対処するために,
管理値の上限付近で管理する。ただし,りん酸イオン以外に,カルボン酸塩系ポリマー(ポリアクリ
ル酸塩,ポリマレイン酸塩など),ホスホン酸塩(ヒドロキシエチリデンジホスホン酸塩,ホスホノブ
タントリカルボン酸塩など)及び/又はキレート剤(エチレンジアミン四酢酸塩など)によって硬度
成分によるスケール及びスラッジの防止が可能である。これらの方法を用いる場合の保持濃度につい
ては,供給する薬剤製造業者と相談するのが望ましい。
c) 脱気器を設置するボイラにおいてヒドラジンを使用する場合には,N2H4: 0.1〜0.5 mg/Lで管理する。
直接食品加工,室内加湿など人体が直接摂取するか,又は触れる用途に蒸気を使用する場合には,
安全性を考慮してヒドラジンに代わる脱酸素剤を使用するなどによって,蒸気中にヒドラジンが検出
されないようにする。詳細は,B.8を参照。
d) 亜硫酸塩を脱酸素剤として使用する場合,上限値を設定していないが,亜硫酸塩と酸素との反応によ
って生じる硫酸イオン及びアルカリ金属イオンの濃度の増大によってボイラ水の電気伝導率の増大を
防ぐため,脱気器を設置しないものでは,SO3: 50 mg/Lを大きく上回らない範囲とする。脱気器を使
用する場合は,SO3: 10〜20 mg/Lとする。ボイラ水中では,反応生成物として硫酸イオンを生じ,脱
酸素処理が不十分な場合(亜硫酸イオンが残留しない場合)は,溶存酸素による腐食を加速するので
注意する。
7
特殊循環ボイラの水質
7.1
単管式特殊循環ボイラの水質
7.1.1
水質の管理項目及び管理値
単管式特殊循環ボイラの給水の水質は,常用使用圧力によって区分し,表3によるほか,次による。
a) 単管式特殊循環ボイラの給水とは,補給水に戻り水が加わったものに薬品を添加したものをいう。具
体的には,この給水は戻り水が加わっているため,丸ボイラなどでいうボイラ水に相当している。た
だし,硬度は,戻り水の加わる前の補給水に適用する。
b) 補給水にイオン交換水を用いる場合には,表5の該当する圧力区分の補給水にイオン交換水を用いる
場合の水質を適用する。
c) 船用の補給水の場合,造水器で精製した蒸留水もイオン交換水と同様の水質を適用する。
d) 船用に用いる場合には,補給水に軟化水を用いる場合もイオン交換水を用いる場合も表3の水質を適
用する。

8
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
表3−単管式特殊循環ボイラの給水の水質の管理項目及び管理値
区
分
常用使用圧力
MPa
1以下
1を超え3以下
補給水の種類
軟化水
処理方式
アルカリ処理a)
給
水
pH(25 ℃における)
11.0〜11.8
10.5〜11.0
硬度
CaCO3: mg/L
1以下
1以下
電気伝導率(25 ℃における)
mS/m
(μS/cm)
450以下
(4 500以下)
400以下
(4 000以下)
酸消費量(pH 4.8)
CaCO3: mg/L
300〜800
600以下
酸消費量(pH 8.3)
CaCO3: mg/L
200〜600
500以下
ヒドラジンb)
N2H4: mg/L
0.05〜1.00
0.05〜1.00
塩化物イオン
Cl: mg/L
600以下
400以下
りん酸イオンc)
PO4: mg/L
20〜60
20〜60
注a) 給水に薬品を添加しない水処理方式を含む。
b) ヒドラジンを添加する場合に適用する。ヒドラジンの濃度は,pHがその上限を超え
ない値とするとともに,脱気器出口の溶存酸素の濃度に応じて低減することも可能
である。
c) りん酸塩を添加する場合に適用する。
7.1.2
水質に関する留意事項
給水の水質については,次の事項について留意することが望ましい。
a) 軟化水又はイオン交換水を補給水として用い,ドレン(復水)を回収する場合には,給水温度の上昇
が,給水系統の腐食増大の一因となることから腐食抑制のために,補給水のpHを7以上に高めて管
理する。
b) 軟化水を補給水とする単管式特殊循環ボイラでは,不測の硬度成分の漏えいによる硬度の増加及びシ
リカのスケール化を防止するために,水管内のりん酸イオンを管理値内で保持し,かつ,pHを10.5
〜11.8で管理する。
c) 単管式特殊循環ボイラでは,ボイラ内処理としてブロー管理だけでは硬度成分に起因するスケール障
害の防止が困難なため,補給水には必ず軟化水又はイオン交換水を使用する。
d) 給水に含まれる溶存酸素は,火力発電プラント全体の水側の金属材料の腐食を防止する目的でも管理
する必要があり,低く保つことが望ましい。
なお,単管式特殊循環ボイラでは脱気タンク(ホットウェルタンク)に戻り水を戻しているため,
溶存酸素の値は比較的低く保たれている。
e) 給水の酸消費量は,給水のpHを間接的に管理するとともに,シリカによるスケール付着を防止する
目的で管理する。軟化水を給水とする単管式特殊循環ボイラでは,給水のシリカの濃度を規定してい
ないが,ボイラ水の酸消費量(pH 8.3)の上限値に7.11を乗じた値,すなわち,圧力1 MPa以下ではSiO2:
350 mg/L,1 MPaを超え3 MPa以下ではSiO2: 300 mg/Lを超えないようにブローによって調節するこ
とが望ましい(B.14を参照)。
f)
給水のヒドラジンは,ボイラの腐食を防止する目的で管理する。給水のヒドラジンは,N2H4: 0.05 mg/L
以上と規定しているが,脱気タンク出口水又はホットウェルタンク出口水の溶存酸素の濃度に対して
当量以上の値で管理する必要がある。過剰な注入を防止するため,上限をN2H4: 1.00 mg/Lとする。
なお,蒸気を直接食品加工,人体に触れる用途などに使用する場合は,安全性を考慮して蒸気中に
ヒドラジンが検出されないようにするのがよい(B.8を参照)。
9
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
g) 給水の塩化物イオンは,濃縮倍数の推定を行うとともに,腐食を抑制する目的で管理する。
なお,単管式特殊循環ボイラでは,全蒸発残留物の濃度の間接的管理に重点をおき,防食上の考慮
も加えて給水の塩化物イオンの濃度の上限を規定する。
h) 給水のりん酸イオンは,補給水がもち込むカルシウムによるスケール化を防止する目的で管理する。
水管内におけるカルシウムとりん酸イオンとの反応によって,カルシウムCaCO3: 1 mg当たり必要な
りん酸イオンは,PO4: 0.57 mgである。管理値は,給水のりん酸イオンの濃度をPO4: 20〜60 mg/Lと
しているが,不測の硬度成分の漏えいに対処するためには,上限付近の高めで管理することが望まし
い。船用で用いる場合にも,りん酸イオンは海水の混入を考慮して管理値の上限付近で管理する。
7.2
多管式特殊循環ボイラの水質
7.2.1
給水の水質
7.2.1.1
水質の管理項目及び管理値
多管式特殊循環ボイラの給水の水質は,常用使用圧力,及び補給水の種類によって区分し,表4による
ほか,次による。
a) イオン交換水を用いる場合で,常用使用圧力が3 MPaを超える場合は,表8の該当する圧力区分の補
給水にイオン交換水を用いる場合の水質を適用する。
b) 船用に用いる場合には,表4の該当する圧力区分の補給水に軟化水又はイオン交換水を用いる場合の
水質を適用する。
c) 船用の補給水の場合,造水器で精製した蒸留水もイオン交換水と同様の水質を適用する。
表4−多管式特殊循環ボイラの給水の水質の管理項目及び管理値
区
分
常用使用圧力
MPa
3以下
2以下
2を超え3以下
補給水の種類
軟化水
イオン交換水
給
水
pH(25 ℃における)
5.8〜9.0
5.8〜9.7
硬度
CaCO3: mg/L
1以下
検出せずa)
鉄
Fe: mg/L
0.3以下
0.1以下
0.1以下
ヒドラジンb)
N2H4: mg/L
−
−
0.2以上
注a) カルシウム及びマグネシウムの試験方法(JIS B 8224参照)のうち,適用した試験
方法の定量下限値から硬度を算出したとき,その値より低い値とする。
b) ヒドラジンを添加する場合に適用する。
7.2.1.2
水質に関する留意事項
給水の水質については,次の事項について留意することが望ましい。
a) 軟化水又はイオン交換水を給水として用い,ドレン回収をする場合には,給水温度が上昇し,給水系
統の腐食増大の一因となることから,腐食を抑制する目的で,アルカリ,アミンなどを添加すること
によってpHを7以上に高めて管理する。
なお,船用に用いる場合には,pHは7.0〜9.2とする。
b) 給水系統の腐食をできるだけ抑制するためには,溶存酸素を低く保つ。脱気器を設置しない場合は,
給水タンクなどの開放部において給水温度を上昇させることによって溶存酸素を低く保つ。また,常
用使用圧力1 MPaを超え3 MPa以下のボイラでは,溶存酸素による腐食及びその影響が大きくなるこ
とから,溶存酸素の上限をO: 0.5 mg/Lとするのが望ましい。
c) 硬度成分及びシリカによるスケール化を防止するために,不測の硬度成分の漏えいによるカルシウム,
マグネシウムに注意する。

10
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
d) 給水に鉄が多く含まれる原因としては,原水に含まれる場合,給水系統が腐食している場合,ドレン
回収を行っている場合はドレン回収系統の腐食が考えられ,除鉄装置の利用,耐食材への変更,復水
処理剤の使用など,低減するための処置を行う。
e) 給水中のシリカが高い場合には,ボイラ水のpHが上がりにくくなるため,ブローの調整,清缶剤の
使用,逆浸透膜装置などのシリカが除去できる水処理装置などを併用する。
f)
ヒドラジンの濃度は,pHがその上限を超えない値とするとともに,脱気器出口の溶存酸素の濃度に応
じて低減することができる。蒸気を直接,食品加工又は人体に触れる用途などに使用する場合は,安
全性を考慮して蒸気中にヒドラジンが検出されないようにする,又はヒドラジンに代わる脱酸素剤な
どを使用する(B.8を参照)。
7.2.2
ボイラ水の水質
7.2.2.1
水質の管理項目及び管理値
多管式特殊循環ボイラのボイラ水の水質は,常用使用圧力及び補給水の種類によって区分し,表5によ
るほか,次による。
a) イオン交換水を用いる場合で,常用使用圧力が3 MPaを超える場合,又はりん酸塩処理を行う場合は,
表9の該当する圧力区分の補給水にイオン交換水を用いる場合の水質を適用する。
b) 船用に用いる場合には,表5の該当する圧力区分の補給水に軟化水又はイオン交換水を用いる場合の
水質を適用する。
c) 船用の補給水の場合,造水器で精製した蒸留水もイオン交換水と同様の水質を適用する。
表5−多管式特殊循環ボイラのボイラ水の水質の管理項目及び管理値
区
分
常用使用圧力
MPa
1以下
1を超え3以下
2以下
2を超え3以下
補給水の種類
軟化水
イオン交換水
処理方式
アルカリ処理a)
ボ
イ
ラ
水
pH(25 ℃における)
11.0〜11.8
10.5〜11.5
10.0〜11.0
酸消費量(pH 4.8)
CaCO3: mg/L
100〜800
600以下
250以下
150以下
酸消費量(pH 8.3)
CaCO3: mg/L
80〜600
500以下
200以下
120以下
電気伝導率(25 ℃における)
mS/m
(μS/cm)
400以下
(4 000以下)
300以下
(3 000以下)
150以下
(1 500以下)
100以下
(1 000以下)
塩化物イオン
Cl: mg/L
400以下
300以下
150以下
100以下
りん酸イオンb)
PO4: mg/L
20〜40
10〜30
5〜15
亜硫酸イオンc)
SO3: mg/L
10以上
10〜20
10〜20
5〜10
ヒドラジンd)
N2H4: mg/L
0.1〜1.0
0.1〜0.5
0.1〜0.5
−
注a) 給水に薬品を添加しない水処理方式を含む。
b) りん酸塩を添加する場合に適用する。
c) 亜硫酸塩を添加する場合に適用する。
d) ヒドラジンを添加する場合に適用する。
7.2.2.2
水質に関する留意事項
ボイラ水の水質については,次の事項について留意することが望ましい。
a) 硬度成分及びシリカによるスケール化を防止するために,不測の硬度成分の漏えいによるカルシウム,
及びマグネシウムに注意する。
b) ボイラ水の塩化物イオンは,ボイラ水の濃縮の程度を知るとともに,腐食を抑制する目的で管理する。
船用の場合には,ボイラ水の濃縮倍率を配慮して電気伝導率及び塩化物イオンの濃度はできる限り低
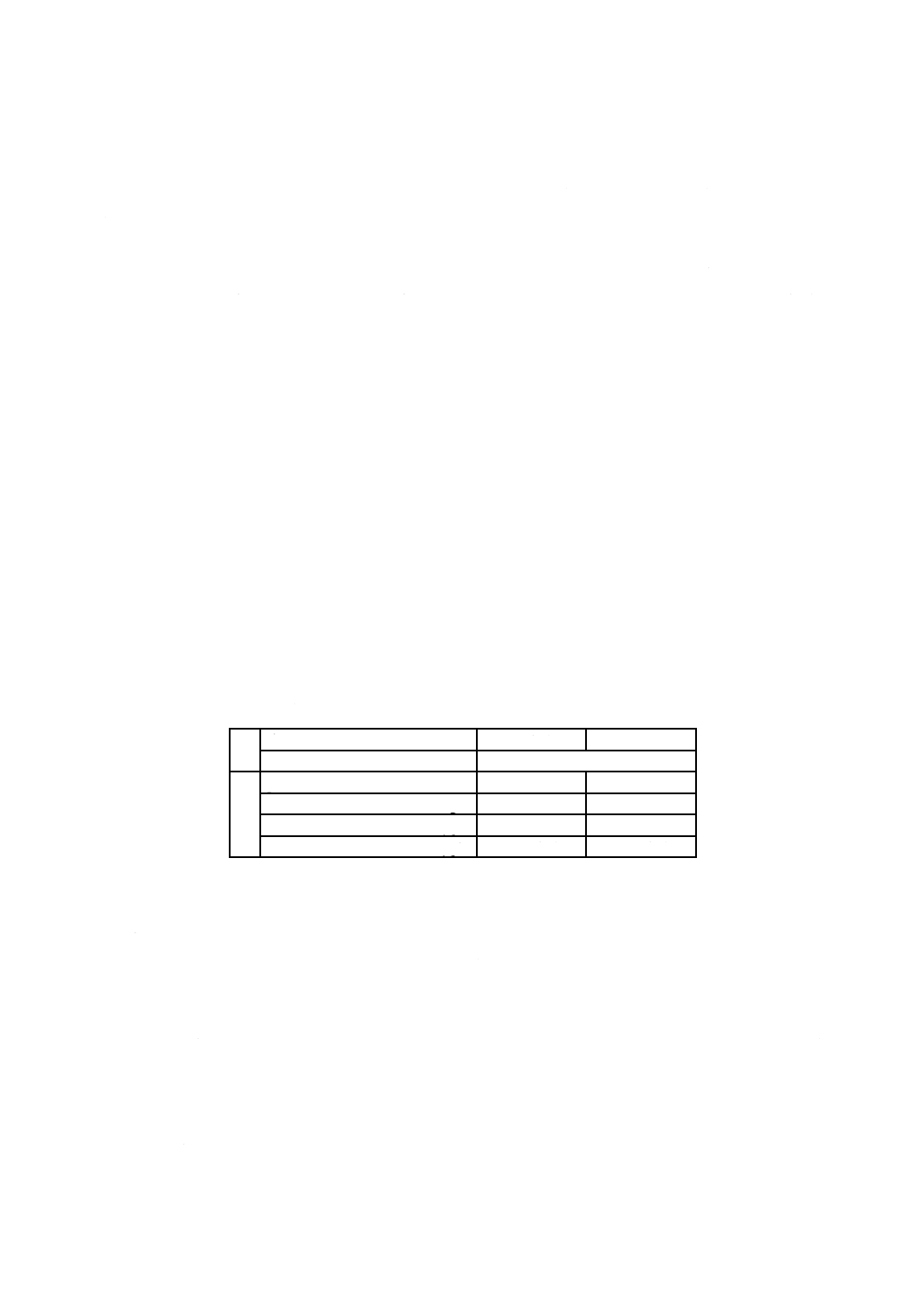
11
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
く維持する。
c) ボイラ水のりん酸イオンは,不測の硬度成分の漏れに対処するために,管理値の上限付近で管理する。
船用で用いる場合にも,りん酸イオンは海水の混入を考慮して管理値の上限付近で管理する。
d) 亜硫酸塩を脱酸素剤として使用する場合は,亜硫酸塩と酸素との反応によって生じる硫酸イオン及び
アルカリ金属イオンの濃度の増大によってボイラ水の電気伝導率の増大を防ぐため,脱気器を設置し
ないものでは,SO3: 50 mg/Lを大きく上回らない範囲とする。脱気器を使用する場合は,SO3: 10〜20
mg/Lとする。ボイラ水中では,反応生成物として硫酸イオンを生じ,脱酸素処理が不十分な場合(亜
硫酸イオンが残留しない場合)は,溶存酸素による腐食を加速するので注意する。船用に亜硫酸ナト
リウムを脱酸素剤として使用する場合は連続投入とし,脱気器を設置しないものでは亜硫酸イオン濃
度上限値をSO3: 50 mg/Lとする。
e) ヒドラジンを用いて脱気器を使用する場合には,N2H4: 0.1〜0.5 mg/Lとする。蒸気を直接食品加工又
は人体に触れる用途などに使用する場合は,安全性を考慮して蒸気中にヒドラジンが検出されないよ
うにする,又はヒドラジンに代わる脱酸素剤などを使用する(B.8を参照)。
8
水管ボイラ,循環ボイラの水質
8.1
産業用水管ボイラの水質(軟化水を使用する場合)
8.1.1
給水の水質
8.1.1.1
水質の管理項目及び管理値
軟化水を使用する水管ボイラの給水の水質は,常用使用圧力によって区分し,表6によるほか,次によ
る。
船用に用いる場合には,表4の該当する圧力区分の補給水に軟化水を用いる場合の水質を適用する。
表6−産業用水管ボイラの給水の水質(軟化水を使用する場合)の管理項目及び管理値
区
分
常用使用圧力
MPa
1以下
1を超え2以下
補給水の種類
軟化水
給
水
pH(25 ℃における)
5.8〜9.0
5.8〜9.0
硬度
CaCO3: mg/L
1以下
1以下
溶存酸素
O: μg/L
−
500以下
鉄
Fe: μg/L
300以下
300以下
8.1.1.2
水質に関する留意事項
給水の水質については,次の事項について留意することが望ましい。
a) 常用使用圧力2 MPa以下の水管ボイラでは,軟化水を給水として用いるが,最近,ドレンを回収した
り,給水熱交換形連続ブロー装置を設置する例が多くなっており,それに伴い給水温度が上昇し,こ
れらの給水系統の腐食増大の一因となっていることから,腐食をできるだけ抑制するためにはアンモ
ニア,アミンなどを添加することによってpHを7以上に高めに管理する。
b) 一般に,腐食は電気化学的な反応であり,給水のpHが中性又はアルカリ性であっても,水中に溶存
酸素が存在すると腐食が生じる(B.7を参照)。1 MPa以下の圧力区分のボイラでは,給水系統に脱気
器をほとんど設置しないために,給水中の溶存酸素の濃度は一般的に高い。したがって,給水タンク
などの開放部において給水温度を上昇させたり,膜式脱気装置などによって溶存酸素をできるだけ給
水から除去する。

12
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
c) 給水中ヒドラジンの管理値を設定していないが,ヒドラジンを脱酸素剤として注入する場合は,注入
点については,給水が空気と接触しない系統のなるべく上流側に,脱気器があればその上流側に,ヒ
ドラジンを注入して注入点以降の系統の腐食を抑制することが有効である。ただし,100 ℃以下では
反応速度が遅いのでほとんど脱酸素効果が期待できないことに注意する。
8.1.2
ボイラ水の水質
8.1.2.1
水質の管理項目及び管理値
軟化水を使用する水管ボイラのボイラ水の水質は,アルカリ処理方式とし,常用使用圧力によって区分
し,表7による。
船用に用いる場合には,表5の該当する圧力区分の補給水に軟化水を用いる場合の水質を適用する。
表7−産業用水管ボイラのボイラ水の水質(軟化水を使用する場合)の管理項目及び管理値
区
分
常用使用圧力
MPa
1以下
1を超え2以下
補給水の種類
軟化水
処理方式
アルカリ処理
ボ
イ
ラ
水
pH(25 ℃における)
11.0〜11.8
酸消費量(pH 4.8)
CaCO3: mg/L
100〜800
600以下
酸消費量(pH 8.3)
CaCO3: mg/L
80〜600
500以下
電気伝導率(25 ℃における)
mS/m
400以下
300以下
(μS/cm)
(4 000以下)
(3 000以下)
塩化物イオン
Cl: mg/L
400以下
300以下
りん酸イオンa)
PO4: mg/L
20〜40
亜硫酸イオンb)
SO3: mg/L
10以上c)
10〜20
ヒドラジンd)
N2H4: mg/L
0.1〜1.0
0.1〜0.5
注a) りん酸塩を添加する場合に適用する。
b) 亜硫酸塩を脱酸素剤として添加する場合に適用する。
c) 亜硫酸イオンの上限は規定しないが,ボイラ水の電気伝導率が規定値の上限を超え
ない範囲とする。
d) ヒドラジンを脱酸素剤として給水に添加する場合に適用する。
8.1.2.2
水質に関する留意事項
軟化水を使用する水管ボイラのボイラ水の水質については,次の事項について留意することが望ましい。
a) 軟化水を補給水とするボイラでは,硬度成分及びシリカによるスケール化を防止するために,ボイラ
水中のりん酸イオンの濃度を十分に高く保持し,かつ,pHを11以上で管理する。また,軟化水を使
用する水管ボイラでは,不測の硬度成分の漏えいによるカルシウム及びマグネシウムに注意する。
b) 塩化物イオンは,鋼面の酸化鉄の防食皮膜の安定性を阻害するため,なるべく低濃度に維持する。
c) ボイラ水のりん酸イオンは,不測の硬度成分の漏れ及び原水を補給水とする場合に対処するために,
管理値の上限付近で管理する。ただし,りん酸イオン以外に,カルボン酸塩系ポリマー(ポリアクリ
ル酸塩,ポリマレイン酸塩など),ホスホン酸塩(ヒドロキシエチリデンジホスホン酸塩,ホスホノブ
タントリカルボン酸塩など)及び/又はキレート剤(エチレンジアミン四酢酸塩など)によって硬度
スケール及びスラッジの防止が可能である。これらの方法を用いる場合の保持濃度については,供給
する薬剤製造業者と相談するのが望ましい。
d) 脱気器を設置するボイラにおいて,ヒドラジンを使用する場合には,N2H4: 0.1〜0.5 mg/Lで管理する。
ヒドラジンの分配係数(ボイラ水中の濃度に対する蒸気中の濃度の比,揮発度ともいう。)は2〜6 %
であり,ボイラ水中に残留したヒドラジンの一部が蒸気へ移行する。また,ヒドラジンはボイラ水中
13
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
においては,ヒドラジンの一部が自己分解してアンモニアを生じる。このアンモニアもまたヒドラジ
ンと同様に蒸気中に移行し,ドレン系の銅合金材の腐食の原因となる。以上のことから,ボイラ水中
に多量のヒドラジンを残留させることは避けなければならない。
直接食品加工,室内加湿など人体が直接摂取するか又は触れる用途に蒸気を使用する場合には,安
全性を考慮してヒドラジンに代わる脱酸素剤を使用するなどによって,蒸気中にヒドラジンが検出さ
れないようにする。詳細は,B.8を参照。
e) 亜硫酸塩を脱酸素剤として使用する場合,1 MPa以下のボイラでは上限値を設定していない。しかし,
亜硫酸塩と酸素との反応によって生じる硫酸イオン及びアルカリ金属イオンの増加に伴うボイラ水の
電気伝導率の増大を防ぐため,脱気器を設置しないものでは,SO3: 50 mg/Lを大きく上回らない範囲
とする。脱気器を使用する場合は,SO3: 10〜20 mg/Lとする。ボイラ水中では,反応生成物として硫
酸イオンを生じ,脱酸素処理が不十分な場合(亜硫酸イオンが残留しない場合)は,溶存酸素による
腐食を加速するので注意する。
8.2
産業用水管ボイラの水質(イオン交換水を使用する場合)
8.2.1
給水の水質
8.2.1.1
水質の管理項目及び管理値
イオン交換水を使用する産業用水管ボイラの給水の水質は,常用使用圧力及びボイラ水の処理方式によ
って区分し,表8によるほか,次による。
a) 船用の主ボイラに用いる場合には,表8の該当する圧力区分の同一水処理方式を用いた場合の水質を
適用する。
b) 船用の補助ボイラに用いる場合には,表4の該当する圧力区分の補給水にイオン交換水を用いた場合
の水質を適用する。
c) 船用の補給水の場合,造水器で精製した蒸留水もイオン交換水と同様の水質を適用する。
注記 イオン交換水とは,強酸性陽イオン交換樹脂と強塩基性陰イオン交換樹脂とを用いたイオン
交換装置で精製した水,又は船用の場合のように,造水器で精製した水(蒸留水)をいう。
14
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
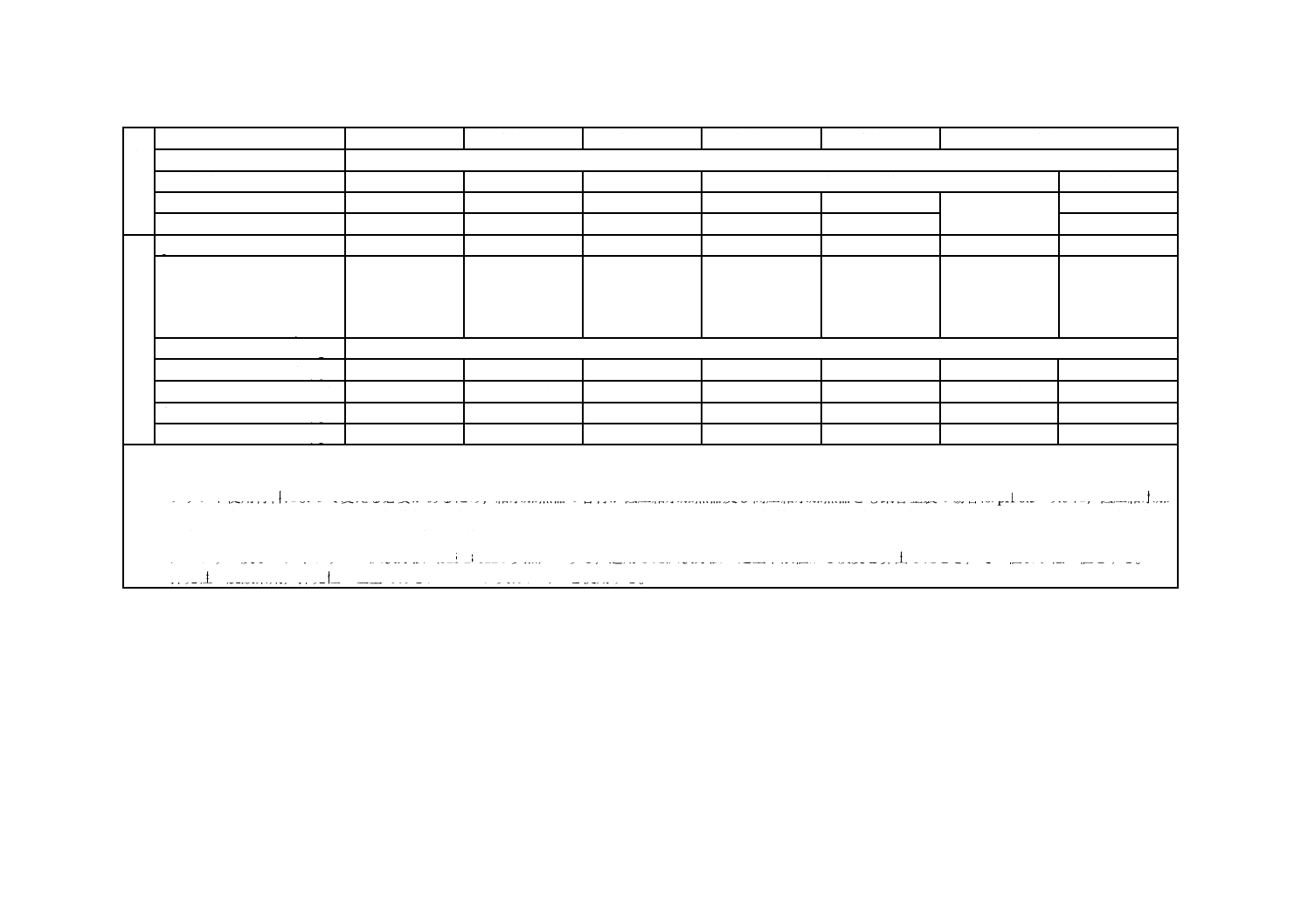
表8−産業用水管ボイラの給水の水質(イオン交換水を使用する場合)の管理項目及び管理値
区
分
常用使用圧力
MPa
2以下
2を超え3以下
3を超え5以下
5を超え7.5以下 7.5を超え10以下
10を超え15以下
補給水の種類
イオン交換水
処理方式
−
−
−
揮発性物質処理d)
酸素処理
還元剤
−
−
−
−
−
あり
なし
酸化還元性
−
−
−
−
−
酸化型(OT)
給
水
pH(25 ℃における)
8.5〜10.3 b)
8.5〜10.3 b)
8.5〜10.3 b)
8.5〜10.3 b)
8.5〜10.3 b)
8.5〜10.3 b)
8.0〜10.3
酸電気伝導率
(25 ℃における)
mS/m
(μS/cm)
−
−
−
−
−
−
−
−
−
−
0.05以下
(0.5以下)
0.02以下
(0.2以下)
硬度
CaCO3: mg/L
検出せずc)
溶存酸素
O: μg/L
500以下
100以下
30以下
7以下
7以下
7以下
20〜50
鉄
Fe: μg/L
100以下
100以下
100以下
50以下
30以下
30以下
5以下
銅
Cu: μg/L
−
−
50以下
30以下
20以下
10以下
10以下
ヒドラジンa)
N2H4: μg/L
−
200以上
60以上
10以上
10以上
10以上
−
注a) 脱酸素剤としてヒドラジンを使用する場合に規定する。ヒドラジンの濃度は,pHがその上限を超えない値とするとともに,脱気器出口の溶存酸素の濃度に応
じて低減することも可能である。
b) プラント使用材料によって変える必要があるため,給水加熱器の管材が低圧給水加熱器及び高圧給水加熱器とも銅合金製の場合はpH 8.5〜9.0に,低圧給水加
熱器が銅合金で高圧給水加熱器が鋼管製の場合にはpH 9.0〜9.4に,両加熱器及び復水器とも鋼管又はチタン製の場合にはpH 9.3〜10.3(復水器が銅合金製の
場合は,pHの上限を9.4とする。)に調節し,管理する。
c) カルシウム及びマグネシウムの試験方法(JIS B 8224参照)のうち,適用した試験方法の定量下限値から硬度を算出したとき,その値より低い値とする。
d) 揮発性の脱酸素剤,揮発性の塩基であるアンモニア又はアミンを使用する。
6
B
8
2
2
3
:
2
0
1
5
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
15
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
8.2.1.2
水質に関する留意事項
給水の水質については,表8によるほか,次の事項について留意することが望ましい。
a) アルカリ処理,低濃度水酸化ナトリウム処理,りん酸塩処理及び揮発性物質処理[AVT(R)]
1) 給水のpH調節には,アンモニア,アミンなどの揮発性の塩基,又は水酸化ナトリウムなどの非揮
発性の塩基を用いる。発生蒸気の用途上,安全性及び純度を重視し,揮発性の脱酸素剤,アンモニ
ア,アミンなどの使用に制限がある場合は,非揮発性の塩基である水酸化ナトリウムなどを使用す
る。
なお,発電ボイラでは,過熱蒸気温度低減スプレー水を給水系統から分岐するので,水酸化ナト
リウムなどの非揮発性の塩基を蒸気過熱器又は蒸気タービンにスプレーすることによる障害が発生
しないように,注入位置に注意する必要がある。
2) 給水の試料採取点は,給水のpHを調節する塩基の注入点より下流側でも差し支えないが,ボイラ
水用処理剤として非揮発性のりん酸塩,水酸化ナトリウムなどの塩基を給水に注入する場合には,
りん酸塩及び塩基による影響を避けるためにその注入点よりも上流側を選ぶ。
3) 銅材料を使用していない場合の給水pHの上限値は,流れ加速型腐食(FAC)1)対策上高めが望まし
い。
なお,復水器が銅合金の場合の給水pHの上限を電力事業用では9.6に引き上げているが,産業用
では補給水量が多いことによる空気のもち込み量が多いこと又は復水器のシール性の劣化による空
気の漏えいが抑えきれない場合もあり,復水器管の腐食を懸念して,従来どおりに9.4とする。一
方,1)に示したように,発生蒸気の用途上,安全性及び純度を重視し,揮発性の脱酸素剤,アンモ
ニア,アミンなどの使用に制限があり,pH調節を行わない場合又は基準の下限値を下回る場合は,
給水系統を耐食材にするなどの防食対策を行うことが望ましい。
注1) 流れ加速型腐食(FAC: Flow Accelerated Corrosion)とは,金属材料表面の保護性皮膜(マグ
ネタイトなど)が,水管の流れの乱れによって溶解反応が加速され,その結果,母材が減
肉する現象をいう。
4) 常用使用圧力が10 MPaを超えるボイラでは,給水の電気伝導率は酸電気伝導率として測定し,実
績を勘案し0.05 mS/m(0.5 μS/cm)(25 ℃において)以下とする。しかし,実際の管理では,正常
な水質の状態の酸電気伝導率の値[通常0.02〜0.03 mS/m(0.2〜0.3 μS/cm)(25 ℃において)以下]
を把握し,管理値の範囲内における変動においても,その変動の要因となる復水器の冷却水の微量
の漏えい,補給水の水質悪化などの有無を確認して的確な処置を行うことが望ましい。
5) 常用使用圧力2 MPa以下のボイラのうち,1 MPa以下のボイラについては,脱気器を設置しないも
のが多いので,給水中の溶存酸素の濃度は低く保つ。一方,常用使用圧力が1 MPa以上で,蒸気ド
ラム内などに脱気器を設置している場合は,給水中の溶存酸素の濃度をO: 500 μg/L以下とする。常
用使用圧力2 MPaを超えるボイラに対しては,経験的に,また,現在の脱気器の性能保証値などに
基づいて圧力区分ごとに給水中の溶存酸素の上限濃度を設定して管理することが望ましい。
6) ヒドラジンは,給水が空気と接触しない系統のなるべく上流側に,脱気器があればその上流側に注
入して注入点以降の系統の腐食を抑制することが有効である。脱気器で溶存酸素の大部分を除去す
る常用使用圧力1 MPaを超える水管ボイラの給水のヒドラジンの濃度は,脱気後の溶存酸素の濃度
の1.5倍よりも大きくなるようにするのが望ましい。ただし,常用使用圧力が5 MPa以下の水管ボ
イラ(循環ボイラ)の給水のように脱気後の溶存酸素の濃度がO: 7 μg/Lを超える場合には,給水の
ヒドラジン濃度はその2倍よりも大きくなるようにその下限値を管理することが望ましい。一般に,
16
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
給水中のヒドラジンの濃度は,ボイラ入口(エコノマイザがある場合は,エコノマイザ入口)の給
水に残留することが望まれる下限値であり,ヒドラジンの注入量は,この下限値を維持するように
調節する必要がある。給水のヒドラジン濃度は上限値を設定していないが,ヒドラジンの注入量が
過剰になると,ボイラ内でヒドラジンが熱分解(図A.8のヒドラジンの分解を参照)して生じるア
ンモニアの量が増加し,蒸気へのアンモニアの溶解量が増加し,復水器の復水のpHが上昇する原
因になる。そのため,銅合金を使用している復水器の場合には,特に注意が必要で,給水のpHと
銅濃度を監視しながらヒドラジンの注入量を調節しなければならない。
7) 鉄については,常用使用圧力が7.5 MPaを超え15 MPa以下の揮発性物質処理の場合には,Fe: 20 μg/L
以下に保つことが望ましい。
8) 常用使用圧力が3 MPa以下のボイラでは,給水中の銅の濃度を規定しないが,低く維持することが
望ましい。目安としては,常用使用圧力が3 MPaを超え5 MPa以下のボイラに準じてCu: 50 μg/L
以下とすることが望ましい。
b) 酸素処理
1) 循環ボイラでは,酸素が十分供給されないドレン系統の鉄抑制対策としてpHを9.4〜9.5に上昇さ
せる場合がある。
2) 溶存酸素による腐食抑制効果を保持するため,酸電気伝導率は管理値0.02 mS/m以下に対し,0.01
mS/m以下とすることが望ましい。
3) 保護皮膜を形成して定常運転が継続した場合は,溶存酸素の濃度が低めの値でも保護皮膜を保持で
きることから,管理値の範囲内で給水の鉄,銅などの濃度が最小になるのに適した溶存酸素の値を
設定することが望ましい。
4) 各系統の鉄の濃度は酸化鉄の溶解度の減少に伴い低下するため,給水の鉄の濃度は従来の水処理に
比べ抑制できると考え,実際の管理としては鉄の濃度をFe: 2 μg/L以下に保つことが望ましい。
5) 酸素処理を適用する設備では,酸素とアンモニアとによる腐食・破孔事故の発生を避けるために,
復水器細管及び給水加熱器加熱管に銅合金を使用しないことが望ましい。
8.2.2
ボイラ水の水質
8.2.2.1
水質の管理項目及び管理値
イオン交換水を使用する産業用水管ボイラのボイラ水の水質は,アルカリ処理,低濃度水酸化ナトリウ
ム処理,りん酸塩処理,揮発性物質処理[AVT(R)]及び酸素処理の処理方式,並びに常用使用圧力によっ
て区分し,表9によるほか,次による。
a) 船用の主ボイラに用いる場合には,表9の該当する圧力区分の同一水処理方式を用いた場合の水質を
適用する。
b) 船用の補助ボイラに用いる場合には,表5の該当する圧力区分のイオン交換水を用いた場合の水質を
適用する。
c) 船用の補給水の場合,造水器で生成した蒸留水もイオン交換水と同様の水質を適用する。
なお,10 MPaを超えるボイラ用の補給水としては,蒸留水をポリシャー(純水装置)で処理するこ
とが望ましい。
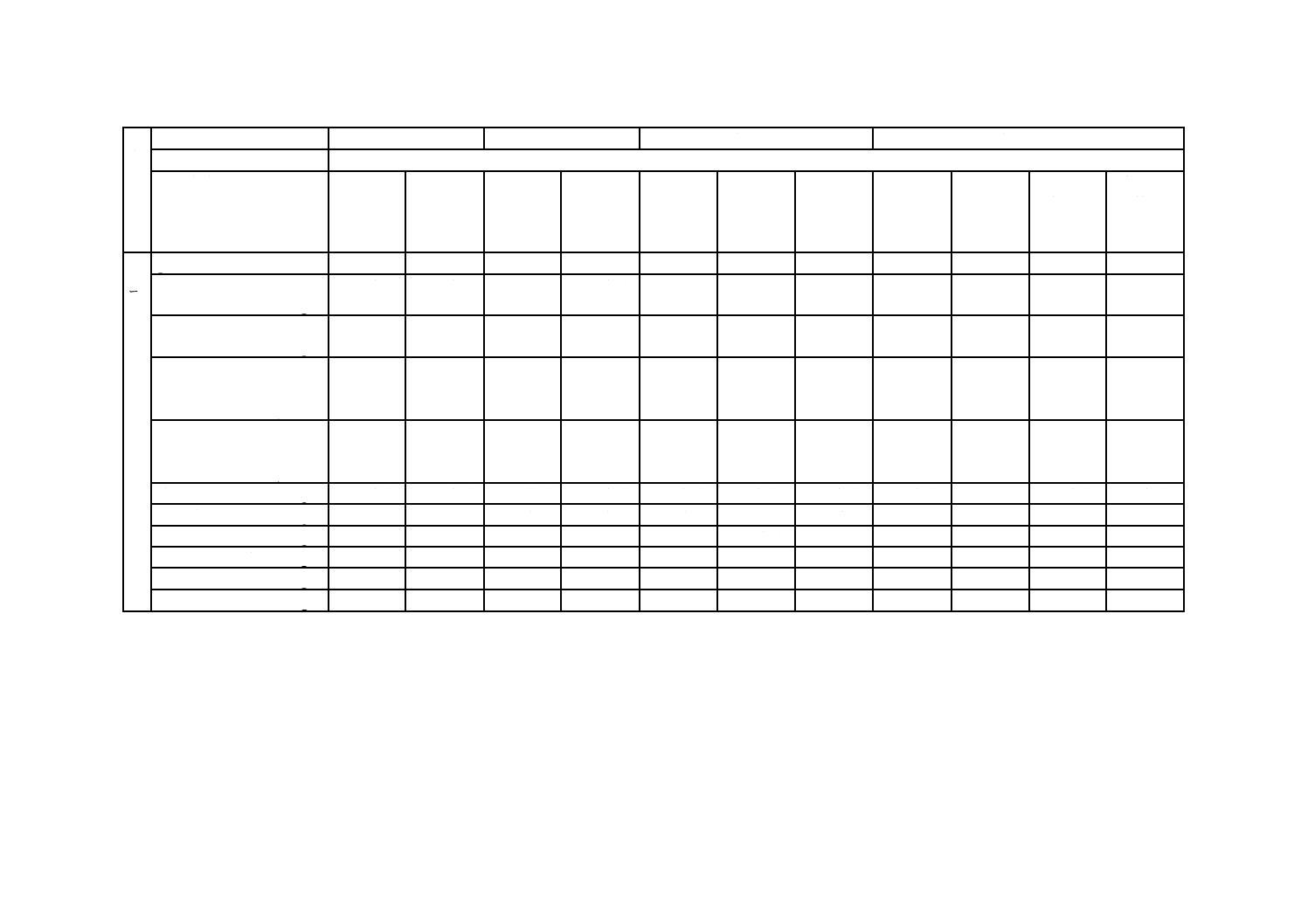
17
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
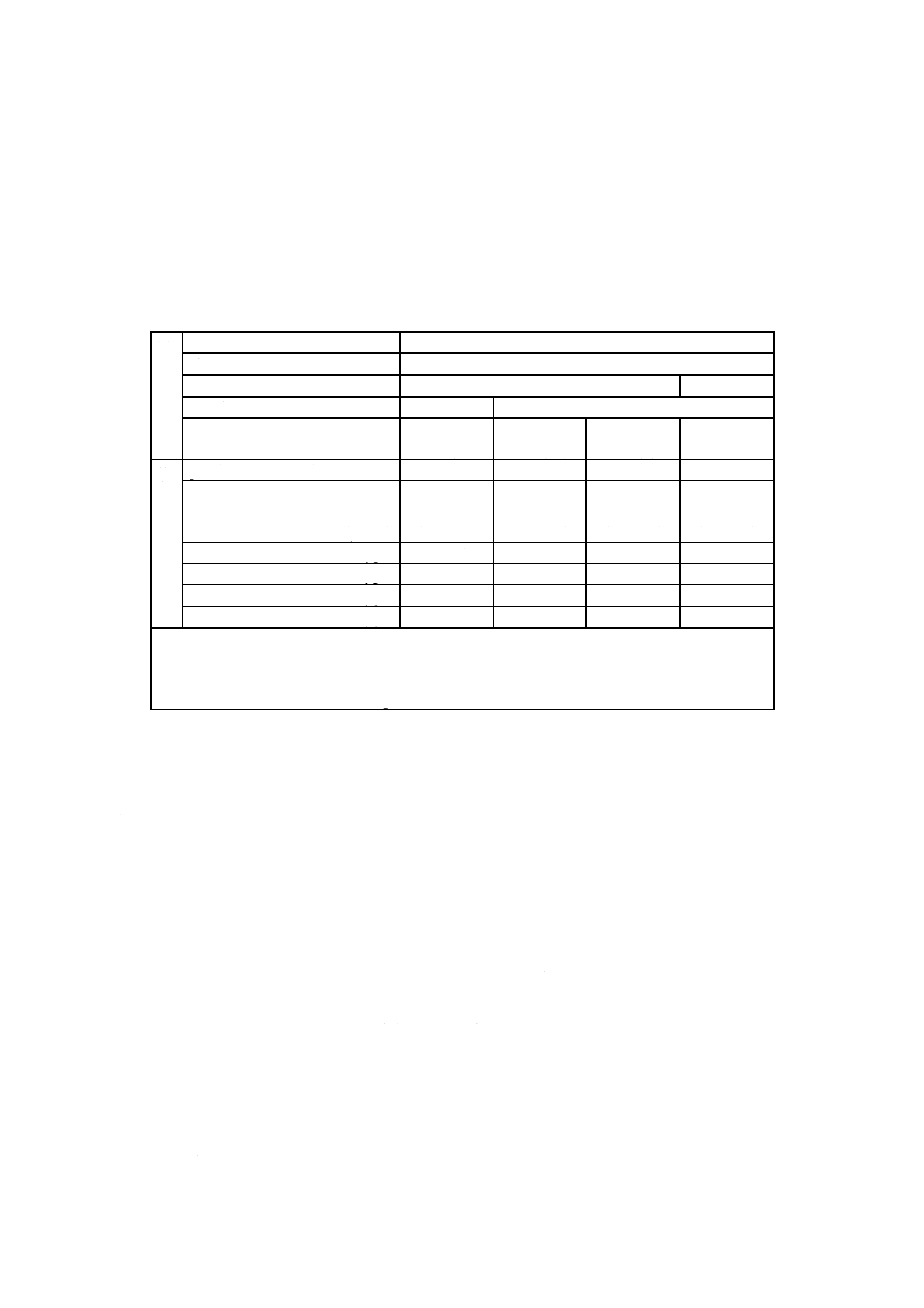
表9−産業用水管ボイラのボイラ水の水質(イオン交換水を使用する場合)の管理項目及び管理値
区
分
常用使用圧力
MPa
2以下
2を超え3以下
3を超え5以下
5を超え7.5以下
補給水の種類
イオン交換水
処理方式
アルカリ
処理
りん酸塩
処理
アルカリ
処理
りん酸塩
処理
アルカリ
処理
低濃度
水酸化
ナトリウ
ム処理
りん酸塩
処理
アルカリ
処理
低濃度
水酸化
ナトリウム
処理
りん酸
塩処理
揮発性
物質処理
[AVT(R)]
ボ
イ
ラ
水
pH(25 ℃における)
10.5〜11.5
9.8〜10.8
10.0〜11.0
9.4〜10.5
9.6〜10.8
9.4〜10.0
9.4〜10.5
9.6〜10.5
9.4〜10.0
9.2〜10.2
8.5〜9.7
酸消費量(pH4.8)
CaCO3: mg/L
250以下
130以下
150以下
100以下
−
−
−
−
−
−
−
酸消費量(pH8.3)
CaCO3: mg/L
200以下
100以下
120以下
80以下
−
−
−
−
−
−
−
電気伝導率
(25 ℃における) mS/m
150以下
120以下
100以下
80以下
80以下
3以下
60以下
50以下
3以下
40以下
−
(μS/cm)(1 500以下)
(1 200以下)
(1 000以下)(800以下)(800以下)(30以下) (600以下)(500以下)(30以下) (400以下)
−
酸電気伝導率
(25 ℃における) mS/m
−
−
−
−
−
6以下
−
−
6以下
−
6以下
(μS/cm)
−
−
−
−
−
(60以下)
−
−
(60以下)
−
(60以下)
塩化物イオン
Cl: mg/L
150以下
150以下
100以下
100以下
80以下
2以下
80以下
50以下
2以下f)
50以下
2以下
りん酸イオンa) PO4: mg/L
10〜30
10〜30
5〜15
5〜15
5〜15
−g)
5〜15
3〜10
−g)
10以下
−h)
ナトリウム
Na: mg/L
−
−
−
−
−
2.8以下
−
−
2.8
−
−
亜硫酸イオンb) SO3: mg/L
10〜20
10〜20
5〜10
5〜10
5〜10
−e)
5〜10
−
−
−
−
ヒドラジンc) N2H4: mg/L
0.1〜0.5
0.1〜0.5
−
−
−
−
−
−
−
−
−
シリカd)
SiO2: mg/L
50以下
50以下
50以下
50以下
20以下
20以下
20以下
3以下
3以下
3以下
3以下
6
B
8
2
2
3
:
2
0
1
5
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
18
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
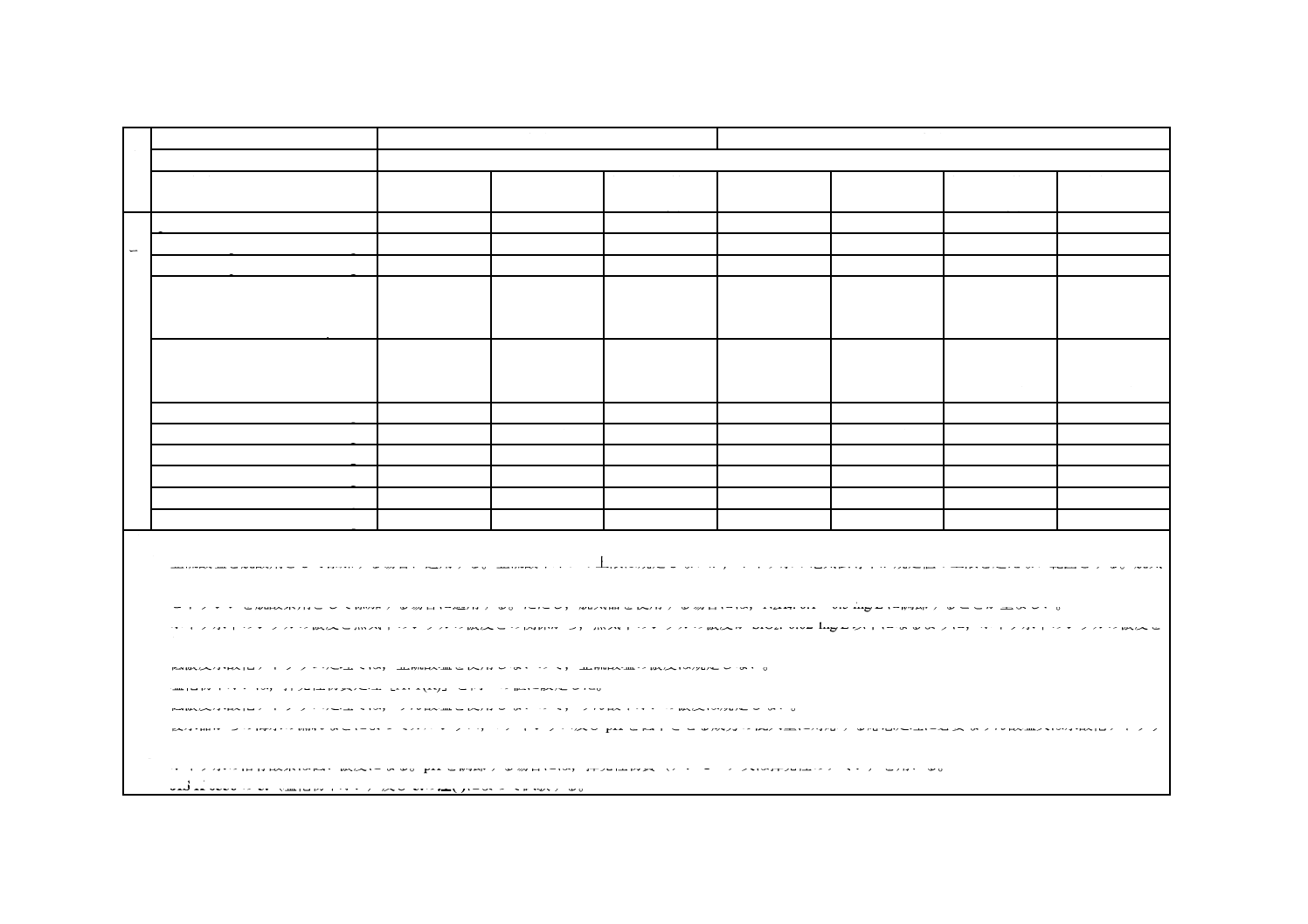
表9−産業用水管ボイラのボイラ水の水質(イオン交換水を使用する場合)の管理項目及び管理値(続き)
区
分
常用使用圧力
MPa
7.5を超え10以下
10を超え15以下
補給水の種類
イオン交換水
処理方式
低濃度水酸化
ナトリウム処理
りん酸塩処理
揮発性物質処理
[AVT(R)]
低濃度水酸化
ナトリウム処理
りん酸塩処理
揮発性物質処理
[AVT(R)]
酸素処理i)
ボ
イ
ラ
水
pH(25 ℃における)
9.4〜10.0
9.0〜10.0
8.5〜9.7
9.1〜9.5
8.5〜9.8
8.5〜9.7
8.0〜10.0 i)
酸消費量(pH4.8) CaCO3: mg/L
−
−
−
−
−
−
−
酸消費量(pH8.3) CaCO3: mg/L
−
−
−
−
−
−
−
電気伝導率
(25 ℃における)
mS/m
43以下
15以下
−
1以下
6以下
−
−
(μS/cm)
(30以下)
(150以下)
−
(10以下)
(60以下)
−
−
酸電気伝導率
(25 ℃における)
mS/m
6以下
−
6以下
2以下
−
2以下
0.3以下
(μS/cm)
(60以下)
(−)
(60以下)
(20以下)
−
20以下
3以下
塩化物イオン
Cl: mg/L
2以下f)
10以下
2以下
1以下f)
2以下
1以下
0.05以下j)
りん酸イオンa)
PO4: mg/L
−g)
6以下
−h)
−g)
3以下
−h)
−
ナトリウム
Na: mg/L
2.8以下
−
−
0.9以下
−
−
−
亜硫酸イオンb)
SO3: mg/L
−
−
−
−
−
−
−
ヒドラジンc)
N2H4: mg/L
−
−
−
−
−
−
−
シリカd)
SiO2: mg/L
2以下
2以下
2以下
0.3以下
0.3以下
0.3以下
0.3以下
注a) りん酸塩を添加する場合に適用する。
b) 亜硫酸塩を脱酸剤として添加する場合に適用する。亜硫酸イオンの上限は規定しないが,ボイラ水の電気伝導率が規定値の上限を超えない範囲とする。脱気
器を使用する場合は,SO3: 10〜20 mg/Lに調節する。
c) ヒドラジンを脱酸素剤として添加する場合に適用する。ただし,脱気器を使用する場合には,N2H4: 0.1〜0.5 mg/Lに調節することが望ましい。
d) ボイラ水中のシリカの濃度と蒸気中のシリカの濃度との関係から,蒸気中のシリカの濃度がSiO2: 0.02 mg/L以下になるように,ボイラ水中のシリカの濃度を
低く保つ。
e) 低濃度水酸化ナトリウム処理では,亜硫酸塩を使用しないので,亜硫酸塩の濃度は規定しない。
f) 塩化物イオンは,揮発性物質処理[AVT(R)]と同一の値に設定した。
g) 低濃度水酸化ナトリウム処理では,りん酸塩を使用しないので,りん酸イオンの濃度は規定しない。
h) 復水器からの海水の漏れなどによってカルシウム,マグネシウム及びpHを低下させる成分の混入量に対応する応急処理に必要なりん酸塩又は水酸化ナトリウ
ムを添加する。
i) ボイラ水の溶存酸素は低い濃度になる。pHを調節する場合には,揮発性物質(アンモニア又は揮発性のアミン)を用いる。
j) JIS K 0556の5.(塩化物イオン)及び5.の注(6)によって試験する。
6
B
8
2
2
3
:
2
0
1
5
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
19
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
8.2.2.2
水質に関する留意事項
ボイラ水の水質については,表9によるほか,次の事項について留意することが望ましい。
a) アルカリ処理
1) ボイラの運転圧力が高いほど伝熱面でのボイラ水の濃縮が著しくなることから,各圧力区分ごとに
pHの範囲を遵守する。
2) 酸消費量はボイラ水のpHを間接的に管理するとともに,シリカによるスケール付着を防止する目
的でボイラ水の酸消費量を管理するが,次の点を考慮して上限を超えないように管理することが望
ましい。
− 圧力3 MPa以下のボイラで補給水にイオン交換水を用いる場合は,ボイラ水の酸消費量は主とし
て水質調整剤に由来するので,容易に低い値に維持できる。
− 圧力3 MPaを超えるボイラでは,補給水がイオン交換水又はこれと同等以上の水質の水を使用し,
ボイラ水のシリカの濃度を低く調節するので,ボイラ水のpHを管理すれば酸消費量を直接管理
する必要はないと考え,規定の対象から除外する。
3) 脱酸素剤として亜硫酸塩を使用する場合,イオン交換水を使用する運転圧力2 MPa以下のボイラに
ついては脱気器を設置しないものとして,下限濃度を設定する。ただし,1〜5 MPaのボイラで脱気
器を設置するものは,その脱気器の性能保証値に合わせて下限濃度及び上限濃度を設定する。
なお,常用使用圧力が5 MPa以上のボイラについては,高温下では亜硫酸塩の自己分解による二
酸化硫黄(SO2)又は硫化水素(H2S)の発生による蒸気系統及びボイラ内の腐食を助長することか
ら,亜硫酸塩の使用を避けることが望ましい。そのため,常用使用圧力が5 MPaを超えるボイラに
対しては濃度を設定しない。
4) 脱酸素剤としてヒドラジンを使用する場合,ボイラ水の残留濃度として,常用使用圧力が2 MPa以
下のボイラについては脱気器を設置しない場合は上限濃度を高く,一方,脱気器を設置する場合は
上限濃度を低く設定する。常用使用圧力が2 MPaを超えるボイラでは脱気器を設置するので,ボイ
ラ水ではなく,給水中の溶存酸素の濃度に応じた給水中の残留ヒドラジン濃度を設定する。
5) ボイラ水中のシリカの濃度と蒸気中のシリカの濃度との関係から,蒸気中のシリカの濃度がSiO2:
0.02 mg/L以下になるように,ボイラ水中のシリカの濃度を低く保つことが望ましい。
b) 低濃度水酸化ナトリウム処理
1) ボイラ水中のシリカの濃度と蒸気中のシリカの濃度との関係から,蒸気中のシリカの濃度がSiO2:
0.02 mg/L以下になるように,ボイラ水中のシリカの濃度を低く保つことが望ましい。
2) 低濃度水酸化ナトリウム処理では,ボイラ水中の腐食性陰イオンの管理が重要であるため,硫酸イ
オンの発生源の一つとなる亜硫酸塩は脱酸素剤として使用しない。
c) りん酸塩処理 ボイラ水中のシリカの濃度と蒸気中のシリカの濃度との関係から,蒸気中のシリカの
濃度がSiO2: 0.02 mg/L以下になるように,ボイラ水中のシリカの濃度を低く保つことが望ましい。
d) 揮発性物質処理[AVT(R)] ボイラ水中のシリカの濃度と蒸気中のシリカの濃度との関係から,蒸気
中のシリカの濃度がSiO2: 0.02 mg/L以下になるように,ボイラ水中のシリカの濃度を低く保つことが
望ましい。
e) 酸素処理 ボイラ水中のシリカの濃度と蒸気中のシリカの濃度との関係から,蒸気中のシリカの濃度
がSiO2: 0.02 mg/L以下になるように,ボイラ水中のシリカの濃度を低く保つことが望ましい。
20
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
8.3
電力事業用循環ボイラの水質
8.3.1
給水の水質
8.3.1.1
水質の管理項目及び管理値
電力事業用循環ボイラの給水の水質は,常用使用圧力によって区分し,表10による。
a) 常用使用圧力が15 MPa以下の場合は,産業用水管ボイラ(イオン交換水を使用する場合)の当該圧
力区分を参照する。
表10−電力事業用循環ボイラの給水の水質の管理項目及び管理値
区
分
常用使用圧力
MPa
15を超え20以下
補給水の種類
イオン交換水
処理方式
揮発性物質処理
酸素処理
還元剤
あり
なし
酸化還元性
還元形
[AVT(R)]
低酸化形
[AVT(LO)]
酸化形
[AVT(O)]
酸化形
(OT)
給
水
pH(25 ℃における)
8.5〜10.3 a)
8.5〜10.3 a)
8.5〜10.3 a)
8.0〜10.3
酸電気伝導率(25 ℃における)
mS/m
(μS/cm)
0.05以下
(0.5以下)
0.05以下
(0.5以下)
0.02以下
(0.2以下)
0.02以下
(0.2以下)
溶存酸素
O: μg/L
7以下
5未満
5〜20
20〜50
鉄
Fe: μg/L
20以下
20以下
10以下
5以下
銅
Cu: μg/L
5以下
5以下
5以下
5以下
ヒドラジン
N2H4: μg/L
10以上
−
−
−
注a) プラント使用材料によって変える必要があるため,給水加熱器の管材が低圧給水加熱器及
び高圧給水加熱器とも銅合金製の場合はpH 8.5〜9.0に,低圧給水加熱器が銅合金で高圧給
水加熱器が鋼管製の場合にはpH 9.0〜9.4に,両加熱器とも鋼管製の場合にはpH 9.3〜10.3
(復水器が銅合金製の場合はpHの上限を9.6とする。)に調節し,管理する。
8.3.1.2
水質に関する留意事項
電力事業用循環ボイラの給水の水質については,次の事項について留意することが望ましい。
a) 揮発性物質処理[AVT(R)及びAVT(LO)]
1) 給水pHは,FAC対策上高めに保持するのが望ましい。
2) AVT(LO)の場合,銅材料を使用するプラントにおいて,溶存酸素濃度O: 5 μg/L以上となる場合は,
AVT(R)に変更することが望ましい。
3) ボイラにもち込む鉄は,極力低減することが望ましいことから,Fe: 10 μg/L以下に保つことが望ま
しい。
4) AVT(R)の場合,ヒドラジンの濃度は,ボイラ入口(エコノマイザがある場合は,エコノマイザ入口)
の給水に残留することが望まれる下限値であり,ヒドラジンの注入量は,この下限値を維持するよ
うに調節するのが望ましい。ただし,近年,復水器の性能向上によって通常運転時のヒドラジンの
注入を停止しても,脱気器入口の溶存酸素の濃度を1 μg/L以下に保持できるプラントもあり,ヒド
ラジンの濃度の低減化が可能である。
5) AVT(R)の場合,ヒドラジンを注入することによって,確実に給水が還元性の環境になることから,
溶存酸素濃度の管理値は,脱気器性能の保証値であるO: 7 μg/L以下とする。
6) 還元剤(ヒドラジン)の注入を停止することによって,蒸気の過熱低減器スプレー水のノズルが頻
繁に閉塞する場合があるので,そのような場合は,AVT(R)に戻すことが望ましい。
21
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
7) AVT(LO)の処理方法を用いた循環ボイラでの導入実績は,国内ではないことから,導入に当たって
は全系統の鉄濃度を監視することが望ましい。
b) 揮発性物質処理[AVT(O)]
1) 給水pHは,防食対策上高めに保持するのが望ましい。
2) 還元剤(ヒドラジン)の注入を停止することによって,蒸気の過熱低減器スプレー水のノズルが頻
繁に閉塞する場合があるので,そのような場合は,AVT(R)に戻すことが望ましい。
3) AVT(O)の処理方法を用いた循環ボイラでの導入実績は,国内ではないことから,導入に当たっては
全系統の鉄濃度を監視することが望ましい。
c) 酸素処理
1) 循環ボイラでは,酸素が十分供給されないドレン系統の鉄抑制対策としてpHを9.4〜9.5に上昇さ
せる場合がある。ただし,復水脱塩装置の再生頻度が増加するとともに,系統に銅合金が使用され
ているプラントでは,高pH域におけるアンモニアによる腐食が発生するので注意する。
そのほかに,抽気系へのアンモニア注入,ステンレス鋼の採用などを考える。
2) 酸電気伝導率は,ボイラの鋼材表面に形成される酸化鉄の皮膜が,水中の塩化物イオンなどの陰イ
オンの増加によって破壊されるので,それらの総量に相当する電気伝導率よりも低い0.01 mS/m以
下であることが望ましい。
3) 保護皮膜を形成して定常運転が継続した場合は,溶存酸素が低めの値でも保護皮膜を保持できるの
で,管理値の範囲内で給水の鉄,銅などの濃度が最小になるのに適した溶存酸素の値を設定するこ
とが望ましい。
4) 各系統の鉄の濃度は酸化鉄の溶解度の減少に伴い低下するため,給水の鉄の濃度は従来の水処理に
比べ抑制できると考え,実際の管理としては鉄濃度をFe: 2 μg/L以下に保つことが望ましい。
8.3.2
ボイラ水の水質
8.3.2.1
水質の管理項目及び管理値
電力事業用循環ボイラのボイラ水の水質は,常用使用圧力によって区分し,表11による。

22
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
表11−電力事業用循環ボイラのボイラ水の水質の管理項目及び管理値
区
分
常用使用圧力
MPa
15を超え20以下
補給水の種類
イオン交換水
処理方式
りん酸塩
処理
揮発性物質処理
酸素処理
低濃度
水酸化ナトリ
ウム処理a)
還元剤
あり
なし
酸化還元性
還元形
[AVT(R)]
低酸化形
[AVT(LO)]
酸化形
[AVT(O)]
酸化形
(OT)
ボ
イ
ラ
水
pH(25 ℃における)
8.5〜9.8
8.5〜10.0
8.5〜10.0
8.5〜10.0 8.0〜10.0 b)
9.1〜9.5
電気伝導率(25 ℃における)
mS/m
(μS/cm)
6以下
(60以下)
−
(−)
−
(−)
−
(−)
1以下
(10以下)
酸電気伝導率(25 ℃における)
mS/m
(μS/cm)
−
(−)
2以下
(20以下)
0.3以下
(3以下)
0.3以下
(3以下)
2以下
(20以下)
ナトリウム
Na: mg/L
−
−
−
−
0.9以下
塩化物イオン
Cl: mg/L
2以下
1以下
0.1以下
0.05以下c)
1以下
りん酸イオン
PO4: mg/L
3以下
d)
−
−
−
シリカ
SiO2: mg/L
0.2以下
0.2以下
0.2以下
0.2以下
0.2以下
注a) 低濃度水酸化ナトリウム処理を適用するボイラの圧力区分は,16.5 MPa以下とする。
b) ボイラ水の溶存酸素の濃度は低くなる。pHを調節する場合には,揮発性物質(アンモニア又は揮発性のアミ
ン)を用いる。
c) JIS K 0556の5.(塩化物イオン)及び5.の注(6)によって試験する。
d) 復水器からの海水の漏れなどによってカルシウム,マグネシウム及びpHを低下させる成分が混入した場合に
は,カルシウム,マグネシウム及びpHを低下させる成分の混入量に対応する応急処理に必要なりん酸塩又は
水酸化ナトリウムを添加する。
8.3.2.2
水質に関する留意事項
電力事業用循環ボイラのボイラ水の水質については,次の事項について留意することが望ましい。
a) 共通事項 ボイラ水中のシリカの濃度と蒸気中のシリカの濃度との関係から,蒸気中のシリカの濃度
がSiO2: 0.02 mg/L以下になるように,ボイラ水中のシリカの濃度を低く保つことが望ましい。
b) 揮発性物質処理[AVT(R)及びAVT(LO)] 給水pHは,FAC対策上高めに保持するのが望ましい。ま
た,揮発性物質処理によるボイラ水のpHは,ボイラ水中に残留するアンモニウムなどの揮発性塩基
だけで保たれる。このため,アンモニウムが蒸気側に揮発するとボイラのpHは低下するが,給水と
ボイラ水とのpHの差は,ボイラの運転条件その他の影響を受けて一定ではないので,ボイラ水のpH
は給水のpHと同じ範囲を目標にして管理することが望ましい。
c) 揮発性物質処理[AVT(O)] ボイラ水のpHは,防食対策上高めに保持することが望ましい。
d) 酸素処理 酸電気伝導率は,ボイラの鋼材表面に形成される酸化鉄の皮膜が,水中の塩化物イオンな
どの陰イオンの増加によって破壊されるので,それらの総量に相当する電気伝導率もより低い0.01
mS/m以下であることが望ましい。
9
電力事業用排熱回収ボイラの水質
9.1
一般
通常運転中の水質について規定する。高圧系にドラムを設置しないなど,貫流ボイラの要素を含んだ電
力事業用排熱回収ボイラの場合は,当該要素の部位だけ表14の貫流ボイラの水質を適用する。
23
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
9.2
給水の水質
9.2.1
水質の管理項目及び管理値
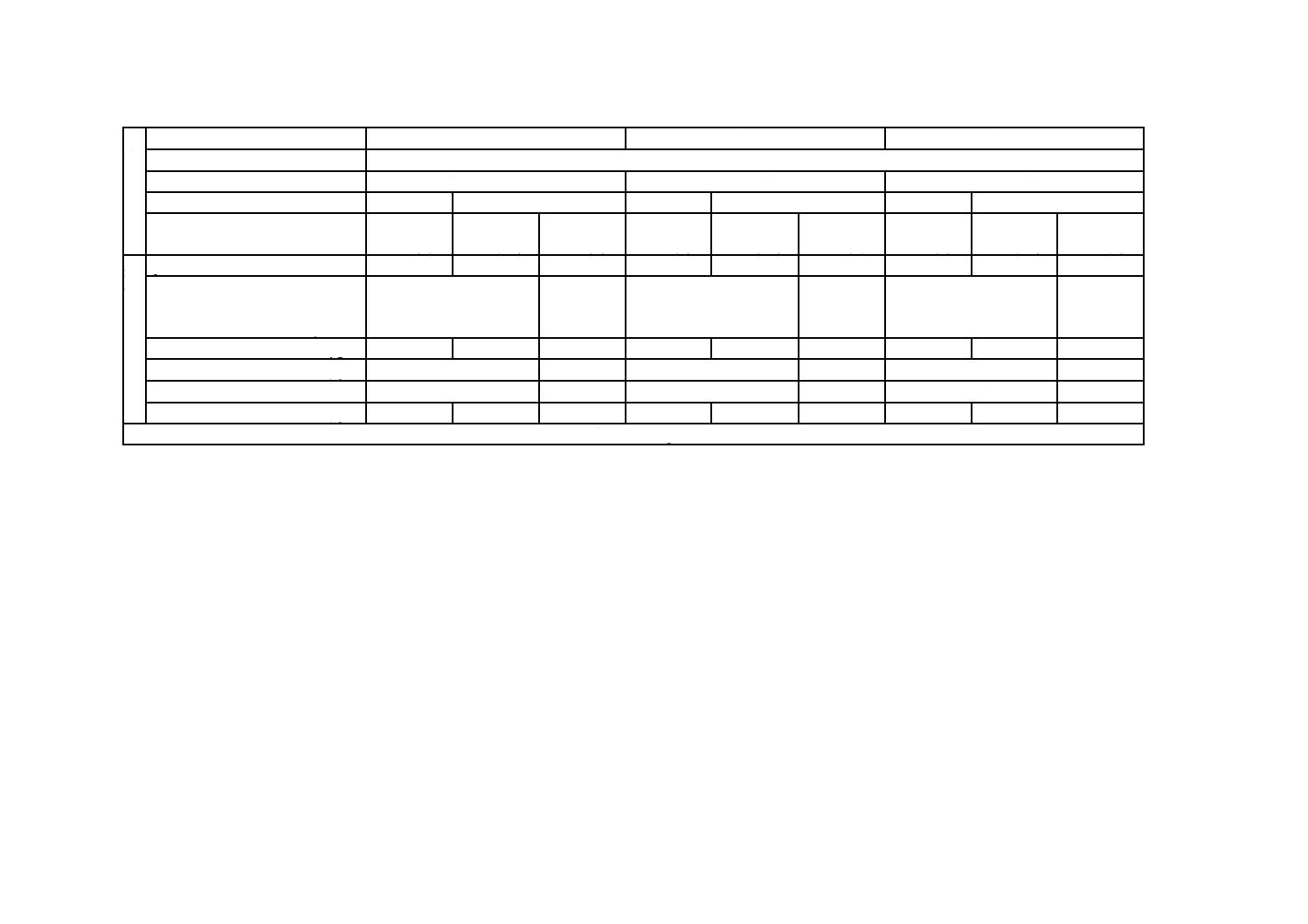
電力事業用排熱回収ボイラは,補給水にイオン交換水を用い,同一の給水を複数圧のドラムに供給する。
電力事業用排熱回収ボイラの給水の水質は,表12のとおり,構成される複数圧のドラムのうち,最も高
い常用使用圧力の区分を用いて管理する。
9.2.2
水質に関する留意事項
電力事業用排熱回収ボイラの給水の水質については,次の事項について留意することが望ましい。
a) 揮発性物質処理[AVT(R)]
1) ボイラ水に揮発性物質処理を適用する場合,給水pHは,ボイラ水のpHを保持できる値とし,かつ,
銅材料を使用していない場合の給水pHは,FAC対策上高めに保持することが望ましい。
2) ヒドラジンの濃度は,ボイラ入口(エコノマイザがある場合は,エコノマイザ入口)の給水に残留
することが望まれる下限値であり,ヒドラジンの注入量は,この下限値を維持するように調節する
のが望ましい。ただし,近年,復水器の性能向上によって通常運転時のヒドラジンの注入を停止し
ても,脱気器入口の溶存酸素の濃度をO: 1 μg/L以下に保持できるプラントもあり,ヒドラジンの濃
度の低減化が可能である。
3) ヒドラジンを注入することによって,確実に給水が還元性の環境になることから,溶存酸素濃度の
管理値は脱気器性能の保証値であるO: 7 μg/L以下とする。
4) 常用使用圧力15 MPa以下の場合の鉄濃度はFe: 20 μg/L以下,15 MPaを超える場合の鉄濃度はFe: 10
μg/L以下に管理することが望ましい。
b) 揮発性物質処理[AVT(LO)]
1) 銅材料を使用していない場合の給水pHは,FAC対策上高めに保持することが望ましい。
2) 銅合金を使用するプラントにおいて,溶存酸素濃度がO: 5 μg/L以上となる場合は,揮発性物質処理
AVT(R)に変更することが望ましい。
3) 常用使用圧力15 MPa以下の鉄濃度はFe: 20 μg/L以下,15 MPaを超える鉄濃度はFe: 10 μg/L以下に
管理することが望ましい。
4) 還元剤(ヒドラジン)の注入を停止することによって,蒸気の過熱低減器スプレー水のノズルが頻
繁に閉塞する場合があるので,そのような場合はAVT(R)に戻すことが望ましい。
c) 揮発性物質処理[AVT(O)]
1) 給水pHは,防食対策上高めに保持することが望ましい。
2) 還元剤(ヒドラジン)の注入を停止することによって,蒸気の過熱低減器スプレー水のノズルが頻
繁に閉塞する場合があるので,そのような場合はAVT(R)に戻すことが望ましい。
9.3
ボイラ水の水質
9.3.1
水質の管理項目及び管理値
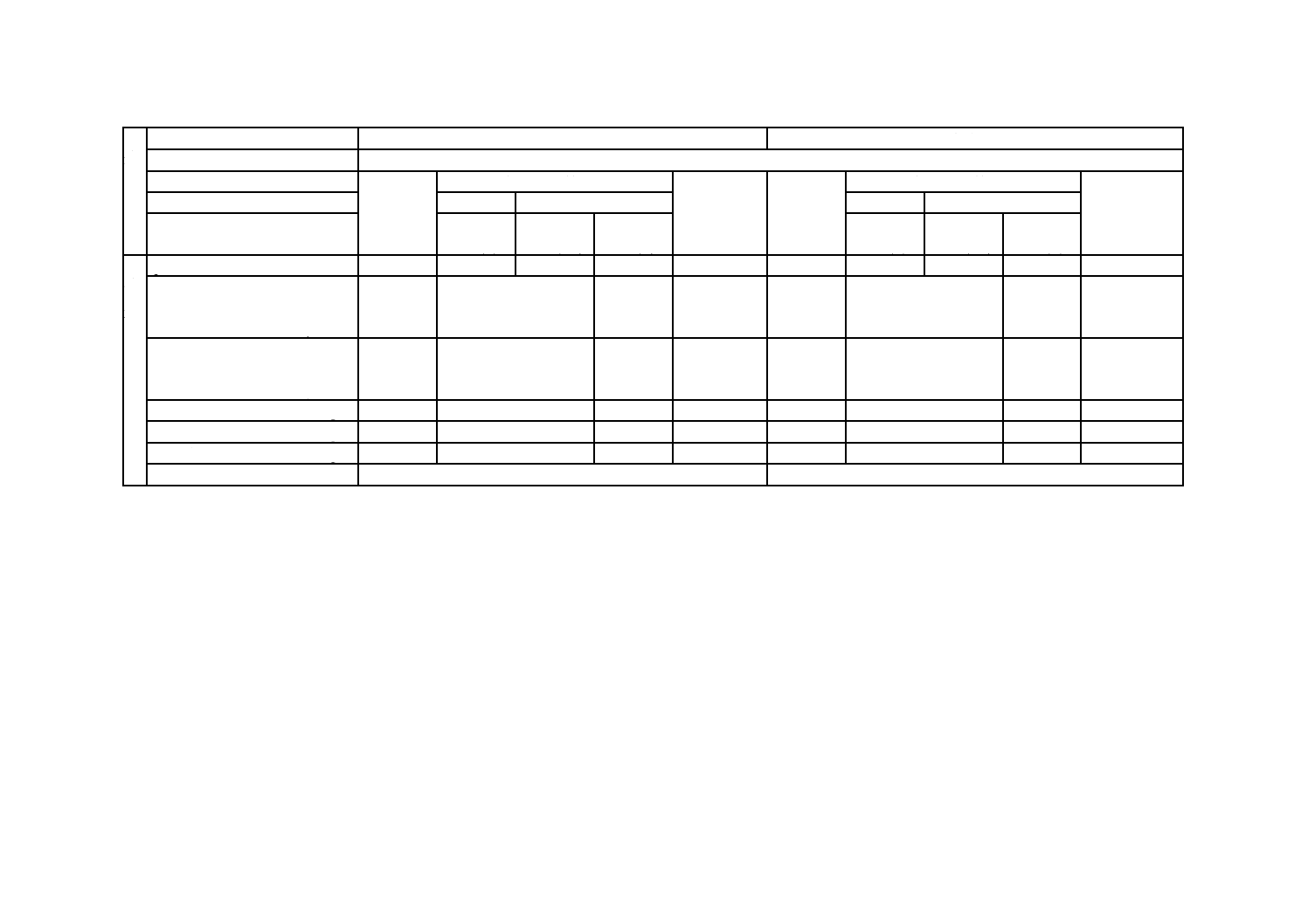
電力事業用排熱回収ボイラは,補給水にイオン交換水を用い,同一の給水を複数圧のドラムに供給する。
電力事業用排熱回収ボイラのボイラ水の水質は,表13のとおり,構成されるドラムの常用使用圧力に応
じた水質の管理値に基づき管理する。
9.3.2
水質に関する留意事項
電力事業用排熱回収ボイラのボイラ水の水質の共通事項については,次の事項について留意することが
望ましい。
a) ボイラ水のpHは,低圧ドラムの温度が低いことから,FAC対策上高めに保持することが望ましい。
24
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
b) ボイラ水中のシリカの濃度と蒸気中のシリカの濃度との関係から,蒸気中のシリカの濃度がSiO2: 0.02
mg/L以下になるように,ボイラ水中のシリカの濃度を低く保つことが望ましい。
10 貫流ボイラの水質
10.1 水質の管理項目及び管理値
貫流ボイラの給水水質は,常用使用圧力及び処理方法によって区分し,表14による。
10.2 水質に関する留意事項
給水の水質については,次の事項について留意することが望ましい。
a) 共通事項
1) 貫流ボイラは,高純度の給水を要求するため,補給水はイオン交換水が用いられ,運転中の循環水
の不純物を除くため,汽水循環系統にろ過装置及び復水脱塩装置を設置することが多い。
2) 給水のpH調整は,通常アンモニアにて行われており,鉄系酸化物のFAC防止にはpHを高くする
ことが望ましい。実際に,復水及び給水の溶存酸素を低値に管理するプラントでは,pH 9.3以上で
は系統中の鉄濃度が減少する傾向にある。ただし,復水器に銅系の管材を使用しているプラントで
は,高pH域におけるアンモニアによる腐食の発生に注意する。
3) 貫流ボイラは,給水の水質が障害の発生及び蒸気純度に直接影響を及ぼすため,給水中の全蒸発残
留物,すなわち,その大部分である給水の電解質成分を,可能な限り低く抑える必要がある。
b) 揮発性物質処理
1) 負圧状態で運転する復水系統及び低圧給水加熱器の抽気ドレン系統では空気の吸い込みによって,
又は補給水からのもち込みによって,溶存酸素に影響を与える場合がある。
2) AVT(R)の場合,溶存酸素を低減する目的で系統水中にヒドラジンを投入し,エコノマイザ入口の給
水に残留するレベルで投入することが望ましいが,脱気器出口の溶存酸素濃度に応じて管理値を低
減することも可能である。また,ボイラにもち込む鉄は極力低減することが望ましく,10 MPa以下
ではFe: 20 μg/Lに,10 MPaを超え20 MPa以下ではFe: 10 μg/Lとすることが望ましい。
3) AVT(LO)の場合,ボイラにもち込む鉄は極力低減することが望ましく,10 MPa以下ではFe: 20 μg/L
に,10 MPaを超え20 MPa以下ではFe: 10 μg/Lとすることが望ましい。
4) AVT(O)の場合,溶存酸素による腐食影響を低減するため,酸電気伝導率は管理値0.02 mS/m以下に
対し,0.01 mS/m以下とすることが望ましい。
5) 還元剤(ヒドラジン)の注入停止によって,蒸気の過熱低減用スプレー水のノズルが頻繁に閉塞す
る場合があるので,その際はAVT(R)に変更するなどの対応が必要となる。
c) 酸素処理
1) 酸素処理では,酸素が十分供給されないドレン系統の鉄抑制対策として(系統に銅合金が使用され
ていない場合),pHを9.4〜9.5に上昇させる場合がある(ただし,復水脱塩装置の再生頻度が増加
する。)。そのほかに,抽気系へのアンモニア注入,ステンレス鋼の採用などを考える。
2) 溶存酸素による腐食抑制効果を保持するため,酸電気伝導率は管理値0.02 mS/m以下に対し,0.01
mS/m以下とすることが望ましい。
3) 鉄系酸化物表面のち(緻)密な保護皮膜の形成には,溶存酸素O: 20〜200 μg/L程度が必要である。
O: 200 μg/L以上存在すると,すぐに保護皮膜が不安定になることはないが,場合によっては孔食の
発生が徐々に進展するなど,腐食性が増すので注意が必要である。一方,保護皮膜を形成して定常
運転が継続した場合は,溶存酸素が低めの値でも保護皮膜を保持できるので,管理値の範囲内で給
25
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
水の鉄,銅などの濃度が最小になるのに適した溶存酸素の値を設定することが望ましい。
4) 酸素処理では,鉄の管理値をFe: 5 μg/L以下(目標Fe: 2 μg/L)と規定しているが,鉄系酸化物がボ
イラ内で局所的に堆積し,加熱噴破する事例があることから,給水の鉄濃度はできるだけ低い値に
管理することが望ましい。
26
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
表12−電力事業用排熱回収ボイラの給水の水質の管理項目及び管理値
区
分
常用使用圧力
MPa
10以下
10を超え15以下
15を超え20以下
補給水の種類
イオン交換水
処理方式
揮発性物質処理
揮発性物質処理
揮発性物質処理
還元剤
あり
なし
あり
なし
あり
なし
酸化還元性
還元形
[AVT(R)]
低酸化形
[AVT(LO)]
酸化形
[AVT(O)]
還元形
[AVT(R)]
低酸化形
[AVT(LO)]
酸化形
[AVT(O)]
還元形
[AVT(R)]
低酸化形
[AVT(LO)]
酸化形
[AVT(O)]
給
水
pH(25 ℃における)a)
8.5〜10.3
8.5〜10.3
8.5〜10.3
8.5〜10.3
8.5〜10.3
8.5〜10. 3
8.5〜10.3
8.5〜10.3
8.5〜10.3
酸電気伝導率(25 ℃における)
mS/m
(μS/cm)
0.05以下
(0.5以下)
0.02以下
(0.2以下)
0.05以下
(0.5以下)
0.02以下
(0.2以下)
0.05以下
(0.5以下)
0.02以下
(0.2以下)
溶存酸素
O: μg/L
7以下
5未満
5〜20
7以下
5未満
5〜20
7以下
5未満
5〜20
鉄
Fe: μg/L
30以下
20以下
30以下
10以下
20以下
5以下
銅
Cu: μg/L
20以下
10以下
10以下
10以下
5以下
5以下
ヒドラジン
N2H4: μg/L
10以上
−
−
10以上
−
−
10以上
−
−
注a) プラント使用材料によって変える必要があるため,復水器が銅合金製の場合はpHの上限を9.6に調節し管理する。
6
B
8
2
2
3
:
2
0
1
5
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
27
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
表13−電力事業用排熱回収ボイラのボイラ水の水質の管理項目及び管理値
区
分
常用使用圧力
MPa
3以下
3を超え5以下
補給水の種類
イオン交換水
処理方式
りん酸塩
処理
揮発性物質処理
低濃度水酸化
ナトリウム
処理
りん酸塩
処理
揮発性物質処理
低濃度水酸化
ナトリウム
処理
還元剤
あり
なし
あり
なし
酸化還元性
還元形
[AVT(R)]
低酸化形
[AVT(LO)]
酸化形
[AVT(O)]
還元形
[AVT(R)]
低酸化形
[AVT(LO)]
酸化形
[AVT(O)]
ボ
イ
ラ
水
pH(25 ℃における)
9.8〜10.7
8.5〜10.0
8.5〜10.0
8.5〜10.0
9.4〜10.0
9.8〜10.7
8.5〜10.0
8.5〜10.0 8.5〜10.0
9.4〜10.0
電気伝導率(25 ℃における)
mS/m
(μS/cm)
40以下
(400以下)
−
(−)
−
(−)
3以下
(30以下)
40以下
(400以下)
−
(−)
−
(−)
3以下
(30以下)
酸電気伝導率(25 ℃における)
mS/m
(μS/cm)
−
(−)
6以下
(60以下)
0.3以下
(3以下)
6以下
(60以下)
−
(−)
6以下
(60以下)
0.3以下
(3以下)
6以下
(60以下)
ナトリウム
Na: mg/L
−
−
−
2.8以下
−
−
−
2.8以下
塩化物イオン
Cl: mg/L
10以下
2以下
0.1以下
2以下
10以下
2以下
0.1以下
2以下
りん酸イオン
PO4: mg/L
a)
−
−
−
a)
−
−
−
シリカ
SiO2: mg/L
20以下
20以下
6
B
8
2
2
3
:
2
0
1
5
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
28
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
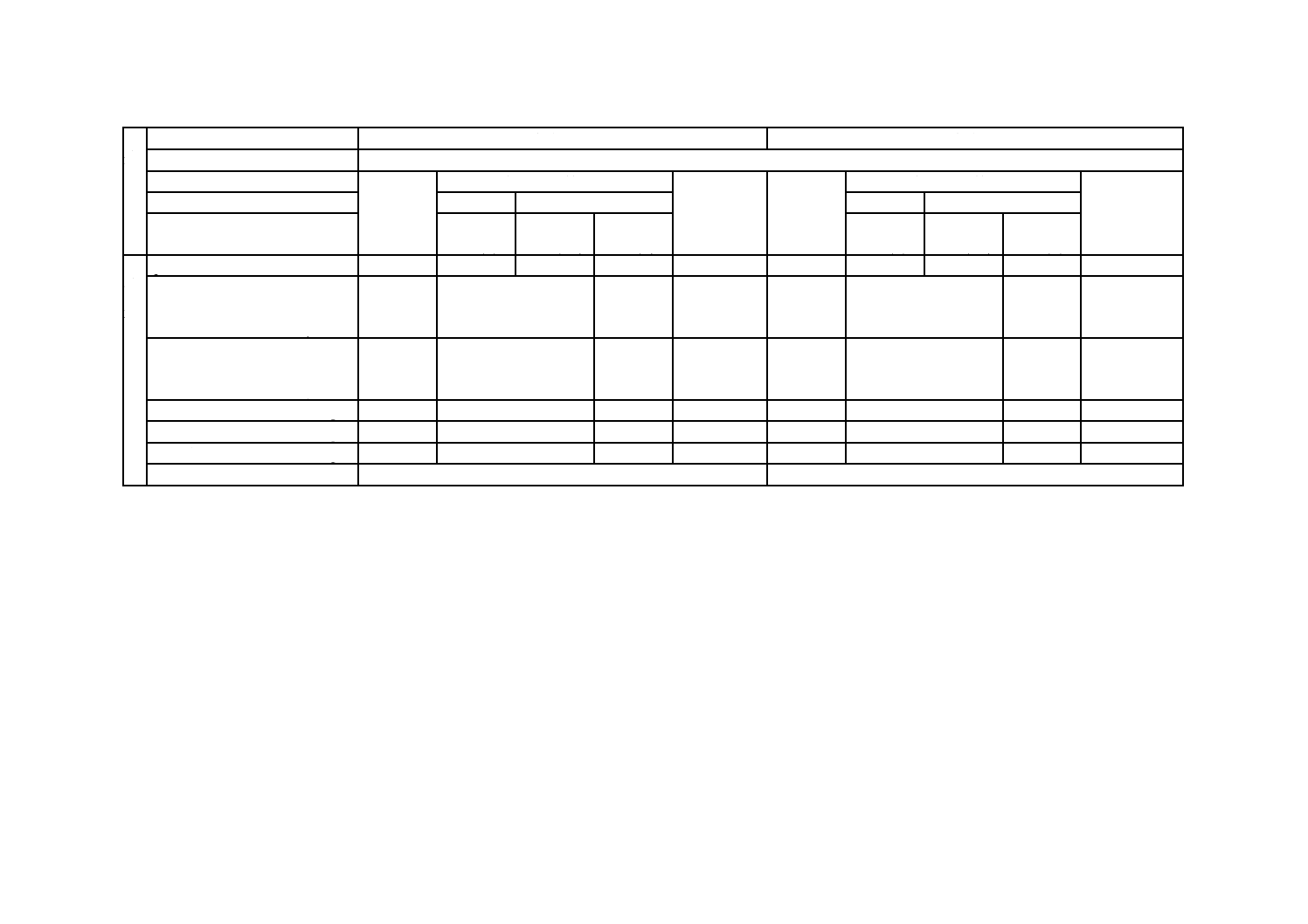
表13−電力事業用排熱回収ボイラのボイラ水の水質の管理項目及び管理値(続き)
区
分
常用使用圧力
MPa
5を超え7.5以下
7.5を超え10以下
補給水の種類
イオン交換水
処理方式
りん酸塩
処理
揮発性物質処理
低濃度水酸化
ナトリウム
処理
りん酸塩
処理
揮発性物質処理
低濃度水酸化
ナトリウム
処理
還元剤
あり
なし
あり
なし
酸化還元性
還元形
[AVT(R)]
低酸化形
[AVT(LO)]
酸化形
[AVT(O)]
還元形
[AVT(R)]
低酸化形
[AVT(LO)]
酸化形
[AVT(O)]
ボ
イ
ラ
水
pH(25 ℃における)
9.2〜10.7
8.5〜10.0
8.5〜10.0 8.5〜10.0
9.4〜10.0
9.0〜10.7
8.5〜10.0
8.5〜10.0 8.5〜10.0
9.4〜10.0
電気伝導率(25 ℃における)
mS/m
(μS/cm)
40以下
(400以下)
−
(−)
−
(−)
3以下
(30以下)
40以下
(400以下)
−
(−)
−
(−)
3以下
(30以下)
酸電気伝導率(25 ℃における)
mS/m
(μS/cm)
−
(−)
6以下
(60以下)
0.3以下
(3以下)
6以下
(60以下)
−
(−)
6以下
(60以下)
0.3以下
(3以下)
6以下
(60以下)
ナトリウム
Na: mg/L
−
−
−
2.8以下
−
−
−
2.8以下
塩化物イオン
Cl: mg/L
10以下
2以下
0.1以下
2以下
10以下
2以下
0.1以下
2以下
りん酸イオン
PO4: mg/L
b)
−
−
−
c)
−
−
−
シリカ
SiO2: mg/L
3以下
2以下
6
B
8
2
2
3
:
2
0
1
5
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
29
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
表13−電力事業用排熱回収ボイラのボイラ水の水質の管理項目及び管理値(続き)
区
分
常用使用圧力
MPa
10を超え15以下
15を超え20以下
補給水の種類
イオン交換水
処理方式
りん酸塩
処理
揮発性物質処理
低濃度水酸化
ナトリウム
処理
りん酸塩
処理
揮発性物質処理
低濃度水酸化
ナトリウム
処理e)
還元剤
あり
なし
あり
なし
酸化還元性
還元形
[AVT(R)]
低酸化形
[AVT(LO)]
酸化形
[AVT(O)]
還元形
[AVT(R)]
低酸化形
[AVT(LO)]
酸化形
[AVT(O)]
ボ
イ
ラ
水
pH(25 ℃における)
9.0〜10.0
8.5〜10.0
8.5〜10.0
8.5〜10.0
9.1〜9.5
8.5〜9.8
8.5〜10.0
8.5〜10.0 8.5〜10.0
9.1〜9.5
電気伝導率(25 ℃における)
mS/m
(μS/cm)
15以下
(150以下)
−
(−)
−
(−)
1以下
(10以下)
6以下
(60以下)
−
(−)
−
(−)
1以下
(10以下)
酸電気伝導率(25 ℃における)
mS/m
(μS/cm)
−
(−)
2以下
(20以下)
0.3以下
(3以下)
2以下
(20以下)
−
(−)
2以下
(20以下)
0.3以下
(3以下)
2以下
(20以下)
ナトリウム
Na: mg/L
−
−
−
0.9以下
−
−
−
0.9以下
塩化物イオン
Cl: mg/L
2以下
1以下
0.1以下
1以下
2以下
1以下
0.1以下
1以下
りん酸イオン
PO4: mg/L
d)
−
−
−
3以下
−
−
−
シリカ
SiO2: mg/L
0.3以下
0.2以下
注a) ボイラ水のpHが9.8〜10.7を維持できるよう調整する。
b) ボイラ水のpHが9.2〜10.7を維持できるよう調整する。
c) ボイラ水のpHが9.0〜10.7を維持できるよう調整する。
d) ボイラ水のpHが9.0〜10.0を維持できるよう調整する。
e) 低濃度水酸化ナトリウム処理を適用するボイラの圧力区分は,16.5 MPa以下とする。
6
B
8
2
2
3
:
2
0
1
5
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
30
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
表14−貫流ボイラの給水の水質の管理項目及び管理値
区
分
常用使用圧力
MPa
7.5を超え10以下
10を超え15以下
補給水の種類
イオン交換水
処理方法
揮発性物質処理
酸素処理
揮発性物質処理
酸素処理
還元剤
あり
なし
あり
なし
酸化還元性
還元形
[AVT(R)]
低酸化形
[AVT(LO)]
酸化形
[AVT(O)]
酸化形
(OT)
還元形
[AVT(R)]
低酸化形
[AVT(LO)]
酸化形
[AVT(O)]
酸化形
(OT)
給
水
pH(25 ℃における)a)
8.5〜10.0
8.5〜10.0
8.5〜10.0
8.0〜10.0
8.5〜10.0
8.5〜10.0
8.5〜10.0
8.0〜10.0
酸電気伝導率(25 ℃における)
mS/m
(μS/cm)
0.03以下
(0.3以下)
0.03以下
(0.3以下)
0.02以下
(0.2以下)
0.02以下
(0.2以下)
0.03以下
(0.3以下)
0.03以下
(0.3以下)
0.02以下
(0.2以下)
0.02以下
(0.2以下)
溶存酸素
O: μg/L
7以下
5未満
5〜20
20〜200
7以下
5未満
5〜20
20〜200
鉄
Fe: μg/L
30以下
30以下
20以下
20以下
20以下
20以下
10以下
10以下
銅
Cu: μg/L
10以下
10以下
10以下
10以下
5以下
5以下
5以下
5以下
ヒドラジン
N2H4: μg/L
10以上
−
−
−
10以上
−
−
−
シリカ
SiO2: μg/L
40以下 b)
20以下 c)
40以下 b)
20以下 c)
40以下 b)
20以下 c)
40以下 b)
20以下 c)
30以下 b)
20以下 c)
30以下 b)
20以下 c)
30以下 b)
20以下 c)
30以下 b)
20以下 c)
6
B
8
2
2
3
:
2
0
1
5
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。

31
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
表14−貫流ボイラの給水の水質の管理項目及び管理値(続き)
区
分
常用使用圧力
MPa
15を超え20以下
20を超えるもの
補給水の種類
イオン交換水
処理方法
揮発性物質処理
酸素処理
揮発性物質処理
酸素処理
還元剤
あり
なし
あり
なし
酸化還元性
還元形
[AVT(R)]
低酸化形
[AVT(LO)]
酸化形
[AVT(O)]
酸化形
(OT)
還元形
[AVT(R)]
低酸化形
[AVT(LO)]
酸化形
[AVT(O)]
酸化形
(OT)
給
水
pH(25 ℃における)a)
8.5〜10.0
8.5〜10.0
8.5〜10.0
8.0〜10.0
8.5〜10.0
8.5〜10.0
8.5〜10.0
8.0〜10.0
酸電気伝導率(25 ℃における)
mS/m
(μS/cm)
0.03以下
(0.3以下)
0.03以下
(0.3以下)
0.02以下
(0.2以下)
0.02以下
(0.2以下)
0.025以下
(0.25以下)
0.025以下
(0.25以下)
0.02以下
(0.2以下)
0.02以下
(0.2以下)
溶存酸素
O: μg/L
7以下
5未満
5〜20
20〜200
7以下
5未満
5〜20
20〜200
鉄
Fe: μg/L
20以下
20以下
5以下
5以下
10以下
10以下
5以下
5以下
銅
Cu: μg/L
3以下
3以下
3以下
3以下
2以下
2以下
2以下
2以下
ヒドラジン
N2H4: μg/L
10以上
−
−
−
10以上
−
−
−
シリカ
SiO2: μg/L
20以下
20以下
20以下
20以下
20以下
20以下
20以下
20以下
注a) 給水加熱器の管材が,低圧給水加熱器及び高圧給水加熱器とも銅合金製の場合はpH 8.5〜9.0に,低圧給水加熱器が銅合金で高圧給水加熱器が鋼管製の場合はpH
9.0〜9.4に,両加熱器及び復水器とも鋼管製又はチタン製の場合はpH 9.3〜10.0(復水器が銅合金製の場合はpHの上限を9.6とする。)に調整し,管理する。
b) セパレータのあるボイラに適用する。
c) セパレータのないボイラに適用する。
6
B
8
2
2
3
:
2
0
1
5
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。

32
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
11 蒸気の質
11.1 蒸気の質の管理項目及び管理値
蒸気の質は,通気する蒸気タービンの方式,及びボイラ水の処理方式によって区分し,表15による。
なお,ここで規定する対象の蒸気は,イオン交換水を給水とするボイラで発生し,タービンに通気され
る蒸気である。
表15−ボイラから発生する蒸気の質の管理項目及び管理値
区
分
蒸気タービンの方式
復水式
背圧式
ボイラ水の処理方式
アルカリ処理
低濃度水酸化
ナトリウム処理
りん酸塩処理
揮発性物質処理
酸素処理
−
蒸
気
酸電気伝導率(25 ℃における)
mS/m
(μS/cm)
0.02以下
(0.2以下)
0.03以下
(0.3以下)
0.02以下
(0.2以下)
−
シリカ
SiO2: μg/L
20以下
ナトリウム
Na: μg/L
5以下
−
11.2 蒸気の質に関する留意事項
蒸気の質については,附属書Bに示す管理項目ごとの一般的な留意事項に加え,次の事項について留意
することが望ましい。
なお,管理値を逸脱した場合の対処方法は,附属書Dを参考とする。
a) 評価方法 蒸気中の不純物で問題となるのは,溶解性塩類,シリカ,鉄,銅などであり,ボイラ水の
気液分配率による化学的キャリオーバ(carry-over),プライミング(priming:水気立ち)又はホーミ
ングによるメカニカルキャリオーバ,及び不純物を含む給水の蒸気の過熱低減器スプレー水としての
使用が,不純物を蒸気中にもち込む。ボイラ水のキャリオーバは,ボイラ水中の不純物の増加,運転
条件の急激な変動などが促進する。蒸気の質の評価は,蒸気サンプルを冷却して生成した凝縮水を分
析することで行う。
b) 管理項目
1) 酸電気伝導率 水酸化物イオン(OH−)以外の陰イオンを含む溶解性塩類(電解質)の混入度合を
評価する指標として測定する。溶解性塩類は,蒸気系統のスケール付着の原因となるほか,蒸気が
凝縮する際に凝縮水中に溶解して電離し,腐食を促進するので,乾湿交番域をもつ復水式のタービ
ン(復水タービン)に通気する蒸気においては,腐食抑制の観点から蒸気中の濃度を可能な限り低
く保つことが望ましい。特に,国内外の運転実績から,補給水率が低く,かつ,ボイラ水の管理が
良好な電力事業用プラントにおいては,蒸気の酸電気伝導率は0.02 mS/m以下で運用できることが
知られていることから,不純物の混入を最小限に抑制する観点からは0.02 mS/m以下に保つことが
望ましい。
なお,アンモニア,ヒドラジン以外の有機系の給水pH調整剤又は脱酸素剤を用いた場合,種類
及び使用量によっては,それらの分解によって生成する二酸化炭素又は有機酸が酸電気伝導率を上
昇させ,管理値を満足できない場合がある。また,復水タンク,給水タンクが大気開放系の場合,
大気中の二酸化炭素が給水に混入し酸電気伝導率を上昇させ,管理値を満足できない場合がある。
これらの場合は,二酸化炭素又は有機酸が系統の腐食を増長する可能性についてプラント製造業
者・薬剤製造業者と協議した上で対処する必要がある。
33
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
2) シリカ シリカは,高温・高圧になるほど蒸気中への溶解度が増大し,蒸気タービン側ヘキャリオ
ーバしやすくなる性質がある。このため,キャリオーバしたシリカは,蒸気タービン低圧部では溶
解度以上の過飽和の状態になり,シリカスケールとして析出し,蒸気タービンの効率低下を引き起
こす。このシリカスケールの付着を防止するために蒸気中のシリカ濃度を低値に管理する必要があ
る。
なお,欧米での運転実績・研究の成果から,蒸気タービンへのシリカスケールの付着をほぼ完全
に抑制するにはSiO2: 10 μg/L以下で運用するのがよいとの意見があり,また,国内外の運転実績と
して補給水率が低く,かつ,ボイラ水の管理が良好な発電事業用プラントにおいてはSiO2: 10 μg/L
以下での運用を達成しており,シリカスケールの付着を最小限に抑制する観点からはSiO2: 10 μg/L
以下に保つことが望ましい。
3) ナトリウム 蒸気系にナトリウムが混入した場合,塩基性のナトリウム塩が凝縮域に溶解・濃縮し
て構成材料の腐食(応力腐食割れなど)の原因となるため,乾湿交番域をもつ復水タービンに通気
する蒸気に対して,ナトリウムの混入を極力防止することが重要である。中でもボイラ水の処理に
アルカリ処理及び低水酸化ナトリウム処理を適用しているユニットでは,ボイラ水のキャリオーバ
によって強塩基性の水酸化ナトリウムとして混入する割合が高く,水酸化ナトリウムは濃縮した場
合の腐食性が大きい上,酸電気伝導率では検出できないことからナトリウム濃度の管理が重要であ
る。
なお,ボイラ水の処理にりん酸塩処理及び揮発性物質処理を適用しているユニットについては,
経験的に強塩基性のナトリウム塩の濃縮に起因する不適合の事例は少なく,蒸気中のナトリウム濃
度とタービンの腐食との因果関係が明確でないことから管理値は設けていないが,経済的運転を達
成しているユニットの実績を踏まえるとNa: 10 μg/L以下に保つことが望ましい。
12 試験
ボイラの給水及びボイラ水の水質試験方法は,JIS B 8224及びJIS K 0556による。ボイラの給水及びボ
イラ水の水質を連続的に監視する場合には,自動計測器を用いるとよい。
注記 自動計測器には,pH自動計測器,電気伝導率自動計測器,溶存酸素自動計測器,シリカ自動
計測器,ヒドラジン自動計測器などがある。
34
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書A
(参考)
ボイラ水の水処理方式
A.1 一般
ボイラ水の処理は,ボイラ内での腐食,スケールの生成,キャリオーバなどの障害を防止するために行
う。ボイラには,それぞれの使用目的に応じて,丸ボイラ,特殊循環ボイラ,水管ボイラ(循環ボイラ),
排熱回収ボイラ及び貫流ボイラがあり,構造,温度及び圧力条件が大きく異なっている。このため,それ
ぞれのボイラの使用目的,構造,温度及び圧力条件に応じた水処理方式を採用する。この附属書では,ア
ルカリ処理,りん酸塩処理,揮発性物質処理,酸素処理及び低濃度水酸化ナトリウム処理について記載す
る。
A.2 アルカリ処理
A.2.1 適用ボイラ
次のボイラ及び常用使用圧力のボイラ水に適用する。
a) 丸ボイラ 常用使用圧力:3 MPa以下
b) 特殊循環ボイラ 常用使用圧力:3 MPa以下
c) 水管ボイラ(循環ボイラ) 常用使用圧力:7.5 MPa以下
A.2.2 処理方法
アルカリ処理は,水酸化ナトリウムなどのアルカリ成分によってボイラ水のpHを調整し,各種のりん
酸塩及びヒドラジン又は非ヒドラジン系脱酸素剤,並びにこれらの複合添加によってボイラ水の水質を調
整する水処理方式である。
この方式は,アルカリ腐食の発生の懸念が少ない温度であること,圧力の低い条件(常用使用圧力7.5
MPa以下)であること,補給水水質及び水質調整剤の種類に制約が少ないことなどのため,低圧ボイラに
広く適用実績がある。
A.2.3 処理の原理
A.2.3.1 軟化水を使用する場合の原理
常用使用圧力2 MPa以下のボイラには補給水に軟化水を使用しているものが多い。
補給水に軟化水を用いれば,水質調整剤として水酸化ナトリウム又は熱分解して水酸化ナトリウムを生
じる薬剤を注入しなくても,軟化水のアルカリ成分(炭酸水素塩及び炭酸塩)が次の反応式のように熱分
解して水酸化ナトリウムを生じるので,結果的にアルカリ処理になる。
2NaHCO3 → Na2CO3+CO2+H2O ··········································· (A.1)
Na2CO3+H2O → 2NaOH+CO2 ·············································· (A.2)
ただし,軟化水のアルカリ成分が熱分解して生じた水酸化ナトリウムの量が,ボイラ水のpH及び酸消
費量を所定の量にまで増加させるのに足りない場合には,更に水質調整剤として水酸化ナトリウム,水酸
化カリウム又は炭酸ナトリウムを加えて調節する。
なお,カルシウムを主体とするスケール付着を防止するための水質調整剤として,従来,りん酸塩を使
用してきたが,排水が富栄養化など水質汚濁の要因の一つとなるため,最近はその使用が避けられ,常用
使用圧力が2 MPa以下のボイラでは,その代替として水溶性の合成高分子ポリマーなどを多く使用する。
35
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
A.2.3.2 イオン交換水を使用する場合の原理
補給水にイオン交換水を用いる場合,pH調整剤として水酸化ナトリウム,各種のりん酸塩,及びヒドラ
ジン又は非ヒドラジン系脱酸素剤,並びにこれらの複合添加によってボイラ水の水質を調節する水処理方
式である。
りん酸塩を使用する場合,Na/PO4モル比は3.0を上回るように水酸化ナトリウムをりん酸イオンに対し
て過剰となるように添加する。
なお,りん酸塩はカルシウムを主体とするスケール付着を防止するための水質調整剤として,軟化水を
使用する場合と同様に使用してきたが,排水が富栄養化など水質汚濁の要因の一つとなるので,最近はそ
の使用を避け,常用使用圧力が5 MPa以下のボイラではりん酸の代替として水溶性の合成高分子ポリマー
を多く使用している。
A.2.4 管理項目
A.2.4.1 軟化水を使用する場合
軟化水を使用する場合のボイラ水の水質の管理項目は,次のとおりである。
a) pH ボイラ水のpHは,腐食の抑制及びスケールの付着防止を目的として管理する項目である。
pHは,ボイラ水のアルカリ成分(NaOH,NaCO3,NaHCO3,Na3PO4及びNa2HPO4)の濃度を表す
指標となる。
ボイラ水のアルカリ成分は,給水がもち込むカルシウム,マグネシウム及びシリカと反応して,カ
ルシウム及びマグネシウムは懸濁状のりん酸塩[水酸化トリス(りん酸)五カルシウム,Ca5(OH)(PO4)3]
及び水酸化物[水酸化マグネシウム,Mg(OH)2]を生成させ,シリカはメタけい酸イオン(SiO32−)
として溶存されるので,スケール化を防止することができる。また,ボイラ水のマグネシウム
(Mg2+)は,pH 11以上では硬質のスケールであるけい酸マグネシウム(MgSiO3)を生成するよりも,
主として水酸化イオン(OH−)と反応して懸濁状(又は浮遊状)の水酸化マグネシウム[Mg(OH)2]
となり,ボイラの底部に堆積するか,又はブローでボイラ外に排出することによって伝熱面上でのス
ケール化を防止することができる。このように,ボイラ水のpHの下限値は,腐食防止はもちろんス
ケール付着の防止の観点も考慮した。
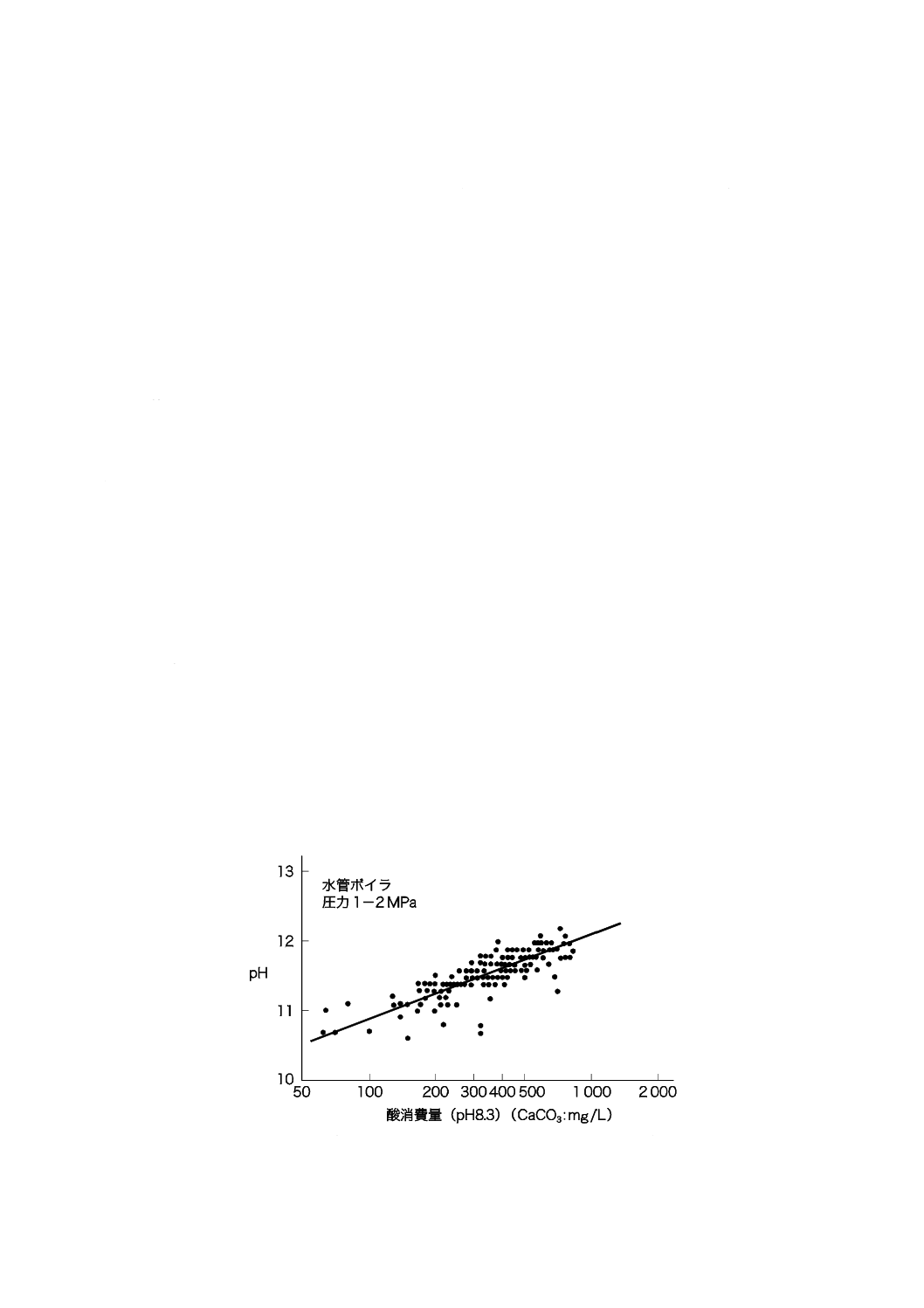
なお,常用使用圧力1 MPaを超え2 MPa以下のボイラ水のpHの範囲は,図A.1 [1]に示す実態調査
結果などを基に規定した。
図A.1−ボイラ水のpHと酸消費量(pH 8.3)との関係[1]
36
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
b) 酸消費量 ボイラ水の酸消費量は,ボイラ水のpHを間接的に管理するとともに,シリカ(SiO2)に
よるスケール付着を防止する目的で管理する項目である。
原水又は軟化水を給水とするボイラでは,硬度成分及びシリカによるスケール化を防止するために
は,ボイラ水のりん酸イオンの濃度を十分に保持し,かつ,pHを11以上で管理する必要がある。
原水又は軟化水を給水とするボイラ水に含まれる溶解性の蒸発残留物のうち,酸消費量の成分は,
通常,水酸化ナトリウム,炭酸ナトリウム,りん酸ナトリウム,けい酸ナトリウムなどの物質である。
これらは,原水の塩類が軟化によってナトリウム塩となったものと,清缶剤の添加に起因するものと
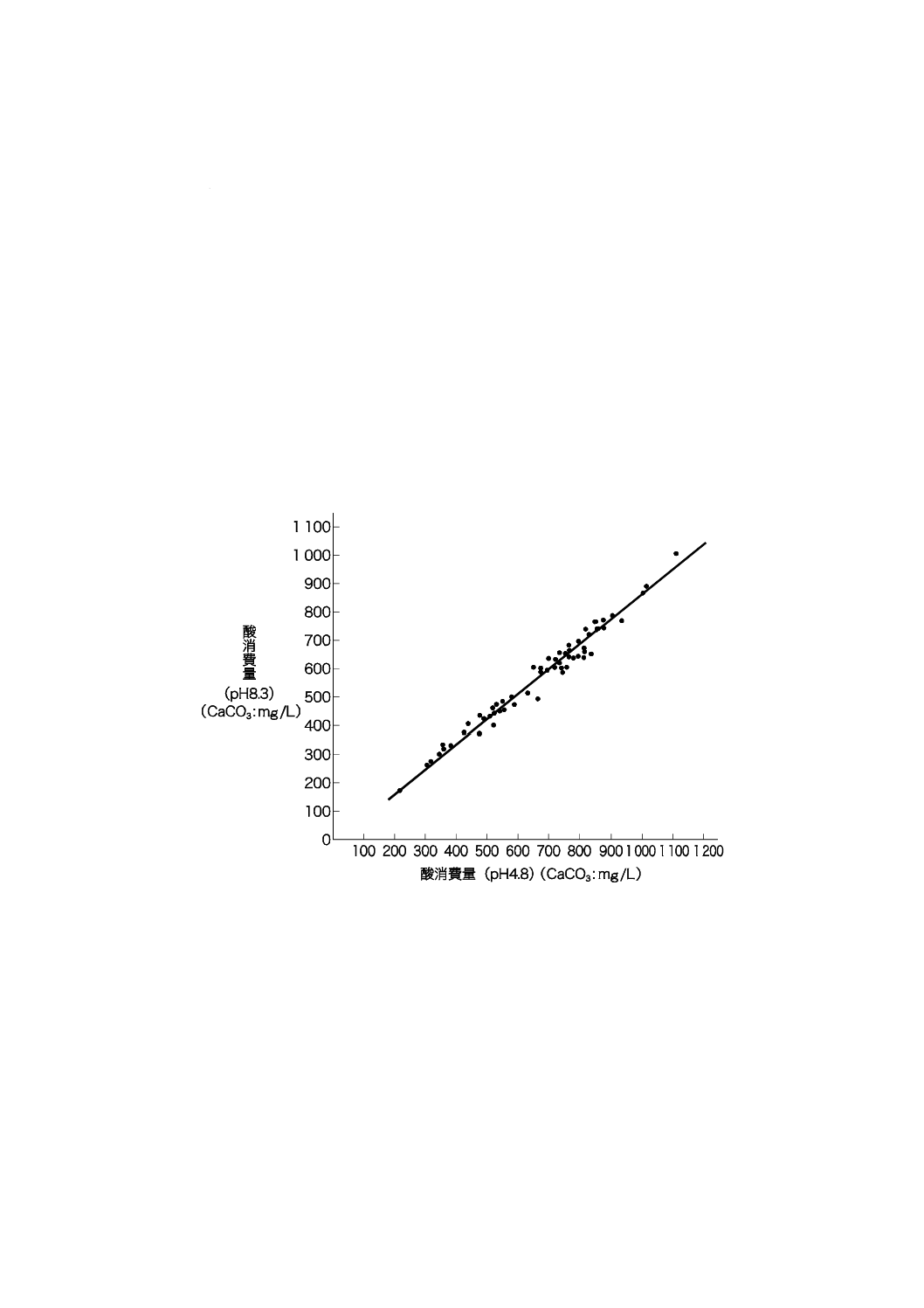
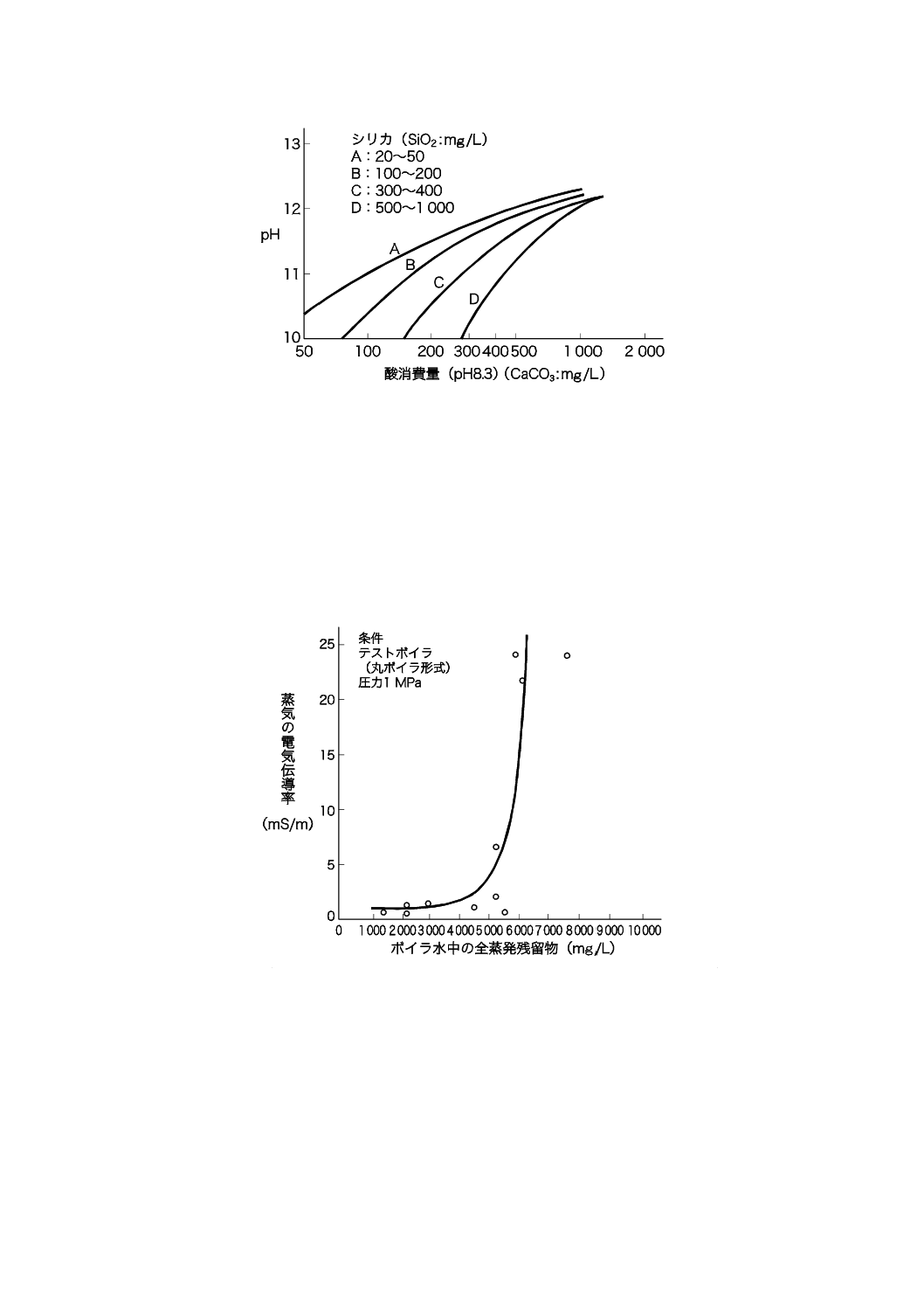
がある。ボイラ水の酸消費量(pH 8.3)及び酸消費量(pH 4.8)の範囲及び上限を図A.2 [1]に示す。ボ
イラ水のシリカ濃度に対応するpHと酸消費量(pH 8.3)との関係を図A.3 [1]に示す。
軟化水を給水とするボイラでは,イオン交換水を給水とするボイラに比べてボイラ水のシリカの濃
度が高くなり,そのためシリカスケールが問題となる場合が多い。しかし,管理値では,シリカの濃
度を規定しないが,シリカのスケールを防止するには,カルシウムを共存させないようにするととも
に,ボイラ水の酸消費量(pH 8.3)は,その上限値に1/1.7を乗じた値とする。これらの濃度以下にな
るようにブロー量を調節して管理するとよい。
図A.2−ボイラ水の酸消費量(pH 8.3)と酸消費量(pH 4.8)との関係(一例)[1]
37
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
図A.3−ボイラ水のシリカ濃度に対応するpHと酸消費量(pH8.3)との関係(一例)[1]
c) 電気伝導率 ボイラ水の電気伝導率は,キャリオーバの防止及びスラッジの堆積の防止を目的として
管理する項目である。
以前は,ボイラ水の全蒸発残留物も規定したが,全蒸発残留物中の溶解性蒸発残留物は,そのほと
んど全量が電解質であるので,全蒸発残留物の濃度と電気伝導率とはほぼ比例関係にある。そこで,
全蒸発残留物の項目を廃止し,電気伝導率で管理することとした。
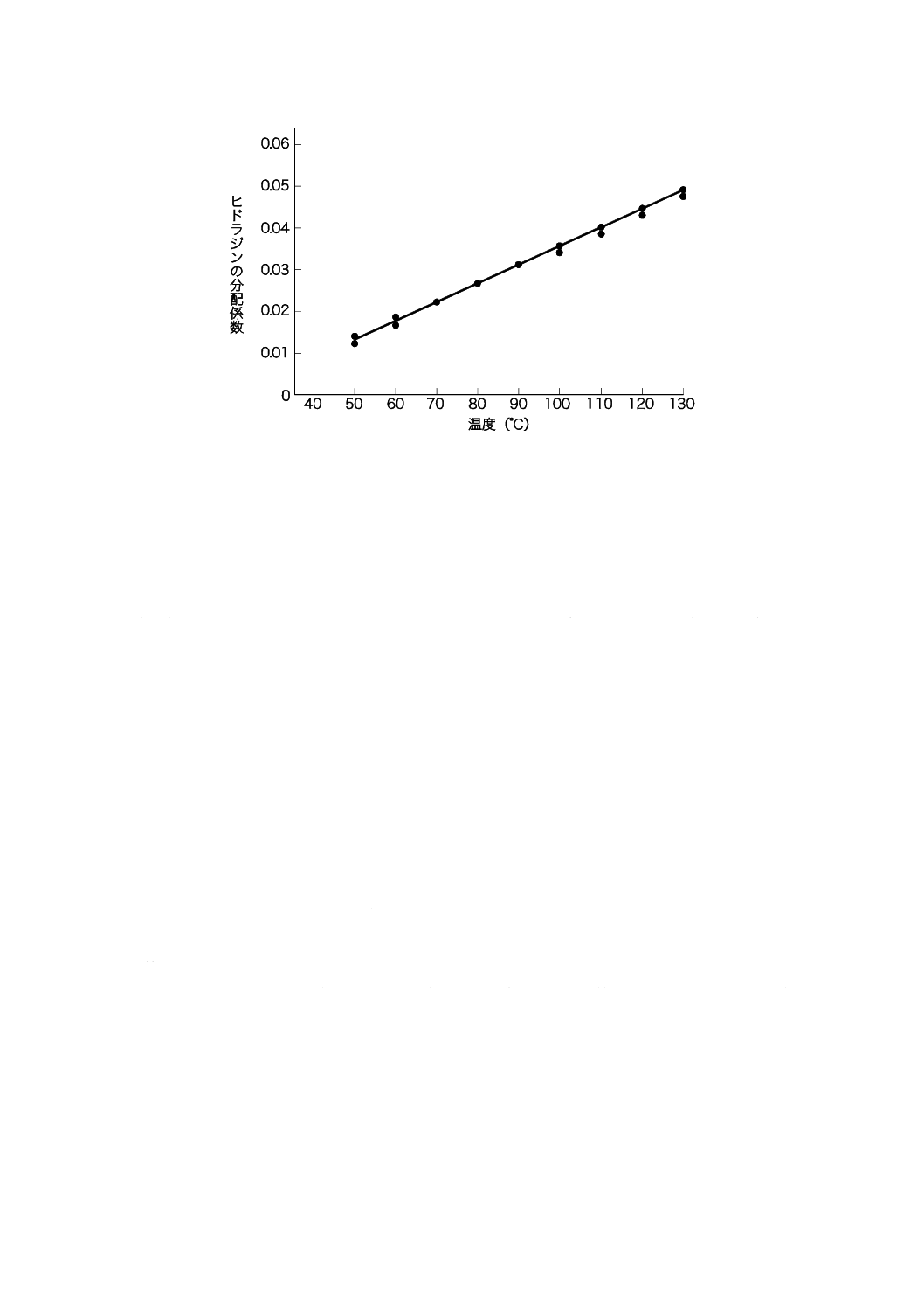
なお,ボイラ水の全蒸発残留物の濃度とキャリオーバ(キャリオーバ量は蒸気の電気伝導率に反映
する。)との関係を図A.4 [2]に示す。
図A.4−ボイラ水の全蒸発残留物の濃度とキャリオーバとの関係(一例)[2]
d) 塩化物イオン ボイラ水の塩化物イオンは,腐食を抑制する目的で管理するとともに,ボイラ水の濃
縮の程度を知る目的で管理する項目である。塩化物イオンは,火力発電プラントの各系統の水中にお
いて沈殿物を生成しないで,常に溶存していることから,ボイラ水及び給水の塩化物イオンの濃度を
測定すれば,ボイラ水の濃縮倍数が推定できる。
また,塩化物イオンは,鋼面の酸化鉄の防食皮膜の安定性を阻害するため,なるべく低濃度に維持
することが望ましい。
38
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
丸ボイラ・水管ボイラ(循環ボイラ)では,全蒸発残留物の濃度の間接的な管理に重点をおき,防
食上の考慮も加え,ボイラ水の塩化物イオンの濃度の上限を規定した。
e) りん酸イオン ボイラ水のりん酸イオンは,給水がもち込むカルシウムによるスケール化を防止する
目的で管理する項目である。
ボイラ水中でのカルシウムとりん酸イオンとの反応は,
5Ca2++OH−+3PO43− → Ca5(OH)(PO4)3 ··································· (A.3)
のとおりであり,炭酸カルシウムCaCO3: 1 mg/L当たり必要なりん酸イオンは,PO4: 0.57 mg/Lである。
丸ボイラ・水管ボイラのボイラ水の水質管理値では,りん酸イオンの濃度をPO4: 20〜40 mg/Lとし
ているが,不測の硬度成分の漏れに対処するためには,上限付近で管理することが必要である。また,
船用に用いる場合の運用については,りん酸イオンの濃度を上限付近に調節する。
f)
亜硫酸イオン又はヒドラジン ボイラ水の亜硫酸イオン又はヒドラジンは,ボイラの腐食因子である
溶存酸素の除去を目的で管理する項目である。給水の溶存酸素を還元除去するために,亜硫酸ナトリ
ウム又はヒドラジンのいずれか一方を注入する(B.8及びB.9を参照)。
亜硫酸ナトリウム又はヒドラジンを注入すると,水中でそれぞれ式(A.4),式(A.5)に示すように溶存
酸素と反応する。したがって,ボイラ水に亜硫酸イオン又はヒドラジンが残留していれば,ボイラ水
中の溶存酸素の除去は十分に行われているものと考えてよい。ボイラ水の水質基準では,これらの残
留濃度の管理値を設定している。
Na2SO3+21O2 → Na2SO4 ······················································ (A.4)
N2H4+O2 → N2+2H2O ························································ (A.5)
ヒドラジンの分配係数(ボイラ水中の濃度に対する蒸気中の濃度の比,揮発度ともいう。)には温度
依存性があり,その一例を,図A.5 [3]に示した。それによるとヒドラジンの分配係数は2〜6 %であり,
ボイラ水に残留したヒドラジンの一部が蒸気へ移行する。また,ヒドラジンはボイラ水においては,
ヒドラジンの一部が式(A.6)に示すように自己分解してアンモニアを生じる。
3N2H4 → 4NH3+N2 ····························································· (A.6)
このアンモニアもまたヒドラジンと同様に蒸気中に移行し,ドレン系の銅合金材の腐食の原因とな
る。以上のことから,ボイラ水に多量のヒドラジンを残留させることは避ける。
常用使用圧力2 MPa以下の水管ボイラには管理値を設定していないが,ヒドラジンを脱酸素剤とし
て注入する場合は,注入点は,給水が空気と接触しない系統のなるべく上流側に,脱気器があればそ
の上流側に,ヒドラジンを注入して注入点以降の系統の腐食を抑制することが有効である。
なお,ヒドラジンは,脱気器での損失が通常極めて少なく,また,その注入によって銅合金の腐食
を生じるほどの高いpHにはならない。しかし,一般に給水の溶存酸素の濃度が高く,ボイラ水に流
入した溶存酸素の相当量が蒸気とともに気化するので,給水の溶存酸素の全量を還元する理論所要量
のヒドラジンを注入する必要はない。また,給水の溶存酸素の濃度が不明なことも多い。このため,
ボイラ水にヒドラジンが残留すれば,ボイラ水には溶存酸素は残留しないとの考えから,亜硫酸イオ
ンの場合と同じようにボイラ水に維持するのが望ましいヒドラジンの濃度範囲を規定している。
39
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
図A.5−ヒドラジンの分配係数の温度依存性[3]
一方,亜硫酸ナトリウムを脱酸素剤として使用した場合は,必ずボイラ水に亜硫酸イオンを常時SO3:
10 mg/L以上残留させることが必要である。このような観点から,常用使用圧力が1 MPa以下の脱気
器を設置しないボイラについては,給水の溶存酸素の濃度の変動及び亜硫酸イオンの反応性を考慮し
て,ボイラ水の亜硫酸イオンの濃度の下限を設定し,また,一方,上限を撤廃した。ボイラ水の亜硫
酸イオンの濃度の上限を設定していないが,亜硫酸イオンの熱分解によって発生する二酸化硫黄
(SO2)の量をできるだけ少なくすることから,SO3: 50 mg/Lを大きく上回らない範囲に制御すること
が望ましい。さらに,熱分解が著しくなる5 MPaを超える常用使用圧力のボイラには亜硫酸ナトリウ
ムは使用しない。
なお,常用使用圧力が1 MPa以下のボイラで脱気器を設置する場合は,上限濃度をSO3: 10〜20 mg/L
と設定している[表9の注b)を参照]。
一般に脱気器を設置する常用使用圧力1 MPa以上のボイラ水に対する亜硫酸イオンの濃度もまた前
記の点を考慮して設定(SO32−: 10〜20 mg/L)している。
A.2.4.2 イオン交換水を使用する場合
イオン交換水を使用する場合のボイラ水の水質管理項目は,次のとおりである。
a) pH ボイラ水において炭素鋼の腐食が最小となる最適なpHについては,これまで幾つかの実験報告
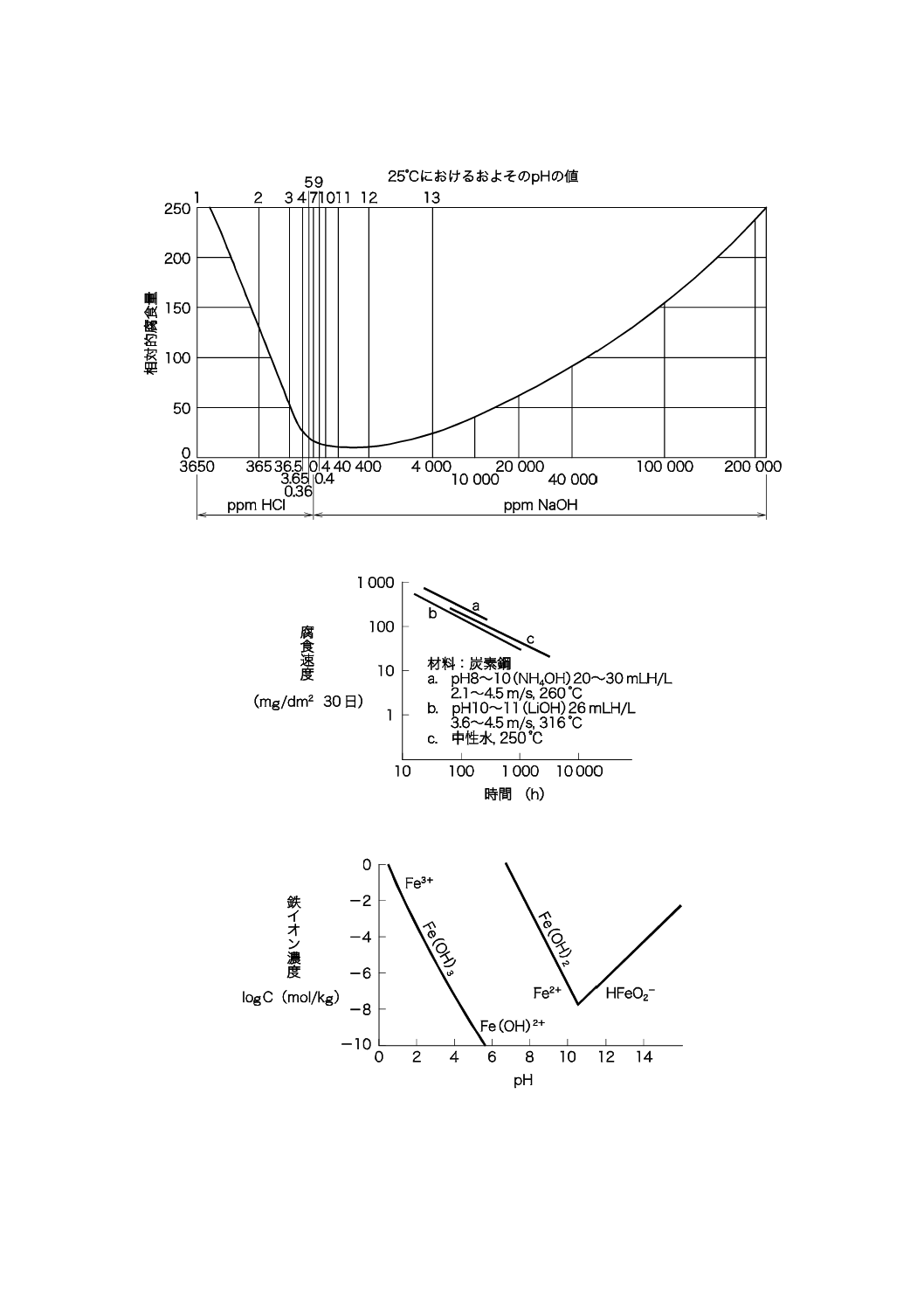
があり,種々の議論がある。その代表的な実験結果として図A.6 [4]に示すE. Berlらの腐食実験でpH 11
〜12の範囲に腐食量の最低域が存在するとされ,従来,この実験結果を基にボイラ内での局部的な濃
縮を考慮してアルカリ処理ではpHを10.5〜11.5の範囲内に保持することが望ましいとの考え方が一
般的であった。
しかし,給水にイオン交換水を使用し溶存酸素の濃度を低い値に管理する最近のボイラの実績及び
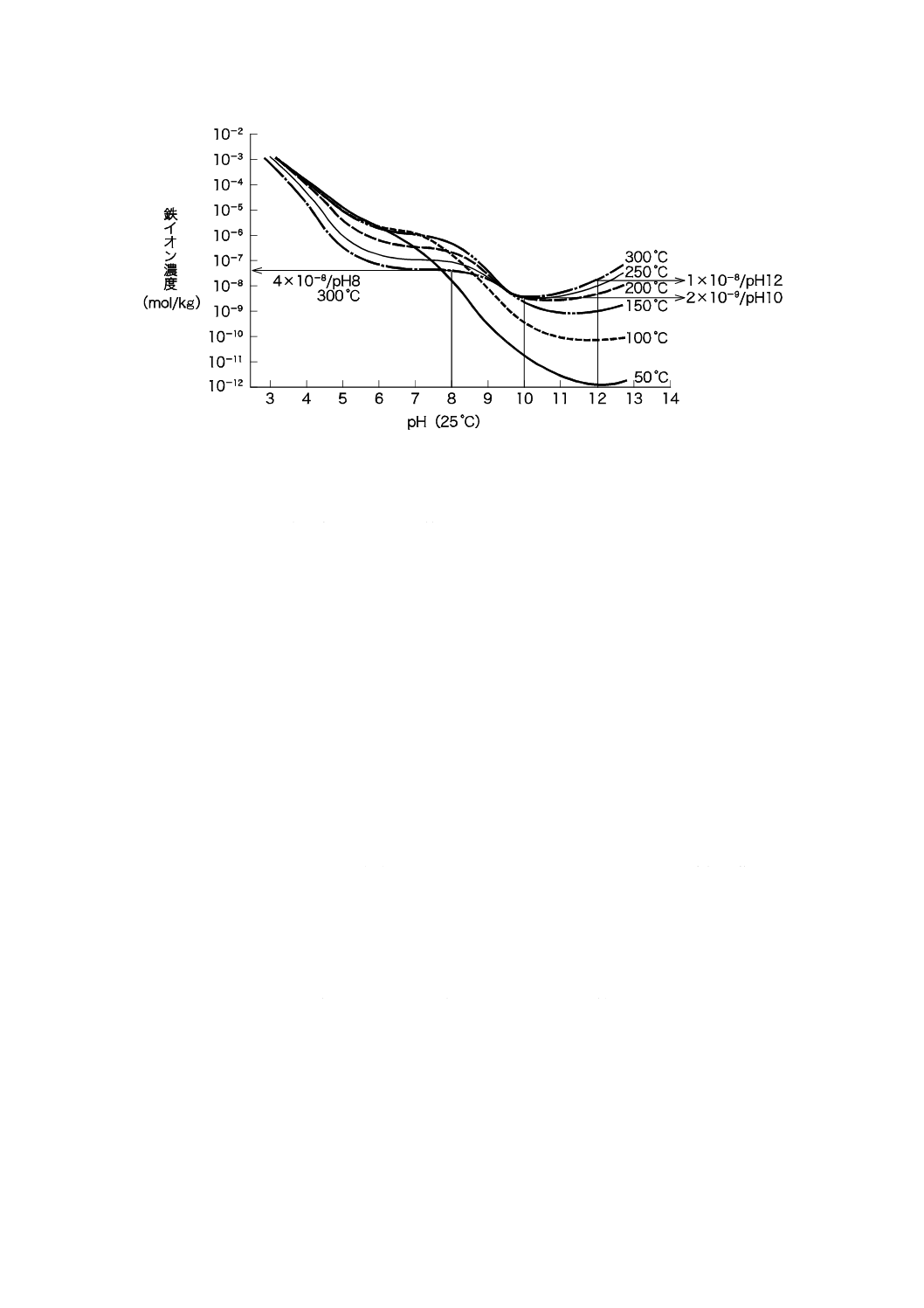
図A.7 [5]に示す高温水中における炭素鋼の腐食速度,図A.8 [6]に示す水酸化鉄の溶解度,並びに図A.9 [7]
に示す四酸化三鉄(マグネタイト)の溶解度からみて腐食が最小のpHは前述の11〜12の範囲にある
ことは疑わしく,pHの相違は腐食の初期段階で若干の差異を与えるだけで,時間の経過に伴って,ほ
とんど腐食速度に差異がないものと考えるようになってきた。
これらの点を考慮し,更にボイラの常用使用圧力が高いほど沸騰伝熱面でのボイラ水のアルカリ成
分を始めとする溶解性蒸発残留物の濃縮が著しくなることから,常用使用圧力の各区分ごとにpHの
40
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
範囲を規定した。すなわち,常用使用圧力が高くなるほどpHを低い値に規定している。
図A.6−pHと鉄の腐食との関係[4]
図A.7−高温水中における炭素鋼のpHによる腐食速度[5]
図A.8−水酸化鉄(II,III)の溶解度に及ぼすpHの影響(25 ℃)[6]
41
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
図A.9−四酸化三鉄(マグネタイト)の溶解度に及ぼすpHの影響[7]
b) 酸消費量 ボイラ水の酸消費量は,ボイラ水のpHを間接的に管理するとともに,シリカを可溶状態
に維持してスケール付着を防止する目的で管理する項目である(B.11を参照)。
常用使用圧力3 MPaを超える水管ボイラ(循環ボイラ)は,補給水にイオン交換水又はこれと同等
以上の水質の水を使用し,ボイラ水のシリカの濃度も低く調節するので,ボイラ水のpHを管理すれ
ば酸消費量を直接管理する必要はないと考え,規定の対象から除外している。
常用使用圧力3 MPa以下のボイラで補給水にイオン交換水を用いた場合は,ボイラ水の酸消費量は
主として水質調整剤に由来し,低い値に維持できる。また,発生蒸気は発電用タービンなどに用いる
こともあるので,キャリオーバを防止するため,酸消費量の抑制が必要となる。これらの点を考慮し
上限を規定する。
c) 電気伝導率 ボイラ水の全蒸発残留物は,給水から導入されたものとボイラ水処理に用いる薬剤から
由来したものとが主なものである。ボイラ水の個々の塩類の作用は種々考えられるが,これを一括し
て総称する全蒸発残留物の濃度が高くなることは,キャリオーバを促進する有力な一因となる。全蒸
発残留物中の溶解性蒸発残留物は,そのほとんど全量が電解質であり,その濃度が高いほどボイラ水
の電気伝導率が高くなるのが通例である。
したがって,測定が容易な電気伝導率を測定することによって,測定が煩雑な溶解性蒸発残留物,
ひいては全蒸発残留物の濃度を推定できるので,電気伝導率を日常管理に利用することが可能である。
イオン交換水を補給水とする場合は,共存する電解質成分が低濃度であり,電気伝導率での管理で
十分に水質の状態を把握できることから全蒸発残留物は規定しないで,前述の関係から電気伝導率を
規定している。
d) 塩化物イオン ボイラ水の塩化物イオンは,腐食を抑制する目的で管理するとともに,ボイラ水の濃
縮の程度を知る目的で管理する項目である。また,復水器を備えたボイラ設備の場合,塩化物イオン
は復水器冷却水の漏えいの有無と漏えいの程度とを表す指標となる。
アルカリ処理のボイラ水の場合,pHの緩衝能力が高いので,復水器冷却水の漏えいによって塩化物
イオン,硫酸イオンなどの腐食性成分をもち込んでも,直ちにpHの低下を示さないが,腐食の防止
のために,もち込みと濃縮とを監視する必要がある。
常用使用圧力の各区分でそれぞれ管理値を設定し,常用使用圧力が高くなるほど塩化物イオンの及
42
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
ぼす影響が大きいことを考慮して低い値に規定している。
e) りん酸イオン ボイラ水のりん酸イオンは,給水がもち込んだカルシウムによるスケール化を防止す
る目的及び鉄鋼に対する防食作用を維持するために管理する項目である。
りん酸イオンは,復水器冷却水の漏えい,補給水の水質悪化などによってボイラにもち込むカルシ
ウムと反応して沈殿物を生成し,これをボイラ水のブローによってボイラの外に除去することによっ
てボイラ伝熱面でのスケール生成を防止することができる。
また,りん酸イオンは,鉄鋼面にりん酸鉄の皮膜を形成し,防食作用があるといわれている。この
ため,新設のボイラの試運転初期の段階ではりん酸イオンを選択的に消費する傾向が強く,ボイラ水
のりん酸イオン濃度が低下する一方で,Na/PO4モル比が投入薬品のNa/PO4モル比よりも高くなる傾
向を示すことがある。ただし,アルカリ処理のボイラ水では,投入薬品のNa/PO4モル比がそもそも共
存する水酸化ナトリウム及びナトリウム塩類によって3.0よりも大きいので,Na/PO4モル比の変動及
びそれに伴うpHの変動はほとんど目立たない。
f)
亜硫酸イオン又はヒドラジン 亜硫酸イオンについては,常用使用圧力1 MPa以下の脱気器を設置し
ないボイラについては残留濃度の不足を回避するために,管理値に下限値を規定し,一方,上限値は
規定しない。
ヒドラジンについては,残留濃度の不足を回避するために管理値に下限値を規定するとともに,過
剰添加によるアンモニアの発生を抑えるために上限値も規定する。
g) シリカ ボイラ水のシリカは,低圧ボイラではボイラ内面に硬質スケールを付着させる原因となり,
中圧ボイラ・高圧ボイラではシリカの選択的キャリオーバによるタービン翼へのシリカ付着の原因に
もなる。
水管ボイラの補給水には通常イオン交換水が用いられ,また,高圧力になるほど蒸気復水の回収率
が大きいのが通例であり,定常運転状態ではボイラ水のシリカの濃度を管理値以下に保つことは可能
である。一方,シリカの選択的キャリオーバはボイラの運転圧力及びボイラ水のシリカの濃度が高く
なるほど著しいので,常用使用圧力が高くなるほどボイラ水のシリカの管理値の上限を低く規定して
いる。
A.2.4.3 留意事項
ボイラ水のアルカリ処理の留意事項は,次のとおりである。
a) 水管ボイラ(循環ボイラ)において,常用使用圧力が7.5 MPa以下であっても,蒸発管伝熱面などで
アルカリ腐食による減肉の懸念・可能性がある場合には,アルカリ処理を適用せず,りん酸ナトリウ
ムによるりん酸塩処理を適用することが望ましい。
b) 水管ボイラ(循環ボイラ)において,りん酸カリウム塩及び水酸化カリウムを使用したアルカリ処理
を適用するのは常用使用圧力2 MPa以下までとする。2 MPa以下であっても,蒸発管にアルカリ腐食
による減肉の可能性がある場合は,ボイラ水の処理方式として,りん酸ナトリウムによるりん酸塩処
理を適用することが望ましい。
A.3 りん酸塩処理
A.3.1 適用ボイラ
主として中圧ボイラ及び高圧ボイラに適用する。具体的には,産業用水管ボイラでイオン交換水を使用
する場合のボイラ水,電力事業用循環ボイラ及び電力事業用排熱回収ボイラのボイラ水となる。
なお,貫流ボイラには,適用しない。
43
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
A.3.2 処理方法
りん酸塩処理は,ボイラ蒸発管のアルカリ腐食を防止するため,ボイラ水中に過剰のアルカリ成分を共
存させることなく,りん酸塩(通常,りん酸三ナトリウム及びりん酸水素二ナトリウム)の濃度とpHと
の関係を適正に維持してボイラ水の水質を調節する方式である。この方式は,りん酸塩の加水分解によっ
て生じる水酸化物イオンの濃度を適正な値に調節するためにNa/PO4のモル比が重要となる。水質管理では
主としてりん酸三ナトリウムをりん酸水素二ナトリウムと併用して,Na/PO4のモル比が調整される。
常用使用圧力3 MPa以下のボイラでは,このモル比を3.0に維持する。一方,3 MPa以上のボイラの場
合には,沸騰伝熱面でりん酸三ナトリウムが濃縮,析出する場合にNa/PO4のモル比が2.6〜2.8となること
を厳しく考えて,ボイラ水中のNa/PO4のモル比を前述の3.0より小さい2.8に保持してpH調節を行う。
さらに,圧力が高くなるほど,りん酸塩の濃度を低く保持する処理を行う。したがって,この補給水には,
イオン交換水を用いる。低圧ボイラでもアルカリ腐食を起こすことを懸念する場合には,りん酸塩処理を
適用する。りん酸塩処理におけるボイラ水のりん酸イオンの濃度とpHとの関係についてはA.3.4 a) 1)に記
載する。
A.3.3 処理の原理
A.3.3.1 腐食抑制
ボイラ水のpHを,鉄系材料の酸化物の溶解度が小さくなる約pH 8.5〜9.7程度のアルカリ性に保持し,
腐食の抑制を図る。また,りん酸イオンは,鉄鋼面にりん酸鉄の皮膜を形成し,防食作用がある[8]。この
ため,試運転初期の段階ではりん酸イオンを選択的に消費する傾向が強く,ボイラ水中のNa/PO4モル比が
投入薬品のモル比よりも高くなる傾向を示す。
ボイラ水に通常使用するりん酸ナトリウム塩には,前述したようにナトリウム数が1個のりん酸二水素
ナトリウム(NaH2PO4),ナトリウム数2個のりん酸水素二ナトリウム(Na2HPO4),ナトリウム数3個の
りん酸三ナトリウム(Na3PO4)があり,水質管理では主としてりん酸三ナトリウムを使用し,りん酸水素
二ナトリウムを併用してNa/PO4のモル比を調整する。りん酸三ナトリウムは,次のように三段階にわたっ
て加水分解し,図A.10に示すようにアルカリ性を呈する[9]。
Na3PO4+H2O ⇆ Na2HPO4+NaOH ·········································· (A.7)
Na2HPO4+H2O ⇆ NaH2PO4+NaOH ········································ (A.8)
NaH2PO4+H2O ⇆ H3PO4+NaOH ············································ (A.9)
A.3.3.2 スケール付着抑制
りん酸塩処理を適用する産業用水管ボイラ(循環ボイラ)のボイラ水,電力事業用循環ボイラ及び電力
事業用排熱回収ボイラのボイラ水にはイオン交換水を使用することによって,海水漏えいなどを除いて硬
度成分をもち込む可能性は少ない。また,次に記載するようにりん酸塩は,塩化マグネシウムなどの酸性
塩化物に対する中和作用ももつことによって,海水漏えい時にはボイラへの注入剤として使用する。
A.3.3.3 海水漏えい時の緩衝作用
海水の成分には,塩化ナトリウムのほかに,塩化マグネシウムが0.5 %程度含まれており,海水漏えい
時に塩化マグネシウムは,式(A.10)に示すように加水分解によって揮発性の塩酸を生じる。
Mg Cl2+2 H2O → Mg(OH)2+2 HCl ········································(A.10)
この反応によって,ボイラ水のpHが下がり,腐食及び孔食の発生・成長を促進する。
りん酸塩処理の場合には,りん酸三ナトリウム(Na3PO4)の加水分解によって,主にりん酸水素二ナト
リウム(Na2HPO4)と水酸化ナトリウムとがボイラ水中に存在する。これによってNa3PO4とNa2HPO4の
解離平衡とによって,酸性成分,又はアルカリ性成分の影響を弱め,緩衝作用を示す。
44
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
Na2HPO4+HCl → NaH2PO4+NaCl ········································· (A.11)
このように,りん酸塩処理の場合には,海水漏えい時の塩化マグネシウムの加水分解によって生じたHCl
とNa2HPO4が反応するため,ボイラ水中のNaOHの濃度変化は少ない。
A.3.4 管理項目
りん酸塩処理は,産業用水管ボイラのイオン交換水を使用する場合のボイラ水,電力事業用循環ボイラ
のボイラ水及び電力事業用排熱回収ボイラのボイラ水に適用する(A.3.1を参照)。各々のボイラ水の管理
項目は,次のとおりである。
a) 産業用水管ボイラのイオン交換水を使用する場合のボイラ水 管理項目は,pH,酸消費量,電気伝導
率,塩化物イオン,りん酸イオン,亜硫酸イオン又はヒドラジン,及びシリカの7項目である。pHに
ついては,次のとおりである。
りん酸塩処理は,りん酸三ナトリウムを用い,ボイラ水中のNa/PO4のモル比を3.0以下に調節して
管理する水処理で,ボイラ水のpHは,りん酸イオンの濃度と必然的にある関係をもつ。この関係に
ついてMarcyらの実績値を図A.10に示す[9]。しかし,実際のボイラ水中には,給水のpHを調節する
ためにアンモニアなどの揮発性物質が共存している。そのため,ボイラ水中には,分配(気相/液相)
係数に応じた量の揮発性物質が存在し,ボイラのpH上昇に寄与している。アンモニアの分配係数は,
図A.22に示すように,例えば,15 MPaでは約2.5,7.5 MPaでは約4である。ボイラ水中のアンモニ
ア濃度は,ボイラの起動後に経時的に上昇し,通常は数時間程度で定常状態となる。実ボイラのボイ
ラ水中のアンモニア濃度は,プラントの運転条件を考慮して計算すると,おおむね給水中濃度/分配
係数となる[10]。給水のpHをアンモニアで調整している系において25 ℃におけるpHが10.3(アンモ
ニア濃度NH3: 43 mg/L)とすると,15 MPaのボイラ水中のアンモニア濃度はNH3: 17.3 mg/L(pH=10.1),
7.5 MPaのボイラ水中のアンモニア濃度はNH3: 10.8 mg/L(pH=10.0)となる。また,給水の25 ℃に
おけるpHが9.4(アンモニア濃度NH3: 1.05 mg/L)のときは,15 MPaのボイラ水中のアンモニア濃度
はNH3: 0.42 mg/L(pH=9.1),7.5 MPaのボイラ水中のアンモニア濃度はNH3: 0.26 mg/L(pH=9.0)と
なる。同様に,給水の25 ℃におけるpHが9.0(アンモニア濃度NH3: 0.26 mg/L)のときは,15 MPa
のボイラ水中のアンモニア濃度はNH3: 0.10 mg/L(pH=8.7),7.5 MPaのボイラ水中のアンモニア濃度
はNH3: 0.07 mg/L(pH=8.5)となる。ただし,これらは確実に気液が分離している実験系においてで
あり,実ボイラにおいては蒸気ドラム内のサンプリングポイント周囲では蒸気とボイラ水との混合が
あるため,ボイラ水中に高いアンモニア濃度を検出して,見かけの分配係数は小さな値となる場合が
ある。
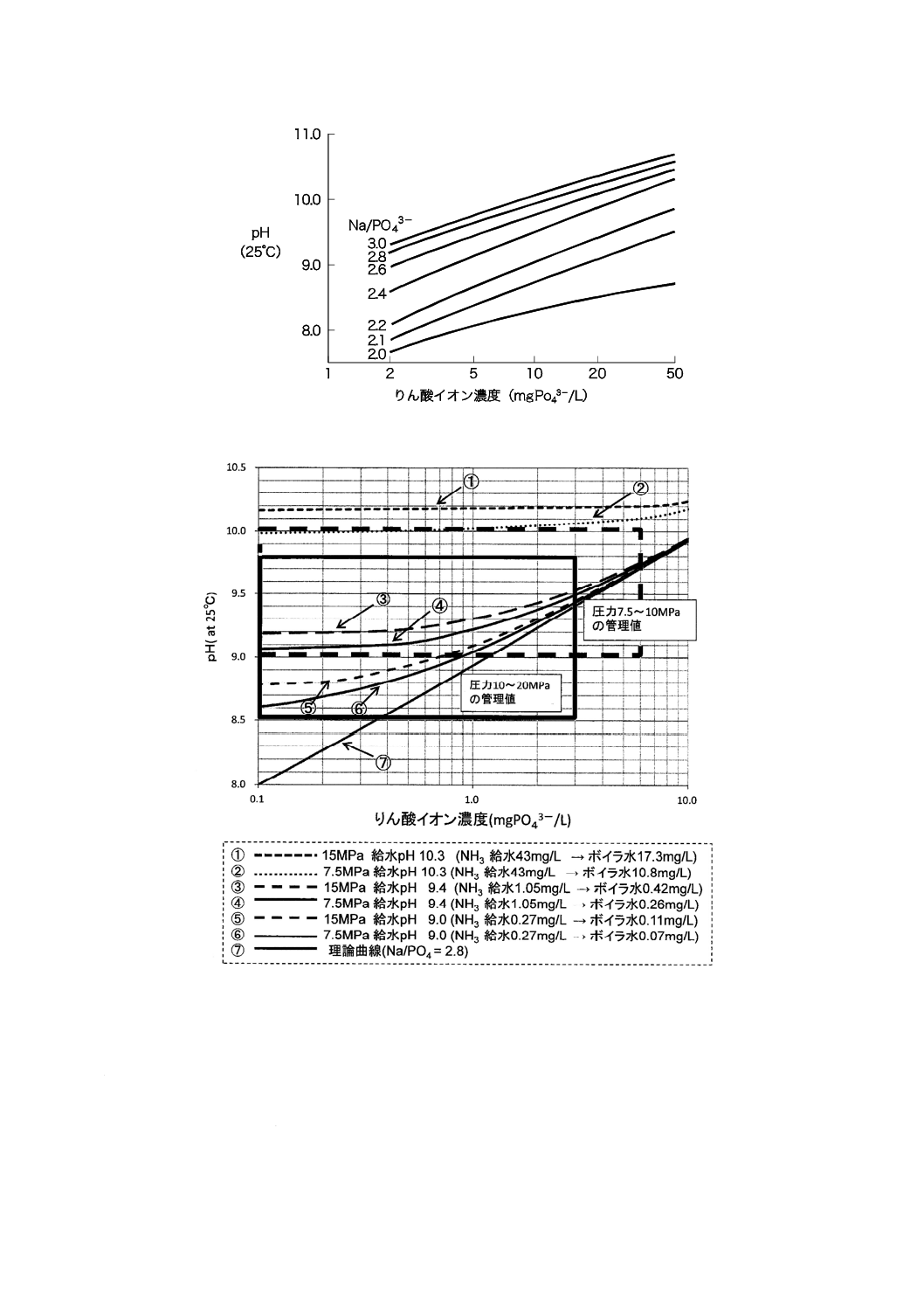
図A.11は,上記の条件でアンモニア共存時のボイラ水中の25 ℃におけるpHとりん酸イオン濃度
(Na/PO4モル比)との関係を示したものであり,ボイラ水中のりん酸イオン濃度が数mg/L以下の場
合は,ボイラ水のpHには,給水中のアンモニア濃度が大きく影響する。したがって,おおむね,7.5 MPa
を超えるボイラ水のpHは,給水中にボイラ水のpHを低下させるような因子が少ない場合は,りん酸
イオンの濃度を数mg/L以下に抑制してアンモニアなどの揮発性物質だけで調整可能となる。
45
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
図A.10−Na/PO4モル比が2.0〜3.0のオルトりん酸ナトリウム溶液の濃度とpHとの関係[9]
図A.11−アンモニア共存時のPO43−濃度とpHとの関係
b) 電力事業用循環ボイラのボイラ水 管理項目は,pH,電気伝導率,塩化物イオン,りん酸イオン,及
びシリカの5項目である。
c) 電力事業用排熱回収ボイラのボイラ水 管理項目は,pH,酸消費量,電気伝導率,塩化物イオン,り
ん酸イオン,亜硫酸イオン又はヒドラジン,及びシリカの7項目である。pH,電気伝導率及びりん酸
イオンについては,次のとおりである。
1) pH 電力事業用排熱回収ボイラは,一般的に,起動・停止の回数が多く,急速起動条件の運用を要
46
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
求するため,停止時及び起動時の防食を考慮し,ボイラ水のpH及びりん酸イオンの濃度を同圧力
区分の水管ボイラの規定より高めに保持すること,更に蒸発管伝熱面の熱負荷が低く定常運転時の
りん酸イオンのハイドアウトが少ないことなどを勘案し,15 MPa以下の圧力区分においては管理値
の上限を表9の産業用水管ボイラの水質に比較し高めている。
2) 電気伝導率 1) のようにpHは産業用水管ボイラの管理値より高めに規定している。このため,ボ
イラ水の電気伝導率も表9の産業用水管ボイラの管理値より高くなるが,その値は,Na/PO4モル比
2.5及び2.8におけるりん酸濃度,pH及び電気伝導率の理論計算から,pHの上限値に対応する電気
伝導率として,圧力10 MPa以下については40 mS/m以下に,10 MPaを超え15 MPa以下では15 mS/m
以下となる。
3) りん酸イオン 15 MPa以下の圧力区分におけるりん酸イオンの濃度は規格化しないで,表13の注 a)
〜注c)に示すようにボイラ水のpHを維持できるように濃度を調整する。例えば,Na/PO4のモル比
を2.6とするとき,pH 9.8〜10.7に相当するりん酸イオン濃度は約PO4: 5〜70 mg/Lとなる。また,
比較的りん酸塩のハイドアウトを懸念する15 MPaを超え20 MPa以下の高圧圧力区分では,過剰の
りん酸塩の注入を防止することを考慮すると,同圧力区分の水管ボイラの水質に準拠し,PO4: 3
mg/L以下となる。
A.3.5 留意事項
A.3.5.1 ハイドアウト(hide out)現象
りん酸ナトリウムの溶解度は,図A.12に示すように120 ℃以上の高温域では温度上昇とともに減少し[11],
固相を形成しやすくなり,ボイラ内で生じるりん酸塩のハイドアウト現象(ボイラ水中のりん酸イオン濃
度が,高負荷時には,管壁への析出によって注入濃度より減少し,一方,低負荷時には再溶解するために
濃度が上昇する現象)の原因となる。高温下で,りん酸塩が析出する際には,常温の場合と異なって,液
相と固相との組成は必ずしも一致せず,複雑な相平衡状態となることが知られている。
りん酸ナトリウムのpH−PO4曲線は,図A.13に示すように,高pH側は,遊離アルカリの存在領域であ
り,りん酸ナトリウム及び水酸化ナトリウムの共存領域である。遊離アルカリ抑制上,この曲線より下側
のpH領域にボイラ水を保持するのが,1942年,Whirl及びPurcellが提唱したコーディネイト(Coordinated)
処理である[12]。
その後,Ravitchなどが最初に見いだしたように,高温のりん酸ナトリウム溶液(Na/PO4=3.0)中で固
相を形成すると,液相側のNa/PO4比は3.0より大きくなり,一方固相側のモル比は3.0より小さくなる。
すなわち,溶液側に遊離アルカリを形成する。図A.14に,固・液平衡状態における,液相及び固相のNa/PO4
モル比を示す[13]。固相と液相との組成が一致する点(コングルエント点)は,243〜300 ℃ではモル比2.1
及び2.8近傍に存在する。したがって,りん酸塩の析出に伴う遊離アルカリの形成を抑制するには,溶液
のNa/PO4モル比を2.8より小さく保持する。このように,アルカリ抑制の観点からモル比を制御するりん
酸塩処理は,コングルエント(Congruent)処理と呼び,従来のコーディネイト(Coordinated)処理を一層
見直したものである。
我が国の高圧ボイラでは,りん酸イオンの濃度を数mg/Lと低めにしてpHを弱アルカリ性に保持し,ア
ルカリ腐食を極力抑制する方法を採用する。この方法を,“低りん酸塩処理”という。
低りん酸塩処理においてもハイドアウト現象は生じるが,国内のプラントでは,水壁管自体の大きな腐
食障害を経験しておらず,低りん酸塩処理における,りん酸塩析出に起因する遊離アルカリの形成は,水
壁管の腐食の程度に対して,あまり影響を与えないという見方もできる。
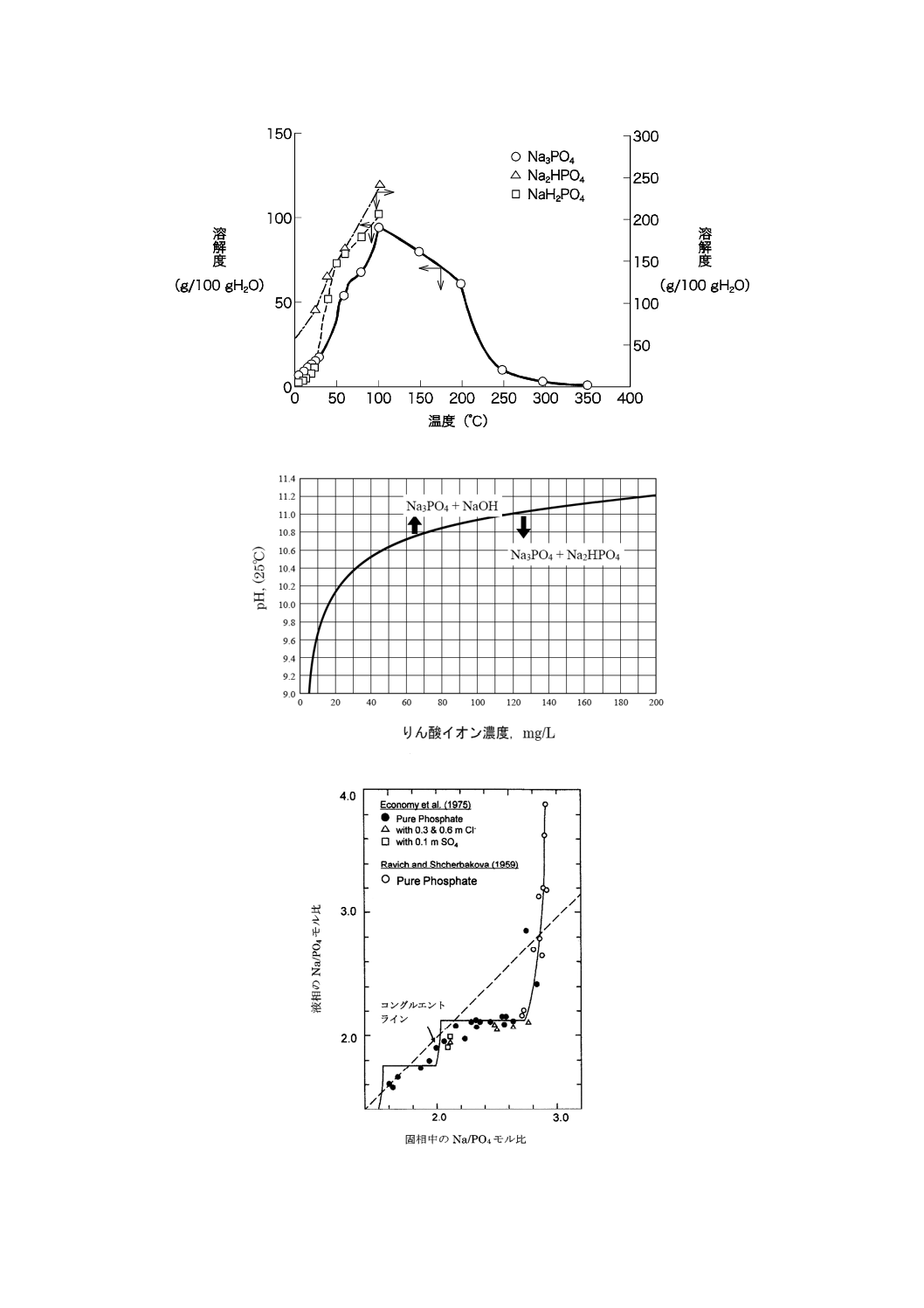
47
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
図A.12−りん酸ナトリウムの溶解度[11]
図A.13−コーディネイトりん酸塩−pH曲線[12]
図A.14−固相及び液相間におけるNa/PO4モル比の関係(243〜300 ℃)[13]

48
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
A.3.5.2 キャリオーバ
りん酸塩処理の場合,りん酸ナトリウムの一部は蒸気に溶解し,移行する。ボイラ水中のりん酸水素二
ナトリウム(Na2HPO4)と蒸気中のNa2HPO4との関係を図A.15,ボイラ水中のりん酸三ナトリウム(Na3PO4)
と蒸気中のNa3PO4との関係を図A.16に示す。亜臨界圧ボイラの温度及び圧力条件の場合,Na2HPO4及び
Na3PO4気液分配係数(蒸気中の物質の濃度/液相中の物質の濃度)は10−2〜10−3とごく小さく,蒸気中の
りん酸ナトリウム濃度は1 μg/L〜0.1 μg/Lと無視できる程度である[14]。このため,通常の低りん酸塩処理
の場合,ドラム内の汽水分離器が,飛まつ(沫)同伴が起こらないように正常に機能していれば,りん酸
ナトリウムのキャリオーバは,実質上,起こっていないとみることができる。逆に,タービンにりん酸ナ
トリウムの析出が起こるような場合には,汽水分離器の性能などを確認する必要がある。
図A.15−ボイラ水中のNa2HPO4の蒸気中への
キャリオーバ[14]
図A.16−ボイラ水中のNa3PO4の蒸気中への
キャリオーバ[14]
A.4 揮発性物質処理
A.4.1 適用ボイラ
揮発性物質処理は,産業用・事業用水管ボイラの給水及びボイラ水,電力事業用排熱回収ボイラの給水
及びボイラ水,並びに貫流ボイラの給水など,主に高圧ボイラに適用する。
A.4.2 処理方法
A.4.2.1 共通事項
揮発性物質処理は,アルカリ腐食の懸念がないうえに,ボイラ水の全蒸発残留物の濃度を可能な限り低
く抑えるので,蒸気純度の向上を図れる。揮発性物質処理のうち,ヒドラジンなどの脱酸素剤を用いる水
処理方法をAVT(R)という。
脱酸素剤を使用せず,極微量の酸素(O: 5 μg/L未満)の存在を許容する水処理方法をAVT(LO)という。
極めて低い酸化性環境であるが,pHが高く(pH 9.2以上)なるとO: 5 μg/L未満の溶存酸素濃度下でも酸
化環境となる[15]。我が国の火力発電プラントで,ヒドラジン注入を取りやめた場合,諸外国の復水器,脱
気器等の性能の相違によって,このような水質環境状態になる傾向にある。
AVT(LO)同様に脱酸素剤を使用せず,微量の酸素(O: 5 μg/L以上20 μg/L未満)の存在を積極的に許容
49
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
し,酸化性環境を保つ水処理方法をAVT(O)という。諸外国の火力発電プラントで,ヒドラジン注入を取
りやめた場合,このような水質環境状態になる傾向にあるという報告が多い。
A.4.2.2 水質調整剤
揮発性物質処理は,pH調整剤として,アンモニア又はアミン類を給水に注入するのが一般的である。
AVT(R)の場合,脱酸素剤としてヒドラジン(ヒドラジン一水和物)を用いる場合が多く,アンモニア同
様,給水に注入している。ヒドラジンをpH調整剤として用いる場合もあるが,高温下では分解してアン
モニアを生成し,pH調整にも寄与する。
なお,AVT(LO)及びAVT(O)については,脱酸素剤の注入を行っていない。
A.4.2.3 水質調整
水管ボイラの場合,pH調整剤・脱酸素剤は,給水入口点(復水ポンプ出口など)で注入して,給水系統
の水質を制御する。図A.17に示すように,各pH調整剤濃度と電気伝導率との相関から,濃度制御する。
0.01
0.1
1
10
100
0.1
1
10
100
1000
濃 度 (mg/L)
電
気
伝
導
率
(m
S/
m
)
モルホリン(pKb=2.09×10-6,λ∞=47(mS・m2/mol))
アンモニア(pKb=1.76×10-5,λ∞=73.5(mS・m2/mol))
2−アミノエタノール(pKb=2.60×10-5,λ∞=42.2(mS・m2/mol))
シクロヘキシルアミン(pKb=3.39×10-4,λ∞=40(mS・m2/mol))
図A.17−各pH調整剤濃度と電気伝導率との関係
溶存酸素は,脱気器などによって脱気されるとともに,脱酸素剤によって消費される。ボイラ水は,一
般的には給水をそのまま補給しており,その水質の影響を受ける。
電力事業用排熱回収ボイラの場合,溶存酸素は復水器にて脱気する。その後,給水入口点(低圧給水ポ
ンプ出口など)でpH調整剤・脱酸素剤が注入され,給水系統の水質を制御する。ボイラ水は給水をその
まま補給することになるが,ほとんどのプラントはりん酸処理を行っている。
貫流ボイラの場合,給水入口点付近に復水脱塩装置を設置し,給水中の不純物を極力除去する。pH調整
剤・脱酸素剤を,復水脱塩装置出口に注入し,給水系統の水質を制御する。水管ボイラ同様,溶存酸素は
脱気器にて脱気し,脱酸素剤によって更に消費される。
なお,AVT(LO)及びAVT(O)については,脱酸素剤の注入を行っていない。
A.4.3 処理の原理
A.4.3.1 AVT(R)
AVT(R)処理法は,給水及びボイラ水のpHをpH調整剤を用いて,鉄系材料の酸化物であるマグネタイ
ト(Fe3O4)の溶解度が小さくなるpH 8.5〜10.3程度のアルカリ性に保持するとともに,ヒドラジンなどの
脱酸素剤を用いて溶存酸素を化学的に除去し,還元雰囲気中で腐食の抑制を図る。
ただし,系統に銅系材料を使用している場合,アンモニアによる腐食影響を考慮して,銅材使用範囲に
合わせてpH上限値を設定する。
pKb 塩基解離定数
λ∞ 極限モル伝導率
50
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
A.4.3.2 AVT(LO)・AVT(O)
AVT(LO)及びAVT(O)処理法は,給水及びボイラ水のpHをpH調整剤を用いて,鉄系材料の酸化物であ
るマグネタイトの溶解度が小さくなるpH 8.5〜10.3程度のアルカリ性に保持する点はAVT(R)と同様であ
る。しかし,AVT(LO)及びAVT(O)処理法は,AVT(R)と異なり,ヒドラジンなどの脱酸素剤を使用しない
場合であっても,溶存酸素濃度を低く保持できる水処理法であり,電力事業用循環ボイラ,電力事業用排
熱回収ボイラ,及び貫流ボイラに適用する。
AVT(LO)の場合,給水中の溶存酸素がO: 5 μg/L未満の低酸化性の水質条件であり,図A.18及び図A.19
に示すように溶存酸素濃度がO: 0 μg/LからO: 5 μg/Lへと増加するに伴い腐食電位は上昇する[16], [17]。図
A.18に示すpH 9.0のAVT(LO)条件下では,O: 2 μg/Lでは,腐食電位は若干上昇するがヘマタイト(Fe2O3)
皮膜は生成しない。しかし,O: 5 μg/LになるとFe2O3皮膜が生成し[16],O: 5 μg/L未満の溶存酸素濃度でも
Fe2O3皮膜を形成する可能性があることを示唆する。図A.19では,pH 9.2のAVT(LO)条件下では,溶存酸
素濃度O: 2 μg/L以上になるとFe2O3皮膜が生成し,それに伴うFACによる腐食抑制効果の報告もあり,
AVT(LO)水質条件下の腐食抑制効果は,AVT(R)と同等ないし優位であると評価できる[17]。同報告によると,
pHが上昇すると,極微量の溶存酸素でもFe2O3皮膜が生成するようになるという記載がある[15], [17]。
我が国の火力発電プラントで,ヒドラジン注入を取りやめた多くの場合で,諸外国との復水器,脱気器
などの性能の相違によって,給水中の溶存酸素がO: 5 μg/L未満のこのような水質環境になるという報告が
ある。
一方,AVT(O)の場合は,水処理方法はAVT(LO)と同様であるが,酸電気伝導率を酸素処理並みに抑制で
きていることを条件に,給水中の溶存酸素をO: 5〜20 μg/Lと微量の存在を積極的に許容し,酸化雰囲気の
中で腐食を抑制する方法である。
AVT(O)の場合,給水中の溶存酸素はO: 5〜20 μg/L未満の酸化性の水質条件であり,図A.18及び図A.19
に示すようにFe2O3皮膜を生成する。また,図A.20は貫流ボイラへのAVT(O)適用の海外事例であり,脱
酸素剤であるカルボヒドラジドの注入条件から無注入条件へと変換した前後の鉄イオン,溶存酸素濃度の
変化を示す。カルボヒドラジドを無注入とすることによって溶存酸素濃度が4.7 ppb(O: 4.7 μg/L)から6.5
ppbへと増大し,一方,鉄イオン濃度は5.3 ppbから1.2 ppbへと減少する[18]。カルボヒドラジド注入を停
止すると,溶存酸素の濃度が微量増加し,酸化雰囲気となり,そのため,鉄の溶出を抑制できたことを示
す。
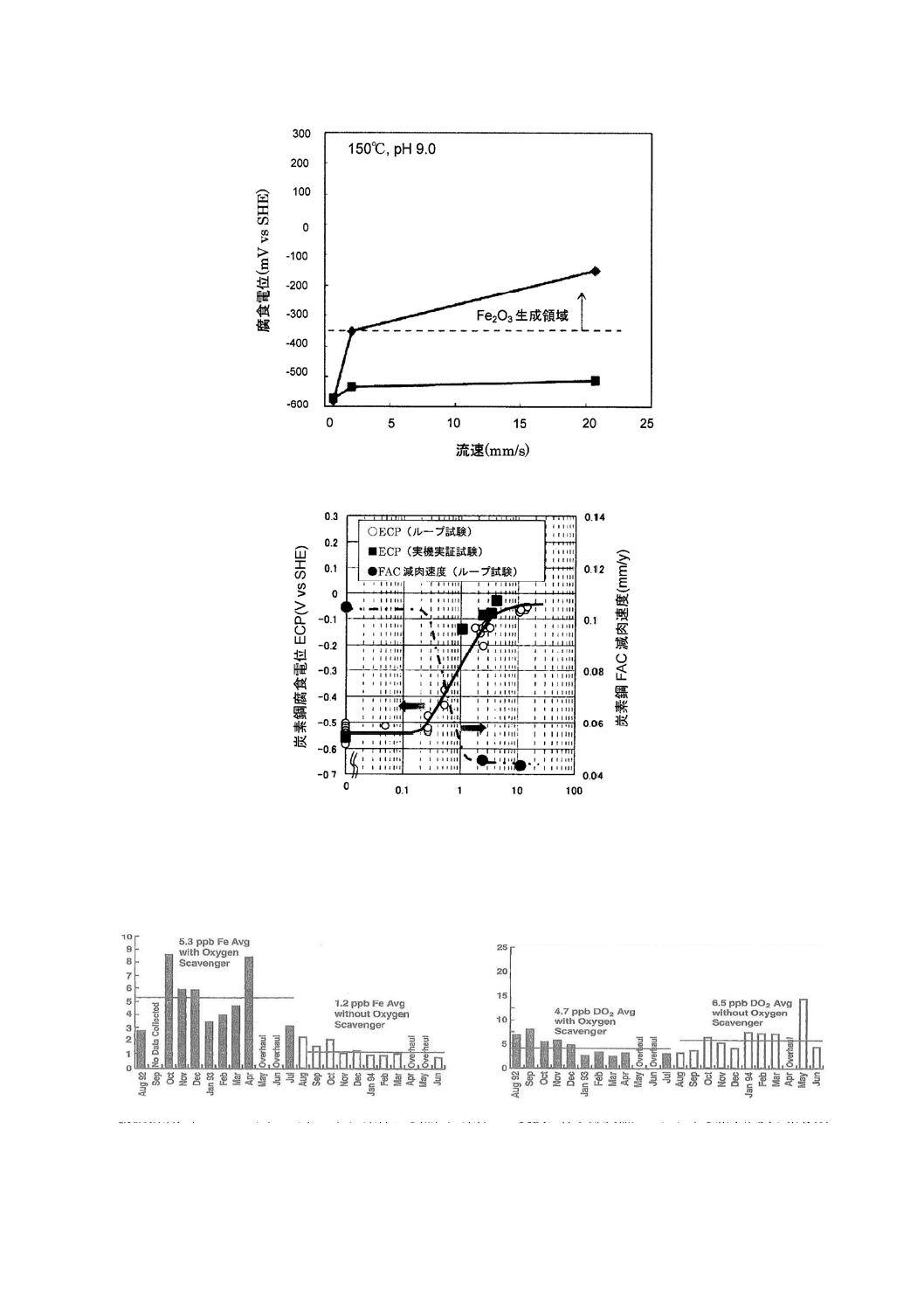
51
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
図A.18−炭素鋼の腐食電位と流速の関係[16]
溶存酸素濃度(μg/L)
図A.19−炭素鋼の腐食電位に及ぼす溶存酸素の影響[17]
(試験温度:180 ℃,pH:9.2,流速:5 m/s)
μ
g
/L
F
e
(M
o
nt
hl
y
A
v
g
)
μ
g
/L
D
O
2
(
M
o
nt
h
ly
A
v
g)
[脱酸素剤(カルボヒドラジド)の注入条件から無注入条件への変換に伴う節炭器入口における給水鉄及び溶存酸
素濃度の変化(700 MW貫流ボイラ,全鉄給水系システム)]
図A.20−海外火力発電プラントにおけるAVT(O)適用に伴う鉄濃度の低減例[18]
脱酸素剤注入条件時の
平均鉄濃度 5.3 μg/L
脱酸素剤無注入条件時の
平均鉄濃度 1.2 μg/L
脱酸素剤無注入条件時の
平均酸素濃度 6.5 μg/L
脱酸素剤注入条件時の
平均酸素鉄濃度 4.7 μg/L
溶存酸素 O: 5 μg/L
溶存酸素 O: 2 μg/L
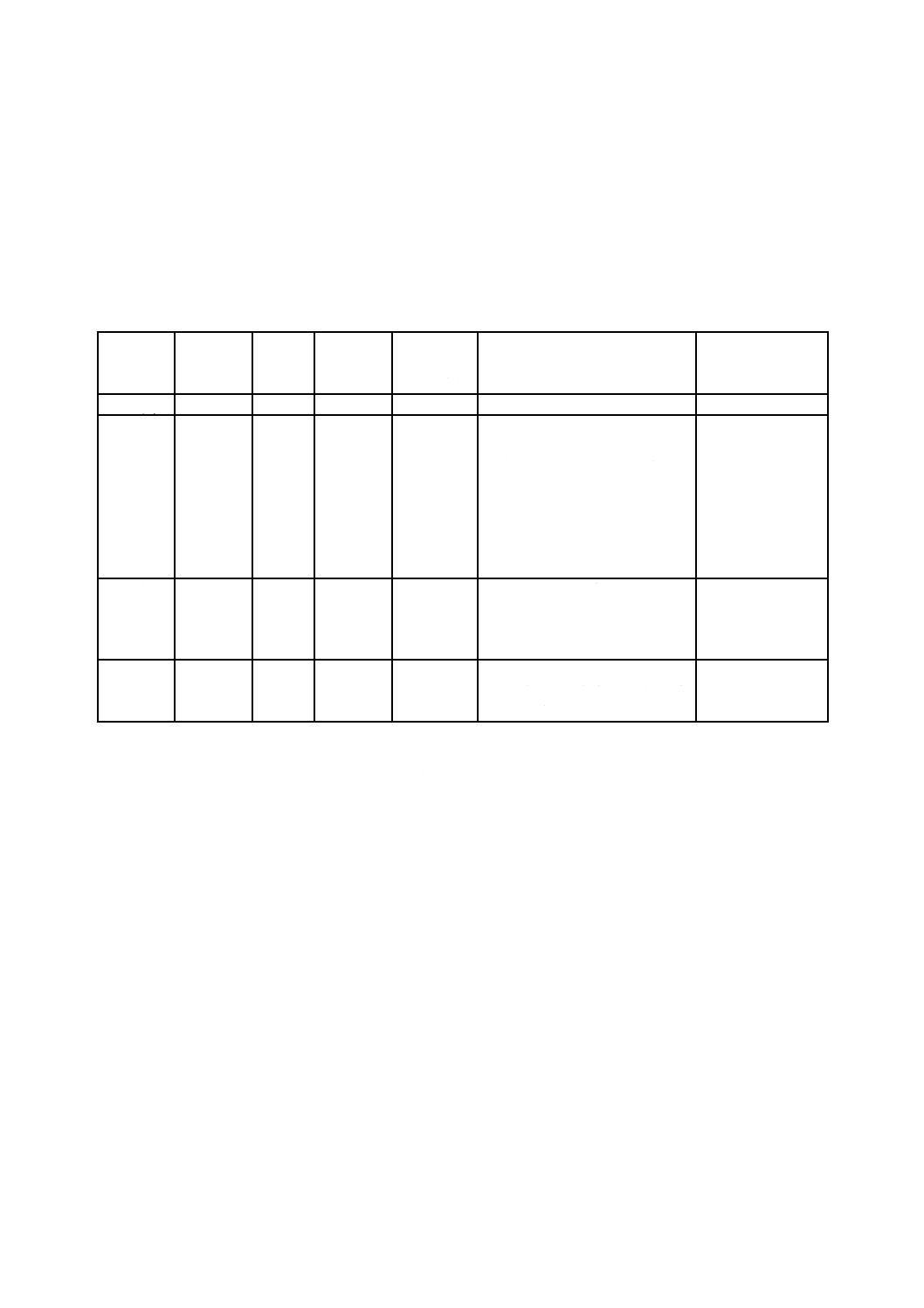
52
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
AVT(O)の方が,AVT(LO)と比較してFe2O3皮膜を確実に形成することよって,腐食抑制効果に関して優
位性があると考えられる。
諸外国の火力発電プラントで,ヒドラジン注入を取りやめた多くの場合で,我が国との復水器,脱気器
などの性能の相違によって,給水中の溶存酸素がO: 5 μg/L以上のこのような水質環境になるという報告が
ある。
AVT(R),AVT(LO),AVT(O)及び酸素処理(OT)について取りまとめた結果を,表A.1に示す。
表A.1−AVT(R),AVT(LO),AVT(O)及び酸素処理(OT)の比較
水処理
水質環境
還元剤
溶存酸素
μg/L
pH
(貫流ボイ
ラの場合)
鉄酸化物形態
補足説明
AVT(R)
還元性
使用
7以下
8.5〜10.0
Fe3O4
−
AVT(LO)
低酸化性
不使用
5未満
8.5〜10.0
pH値及び溶存酸素濃度が低いと
Fe3O4皮膜だけが形成する場合
が多い。pH値及び溶存濃度が高
くなるとFe3O4皮膜の上に極め
て薄いFe2O3皮膜が形成する。一
般にpH値が高くなるに従い,少
量の溶存酸素濃度でもFe2O3皮
膜が形成する傾向にある。
我が国でヒドラジ
ン注入を止めた場
合,このような水
質状態になる。
AVT(O)
酸化性
不使用 5〜20未満
8.5〜10.0
Fe3O4皮膜の上に薄いFe2O3皮膜
が形成する。
諸外国でヒドラジ
ン注入を止めた場
合,このような水
質状態になる。
参考
OT
酸化性
不使用
20〜200
8.0〜10.0
給水・ボイラ系統全体において,
Fe3O4皮膜上に安定でち(緻)密
なFe2O3皮膜が覆う。
酸素注入制御設備
が必要である。
A.4.4 管理項目
A.4.4.1 水管ボイラ及び電力事業用排熱回収ボイラの給水
水管ボイラ及び電力事業用排熱回収ボイラの給水の場合,次のpH,酸電気伝導率,溶存酸素,鉄,銅及
びヒドラジンの6項目が管理項目である。また,産業用循環ボイラだけ,硬度,油脂類を設定する。
a) pH pHの調整は,系統を構成する材料の腐食を抑制するために行うものであり,管理値の設定に対
する基本的な考え方はアルカリ処理の場合と同じで,給水pH 8.5〜10.3を管理値とするが,これは給
水加熱器の管材が鋼管・銅合金管の両者の場合を包括して表した範囲であり,実際のpH管理に当たっ
ては,系統内の材質,温度,圧力などの使用条件を考慮し,防食に適する範囲に設定する必要がある。
各pH調整剤濃度とpHとの関係は,図A.21のとおりである。薬剤の注入濃度は電気伝導率で制御
し,濃度相当のpH値を管理目標として設定する。
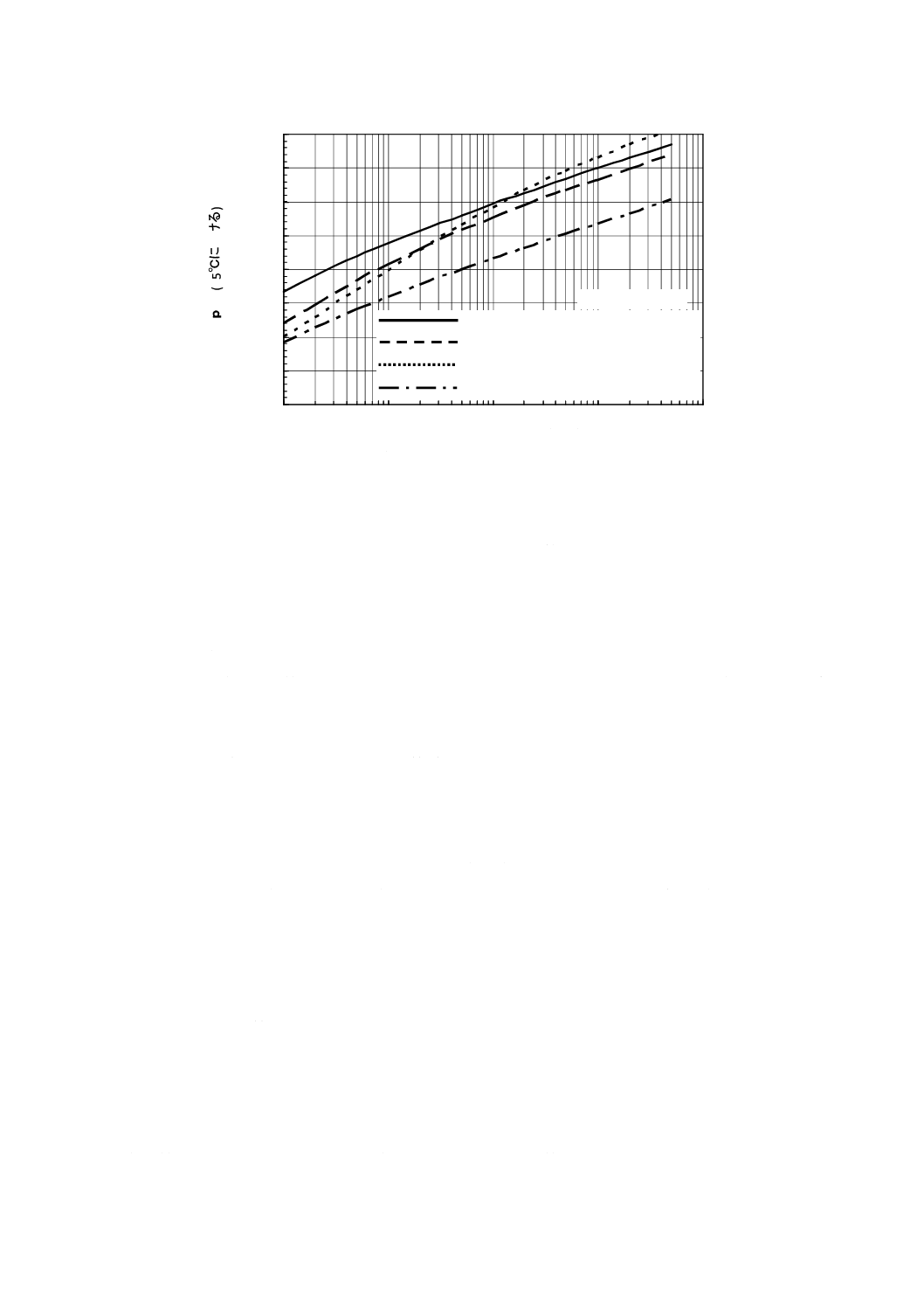
53
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
7.0
7.5
8.0
8.5
9.0
9.5
10.0
10.5
11.0
0.1
1
10
100
1000
濃 度 (mg/L)
p
H
(2
5
℃
に
お
け
る
)
モルホリン(pKb=2.09×10-6)
アンモニア(pKb=1.76×10-5)
2−アミノエタノール(pKb=2.60×10-5)
シクロヘキシルアミン(pKb=3.39×10-4)
図A.21−各pH調整剤濃度とpHとの関係
b) 酸電気伝導率 10 MPa以上の水管ボイラでは,蒸気純度の確保又はスケール生成防止のため,ボイラ
水の全蒸発残留物をできるだけ低く抑える必要があり,この大部分が給水の電解質成分に由来するこ
とから,給水中のpH調整剤の影響を除いた酸電気伝導率で管理する。
AVT(R)及びAVT(LO)では0.05 mS/m以下とするが,AVT(O)では溶存酸素の影響を考慮して0.02
mS/m以下と厳しく管理する。
なお,測定については,水素イオン形の強酸性陽イオン交換樹脂層を通過後の電気伝導率を測定し,
給水中に存在する微量の電解質を指標とする。
c) 溶存酸素 溶存酸素の管理値は,系統を構成する材料の防食を目的として定める。溶存酸素による腐
食は,局部的に進行する孔食の形態で発生することが多く,また,給水の溶存酸素は定常運転時にお
いて,給水の鉄・銅の溶出を高める原因となることから,できるだけ低く抑えて管理する。
AVT(R)の場合,2 MPa以下の産業用水管ボイラは,脱気器を設置しないものは酸素を“低く保つ”
こととなるが,脱気器を設置する場合はO: 500 μg/L以下とする。また,5 MPa以上の産業用・電力事
業用循環ボイラ,及び電力事業用排熱回収ボイラでは,脱気器性能に基づいてO: 7 μg/L以下とする。
AVT(LO)及びAVT(O)の場合,対象は電力事業用循環ボイラ,及び電力事業用排熱回収ボイラとなる
が,O: 5 μg/L未満を低酸化形,O: 5〜20 μg/Lを酸化形として,O: 5 μg/Lを境界に区分する。
d) 鉄・銅 給水の鉄・銅は,ボイラの伝熱面にその大部分がスケールとして付着し,伝熱抵抗となり,
熱効率の低下とともに,管壁温度を高めて高温腐食及び膨出噴破の原因となる。また,銅の蒸気に対
する溶解度は,蒸気の比体積の減少,すなわち,圧力の上昇とともに大きくなることから,ボイラに
もち込む銅は,蒸気に溶解してタービン側に移行し,スケール化する問題がある。特に,高圧になる
ほどスケールの堆積による水壁管過熱の影響が強くなる。
このことから,管理値は高圧になるほど低くなっており,15 MPaを超え20 MPa以下の電力事業用
循環ボイラ及び電力事業用排熱回収ボイラでは,Fe: 20 μg/L以下とする。また,AVT(O)の場合は,OT
レベルでの管理が必要である。
給水の鉄・銅は,復水・給水系統の機器,配管から腐食によって溶出したものであり,鉄分の溶出
は主として低いpHと溶存酸素,また,銅の溶出は高いpHと溶存酸素とが促進することから,鉄及び
銅の管理値を維持するためには,溶存酸素及びpHを適正に管理する。
pKb 塩基解離定数
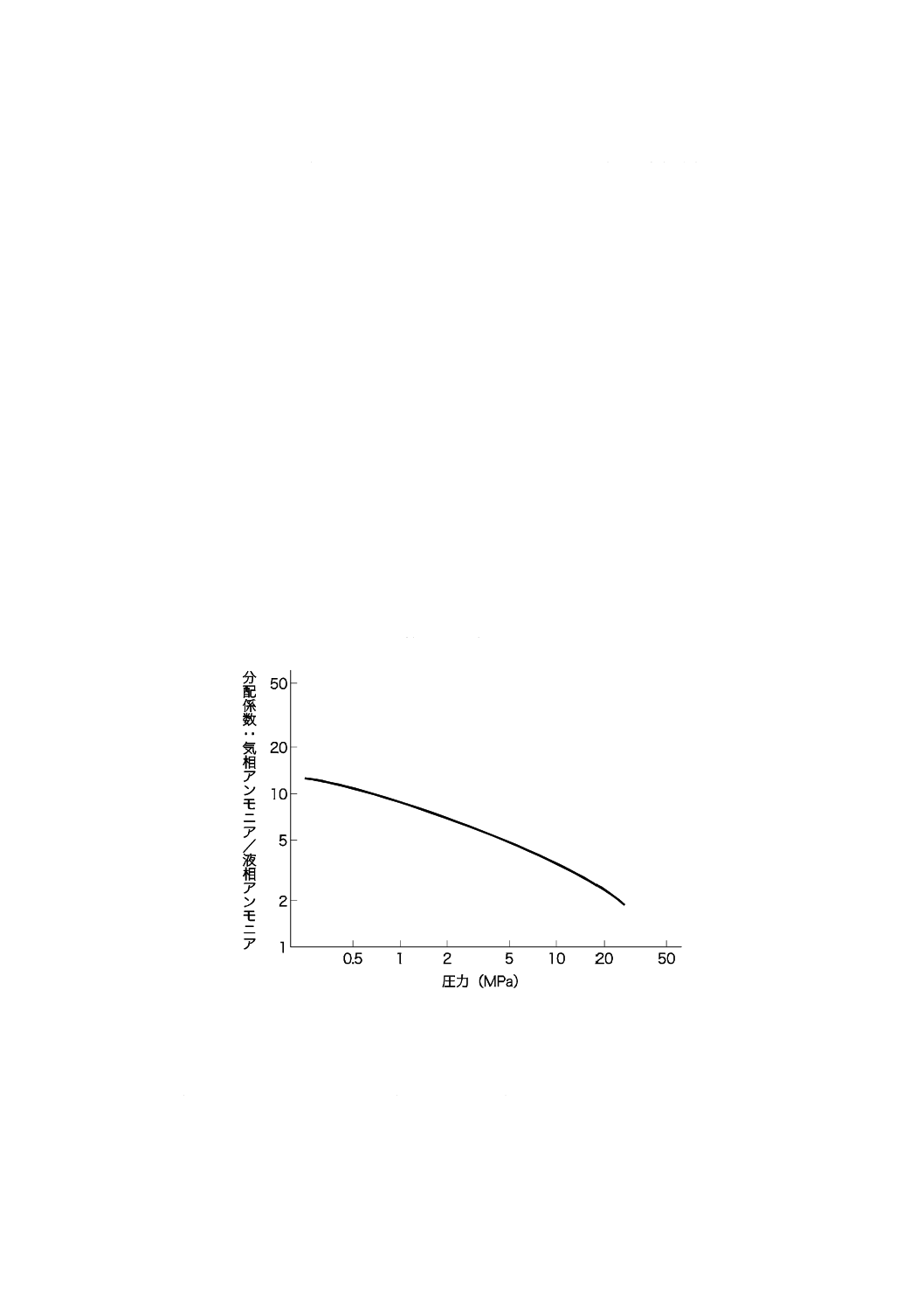
54
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
e) ヒドラジン ヒドラジンは,AVT(R)の場合に主として溶存酸素による腐食を抑制するために注入す
る。系統水中でのヒドラジンの挙動はB.8に示すとおりで,ヒドラジンと溶存酸素との直接反応は遅
いが,復水・給水系統の酸化鉄及び酸化銅が触媒的な役割をするので,復水系統にヒドラジンを注入
すると溶存酸素の除去の効果は十分に期待できる。
管理値は,5 MPa以下の産業用水管ボイラでは,溶存酸素の2倍となるように設定し,5 MPaを超
えるボイラでは,溶存酸素がO: 7 μg/L以下と設定するため,N2H4: 10 μg/L以上残留するように設定す
る。
f)
硬度 給水の硬度は,ボイラ伝熱面に硬度成分が起因するスケールを付着させ,また,スラッジ生成
の原因になる。硬度成分が給水に混入するのは,復水器などの冷却水の漏えい,送気先の被加熱源で
の回収復水への漏えい・汚染を除けば,イオン交換処理装置の不調などによる補給水の水質の低下が
主因である。
A.4.4.2 水管ボイラ及び電力事業用排熱回収ボイラのボイラ水
5 MPa以上の産業用・事業用水管ボイラ及び電力事業用排熱回収ボイラで設定しており,次のpH,酸電
気伝導率,塩化物イオン及びシリカの4項目が管理項目である。
a) pH 水管ボイラの場合,揮発性物質処理によるボイラ水のpHは,給水経由でボイラに流入し,ボイ
ラ水中に残留するアンモニウムイオンなどの揮発性塩基だけによって保たれる。ボイラにもち込まれ
たアンモニアは,ボイラ水中の濃度と蒸気中の濃度とが同一でなく,図A.22に示すように温度・圧力
によってある分配係数をもち,ボイラ水中の濃度が若干低い値となる[19]。しかし,給水とボイラ水と
のpHの差は,ボイラの運転条件その他の影響を受けて一定でないので,ボイラ水のpHは給水のpH
とほぼ同じ,pH 8.5〜10.0を目標にして管理すればよい。
図A.22−アンモニアの分配係数と圧力との関係[19]
電力事業用排熱回収ボイラの場合,各ボイラ水及び給水のpHは低圧ボイラ(一般的に1 MPa以下)
のpHが左右する。水管ボイラでも記載したように,低圧ボイラでの蒸気側へのアンモニア分配率が
高く,ボイラ水のpH維持が他の中圧ボイラ及び高圧ボイラに比較し困難であるため,給水のpHは低
圧ボイラ水のpHが8.5〜10.3となるように制御し,中圧ボイラ及び高圧ボイラ水のpHはそれに従っ
て変化する。
55
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
b) 酸電気伝導率 揮発性物質処理では,ボイラ水中に溶解性蒸発残留物をほとんど含まないので,直接
の電気伝導率の測定値では判定が不十分である。ボイラ水中の腐食性成分(アニオン)の濃度を高精
度で測定するために,酸電気伝導率を指標として管理する。
管理値は,10 MPa以下では6 mS/m以下で,10 MPaを超える場合は2 mS/mで管理する。
c) 塩化物イオン ボイラ水の塩化物イオンは,ボイラ水の濃縮程度を知るとともに,腐食を抑制する目
的で管理する項目である。また,塩化物イオンは復水器冷却水の漏えいの有無及び漏えいの程度を表
す指標となる。復水器の冷却水として一般に使用する海水の系統水への混入は,塩化物イオン,硫酸
イオンなどの腐食性成分を急激にもち込むため,pH低下による腐食促進,塩類によるスケールの生
成・堆積など,プラント各部に多大の障害をもたらす。
揮発性物質処理では,塩化物イオン混入の影響が他の処理と比較して大きいことから,より低く設
定しており,また,圧力が高いほど,より低く設定する。
d) シリカ A.2.4.2 g)を参照。
A.4.4.3 貫流ボイラの給水
貫流ボイラの給水では,次のpH,酸電気伝導率,溶存酸素,鉄,銅,ヒドラジン及びシリカの7項目が
管理項目である。
a) pH A.4.4.1 a)を参照。
b) 酸電気伝導率 貫流ボイラでは,給水の水質が障害の発生及び蒸気純度に直接的な影響を及ぼすので,
給水の全蒸発残留物,すなわち,その大部分である給水の電解質成分を可能な限り低く規制する必要
がある。
AVT(R)及びAVT(LO)では0.03 mS/m以下とするが,AVT(O)では溶存酸素の影響を考慮して0.02
mS/m以下と厳しく管理する。
なお,測定については,水素イオン形の強酸性陽イオン交換樹脂層を通過後の電気伝導率を測定し,
給水中に存在する微量の電解質を指標とする。
c) 溶存酸素 溶存酸素は,A.4.4.1 c)で記載したように,できるだけ低く抑えて管理する必要がある。
AVT(R)の場合,脱気器性能に基づいてO: 7 μg/L以下とし,AVT(LO)及びAVT(O)の場合,O: 5 μg/L
未満を低酸化形,O: 5〜20 μg/Lを酸化形として,O: 5 μg/Lを境界に区分する。
d) 鉄・銅 給水の鉄・銅は,A.4.4.1 d)で記載したように,ボイラの伝熱面にその大部分がスケールとし
て付着することによる高温腐食及び膨出噴破の原因となる。
特に,高圧になるほどスケールの堆積による水壁管過熱の影響が強くなるので,超臨界圧力条件で
は亜臨界圧力条件と比べて鉄は約50 %低い値とし,銅は約30 %低い値とする。
給水の鉄・銅は,復水・給水系統の機器及び/又は配管から腐食によって溶出したものであり,鉄
分の溶出は主として低いpHと溶存酸素,また,銅の溶出は高いpHと溶存酸素とが促進することから,
鉄及び銅の管理値を維持するためには溶存酸素とpHとを適正に管理する。
e) ヒドラジン ヒドラジンは,A.4.4.1 e)で記載したように,主として溶存酸素による腐食を抑制するた
めに注入する。その管理値は,エコノマイザ入口の給水に残留するように設定する。
給水中の溶存酸素をO: 7 μg/L以下と設定するため,ヒドラジンがN2H4: 10 μg/L以上残留するよう
に設定する。
f)
シリカ 水管ボイラでは,ボイラ水にシリカの濃度の上限を規定したが,貫流ボイラではセパレータ
がない場合に給水の水質が蒸気純度に直接影響を与えるので,セパレータをもつボイラと,もたない
ボイラとについて蒸気中のシリカがSiO2: 20 μg/L以下となる濃度を基にそれぞれ給水のシリカの濃度
56
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
を規定する。
A.4.5 留意事項
一般的な留意事項は,次のとおりである。
a) 海水漏えい時の対応 水管ボイラ又は排熱回収ボイラのボイラ水が揮発性物質処理の場合,ボイラ水
pHは揮発性塩基だけによって維持するので,緩衝機能がなく復水器における冷却水の漏れなどによっ
てボイラに硬度成分及びpHを低下させる成分が流入しても,ボイラ水中にはこれらの成分を無害化
できる薬剤が共存していないことになる。したがって,このような場合には,りん酸塩又は水酸化ナ
トリウムを至急注入できるような態勢が必要であり,状況によっては運転停止が必要となる。
貫流ボイラにおいては,復水脱塩装置の活用,更には漏えい防止に対する措置,場合によってはボ
イラの運転停止による対処が必要となる。
b) pH調整剤としてのアミン類使用上の留意点 アミンは復水器及びプレボイラ系統に銅系材を多く使
用する産業用ボイラで多用する。
アミンの長所は,銅に対する腐食性が低く,また,臭気が弱く薬品補充作業などでも取り扱いやす
いことから,復水器及びプレボイラ系統に銅系材を多く使用する産業用ボイラで多く使用する。また,
アミンの分配比は1以下から10以上の種類と温度条件とによって異なることから,給水に添加するこ
とで給水のpHを制御できることに加えて,ボイラ水及び蒸気にその分配比に応じた濃度で分配され
てボイラ水及び蒸気(復水)のpHも制御できる。
一方,アミンはアンモニアに比較して解離度が大きいものと小さいものとがあるが,分子量が大きいこ
とから,水のpHを同じに調整するためには,図A.21に示すように添加濃度を数倍程度多く要するものが
多い。また,アンモニアは熱的に安定であるが,アミンは運転中のボイラ水又は過熱蒸気の温度条件下で
その一部が熱分解するので,その温度条件での分解率と分解生成物(アンモニア,二酸化炭素,有機酸な
どの有機物など)の種類・濃度及び水質への影響(pH・酸電気伝導率)も考慮して使用する必要がある。
したがって,アミンを使用するに当たっては,目的の給水・蒸気復水のpHに対する添加濃度,分配比,
ボイラの常用使用圧力,飽和水温度,飽和蒸気温度,及び過熱蒸気温度による熱安定性を考慮して使い分
ける。また,アミンの種類による毒物及び劇物取締法,消防法(危険物),PRTR法などの適用法規制,蒸
気を噴霧する環境,加熱対象による蒸気中の濃度の制限などによっても使い分けする場合がある。
A.5 酸素処理
A.5.1 適用ボイラ
我が国の事業用大容量貫流ボイラヘの酸素処理の適用例としては,1990年(平成2年)8月からのA発
電所が初めてであるが[20], [21] 2014年1月現在,54ユニットにこの処理方式が適用され,良好な実績を得て
いる。
水管ボイラ(循環ボイラ)ヘの酸素処理の適用例は少ないが,貫流ボイラにおいて良好な実績を得てい
たので,10 MPa以上の水管ボイラ(循環ボイラ)に対して適用できることとした。ただし,この処理方法
の適用は,高純度な水質である必要があることから,復水脱塩装置を設置し,系統には銅合金材料を使用
しないことが望ましい。
電力事業用排熱回収ボイラヘの酸素処理の適用例はまだないが,水質・材料面の条件が整った場合には,
適用することは可能である。
A.5.2 処理方法
酸素処理(OT)は,高純度水中に微量の酸素ガスなどの酸化剤及び揮発性アルカリ薬品,又は酸素ガス
57
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
だけを復水系統(復水昇圧ポンプ出口など)及び給水系統(脱気器出口など)に注入することによって,
水中の鉄成分を2価からより溶解度の低い3価の状態に維持して水質管理を行う方式である。
この処理方式を行うことによって,①スケール成長速度抑制による化学洗浄頻度の低減,②波状スケー
ル生成抑制によるボイラ差圧上昇の低減,③アンモニア使用量抑制による環境保全の向上,④構成機器へ
のスケール付着の低減,⑤FACの低減などの利点がある。
A.5.3 処理の原理
従来の水処理方式においては,溶存酸素は最も腐食性のある水質成分とみなしていたので,溶存酸素の
濃度をできるだけ低く保持し,pH調節を行うことによって腐食を防止することを基本にしていた。しかし,
酸素処理は,高純度の水中で酸素ガス及び揮発性アルカリ薬品,又は酸素ガスだけを用いて,難溶性の腐
食生成物を鉄の表面上に均一に生成させることによって,その後の鋼の腐食及び腐食生成物の水中への放
出を抑制させることができるとの考え方に基づいたものである。
酸素処理は,現在では,アンモニアなどによってpH 8.0〜10.0程度のアルカリ性を条件とし,溶存酸素
の共存によって腐食を抑制させる水処理方法であり,複合水処理(CWT)ともいう[22], [23]。一方,高純度
水中に酸素だけを添加する水処理方法は,中性水処理(NWT)といい,1970年代から適用されてきたが[24],
不純物に対するpH緩衝作用が乏しいこと,ドレン系の腐食抑制対策を要することなどから,世界的に見
て適用実績が少なく,アルカリ薬品が使用できないなどの条件下で使用する方法である[23]。
なお,ドレン系統の鉄の溶出制御に特化した対策としては,ドレン系へのアンモニア注入,低合金鋼又
はステンレス鋼の採用なども考えられる。
これらの処理方式及び揮発性物質処理(AVT)における鉄の電位−pH図を図A.23 [25]に示す。図A.23
から,AVTの条件では,鉄の安定な酸化物はマグネタイト(Fe3O4)であり,酸素処理の条件ではヘマタ
イト(Fe2O3)が安定であることが分かる。これらが腐食生成物として鉄の表面上に皮膜として保持するこ
とによって腐食抑制作用を得る。一方,鉄(III)イオンの溶解度は,図A.24 [26]に示すように,鉄(II)イ
オンより10桁程度低く無視できる程度である。
水の純度が低い場合には,良好な保護皮膜を形成しにくくなるので,この処理の場合は,特に電気伝導
率の厳しい管理が必要となる。また,溶存酸素による鉄の保護皮膜の形成には,流動条件が必須となる。
この限界流速については,25 ℃の高純度水(空気飽和水)の場合には,0.1 cm/s以上の流速で不動態化し
たという報告がある[27]。このことから,酸素処理条件下で腐食抑制効果を維持するためには,最低,数cm/s
程度の比較的低い流動条件を与えればよいと考えられる。
銅合金に対しては,酸素の共存条件において生成する酸化銅(II)(CuO)の皮膜の溶解度は,脱気条件
における酸化銅(I)(Cu2O)の皮膜の溶解度より一般的に高いため,酸素の共存は好ましくない。この場
合には,pHを8.5〜9.0のアルカリ性にするなど,鉄系材料と銅系材料との両者を考慮した最適の濃度条件
及び注入方法の設定及び運用面での慎重な対応が必要となる。
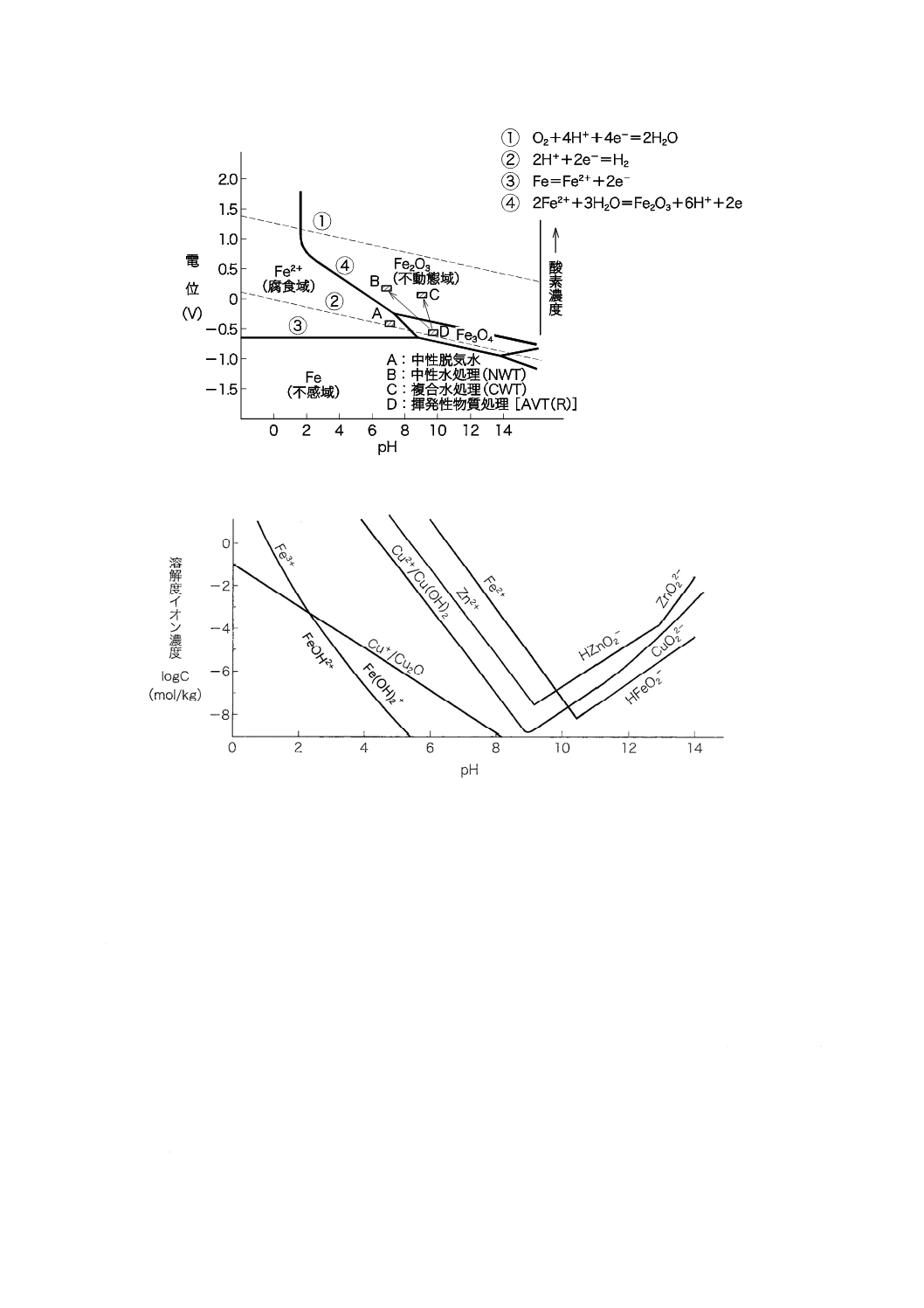
58
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
図A.23−鉄−水系の電位−pH図(25 ℃)[25]
図A.24−酸化物,水酸化物の溶解度に対するpHの影響(25 ℃)[26]
A.5.4 管理項目
A.5.4.1 水管ボイラ(循環ボイラ)の給水
水管ボイラ(循環ボイラ)の給水の場合,次のpH,酸電気伝導率,溶存酸素,鉄及び銅の5項目が管理
項目である。
a) pH 鉄系酸化物の溶解防止にはpHを高くすることが望ましく,A.2.4.2 a)から給水の温度において鉄
イオン濃度が最も低くなる値を上限値に設定する。
b) 酸電気伝導率 管理値の設定では,溶存酸素による腐食抑制効果を保持するため,りん酸塩処理及び
揮発性物質処理の管理値よりも厳しい値で管理する。
酸素処理では,A.5.4.3 b)で記載するように,給水,ボイラ水中に不純物をほとんど含まない高純度
の水が要求され,塩化物イオン,硫酸イオンなどの陰イオンが増加すると3価の鉄化合物による保護
皮膜を破壊し,腐食が進行する。このため,水管ボイラの酸素処理においても,復水処理装置の設置
が望ましい。
c) 溶存酸素 酸素処理では,A.5.4.3 c)で記載するように,鉄系材料の表面のち(緻)密な保護皮膜の形
59
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
成には,溶存酸素が20〜200 μg/L必要である。しかし,水管ボイラにおいては,給水中の溶存酸素濃
度の上限値からボイラ水への影響を考慮すると,溶存酸素濃度の上限値を低くする必要があるため,
管理値を見直している。
d) 鉄 酸素処理では,A.5.4.3 d)で記載するように,各系統の鉄の濃度は,酸化鉄の溶解度の減少に伴い
低下する。このため,給水の鉄の濃度は,従来の水処理に比べ抑制できると考えられる。国内での水
管ボイラでは実績が少ないが,海外の実績では,貫流ボイラと同様な水質を維持できていることから,
貫流ボイラの酸素処理の管理値を用いる。
e) 銅 酸素処理では,A.5.4.3 e)で記載するように,揮発性物質処理と比較して給水中の銅の濃度は高い
値となる可能性もある。しかし,水管ボイラの場合は,実績が少なく,銅の挙動が不明確であること
から,水管ボイラの該当する圧力区分の揮発性物質処理の管理値を用いる。
A.5.4.2 水管ボイラ(循環ボイラ)のボイラ水
水管ボイラ(循環ボイラ)のボイラ水の場合,次のpH,酸電気伝導率,塩化物イオン及びシリカの4
項目が管理項目である。
a) pH ボイラ水のpHは,給水に含まれてボイラに流入し,ボイラ水中に残留するアンモニウムイオン
などの揮発性塩基だけによって保たれる。このため,A.4.4.2で記載したように給水とボイラ水とのpH
との差は,ボイラの運転条件その他の影響を受けて一定ではないので,ボイラ水のpHは,給水のpH
と同じ範囲を目標にして管理すればよい。
なお,鉄系酸化物の溶解防止にはpHを高くすることが望ましく,A.2.4.2 a)からボイラ水の温度に
おいて,鉄イオン濃度が最も低くなる値を上限値に設定する。
b) 酸電気伝導率 給水系統に酸素処理を適用する場合,給水及びボイラ水のpHを調節するために,通
常,アンモニアなどの揮発性物質を添加するが,この管理値はこれらの影響を除去するために,水素
イオン形の強酸性陽イオン交換樹脂層を通した後の値である。酸素処理においてボイラの鋼材表面に
形成する酸化鉄の皮膜は,水中の塩化物イオンなどの陰イオンの増加によって皮膜を破壊するので,
それらの総量に相当する酸電気伝導率もより低い値が好ましく,実績から判断して0.01 mS/m以下で
あることが望ましい。
c) 塩化物イオン 上述のように陰イオンの存在は,酸素処理において鋼材の表面に形成する酸化鉄の皮
膜に対して好ましくない。そのため,塩化物イオンの管理値を国内外の実績を考慮して厳しく設定し
た。
d) シリカ シリカ濃度の管理値設定に対する基本的な考え方は,A.2.4.2 g)を参照。
A.5.4.3 貫流ボイラの給水
貫流ボイラの給水では,次のpH,酸電気伝導率,溶存酸素,鉄,銅及びシリカの6項目が管理項目であ
る。
a) pH 酸素処理においては,鉄系材料の保護皮膜として生成が推測されるのは,低温で酸化水酸化鉄
(III)[FeO(OH)],高温でα-酸化物(III)[(α- Fe2O3):ヘマタイト]の3価の鉄酸化物であり,これ
ら3価の鉄酸化物の水への溶解度は,pH 6以上では無視し得るほど小さい(図A.24を参照)[26]。し
かし,酸素処理は揮発性物質処理に比べて不純物の濃度を厳しく管理することが要求され,復水処理
装置はNH4+- OH−形の運用では不十分で,H+- OH−形の運用が必要となる。そこで,復水器,給水加
熱器などの系統に銅合金材料を使用していない場合には,アンモニアなどによる水質の調節は全く行
わず,復水脱塩装置の再生頻度も少なくなるpH 7付近を目標とした中性水処理と称する水処理が可能
となるが,A.5.3で述べたように,CWTに比べて適用実績は少ない。また,銅の溶解度は,図A.25
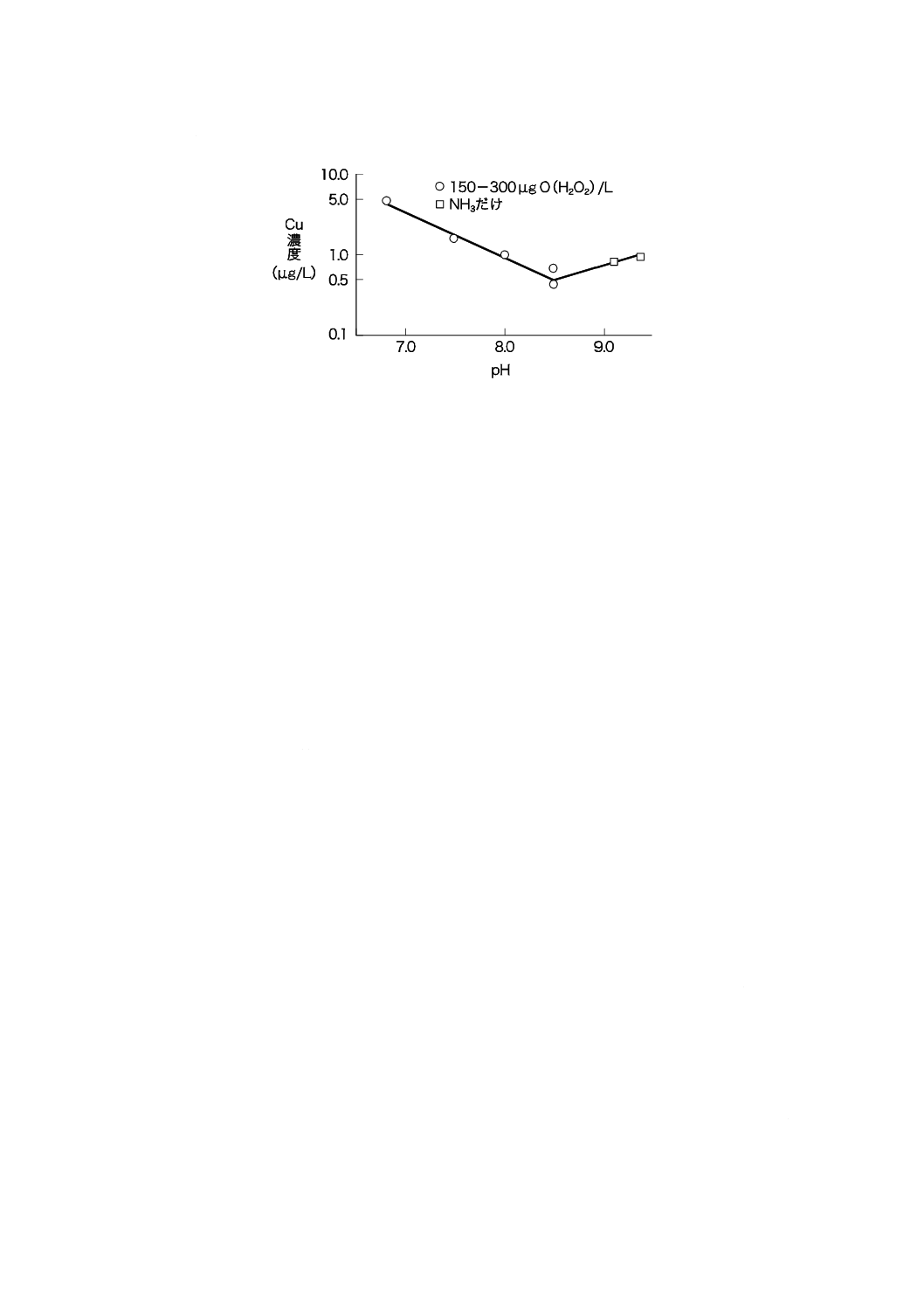
60
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
に示すように,pH 8.5付近で最小となる[28]。
図A.25−pHと銅の濃度との関係[28]
給水の溶存酸素の濃度を低い値に管理する揮発性物質処理においては,保護皮膜として酸化銅(I)
(Cu2O)が生成するが,酸素処理では酸化銅(II)(CuO)の生成も予測される。酸化銅(II)の溶解
度は,酸化銅(I)の溶解度より大きいことから,復水器,給水加熱器などに銅合金材料を使用してい
る場合は,酸化銅(II)の溶解度が最小となるpH 8.5程度に保持する必要がある。
これらのことから,酸素処理のpHは,揮発性物質処理におけるpHの範囲,及び酸素が十分に供給
されない復水器出口及びドレン系統での鉄の溶出を抑制するため系統水を高いpHで運転しているプ
ラントの実証試験[21]の結果を考慮し,A.2.4.2 a)から,鉄イオン濃度が最も低くなる値を上限値に設定
する。
なお,ドレン系統の鉄濃度の高い一部のプラントでは,一時的にpHを9.4〜10.0まで上昇させて鉄
の溶出を抑制しているが,系統に銅合金を使用していなければ,特に問題にはならない。ただし,高
いpH域での給水管理は,復水脱塩装置の再生頻度を増加させること,及び復水器に銅合金を使用し
ている場合はアンモニア・アタックの原因となるため,プラントの水質状況を勘案しながら,上限値
をできるだけ低い値に調節することが望ましい。
ドレン系統の鉄の溶出制御に特化した対策としては,ドレン系へのアンモニア注入,低合金鋼又は
ステンレス鋼の採用なども考えられる。
b) 酸電気伝導率 酸素処理で生成する鉄系酸化物は,水側からヘマタイト,マグネタイトの二層構造を
形成し,鉄系材料に対する安定した腐食抑止効果があるということを,ヨーロッパでの約40年の実績
が示している。ただし,これは給水及びボイラ水中に不純物をほとんど含まない高純度の水の場合で
あり,塩化物イオン,硫酸イオンなどの陰イオンが増加すると,前述の保護皮膜は破壊し,腐食が進
行する。このため,揮発性物質処理[AVT(R)]の管理値よりも厳しい管理値以下に設定する。
c) 溶存酸素 酸素処理で鉄系材料の表面に生成する金属酸化物は,b)で記載したように水側からヘマタ
イト,マグネタイトの二層構造となる。溶存酸素の共存下で,ヘマタイトの微細粒子が多孔性のマグ
ネタイトの空孔を埋めること,及び生成したマグネタイトの結晶径も揮発性物質処理に比べて小さい
ことから,極めて安定な保護皮膜として材料の腐食を抑制する。また,低温側で最上層部の水酸化鉄
(III),高温側で生成する酸化鉄(III)の溶解度は,極めて小さいので,各系統の鉄の濃度は減少する。
また,鉄系材料の表面のち(緻)密な保護皮膜の形成には,溶存酸素20〜200 μg/L程度が必要である。
上限値を超過した場合には,直ちに保護皮膜が不安定になるわけではないが,200 μg/L以上存在し続
けると保護皮膜が不安定になりやすく,徐々に腐食性を増す。
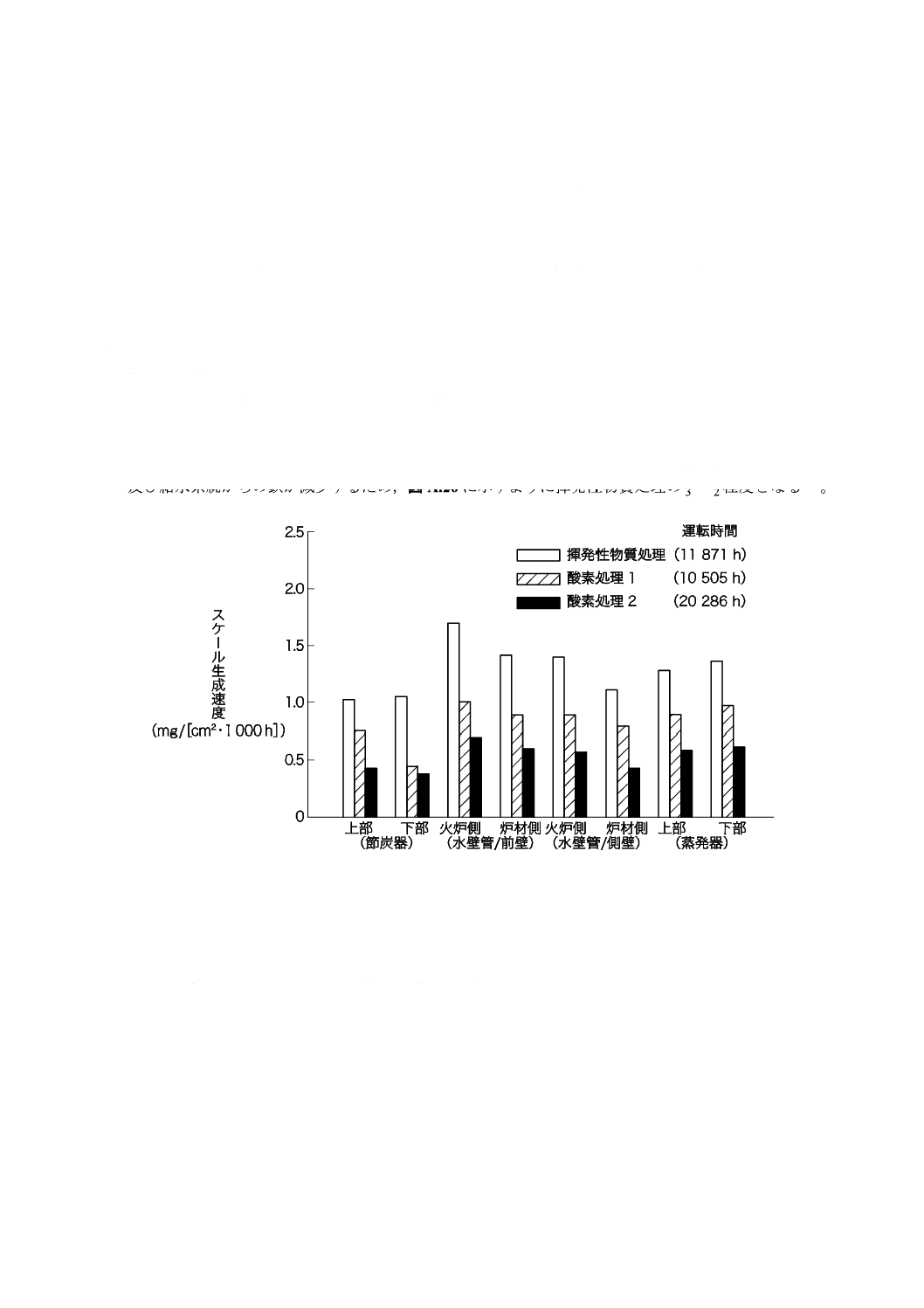
61
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
この溶存酸素の濃度は,これまでの炭素鋼の腐食に対する微量の溶存酸素による腐食抑制効果の研
究結果,沸騰水形軽水炉(BWR)での実績などから,酸素処理における不働態化に必要な溶存酸素の
下限値は,20 μg/L程度と考えられる。また,実機の給水系での腐食電位の測定結果においても20〜
25 μg/L程度の溶存酸素の濃度でヘマタイトの安定域に移行するという報告がある[29]。酸素処理へ転換
した初期には,ヘマタイトの早期生成のため,上限の200 μg/L付近まで溶存酸素を高めて運転するこ
とが必要であると考えられる。一方,保護皮膜を形成して定常運転が継続した場合には,低めの値で
も保護皮膜を保持することから,溶存酸素の濃度は,管理値の範囲で給水の鉄,銅などの濃度が最小
になるのに適した値とする。
d) 鉄 酸素処理では,各系統の鉄の濃度は,酸化鉄の溶解度の減少に伴い低下する。給水の鉄の濃度は,
揮発性物質処理に比べ50 %以下に抑制できる。
なお,分析精度の問題はあるが,実機の実績では1 μg/L以下を示している場合がほとんどであるこ
とから,鉄の濃度は,できるだけ低い値に管理するのが望ましい。
酸素処理における火炉水冷壁管のスケール生成速度は,前述のち(緻)密な皮膜による腐食の抑制,
及び給水系統からの鉄が減少するため,図A.26に示すように揮発性物質処理の32〜21程度となる[30]。
図A.26−スケール生成速度[30]
また,揮発性物質処理では,しばしばボイラ系統にマグネタイトの波状スケールによって圧力損失
が増大する。一方,酸素処理では,一般に波状スケールの生成は少ない。このため,揮発性物質処理
から酸素処理へ変更すると,波状スケールが平滑化し,図A.27に示すように,揮発性物質処理で上昇
した圧力損失が初期の値以下に緩やかに減少する傾向も見られる[30]。
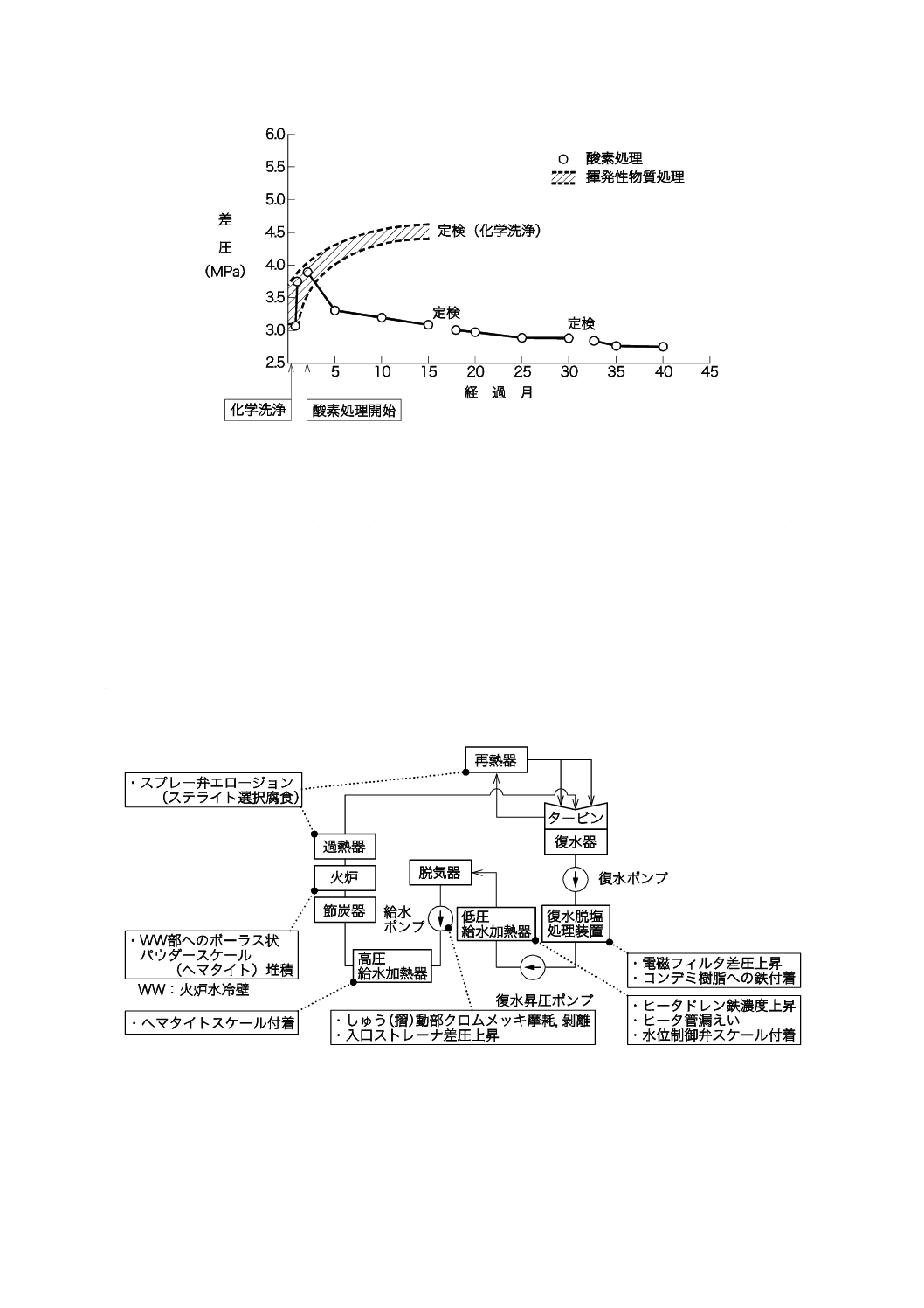
62
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
図A.27−圧力損失及び運転時間[30]
e) 銅 平衡条件での水と接触する銅の表面に生成する銅酸化物の溶解度を図A.24に示す。A.5.4.3 a)で
記載したように,酸化銅(II)は酸化銅(I)に比べ溶解度が大きいため,酸素処理では,揮発性物質
処理と比較して,給水中の銅の濃度が高い値となる可能性があった。しかし,実機での運用実績では
この値を十分満足する結果を示していることから,より低い管理値を設定した。
f)
シリカ シリカの給水及びボイラ水中での挙動は,溶存酸素の有無にほとんど影響を受けないため,
揮発性物質処理と同一の基準で管理する。
A.5.5 留意事項
酸素処理の留意事項は,次のとおりである。
a) 酸素処理適用プラントにおけるトラブル事例を図A.28 [31]に示す。ただし,酸素処理の導入に当たり,
設備・運用対策を行うことによって,現在は特に運用の支障となるケースはない。
図A.28−酸素処理適用プラントにおけるトラブル事例[31]
b) 給水処理に酸素処理法を適用しているプラントでは,近年,幾つかのプラントにおいて,酸素処理適
用後に,低圧給水加熱器ドレン系統の鉄濃度が上昇する事象が発生し,火炉壁管メタル温度上昇の要
因となるパウダースケールが火炉壁管内面へ生成・付着していることが確認された。
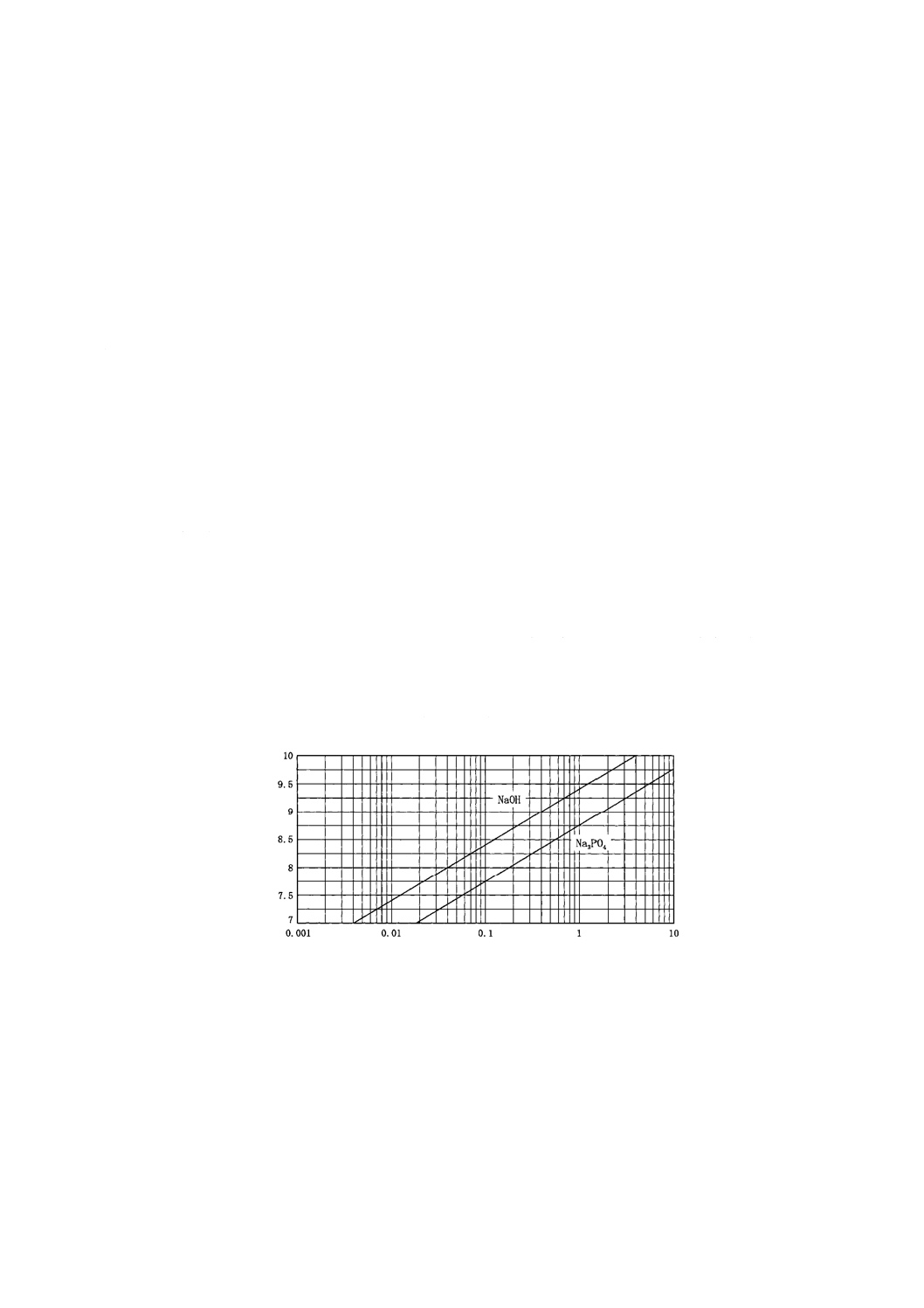
63
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
水壁管へのスケール生成は,メタル温度を上昇させ,過熱損傷又は周方向亀裂(エレファントスキ
ン)の原因となり,場合によっては高温腐食による減肉,クリープ破断などに至る。このため,水質
及び運転データの管理を着実に行う必要がある。
A.6 低濃度水酸化ナトリウム処理
A.6.1 適用ボイラ
次のボイラの圧力区分のボイラ水に適用する。
a) イオン交換水を使用する産業用水管ボイラ:常用使用圧力3 MPaを超え15 MPa以下
b) 電気事業用排熱回収ボイラ:常用使用圧力3 MPa以下,及び3 MPaを超え16.5 MPa以下
c) 電気事業用循環ボイラ:常用使用圧力15 MPaを超え16.5 MPa以下
低濃度水酸化ナトリウム処理は,海外で実用化され十分な使用実績をもつが,国内では使用実績がない。
このため,低濃度水酸化ナトリウム処理の適用に当たっての留意点などについて記載する。
A.6.2 処理方法
低濃度水酸化ナトリウム処理は,ボイラ水の注入薬品をりん酸ナトリウムに替えて,水酸化ナトリウム
(NaOH)で調整する処理方式である。また,注入点は,りん酸塩処理の場合とほぼ同様で,一般に,ド
ラム入口(降水管)である。
この低濃度水酸化ナトリウム処理では,水酸化ナトリウムの濃度を,およそ0.4〜4 mg/L,すなわち,pH
9〜10の範囲を中心にして調整する。NaOHは強電解質であり,水酸化物イオン(OH−イオン)として解
離しやすい。このため,常温下において,アンモニア(NH3)又はりん酸三ナトリウム(Na3PO4)と比較
して,pH上昇効果が大きい。また,アンモニアと比較した場合,高温水中においても解離しやすいこと,
気相側への分配比が小さいことなどから,高温水中においてもpHは低下しにくく,ボイラ水のpHはアル
カリ性を保持しやすい。
一方,水酸化ナトリウムの濃度とpH(25 ℃)との関係を図A.29に示す[32]。
pH
濃度(mg/kg)
図A.29−水酸化ナトリウム及びりん酸三ナトリウムの濃度とpH(25 ℃)との関係[32]
この図によって,水酸化ナトリウムの場合には,りん酸三ナトリウムの場合と比較して,例えば,pH 9
〜10程度の弱アルカリに保持するために必要な濃度は,数分の一程度と低濃度でよいことが分かる。この
ことは,水質調整の面からは,有利な点の一つと考えられる。
A.6.3 処理の原理
上述のように,低濃度水酸化ナトリウム処理では,水酸化ナトリウムの濃度を,およそ0.4〜4 mg/L(pH
9〜10)程度に保持し,また,溶存酸素については低く管理する。このように,低濃度水酸化ナトリウム処
64
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
理は,十分に脱気した,弱アルカリ性の高温水環境下において,式(A.12)に示すように,炭素鋼の表面に
安定なマグネタイトから成る保護皮膜を形成して,腐食を抑制する水処理方式である。
なお,これは,りん酸塩処理及び揮発性物質処理AVT(R)とも,基本的に同様である。
3 Fe+4 H 2O → Fe 3O4+4 H2 ················································(A.12)
低濃度水酸化ナトリウム処理の主な特徴のうち,長所としては,次の点がある。
− りん酸塩の場合とは異なり,高温水中で水酸化ナトリウムの溶解度が高く,りん酸塩処理時にしば
しば経験する,いわゆるハイドアウト現象を生じにくい。
− 上述のハイドアウトによる水質変化を生じにくく,また,強電解質でpH上昇効果が大きいことな
どから,pHの管理が容易になる。
− 薬剤中にりん(P)成分を含まないため,りん酸塩処理の場合と比較して,環境に対する負荷が少
ない。
これらの特徴のうち,主なものについて,次に詳細に記載する。
a) 溶解度の温度特性 水酸化ナトリウムの水に対する溶解度を,表A.2に示す[33]。この表から明らかな
ように,水酸化ナトリウムは,100〜300 ℃の温度領域において,温度上昇とともに溶解度が増加する
性質をもっている。このため,りん酸塩処理時にしばしば経験する,負荷上昇に伴ってりん酸イオン
の濃度が減少する,いわゆるハイドアウト現象は,本水処理では生じにくいものと判断できる。
表A.2−水酸化ナトリウムの水に対する溶解度の温度による変化(抜粋値)[33]
温度(℃)
25
50
100
150
200
250
300
溶解度(g/100 g H2O)
113
146
337
418
554
920
2 841
b) 気液分配特性 りん酸三ナトリウム,水酸化ナトリウムなどの無機物質における液相中の濃度に対す
る蒸気中の濃度の比(気液分配比)を,ドラム圧力の関数で示した気液分配特性のデータの一例とし
て,図A.30に示す[34]。
この図から,各物質の気液分配比は,ドラム圧力(温度)との関係で決まることとなり,高温,高
圧下になるほど大きな値となり,蒸気中に移行しやすいこと,また,各物質間の差異が少なくなるこ
とを示している。また,このほか,水酸化ナトリウムは,350 ℃から臨界温度付近で気液分配比が急
激に増大することから,この温度領域では水酸化ナトリウムが蒸気中に移行しやすくなることを示し
ている[35]。

65
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
ドラム圧力(psia)
220
C
o
n
c
e
n
t
r
a
t
i
o
n
i
n
v
a
p
o
r
C
on
ce
n
t
r
a
t
i
on
i
n
li
q
u
i
d
200
10
160
10-1
10-2
10-3
10-4
10-5
10-6
10-7
120 80 60 40 30 20
10
3
2
0
0
3
0
0
0
2
8
0
0
2
6
0
0
2
2
0
0
2
0
0
0
1
6
0
0
1
2
0
0
1
0
0
0
6
0
0
4
0
0
2
0
0
蒸気中濃度
液相中濃度
1
2
6
10
20
60 100
0
ドラム圧力(atm)
Drum pressure(atm)
Density of liquid
Density of steam
図A.30−りん酸三ナトリウム,水酸化ナトリウムなどの無機物質のドラム圧力と
気液分配比との関係(Ray diagram)[34]
一方,図A.30においては,水酸化ナトリウム及びりん酸三ナトリウムの両者の比較が可能である。
この場合には,例えば,12.16 MPa(120 atm)程度の圧力条件下では,りん酸三ナトリウムの気液分
配比は約3×10−5であるのに対して,水酸化ナトリウムの気液分配比は約1×10−4程度であり,数倍
程度高いことが分かる。しかし,図A.29に示したように,同一pHの水中では,りん酸三ナトリウム
の方が水酸化ナトリウムより数倍濃度が高い。
したがって,蒸気中に存在するナトリウム濃度で比較した場合には,両者の比較では,ほぼ同程度
となるものと考えられる。また,濃度も低いことが推定される。ただし,A.6.5 a)に記載するように,
りん酸三ナトリウムと比較して水酸化ナトリウムの腐食性が大きい。このことから,蒸気系統に移行
した場合の腐食への影響を低減するため,低濃度水酸化ナトリウム処理においては,りん酸塩処理の
場合と比較して,ナトリウム成分のキャリオーバには,より留意する必要がある。
なお,ボイラ水中の化学成分の化学的キャリオーバは,一般にドラム圧力16 MPa以上で顕著にな
ることから,低濃度水酸化ナトリウム処理の場合に,運転経験としては,ドラム圧力が17 MPaまで
に限るという報告がある[36]。したがって,低濃度水酸化ナトリウム処理では,適用可能なボイラの圧
力は17 MPaまでが望ましい。
c) 塩化物イオンに対する腐食抑制効果 低濃度水酸化ナトリウム処理のその他の特徴の一つは,塩化物
イオンに対する腐食抑制効果の度合いである。その一つとして,海水漏えい時においては,塩化マグ
ネシウムの加水分解によって生じた酸性の塩化物を水酸化ナトリウムで中和するため,塩化物イオン
に起因する酸腐食に対する許容度をもつ。
海水漏えい時には,A.3.3.3の式(A.10)で示したように,塩化マグネシウムの加水分反応によって,
ボイラ水のpHが低下し,腐食が促進されやすくなる。
この場合に,既にA.3.3.3で記載したように,りん酸塩処理の場合には,りん酸三ナトリウム(Na3PO4)
の加水分解によって生成するNa2HPO4が,式(A.11)で示した中和反応を生じ,酸性成分の影響を抑制
液体の密度
蒸気の密度
66
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
するため,ボイラ水中のNaOHの濃度変化は少ない。
これに対して,低濃度水酸化ナトリウム処理の場合には,ボイラ水中に存在する水酸化ナトリウム
によって,次の式(A.13)の中和反応によって,pHの低下を一定程度防止できる。
NaOH+HCl → NaCl+H2O ··················································(A.13)
しかし,HClを中和するため,当量のNaOHを消費することで,ボイラ水の緩衝作用は,りん酸塩
処理と比較した場合には低くなる。
一方,AVT(R)の場合には,同様な反応によって,強酸−弱塩基から成る塩(塩化アンモニウム)を
生成することになるが,中和反応は期待できない[37]ことから,緩衝作用は乏しい。
このように,低濃度水酸化ナトリウム処理は,AVT(R)との比較では優位であるが,一方,りん酸塩
処理と比較すると,pHの変動又は硬度成分に対する緩衝作用は,やや乏しいと考えられる。
A.6.4 管理項目
低濃度水酸化ナトリウム処理の管理項目は,次のとおりである。
a) pH 低濃度水酸化ナトリウム処理の適用時においては,アルカリ濃縮による腐食を防止することが不
可欠である。アルカリ腐食は高温・高圧になるほど,その危険性が高まることから,いずれの圧力区
分においてもpHが10以下となるように設定した。特に,10 MPaを超える産業用循環ボイラ,15 MPa
を超える電力事業用循環ボイラ,及び排熱回収ボイラについては,この点を考慮して,pH 9.1〜9.5の
範囲に設定している。一方,10 MPa以下の圧力区分の産業用循環ボイラ及び排熱回収ボイラについて
は,いずれの圧力区分においても同一の値として,pH 9.4〜10.0の範囲に設定している。
b) 電気伝導率 電気伝導率については,ボイラ水のpHの上限値及びナトリウム濃度の上限値に相当す
る水酸化ナトリウムの電気伝導率を考慮して設定している。一例として,10 MPaを超える産業用及び
15 MPaを超える電力事業用の循環ボイラについては,1 mS/m以下に設定している。
なお,低濃度水酸化ナトリウム処理における水質純度の指標となる酸電気伝導率に関しては,次の
c)の塩化物イオンに着目した場合には,A.6.3 c)に記載したように,AVT(R)と比較して,不純物に対す
る裕度があるため,許容値は高めに設定可能となる。一方,りん酸塩処理と比較した場合には,より
制限された値が要求される。これらの関係を考慮した上で,水質純度を保持する観点から,許容し得
る塩化物イオン濃度に対応する酸電気伝導率を,各圧力区分における上限値として設定している。こ
の結果,本水処理では揮発性物質処理AVT(R)と同一の値に設定している。一例として,10 MPaを超
える産業用及び15 MPaを超える電力事業用の循環ボイラについては,揮発性物質処理AVT(R)では2
mS/m以下であり,本水処理では,2 mS/m以下に設定している。B.3を参照する。
c) 塩化物イオン A.6.3 c)で記載したように,塩化物イオンに対する緩衝作用の程度は,各水処理の比較
では,基本的には,揮発性物質処理AVT(R)<低濃度水酸化ナトリウム処理<りん酸塩処理 の順とな
る。この従来の各水処理における塩化物イオン濃度の許容値との関係を考慮した上で,実運用上は,
A.6.4 e)で記載するナトリウムとの関係で,塩化物イオンをできる限り低減する必要がある。このため,
各圧力区分において許容し得る塩化物イオン濃度は,揮発性物質処理AVT(R)と同一の値に設定した。
一例として,10 MPaを超える産業用及び15 MPaを超える電力事業用の循環ボイラについては,りん
酸塩処理では2 mg/L以下,揮発性物質処理AVT(R)では1 mg/L以下であり,本水処理では,1 mg/L
以下に設定している。
d) シリカ シリカについては,B.14を参照。
e) ナトリウム 低濃度水酸化ナトリウム処理を適用する場合,ナトリウムの蒸気中へのキャリオーバに
よる腐食発生を抑制するため,ボイラ水のナトリウム濃度について設定している。A.6.3で記載したよ
67
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
うに,多くの無機物質と同様に,水酸化ナトリウムは350 ℃付近で気液分配比が急激に増大している
ことから,この温度領域では水酸化ナトリウムが蒸気中に移行しやすいと考えられる。このため,特
に10 MPaを超える産業用及び15 MPaを超える電力事業用の循環ボイラなどにおいては,タービン側
での腐食を抑制する観点から,蒸気中のナトリウム濃度が5 μg/L以下となるよう,ボイラ水のナトリ
ウム濃度を低く管理する。すなわち,メカニカルキャリオーバ(キャリオーバ率を10 MPa以下:0.11 %,
10 MPaを超える場合:0.2 %と仮定[38])によるナトリウム濃度に加えて,図A.30に示した水酸化ナト
リウムの気液分配比からケミカルキャリオーバ(キャリオーバ率を10 MPa以下:0.003 %,10 MPaを
超え15 MPa以下:0.08 %,15 MPaを超える場合:0.3 %と仮定)によるナトリウム濃度を算出するこ
とによって,蒸気中のナトリウムを試算した。ボイラ水の水質管理値を維持できる範囲内で,この値
が5 μg/L以下となるように,10 MPaを超えるボイラの場合,ナトリウム濃度を0.9 mg/Lに設定して
いる。また,10 MPa以下のボイラの場合には,キャリオーバ防止の点からは,ボイラ水中のナトリウ
ム濃度の上限値は約4.4 mg/Lと試算した。この結果に基づき,ボイラ水のpH,塩化物イオン濃度な
どの水質管理値を維持できる範囲内の値として,2.8 mg/Lに設定している。
なお,蒸気中のナトリウムについては,B.16を参照。
A.6.5 留意事項
低濃度水酸化ナトリウム処理の留意事項は,次のとおりである。
a) アルカリ腐食の防止の必要性 この低濃度水酸化ナトリウム処理の場合には,熱負荷の高い箇所又は
スケールが付着して管壁温度が上昇した箇所(ホットスポット)においては,管内面の表面状態など
によってボイラ水の濃縮が起こると,高濃度のNaOHが生成しやすい。この場合の,過熱度(管壁温
度−ボイラ水の飽和温度の温度差)と,濃縮境膜における水酸化ナトリウムの最高到達濃度との関係
を図A.31に,NaOH濃度と炭素鋼の腐食量との関係を図A.32に示す[39], [40]。
すなわち,図A.31に示すように,過熱度が10 ℃を超えるとNaOHの濃度は10〜20 %に達し,過
熱度の上昇とともに,数十パーセント程度にまで濃縮され得ることが分かる。一方,腐食の面からは,
図A.32に示すように,310 ℃ではNaOHの濃度10 %程度から炭素鋼の腐食速度が増大し始め,20 %
以上の高濃度になると腐食速度は急速に増大することが知られている。また,りん酸三ナトリウムと
比較して高濃度側での水酸化ナトリウムの腐食が顕著であることが分かる。このような高濃度の
NaOHの環境下では,次の式(A.14)及び式(A.15)の反応によって,炭素鋼が繰り返し腐食することにな
る[39], [40]。
Fe+2NaOH → Na2FeO2+2H ················································(A.14)
3Na2FeO2+4H2O → 6NaOH+Fe3O4+2H ·································(A.15)
また,式(A.14)及び式(A.15)において,発生した水素が鋼材中の炭素と反応してメタンとなり,材料
強度を低下させる水素ぜい(脆)化を生じることもある。
一方,NaOHの濃度が高濃度の場合,炭素鋼において,応力腐食割れ(SCC)の感受性を増大させ
ることも知られている[41]。このため,低水酸化ナトリウム処理の適用に当たっては,このような高濃
度NaOHの生成を抑制する必要があり,ボイラ水のpHを適切に管理するとともに,ボイラ水系統で
の局部過熱する箇所を生じさせないように留意する必要がある。
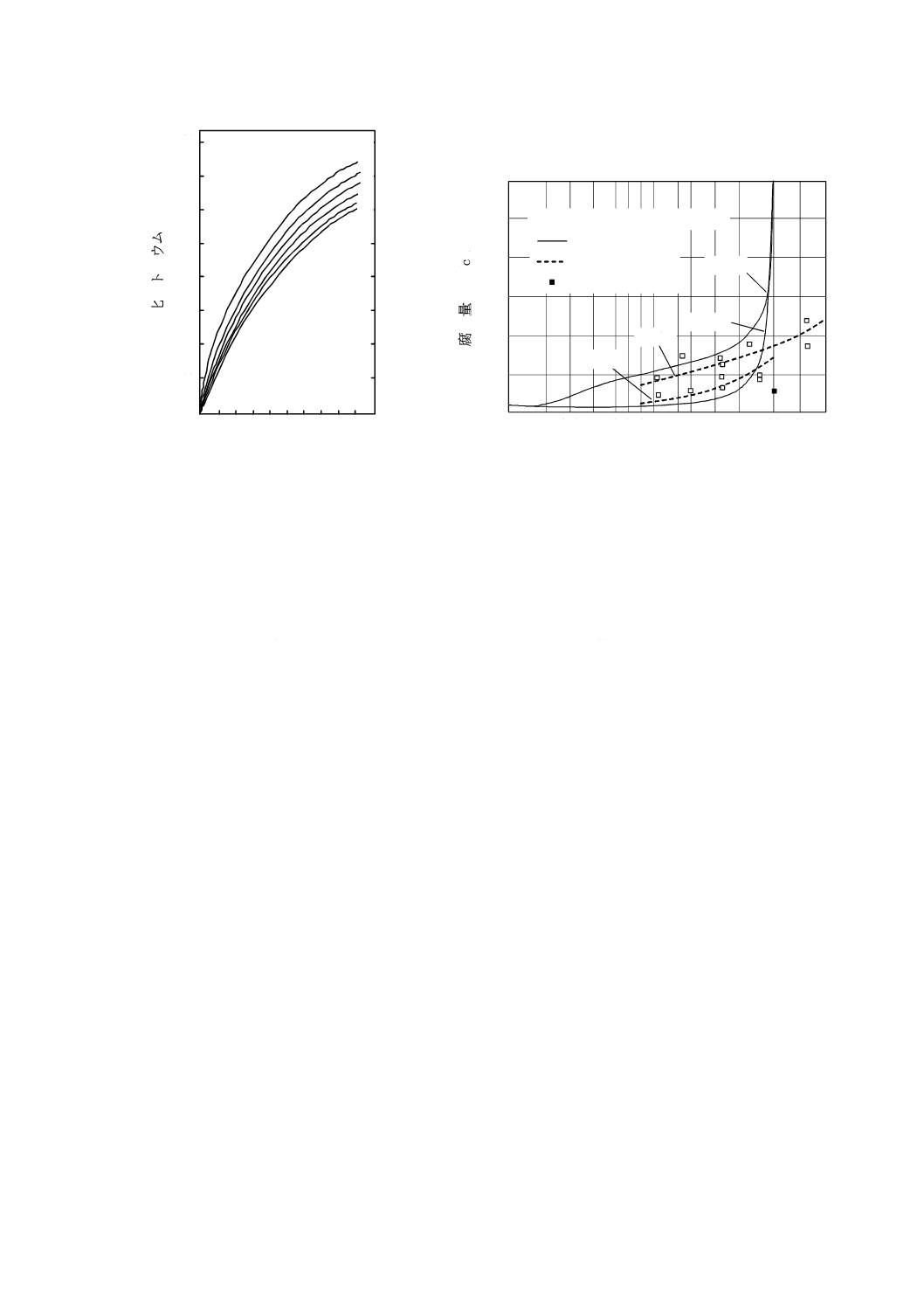
68
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
80
70
60
50
40
0
温度差 ℃
水
酸化
ナト
リウム
%
30
100
80
40
30
20
10
50 60 70
90
0
20
10
圧力(Kgf/cm2)
10
30
80
120
160
180
60
50
40
30
20
0
15 20
30 40
NaOH濃度(%)
腐
食
量
m
g
/c
m
2
10
310℃
10
8
5
4
3
2
1
0.4
0.1
400℃
310℃
400℃
400℃,100h,鋼棒(C:0.16%)
NaOH 水溶液
Na3PO4 水溶液
Na2HPO4水溶液
図A.31−過熱度(管壁温度−ボイラ水の飽和温度)と
濃縮膜におけるNaOHの最高到達濃度との関係[39], [40]
図A.32−NaOH濃度と炭素鋼の腐食量との
関係[39], [40]
b) 海水漏えい時の対応 低濃度水酸化ナトリウム処理においては,A.6.3 c)で記載したように,海水漏え
い時の不純物の混入によるpHなどの変動に対する緩衝性は,AVT(R)との比較では,優位である。し
かし,一方,りん酸塩処理と比較した場合には,pH及び硬度成分の緩衝作用の面では,やや劣るもの
と考えられる。このため,海水漏えい時においては,より安全側の対応処置として,水酸化ナトリウ
ムのほかに,りん酸塩(りん酸三ナトリウム)を注入できる体制を整えておくことが望ましい。
c) 適用上の課題 国内においては,1950年代に,電気事業用循環ボイラに対して水酸化ナトリウムを用
いたアルカリ処理を導入した経験はある。しかし,このときには,比較的高濃度のアルカリで運用し
たことによって,ボイラ水壁管部で不具合を生じた経緯があり,その後,国内での電気事業用ボイラ
への本水処理の適用事例はない。一方,海外では,英国及びドイツを中心とした欧州並びに南アフリ
カなどにおいて,事業用高圧循環ボイラにおいて本水処理を広く適用しており,水質管理基準を策定
している。また,同処理法の国際的なガイダンスドキュメントをIAPWSが発表している[42]。
したがって,本水処理法の事業用ボイラへの実機適用に際しては,コンバインドサイクルプラント
の排熱回収ボイラのように,熱負荷が50 000〜60 000 kcal/(m2・h)程度で,化石燃料の場合の160 000〜
500 000 kcal/(m2・h)と比較して,数分の一から十分の一程度の低熱負荷のボイラなどを対象として,短
期・長期の適用試験などで運転実績を蓄積した上で,実用化することが望ましい。
69
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書B
(参考)
ボイラの給水及びボイラ水の水質の管理項目
B.1
一般
この附属書は,ボイラの給水及びボイラ水の各水質管理項目と関連する水質項目の意義について記載す
る。
B.2
pH
B.2.1 25 ℃でのpH
給水及びボイラ水のpHは,給水系統及びボイラ内部の腐食防止のために管理するものであり,25 ℃に
おける値を示す。
pHは,ガラス電極pH計を用いてJIS Z 8802 [1]に従って測定する。このJIS Z 8802は国際計量法機関
(OIML)から出されたpHに関する勧告(International Recommendation N°54,pH Scale for Aqueous solution)
に従って,pH標準液の調製方法及びpH目盛を整合させている。また,欧米諸国のpH測定方法の規格ASTM
E 70,BS 1647,DIN 19266,NF T90-008などにも整合している。
B.2.2 ボイラ水及び高温高圧状態での水のpH
一般に稼働状態のボイラ水及び高温高圧状態での水のpHを直接測定するのは簡単ではないので,減圧
器及び冷却器を用いて室温まで冷却し,101.325 kPa(1気圧)に減圧したものを試料として採取し,これ
を25 ℃に調節してpHの測定を行っている。したがって,実際の稼働状態にあるボイラ水のpHは,この
規格に記載された値とは異なっている。
すなわち,水は弱電解質であるため,水素イオンと水酸化物イオンとに解離している。この解離の割合
は温度が上昇すると大きくなり約250 ℃近傍で最大となる。各温度における水の解離定数Kw及びpHを
表B.1[2], [3], [4]に示す。
表B.1−水(純粋な水)の解離定数
温度
(℃)
解離定数
Kw
pH
温度
(℃)
解離定数
Kw
pH
温度
(℃)
解離定数
Kw
pH
0
1.15×10−15
7.47
150
2.28×10−12
5.82
300
5.00×10−12
5.65
25
1.02×10−14
7.00
175
3.62×10−12
5.72
325
1.96×10−12
5.85
50
5.34×10−14
6.64
200
5.00×10−12
5.65
350
5.06×10−13
6.15
75
1.95×10−13
6.35
225
6.00×10−12
5.61
374.14
1.84×10−16
7.87
100
5.44×10−13
6.13
250
6.37×10−12
5.60
125
1.22×10−12
5.96
275
5.97×10−12
5.61
上述のようにpHは25 ℃での値になっているので,pHを測定する場合には,試料の温度を25 ℃に調
節し,pH計の温度補償回路が25 ℃での起電力を得るように温度補償回路を設定する。
温度補償回路が25 ℃に設定してあれば,試料の温度は25 ℃でなくても25 ℃でのpHを得るように思
えるがこれは厳密にいえば正確ではない。
試料には各種の塩類及び塩基が含まれており,それらのpHへの寄与の温度依存性はそれぞれに固有で
あるので,温度補償回路でも十分には補償し得ない。このため,正確なpHの測定に当たっては,試料の
70
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
温度を25 ℃に調整する。
例えば,軟水給水の丸ボイラ,特殊循環ボイラ,水管ボイラ,又は純水給水の水管ボイラでも給水への
補給水の比率が高く,給水及びボイラ水に補給水中の微量不純物又は薬剤の成分に起因する各種の塩類及
び塩基が比較的高濃度で含まれており,また,添加剤として有機系の脱酸素剤及び分散剤とアルカリ剤と
を組み合わせて使用している場合には,その各塩類,塩基の種類及び濃度の組合せも多岐にわたるため,
それらのpHの温度依存性も多様になり,温度補償回路では,対応が困難である。さらに,純水給水ボイ
ラで給水系・復水系のpH調整剤にアンモニアに代えてアミンを使用し,その発生蒸気の凝縮水を回収し
て給水としている場合には,蒸気凝縮水及び給水中にアミンとその熱分解生成物であるアンモニアとが共
存し,それらの濃度の組合せも多様となるので,やはりそれらのpHの温度依存性も多様になり,温度補
償回路では正確な対応が困難である。
一方,事業用の火力発電設備などのように,補給水として高純度のイオン交換水を使用し,発生蒸気か
ら生じる清浄な凝縮水のほぼ全量を回収して給水とし,水処理用薬剤としてりん酸ナトリウム,アンモニ
ア,水加ヒドラジンなど単一で,かつ,熱分解などによる化学変化の影響の極めて小さい物質だけを低濃
度添加する場合については,ボイラ水に対してはりん酸ナトリウムのそのNa/PO4モル比に応じたpH−濃
度−温度曲線,給水・蒸気・凝縮水に対してはアンモニアのpH−濃度−温度曲線に沿った試料水の温度補
償回路の設定で実用上問題のない補償ができる(水加ヒドラジンの酸素との反応生成物は水及び窒素,熱
分解生成物としてはアンモニア及び窒素であり,試料水の組成及びpHへの影響が小さい。)。実際に,事
業用の火力発電設備では,pH計の起電力の温度依存性及び試料のpHの温度依存性の両方に対応した二重
の温度補償回路をもったpH計が使用され始めている。
B.3
電気伝導率
電気伝導率は,ボイラの給水及びボイラ水中の電解質の濃度の指標として測定する。ただし,揮発性物
質処理及び酸素処理を行っている給水を対象とする場合には,試料(給水)を水素イオン形にした強酸性
陽イオン交換樹脂を充塡したカラム通過後の電気伝導率を測定する。
電気伝導率は試料中の強電解質(塩類)の濃度と相関関係があるので,この強電解質の濃度は試料の溶
解性蒸発残留物に相当する。懸濁物を全く含まない試料の場合には,全蒸発残留物の濃度が溶解性蒸発残
留物の濃度に等しい。
したがって,このような場合には,溶解性蒸発残留物(全蒸発残留物)と電気伝導率とを測定して両者
の相関関係を求めておけば,電気伝導率だけを測定して,溶解性蒸発残留物を推定することが可能になる。
しかし,ボイラ水の場合は,水酸化物イオンが存在するためアルカリ性になっているが,水酸化物イオン
の極限モル伝導率の値[19.83 mS・m2/mol(25 ℃)]は,塩化物イオン及び硫酸イオンの極限モル伝導率の
値の2.5〜2.7倍[Cl−: 7.63 mS・m2/mol(25 ℃),SO42−: 8.00 mS・m2/mol(25 ℃)]であるので,水酸化物
イオンの濃度の僅かな変動によっても電気伝導率の値が変動するので注意する。それぞれのボイラの水質
調節の条件によって水質が変動するので,電気伝導率と溶解性蒸発残留物との関係をそれぞれの条件で求
めておくことが必要である。
B.4
酸電気伝導率
強酸性陽イオン交換樹脂(水素イオン形)層通過後の電気伝導率を指す。給水,発生蒸気及び蒸気凝縮
水中の微量の塩類(電解質)の存在を知るために,水素イオン形に変換した強酸性陽イオン交換樹脂層を
通過した後の電気伝導率を測定する。特に,塩化物,硫酸塩など防食皮膜の安定性を阻害し,蒸気タービ
71
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
ンでの割れ発生の原因ともなる塩類の濃度は極力低く抑える。これらの塩類は水中で陽イオンと陰イオン
(塩化物イオン,硫酸イオンなど)とに解離しているが,水素イオン形の強酸性陽イオン交換樹脂層に通
すと,陽イオンは水素イオンと交換反応を行い,当量の水素イオンを生成する。水素イオンはナトリウム
イオン,アンモニウムイオンなどの陽イオンに比較して,極限モル伝導率が大きいので塩類濃度が強調さ
れる。この水素イオンによる電気伝導率を測定して,微量に共存する塩類の濃度を推定することができる。
また,水酸化ナトリウムなどのアルカリ成分は,水中で解離して陽イオンであるナトリウムイオン及び陰
イオンである水酸イオンに解離しているが,水素イオン形の強酸性陽イオン交換樹脂層を通過させるとナ
トリウムイオンは前述の交換反応によって水素イオンに変わり,これが当量の水酸イオンと反応して,水
(H2O)を生成してこれらのイオンによる電気伝導率は消滅する。さらに,揮発性物質,例えば,ヒドラ
ジン,アンモニア,モルホリン(テトラヒドロキシ-1,4-オキサジニウム)などは,水中で解離してヒドラ
ジニウムイオン,アンモニウムイオン,テトラヒドロキシ-1,4-オキサジニウムイオンなどの陽イオンとし
て存在しているが,これらによる電気伝導率も同じ反応によって消滅する。
なお,給水中に二酸化炭素(CO2)が存在すると,二酸化炭素はこれらの揮発性物質及び炭酸塩を形成
するが,水素イオン形の強酸性陽イオン交換樹脂層を通過させると炭酸(H2CO3)を遊離し,炭酸による
電気伝導率を示すことになり,電解質の共存と誤認することになるので注意を要する。このような場合に
は,二酸化炭素を除去した後に水素イオン形の強酸性陽イオン交換樹脂層に通して電気伝導率を測定する
必要がある。
なお,イオン交換膜等を使用した電気式カチオン交換器を通して測定する方法も一部のプラントにおい
て既に実用化している。
B.5
硬度
硬度は,水中のカルシウム及びマグネシウムの量を,これに対応する炭酸カルシウムの量に換算して試
料1 Lについてのmg数で表し,全硬度,カルシウム硬度及びマグネシウム硬度に区分する。この規格で
用いる“硬度”は,全硬度を意味する。
イオン交換水を給水としている場合には,イオン交換水の電気伝導率を監視しているのでカルシウム,
又はマグネシウムが漏えいしていることはほとんどない。
カルシウム及びマグネシウムは,その化学的性質が異なるので,水道水などの天然水をそのまま給水と
して用いる場合の指標としては,硬度の代わりにカルシウム及びマグネシウムの濃度を別々に定量してそ
れぞれの管理値を定めるのが理想であるが,この規格では硬度を用いた。また,カルシウム及びマグネシ
ウムはアルカリ処理で無害化できる。すなわち,カルシウムはアルカリ性でりん酸イオンと式(B.1)のよう
に反応させ,りん酸塩Ca5(OH)(PO4)3[水酸化トリス(りん酸)五カルシウム]2)として沈殿させる。
5Ca2++OH−+3PO43− → Ca5(OH)(PO4)3 ··································· (B.1)
この反応を完結させるために,添加するりん酸塩は,給水のカルシウム濃度と当量の濃度とが必要であ
り,ボイラ水では,りん酸イオンが過剰になる(この規格で規定した濃度)ように設定する。また,炭酸
イオンが過剰に存在すると炭酸カルシウムが生じる。水道水などを給水としているボイラ水の処理では,
炭酸カルシウムが生成しないようにりん酸イオンをカルシウムの当量(Ca l mgについてPO43− 1.42 mgが,
また,CaCO3 1 mgについてPO43− 0.57 mgが必要)以上に過剰に存在させ,更に十分なアルカリ性を保持
することが必要である。
注2) 慣用名でヒドロキシアパタイトともいう。また,組成式はCa(OH)2・3Ca3(PO4)2又は
Ca10(OH)2(PO4)6で示されることがある。
72
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
マグネシウムは,水酸化物として沈殿させる[式(B.2)参照]。すなわち,マグネシウムと当量の水酸化
ナトリウム[Mg 1 mgについて水酸ナトリウム3.29 mgが必要である。また,マグネシウム硬度CaCO3: 1
mg/Lについて酸消費量(pH 8.3)CaCO3: 1 mg/Lを必要とする。]と更に過剰(目安としてpH 10以上)の
水酸化ナトリウムが共存するように水酸化ナトリウムを添加する。
なお,シリカが多量に存在すると一部のカルシウム及びマグネシウムが式(B.3)及び式(B.4)に示すように
けい酸カルシウム,けい酸マグネシウムとして沈殿することがある。
Mg2++2OH− → Mg(OH)2 ····················································· (B.2)
Ca2++SiO32− → CaSiO3 ······················································· (B.3)
Mg2++SiO32− → MgSiO3 ······················································ (B.4)
B.6
油脂類
ボイラの給水が油脂類を含むと,ボイラに入ってボイラ水のホーミングが生じる。特に,動植物油脂は
ボイラ水中のアルカリ成分によってけん化され,ホーミングを著しくする。また,ボイラ内面に付着した
油脂類は酸化鉄,酸化銅などの腐食生成物が付着する核になり,硬質のスケール状物質を生成する。
伝熱面に付着した油脂類は加熱によって炭化し,炭素質の硬いスケールになり,伝熱面の過熱原因にな
る。このような障害を防止するために,給水の油脂類の濃度をできるだけ低く保つ。
油脂類としてJIS B 8224 [5]のヘキサン抽出物質だけを指定し,その濃度は,5.1において“低く保つこと
が望ましい”とし,数値での記載は行わない。
B.7
溶存酸素
水中の溶存酸素は,火力発電プラントの水側の金属材料を腐食させる主な不純物であるが,その挙動は
アルカリ処理,りん酸塩処理及び揮発性物質処理を行っているボイラと酸素処理を行っているボイラとに
区分して考える必要がある。次に詳述する。
a) アルカリ処理,りん酸塩処理及び揮発性物質処理を行っているボイラの場合 これらの処理方式の場
合には,水中の溶存酸素は,火力発電プラントの水側の金属材料を腐食させる主な不純物である。溶
存酸素による腐食は,孔食の形態で生じることが多い。
一般に腐食反応は,電気化学的に生じる。給水のpHが中性又はアルカリ性であっても水中に溶存
酸素が存在すると式(B.5)〜式(B.7)に示すような反応が起こる。
陽極部 Fe → Fe2++2e− ····················································· (B.5)
陰極部 H2O+21O2+2e− → 2OH− ········································ (B.6)
式(B.5)及び式(B.6)の反応式をまとめると式(B.7)のようになる。
Fe+H2O+21O2 → Fe(OH)2 ··················································· (B.7)
式(B.7)に示すように鋼面から水中に溶出した水酸化鉄(II)は,更に水中の溶存酸素によって式(B.8)
に示すように酸化され水酸化鉄(III)になる。
2Fe(OH)2+H2O+21O2 → 2Fe(OH)3········································· (B.8)
また,銅合金に対してはアンモニアが共存すると式(B.9)に示すようにテトラアンミン銅が生成し腐
食が生じる。
73
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
Cu+21O2+4NH3+H2O → [Cu(NH3)4](OH)2 ······························ (B.9)
溶存酸素の腐食作用は200 ℃以下の低温で,流れが停滞している条件のときに生じやすい。高温の
ボイラでは,電気伝導率の高いボイラ水の場合には,停滞環境ばかりではなく流動条件でも,孔食,
割れなどを生じる懸念がある。したがって,アルカリ処理,りん酸塩処理及び揮発性物質処理を行っ
ているボイラでは,脱酸素剤の添加によって溶存酸素の濃度を可能な限り低く抑えることが必要であ
る。特に,圧力の高いボイラでは,脱気器の設置及び脱酸素剤の添加によって溶剤酸素を除去するこ
とが不可欠である。規格本体では,ボイラの給水中の溶存酸素の濃度をボイラの形態別及び圧力別に
それぞれ規定している。
b) 酸素処理を行っているボイラの場合 a)で記載したようにアルカリ処理,りん酸塩処理及び揮発性物
質処理を行っているボイラでは,溶存酸素濃度をゼロ近傍まで低く抑えているが,酸素処理を行って
いるボイラの場合は,給水中に酸化剤としてごく少量の溶存酸素(O: 20〜200 μg/L)を添加するよう
になっている。
酸素処理では,式(B.8)に示した水酸化鉄(III)は水酸化鉄(II)より水に対する溶解度が小さいこ
とを利用し,水中の電解質の濃度を極めて低く保って溶存酸素の濃度がO: 20〜200 μg/Lになるように
調節した場合に,鉄鋼面上に鉄(III)化合物の不溶性の酸化皮膜が形成され,その後の腐食の進行を
抑制することが可能になることに基づく。
B.8
ヒドラジン(N2H4)
ヒドラジンは,アルカリ処理,りん酸塩処理及び揮発性物質処理を行っているボイラの給水中の溶存酸
素を還元除去するために給水系統に注入する。ヒドラジンは,一般にヒドラジン一水和物を用いる。
ヒドラジン(NH2NH2)は,アンモニア(NH3)の水素原子1個がアミノ基(−NH2)1個と置換した化
合物と考えることができる。また,水と結合が強く水和物として存在する。ヒドラジンの水和物はヒドラ
ジン一水和物(N2H4・H2O)として50 %,60 %,80 %及び98 %濃度のものが市販されている。
ヒドラジンは機能として給水,ボイラ水及び蒸気の質への影響が最も小さい還元剤であるが,その有害
性が問題視されている。
事業用ボイラに対しては,脱酸素剤・還元剤を使用しない水処理法として,揮発性物質処理AVT(LO),
AVT(O)及び酸素処理の規格が提示され,それらがヒドラジンを使用しない処理法となっている。一方,産
業用の低圧から高圧までのボイラに対しては,まだ脱酸素処理が必要とされ,ヒドラジンの使用も続いて
いるが,ヒドラジンに代わる溶存酸素の還元除去物質(脱酸素剤)として,この規格で規定している亜硫
酸ナトリウムのほか,この規格では規定しないが,既に糖類,グルコン酸塩,タンニン酸塩などを広く使
用し,また,アスコルビン酸,エリソルビン酸及びその塩に加えて数種の脱酸素性のアミンを低圧ボイラ
から高圧ボイラにまで広く使用されている。これらの処理の中には,ボイラ内の鋼材表面に綿密な皮膜を
形成し,酸素などの腐食因子を遮断することで防食する皮膜処理方法も行われている。ただし,脱酸素処
理ではないので,主蒸気がもち込む酸素による腐食を防止する処理を併用する必要がある。
これらのヒドラジンを代替する物質については,それぞれの物質の酸素を除去又は腐食を防止する性能
に加えて,使用に伴う化学反応又は熱分解によって発生する化合物の種類,それらの給水,ボイラ水及び
蒸気の質への影響,挙動なども理解したうえで使用するのが望ましい。

74
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
B.9
亜硫酸イオン(SO32−)
亜硫酸イオンは,アルカリ処理,及びりん酸塩処理を行っているボイラの溶存酸素を除去するために,
亜硫酸塩を脱気器以降の給水系統又はボイラに添加したとき,ボイラ水中に存在する。添加剤には,一般
にはナトリウム塩を用いる。ナトリウム塩には無水物と七水和物とがあるが,ボイラの水処理には無水物
を用いることが多い。亜硫酸イオンはヒドラジンと相違して,常温でも脱酸素効果が著しいので,脱気器
以前の系統での脱酸素にも効率よく使用できる。ただし,ボイラでの濃縮に注意する必要がある。
溶存酸素と亜硫酸ナトリウムとの反応は,亜硫酸ナトリウム1 mol(126.04 g)と溶存酸素0.5 mol(16.00
g)とが式(B.10)に示すように反応する。したがって,溶存酸素1 mgに対し亜硫酸ナトリウム7.9 mgの割
合で反応するが,実際には亜硫酸イオンとして一定過剰量がボイラ水中に存在するように亜硫酸ナトリウ
ムを添加する。
Na2SO3+21O2 → Na2SO4 ····················································· (B.10)
ヒドラジンは溶存酸素と反応して窒素と水とに分解するが,亜硫酸ナトリウムの場合には,硫酸ナトリ
ウムに変化するので,ボイラ水中の溶解性蒸発残留物の濃度が上昇する。
また,亜硫酸イオンは高温で,自己分解して二酸化硫黄(SO2)又は硫化水素(H2S)を生成し,復水系
統のpHの低下による腐食又はボイラへの再流入による腐食を生じるので,過剰注入を避けるとともに分
解反応が著しくなる圧力5 MPa以上のボイラには使用せず,ヒドラジンだけを用いるようにする。
B.10 銅・鉄
銅・鉄などの重金属元素の濃度は,全量を示す。これは,JIS K 0102 [6],JIS K 0101 [7]及びJIS B 8224
では金属元素(アルカリ金属元素は除く。)の試験は,その全量を定量することを規定しているため,試験
結果に“全”を付けなくても十分に理解できるので,“全”は省略した。そのため,溶存状態の金属元素を
試験した場合には,接頭語に“溶存”を付けて表示する。
ボイラ水及びボイラの給水中では,アルカリ金属元素はイオン状で存在するが,アルカリ金属元素以外
の金属元素はイオン状のほか,酸化物,水酸化物,りん酸塩,有機物との錯体などの複雑な形態で,かつ,
不均一の状態で存在する。
B.11 酸消費量
酸消費量は,次の二つに区分する。
a) 酸消費量(pH 8.3) 酸消費量(pH 8.3)は,試料のpHをpH 8.3まで中和するのに要する水素イオン
の量(酸の量)を,試料1 Lについてのmmol数で表すか又は水素イオン(酸)に相当する炭酸カル
シウム(CaCO3)の量に換算して,試料1 Lについてのmg数で表す。
ボイラ水中には炭酸塩,炭酸水素塩,りん酸塩,水酸化物などによるアルカリ分が存在するので,
これらの量を知るために酸消費量(pH 8.3)を測定する。
酸消費量(pH 8.3)では水酸化物,炭酸塩の21量,りん酸塩の31量,けい酸塩などによるアルカリの
分含量を知ることができる。
b) 酸消費量(pH 4.8) 酸消費量(pH 4.8)は,試料のpHをpH 4.8まで中和するのに要する水素イオン
の量(酸の量)を,試料1 Lについてのmmol数で表すか又は水素イオン(酸)に相当する炭酸カル
シウム(CaCO3)の量に換算して,試料1 Lについてのmg数で表す。
酸消費量(pH 4.8)では水酸化物,炭酸塩,炭酸水素塩,りん酸塩の32量,けい酸塩などによるアル
75
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
カリの分含量を知ることができる。
なお,天然水はpHが7未満の中性であるが,炭酸水素イオンが存在するためpHをpH 4.8まで中
和するのに要する酸消費量が存在する。
B.12 塩化物イオン(Cl−)
塩化物イオンは,ボイラで加熱濃縮しても分解及び沈殿物を生成せず,ボイラ水中でイオン状で存在す
る。そのため,給水の塩化物イオンの濃度及びボイラ水の塩化物イオンの濃度を定量すると,ボイラ水の
濃縮度が推定できる。塩化物イオンの定量は,ボイラ水の濃縮の指標になるので,ボイラ水の水質の管理
値の一つになっている。
なお,塩化物イオンの濃度が上昇すると,鋼面の酸化鉄の防食皮膜の安定性を阻害するので,ボイラの
形式及び圧力区分によってボイラ水中の塩化物イオンの濃度について管理値を定めている。
B.13 りん酸イオン(PO43−)
アルカリ処理及びりん酸塩処理を適用しているボイラ水中に存在する。りん酸イオンは,ボイラの腐食
防止の機能,並びに丸ボイラ及び特殊循環ボイラで硫酸カルシウムなどの硬質のスケールの付着を防止す
る機能がある。
ボイラ水中のりん酸イオンの濃度は,ボイラの形式,圧力区分及びボイラ水の処理方式(アルカリ処理
及びりん酸塩処理)によって管理値を定めている。
なお,ボイラ水中のりん酸イオンはイオン状で溶存しているものを対象とし,カルシウムなどと結合し
た懸濁状態のものは除外する。
りん酸イオンは,アルカリ性ではアルカリ金属元素以外の金属元素と反応して懸濁状のりん酸塩の沈殿
を生じる。
りん酸塩は,一般にはオルトりん酸塩(Na3PO4,Na2HPO4など)を用いるが,縮合及び重合りん酸塩を
用いることもある。これは,縮合及び重合りん酸塩がアルカリ溶液中で加水分解(アルカリを消費して)
してオルトりん酸塩に変わる性質があるので,この性質を利用して丸ボイラなどでボイラ水のアルカリ成
分の濃度の調節に用いることがある。
近年,閉鎖性水域での富栄養化の概念からりんの排水規制が強化され,ボイラ水処理においても,りん
を使用しない処理が年々増加の傾向となっている。
B.14 シリカ
天然水中のシリカは,イオン状,コロイド状及び懸濁状の三つの形態で存在する。イオン状のシリカは
pH 1.1〜1.6で七モリブデン酸六アンモニウムと反応して黄緑のヘテロポリ酸(ドデカモリブドけい酸)を
生じる。
コロイド状のシリカは,弱アルカリ性で加熱するとイオン状シリカに変わる。肉眼では透明でコロイド
粒子は確認できない。
懸濁状のシリカは,微細の土壌成分(不溶性のけい酸塩),微生物(けい藻類)などの濁り成分中のシリ
カである。
全シリカは,これら三つの形態のシリカの合量をいう。規格本体のシリカはイオン状のシリカの濃度を
示している。ボイラ水はアルカリ性で,かつ,高温であるため,コロイド状及び懸濁状のシリカは加水分
解して,イオン状のシリカに変わる。したがって,ボイラ水中のシリカの濃度を,ボイラ給水中のシリカ
76
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
の濃度と濃縮倍数との関係(給水量及びブロー量)から見た場合,濃縮倍数が低いにもかかわらず,ボイ
ラ水中のシリカの濃度が高いのは,コロイド状及び懸濁状のシリカの混入によるものである。
なお,懸濁状のシリカは凝集沈殿・ろ過処理で除去することができるが,コロイド状のシリカを凝集さ
せるのは難しい。また,イオン状のシリカは強塩基性陰イオン交換樹脂を用いたイオン交換処理で除去で
きる。次に詳述する。
a) 低圧ボイラでのシリカ 我が国の天然水のシリカの濃度は高いので,原水及び軟化水をボイラの給水
としている丸ボイラ,特殊循環ボイラ及び低圧水管ボイラの場合には,ボイラ水中のシリカの濃度が
上昇しやすい。シリカは比較的溶解度が小さいため,シリカの濃度が高くなるとボイラドラム及び水
管に硬質のスケールが付着する。
シリカのスケールの生成を防止するには,アルカリを加えて式(B.11)に示すように,シリカをメタ
けい酸イオンの形態になるようにボイラ水の酸消費量(pH 8.3)を調節する。
SiO2+2 NaOH → Na2SiO3+H2O ············································ (B.11)
式(B.11)からシリカ1 molと水酸化ナトリウム2 molとの割合で反応するので,シリカ1 mgに対し
水酸化ナトリウム1.33 mgが必要で,炭酸カルシウムの相当量に換算すると1.66 mgになる。すなわ
ち,シリカの濃度に対し酸消費量(pH 8.3)の値を1.7倍(1.66≒1.7)以上に保つことが必要になる。
ボイラの形式及び圧力によって酸消費量(pH 8.3)の管理値を決めているが,ボイラ水中の酸消費
量(pH 8.3)の成分が,水酸化ナトリウムだけの場合は,この管理値に7.11を乗じた値がボイラ水中の
シリカの濃度の上限とみなしてシリカの濃度を調節する。したがって,ボイラ水中の水酸化ナトリウ
ム濃度を測定するためには水酸化物イオンを定量し求める(JIS K 0101を参照)ことになるが,この
方法はボイラ水のようにシリカの濃度が高い場合には誤差が大きいため,ボイラ水への適用が困難で
ある。そのため,実際にはこの方法を用いないで酸消費量(pH 8.3)の濃度で管理する。
B.11 a)で記載したように,ボイラ水の酸消費量(pH 8.3)は,水酸化物イオン,炭酸イオン,りん
酸イオンなどのアルカリ成分を含むが,これらの中でシリカに対して有効に作用するのは水酸化物イ
オンだけであるので,シリカの濃度が高い補給水を給水する場合には,式(B.11)に示したようにシリ
カをメタけい酸イオンとして保つことが困難になるので,ボイラ水のシリカの濃度に注意が必要であ
る。
ボイラ水のシリカの濃度の概略を知るには,補給水中のシリカ,塩化物イオン及びボイラ水中の塩
化物イオンをそれぞれ定量し,ボイラ水の濃縮倍数を求めればボイラ水中のシリカの濃度が推定でき
る。
b) 高圧ボイラでのシリカ 高圧ボイラでは,ボイラ給水としてイオン交換水を用いるので,ボイラ水中
のシリカの濃度を低く保つことができるが,それぞれの圧力区分ごとにシリカの管理値を定めている。
これは,シリカが蒸気中へ溶解する性質があるので,蒸気中への溶解量をタービンの効率低下を引き
起こさない程度以下に少なくするためである。すなわち,シリカの蒸気中への溶解度は,圧力の上昇
とともに指数関数的に増加する(特に,圧力6 MPa以上から著しくなる。)。この現象をシリカの選択
的キャリオーバという。蒸気へのシリカの分配係数の関係を図B.1 [8], [9]に示す。また,圧力が一定な
場合は,ボイラ水中のシリカの濃度の増加,pHの低下とともに蒸気中へのシリカの溶解量が増加する。
キャリオーバしたシリカは,タービン低圧部で溶解度以上の過飽和の状態になると,シリカスケール
として析出し,タービンの効率低下を引き起こす。これを防止するために高圧ボイラでは,蒸気中の
シリカの濃度がSiO2: 20 μg/L以下になるようにボイラ水中のシリカの濃度を調節する。イオン交換水
を使用する循環ボイラの場合は,ドラム中のシリカが圧力に応じて図B.1に示す分配係数を乗じた割
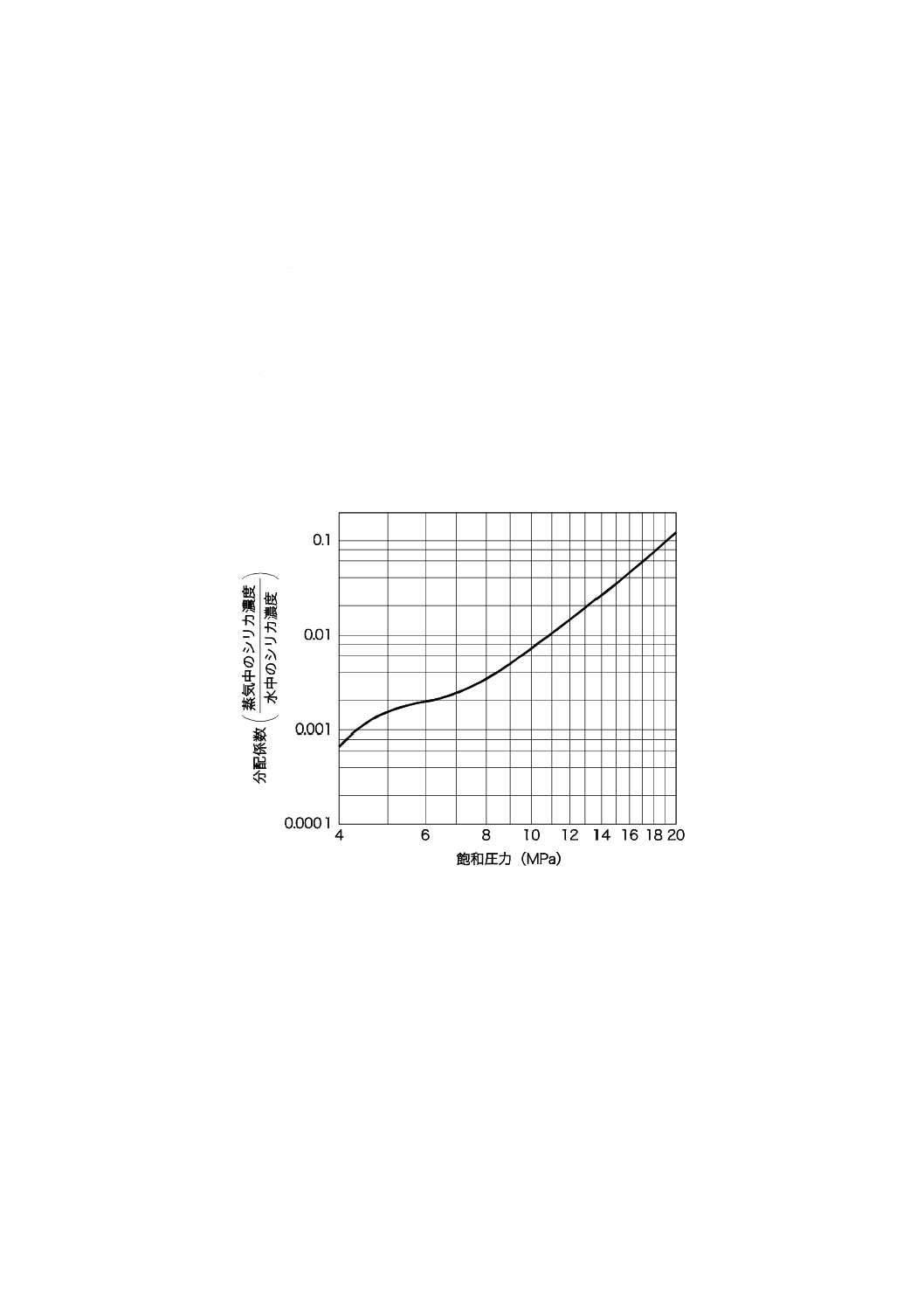
77
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
合で蒸気中に移行する。本体の各圧力区分ごとにボイラ水中のシリカの濃度は,図B.2 [10]に示すよう
にpHを上昇させれば基準値をある程度大きくすることは可能であるが,その影響は圧力に比べて小
さいこともあり,下限側のpHを考慮し基準値を設定した。一方,貫流ボイラの場合は,給水中のシ
リカがほぼそのまま蒸気中に移行するため,セパレータのないボイラ,又は圧力15 MPa以上のボイ
ラに関しては一律にSiO2: 20 μg/Lと設定した。蒸気中のシリカの濃度をSiO2: 20 μg/Lにするためのボ
イラ水中のシリカの濃度,圧力,及びpHの関係を図B.3 [11]に,また,シリカの過熱蒸気への溶解度
を図B.4 [12]に示す。
シリカの過熱蒸気への溶解度を図B.4に示したが,蒸気中にほかの不純物,例えば,ナトリウム塩
などが存在するとシリカと結合して複雑な化合物を生成し,タービンの,中圧部・高圧部に析出する
ことがあるので注意が必要である。
なお,飽和・過熱蒸気のシリカ濃度としては,前述のような蒸気への溶解のほかに,水滴同伴に伴
うメカニカルキャリオーバによる分も考慮する必要があり,このため,運用上は,ボイラごとに水滴
同伴に伴うメカニカルキャリオーバを実測によって把握し,その分,管理値よりも低く保つように維
持することが望ましい。
図B.1−蒸気へのシリカの分配係数[8], [9]
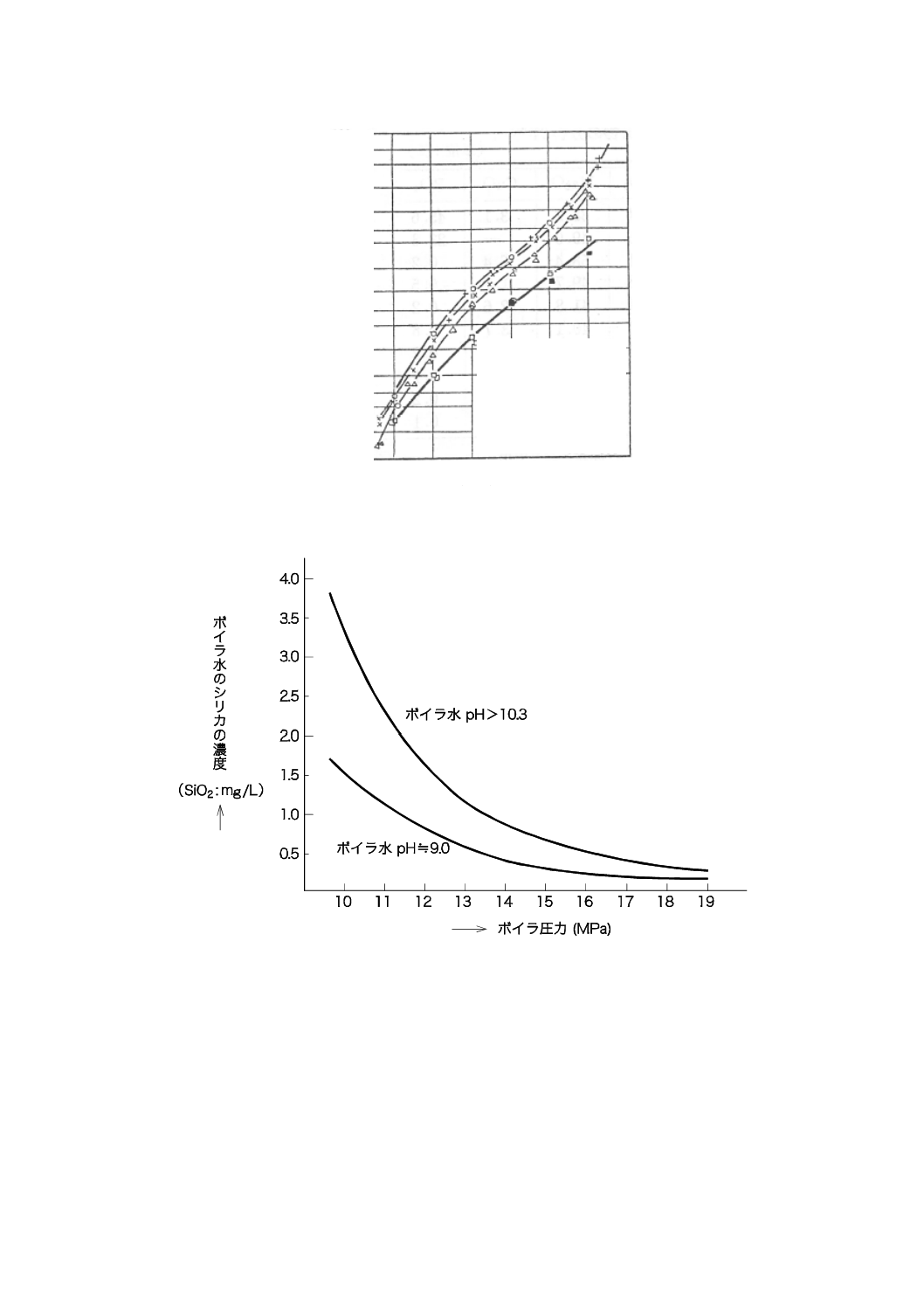
78
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
水
中
の
シ
リ
カ
に
対
す
る
蒸
気
中
の
シ
リ
カ
比
率
(
%
)
0
3.4
6.9
10.3 13.8 17.2 20.7 24.1
圧力(MPa)
図B.2−圧力,pH及び水中シリカの濃度が蒸気中のシリカ比率に及ぼす影響[10]
図B.3−蒸気中のシリカの濃度をSiO2: 0.020 mg/Lとする
ボイラ水のシリカの濃度,圧力及びpHとの関係[11]
水質条件
平均のpH
シリカppm
○
7.8
114-151
+
9.0
12-24
× 10.3
50-76
△
11.3
107-194
□ 12.1
119-172
■ 12.1
622-996
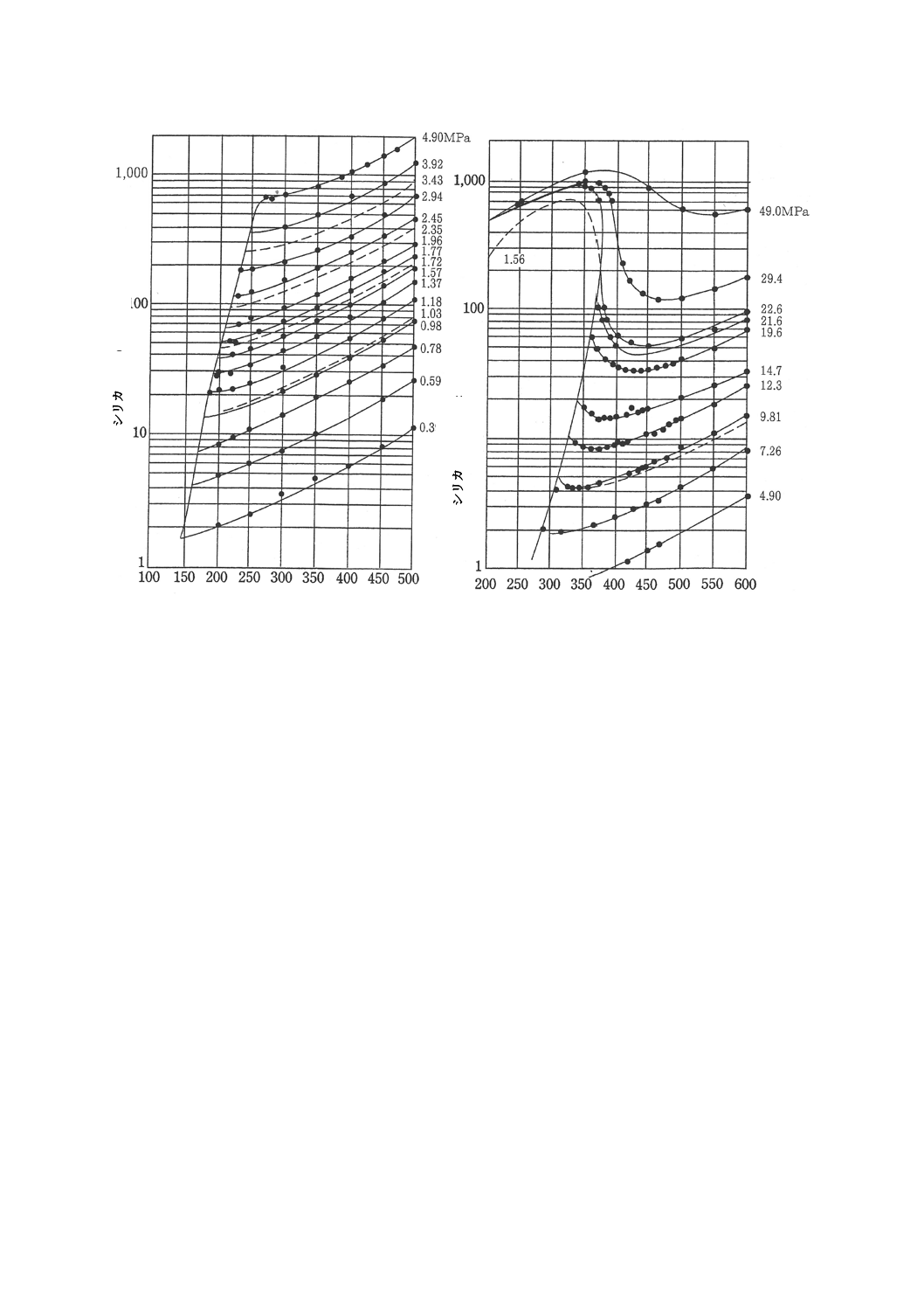
79
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
蒸気温度(℃)
蒸気温度(℃)
(蒸気圧力0.39 MPa〜4.90 MPa)
(蒸気圧力4.90 MPa〜49.0 MPa)
図B.4−シリカの過熱蒸気への溶解度[12]
B.15 全蒸発残留物
全蒸発残留物は,水を蒸発乾固したときに残留する物質の質量を,試料1 Lについてのmg数で表した
ものである。
全蒸発残留物は,水中の溶解性蒸発残留物と懸濁物との合量である。したがって,懸濁物を含まない試
料の場合には,全蒸発残留物は溶解性蒸発残留物と等しいことになり,あらかじめ電気伝導率との相関関
係を求めておけば,電気伝導率を測定して,全蒸発残留物の値を推定することが可能になる。
原水及び軟化水を給水としているボイラのボイラ水は懸濁物を含むので,電気伝導率と全蒸発残留物と
の相関関係を求めることが困難である。
全蒸発残留物の濃度が高くなると水滴同伴,及びホーミングによるキャリオーバが増加する原因になる。
B.16 ナトリウム
アルカリ処理及び低濃度水酸化ナトリウム処理を適用しているボイラにおいては,強塩基性である水酸
化ナトリウムがボイラ水中に存在する。ボイラ水中の水酸化ナトリウム濃度が高いほど,ボイラの高熱負
荷部に水酸化ナトリウム成分が濃縮し,局部的に高アルカリ条件を形成し,激しい減肉(アルカリ腐食)
が進行しやすいため,ドラムボイラ水中のナトリウム濃度を適切な範囲に管理する必要がある。
蒸気系にナトリウムが混入した場合,塩基性のナトリウム塩が凝縮域に溶解・濃縮して構成材料の腐食
(応力腐食割れなど)の原因となるため,乾湿交番域をもつ復水タービンに通気する蒸気に対して,ナト
リウムの混入を極力防止することが重要である。中でもボイラ水の処理にアルカリ処理及び低水酸化ナト
シ
リ
カ
溶
解
度
(S
iO
2
:
μ
g
/L
)
シ
リ
カ
溶
解
度
(S
iO
2
:
m
g
/L
)
80
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
リウム処理を適用しているユニットでは,ボイラ水のキャリオーバによって強塩基性の水酸化ナトリウム
として混入する割合が高く,水酸化ナトリウムは濃縮した場合の腐食性が大きい上,酸電気伝導率では検
出できないことから,蒸気中のナトリウム濃度の管理が重要である。
強塩基性のナトリウム塩の濃縮による機器の損傷トラブルを防止するための対策として,ボイラ水処理
薬剤の注入濃度の適切な管理,及び復水脱塩装置・補給水処理装置からのナトリウム漏えい防止が重要で
ある。

81
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書C
(参考)
補給水の水質
C.1 一般
補給水とは,火力発電プラントの外部から給水の一部として補給する水をいい,補給水処理とは,その
ボイラに補給する水を,ボイラの給水及びボイラ水の水質に適合させるために行う処理である。補給水の
処理方法には,凝集沈殿,凝集加圧浮上,凝集ろ過,ろ過,吸着,イオン交換,膜浸透,電気式脱塩,脱
気,蒸留などの種々の方法があり,処理目的に応じてこれらの方法を単独又は幾つかを組み合わせて用い
る。
補給水の種類は,原水,軟化水,及びイオン交換水に分類する。原水とは水道水,工業用水,地下水,
河川水,湖沼水などである。軟化水とは原水を軟化装置(陽イオン交換樹脂を充塡した)で処理したもの
である。イオン交換水とは,陽イオン交換樹脂と陰イオン交換樹脂とを用いたイオン交換樹脂で精製した
水である。
なお,船用,低圧ボイラなどにおいて要求水質を満足する場合は,造水器で精製した水(蒸留水),又は
逆浸透膜装置及び電気式脱塩などで処理した水もイオン交換水として同様に取り扱うことができる。ただ
し,逆浸透膜装置においては,脱塩率が低いタイプ(ルーズROとも呼ぶ。)もあるため,取扱いには注意
が必要である。
C.2 管理値の例
参考として,イオン交換水を使用する場合の水質の設定値例を表C.1及び表C.2に示す。
表C.1−火力発電プラント補給水の水質例
プラント
又は会社
電気伝導率
シリカ
溶存酸素
A
≦0.05 mS/m
(≦0.5 μS/cm)
≦0.02 mg/L
≦0.3 mg/L
B
≦0.05 mS/m
(≦0.5 μS/cm)
≦0.015 mg/L
≦0.3 mg/L
C
≦0.125 mS/m
(≦1.25 μS/cm)
≦0.01 mg/L
≦0.3 mg/L
D
≦0.05 mS/m
(≦0.5 μS/cm)
≦0.01 mg/L
設定値なし
E
≦0.1〜0.05 mS/m
(≦1〜0.5 μS/cm)
≦0.015 mg/L
設定値なし
F
≦0.15 mS/m
(≦1.5 μS/cm)
≦0.01 mg/L
設定値なし
又は
≦0.3 mg/L
G
≦0.1 mS/m
(≦1 μS/cm)
≦0.02 mg/L
設定値なし

82
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
表C.2−船用補給水の水質例 造水器(蒸留水)
船型式
塩分濃度
ディーゼル船
≦10 mg/L
蒸気タービン船
≦1.5 mg/L
C.3 水質に関する留意事項
C.3.1 有機体炭素(TOC)
有機体炭素(TOC)とは,水中に存在する有機物中の炭素をいう。ボイラ給水,及びボイラ水質共に規
定値として定めていないが,トラブルの報告例もあるため原因及び暫定目標値について記載する。
ボイラ水の処理方式として,りん酸塩処理又は揮発性物質処理を適用する場合に,特に,留意が必要で
ある。アルカリ処理であれば基本的に問題はない。水管ボイラでも,事業用発電ボイラと異なり,給水へ
の復水回収率が様々な産業用発電ボイラでは補給水率が高い場合があり,補給水中の有機物のもち込み量
が多くなることがある。その場合は,高温のボイラ水中での熱分解などによって低分子の有機酸成分が発
生しボイラ水のpHを低下させるなどの影響を及ぼす。ボイラ水のpH緩衝能力が小さい揮発性物質処理又
はりん酸塩処理の場合に顕著である。特に,pH緩衝能力が小さい揮発性物質処理では有機物のもち込みに
留意が必要である。また,揮発性物質処理よりもpH緩衝能力が大きいりん酸塩処理の場合でも,りん酸
イオンの保持濃度をより低く規定している圧力の高いボイラほどpHの緩衝能力が小さくなり,有機物も
ち込みの影響は大きくなる。これを防ぐためには,補給水処理装置出口で有機体炭素(TOC)C: 0.2 mg/L [1]
以下であることが望ましい。また,産業用ボイラで,蒸気タービンから抽気した蒸気をプロセスで消費す
る,又はその復水を回収しないなどの理由で復水回収率が低く,補給水率が高い場合はC: 0.1 mg/L [1]以下
であることが望ましい。
なお,補給水処理プロセスの前処理としてイオン交換処理を実施しても除去し難い有機体炭素成分であ
るため,そのほとんどは溶存有機体炭素(DOC)が主成分と考えられるが,補給水処理装置から僅かに漏
えいするその他の有機体炭素成分と併せて,分析方法としてはTOCを測定すればよい。
新規に補給水処理装置を設置する場合にTOCの値を具体的に設定する場合は,十分な検討を行う必要が
ある。場合によっては実際に使用する原水を用いてラボテストなどによる評価を行い,想定する補給水処
理装置システムの妥当性について検討を行う。その場合は季節変動を考慮した複数回の確認が必要である。
C.3.2 軟化水,塩化物イオン及び硫酸イオン
軟化水を補給水とするボイラ水質には,管理項目として塩化物イオンを設定する。塩化物イオンは,鋼
面の酸化鉄の防食被膜の安定性を阻害するため,なるべく低濃度に維持する必要がある。硫酸イオンにも
同様の作用があるため,なるべく低濃度に維持する必要がある。軟化水補給水中の塩化物イオン,硫酸イ
オン濃度を把握することでボイラ水中の塩化物イオン濃度の測定から,硫酸イオン最大濃度が推定できる。
よって,定期的に分析を行い記録することが望ましい。
83
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書D
(参考)
水質管理項目が管理値を逸脱した場合の一般的対処方法
D.1 一般
通常運転時の水質管理は,復水,給水,ボイラ水及び蒸気のサンプル水ごとに水質管理項目及び管理値
を設定して実施している。このうち,計器測定については,CRT又は記録計に表示できるようになってお
り,異常時は警報発信又は運転員による監視によって確認できる。
水質管理項目が管理値を逸脱した場合には,一般に次の処置を行う。
なお,水質管理は長期間の傾向管理が重要なため,監視計器で確認できる水質管理項目,鉄・銅など化
学分析によって確認する項目,定期点検時の機器内部点検結果(タービン翼の付着物など)を総合的に判
断し,最適な水質管理の確立及び安定運転に努めることが必要である。
D.2 pHが管理値を逸脱した場合の対処方法[1]
給水のpHが管理値より低い又は高い場合は,給水処理薬品(アンモニア,ヒドラジンなど)の注入量
の不足又は過剰が考えられる。薬品注入ポンプ動作,バルブ操作(開閉),注入量,薬品タンク濃度・充塡
薬品について確認する。
不純物混入によって,給水又はドラム水の電気伝導率が高い場合,電気伝導率制御による薬品注入シス
テムが動作せずに,薬品を注入できないケースもある。また,監視計器(pH計)の異常も考えられるので,
他のpH計による相互確認を行う。
水管ボイラにおいて,ボイラ水のpH異常は,給水の事例に加えて,海水漏えいによるpH低下,又は,
りん酸塩のハイドアウトリターンによるpH低下の場合に確認できる[2]。
りん酸塩のハイドアウト現象は,りん酸ナトリウムの溶解度が比較的小さく,しかも高温になるほど小
さくなることによって生じる現象である。すなわち,ボイラの圧力が上昇し,管壁温度が高くなると,水
中のりん酸ナトリウムが管壁に析出し,液系から失われて,ボイラ水中のりん酸イオンの濃度が低くなる
現象で,図D.1に示すように[3],ボイラ水のpH低下の要因となる事例がある。ボイラ水管内に付着したス
ケールが関与する場合もあり,対策としては,使用するりん酸ナトリウムのNa/PO4モル比の調整(2.5〜
2.8),及びボイラスケール除去のための定期的な化学洗浄が有効である。
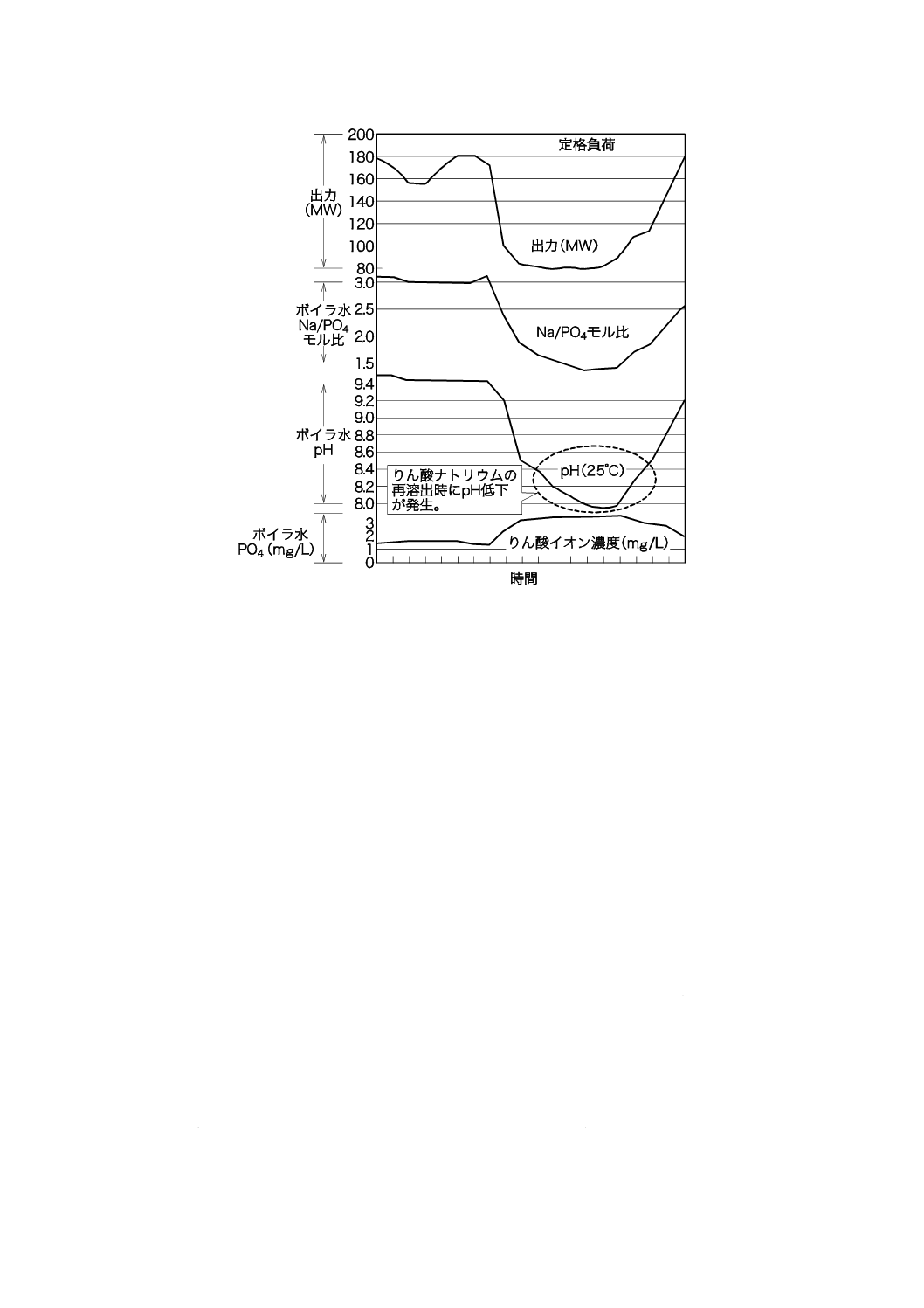
84
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
図D.1−りん酸塩のハイドアウト現象の一例[3]
D.3 溶存酸素濃度が管理値を逸脱した場合の対処方法
給水の溶存酸素濃度が管理値を逸脱する要因としては,脱気器の性能低下,復水器の真空低下,復水ポ
ンプ又はヒータドレンポンプからの空気混入,海水漏えい,ヒドラジン注入量の低下が考えられる。脱気
器の性能低下は,加熱蒸気の供給量低・バルブ閉,大気(又は復水器へ接続の)放出弁の閉など機械的な
要因であるため,プラント停止時に補修する必要がある(復水器の真空低下及び復水ポンプ又はヒータド
レンポンプからの空気混入についても同様。)。
溶存酸素濃度高の場合,系統機器に銅合金を含むと,給水中の銅濃度が上昇することがあるため,化学
分析によって銅濃度の挙動を確認する。
酸素処理(CWT)運用時に溶存酸素濃度低となる場合は,酸素注入装置の異常が考えられるため,速や
かにAVT(ヒドラジン不使用)に切り替え,補修する。また,監視計器(溶存酸素計)の異常も考えられ
るので,化学分析による相互確認を行う。
D.4 シリカ濃度が管理値を逸脱した場合の対処方法
蒸気中のシリカ濃度は,SiO2: 0.02 mg/L以下であれば,タービン翼にほとんど付着物を生成しないこと
が経験的に知られている。蒸気中のシリカ濃度管理は,ボイラ水中のシリカ濃度によって間接的に管理で
きるため,常時はボイラ水のシリカ濃度を測定し,蒸気中のシリカ濃度を管理する。ボイラ水のシリカ濃
度の許容値は,ボイラの圧力区分によって設定する。
蒸気中又はボイラ水のシリカ濃度が管理値を逸脱した場合(シリカ高)は,ボイラの連続ブローを実施
し,シリカ濃度の低減を行う。また,監視計器(シリカ計)の異常も考えられるので,化学分析による相
互確認を行う。
85
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
D.5 酸電気伝導率が管理値を逸脱した場合の対処方法
酸電気伝導率の管理値は,復水・給水及び蒸気に設定する。復水・給水の酸電気伝導率が上昇する要因
としては,海水漏えいが考えられる。
起動時には,補給水に含まれる炭酸ガスの影響で,酸電気伝導率が上昇することがあるので,酸電気伝
導率上昇時には,塩化物イオンの分析を行い,海水漏えいの有無を確認する。
蒸気の酸電気伝導率が上昇する要因としては,海水漏えいのほかに,補給水中の全有機炭素(TOC)又
はヒドラジン代替薬品の分解によって生成する有機酸又は炭酸ガスの影響,汽水分離性能の低下,蒸気ド
ラムの水位の変動が考えられる。薬品注入時には,酸電気伝導率の基準を逸脱しない注入要領とする必要
がある。また,監視計器(酸電気伝導率計)の異常も考えられるので,電気伝導率計の入口に設置するイ
オン交換樹脂のイオン交換容量が飽和していないか,pH計測による確認を行う(飽和している場合は,試
料水に復水・給水のアンモニアが含まれており,pH 6以上を示す。)。
D.6 復水器海水漏えい時の対処方法[4]
復水器海水漏えい時の対処法方は,次による。
a) 海水漏えいによる障害 復水器の冷却水として海水を使用する場合,復水器管又は管板部の腐食・損
傷,復水ポンプの腐食による海水混入,及び復水器へ回収するドレンタンクへの海水又は不純物の混
入によって,次のような障害が発生する場合がある。
1) カルシウム,マグネシウム分によるボイラ水管内でのスケール生成,熱伝達阻害。
2) 塩化マグネシウムによるボイラ水のpHの低下及び腐食。
MgCl2+2H2O → Mg(OH)2↓+2HCl ·········································· (D.1)
3) 塩類などのキャリオーバによる過熱器管,タービン翼などの汚染及び腐食。
4) 過熱低減器用スプレー水中の塩化物イオンによるステンレス鋼の腐食(応力腐食割れ)。
b) 海水漏えいの検知 海水の漏えいは,まず復水器ホットウェル(検塩計),復水(ポンプ出口),給水,
ボイラ水の酸電気伝導率又は電気伝導率の上昇によって検知することができる。また,電気伝導率が
上昇したときに,塩化物イオンの分析を行う。復水及び給水の酸電気伝導率による海水漏えいの判定
基準の一例を,表D.1に示す。
表D.1−海水漏えいの判定基準の一例(復水,給水)
酸電気伝導率
mS/m(μS/cm)
塩化物イオン
mg/L
正常値
0.03以下(0.3以下)
0.05以下
要監視
(警報値)
0.03〜0.05(0.3〜0.5)
微量漏えい
0.05〜0.2(0.0〜2)
0.05〜0.2
大量漏えい
0.2以上(2以上)
0.2以上
c) 海水漏えい時の対処方法 漏えいを検知した場合には,過熱器及び再熱器スプレー水を停止する。大
量漏えいと判断できる場合は,速やかにプラントを停止することが必要である。
1) 水管ボイラ 海水漏えいによる障害を防止するための処置として,水管ボイラでは,海水の漏れ量
及びボイラ水の水質の変化に応じて,ボイラ水のブロー,硬度除去剤であるりん酸ナトリウムの注
入,ボイラ水のpH調整などを速やかに行う。また,微量漏えいであっても,りん酸塩注入時に,
ボイラ水のブローが最大で,ボイラ水の水質が悪化(pH 8.5以下)する場合は,速やかにプラント
86
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
運転を停止する。
2) 貫流ボイラ 復水脱塩装置をH型運用で,全量通水とする。また,微量漏えいであっても,復水脱
塩装置が許容できる漏えい量を超えた場合は,速やかにプラント運転を停止する。
87
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
参考文献
附属書A
[1] 栗田工業薬品ハンドブック編集委員会編:薬品ハンドブック(1989),p.92
[2] 栗田工業薬品ハンドブック編集委員会編:薬品ハンドブック(1989),p.84
[3] G.Dnath, G.H.Heitmann, H.J.Messer, M.Schott (1977): Ermittlung der Verteilungskoeffizentin flüchtiger
Alkalisierungsmittel zwischen Dampf und Wasser deren Bedeutung für das Korrosionsverhalten der
Werkstoffe im Wasser-Dampfkraislauf von Kraftwerken: Jahrbuch VOM WASSER 49.Bd., S.221〜243, Ver
lag Chemie
[4] Herbert H.Uhlig (1948): Corrosion Handbook, P.525 (Curve by Partridge and Hall, based on data of Berl and
Taack)
[5] K. Viedem (1977): Proc. of 7th Scand, Congr., 444
[6] M. Pourbaix (1966): Atlas of Electrochemical Equilibria in Aqueous Solutions
[7] H. Bohnsack (1985): IAPWS. Release on solubility of Magnetite in Water and Aqueous Solutions of Acid and
Alkali
[8] 湯浅真(2001):表面科学 Vol.22,No.2,1: p.38
[9] V. M. Marcy, S. L. Halstead (1964); Combustion, Jan., 45
[10] 坂本惇,ボイラ研究,191(1982)p.19-22. ボイラ研究,198(1983)p.22-25. ボイラ研究,205(1984)
p.17-22.
[11] W. C. Schroeder, et al (1937); J. Amer. Chem. Soc., 59, 1783
[12] S. F. Whirl, et al (1942); Engr. Soc. of Western Pa. Water Conference, Proceedings, 45
[13] P. V. Balakrishnan (1977); The Canad., J. of Chem. Engr. 55, 592
[14] S. L. Goodstine (1974), “Vaporous Carryover of Sodium Salts in High Pressure Steam”, Presented at
American Power Conf., Chicago, II, April 1974
[15] 阿部博志,渡邊豊(2012),表面技術,Vol.63,No.5,p.290
[16] 広田守ほか(2011),火力原子力発電 Vol.62 No.7,p.491-498
[17] W.Sugino, T.Ohira, N.Nagata, A.Abe and H.Takiguchi (2009): Proc. Symposium on Water Chemistry and
Corrosion in Nuclear Plants in ASIA 2009, p.84
[18] B. Dooley et al (1994). The International Water Conference, 55th Annual Meeting, Engineersʼ Society of
Western Pennsylvania, Pittsburg, October (1994): 454
[19] F.J.Pocock, J.A.Lux and P.V.Seibel: Proc. Am.Power Conf., XXVIII (1966): p.758
[20] 若原高生,ほか(1993):火力原子力発電,44,154
[21] 酸素処理法情報交換委員会(1995年5月):電力中央研究所委員会報告 T94803
[22] IAPWS Technical Guidance Document (2010) “Volatile treatments for the steam-water circuits of fossil and
combined cycle/HRSG power plants”.
[23] VGB Power Tech e.V (2011).: “VGB- standard Feed Water, Boiler Water and Steam Quality for Power
Plants/Industrial Plants”.
[24] VGB Kraftwerkstechnik (1972), 53-2, 167
[25] M.Pourbaix (1966): Atlas of Electrochemical Equilibria in Aqueous Solutions (Pergamon Press)
88
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
[26] 新給水処理研究会(1988):火力原子力発電,39,763及び39,883
[27] 岩堀徹 ほか(1983).:防食技術,Vol.32,No.8,435-441
[28] P.H.Effertz (1978): VGB.KRAFTWERKSTECHNIK 58, 5853
[29] 河合登ほか(1998):火力原子力発電,49-2,193
[30] 若原高生ほか(1994):火力原子力発電,45-9,11008
[31] 椿崎仙市ほか(2012):三菱重工技報Vol.49 No.1
[32] VGB Power Tech e.V (2011).: “VGB- standard Feed Water, Boiler Water and Steam Quality for Power
Plants/Industrial Plants”.
[33] P. Cohen (1989): “ASME Handbook on Water Technology for Thermal Power Plants”, p.557.
[34] M.A.Styrikovich, O.I.Martynova, Z.S.Belova Thermal Engineering, 12, (9), p.115-119.
[35] IAPWS Technical Guidance Document “Procedures for the Measurement of Carryover of Boiler Water into
Steam”, p.11, (2008).
[36] Albert Bursik (2008); Power Plant Chmistry10, (3),.
[37] 日本ボイラ協会編(1984).:“ボイラの水管理”p.79-106,日本ボイラ協会.
[38] IAPWS Technical Guidance Document (2008) “Procedures for the Measurement of Carryover of Boiler
Water into Steam”, p.10.
[39] 小若正倫:防食技術(1971).20,7,p.305-313
[40] 小若正倫(1983).:“金属の腐食損傷と防食技術”,p.96-98,株式会社アグネ
[41] P. Cohen (1989): “ASME Handbook on Water Technology for Thermal Power Plants”, p.847.
[42] IAPWS Technical Guidance Document (2011) “Phosphate and NaOH Treatments for the Steam-Water
Circuits of Drum Boilers of Fossil and Combined Cycle/HRSG Power Plants”.
附属書B
[1] JIS Z 8802:2011(pH測定方法)
[2] P. Cohen: The ASME Handbook on Water Technology for Thermal Power Systems. p.554 (1992)
[3] F.H. Sweeton, R.E. Mesmer, and C.F. Baes: Journal of Solution Chemistry 3 (No.3, March 1974): p.191-214
[4] W.L. Marshall and E.U. Frank: Journal of Physical Chemistry Reference Data 10 (No.2, 1981): p.295-304
[5] JIS B 8224:2005(ボイラの給水及びボイラ水−試験方法)
[6] JIS K 0102:2013(工場排水試験方法)
[7] JIS K 0101:1998(工業用水試験方法)
[8] 日本ボイラ協会編(1984):ボイラの水管理(基礎と実際)p.104(社団法人日本ボイラ協会)
[9] H.E. Homig (1963): Physikochemische Grundlagen des Speisewasserchemie, p.175 (Vukan-Verlan Dr. W.
Clacsen)
[10] E.E. Coulter, E.A. Pirsh & E.J. Wagner, ASTM, Trans., Vol.78, NO.4, 869〜873 (1956)
[11] Grabowski (1950): Current Practice in water treatment technology for high pressure boilers, (Southeastern
Elect. Exchange Eng. And Operation Section Conf. 1950 Atlanta)
[12] R. Feitsma (1961): Mitteilungen Der VGB Heft 72, 170
附属書C
[1] VGB Guideline Guidelines for Feed Water, Boiler Water and Steam Quality for Power Plants/Industrial
Plants VGB-R 450 Le Second Edition 2004
89
B 8223:2015
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書D
[1] 坪谷久男,ほか(1992):火力原子力発電,Vol.13,No.10,p.128
[2] 電力中央研究所:汽力発電所給水処理ハンドブックp.92,p.316(1985)
[3] 水野孝之(1992):火力原子力発電,Vol.43,No.9,p.14
[4] JIS B 8223:1989(ボイラの給水及びボイラ水の水質) 解説p.68