T 6130:2013
(1)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
目 次
ページ
序文 ··································································································································· 1
1 適用範囲························································································································· 1
2 引用規格························································································································· 1
3 用語及び定義 ··················································································································· 2
4 構成及び各部の名称 ·········································································································· 3
5 物理的要求事項 ················································································································ 3
5.1 外観及び清浄度 ············································································································· 3
6 化学的要求事項 ················································································································ 3
6.1 溶出金属の制限 ············································································································· 3
7 針管の要求事項 ················································································································ 4
7.1 材料 ···························································································································· 4
7.2 外観 ···························································································································· 4
7.3 寸法 ···························································································································· 4
7.4 栓刺通針 ······················································································································ 4
7.5 針先 ···························································································································· 4
8 針基の要求事項 ················································································································ 4
8.1 カートリッジシリンジとの適合性······················································································ 4
8.2 受け口深さ ··················································································································· 4
8.3 カラーコード ················································································································ 4
9 針基と針管との接合 ·········································································································· 5
10 生物学的安全性 ·············································································································· 5
11 無菌性の保証 ················································································································· 5
12 エンドトキシン ·············································································································· 5
13 包装 ····························································································································· 5
13.1 一次包装 ····················································································································· 5
13.2 二次包装 ····················································································································· 5
14 表示 ····························································································································· 5
14.1 一次包装 ····················································································································· 5
14.2 二次包装 ····················································································································· 6
14.3 図記号の使用 ··············································································································· 6
附属書JA(参考)JISと対応国際規格との対比表 ······································································· 7
T 6130:2013
(2)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
まえがき
この規格は,工業標準化法第14条によって準用する第12条第1項の規定に基づき,日本医療器材工業
会(JMED)及び一般財団法人日本規格協会(JSA)から,工業標準原案を具して日本工業規格を改正すべ
きとの申出があり,日本工業標準調査会の審議を経て,厚生労働大臣が改正した日本工業規格である。こ
れによって,JIS T 6130:2007は改正され,この規格に置き換えられた。
この規格は,著作権法で保護対象となっている著作物である。
この規格の一部が,特許権,出願公開後の特許出願又は実用新案権に抵触する可能性があることに注意
を喚起する。厚生労働大臣及び日本工業標準調査会は,このような特許権,出願公開後の特許出願及び実
用新案権に関わる確認について,責任はもたない。
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
日本工業規格 JIS
T 6130:2013
歯科用注射針
Sterile dental injection needles for single use
序文
この規格は,2010年に第3版として発行されたISO 7885を基とし,我が国の実情に合わせるため技術
的内容を変更して作成した日本工業規格である。
なお,この規格で点線の下線を施してある箇所は,対応国際規格を変更している事項である。変更の一
覧表にその説明を付けて,附属書JAに示す。
1
適用範囲
この規格は,主として局所麻酔用の歯科用カートリッジ注射筒に装着することを目的とした滅菌済みの
注射針で,そのまま直ちに使用でき,かつ,単回使用する歯科用注射針(以下,注射針という。)について
規定する。
注記 この規格の対応国際規格及びその対応の程度を表す記号を,次に示す。
ISO 7885:2010,Dentistry−Sterile injection needles for single use(MOD)
なお,対応の程度を表す記号“MOD”は,ISO/IEC Guide 21-1に基づき,“修正している”
ことを示す。
なお,平成28年8月31日までJIS T 6130:2007は適用することができる。
2
引用規格
次に掲げる規格は,この規格に引用されることによって,この規格の規定の一部を構成する。これらの
引用規格は,記載の年の版を適用し,その後の改正版(追補を含む。)は適用しない。
JIS G 4305:2012 冷間圧延ステンレス鋼板及び鋼帯
JIS T 0307:2004 医療機器−医療機器のラベル,ラベリング及び供給される情報に用いる図記号
注記 対応国際規格:ISO 15223:2000,Medical devices−Symbols to be used with medical device labels,
labelling and information to be supplied及びAmendment 1(2002)(IDT)
JIS T 0993-1:2012 医療機器の生物学的評価−第1部:リスクマネジメントプロセスにおける評価及
び試験
JIS T 3209:2011 滅菌済み注射針
注記 対応国際規格:ISO 7864:1993,Sterile hypodermic needles for single use(MOD)
ISO 6009:1992,Hypodermic needles for single use−Colour coding for identification
ISO 9626:1991,Stainless steel needle tubing for the manufacture of medical devices及びAmendment 1:2001
ISO 9997:1999,Dental cartridge syringes
2
T 6130:2013
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
3
用語及び定義
この規格で用いる主な用語及び定義は,次による。
3.1
針構成単位(needle unit)
一次包装,針管及び針基(図1参照)。
3.2
有効針(effective needle length)
針管の人に刺通する側の針先から針基までの部分。
3.3
栓刺通針
針管の注射剤容器の栓を刺通する側の部分。
3.4
公称外径
注射針の包装又は容器に表示する針管の外径の寸法。針管が非円筒形の場合は,刃面直前の針管の外径
寸法。
3.5
公称長さ
注射針の包装又は容器に表示する有効針の長さ。
3.6
エンドトキシン試験用水
日本薬局方(以下,“日局”という。)の医薬品各条に規定する“注射用水”又はその他の方法によって
製造した水で,エンドトキシン試験に用いるライセート(LAL)試薬の検出限界で反応を示さないもの。
3.7
硬包装(hardpack)
一次包装の一つで,硬い栓刺通針さや(鞘)及び硬い有効針さや(鞘)で,完成した注射針を密封した
もの(図1参照)。
3.8
軟包装(softpack)
一次包装の一つで,剝せるカバー,軟包装が付いた成型されたプラスチック容器又は軟包装材料に硬い
さや(鞘)で保護した注射針が入たもの。
注記 栓刺通針さや(鞘)は,あるものとないものがある。
3.9
一次包装(primary container)
注射針を直接に覆う包装で,針の無菌性を保持するためのもの。さらに,これを二次包装する場合には,
いわゆる“内袋”に該当する。一次包装には,硬包装又は軟包装がある。
3.10
二次包装(secondary container)
一次包装を直接に覆う包装。通常,一次包装した注射針を複数(例えば,100本)入れた包装。
3
T 6130:2013
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
4
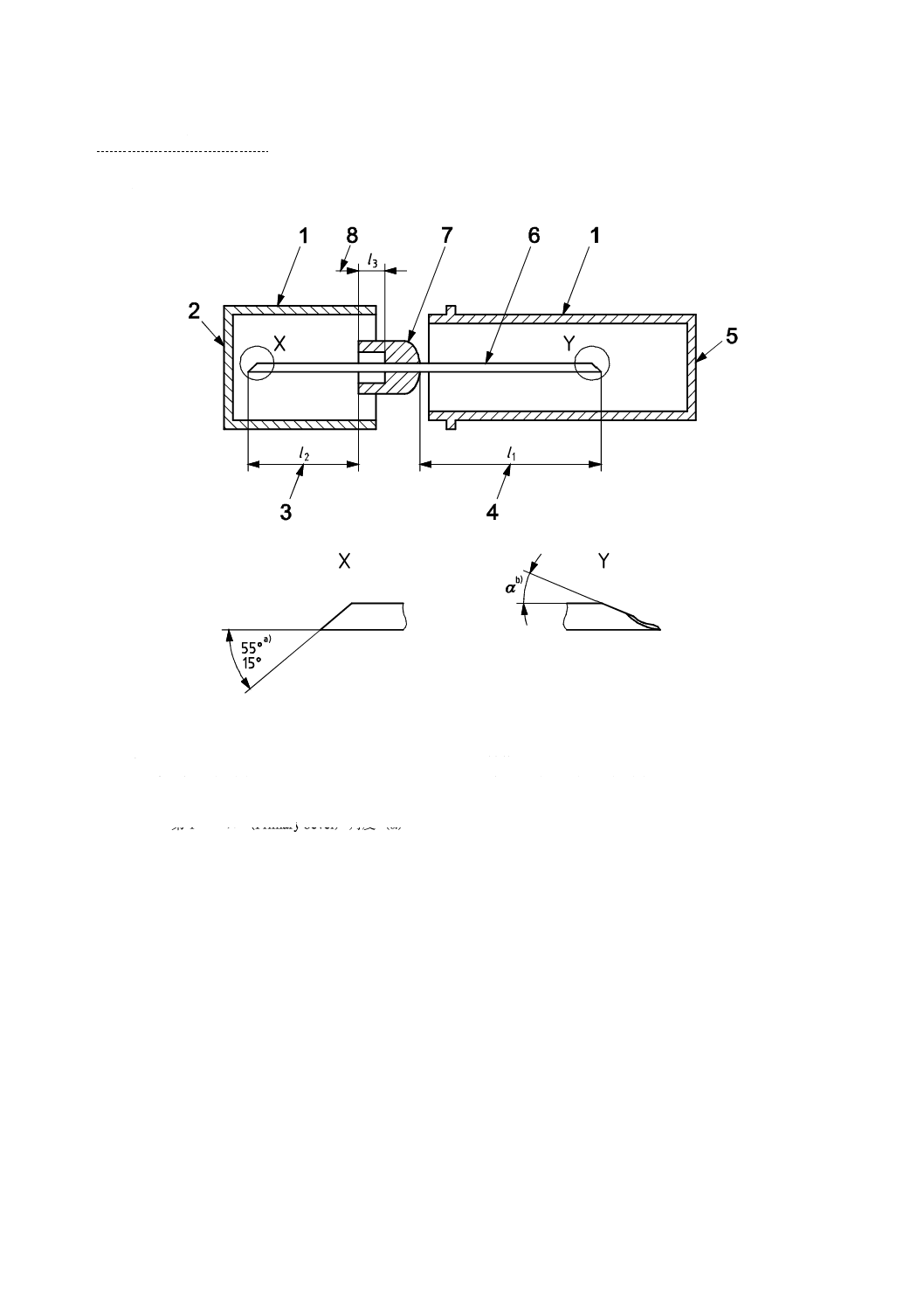
構成及び各部の名称
注射針は,主として針管及び針基で構成し,針管は,円筒形のものと,非円筒形のものがある。一般的
な注射針の構成例及び各部の名称を,図1に示す。
1 一次包装(2部品)
5 有効針さや(鞘)(一次包装)
2 栓刺通針(Butt-end)さや(鞘)(一次包装)
6 針管
3 栓刺通針(Butt-end)長さ(l2)
7 針基
4 有効針長さ(l1)
8 受け口(socket)深さ(l3)
注a) 栓刺通針(Butt-end)角度(15°〜55°)
b) 第1ベベル(Primary bevel)角度(α)
図1−一般的な注射針の構成例及び各部の名称
5
物理的要求事項
5.1
外観及び清浄度
針管と針基との組立品の外面は,拡大せずに,正常又は矯正した視力で観察したとき清浄で,付着物が
あってはならない。外面の潤滑剤は,拡大せずに,正常又は矯正した視力で観察したとき,明らかな液体
の小滴であってはならない。
6
化学的要求事項
6.1
溶出金属の制限
溶出金属の制限は,JIS T 3209:2011の箇条5に適合しなければならない。
4
T 6130:2013
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
7
針管の要求事項
7.1
材料
針管は,JIS G 4305:2012に規定するSUS304,SUS304L,若しくはSUS321を用いJIS T 3209:2011の13.3
及び13.4に適合するもの,又はISO 9626:1991に適合するステンレス針管とする。
針管の潤滑剤としてシリコーン油を用いる場合には,シリコーン油は,シリコーン油基準又はこれと同
等以上の基準に適合しなければならない。
注記 シリコーン油基準には,厚生労働省が定めたシリコーン油基準がある。
7.2
外観
目視で検査したとき,針管は真っすぐであり,正常な切断面及び厚さでなければならない。
7.3
寸法
寸法は,次による。
a) 針管の公称外径は0.2 mm〜0.5 mmの間にあり,公称外径に対する許容差は,−3〜+8 %,又はISO
9626:1991に適合しなければならない。
b) 有効針の公称長さに対する許容差は,次のいずれかによる。
1) 10 mm以下のものは±20 %,10 mmを超え20 mm未満のものは±8 %,20 mm以上40 mm未満のも
のは±7 %,40 mm以上60 mm未満のものは±5 %,60 mm以上のものは±3 %とする。
2) 有効針の公称長さに対する許容差±10 %に適合しなければならない
7.4
栓刺通針
栓刺通針は,次による。
a) 栓刺通針の先端の角度は15°〜55°の範囲内とする。
b) 栓刺通針(Butt-end)長さ(図1のl2参照)は,9.0 mm〜14.0 mmとする。
7.5
針先
注射針の針先は鋭く,かつ,2.5倍に拡大したとき鋭利で,ばり,凹凸,かぎ状及び/又は他の欠陥があ
ってはならない。
8
針基の要求事項
8.1
カートリッジシリンジとの適合性
8.1.1
一般
針基は,ねじ山付きとする。
8.1.2
ねじ山式針基
針基にめす(雌)ねじがある場合は,ISO 9997:1999に適合するM6×0.75のメートル式おす(雄)ねじ
をもつカートリッジシリンジのねじを切った針基とか(噛)み合う,又はインチネジサイズを使用する場
合は0.218インチ(5.54 mm)40 TPI(threads per inch)whitworth形だけとする。
8.2
受け口深さ
針基の受け口深さ(図1のl3参照)は,5 mm以上でなければならない。
8.3
カラーコード
針管の公称外径をカラーコードで示す場合は,ISO 6009:1992(表1参照)に適合したカラーコードによ
って示すことが望ましい。
注記1 針基の見本を作るには,色見本(ISO 6009:1992の附属書Aを参照)の参照色見本が役に立
つ。

5
T 6130:2013
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
注記2 不明瞭な色の色幅及び色図解の番号の中の最も近い色は,ISO 6009:1992の附属書B及び附
属書Cの情報による。
表1−カラーコード
針の公称外径
mm
色
0.2
黒(black)
0.25
白(white)
0.3
黄(yellow)
0.4
中間の灰色(medium grey)
0.5
オレンジ(orange)
注記3 現段階ではISO 6009:1992には“針の公称外径”0.2 mm及び0.25 mmに関する規定はない。
9
針基と針管との接合
針基と針管との接合は,針管の中心軸方向に22 Nで1 mm/sの力を加えたとき破壊してはならない。
10 生物学的安全性
JIS T 0993-1:2012に規定する生物学的安全性の評価を行う。
11 無菌性の保証
無菌性の保証は,滅菌バリデーション基準又はこれと同等以上の基準に基づき,無菌性の担保を行う。
注記 滅菌バリデーション基準には,厚生労働省が定めた滅菌バリデーション基準がある。
12 エンドトキシン
歯科用注射針10本をとり,硬質ガラスの容器に入れ,エンドトキシン試験用水30 mLを加え,溶封又
は適切な栓で密封してよく振り混ぜた後,室温で1時間放置し,この液を試験液とする。日局の一般試験
法のエンドトキシン試験法によって試験をしたとき,0.5 EU/mL未満でなければならない。
13 包装
13.1 一次包装
各注射針は,一次包装に入れ供給する。
有効針さや(鞘)は,使用者が針に触れずに,針をカートリッジシリンジに付ける補助に使えるものと
し,さらに,一次包装は,使用前に容易に破れるおそれがなく,微生物の侵入を防止することができ,通
常の取扱い,輸送及び保管中に製品を適切に保護できるものでなければならない。また,一度開封したら,
包装は簡単に再シールできず,開封したことが明確に分かるものでなければならない。
13.2 二次包装
二次包装は,通常の取扱い,輸送及び保管中に製品を保護できる強度をもたなければならない。
14 表示
14.1 一次包装
一次包装には,次の事項を表示する。

6
T 6130:2013
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
a) 針管の外径(mm)及び有効針の長さ(mm)
b) “滅菌済み”の旨
c) 製造番号又は製造記号
14.2 二次包装
二次包装には,次の事項を表示する。ただし,二次包装を用いないで,一次包装を最小販売単位の包装
として用いる場合には,次の事項を一次包装に表示する。
なお,製造番号又は製造記号が滅菌年月を表している場合には,滅菌年月の表示をする必要はない。
a) 製造販売業者の氏名又は名称,及び住所
b) 販売名
c) 針管の外径(mm)及び有効針の長さ(mm)
d) 数量(入り数)
e) “滅菌済み”の旨
f)
“再使用禁止”の旨(“ディスポーザブル”の表現は使用しない。)
g) 製造番号又は製造記号
h) 滅菌年月
i)
他の法定表示事項
14.3 図記号の使用
14.1及び14.2は,JIS T 0307:2004に規定する適切な図記号を使用することによってこれに替えてもよい。
注記 JIS T 0307:2004に規定する主な図記号の例を,表2に示す。
表2−JIS T 0307に規定する主な図記号の例
附属書JA
(参考)
JISと対応国際規格との対比表
JIS T 6130:2013 歯科用注射針
ISO 7885:2010 Dentistry−Sterile injection needles for single use
(I)JISの規定
(II)
国際規
格番号
(III)国際規格の規定
(IV)JISと国際規格との技術的差異の箇条
ごとの評価及びその内容
(V)JISと国際規格との技術的差
異の理由及び今後の対策
箇条番号
及び題名
内容
箇条番号
内容
箇条ごと
の評価
技術的差異の内容
3 用語及
び定義
10項目の用語の定義
を規定。
3
5項目の用語の定義を規
定。
追加
JISは定義を追加した。
利用者の利便性のため。実質的な
差はない。
4 構成及
び各部の
名称
歯科用注射針の構成
を規定。
−
−
追加
JISは構成を規定。JISは針管
に非円筒形のものも規定。
利用者の利便性のため。実質的な
差はない。
7 針管の
要求事項
7.1 使用する針管及
び潤滑剤を規定。
5.1
JISとほぼ同じ。
選択
JISは,JIS T 3209の針管及び
潤滑剤を規定。
JISは使用できる針管にJIS T
3209の針管も選択可能とした。加
え,シリコーン油基準に適合する
シリコーンを追加。実質的な差は
ない。
7.2 使用する針管の
外観を規定。
−
−
追加
−
JISはJIS間の整合性を取る。実質
的な差はない。
7.3 寸法の規格を規
定。
5.2
JISとほぼ同じ。
選択
JISは,JIS T 3209の針管の規
格を追加。
JISは使用できる針管にJIS T
3209の針管も選択可能とした。実
質的な差はない。
7.5 針先について規
定。
5.4
JISとほぼ同じ。
削除
JISは針先の角度の規定をして
いない。
針先の角度の規定については,技
術の進歩と企業ノウハウにISOが
合っていない事例として削除し
た。
2
T
6
1
3
0
:
2
0
1
3
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
(I)JISの規定
(II)
国際規
格番号
(III)国際規格の規定
(IV)JISと国際規格との技術的差異の箇条
ごとの評価及びその内容
(V)JISと国際規格との技術的差
異の理由及び今後の対策
箇条番号
及び題名
内容
箇条番号
内容
箇条ごと
の評価
技術的差異の内容
8 針基の
要求事項
8.1 カートリッジシ
リンジとの適合性を
規定。
6.1
JISとほぼ同じ。
削除
JISはねじ山なしを削除した。 JISは安全性の観点からねじ山な
し品を削除した。
8.3 カラーコードを
規定。
6.3
JISとほぼ同じ。
変更
JISは,推奨とした。
JISは,ISO 7885がISO 6009で規
定していない太さを規定してい
る,及び現在の市場に存在する歯
科用注射針の外径は必ずしもISO
6009の規定と一致していないも
のもあることから,今回のJISで
は推奨とした。市場に流通してい
る全品種をISO 6009が規定した
時点で見直す。
12 エンド
トキシン
エンドトキシンの確
認方法を規定。
−
−
追加
JISは,エンドトキシン試験を
追加。
JISは,我が国で実績のある方法
を追加した。実質的な差はない。
13 包装
13.2 二次包装を規
定。
−
−
追加
ISO規格は二次容器を規定し
ていない。
JISは他のJISと項立ての整合を
図るためこの項を追加。実質的な
差はない。
−
−
Annex A
(参考)インチネジサイ
ズ
削除
JISは本文へ規定。
JISは本文へ同じ内容を規定。実
質的な差異はない。
−
−
Biblio-
graphy
生物評価の参考文献
削除
JISは翻訳JISを引用規格とす
る。
JISは本文へ同じ内容を規定。実
質的な差異はない。
JISと国際規格との対応の程度の全体評価:ISO 7885:2010,MOD
注記1 箇条ごとの評価欄の用語の意味は,次による。
− 削除……………… 国際規格の規定項目又は規定内容を削除している。
− 追加……………… 国際規格にない規定項目又は規定内容を追加している。
− 変更……………… 国際規格の規定内容を変更している。
− 選択……………… 国際規格の規定内容とは異なる規定内容を追加し,それらのいずれかを選択するとしている。
注記2 JISと国際規格との対応の程度の全体評価欄の記号の意味は,次による。
− MOD…………… 国際規格を修正している。
2
T
6
1
3
0
:
2
0
1
3
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。




