T 3268:2018
(1)
目 次
ページ
序文 ··································································································································· 1
1 適用範囲························································································································· 1
2 引用規格························································································································· 1
3 用語及び定義 ··················································································································· 2
4 構成及び各部の名称 ·········································································································· 4
5 要求事項························································································································· 6
5.1 外観及び清浄度 ············································································································· 6
5.2 エックス線不透過性 ······································································································· 6
5.3 ハブ ···························································································································· 6
5.4 破断強度 ······················································································································ 6
5.5 カテーテルの患者側(先)端及び側孔················································································ 7
5.6 腐食抵抗性 ··················································································································· 7
5.7 気密性 ························································································································· 7
5.8 耐圧性 ························································································································· 7
5.9 持続注入用カテーテル ···································································································· 7
5.10 バルーンカテーテル ······································································································ 7
5.11 スネアカテーテル ········································································································· 8
5.12 構成品 ························································································································ 8
6 生物学的安全性 ················································································································ 8
7 無菌性の保証 ··················································································································· 8
8 包装······························································································································· 9
8.1 一次包装 ······················································································································ 9
8.2 二次包装 ······················································································································ 9
9 表示······························································································································· 9
9.1 一次包装 ······················································································································ 9
9.2 二次包装 ······················································································································ 9
9.3 図記号の使用 ··············································································································· 10
附属書A(規定)破断強度の測定方法 ····················································································· 11
附属書B(規定)腐食抵抗性に対する試験方法 ·········································································· 13
附属書C(規定)カテーテルの気密性 ····················································································· 14
附属書D(規定)一般的なカテーテルの耐圧性 ········································································· 15
附属書E(規定)加圧注入試験(加圧注入に使用するものに限る。) ············································· 17
附属書F(規定)カテーテルの流量 ························································································· 19
附属書G(規定)加圧限界(RBP)の決定方法 ········································································· 21
附属書H(規定)バルーン膨張時の損傷及び漏れに対する疲労試験 ·············································· 22
T 3268:2018 目次
(2)
ページ
附属書I(規定)バルーンの収縮時間に対する試験 ···································································· 24
附属書J(規定)膨張圧に対するバルーン径の確認方法 ······························································ 25
参考文献 ···························································································································· 26
附属書JA(参考)JISと対応国際規格との対比表 ······································································ 27
T 3268:2018
(3)
まえがき
この規格は,工業標準化法第14条によって準用する第12条第1項の規定に基づき,一般社団法人日本
医療機器テクノロジー協会(MTJAPAN)及び一般財団法人日本規格協会(JSA)から,工業標準原案を具
して日本工業規格を改正すべきとの申出があり,日本工業標準調査会の審議を経て,厚生労働大臣が改正
した日本工業規格である。
これによって,JIS T 3268:2012は改正され,この規格に置き換えられた。
この規格は,著作権法で保護対象となっている著作物である。
この規格の一部が,特許権,出願公開後の特許出願又は実用新案権に抵触する可能性があることに注意
を喚起する。厚生労働大臣及び日本工業標準調査会は,このような特許権,出願公開後の特許出願及び実
用新案権に関わる確認について,責任はもたない。
日本工業規格 JIS
T 3268:2018
単回使用滅菌済み血管内カテーテル
Sterile, single-use intravascular catheters
序文
この規格は,2013年に第2版として発行されたISO 10555-1(2014年に発行されたcorrected versionを含
む。),ISO 10555-3及びISO 10555-4を基とし,国内事情に合わせるため,一部の技術的内容を変更して作
成した日本工業規格である。
なお,この規格で点線の下線を施してある箇所は,対応国際規格を変更している事項である。変更の一
覧表にその説明を付けて,附属書JAに示す。
1
適用範囲
この規格は,診断又は治療を行うときに,血管(透析用シャント及び人工血管を含む。)へ挿入留置する
か,又は医療機器を目的部位へ送達させるときに用いる,滅菌済みで単回使用の血管内カテーテル(以下,
カテーテルという。)について規定する。ただし,ヘパリン,ウロキナーゼなどの生物由来材料をコーティ
ングして抗血栓性を発現させるもの,抗菌薬をコーティングして抗菌作用を発現させるもの及び吸水膨潤
形カテーテルは除く。
注記1 2021年1月31日までJIS T 3268:2012を適用することができる。
注記2 この規格の対応国際規格及びその対応の程度を表す記号を,次に示す。
ISO 10555-1:2013,Intravascular catheters−Sterile and single-use catheters−Part 1: General
requirements及びcorrected version:2014
ISO 10555-3:2013,Intravascular catheters−Sterile and single-use catheters−Part 3: Central venous
catheters
ISO 10555-4:2013,Intravascular catheters−Sterile and single-use catheters−Part 4: Balloon dilatation
catheters
(全体評価:MOD)
なお,対応の程度を表す記号“MOD”は,ISO/IEC Guide 21-1に基づき,“修正している”
ことを示す。
2
引用規格
次に掲げる規格は,この規格に引用されることによって,この規格の規定の一部を構成する。これらの
引用規格は,記載の年の版を適用し,その後の改正版(追補を含む。)は適用しない。
JIS T 0307:2004 医療機器−医療機器のラベル,ラベリング及び供給される情報に用いる図記号
JIS T 0993-1:2012 医療機器の生物学的評価−第1部:リスクマネジメントプロセスにおける評価及
び試験
2
T 3268:2018
JIS T 3252:2013 血管造影用活栓,チューブ及び附属品
JIS T 3259:2012 オブチュレータ
JIS T 3260:2017 カテーテル拡張器
JIS T 3261:2017 滅菌済みカテーテルイントロデューサ
JIS T 3262:2017 イントロデューサ針
JIS T 3263:2012 血管カテーテル用Y−コネクタ
ISO 594-1:1986,Conical fittings with a 6 % (Luer) taper for syringes,needles and certain other medical
equipment−Part 1: General requirements
ISO 594-2:1998,Conical fittings with 6 % (Luer) taper for syringes,needles and certain other medical
equipment−Part 2: Lock fittings
ISO 7886-1:2017,Sterile hypodermic syringes for single use−Part 1: Syringes for manual use
ISO 80369-7:2016,Small-bore connectors for liquids and gases in healthcare applications−Part 7: Connectors
for intravascular or hypodermic applications
3
用語及び定義
この規格で用いる主な用語及び定義は,次による。
3.1
血管内カテーテル(intravascular catheter)
血管に挿入留置する診断用又は処置用のカテーテル,又は医療機器を目的部位へ送達させるときに用い
るカテーテル。
3.2
診断用カテーテル(diagnostic catheter)
診断を主な目的とし,血管の走行,血流量,血圧,電位,管くう(腔)内の状態などの生体情報を得る
ために用いるカテーテルの総称。採血を行うこともある。ただし,この規格では,接続する医用電気機器
を含まない。
3.2.1
血管造影用カテーテル(angiographic catheter)
目的とする血管の可視化のため,造影剤の注入を主たる目的として使用するカテーテル。
3.3
加圧注入(power injection)
加圧注入器を用いて,高圧を伴う急速な薬液等の注入をすること。
3.4
処置用カテーテル(therapeutic catheter)
処置を主な目的とし,狭さく(窄)血管の拡張,一時的な血流の遮断,薬液などの注入,血栓又は異物
の除去などを行うために用いるカテーテルの総称。デリバリーシステムも含まれる。
ただし,この規格では,接続する医用電気機器及び皮下植込み用ポートは含まない。
3.4.1
ガイディングカテーテル(guiding catheter)
主としてカテーテルをその内くう(腔)に通し,目的とする部位まで誘導し,到達させるために使用す
るカテーテル。
3
T 3268:2018
3.4.2
マイクロカテーテル(microcatheter)
選択的な血管造影,塞栓療法などに用いる細径のカテーテル。デリバリーシステムとして用いる場合も
ある。
3.4.3
ブラッドアクセスカテーテル(blood access catheter)
体外循環のため,血液の出入口(ブラッドアクセス)を確保する場合に使用するカテーテル。
3.4.4
バルーンカテーテル(balloon catheter)
バルーンを備えたカテーテルで,血管狭さく(窄)部の拡張(血管形成術)用,一時閉塞(血管閉塞術)
用,血栓又は異物除去用などがある。デリバリーシステムとして用いる場合もある。
3.4.5
スネアカテーテル(snare catheter)
血管内に挿入し,スネアワイヤの操作にて血栓及び異物を除去するためのカテーテル。
3.4.6
デリバリーシステム(delivery system, delivery catheter)
血管用ステント,塞栓コイルなどの体内植込み形の医療機器を,目的の部位まで送達するために使用す
る医療機器。
3.5
持続注入用カテーテル(continuous infusion catheter)
処置用カテーテルのうち,中心静脈,門脈など,特定の動静脈血管に留置し,持続的な薬液注入を主た
る目的とするカテーテルの総称。
3.5.1
静脈用カテーテル(intravenous catheter)
薬液の持続注入,血液の吸引,血圧の監視,輸血などを目的として,静脈系に挿入留置するカテーテル。
3.5.2
ポート用カテーテル(catheter for access port)
皮下植込み用ポートに接続して,薬液を臓器又は血管に送達,又は持続注入するためのカテーテル。中
心静脈栄養に用いる場合がある。
3.5.3
皮下植込み用ポート(subcutaneous implantable port)
薬液を貯留する空間を備え,注射針等でセプタム(隔壁)を介して経皮的に薬液を注入することができ
る医療機器。カテーテルと接続して皮下に植え込んで使用される。ポート又はリザーバということもある。
ただし,この規格が適用されるものではない。
3.6
シャフト(shaft)
カテーテルの主軸となる管の部分。
3.7
ハブ(hub)
カテーテルのシャフト手元部にある接続端。カテーテルに取り付けて,接続に用いることのできるもの
4
T 3268:2018
もある。コネクタということもある。
3.8
マーカ(marker)
シャフト,バルーンなどに備えられ,カテーテルの挿入位置及び挿入部位における距離を確認すること
ができるもの。深度目盛ということもある。
3.9
枝管(branched tubing)
バルーンカテーテルなどにおいて,シャフトの接合部から分かれる管。
3.10
バルーン(balloon)
カテーテルに備えられた,風船様の部品。
3.11
外径(outside diameter)
シャフト直径の最大値。
3.12
有効長(effective length)
身体又は併用する医療機器に挿入できるシャフト部分の長さ。
3.13
患者側(先)端(distal end, tip)
カテーテルの,術者から見て患者側又はその先端。
3.14
手元端(手元部)(proximal end, access end)
カテーテルの,術者から見て手元側又はその先端。機器側端ということもある。
3.15
加圧限界(rated burst pressure, RBP)
拡張用バルーンカテーテルについて,統計的にも保証し得るバルーンの膨張限度とした圧力。最大拡張
圧ともいう。
4
構成及び各部の名称
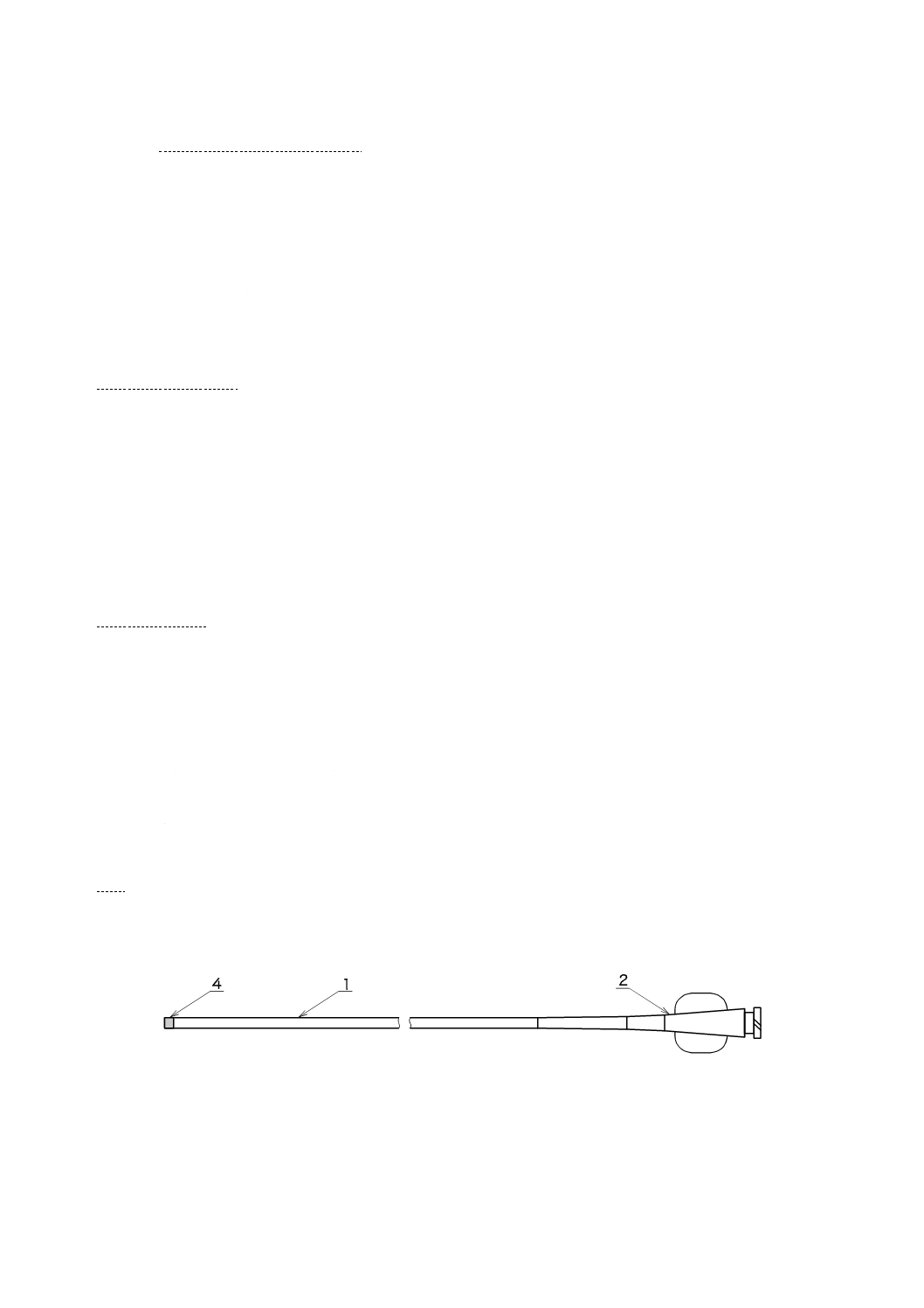
一般的なカテーテルとして,構成及び各部の名称の例を図1に示す。
なお,製品の種類及び形状については,この限りではない。
a) 診断用カテーテル(血管造影用カテーテル)
図1−カテーテル例
5
T 3268:2018
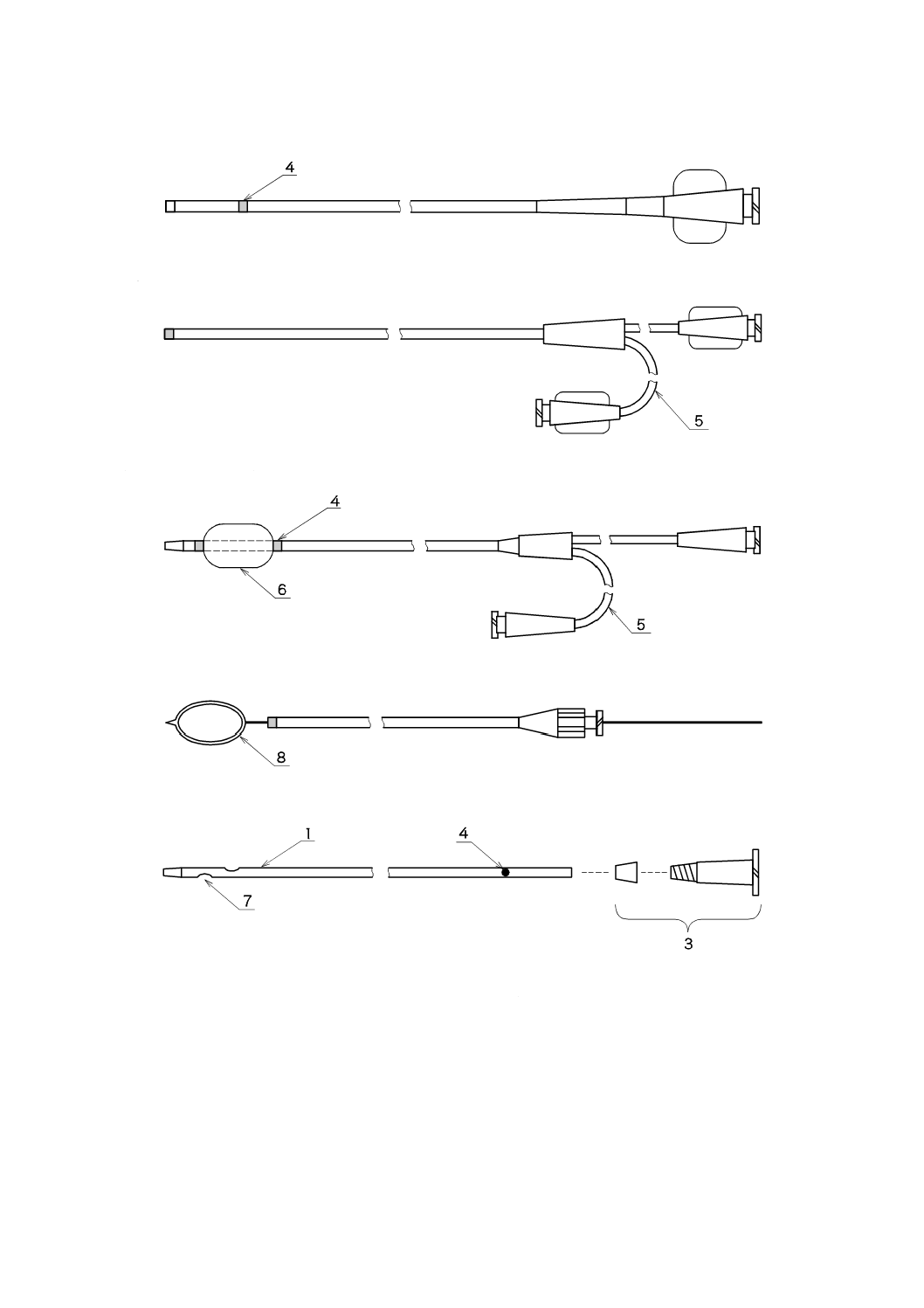
(ガイディングカテーテル,マイクロカテーテル)
(ブラッドアクセスカテーテル)
(バルーンカテーテル)
(スネアカテーテル)
(持続注入用カテーテル:静脈用カテーテル)
b) 処置用カテーテル
図1−カテーテル例(続き)
6
T 3268:2018
(持続注入用カテーテル:ポート用カテーテル)
b) 処置用カテーテル(続き)
1 シャフト
4 マーカ(深度目盛)
7 側孔
2 ハブ
5 枝管
8 スネアワイヤ
3 ハブ(取付式のもの)
6 バルーン
9 皮下植込み用ポート
注記1 カテーテルには,せん(穿)刺針,(スタイレット,オブチュレータなどの)形状保持具,カテーテル拡張器
(ダイレータ),ガイドワイヤインサータ,Y−コネクタ,活栓又は混注部,逆止弁又は止血弁,注射筒又は
インフレータ,開閉器,トルクデバイス又はハンドル,固定翼などを備えるものもある。
注記2 カテーテルには側孔のないもの,単くう(腔)式及び多くう(腔)式のものもある。
注記3 ポート用カテーテルについて,図中の皮下植込み用ポートには,この規格を適用しない。
図1−カテーテル例(続き)
5
要求事項
5.1
外観及び清浄度
カテーテル及び構成品は,外表面に異常がなく,目視で検査したとき,きず,ばり又は異物の付着があ
ってはならない。潤滑剤処理などが施されている場合には,外表面にその液滴があってはならない。
5.2
エックス線不透過性
カテーテル(構成品が該当する場合を含む。)を透視下で使用する場合には,エックス線不透過性をもち,
このエックス線不透過性は適切な方法で評価しなければならない。
5.3
ハブ
ハブは,ISO 594-1,ISO 594-2又はISO 80369-7に適合しなければならない。
5.4
破断強度
附属書Aに従って試験を行うとき,カテーテルの破断強度は表1に適合しなければならない。さらに,
ハブの接合部/接続部についても,その強度は表1に適合しなければならない。
表1−カテーテルの破断強度
シャフト径
(最小値)
mm
破断強度
(最小値)
N
シリコーン製カテーテルの
破断強度(最小値)
N
0.55未満
1
−
0.55以上,0.75未満
3
−
0.75以上,1.15未満
5
4
1.15以上,1.85未満
10
8
1.85以上
15
12

7
T 3268:2018
5.5
カテーテルの患者側(先)端及び側孔
血管に対する傷害を最小限とするため,カテーテルの患者側(先)端は滑らかで,かつ,丸みを帯び,
テーパ形状を施すか又は同等に加工されているものでなければならない。
また,カテーテルに側孔を備えるものは,側孔の数,形状及び配置について,同様に血管に対する傷害
を最小限に抑えるものでなければならない。
5.6
腐食抵抗性
カテーテル及び構成品に金属材料を使用し,かつ,それが直接的又は間接的に薬液又は体液との接触が
ある場合,附属書Bに従って試験を行うとき,金属部分に腐食の兆候があった場合,用途及びリスクアセ
スメントについて腐食の程度を評価して,製品の性能,安全性に影響がないことを確認しなければならな
い。
5.7
気密性
附属書Cに従って試験を行うとき,カテーテルのシャフト及びハブ,接続部又は接合部に漏れが生じて
はならない。ただし,耐圧性のあるカテーテルで5.8の試験を行う場合には,この試験に代えてもよい。
5.8
耐圧性
5.8.1
カテーテルの耐圧性
使用時における耐圧性を示す場合は,附属書Dに従って試験を行うとき,製造販売業者が設定した耐圧
値の圧力に対してカテーテルは破裂又は漏れを生じてはならない。ただし,拡張用バルーンを備えるカテ
ーテルは5.10.1を適用する。
5.8.2
加圧注入に使用するカテーテルの耐圧性
加圧注入器との併用を意図するものは,5.8.1の評価に加えて,附属書Eに従って試験を行い,その破裂
限界は最大流量の状態にあるカテーテルの圧力を超えるものでなければならない。
5.9
持続注入用カテーテル
5.9.1
くう(腔)の認識
複数のハブをもつ多くう(腔)式のカテーテルは,使用者がそれぞれのくう(腔)を識別できなければ
ならない。
5.9.2
流量
カテーテルが流量を標榜する場合,附属書Fに従って流量を測定するとき,表2に適合しなければなら
ない。多くう(腔)式カテーテルの場合は,それぞれのくう(腔)で試験をしなければならない。
注記 持続注入用カテーテルだけでなく,薬液の注入が主たる用途となるカテーテルの場合も考慮す
ることが望ましい。
表2−カテーテルの流量
カテーテルの外径
(公称値)
mm
くう(腔)の流量
(対表示値)
%
1.0 mm未満
80以上
1.0 mm以上
90以上
5.10 バルーンカテーテル
5.10.1 拡張用バルーンカテーテル
a) 拡張用バルーンを備えるものは,附属書Gに従って試験を行い,適切に安全マージンを考慮した加圧

8
T 3268:2018
限界を決定しなければならない。
b) 附属書Hに従って評価を行うとき,漏れ,破損,ヘルニア化などの兆候があってはならない。
c) 附属書Iに従って,拡張用バルーンの加圧限界からの収縮時間を決定した後,附属書Jに従って拡張
用バルーンのバルーン径と膨張圧との相関性を評価しなければならない。
5.10.2 その他のバルーンの漏れ
製造販売業者の指定する規定圧又は規定量を注入してバルーンを膨張させるとき,漏れがあってはなら
ない。
5.11 スネアカテーテル
スネアカテーテルは,製造販売業者の指定する操作方法によってスネアワイヤの操作(展開・収納)を
行うとき,異常があってはならない。
5.12 構成品
5.12.1 一般
5.12.2〜5.12.7に該当する場合には,それぞれの要求事項を適用する。
5.12.2 せん(穿)刺針
せん(穿)刺針は,JIS T 3262の5.4[せん(穿)刺針の要求事項]及び5.5[外とう(套)管の要求事
項]に適合しなければならない。
5.12.3 オブチュレータ
オブチュレータは,JIS T 3259の5.4(破断強度),5.5[かん(嵌)合],5.6(耐圧性),5.7(公称外径),
5.8(有効長)及び5.9(着色)に適合しなければならない。
5.12.4 カテーテル拡張器
カテーテル拡張器(ダイレータ)は,JIS T 3260の5.4(ハブ)及び5.5(ガイドワイヤの通過性)に適
合しなければならない。
5.12.5 Y−コネクタ
Y−コネクタは,JIS T 3263の箇条4(構成及び各部の名称)及び5.1(物理的要求事項)に適合しなけ
ればならない。
5.12.6 止血弁
止血弁は,JIS T 3261の5.4.2(止血弁の耐圧性)に適合しなければならない。
5.12.7 血管造影用活栓
血管用造影活栓(混注部の場合を含む。)は,JIS T 3252の5.2(気密性),5.3(耐圧性),5.4(血管造影
用活栓)及び5.5[おす(雄)めす(雌)かん(嵌)合部,継ぎ管及び導管の接続部]に適合しなければな
らない。
6
生物学的安全性
JIS T 0993-1に規定する生物学的安全性の評価を行わなければならない。
7
無菌性の保証
滅菌バリデーション基準又はこれと同等以上の基準に基づき,無菌性の担保を行わなければならない。
注記 滅菌バリデーション基準には,厚生労働省が定めた滅菌バリデーション基準がある。
9
T 3268:2018
8
包装
8.1
一次包装
一次包装は,微生物の侵入を防止することができ,かつ,通常の取扱い,輸送及び保管中に,内容製品
を適切に保護できるものでなければならない。また,一次包装は,一度開封したならば簡単に再シールで
きず,開封したことが明確に分からなければならない。
8.2
二次包装
二次包装は,通常の取扱い,輸送及び保管中に内容製品を保護できる強度をもたなければならない。
9
表示
9.1
一次包装
一次包装には,次の事項を記載する。
a) 外径(mm)及び有効長(mm又はcm)。ただし,外径をミリメートル(mm)で示すほか,フレンチ
(シャリエール)又はゲージを参考に併記してもよい。
注記 フレンチ(シャリエール)はF(Ch)などで表記するのがよい。1 mmが3 F(Ch)に相当し,
1/3 mm刻みで表記する。ゲージは,Gなどで表記するのがよい。
b) 製造番号又は製造記号
c) 使用期限
d) “滅菌済み”の旨
e) “再使用禁止”の旨(“ディスポーザブル”の表現は,使用しない。)
f)
血管造影用カテーテルについて,カテーテルの先端形状が包装からは確認できない場合は,図示する
か又は説明をしなければならない。
g) その他,必要に応じて製品に関する注意事項
9.2
二次包装
二次包装には,次の事項を表示する。ただし,二次包装を用いないで,一次包装を最小単位の包装とし
て用いる場合には,次の事項を一次包装に表示する。
なお,製造番号又は製造記号が滅菌年月を表示している場合は,改めて滅菌年月の表示は必要としない。
また,滅菌年月の代わりに使用期限を表示してもよい。
a) 製造販売業者の氏名又は名称,及び住所
b) 医療機器の認証番号又は承認番号
c) 販売名
d) 外径(mm)及び有効長(mm又はcm)。ただし,外径をミリメートル(mm)で示すほか,フレンチ
(シャリエール)又はゲージを参考に併記してもよい。
注記 フレンチ(シャリエール)はF(Ch)などで表記するのがよい。1 mmが3 F(Ch)に相当し,
1/3 mm刻みで表記する。ゲージは,Gなどで表記するのがよい。
e) 数量(入り数)
f)
“滅菌済み”の旨
g) “再使用禁止”の旨(“ディスポーザブル”の表現は,使用しない。)
h) 天然ゴムを使用しているものは,その旨
i)
製造番号及び製造記号
j)
滅菌年月

10
T 3268:2018
k) ガイドワイヤ,ガイディングカテーテル,イントロデューサ等の適合性及び使用推奨サイズ(該当す
る場合)
次の項目については,添付文書に記載してもよい。
l)
使用時に耐圧性を示す場合は,耐圧値。また,加圧注入器と併用するものについては,注入器使用時
の設定推奨圧(又は耐圧値)及び流量。
m) 拡張用バルーンカテーテルの加圧限界(RBP),及び公称径までに要するバルーンの膨張圧
n) 拡張用ではないカテーテルで,バルーンを膨張させるための規定圧又は規定量
o) その他,必要に応じて製品に関する情報及び注意事項
9.3
図記号の使用
9.1及び9.2の要件は,JIS T 0307に規定する適切な図記号を使用することによってこれに替えてもよい。
注記 JIS T 0307に規定する主な図記号の例を,表3に示す。
表3−JIS T 0307に規定する主な図記号の例

11
T 3268:2018
附属書A
(規定)
破断強度の測定方法
A.1 概要
カテーテルの,試料となる試験片は,それぞれシャフト,枝管,ハブ又はコネクタと接合部,及びチュ
ーブどうしとの接合部について試験が行えるように選択する。チューブ及び接合部が破断するまで,試料
に力を加える。
A.2 装置
A.2.1 引張試験機 15 N以上の力を負荷することができる試験装置
A.3 手順
A.3.1 カテーテルを製造販売業者の指示に従って組み立てる。カテーテルから試験に供する試料を選定す
るが,試料には(存在する場合)ハブ及びコネクタを含め,シャフトと患者側(先)端との接合部なども
含める。ただし,これらが3 mm未満の場合は試料に含めない。
A.3.2 試料を適切な水溶液(37±2 ℃)中に適切な時間で浸せき(漬)し,処理後は直ちに試験を行う。
A.3.3 引張試験機に試料をセットする。試料にハブ及びコネクタを含む場合には,これらの変形を避ける
ために,適切なつかみ具を使用する。
A.3.4 試料のゲージ長,すなわち,引張試験機のつかみ具間の距離,又は試料の両端(ハブともう一方の
試料を把持するつかみ具との間)の距離を適宜測定する。
A.3.5 試料が2片以上に分離するまで,ゲージ長1 mm当たり20 mm/minのひずみ速度で力を加える(表
A.1参照)。
破断が起こったときにかかった力(単位:ニュートン)を記録し,破断強度とする。
注記 カテーテルが異なる外径をもつ単くう(腔)式であるとき,試料には最小外径の部分を含める
ことが望ましい。
A.3.6 枝管を備えるカテーテルで試験を行う場合は,次による。
a) それぞれの枝管に対し,A.3.2〜A.3.5の操作を行う。
b) カテーテルの身体に挿入される部分の近隣及び枝管の接合部が含まれる試料を用いてA.3.2〜A.3.5の
操作を行う。
c) 接合部のそれぞれに対して,b)の操作を行う。
A.3.7 一つの試料に対して2回以上の試験を行ってはならない。
表A.1−ゲージ長1 mm当たり20 mm/minのひずみ速度の条件(例)
ゲージ長
mm
ひずみ速度
mm/min
10
200
20
400
25
500
12
T 3268:2018
A.4 試験報告書には,少なくとも次の事項を記載する。
a) 試料の個体識別(ロット番号など)
b) 各試料の外径(mm)及び破断強度(単位:N)
c) 破損した箇所
13
T 3268:2018
附属書B
(規定)
腐食抵抗性に対する試験方法
B.1
概要
カテーテルを生理食塩水に浸せき(漬)し,次に沸騰する水に浸せき(漬)した後,腐食の兆候の有無
を目視などによって確認する。
B.2
試薬
B.2.1 生理食塩水 分析用試薬グレードの塩化ナトリウムを,水に溶解させた溶液 [c(NaCl)=0.15 mol/L]。
B.2.2 水 蒸留水又は脱イオン水。
B.3
器具
B.3.1 ビーカー(ほうけい酸ガラス製ビーカー)
B.4
手順
室温にて,ビーカー(B.3.1)の生理食塩水(B.2.1)の中に試料となるカテーテルを5時間浸せき(漬)
する。試料を取り出し,沸騰する水(B.2.2)の中に30分間浸せき(漬)する。これらを37 ℃まで冷却し,
この温度にて48時間維持する。試料を取り出し,室温で乾燥させる。実際の使用において2片以上の部品
に分離されるものは分離する。このとき腐食の兆候がないか,試料を目視などによって確認する。
B.5
試験報告書
試験報告書には,少なくとも次の事項を記載する。
a) 試料の個体識別(ロット番号など)
b) 試験における腐食の有無について
14
T 3268:2018
附属書C
(規定)
カテーテルの気密性
C.1 概要
液漏れ防止コネクタを介して,カテーテルに注射筒を接続する。カテーテル及びハブ(該当する場合,
取付式のハブ)に水圧をかけ,漏れが生じないかを試験する。
C.2 試薬
C.2.1 水 蒸留水又は脱イオン水。
C.3 器具
C.3.1 液漏れ防止コネクタ カテーテルと注射筒(C.3.3)とを接続するためのもので,デッドボリュー
ムが小さく,300 kPa以上の圧力での測定に耐え得るもの。
C.3.2 コネクタ 注射筒(C.3.3)とハブがないカテーテルとを接続するために用いる,気密性のあるも
の。
C.3.3 注射筒 適切な容量のもので,注射筒自身が気密性をもち,ISO 7886-1に適合する外筒及び押子。
又は同等の注入器。
C.3.4 試料を閉塞するためのもの 例:開閉器
C.4 手順
C.4.1 ハブをもつカテーテルのハブは,液漏れ防止コネクタ(C.3.1)に接続して気密にしておく。必要
であれば,製造販売業者の指示に従って取付式のハブを取り付けておく。
C.4.2 ハブのないカテーテルで試験を行う場合には,コネクタ(C.3.2)を用いて注射筒(C.3.3)に接続
する。
C.4.3 注射筒(C.3.3)を22±2 ℃の水(C.2.1)で満たし,空気を取り除く。注射筒内の水量は,表示目
盛によって調整する。試料はできるだけ患者側(先)端に近い位置で閉塞(C.3.4)する。
C.4.4 300 kPa以上の圧力をかけ,30秒間維持する。カテーテルとハブとの接合部などについて検査し,
漏れ(一つ又は複数の水滴が落下した状態)があったかどうかを記録する。
C.5 試験報告書
試験報告書には,少なくとも次の事項を記載する。
a) 試料の個体識別(ロット番号など)
b) ハブ,カテーテルのシャフト又はこれら接合部などで漏れが生じたか,漏れの有無についての考察。
15
T 3268:2018
附属書D
(規定)
一般的なカテーテルの耐圧性
D.1 概要
カテーテルのハブ又は手元端と水圧源とを接続する。破裂及び漏れが起こるまで,一定時間圧をかけ,
破裂又は漏れが生じた時の圧力を記録する。
D.2 装置及び器具
D.2.1 加圧装置(圧力源) 加圧流体に液体を用いるもの。
D.2.2 液漏れ防止コネクタ
D.2.3 固定具 カテーテルを液漏れ防止コネクタ(D.2.2)に固定するもの。
D.2.4 試料を閉塞するためのもの 例:開閉器
D.2.5 液体で満たした,温度管理可能な試験用チャンバ
注記 試験系の構成例を,図D.1に示す。加圧装置及びその制御装置は,形状,機器の構成又は自動
化といった面から多様であるため,その詳細は示さない。
D.3 手順
警告 加圧装置の不具合による高圧液体の漏れに対して,試験を行う者を保護するための適切な予防
措置及び防護策を講じなければならない。
D.3.1 例えば,生理食塩水にあらかじめ浸せき(漬)する,試験用チャンバの液体に通す,又は滅菌条件
下に置くなど,試料を試験環境に慣らす。
D.3.2 試験用チャンバ内の液体は,試験実施中に37±2 ℃の温度で維持する。
D.3.3 試料の手元部を液漏れ防止コネクタ(D.2.2)に接続する。さらに,これを固定具(D.2.3)で保持
してもよい。
D.3.4 試料内の空気を液体で置換後,閉塞(D.2.4)する。
D.3.5 試験系において,破損及び漏れがないことを確認する。
D.3.6 試料を試験用チャンバに用いる液体に1分以上浸せき(漬)し,液温に訓化させる。
D.3.7 液漏れ又は破裂を引き起こすために,試料への注液量を1 mL/sに調節する。加圧によるカテーテ
ルの破裂を正確に検知するため,圧力勾配(動水勾配)による制御を行うことが望ましい。
D.3.8 液漏れ又は破裂が起こるまで,試料に注液する。試験系を加圧している間,ハブでの圧力を記録し,
最大加圧の到達に注意する。
D.4 試験報告書
試験報告書には,少なくとも次の事項を記載する。
a) 試料の個体識別(ロット番号など)
b) 液漏れ又は破裂が起きたときの圧力
c) 液漏れ又は破裂が生じた試料の箇所
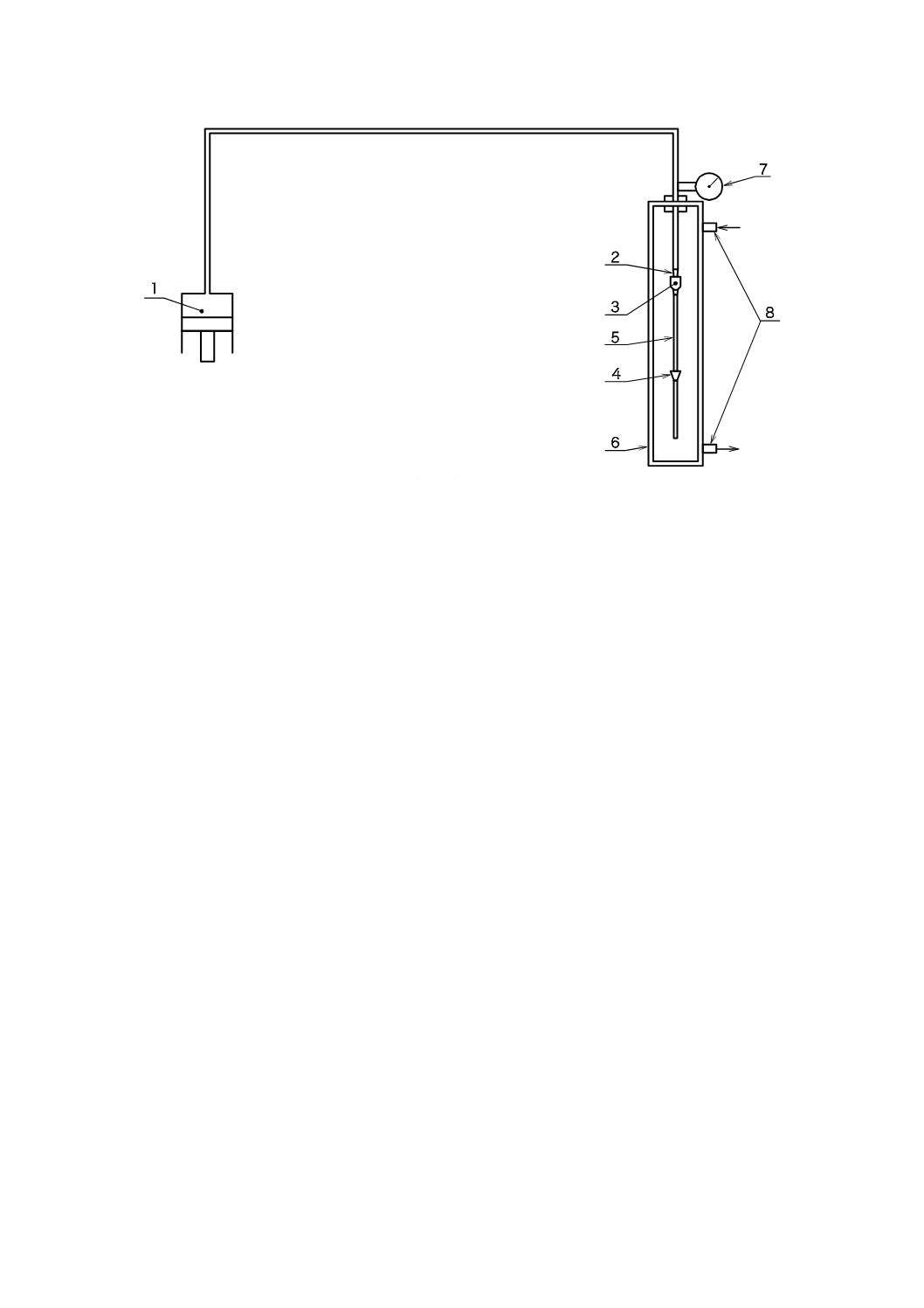
16
T 3268:2018
1 加圧装置(圧力源)
2 液漏れ防止コネクタ(D.2.2)
3 固定具(D.2.3)
4 開閉器(D.2.4)
5 試料(カテーテル)
6 液体で満たし,温度管理の可能な試験用チャンバ
7 圧力監視及び記録装置
8 試験用チャンバにおける入口及び出口ポート(任意)
図D.1−試験系の構成例
17
T 3268:2018
附属書E
(規定)
加圧注入試験(加圧注入に使用するものに限る。)
E.1
概要
カテーテルをハブ又は手元端で注入器に接続し,その先にコネクタ又は延長チューブを接続する。試験
系を注入用の液体又はその疑似液で満たす。製品の推奨圧で注入器の設定を行い,試験系での流量は容積
比又はその他の適切な方法によって算出する。カテーテルの手元端には,直接圧トランスデューサを接続
して最大圧力を記録する。
E.2
装置及び器具
E.2.1 定圧注入器 カテーテルに注液を行い,設定温度に対して±2 ℃,圧力に対して±5 %を試験にて
維持できるもの。
E.2.2 注入する液体又は疑似液 例として,グリセリン溶液など。試料に注入する液体は,粘度(力学的
粘度,液体の密度)の再現性をもって調製したもの(一例として,ISO 3104及びISO 3105を参照)。
E.2.3 コネクタ又は延長チューブ 内径及び長さは,カテーテルに対して実際に使用可能なもの。
E.2.4 圧トランスデューサ(インライン形)及び記録計 カテーテルと延長チューブとの間に配置するも
の。
E.2.5 流量を計測するための器具 ±2 %の精度で流量収支(マスバランス)を算出できるもの,タイマ,
又は流量計(直結形)。
注記 試験系の構成例を,図E.1に示す。これらの装置は複雑で多様であるため,その詳細は示さな
い。
E.3
手順
警告 定圧注入器の不具合による高圧液体の漏れに対して,試験を行う者を保護するための適切な予
防措置及び防護策を講じなければならない。
E.3.1 注入器のリザーバ部分を液で満たし,設定温度まで加温する。
E.3.2 接続チューブを注入器に接続する。また,圧力トランスデューサを延長チューブの患者側端に接続
する。
E.3.3 製造販売業者の指示に従ってカテーテルを組み立て,ハブに圧トランスデューサを接続する。注入
する液体を安全に回収するため,必要に応じてカテーテルの患者側端を固定する。
E.3.4 試験系内部の空気を取り除く。
E.3.5 注入器の圧力設定を規定値に設定する。
E.3.6 試験系に注液し,規定圧及び規定量に達するのを待ち,規定圧に達したならば記録する。また,カ
テーテルの手元端で規定の流量に達したことを記録する。持続的に流量をモニタリングする場合は,安定
した状態での流量を記録しておく。
E.3.7 流量収支(マスバランス)にて計測する場合には,注入する液体の回収時間が15秒を超えないも
のとし,その体積はメスシリンダ及び質量から液体の密度(E.2.2)を考慮して算出する。
18
T 3268:2018
E.4
試験報告書
試験報告書には,少なくとも次の事項を記載する。
a) 試料の個体識別(ロット番号など)
b) 注入液に関する記載,粘度[mPa・s]及び密度[kg/m3]並びに試験における温度
c) 発生した圧力(Pa)
d) 接続チューブの内径及び長さ
e) 安定な状態に達したときの試験系の流量(mL/s),及びカテーテルの手元端側での圧力(Pa)
1
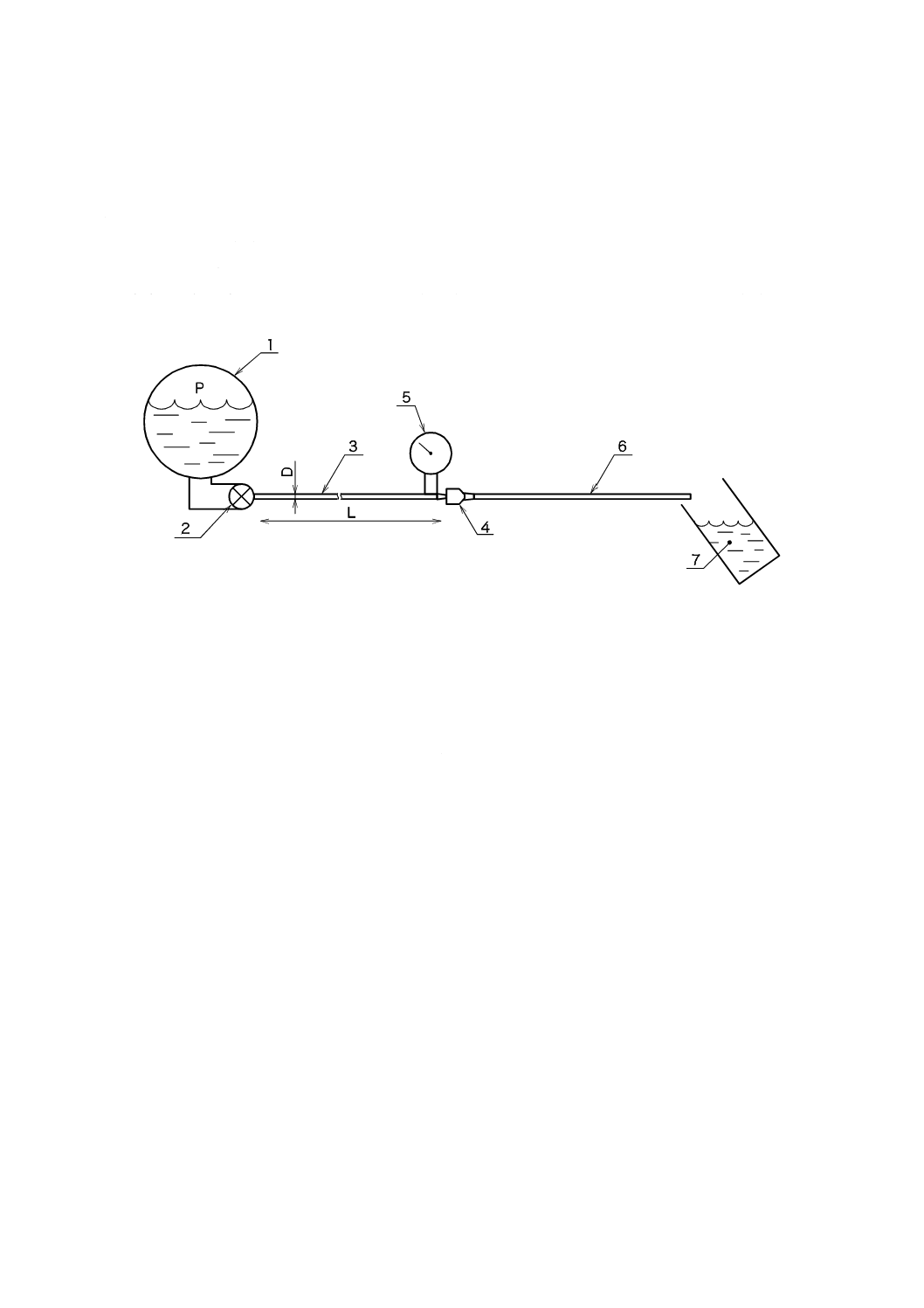
注入する液体(E.2.2)で満たした,一定の圧力Pが負荷できる定圧注入器(E.2.1)の例
2
注入制御のためのバルブ
3
延長チューブ(E.2.3)の長さL及び内径D
4
適宜,カテーテルの手元端の接続を補強するための固定具
5
圧トランスデューサ(インライン形)及び記録計(E.2.4)
6
試料(カテーテル)
7
流量を計測するための器具(E.2.5)の例
図E.1−加圧注入による流量及び耐圧の評価のための,試験系の構成例
19
T 3268:2018
附属書F
(規定)
カテーテルの流量
F.1
概要
カテーテルのくう(腔)に水を流し,体積又は水の質量を測定することによって流量を算出する。
F.2
試薬
F.2.1
水 蒸留水又は脱イオン水。生理食塩水を用いてもよい。
F.3
装置及び器具
F.3.1
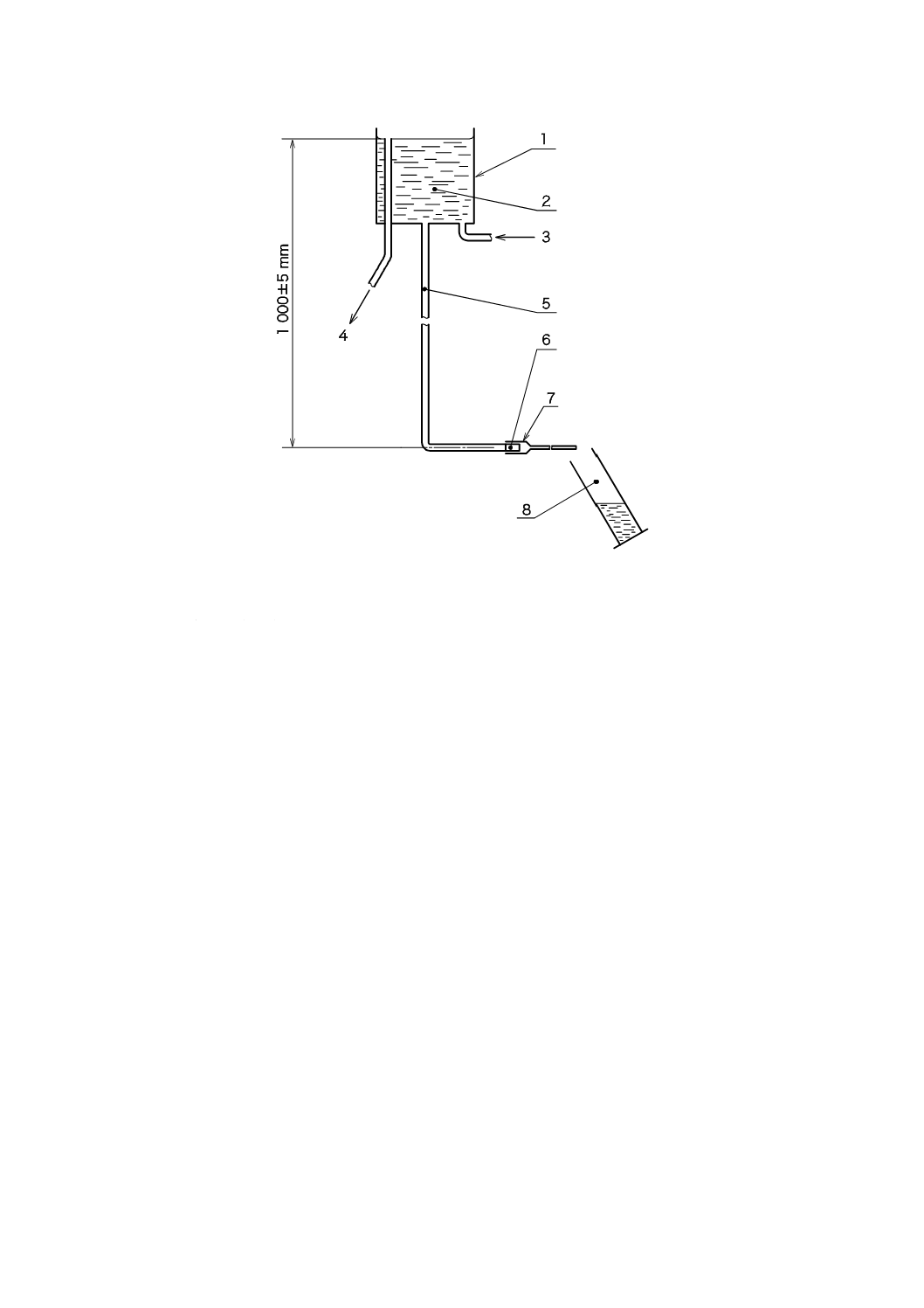
定水位タンク 注水用のチューブ及びおす(雄)のコネクタを備え,試料となるカテーテルを接続
しない状態で525±25 mL/minの流量を供給することが可能で,静水時の水位が1 000±5 mmで維持でき
るもの。
F.3.2
測定器具 カテーテルから流出した水を収集し,体積又は質量を±1 %の精度で測定できるもの。
F.3.3
タイマ 通水時間を測定するためのもの。
F.4
手順
F.4.1
定水位タンク(F.3.1)に22±2 ℃の水(F.2.1)を入れる。試料をおす(雄)のコネクタと接続す
る(図F.1)。
F.4.2
試料を通じて水を流し始める。試料から流出してきた水を一定時間(30秒以上とする。)適切な容
器に集め,これを測定器具にて体積を量るか,又は質量を量る。このとき,水の密度は1 000 kg/m3とする。
F.4.3
試料のそれぞれのくう(腔)にて3回ずつ測定を行う。
F.5
試験結果の表記
3回の測定結果の平均値を算出し,試料としたカテーテルの流量としてmL/minで表す。流量の計算値(平
均値)は,小数点以下第1位を四捨五入する。
F.6
試験報告書
試験報告書には,少なくとも次の事項を記載する。
a) 試料の個体識別(ロット番号など)
b) mL/minで表した,それぞれのくう(腔)の平均流量
20
T 3268:2018
1 定水位タンク(F.3.1)
2 水(F.2.1)
3 (定水位タンクの)注水口
4 (定水位タンクの)排水管
5 注水用チューブ
6 おす(雄コネクタ)
7 試料(カテーテル)
8 測定器具(F.3.2)
図F.1−試験系の構成例
21
T 3268:2018
附属書G
(規定)
加圧限界(RBP)の決定方法
G.1
概要
拡張用バルーンカテーテルのバルーンについて,その加圧限界を決定する。
G.2
装置及び器具
G.2.1 ガイドワイヤ カテーテルの使用に際して推奨するもの,又はそれと同等のもの。
G.2.2 恒温槽 37±2 ℃で管理できるもの。
G.2.3 漏れが確認できるための工夫 例えば,試験液に顔料を加える,圧力漏れモニタ及び流量モニタの
設置。
G.2.4 バルーンを膨張させるための液体 例えば,室温の水。
G.2.5 時間計測のための器具 一定の精度をもつもの。
G.2.6 定圧注入器(圧力源) 圧力測定のための器具と接続することができ,かつ,コネクタによってカ
テーテルと接続できるもの。さらに,±5 %の精度をもってバルーンの膨張圧を維持できるもの。
G.3
手順
G.3.1 定圧注入器(G.2.6)を液体(G.2.4)で満たす。
G.3.2 カテーテルの取扱説明書等によって,バルーンの膨張時にガイドワイヤの使用を指示しているもの
は,適切にガイドワイヤ(G.2.1)を挿入する。
G.3.3 カテーテルを定圧注入器に接続し,バルーン全体を37±2 ℃の恒温槽(G.2.2)に浸せき(漬)す
る。
G.3.4 カテーテルを2分以上平衡化させる。
G.3.5 バルーンの膨張操作に係る時間に対して,圧力プロファイルを取りながらカテーテルが破裂するか
損傷するまでバルーンを膨張させる。破裂時には,圧力,損傷の状態,箇所を記録する。
G.4
試験報告書
試験報告書には,少なくとも次の事項を記載する。
a) カテーテル(試料)の個体識別(ロット番号など)
b) バルーンの破裂に対する圧力について,拡張限界,及び最大値,最小値,標準偏差(kPa)
c) 損傷している場合,全ての試料に対する損傷の状況
22
T 3268:2018
附属書H
(規定)
バルーン膨張時の損傷及び漏れに対する疲労試験
H.1 概要
拡張用バルーンカテーテル(図H.1)のバルーンを,複数回,膨張と収縮とを繰り返す。このとき,バ
ルーンが膨張している状態で漏れ,破裂又はヘルニア化がないか試験する。
H.2 装置及び器具
H.2.1 ガイドワイヤ カテーテルの使用に際して推奨するもの,又はそれと同等のもの。
H.2.2 恒温槽 37±2 ℃で管理できるもの。
H.2.3 漏れが確認できるための工夫 例えば,試験液に顔料を加える,圧漏れモニタ及び流量モニタの設
置。
H.2.4 時間計測のための器具 一定の精度をもつもの。
H.2.5 定圧注入器(圧力源) 圧力測定のための器具と接続することができ,かつ,コネクタによってカ
テーテルと接続できるもの。さらに,±5 %の精度をもってバルーンの膨張圧を維持できるもの。
H.2.6 コンプライアンスチューブ (例えば,バルーンカテーテルをステントのデリバリーシステムとし
て使用する場合,この試験において血管を模したチューブを用いる。)使用する場合は,カテーテルに推奨
される血管径となっているもの。
H.3 手順
H.3.1 定圧注入器(H.2.5)を水又は同等の液体(妥当性をもって選択すること)で満たす。
H.3.2 バルーン膨張時にガイドワイヤの使用を求めるものについては,適切なガイドワイヤ(H.2.1)を
カテーテルに挿入する。
H.3.3 定圧注入器をカテーテルに接続し,少なくともバルーンの部分を37±2 ℃の条件の下,恒温槽に
浸せき(漬)する。コンプライアンスチューブを使用する場合には,コンプライアンスチューブにカテー
テルを挿入しておく。
H.3.4 2分以上カテーテルを(温度条件下で)平衡化する。加圧限界までバルーンを膨張させ,30秒間維
持してからバルーンを収縮させる。この操作を8回繰り返しながら漏れを確認する。
H.3.5 上記の操作によって,9回の膨張/収縮の後,更に1度バルーンを加圧限界まで膨張させ,恒温槽
からカテーテルを引き上げる。このとき,バルーンは膨張させたまま維持する。
H.3.6 カテーテル全体の漏れ,破損,ヘルニア化,バルーンの破損の方向性及び破損が起こった場合には
破損断片が生じたか否かを確認する。
H.3.7 試験報告書
試験報告書には,少なくとも次の事項を記載する。
a) カテーテル(試料)の個体識別(ロット番号など)
b) バルーンの膨張圧(kPa)
c) カテーテルに漏れが生じたか否か。
d) カテーテルシャフト及びバルーンの破損,並びにヘルニア化についての記載。バルーンの破損につい
23
T 3268:2018
ては,その方向及び破損断片が生じたか否かの記載
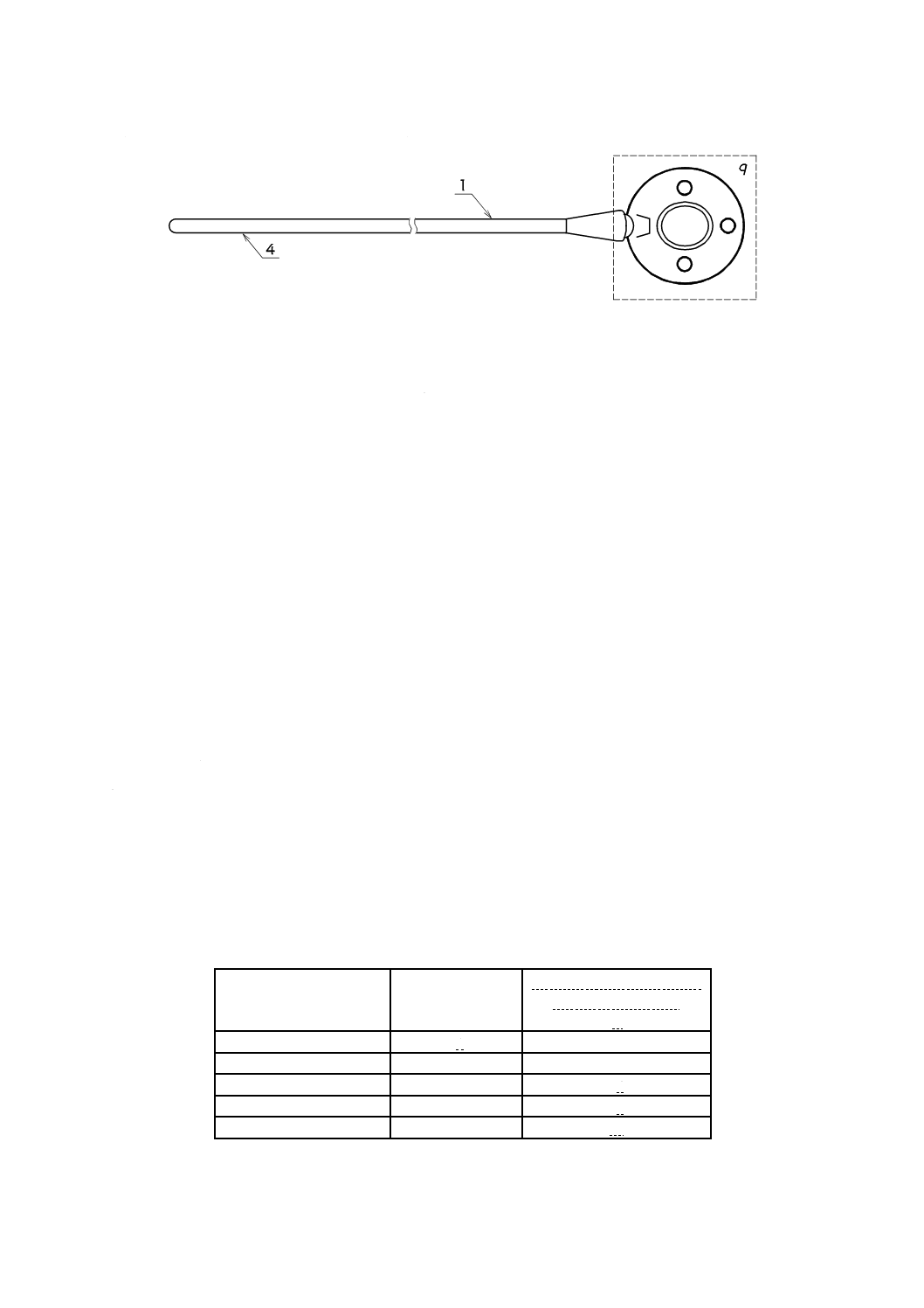
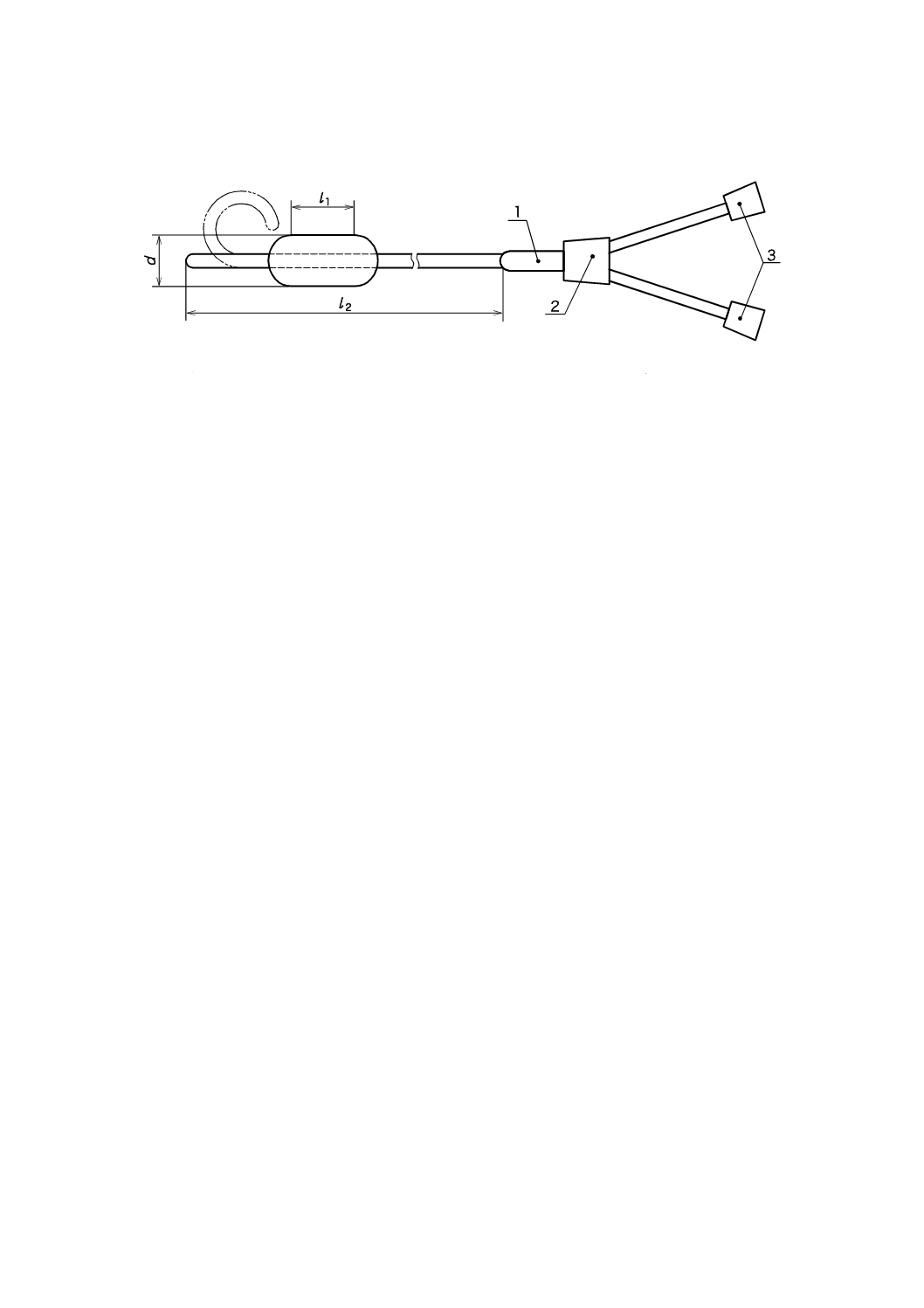
d 膨張時のバルーン径
l1 バルーンの有効長
l2 カテーテルの有効長
1 補強部(ストレインリリーフ)
2 接合部
3 ハブ
注記 この図は寸法を規定するものであるが,略図として使用している。
図H.1−拡張用バルーンカテーテルの寸法
24
T 3268:2018
附属書I
(規定)
バルーンの収縮時間に対する試験
I.1
概要
バルーンの加圧限界の状態から収縮状態までに要する時間を確認する。
I.2
装置及び器具
I.2.1
ガイドワイヤ カテーテルの使用に際して推奨するもの,又はそれと同等のもの。
I.2.2
恒温槽 37±2 ℃で管理できるもの。
I.2.3
バルーンを膨張させるための液体 取扱説明書等に従うもの,又はこれと同等のもの。
I.2.4
時間計測のための器具 一定の精度をもつもの。
I.2.5
定圧注入器(圧力源) 圧力測定のための器具と接続することができ,かつ,コネクタによってカ
テーテルと接続できるもの。さらに,±5 %の精度をもってバルーンの膨張圧を維持できるもの。
I.2.6
リジッドチューブ 必要な場合,バルーンの推奨径(最大値)のもの。
I.3
手順
I.3.1
取扱説明書等に従って定圧注入器(I.2.5)に液体を満たす。
I.3.2
カテーテルに適切なガイドワイヤを挿入する。
I.3.3
定圧注入器をカテーテルに接続し,少なくともバルーンの部分を37±2 ℃の条件で恒温槽(I.2.2)
に浸せき(漬)する。必要であれば,リジッドチューブ(I.2.6)にカテーテルを挿入する。
I.3.4
2分以上カテーテルを(温度条件下で)平衡化する。
I.3.5
取扱説明書等に従い,バルーンを加圧限界まで膨張させる。
I.3.6
取扱説明書等に従い,バルーンを収縮させ,規定する収縮状態に至るまでの時間を測定する。
I.4
試験報告書
試験報告書には,少なくとも次の事項を記載する。
a) カテーテル(試料)の個体識別(ロット番号など)
b) バルーンの収縮時間について,最大値,最小値,標準偏差(を秒で記載する。)
c) バルーンの収縮に対して,到達点(エンドポイント)の定義
d) バルーンの膨張に用いた液体に関する記載
e) その他,観察された異常等について。
25
T 3268:2018
附属書J
(規定)
膨張圧に対するバルーン径の確認方法
J.1
概要
バルーン径と膨張圧との相関性を確認する。
J.2
装置及び器具
J.2.1
ガイドワイヤ カテーテルの使用に際して推奨するもの,又はそれと同等のもの。
J.2.2
恒温槽 37±2 ℃で管理できるもの。
J.2.3
バルーンを膨張させるための液体 取扱説明書等に従うもの,又は水。
J.2.4
定圧注入器(圧力源) 圧力測定のための器具と接続することができ,かつ,コネクタによってカ
テーテルと接続できるもの。
J.2.5
バルーン径を測定するための器具 適切な精度をもち,10 %の許容差又は1 %の測定誤差にて計測
可能なもの(例 ミクロメータ,光学投影機,レーザミクロメータ)。許容差を規定する場合は,上記の
うち小さい方を用いなければならない。
J.3
手順
J.3.1
定圧注入器(J.2.4)にバルーンを膨張させるための液体(J.2.3)を満たす。
J.3.2
適切なガイドワイヤ(J.2.1)をカテーテルに挿入する。
J.3.3
定圧注入器をカテーテルに接続し,少なくとも,バルーンの部分を37±2 ℃の条件にて恒温槽
(J.2.2)に浸せき(漬)する。
J.3.4
2分以上カテーテルを(温度条件下で)平衡化する。
J.3.5
バルーンは徐々に膨張させる。その時々のバルーン径を確認するためにも,表示径を超えたら適宜
(例えば,100 kPaごと)膨張を止め,試験系を安定させて操作を行うことが望ましい。
J.3.6
それぞれの膨張圧にて,バルーンの適切な箇所の径を計測する。計測は試験系が安定したら速やか
に行うことが望ましい。
J.3.7
加圧限界に達するまでバルーンの膨張を止めない方がよい。
液体の粘弾性への影響を最小限に抑えるためにも,また,より臨床的な使用方法を模擬するためにも一
連の試験は速やかに完了させることが望ましい。
J.4
試験報告書
試験報告書には,少なくとも次の事項を記載する。
a) カテーテル(試料)の個体識別(ロット番号など)
b) バルーン径(mm)の最大値,最小値,標準偏差,及びこれに対する膨張圧(kPa)
26
T 3268:2018
参考文献
[1] ISO 3104,Petroleum products−Transparent and opaque liquids−Determination of kinematic viscosity and
calculation of dynamic viscosity
[2] ISO 3105,Glass capillary kinematic viscometers−Specifications and operating instructions
[3] ISO 80369-1,Small-bore connectors for liquids and gases in healthcare applications−Part 1: General
requirements
[4] ISO 80369-6,Small bore connectors for liquids and gases in healthcare applications−Part 6: Connectors for
neuraxial applications
[5] ISO 10993-1,Biological evaluation of medical devices−Part 1: Evaluation and testing within a risk
management process
[6] ISO 11070,Sterile single-use intravascular introducers, dilators and guidewires
[7] ISO 11135-1,Sterilization of health care products−Ethylene oxide−Part 1: Requirements for development,
validation and routine control of a sterilization process for medical devices
[8] ISO 11137-1,Sterilization of health care products−Radiation−Part 1: Requirements for development,
validation and routine control of a sterilization process for medical devices
[9] ISO 11607-1,Packaging for terminally sterilized medical devices−Part 1: Requirements for materials, sterile
barrier systems and packaging systems
[10] ISO 11607-2,Packaging for terminally sterilized medical devices−Part 2: Validation requirements for forming,
sealing and assembly processes
[11] ISO/TS 12417,Cardiovascular implants and extracorporeal systems−Vascular device-drug combination
products
[12] ISO 14630,Non-active surgical implants−General requirements
[13] ISO 14971,Medical devices−Application of risk management to medical devices
[14] ISO 17665-1,Sterilization of health care products−Moist heat−Part 1: Requirements for the development,
validation and routine control of a sterilization process for medical devices
[15] ISO 25539-2,Cardiovascular implants−Endovascular devices−Part 2: Vascular stents
[16] ASTM F640-12,Standard Test Methods for Determining Radiopacity for Medical Use
[17] Iserson KV. J.-F.-B. Charriere: the man behind the “French” gauge. 1987 Nov. (abstract only)
[18] Casey RG Joseph-Frederic-Benoit Charriere: master cutler and instrument designer. 2003 Mar. (abstract only)
[19] The Seldinger technique. Reprint from Acta Radiologica 1953. AJR Am. J. Roentgenol. 1984 Jan, 142 (1) pp.
5-7
[20] Nabil Kibriya, Rebecca Hall, Steven Powell, Thien How, Richard G. McWilliams: French Sizing of Medical
Devices is not Fit for Purpose. Cardio Vascular and Interventional Radiology January 2013

27
T 3268:2018
附属書JA
(参考)
JISと対応国際規格との対比表
JIS T 3268:2018 単回使用滅菌済み血管内カテーテル
ISO 10555-1:2013,Intravascular catheters−Sterile and single-use catheters−Part 1:
General requirements
ISO 10555-3:2013,Intravascular catheters−Sterile and single-use catheters−Part 3:
Central venous catheters
ISO 10555-4:2013,Intravascular catheters−Sterile and single-use catheters−Part 4:
Balloon dilatation catheters
(I)JISの規定
(II)国際
規格番号
(III)国際規格の規定
(IV)JISと国際規格との技術的差異の箇条ごと
の評価及びその内容
(V)JISと国際規格との技術的差
異の理由及び今後の対策
箇条番号
及び題名
内容
箇条番号
内容
箇条ごと
の評価
技術的差異の内容
1 適用範囲 血管内カテーテル
の適用範囲につい
て規定。
ISO 10555-1
ISO 10555-3
ISO 10555-4
1
1
1
滅菌済みにて供給
され,全ての用途に
対して単回使用と
される血管内カテ
ーテルの一般的要
求事項を規定。
変更
ISO 10555-1の適用範囲について,
血管内カテーテルの用途を追記し
た。
この規格では,クラスII医療機器
の認証基準及びクラスIII/IV医
療機器の承認基準となることから
生物由来材料又は抗菌剤によるコ
ーティングを除外した。また,吸
水膨潤形カテーテルを除外した。
国内事情であり,特に国際提案な
どはしない。
3 用語及び
定義
ISO 10555-1
ISO 10555-3
ISO 10555-4
3
3
3
JISとほぼ同じ
変更・追加 使用者の利便を考慮し,国内での
流通,呼び方などを考慮して変更,
追加した。
用語でもあることから実質的な差
異はない。
4 構成及び
各部の名称
血管内カテーテル
の種類,各部の名
称を例示した。
−
−
追加
ポート用カテーテルの例示のた
め,皮下植込み用ポート(この規
格の適用外)を参考として挿入し
た。
規格利用者の利便性を図るため追
加したが技術的な差異はない。
3
T
3
2
6
8
:
2
0
1
8
28
T 3268:2018
(I)JISの規定
(II)国際
規格番号
(III)国際規格の規定
(IV)JISと国際規格との技術的差異の箇条ごと
の評価及びその内容
(V)JISと国際規格との技術的差
異の理由及び今後の対策
箇条番号
及び題名
内容
箇条番号
内容
箇条ごと
の評価
技術的差異の内容
5 要求事項 5.1 外観及び清浄
度
ISO 10555-1
4.4
JISとほぼ同じ
変更
他のJISの要求事項に合わせて記
載。
対応国際規格の見直しの際,提案
を検討。
5.2 エックス線不
透過性
ISO 10555-1
ISO 10555-4
4.2
4.2
JISとほぼ同じ
変更
JISでは,透視下で使用する場合
に適用する。
対応国際規格の見直しの際,提案
を検討。
5.3 ハブ
ISO 10555-1
4.8
一致
−
5.4 破断強度
ISO 10555-1
4.6
JISとほぼ同じ
変更・追加 外径0.55 mm未満のカテーテルに
対する破断強度を設定した。また,
シリコーン製カテーテルの破断強
度を設定した。
シリコーン製カテーテルの破断強
度は,過去に制定された他の規格
による。国内事情のため。
5.5 カテーテルの
患者側(先)端及
び側孔
ISO 10555-1
4.11
4.12
一致
−
5.6 腐食抵抗性
ISO 10555-1
4.5
JISとほぼ同じ
変更
金属部分に対して試験を実施する
前提条件を追記した。
対応国際規格の見直しの際,提案
を検討。
5.7 気密性
ISO 10555-1
4.7.1
JISとほぼ同じ
変更
5.8 耐圧性(拡張用バルーンにつ
いては,5.10 バルーンカテーテル
を適用)を実施することによって
気密性を確認できるとして,その
旨を追記した。
対応国際規格の見直しの際,提案
を検討。
5.8 耐圧性
5.8.1 カテーテル
の耐圧性
ISO 10555-1
4.10
JISとほぼ同じ
変更
加圧注入を意図しない,使用時に
耐圧性を示す場合の血管内カテー
テルについても,耐圧性の要求事
項を適用することとした。拡張用
バルーンを備えるカテーテルは,
5.10.1を適用することとした。
対応国際規格の見直しの際,提案
を検討。
5.8.2 加圧注入に
使用するカテーテ
ルの耐圧性
ISO 10555-1
4.10
JISとほぼ同じ
変更
要求事項を5.8.1及び5.8.2に区分
した。
形式的な変更であり実質的な技術
的差異はない。
3
T
3
2
6
8
:
2
0
1
8

29
T 3268:2018
(I)JISの規定
(II)国際
規格番号
(III)国際規格の規定
(IV)JISと国際規格との技術的差異の箇条ごと
の評価及びその内容
(V)JISと国際規格との技術的差
異の理由及び今後の対策
箇条番号
及び題名
内容
箇条番号
内容
箇条ごと
の評価
技術的差異の内容
5 要求事項
(続き)
5.9 持続注入用カ
テーテル
5.9.1 くう(腔)の
認識
ISO 10555-3
4.3
一致
−
5.9.2 流量
ISO 10555-1
4.9
一致
−
5.10 バルーンカ
テーテル
5.10.1 拡張用バル
ーンカテーテル
ISO 10555-4
4.4.1
〜4.4.4
一致
−
5.10.2 その他のバ
ルーンの漏れ
−
−
追加
カテーテルがもつバルーンが耐圧
性のものではない場合を考慮し追
加した。
規格利用者の利便を考慮して追
加。
5.11 スネアカテ
ーテル
−
−
追加
スネアカテーテルの操作性につい
て追加した。
規格利用者の利便を考慮して追
加。
5.12 構成品
5.12.1 一般
5.12.2 せん(穿)
刺針〜5.12.7血管
造影用活栓
−
−
追加
キット品を想定し,規格利用者の
利便を考慮して追加。
対応国際規格の見直しの際,提案
を検討。
6 生物学的
安全性
ISO 10555-1
4.3
一致
−
7 無菌性の
保証
ISO 10555-1
4.1
JISとほぼ同じ
変更
ISO規格と同等の基準であり,国
内で実績のある基準を記載した。
技術的差異はない。
8 包装
8.1 一次包装
8.2 二次包装
−
−
追加
包装を一次包装と二次包装とに区
分した。
国内事情のため。
9 表示
9.1 一次包装
9.2 二次包装
ISO 10555-1
ISO 10555-3
ISO 10555-4
6
4.5
4.5
製造(販売)業者が
提供する情報
変更
表示事項を一次包装と二次包装と
に区分した。
国内事情のため。
9.3 図記号の使用
ISO 10555-1
6
JISとほぼ同じ
変更・追加 図記号の使用を追加した。
国内事情のため。
附属書A
(規定)
破断強度の測定方
法
ISO 10555-1
附属書B
一致
−
3
T
3
2
6
8
:
2
0
1
8

30
T 3268:2018
(I)JISの規定
(II)国際
規格番号
(III)国際規格の規定
(IV)JISと国際規格との技術的差異の箇条ごと
の評価及びその内容
(V)JISと国際規格との技術的差
異の理由及び今後の対策
箇条番号
及び題名
内容
箇条番号
内容
箇条ごと
の評価
技術的差異の内容
附属書B
(規定)
腐食抵抗性に対す
る試験方法
ISO 10555-1
附属書A
一致
−
附属書C
(規定)
カテーテルの気密
性
ISO 10555-1
附属書C
一致
−
附属書D
(規定)
一般的なカテーテ
ルの耐圧性
ISO 10555-1
附属書F
一致
−
附属書E
(規定)
加圧注入試験(加
圧注入に使用する
ものに限る。)
ISO 10555-1
附属書G
一致
−
附属書F
(規定)
カテーテルの流量
ISO 10555-1
附属書E
一致
−
附属書G
(規定)
加圧限界(RBP)
の決定方法
ISO 10555-4
附属書A
一致
−
附属書H
(規定)
バルーン膨張時の
損傷及び漏れに対
する疲労試験
ISO 10555-4
附属書B
一致
−
附属書I
(規定)
バルーンの収縮時
間に対する試験
ISO 10555-4
附属書C
一致
−
附属書J
(規定)
膨張圧に対するバ
ルーン径の確認方
法
ISO 10555-4
附属書D
一致
−
JISと国際規格との対応の程度の全体評価:(ISO 10555-1:2013,ISO 10555-3:2013,ISO 10555-4:2013,MOD)
注記1 箇条ごとの評価欄の用語の意味は,次による。
− 一致 ················ 技術的差異がない。
− 追加 ················ 国際規格にない規定項目又は規定内容を追加している。
− 変更 ················ 国際規格の規定内容を変更している。
注記2 JISと国際規格との対応の程度の全体評価欄の記号の意味は,次による。
− MOD ··············· 国際規格を修正している。
3
T
3
2
6
8
:
2
0
1
8














