T 3265:2018
(1)
目 次
ページ
序文 ··································································································································· 1
1 適用範囲························································································································· 1
2 引用規格························································································································· 1
3 用語及び定義 ··················································································································· 2
4 構成及び各部の名称 ·········································································································· 3
5 物理的要求事項 ················································································································ 4
5.1 外観及び清浄度 ············································································································· 4
5.2 気密性 ························································································································· 4
5.3 おすめす(雄雌)かん(嵌)合部,混注部,継ぎ管,導管及び附属品の接続及び/又は接合部 ····· 4
5.4 導管 ···························································································································· 5
5.5 流量調節器 ··················································································································· 5
5.6 混注部 ························································································································· 5
5.7 おすめす(雄雌)かん(嵌)合部······················································································ 5
5.8 保護キャップ ················································································································ 5
5.9 活栓 ···························································································································· 5
5.10 フィルタ ····················································································································· 5
5.11 輸液フィルタ ··············································································································· 5
5.12 輸血フィルタ ··············································································································· 5
5.13 逆止弁 ························································································································ 5
5.14 潤滑剤 ························································································································ 5
6 化学的要求事項 ················································································································ 6
7 生物学的安全性 ················································································································ 6
8 無菌性の保証 ··················································································································· 6
9 エンドトキシン ················································································································ 6
10 包装 ····························································································································· 6
10.1 一次包装 ····················································································································· 6
10.2 二次包装 ····················································································································· 6
11 表示 ····························································································································· 6
11.1 一次包装 ····················································································································· 6
11.2 二次包装 ····················································································································· 6
11.3 図記号の使用 ··············································································································· 7
附属書A(規定)漏れ試験の方法 ···························································································· 8
T 3265:2018
(2)
まえがき
この規格は,工業標準化法第14条によって準用する第12条第1項の規定に基づき,一般社団法人日本
医療機器テクノロジー協会(MTJAPAN)及び一般財団法人日本規格協会(JSA)から,工業標準原案を具
して日本工業規格を改正すべきとの申出があり,日本工業標準調査会の審議を経て,厚生労働大臣が改正
した日本工業規格である。
これによって,JIS T 3265:2012は改正され,この規格に置き換えられた。
この規格は,著作権法で保護対象となっている著作物である。
この規格の一部が,特許権,出願公開後の特許出願又は実用新案権に抵触する可能性があることに注意
を喚起する。厚生労働大臣及び日本工業標準調査会は,このような特許権,出願公開後の特許出願及び実
用新案権に関わる確認について,責任はもたない。
日本工業規格 JIS
T 3265:2018
滅菌済み延長チューブ
Sterile extension tubes for single use
序文
この規格は,2007年に制定され,2012年の改正を経て,今日に至っている。その後,この規格で引用し
ているコネクタ規格(ISO 594-1:1986及びISO 594-2:1998)に関して,新たにISO 80369-6及びISO 80369-7
が制定されたため,この規格においても引用規格として追加するよう改正をした。
1
適用範囲
この規格は,輸液,輸血,採血,採液,造影剤投与[高耐圧(150 kPaを超える圧力)で使用するものを
除く。]などの自然落下式及びポンプ式の流路を延長するために用いる滅菌済みで,そのまま直ちに使用で
き,かつ,単回使用する延長チューブ(以下,延長チューブという。)について規定する。
注記 2021年1月31日までJIS T 3265:2012を適用することができる。
2
引用規格
次に掲げる規格は,この規格に引用されることによって,この規格の規定の一部を構成する。これらの
引用規格のうちで,西暦年を付記してあるものは,記載の年の版を適用し,その後の改正版(追補を含む。)
は適用しない。西暦年の付記がない引用規格は,その最新版(追補を含む。)を適用する。
JIS T 0307 医療機器−医療機器のラベル,ラベリング及び供給される情報に用いる図記号
JIS T 0993-1:2012 医療機器の生物学的評価−第1部:リスクマネジメントプロセスにおける評価及
び試験
JIS T 3211:2011 滅菌済み輸液セット
JIS T 3213:2011 栄養用チューブ及びカテーテル
JIS T 3219:2011 滅菌済み輸液フィルタ
JIS T 3225:2011 滅菌済み輸血フィルタセット
JIS T 3320:2018 滅菌済み活栓
ISO 594-1:1986,Conical fittings with a 6 % (Luer) taper for syringes, needles and certain other medical
equipment−Part 1: General requirements
ISO 594-2:1998,Conical fittings with 6 % (Luer) taper for syringes, needles and certain other medical
equipment−Part 2: Lock fittings
ISO 80369-6:2016,Small bore connectors for liquids and gases in healthcare applications−Part 6: Connectors
for neuraxial applications
ISO 80369-7:2016,Small-bore connectors for liquids and gases in healthcare applications−Part 7: Connectors
for intravascular or hypodermic applications
2
T 3265:2018
3
用語及び定義
この規格で用いる主な用語及び定義は,次による。
3.1
導管
輸液剤,血液製剤,造影剤などを体内に導く流路となる管,又は採血,採液などの流路となる管。
3.2
おすめす(雄雌)かん(嵌)合部
おす(雄)又はめす(雌)のかん(嵌)合部がテーパ又は他の構造によって器具と器具との接続及び離
脱が可能な部分。
3.3
保護キャップ
おすめす(雄雌)かん(嵌)合部が直接外部に触れることを防ぐためのもの。
3.4
流量調節器
輸液,輸血などの速度を調節するもの。
3.5
開閉器
導管内を開放又は閉塞状態にするもの。
3.6
混注部
輸液,輸血若しくは造影剤投与時の薬剤混注,採血又は採液における流路との接続部分。
3.7
再シール性
混注部に針を刺通し,その後,針を抜いたとき,液が漏れない性質。針不使用式混注部については,製
造販売業者指定のおす(雄)側器具を抜き去った後のバルブシール性。
3.8
三方活栓
流路切替えが可能な薬剤混注部をもつもの。
3.9
多連活栓
三方活栓を2個以上つなげて一体化したもの。一体のものとして成形された本体を使用したもの,及び
三方活栓を接続又は接合して多連としたものがある。
3.10
フィルタ
輸液剤中の固形物を捕捉する又は血液製剤をろ過するもの。
3.11
輸液フィルタ
輸液剤中の微小異物,細菌及び真菌を除去するもの。
3.12
輸血フィルタ
3
T 3265:2018
保存血液など血液製剤中の微小異物を除去するもの。
3.13
逆止弁
輸液剤,血液製剤などの逆流を防止するもの。
3.14
エンドトキシン試験用水
日本薬局方(以下,“日局”という。)の医薬品各条に規定する“注射用水”又はその他の方法によって
製造した水で,エンドトキシン試験に用いるライセート(LAL)試薬の検出限界で反応を示さないもの。
3.15
一次包装
延長チューブを直接に覆う包装。延長チューブの無菌性を保持するためのものをいい,さらに,これが
二次包装される場合には,いわゆる“内袋”に該当する。ただし,無菌性を保持しないものもあり,その
場合は,保護キャップで延長チューブ内部の無菌性を保持する。
3.16
二次包装
一次包装を直接に覆う包装。通常,複数の一次包装をした延長チューブ,例えば,50セット(本)を入
れた包装。
4
構成及び各部の名称
延長チューブは,主として,おす(雄)かん(嵌)合部,導管及びめす(雌)かん(嵌)合部からなり,
開閉器,流量調節器,混注部(針を用いずに混注できる針不使用式のものもある。),三方活栓,多連活栓,
逆止弁,フィルタ,輸液フィルタ,輸血フィルタなどが付くもの,また,おすめす(雄雌)かん(嵌)合
部などに保護キャップが付くものもある。
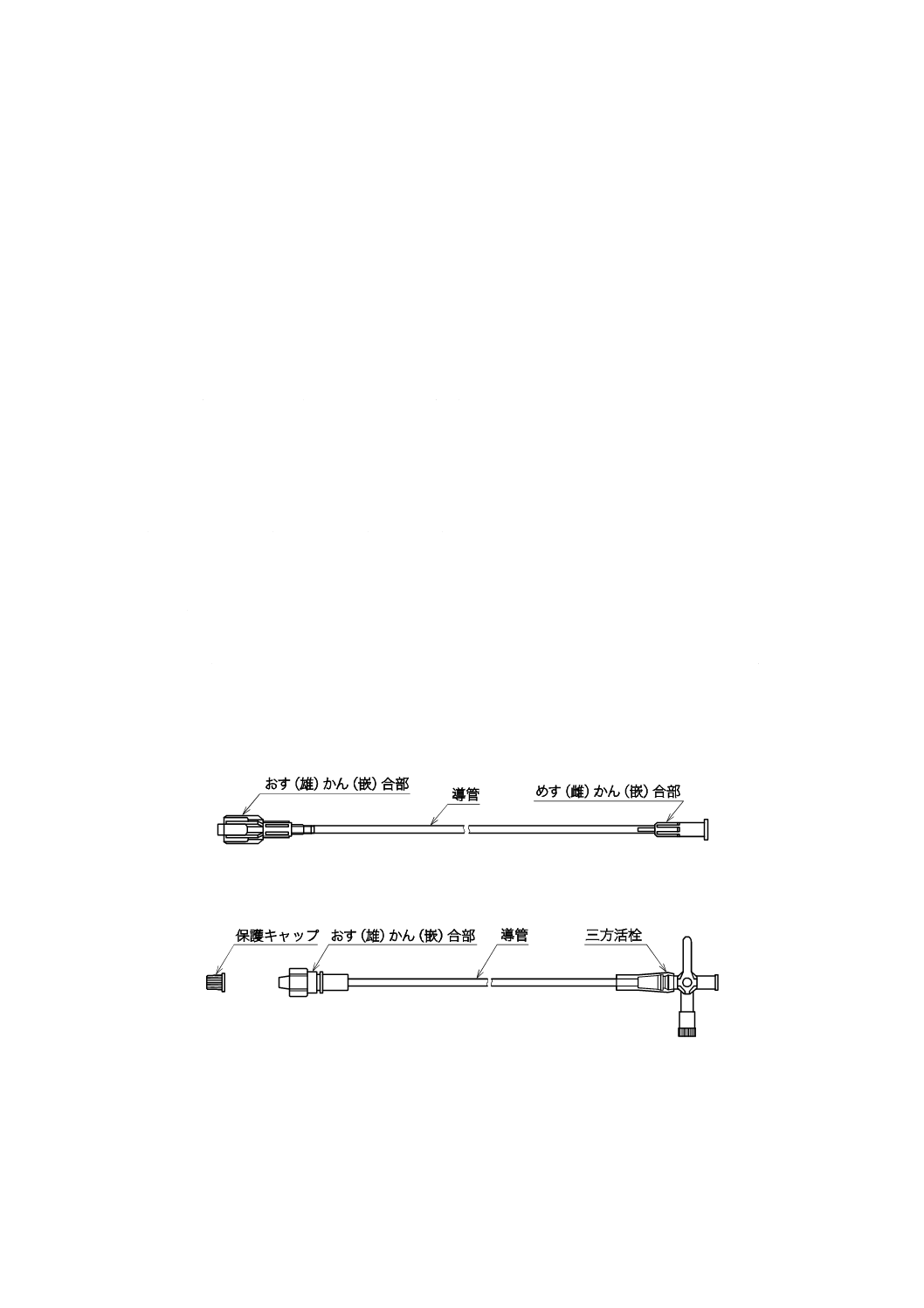
一般的な延長チューブの構成例及び各部の名称例を図1〜図4に示す。
図1−附属品のない延長チューブの構成及び各部の名称例
図2−三方活栓及び保護キャップが附属した延長チューブの構成及び各部の名称例
4
T 3265:2018
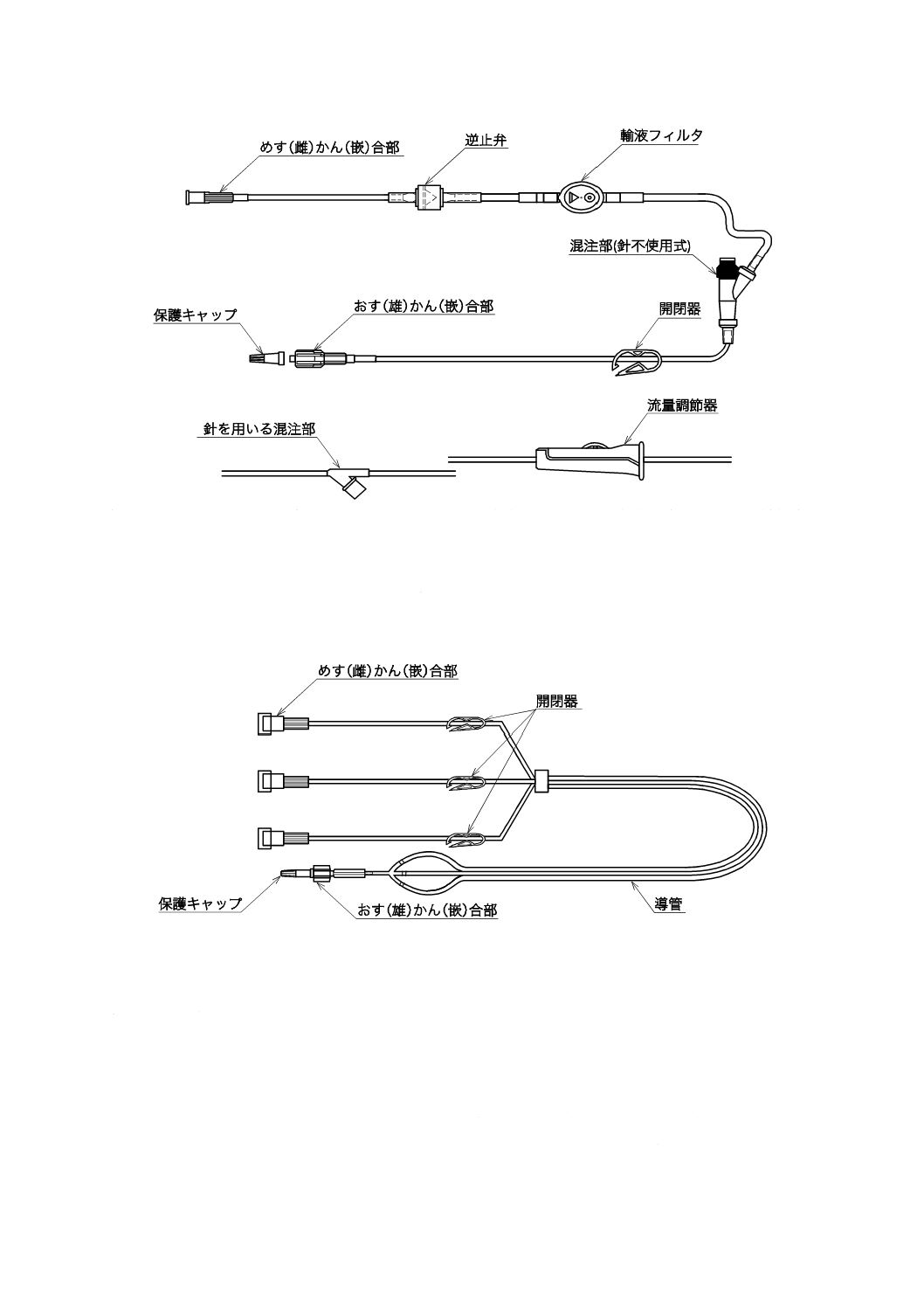
注記 混注部は,延長チューブの端部に直接接続,又はめす(雌)若しくはおす(雄)コネクタにかん(嵌)合で
接続使用する形式のものもある。
図3−開閉器,流量調節器,混注部,逆止弁及び輸液フィルタが附属した延長チューブの構成及び
各部の名称例
図4−多連仕様の延長チューブの構成及び各部の名称例
5
物理的要求事項
5.1
外観及び清浄度
目視で検査したとき,内面に微粒子又は異物の付着があってはならない。
5.2
気密性
JIS T 3211の5.2に適合しなければならない。
5.3
おすめす(雄雌)かん(嵌)合部,混注部,継ぎ管,導管及び附属品の接続及び/又は接合部
各接続部及び/又は接合部は,15 N以上の力で15秒間以上引っ張ったとき,緩んではならない。また,
5
T 3265:2018
ポンプ用延長チューブは,附属書Aによって試験したとき,接続部から水の漏れがあってはならない。
5.4
導管
JIS T 3211の5.6に適合しなければならない。
5.5
流量調節器
流量調節器は,JIS T 3211の5.9に適合しなければならない。
5.6
混注部
混注部の再シール性は,次に適合しなければならない。
a) 金属針を用いて混注する混注部
JIS T 3211の5.10 a) に適合しなければならない。
b) 針不使用式の混注部
JIS T 3211の5.10 b) に適合しなければならない。
c) 混注部が複数附属している場合は,各混注部は,a)及び/又はb)の試験をしたとき,1混注部当たり1
滴を超える漏れがなく,延長チューブの全ての混注部の漏れの合計が10滴を超えてはならない。
5.7
おすめす(雄雌)かん(嵌)合部
おすめす(雄雌)かん(嵌)合部は,ISO 594-1:1986及びISO 594-2:1998,又はISO 80369-6若しくは
ISO 80369-7に適合したものでなければならない。ただし,ISO 80369-6又はISO 80369-7を適用する場合
には,それぞれの規格の適用範囲に該当する製品でなければならない。さらに,製造販売業者が指定した
形状のおすめす(雄雌)かん(嵌)合部へ接続するように設計したもので,製造販売業者が指定する形状
のかん(嵌)合部へ製造販売業者が指定する方法で接続したとき,5.2及び5.3に適合し,かつ,JIS T 3213
又はISO 80369シリーズで規定するコネクタと接続できないものかのいずれかでなければならない。
注記 ISO 80369-6の適用範囲に該当する製品がISO 594-1:1986及びISO 594-2:1998を適用できる期
間については,“神経麻酔分野の小口径コネクタ製品の切替えについて”(平成29年12月27
日付け医政総発1227第1号,薬生薬審発1227第1号,薬生機審発1227第1号,薬生安発1227
第1号厚生労働省医政局総務課長,医薬・生活衛生局医薬品審査管理課長,同医療機器審査管
理課長,同医薬安全対策課長連名通知)に示されている。
5.8
保護キャップ
保護キャップは,JIS T 3211の5.12に適合しなければならない。
5.9
活栓
活栓は,JIS T 3320の5.2,5.3及び5.4に適合しなければならない。
5.10 フィルタ
フィルタは,JIS T 3211の5.7に適合しなければならない。
5.11 輸液フィルタ
輸液フィルタは,JIS T 3219の5.1,5.7及び5.8に適合しなければならない。
5.12 輸血フィルタ
輸血フィルタは,JIS T 3225の5.1,5.10,5.22及び5.23に適合しなければならない。
5.13 逆止弁
逆止弁は,JIS T 3211の5.16に適合しなければならない。
5.14 潤滑剤
三方活栓などに潤滑剤としてシリコーン油を用いる場合には,シリコーン油は,シリコーン油基準又は
これと同等以上の基準に適合しなければならない。
6
T 3265:2018
注記 シリコーン油基準には,厚生労働省が定めたシリコーン油基準がある。
6
化学的要求事項
JIS T 3211の箇条6に適合しなければならない。
7
生物学的安全性
JIS T 0993-1に規定する生物学的安全性の評価を行う。
8
無菌性の保証
無菌性の保証は,滅菌バリデーション基準又はこれと同等以上の基準に基づき,無菌性の担保を行う。
注記 滅菌バリデーション基準には,厚生労働省が定めた滅菌バリデーション基準がある。
9
エンドトキシン
延長チューブ10本をとり,各延長チューブの管内にエンドトキシン試験用水40 mLを約10 mL/minの
速さで流し,日局のエンドトキシン試験法によって試験を行ったとき,エンドトキシンは0.5 EU/mL未満
でなければならない。
10 包装
10.1 一次包装
一次包装は,微生物の侵入を防止することができ,かつ,通常の取扱い,輸送及び保管中に,内容製品
を適切に保護できるものでなければならない。また,一次包装は,一度開封したならば,簡単に再シール
できず,開封したことが明確に分からなければならない。ただし,無菌性を保証しないものの場合は,保
護キャップで延長チューブ内部の無菌性を保証する。
10.2 二次包装
二次包装は,通常の取扱い,輸送及び保管中に内容製品を保護できる強度をもたなければならない。
11 表示
11.1 一次包装
一次包装には,次の事項を表示する。
a) “滅菌済み”の旨
b) 製造番号又は製造記号
c) 天然ゴムを原材料として用いているものは,その旨
d) 一次包装で無菌性を保持しないものは,その旨
11.2 二次包装
二次包装には,次の事項を表示する。ただし,二次包装を用いないで,一次包装を最小販売単位の包装
として用いる場合には,次の事項を一次包装に表示する。
なお,製造番号又は製造記号が滅菌年月を表している場合には,改めて滅菌年月の表示をする必要はな
い。また,滅菌年月の代わりに使用期限を表示してもよい。
a) 製造販売業者の氏名又は名称,及び住所
b) 認証又は承認番号

7
T 3265:2018
c) 販売名
d) 数量(入り数)
e) “滅菌済み”の旨
f)
“再使用禁止”の旨(“ディスポーザブル”の表現は使用しない。)
g) ポンプ用の気密性を満足しないものは,“輸液及び輸血ポンプに使用できない”旨,又は組合せ使用で
安全が保証されているポンプの機種名。
h) ISO 594-1:1986及びISO 594-2:1998,又はISO 80369-6若しくはISO 80369-7に適合したかん(嵌)合
部に接続できない接続部を使用しているものは,ISO 594-1:1986及びISO 594-2:1998,又はISO 80369-6
若しくはISO 80369-7に適合したかん(嵌)合部へ接合できない旨。ただし,ISO 80369-6をかん(嵌)
合部に用いた場合には,k)の識別表示を行うことでよい。
注記 ISO 80369-6の適用範囲に該当する製品がISO 594-1:1986及びISO 594-2:1998を適用できる
期間については,“神経麻酔分野の小口径コネクタ製品の切替えについて”(平成29年12月
27日付け医政総発1227第1号,薬生薬審発1227第1号,薬生機審発1227第1号,薬生安
発1227第1号厚生労働省医政局総務課長,医薬・生活衛生局医薬品審査管理課長,同医療機
器審査管理課長,同医薬安全対策課長連名通知)に示されている。
i)
製造番号又は製造記号
j)
滅菌年月
k) ISO 80369-6をかん(嵌)合部に用いた場合には,識別表示を行う。識別は“ISO 80369-6”の文字又
はISO 80369-6に適合した製品であること等を表示する。
11.3 図記号の使用
11.1及び11.2の要件は,JIS T 0307に規定する適切な図記号を使用することによってこれに替えてもよ
い。
注記 JIS T 0307に規定する主な図記号の例を,表1に示す。
表1−JIS T 0307に規定する主な図記号の例
8
T 3265:2018
附属書A
(規定)
漏れ試験の方法
A.1 概要
リファレンスコネクタにおす(雄)かん(嵌)合部を接続する,又は製造販売業者が指定した形状のめ
す(雌)かん(嵌)合部へ接続するように設計されたおす(雄)かん(嵌)合部の場合には,製造販売業
者が指定する形状のめす(雌)かん(嵌)合部に製造販売業者が指定する方法で接続する。接続部に水圧
を加え,接続部からの漏れを検査する。
A.2 試薬
A.2.1 水 水道水又は同等以上の水。
A.3 器具
A.3.1 リファレンスコネクタ ISO 594-1:1986及びISO 594-2:1998,又はISO 80369-6若しくはISO
80369-7に規定するテーパをもつリファレンスコネクタ(Reference steel female conical fitting)。
A.3.2 加圧装置 150 kPaの圧力まで加圧及び測定できるゲージを取り付けた加圧装置。
A.3.3 恒温槽又は恒温室 23±1 ℃及び40±1 ℃の温度で試験ができるもの。
A.4 手順
ISO 594-1:1986及びISO 594-2:1998,又はISO 80369-6若しくはISO 80369-7に規定するおす(雄)かん
(嵌)合部は,ISO 594-1:1986及びISO 594-2:1998,又はISO 80369-6 Annex C若しくはISO 80369-7 Annex
Cに規定するリファレンスコネクタ(Reference steel female conical fitting)で密封し,そのかん(嵌)合部
に水を満たし,23±1 ℃及び40±1 ℃で150 kPaの圧力を15分間加え,接続部に漏れがないかを調べる。
ただし,ISO 80369-6に規定するかん(嵌)合部の場合は,300〜330 kPaの圧力を30〜35秒間加え,接続
部に漏れがないかを調べる。
注記 ISO 80369-6の適用範囲に該当する製品がISO 594-1:1986及びISO 594-2:1998を適用できる期
間については,“神経麻酔分野の小口径コネクタ製品の切替えについて”(平成29年12月27
日付け医政総発1227第1号,薬生薬審発1227第1号,薬生機審発1227第1号,薬生安発1227
第1号厚生労働省医政局総務課長,医薬・生活衛生局医薬品審査管理課長,同医療機器審査管
理課長,同医薬安全対策課長連名通知)に示されている。
製造販売業者が指定した形状のめす(雌)かん(嵌)合部へ接続するように設計したおす(雄)かん(嵌)
合部は,製造販売業者が指定する形状のめす(雌)かん(嵌)合部に製造販売業者が指定する方法で接続
し,そのかん(嵌)合部を水で満たし,圧力をかける反対側の開口部を密閉し,23±1 ℃及び40±1 ℃で
150 kPaの圧力を15分間加え,接続部に漏れがないかを調べる。
A.5 試験報告書
試験報告書には,次の情報を記載する。
a) 延長チューブの識別(ロット,品種など)
9
T 3265:2018
b) A.4の試験における漏れの有無


