T 3259:2012
(1)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
目 次
ページ
序文 ··································································································································· 1
1 適用範囲 ························································································································· 1
2 引用規格 ························································································································· 1
3 用語及び定義 ··················································································································· 2
4 構成及び各部の名称 ·········································································································· 2
5 要求事項 ························································································································· 2
5.1 一般的要求事項 ············································································································· 2
5.2 生物学的安全性 ············································································································· 2
5.3 表面 ···························································································································· 2
5.4 破断強度 ······················································································································ 3
5.5 かん(嵌)合 ················································································································ 3
5.6 耐圧性 ························································································································· 3
5.7 公称外径 ······················································································································ 3
5.8 有効長 ························································································································· 3
5.9 着色 ···························································································································· 3
5.10 エックス線不透過性 ······································································································ 3
6 包装······························································································································· 3
6.1 一次包装 ······················································································································ 3
6.2 二次包装 ······················································································································ 4
7 表示······························································································································· 4
7.1 一次包装 ······················································································································ 4
7.2 二次包装 ······················································································································ 4
7.3 図記号の使用 ················································································································ 4
附属書A(規定)破断強度の測定方法 ······················································································ 6
参考文献 ····························································································································· 7
附属書JA(参考)JISと対応国際規格との対比表 ······································································· 8
T 3259:2012
(2)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
まえがき
この規格は,工業標準化法第14条によって準用する第12条第1項の規定に基づき,日本医療器材工業
会(JMED)及び一般財団法人日本規格協会(JSA)から,工業標準原案を具して日本工業規格を改正すべ
きとの申出があり,日本工業標準調査会の審議を経て,厚生労働大臣が改正した日本工業規格である。
これによって,JIS T 3259:2007は改正され,この規格に置き換えられた。
この規格は,著作権法で保護対象となっている著作物である。
この規格の一部が,特許権,出願公開後の特許出願又は実用新案権に抵触する可能性があることに注意
を喚起する。厚生労働大臣及び日本工業標準調査会は,このような特許権,出願公開後の特許出願及び実
用新案権に関わる確認について,責任はもたない。
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
日本工業規格 JIS
T 3259:2012
オブチュレータ
Sterile obturators for single use
序文
この規格は,1998年に第1版として発行されたISO 14972を基に作成して2007年に制定されたJIS T
3259を見直し,使用者の利便性のため用語,文書構成などの内容を変更して改正した日本工業規格である。
なお,この規格で側線又は点線の下線を施してある箇所は,対応国際規格を変更している事項である。
変更の一覧表にその説明を付けて,附属書JAに示す。また,附属書JAは対応国際規格にはない事項であ
る。
1
適用範囲
この規格は,無菌状態で提供され,血管用及び透析用製品などのチューブ又はカテーテル(以下,チュ
ーブなどという。)の内くう(腔)に挿入し,体内からの液体(血液など)の漏出を防ぐとともに,チュー
ブなどの折れ防止のために使用するオブチュレータについて規定する。ただし,ウロキナーゼなどの生物
由来材料をコーティングして抗血栓性を発現させるオブチュレータには適用しない。
注記 この規格の対応国際規格及びその対応の程度を表す記号を,次に示す。
ISO 14972:1998,Sterile obturators for single use with over-needle peripheral intravascular catheters
(MOD)
なお,対応の程度を表す記号“MOD”は,ISO/IEC Guide 21-1に基づき,修正していること
を示す。
なお,平成27年9月30日までJIS T 3259:2007は適用することができる。
2
引用規格
次に掲げる規格は,この規格に引用されることによって,この規格の規定の一部を構成する。これらの
引用規格は,記載の西暦年の版を適用し,その後の改正版(追補を含む。)は適用しない。
JIS T 0307:2004 医療機器−医療機器のラベル,ラベリング及び供給される情報に用いる図記号
JIS T 0993-1:2012 医療機器の生物学的評価−第1部:リスクマネジメントプロセスにおける評価及
び試験
注記 対応国際規格:ISO 10993-1:2009,Biological evaluation of medical devices−Part 1: Evaluation and
testing within a risk management process(IDT)
JIS T 3261:2012 滅菌済みカテーテルイントロデューサ
ISO 594-1:1986,Conical fittings with a 6% (Luer) taper for syringes, needles and certain other medical
equipment−Part 1: General requirements
ISO 594-2:1998,Conical fittings with 6% (Luer) taper for syringes, needles and certain other medical
2
T 3259:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
equipment−Part 2: Lock fittings
3
用語及び定義
この規格で用いる主な用語及び定義は,次による。
3.1
オブチュレータ(Obturator)
チューブなどの内くう(腔)を塞ぎ,かつ,チューブなどの折れ防止のために,チューブなどに挿入す
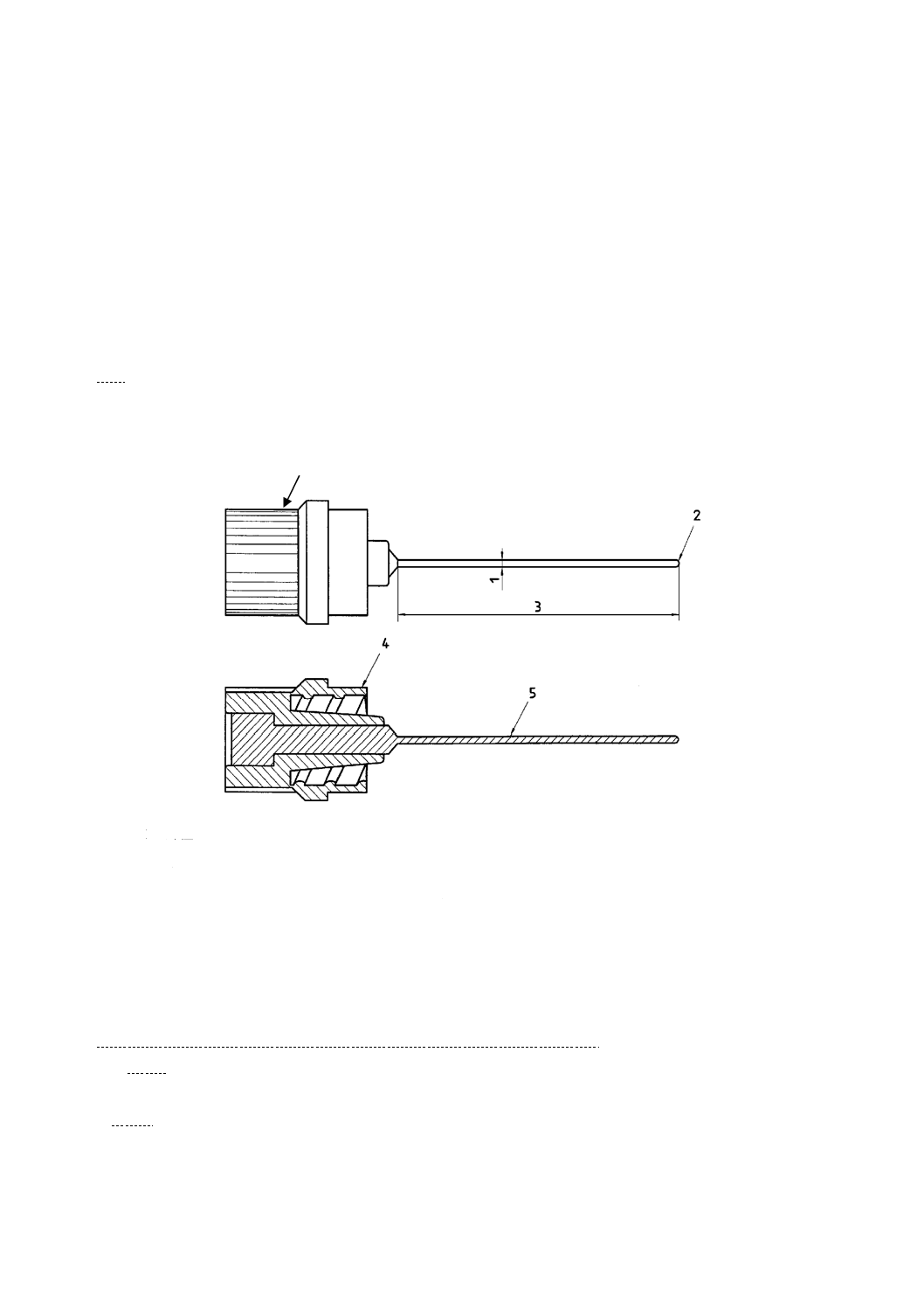
るよう設計された機器(図1参照)。
4
構成及び各部の名称
オブチュレータは,オブチュレータシャフト及び把持部で構成する。図1は,一般的なオブチュレータ
の例である。
1 外径
4 ルアー(ルアーロック)かん(嵌)合
2 チップ
5 オブチュレータシャフト
3 有効長
6 把持部
図1−オブチュレータの例
5
要求事項
5.1
一般的要求事項
無菌性の保証は,滅菌バリデーション基準又はこれと同等以上の基準に基づき,無菌性の担保を行う。
また,滅菌された状態で,5.2〜5.10の規定に適合しなければならない。
注記 滅菌バリデーション基準には,厚生労働省が定めた滅菌バリデーション基準がある。
5.2
生物学的安全性
JIS T 0993-1に規定する生物学的安全性の評価を行う。
5.3
表面
目視などで検査したとき,オブチュレータシャフトの有効長の表面に異物があってはならない。また,
6
3
T 3259:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
使用中に血管及びチューブなどへの損傷を最小限とするために,オブチュレータシャフトの表面及び先端
部は,滑らかで丸みがあり,異常又は欠陥があってはならない。
5.4
破断強度
附属書Aに従い,オブチュレータの破断強度は,表1に示す値とする。
表1−破断強度
オブチュレータシャフトの最小外径
mm
最小破断強度
N
0.35以上 0.75未満
3
0.75以上 1.15未満
5
1.15以上 1.85未満
8
1.85以上
12
5.5
かん(嵌)合
オブチュレータとチューブなどをかん(嵌)合させたとき,血液などが漏出しないようにオブチュレー
タは,次のいずれかでなければならない。
a) ルアーかん(嵌)合するものは,ISO 594-1又はISO 594-2に適合しなければならない。
b) ルアーかん(嵌)合でないものは,オブチュレータとチューブなどとが自然に外れたり,脱落しない
機構をもたなければならない。
5.6
耐圧性
オブチュレータ,チューブなどとがルアーかん(嵌)合でないものは,オブチュレータをかん(嵌)合
させてからJIS T 3261の附属書Dに従って試験したとき,かん(嵌)合部などからの液漏れがあってはな
らない。
5.7
公称外径
オブチュレータシャフトは,使用するチューブなどに確実に挿入できなければならない。
注記 “チューブなどに確実に挿入できる”とは,オブチュレータシャフトがチューブなどに挿入さ
れ,かつ,両者のかん(嵌)合によって血液などの漏出がなければよいことをいう。
5.8
有効長
オブチュレータをチューブなどに挿入したとき,オブチュレータはチューブなどの先端と一致するか,
又はチューブなどの先端から3.0 mm以上出てはならない。
5.9
着色
オブチュレータの把持部は,組み合わせて使用する製品(把持部)と同一の色でなければならない。
なお,組み合わせて使用する製品は,包装上に明確化しなければならない。
5.10 エックス線不透過性
オブチュレータが血管用に使用される場合には,エックス線不透過処理されていることが望ましい。
6
包装
6.1
一次包装
一次包装は,微生物の侵入を防止することができ,通常の取扱い,輸送及び保管中に内容製品に損傷の
おそれがないようにする。また,一度開封したら,包装は簡単に再シールできず,開封されたことが明確
に分かるものでなければならない。
4
T 3259:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
6.2
二次包装
二次包装は,通常の取扱い,輸送及び保管中に内容製品を保護できる強度をもたなければならない。
7
表示
7.1
一次包装
一次包装には,次の事項を表示する。
a) 製品の説明:併用するチューブなどを特定する。
なお,オブチュレータがキットに組み込まれている場合には,使用相手が特定されるため,当該記
載は要求しない。ただし,認証書などに,キットとして構成するもので,“単品で販売することがある。”
旨の記載があるものは,上記の記載方法に従うものとする。
b) オブチュレータの公称外径(mm)及び長さ(mm又はcm)。ただし,外径はミリメートル(mm)で
示すほか,フレンチ(シャリエール)又はゲージを参考に併記してもよい。
注記 フレンチ(シャリエール)は,F(Ch)などで表記するのがよい。1 mmは3 F(Ch)に相当
する。ゲージは,Gなどで表記するのがよい。
c) 製造番号又は製造記号
d) “滅菌済み”の旨
7.2
二次包装
二次包装には,次の事項を表示する。ただし,二次包装を用いないで,一次包装を最小包装単位の包装
として用いる場合には,次の事項を一次包装に記載する。
なお,製造番号又は製造記号が滅菌年月を表している場合は,改めて滅菌年月の表示をする必要はない。
また,滅菌年月の代わりに使用期限を表示してもよい。
a) 製造販売業者の氏名又は名称,及び住所
b) 販売名
c) 医療機器の認証番号
d) 製品の説明 使用対象製品を特定する旨。
なお,オブチュレータがキットに組み込まれている場合には,使用相手が特定されるため,当該記
載は要求しない。ただし,認証書などに,キットとして構成するもので,“単品で販売することがある。”
旨の記載があるものは,上記の記載方法に従うものとする。
e) オブチュレータの公称外径(mm)及び長さ(mm又はcm)。ただし,外径はミリメートル(mm)で
示すほか,フレンチ(シャリエール)又はゲージを参考に併記してもよい。
注記 フレンチ(シャリエール)は,F(Ch)などで表記するのがよい。ゲージは,Gなどで表記
するのがよい。
f)
製造番号又は製造記号
g) “滅菌済み”の旨
h) “再使用禁止”の旨(“ディスポーザブル”の表現は使用しない。)
i)
数量(入り数)
j)
滅菌年月
7.3
図記号の使用
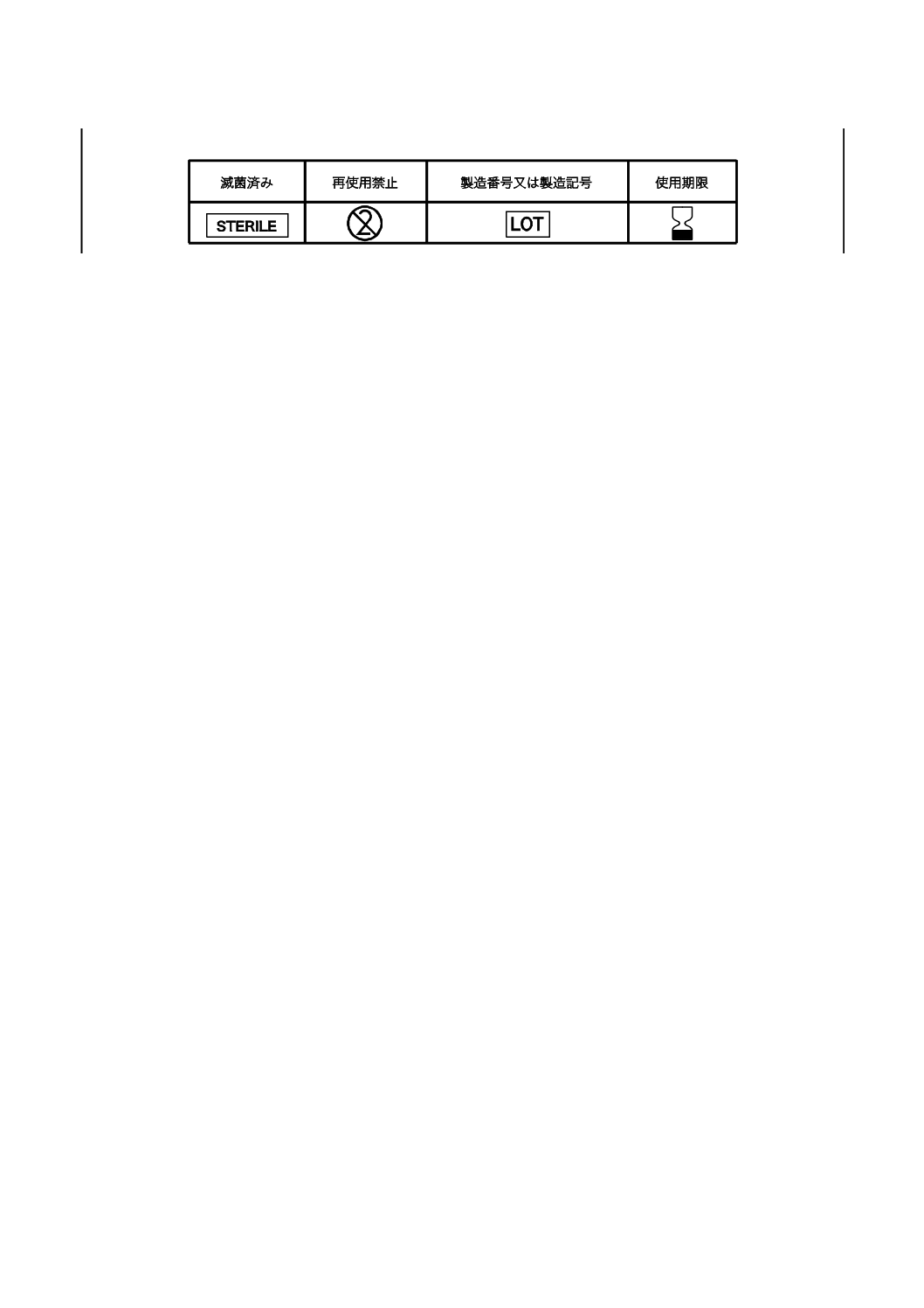
7.1及び7.2の要件は,JIS T 0307に規定する適切な図記号を使用することによってこれに替えてもよい。
注記 JIS T 0307に規定する主な図記号の例を,表2に示す。
5
T 3259:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
表2−JIS T 0307に規定する図記号の例
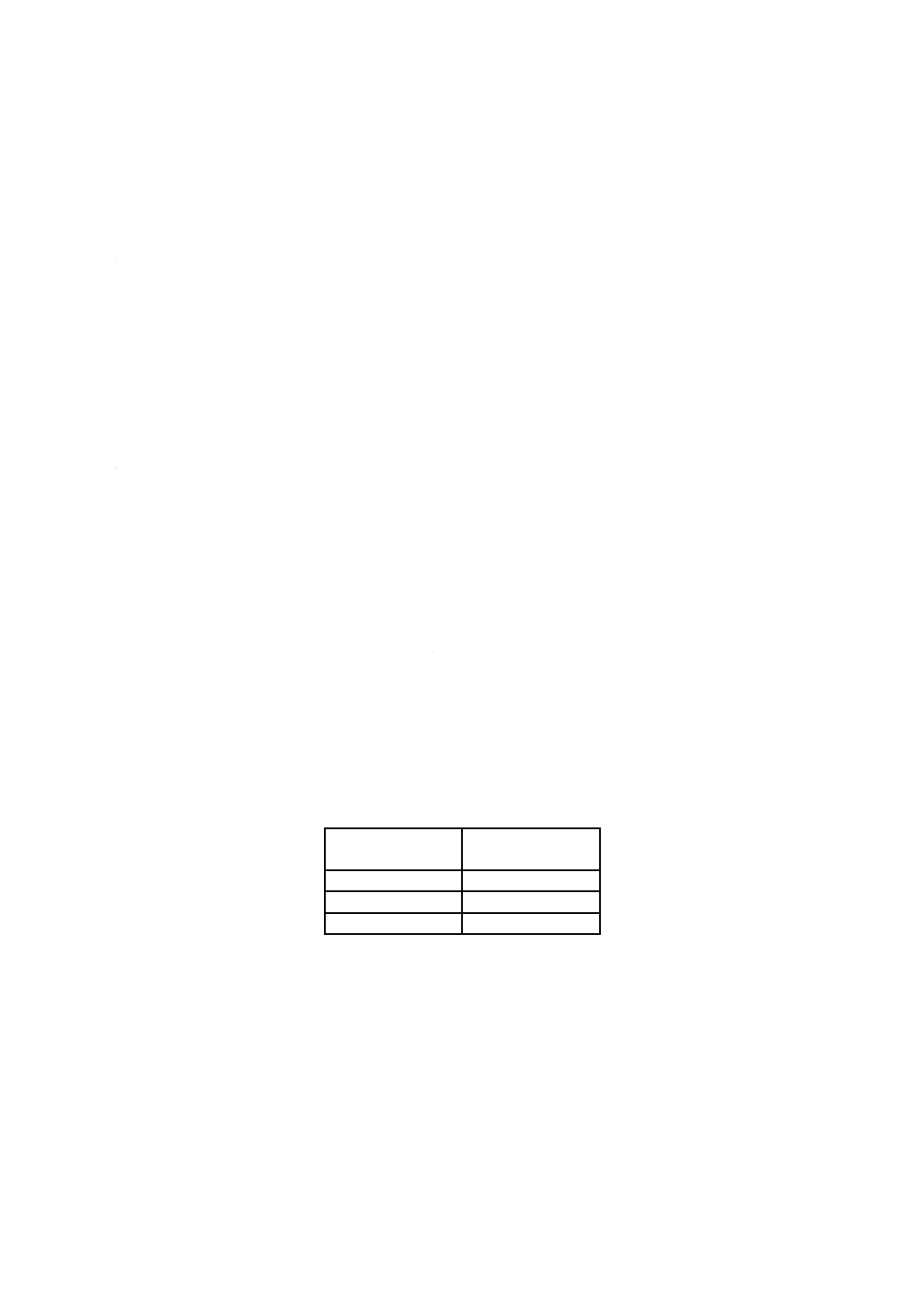
6
T 3259:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書A
(規定)
破断強度の測定方法
A.1 概要
オブチュレータとルアーかん(嵌)合との間の各オブチュレータ及び接続部が試験できるように,オブ
チュレータの試料を選択する。オブチュレータが破損するか又は接続部の外れが起きるまで,各試料に引
張力を加える。
A.2 機器
A.2.1
引張試験機 15 N以上の引張力があるもの
A.3 方法
A.3.1
オブチュレータの試験試料を選択する。試験試料にオブチュレータとルアーかん(嵌)合させたも
のの接続部を含める。
A.3.2
試料を37±2 ℃の(100 %相対湿度の)水中に2時間置く。その後,直ちに試験を行う。
A.3.3
引張試験機(A.2.1)に試料をセットする。オブチュレータ又はルアーかん(嵌)合の変形を避け
るため,適切な固定具を使用する。
A.3.4
試料のゲージ長を測定する。
注記 引張試験機のチャック間距離,又は該当する場合,ルアーかん(嵌)合と試験試料の他端を保
持するチャック間距離をいう。
A.3.5
試料が二つ以上に分離するまで,ゲージ長1 mm当たり20 mm/minの引張速度で引っ張る(表A.1
参照)。破断がおきる引張強度(ニュートン単位)の値に留意し,この値を破断強度として記録する。
A.3.6
各試料につき,試験を2回以上行ってはならない。
表A.1−ゲージ長1 mm当たり20 mm/minの引張速度に対応する条件例
ゲージ長
mm
引張速度
mm/min
10
200
20
400
25
500
A.4 試験報告書
試験報告書には,次の情報を記載する。
a) オブチュレータの識別
b) 試料の破断強度(ニュートン単位)及び外径
7
T 3259:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
参考文献
JIS T 0801-1:2010 ヘルスケア製品の滅菌−エチレンオキサイド−第1部:医療機器の滅菌プロセスの
開発,バリデーション及び日常管理の要求事項
注記 対応国際規格:ISO 11135-1:2007,Sterilization of health care products−Ethylene oxide−Part 1:
Requirements for development, validation and routine control of a sterilization process for medical
devices(IDT)
JIS T 0806-1:2010 ヘルスケア製品の滅菌−放射線−第1部:医療機器の滅菌プロセスの開発,バリデ
ーション及び日常管理の要求事項
注記 対応国際規格:ISO 11137-1:2006,Sterilization of health care products−Radiation−Part 1:
Requirements for development, validation and routine control of a sterilization process for medical
devices(IDT)
JIS T 0806-2:2010 ヘルスケア製品の滅菌−放射線−第2部:滅菌線量の確立
注記 対応国際規格:ISO 11137-2:2006,Sterilization of health care products−Radiation−Part 2:
Establishing the sterilization dose(IDT)
JIS T 0806-3:2010 ヘルスケア製品の滅菌−放射線−第3部:線量測定にかかわる指針
注記 対応国際規格:ISO 11137-3:2006,Sterilization of health care products−Radiation−Part 3: Guidance
on dosimetric aspects(IDT)
JIS T 0816-1 ヘルスケア製品の滅菌−湿熱−第1部:医療機器の滅菌プロセスの開発,バリデーション
及び日常管理の要求事項
注記 対応国際規格:ISO 17665-1,Sterilization of health care products−Moist heat−Part 1: Requirements
for the development, validation and routine control of a sterilization process for medical devices(IDT)
JIS T 3249 血液透析用留置針
注記 対応国際規格:ISO 10555-5,Sterile, single-use intravascular catheters−Part 5: Over-needle peripheral
catheters(MOD)
ISO/TS 11135-2,Sterilization of health care products−Ethylene oxide−Part 2: Guidance on the application of
ISO 11135-1
8
T
3
2
5
9
:
2
0
1
2
8
T
3
2
5
9
:
2
0
1
2
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書JA
(参考)
JISと対応国際規格との対比表
JIS T 3259:2012 オブチュレータ
ISO 14972:1998 Sterile obturators for single use with over-needle peripheral
intravascular catheters
(I)JISの規定
(II)
国際
規格
番号
(III)国際規格の規定
(IV)JISと国際規格との技術的差異の箇条
ごとの評価及びその内容
(V)JISと国際規格との技術的差
異の理由及び今後の対策
箇条番号及
び題名
内容
箇条番号
内容
箇条ごと
の評価
技術的差異の内容
1 適用範囲
無菌状態で提供され,血管
用及び透析用製品などの
チューブ又はカテーテル
の内くう(腔)に挿入し,
体内からの液体(血液な
ど)の漏出を防ぐととも
に,チューブなどの折れ防
止のために使用するオブ
チュレータについて規定
する。ただし,ウロキナー
ゼなどの生物由来材料を
コーティングして抗血栓
性を発現させるオブチュ
レータには適用しない。
1
JISとほぼ同じ
追加
血管用及び透析用への適用及び
使用中のチューブなどの折れ防
止について追加。
生物由来材料をコーティングし
たオブチュレータは,適用しな
い旨を追加。
適用範囲を明確にするため追加
規定。次回のISO規格見直し時に
本JISをMODからIDTにするこ
とを検討。
2 引用規格
3 用語及び
定義
3.1 オブチュレータ
3.1
JISとほぼ同じ
追加
使用中のチューブなどの折れ防
止の追加。
規格使用者の利便を考慮し,追
加。
4 構成及び
各部の名称
オブチュレータシャフト
及び把持部で構成
−
−
追加
3.1を分割化して記載。
規格使用者の利便を考慮し,追
加。
5 要求事項
5.1 一般的要求事項
4.1
JISとほぼ同じ
変更
滅菌バリデーション基準を明記。
5.2 生物学的安全性
4.2
JISとほぼ同じ
変更
ISOは注記に,JISは本文に規
定。
実質的な差異はない。
9
T
3
2
5
9
:
2
0
1
2
9
T
3
2
5
9
:
2
0
1
2
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
(I)JISの規定
(II)
国際
規格
番号
(III)国際規格の規定
(IV)JISと国際規格との技術的差異の箇条
ごとの評価及びその内容
(V)JISと国際規格との技術的差
異の理由及び今後の対策
箇条番号及
び題名
内容
箇条番号
内容
箇条ごと
の評価
技術的差異の内容
5 要求事項
(続き)
5.3 表面
4.3
JISとほぼ同じ
追加
チューブなどを追加。
チューブなどへの損傷も考慮し
て追加。規格使用者の利便を考慮
し,追加。
5.4 破断強度
4.4
変更
細分箇条番号の変更
実質的な差異はない。
5.5 かん(嵌)合
4.5
JISとほぼ同じ
追加
ルアーかん(嵌)合でないもの
を追加。
かん(嵌)合の内容を明確にする
ため追加。次回のISO規格見直し
時に提案を検討。
5.6 耐圧性
−
−
追加
ルアーかん(嵌)合でないもの
の耐圧性を追加。
ISO規格に規定されたかん(嵌)
合以外の内容を明確にするため
追加。
5.7 公称外径
4.6
JISとほぼ同じ
変更
チューブなどに挿入できる内容
を記載。
規格使用者の利便を考慮し,追
加。
5.8 有効長
4.7
変更
細分箇条番号の変更
実質的な差異はない。
5.9 着色
4.8
JISとほぼ同じ
変更
組み合わせて使用する製品は,
包装上に明確化することを規
定。
実質的な差異はない。
6 包装
6.1 一次包装
6.2 二次包装
−
−
追加
一次包装及び二次包装に区分し
た。
実質的な差異はない。
7 表示
7.1 一次包装
7.2 二次包装
4.10
JISとほぼ同じ
変更
一次包装及び二次包装に区分し
た。
実質的な差異はない。
7.3 図記号の使用
−
−
追加
図記号の使用を追加。
JISと国際規格との対応の程度の全体評価:ISO 14972:1998,MOD
注記1 箇条ごとの評価欄の用語の意味は,次による。
− 追加……………… 国際規格にない規定項目又は規定内容を追加している。
− 変更……………… 国際規格の規定内容を変更している。
注記2 JISと国際規格との対応の程度の全体評価欄の記号の意味は,次による。
− MOD…………… 国際規格を修正している。