T 3254:2013
(1)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
目 次
ページ
序文 ··································································································································· 1
1 適用範囲························································································································· 1
2 引用規格························································································································· 1
3 用語及び定義 ··················································································································· 1
4 構成及び各部の名称 ·········································································································· 2
5 採血針の物理的要求事項 ···································································································· 3
6 採血容器の物理的要求事項 ································································································· 3
6.1 外観及び清浄度 ············································································································· 3
6.2 潤滑剤 ························································································································· 3
6.3 潤滑剤の量 ··················································································································· 3
6.4 目盛線 ························································································································· 3
6.5 テーパの合致 ················································································································ 4
6.6 気密性 ························································································································· 4
6.7 通気性 ························································································································· 4
7 化学的要求事項 ················································································································ 4
8 抗凝固能························································································································· 4
9 無菌性の保証 ··················································································································· 4
10 生物学的安全性 ·············································································································· 5
11 エンドトキシン ·············································································································· 5
12 包装 ····························································································································· 5
12.1 採血容器及び/又は採血針の個々の包装 ··········································································· 5
12.2 一次包装 ····················································································································· 5
12.3 二次包装 ····················································································································· 5
13 表示 ····························································································································· 5
13.1 一次包装 ····················································································································· 5
13.2 二次包装 ····················································································································· 6
13.3 図記号の使用 ··············································································································· 6
T 3254:2013
(2)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
まえがき
この規格は,工業標準化法第14条によって準用する第12条第1項の規定に基づき,日本医療器材工業
会(JMED)及び一般財団法人日本規格協会(JSA)から,工業標準原案を具して日本工業規格を改正すべ
きとの申出があり,日本工業標準調査会の審議を経て,厚生労働大臣が改正した日本工業規格である。こ
れによって,JIS T 3254:2007は改正され,この規格に置き換えられた。
この規格は,著作権法で保護対象となっている著作物である。
この規格の一部が,特許権,出願公開後の特許出願又は実用新案権に抵触する可能性があることに注意
を喚起する。厚生労働大臣及び日本工業標準調査会は,このような特許権,出願公開後の特許出願及び実
用新案権に関わる確認について,責任はもたない。
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
日本工業規格
JIS
T 3254:2013
血液ガス検体採取用注射筒
Single-use syringes for blood gas specimen collection
序文
この規格は,2007年に制定され今日に至っている。今回,使用者の利便性のため用語,文書構成などの
内容を変更して改正した日本工業規格である。
なお,対応国際規格は現時点で制定されていない。
1
適用範囲
この規格は,動脈又は血液回路から,血液ガス分析用検体として血液を採取し,血液を空気に触れずに
保管できる針なし採血容器,針付採血容器,又は採血容器と針とのキット包装品において,滅菌済みでそ
のまま直ちに使用でき,かつ,単回使用する血液ガス検体採取用注射筒について規定する。
なお,平成28年8月31日までJIS T 3254:2007は適用することができる。
2
引用規格
次に掲げる規格は,この規格に引用されることによって,この規格の規定の一部を構成する。これらの
引用規格は,記載の年の版を適用し,その後の改正版(追補を含む。)は適用しない。
JIS T 0307:2004 医療機器−医療機器のラベル,ラベリング及び供給される情報に用いる図記号
JIS T 0993-1:2012 医療機器の生物学的評価−第1部:リスクマネジメントプロセスにおける評価及
び試験
JIS T 3209:2011 滅菌済み注射針
ISO 594-1:1986,Conical fittings with a 6 % (Luer) taper for syringes, needles and certain other medical
equipment−Part 1: General requirements
ISO 594-2:1998,Conical fittings with 6 % (Luer) taper for syringes, needles and certain other medical
equipment−Part 2: Lock fittings
ISO 7886-1:1993,Sterile hypodermic syringes for single use−Part 1:Syringes for manual use
3
用語及び定義
この規格で用いる主な用語及び定義は,次による。
3.1
採血針
採血容器に付け,血液ガス検体採取時に動脈へせん(穿)刺する滅菌済み注射針。
3.2
採血容器
2
T 3254:2013
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
血液ガス検体採取用に用いる注射筒様容器。滅菌して供給する。
3.3
公称採血量
包装又は容器に表示した採血量又は最大目盛容量。
3.4
目盛線
公称採血量に応じた一定の容量ごとに,容器の軸方向に対して垂直で等間隔に目盛った線。容量を示す
目盛数字を付した線もある。
3.5
ファーストライン
採血容器の外筒の目盛に合わせるガスケットの先端の最初のピークのライン。
3.6
抗凝固剤
血液の凝固を防止する薬剤。
3.7
密封用具
採血後,採血容器の筒先,又は採血針の針先に装着し,血液と空気との接触を遮断する部品。滅菌して
供給する場合と,滅菌せずに供給する場合がある。
3.8
採血容器及び採血針の個々の包装
採血容器及び採血針を個々に包装滅菌し,一次包装に封入するときに用いる包装。無菌維持を目的とし
た包装は無菌性を保持するものである。また,一次包装に未滅菌品の密封用具と滅菌された採血容器及び
採血針とを同時に入れる場合,相互の交差汚染を防止するために施す場合もある。
3.9
一次包装
採血針,採血容器などをまとめて直接に覆う包装で,血液ガス検体採取用注射筒全体の無菌性を保持す
るためのもの。さらに,これを二次包装する場合には,いわゆる“内袋”に該当する。ただし,一次包装
で無菌性を保持しないものもあり,その場合は,採血針,採血容器などに個々に包装を施し,無菌性を保
持している。
3.10
二次包装
一次包装した血液ガス検体採取用注射筒などを複数[例えば,50セット(本)]入れた包装。
4
構成及び各部の名称
血液ガス検体採取用注射筒は,採血針を採血容器に装着したもの,採血容器及び採血針が未包装又は個々
包装してセット若しくはキット包装したもの,又は採血容器単体のものがある。採血容器は,主として外
筒,ガスケット及び押子からなり,抗凝固剤を封入しているものもある。ガスケットには空気を抜くため
のフィルタが組み込まれているものがある。附属品として密封用具を一次包装に封入している,又は採血
針に組み込んでいるものがあり,採血針には針刺し事故防止装置があるものもある。
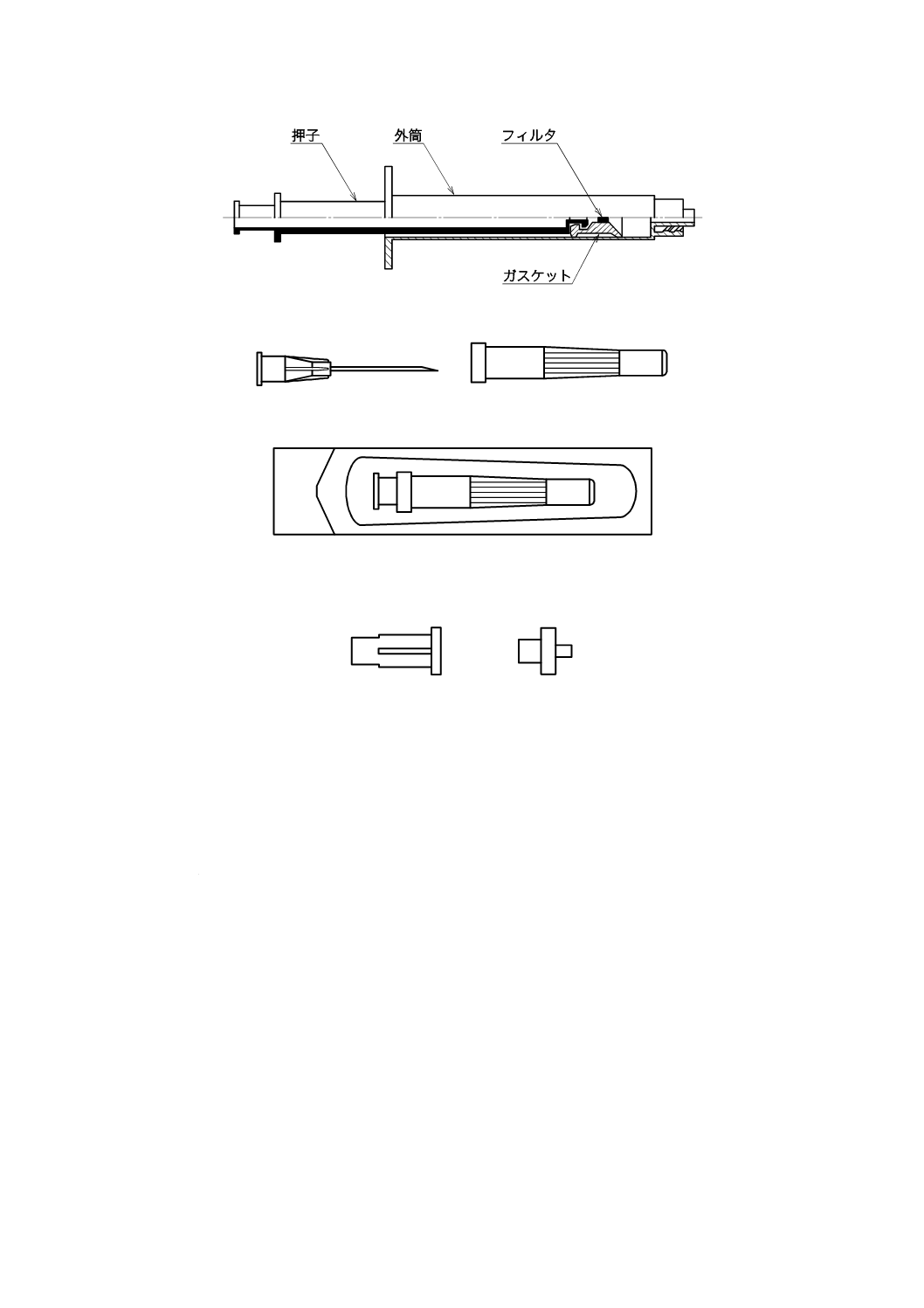
一般的な血液ガス検体採取用注射筒の構成品の例を,図1〜図3に示す。
3
T 3254:2013
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
図1−採血容器例
a) 採血針
b) プロテクタ
c) 包装品
図2−採血針例
図3−密封用具例
5
採血針の物理的要求事項
採血針が附属する場合,採血針はJIS T 3209:2011の箇条4,箇条8,箇条10,箇条11,箇条12及び箇
条13の規定に適合しなければならない。
6
採血容器の物理的要求事項
6.1
外観及び清浄度
採血容器の外筒の内面は,凹凸及びきずがなく,仕上げ面が滑らかでなければならない。また,目視し
たとき,通常の使用で血液が接触する部分には微粒子又は異物の付着があってはならない。
6.2
潤滑剤
潤滑剤としてシリコーン油を用いる場合,シリコーン油は,シリコーン油基準又はこれらと同等以上の
基準に適合するものでなければならない。また,シリコーン油以外の潤滑剤を用いる場合は,ISO
7886-1:1993の潤滑剤に規定するエルカ酸,又はオレイン酸の脂肪酸アミドを用いることができる。
注記 シリコーン油基準には,厚生労働省が定めたシリコーン油基準がある。
6.3
潤滑剤の量
潤滑剤の量は,採血容器の内表面を目視したとき,液滴を認めず,筒先にたまりができてはならない。
6.4
目盛線
採血容器の目盛線及び容量の単位の表示は,ゼロ目盛から公称採血量目盛まで均等で,明瞭かつ容易に
4
T 3254:2013
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
消えてはならない。
6.5
テーパの合致
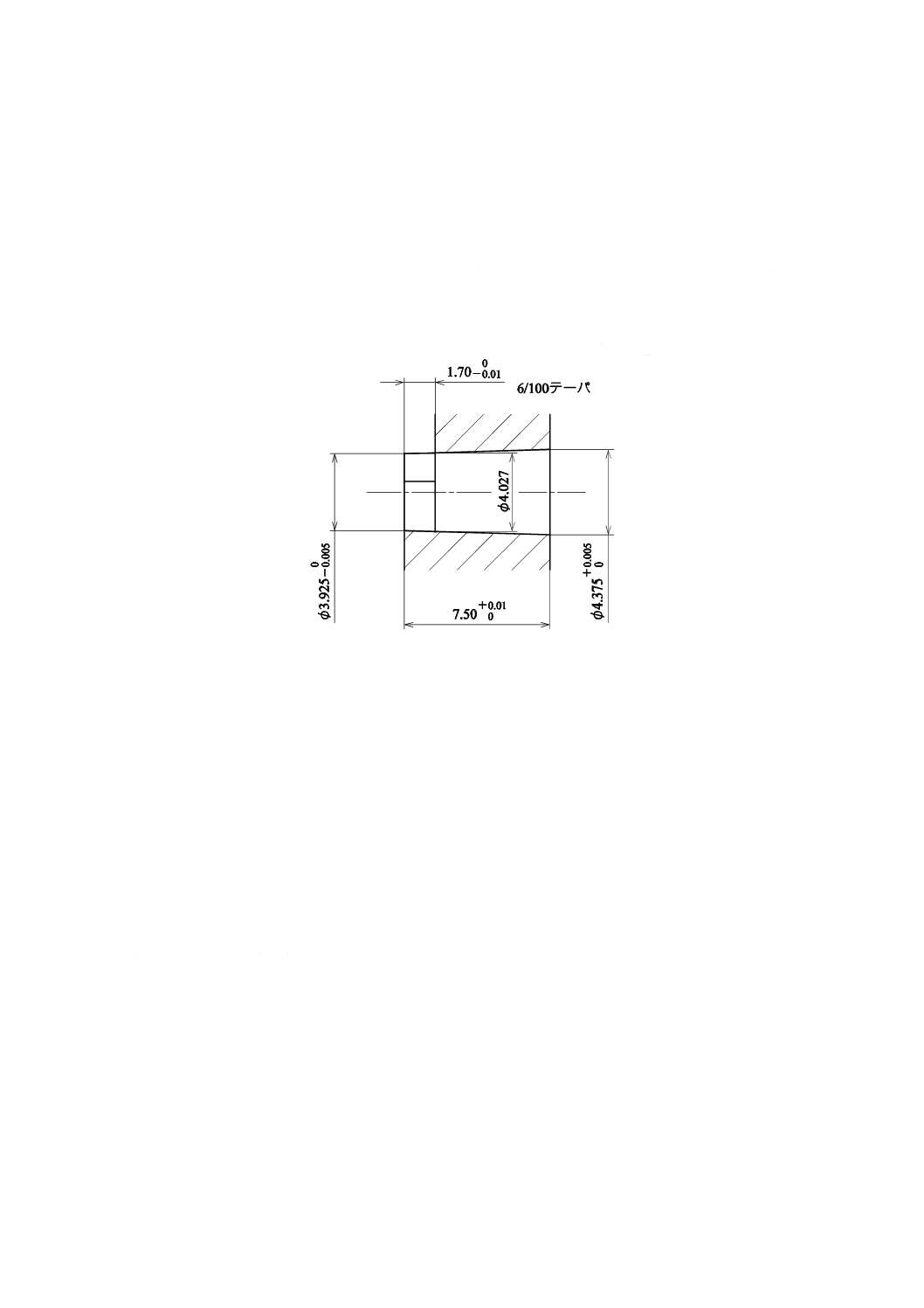
採血容器の筒先は,図4に示すISO 594-1:1986のルアーテーパ検査ゲージ[ISO 594-1:1986の図3 b)参
照]を使用できる構造のものは,筒先を5 Nの力でゲージに入れたとき,筒先のおす(雄)・ルアーテーパ
とゲージのテーパとが合致し,かつ,筒先の先端は,ゲージの限度内になければならない。また,筒先が
図4に示す検査ゲージを使用できない構造(ロック接合)のものは,ISO 594-2:1998のロック接合に規定
する検査ゲージを用いる。
単位 mm
図4−めす(雌)・ルアーテーパ検査ゲージ
6.6
気密性
製造販売業者の指定する使用方法に従って,採血容器へ公称採血量まで水を満たす。フィルタのあるも
のは,フィルタへ水の浸透が終了するまで放置する。採血容器の筒先を閉じ,40 kPaの圧力を押子へ10
秒間かけたとき,ガスケット,外筒及びフィルタからの漏れがあってはならない。また,これと同等以上
の方法で試験したとき,ガスケット,外筒及びフィルタからの漏れがあってはならない。
6.7
通気性
空気を抜くためのフィルタがガスケットに組み込まれているものは,採血容器を公称採血量の採血状態
にして,筒先から水を5.3 kPaの圧力で押し込んだときフィルタまで水が入るものとする。
7
化学的要求事項
採血針が附属する場合,採血針は,JIS T 3209:2011の箇条5の規定に適合しなければならない。
8
抗凝固能
採血容器へ規定採血量の新鮮血を採取し,製造販売業者が指定した方法でかくはん(撹拌)したとき,
目視できる血液の凝固塊が発生してはならない。
9
無菌性の保証
無菌性を保証する場合は,滅菌バリデーション基準又はこれと同等以上の基準に基づき,無菌性の担保
を行う。
5
T 3254:2013
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
注記 滅菌バリデーション基準には,厚生労働省が定めた滅菌バリデーション基準がある。
10 生物学的安全性
採血針が附属する場合,採血針は,JIS T 0993-1:2012に基づき生物学的安全性の評価を行う。
11 エンドトキシン
採血針が附属する場合,採血針は,JIS T 3209:2011の箇条7の規定に適合しなければならない。
12 包装
12.1 採血容器及び/又は採血針の個々の包装
採血容器及び/又は採血針を個々に包装滅菌した後,一次包装に封入する場合で,個々の包装を無菌維
持の目的で行う場合は,使用前に容易に破れるおそれがなく,微生物の侵入を防止することができ,通常
の取扱い,輸送,及び保管中に製品を適切に保護できるものでなければならない。また,一度開封したら,
包装は簡単に再シールできず,開封したことが明確に分かるものでなければならない。ただし,無菌維持
を目的としない場合には,包装は簡単に再シールできず,開封したことが明確に分かるものとする。採血
容器及び採血針の個々の包装は,してもしなくてもよい。
12.2 一次包装
一次包装は,使用前に容易に破れるおそれがなく,微生物の侵入を防止することができ,通常の取扱い,
輸送,及び保管中に製品を適切に保護できるものでなければならない。また,一度開封したら,包装は簡
単に再シールできず,開封したことが明確に分かるものでなければならない。ただし,無菌維持を目的と
した包装が採血容器と採血針ともに施されている場合は,使用前に容易に破れるおそれがなく,通常の取
扱い,輸送,及び保管中に製品を適切に保護できるものとする。
一次包装には,1セットを超えて封入してはならない。ただし,密封用具単品を未滅菌で供給する場合
は,多数個入りの包装で供給してもよい。この一次包装は,輸送,及び保管中に製品を適切に保護できる
ものとする。
12.3 二次包装
二次包装は,通常の取扱い,輸送及び保管中に製品を保護できる強度をもたなければならない。
13 表示
13.1 一次包装
一次包装には,次の事項を表示する。ただし,一次包装内の封入物が個包装されており,個々に次の該
当する必要事項が表示してあり,一次包装の外から個々の表示が見える場合は,個々の封入物の包装に表
示してある表示は,一次包装から省略してもよい。また,密封用具が単品で供給される場合はa)〜e)の該
当する事項だけとする。
a) 採血針が入っている場合は,採血針の外径(mm),及び長さ(mm)
b) 公称採血量(mL)
c) 抗凝固剤名
d) 一次包装内の密封用具を含め全てを無菌保証するものは,“滅菌済み”の旨。未滅菌の密封用具を封入
してある場合は,無菌保証する構成品の名称。
e) 製造番号又は製造記号

6
T 3254:2013
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
13.2 二次包装
二次包装には,次の事項を表示する。ただし,二次包装を用いないで,一次包装を最小販売単位の包装
として用いる場合には,次の事項を一次包装に表示する。
なお,製造番号又は製造記号が滅菌年月を表している場合には,滅菌年月の表示をする必要はない。ま
た,滅菌年月の代わりに使用期限を表示してもよい。また,密封用具が単品で供給される場合はa)〜k)ま
での該当する事項だけとする。
a) 製造販売業者の氏名又は名称,及び住所
b) 販売名
c) 採血針が入っている場合は,採血針の外径(mm),及び長さ(mm)
d) 公称採血量(mL)
e) 抗凝固剤名
f)
数量(入り数)
g) 一次包装内の構成品の全てを無菌保証するものは,“滅菌済み”の旨。全てを無菌保証しない場合は,
無菌保証する構成品の名称を記載又は,“滅菌済み”の旨の記載はしない。
h) “再使用禁止”の旨(“ディスポーザブル”の表現は使用しない。)
i)
製造番号又は製造記号
j)
滅菌年月
k) 他の法定表示事項
13.3 図記号の使用
13.1及び13.2は,JIS T 0307:2004に規定する適切な図記号を使用することによってこれに替えてもよい。
注記 JIS T 0307:2004に規定する主な図記号の例を表1に示す。
表1−JIS T 0307に規定する主な図記号の例


