T 3245:2011
(1)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
目 次
ページ
序文 ··································································································································· 1
1 適用範囲 ························································································································· 1
2 引用規格 ························································································································· 1
3 用語及び定義 ··················································································································· 1
4 構成及び各部の名称 ·········································································································· 2
5 附属器具類 ······················································································································ 3
6 要求事項 ························································································································· 3
6.1 寸法 ···························································································································· 3
6.2 外観及び清浄度 ············································································································· 3
6.3 引張強さ ······················································································································ 3
6.4 シャフト近位部 ············································································································· 3
6.5 シャフト遠位部 ············································································································· 4
6.6 生物学的安全性 ············································································································· 4
6.7 無菌性の保証 ················································································································ 4
7 包装······························································································································· 4
7.1 一次包装 ······················································································································ 4
7.2 二次包装 ······················································································································ 4
8 表示······························································································································· 4
8.1 一次包装 ······················································································································ 4
8.2 二次包装 ······················································································································ 4
8.3 記号の使用 ··················································································································· 5
附属書A(規定)引張強さに対する試験 ··················································································· 6
T 3245:2011
(2)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
まえがき
この規格は,工業標準化法第14条によって準用する第12条第1項の規定に基づき,日本医療器材工業
会(JMED)及び財団法人日本規格協会(JSA)から,工業標準原案を具して日本工業規格を改正すべきと
の申出があり,日本工業標準調査会の審議を経て,厚生労働大臣が改正した日本工業規格である。
これによって,JIS T 3245:2005は改正され,この規格に置き換えられた。
この規格は,著作権法で保護対象となっている著作物である。
この規格の一部が,特許権,出願公開後の特許出願又は実用新案権に抵触する可能性があることに注意
を喚起する。厚生労働大臣及び日本工業標準調査会は,このような特許権,出願公開後の特許出願及び実
用新案権に関わる確認について,責任はもたない。
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
日本工業規格 JIS
T 3245:2011
配偶子・はい(胚)移植用チューブ及びカテーテル
Tubes and catheters designed for gamete or embryo transfers
序文
この規格は,2005年に制定されたJIS T 3245の見直しにおいて,使用者の利便性のため用語,文書構成
などの内容を変更して改正した日本工業規格である。
1
適用範囲
この規格は,経子宮けい(頸)管的,経子宮筋層的又は経腹的に子宮内,卵管内などに,精子及び卵子
又は受精卵[はい(胚)]を注入する目的で,一時的に体内に挿入する配偶子・はい(胚)移植用チューブ
及びカテーテル(以下,カテーテルという。)について規定する。
なお,平成26年7月28日までJIS T 3245:2005は適用することができる。
2
引用規格
次に掲げる規格は,この規格に引用されることによって,この規格の規定の一部を構成する。これらの
引用規格は,記載の西暦年の版を適用し,その後の改正版(追補を含む。)は適用しない。
JIS T 0307:2004 医療機器−医療機器のラベル,ラベリング及び供給される情報に用いる図記号
JIS T 0993-1:2005 医療機器の生物学的評価−第1部:評価及び試験
JIS T 3209:2011 滅菌済み注射針
3
用語及び定義
この規格で用いる主な用語及び定義は,次による。
3.1
カテーテル
精子及び卵子又は受精卵[はい(胚)]を注入する目的で,経子宮けい(頸)管的,経子宮筋層的又は経
腹的に子宮内,卵管内などに挿入する管状の器具。チューブともいう。
3.2
シャフト
主に体内に挿入されるカテーテルの本体部分。
3.3
コネクタ
注射筒などを接続するため,シャフト遠位部に具備される継ぎ手。
3.4
外筒
2
T 3245:2011
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
シャフトの誘導,補強などを目的にシャフトにかぶ(被)された,スライド又は取外し可能な器具。ガ
イドカニューラ又はガイドシースともいう。
3.5
ストッパ
シャフト又は外筒を体内に挿入するときの位置決めをする,移動可能な器具。
3.6
スタイレット
シャフト又は外筒挿入時の誘導,補強などの器具。オブチュレータともいう。
3.7
シャフト遠位部
他の器具などと接続する側のシャフト末端部。
3.8
シャフト近位部
患者の体内へ挿入する側のシャフト末端部。
3.9
先端開口部
シャフト近位部の中央開口部。
3.10
側孔
シャフト近位部付近の側方開口部。
4
構成及び各部の名称
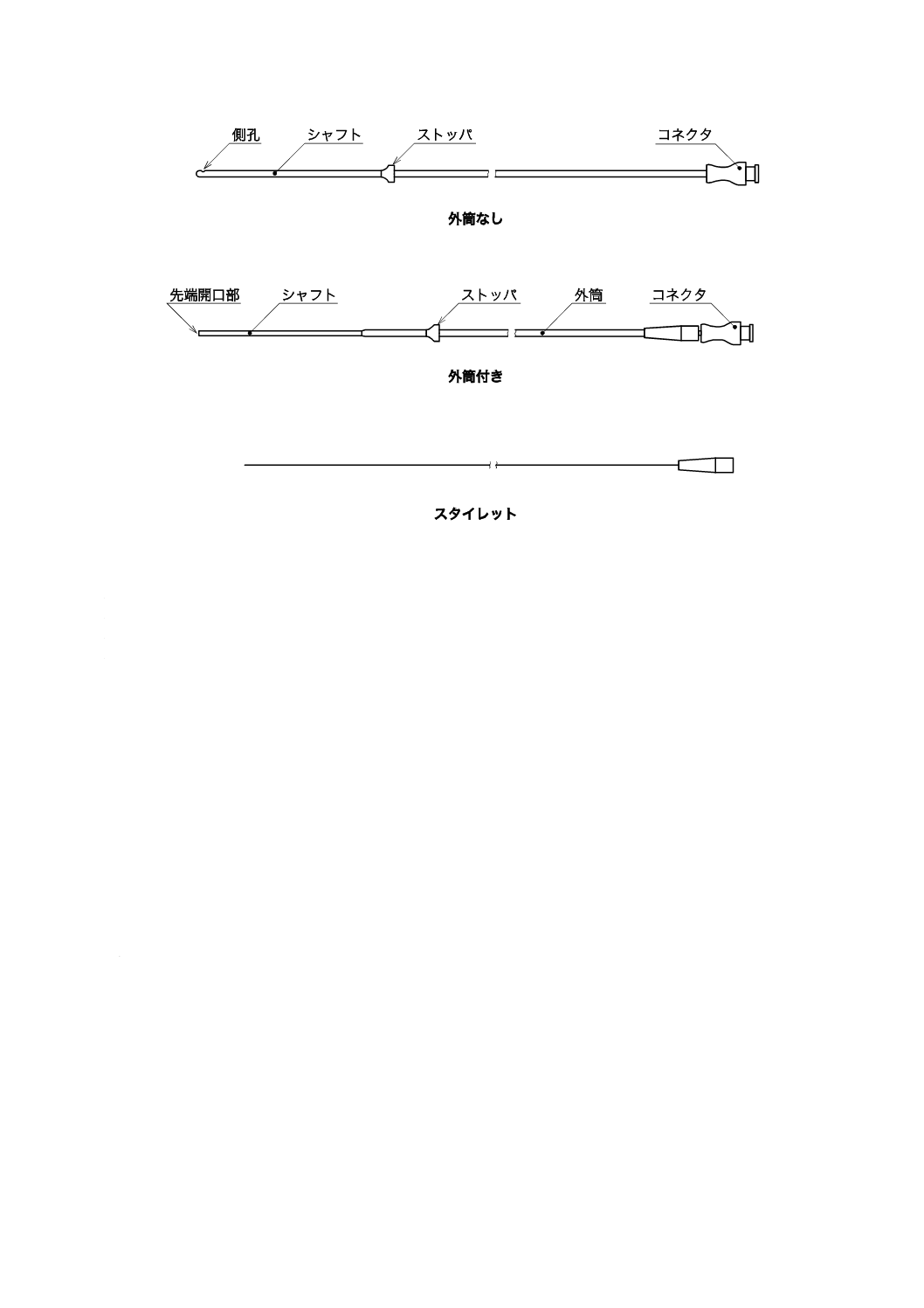
一般的なカテーテルの構成及び各部の名称を,図1に示す。ただし,図1は,カテーテルの構成及び各
部の名称の例である。
3
T 3245:2011
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
注記1 シャフト又は外筒の近位部は,テーパ形状又はバルブチップ状のものもある。
注記2 シャフト又は外筒の近位部分にアングルをもたせたもの,シャフト近位部分の一定長さの外径を細くしたも
のもある。
注記3 シャフト又は外筒の近位部に,溝加工を施したもの,又は金属製のベルト(バンド)を具備したものもある。
注記4 シャフト遠位部に,注射筒を固定したものもある。
注記5 シャフト遠位部側のシャフト外面又は内くう(腔)に,金属又は樹脂製の補強材を具備したものもある。
注記6 ストッパ及び/又はスタイレットを具備しないものもある。
図1−カテーテルの構成及び各部の名称例
5
附属器具類
カテーテルには,試験挿入用のカテーテル(トライアルカテーテルともいう。),トロカール,トロカー
ルスリーブ(トロカール用カニューラともいう。),滅菌済み注射筒,グリップチューブ,プロテクタなど
の附属器具類などを附属してもよい。
6
要求事項
6.1
寸法
シャフトの外径及び長さ(コネクタを除いたシャフト部の長さ)の許容差は,8.1 d)の表示値の±10 %
以内とする。
6.2
外観及び清浄度
シャフトを目視で検査したとき,きず,ばり又は異物の付着があってはならない。
6.3
引張強さ
附属書Aに従ってシャフトを4.9 Nで引っ張ったとき,シャフトは破断及び亀裂を生じてはならない。
6.4
シャフト近位部
シャフト近位部の先端は滑らかに加工されたものであって,先端開口部又は一つ以上の側孔をもってい
なければならない。
4
T 3245:2011
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
6.5
シャフト遠位部
シャフト遠位部は,JIS T 3209に規定する6 %テーパをもつめすコネクタを具備しているか,又は6 %
テーパの筒先をもつ注射筒に接続可能なものでなければならない。
6.6
生物学的安全性
JIS T 0993-1に規定する生物学的安全性の評価を行う。
6.7
無菌性の保証
“滅菌済み”の旨を表示するものは,滅菌バリデーション基準又はこれと同等以上の基準に基づき,無
菌性の担保を行う。
注記 滅菌バリデーション基準には,厚生労働省が定めた滅菌バリデーション基準がある。
7
包装
7.1
一次包装
一次包装は,微生物の侵入を防止することができ,通常の取扱い,輸送及び保管中に,内容製品を適切
に保護できるものでなければならない。一次包装は,一度開封したら,簡単に再シールできず,開封され
たことが明確に分からなければならない。
7.2
二次包装
二次包装は,通常の取扱い,輸送及び保管中に,内容製品を保護できる強度をもつものとする。
8
表示
8.1
一次包装
一次包装には,次の事項を表示する。
a) 製造販売業者の氏名又は名称,及び住所
b) 医療機器の認証番号
c) 販売名
d) シャフトの外径(mm)及び長さ(mm又はcm)。ただし,外径をミリメートル(mm)で示すほか,
フレンチ(シャリエール)又はゲージを参考で併記してもよい。
注記 フレンチ(シャリエール)は,F(Ch)などで表記するのがよい。1 mmが3 F(Ch)に相当
し,1/3 mm刻みで表記する。ゲージは,Gなどで表記するのがよい。
e) 滅菌済みである場合は“滅菌済み”の旨
f)
製造番号又は製造記号
8.2
二次包装
二次包装には,次の事項を表示する。ただし,二次包装を用いず,一次包装を最小販売単位の包装とし
て用いる場合は,次の事項を一次包装に表示する。
なお,製造番号又は製造記号が滅菌年月を表示している場合は,改めて滅菌年月の表示は必要としない。
また,滅菌年月の代わりに使用期限を表示してもよい。
a) 製造販売業者の氏名又は名称,及び住所
b) 医療機器の認証番号
c) 販売名
d) シャフトの外径(mm)及び長さ(mm又はcm)。ただし,外径をミリメートル(mm)で示すほか,
フレンチ(シャリエール)又はゲージを参考で併記してもよい。

5
T 3245:2011
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
注記 フレンチ(シャリエール)は,F(Ch)などで表記するのがよい。1 mmが3 F(Ch)に相当
し,1/3 mm刻みで表記する。ゲージは,Gなどで表記するのがよい。
e) 数量(入り数)
f)
滅菌済みである場合は“滅菌済み”の旨
g) “再使用禁止”の旨(“ディスポーザブル”の表現は使用しない。)
h) “天然ゴム”を使用しているものにあっては,その旨
i)
製造番号又は製造記号
j)
滅菌年月
8.3
記号の使用
8.1及び8.2は,JIS T 0307に規定する適切な記号を使用することによってこれに替えてもよい。
注記 JIS T 0307に規定する主な記号の例を,表1に示す。
表1−JIS T 0307に規定する主な記号の例
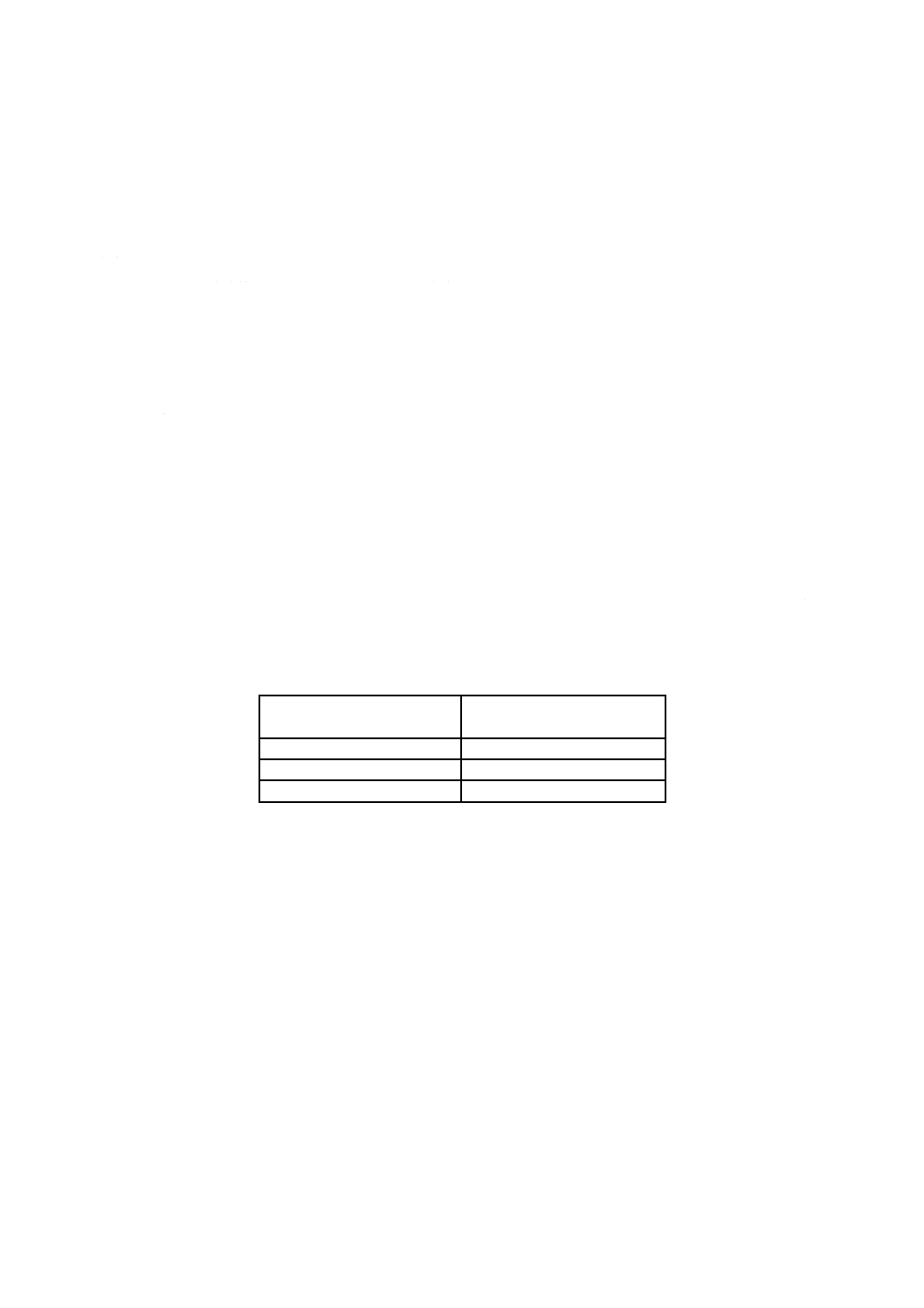
6
T 3245:2011
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書A
(規定)
引張強さに対する試験
A.1 概要
カテーテルの試験箇所を選択し,シャフトの試験を行う。
A.2 試験装置
試験装置は,4.9 N以上の引張力を負荷できる引張試験機とする。
A.3 試験手順
試験手順は,次による。
a) カテーテルを試料とし,室温下で1時間放置する。
b) シャフトから試料を採り,試験を行う。
c) 試料を引張試験機に固定する。
d) 試料のゲージ長を測定する。この場合,引張試験機のつかみ具間の距離と,その逆側の試料先端を把
持しているつかみ具間の距離のいずれかで測定する。
e) 試料が二つ以上に分離するまで,又は製造販売業者の指定した強さになるまで,ゲージ長1 mm当た
り20 mm/minの引張速度で張力を加える(A.1参照)。加えた力をニュートン(N)で記録する。
表A.1−ゲージ1 mm当たり20 mm/minの単位ひずみ速度を生じる引張速度例
ゲージ長
mm
引張速度
mm/min
10
200
20
400
25
500
f)
試験するカテーテルが異なる外径部位をもつ単一材料で構成されるときは,異なる外径の試料それぞ
れについて,b)〜e)まで試験を繰り返さなければならない。
A.4 試験報告書
試験報告書には,次の事項を記載する。
a) カテーテルの種類
b) 破断時の引張力又は印加した指定引張力,及び試料の外径