T 3232:2016
(1)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
目 次
ページ
序文 ··································································································································· 1
1 適用範囲························································································································· 1
2 引用規格························································································································· 1
3 用語及び定義 ··················································································································· 1
3A 構成及び各部の名称 ······································································································· 2
4 要求事項························································································································· 3
4.1 生物学的特性 ················································································································ 3
4.2 物理的特性 ··················································································································· 3
4.3 性能特性 ······················································································································ 3
5 測定及び試験 ··················································································································· 4
5.1 一般事項 ······················································································································ 4
5.2 生物学的特性 ················································································································ 4
5.3 物理的特性 ··················································································································· 4
5.4 性能特性 ······················································································································ 4
6 製造販売業者から提供する情報 ··························································································· 6
6.1 製品 ···························································································································· 6
6.2 包装 ···························································································································· 6
6.3 添付文書 ······················································································································ 6
6.4 添付文書に記載する重要情報 ··························································································· 7
7 包装······························································································································· 7
7.1 一次包装 ······················································································································ 7
7.2 二次包装 ······················································································································ 7
附属書JA(参考)JISと対応国際規格との対比表 ······································································· 8
T 3232:2016
(2)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
まえがき
この規格は,工業標準化法第14条によって準用する第12条第1項の規定に基づき,一般社団法人日本
医療機器テクノロジー協会(MTJAPAN)及び一般財団法人日本規格協会(JSA)から,工業標準原案を具
して日本工業規格を改正すべきとの申出があり,日本工業標準調査会の審議を経て,厚生労働大臣が改正
した日本工業規格である。
これによって,JIS T 3232:2011は改正され,この規格に置き換えられた。
この規格は,著作権法で保護対象となっている著作物である。
この規格の一部が,特許権,出願公開後の特許出願又は実用新案権に抵触する可能性があることに注意
を喚起する。厚生労働大臣及び日本工業標準調査会は,このような特許権,出願公開後の特許出願及び実
用新案権に関わる確認について,責任はもたない。
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
日本工業規格 JIS
T 3232:2016
人工心肺回路用血液フィルタ
Blood filters for cardiopulmonary bypass systems
序文
この規格は,2009年に第2版として発行されたISO 15675を基とし,我が国の実情に合わせるため,技
術的内容を変更して作成した日本工業規格である。
なお,この規格で側線又は点線の下線を施してある箇所は,対応国際規格を変更している事項である。
変更の一覧表にその説明を付けて,附属書JAに示す。
1
適用範囲
この規格は,人工心肺回路に使用し,滅菌済みで単回使用の血液フィルタ及び除泡器について規定する。
注記1 平成31年9月30日までJIS T 3232:2011を適用することができる。
注記2 この規格の対応国際規格及びその対応の程度を表す記号を,次に示す。
ISO 15675:2009,Cardiovascular implants and artificial organs−Cardiopulmonary bypass systems−
Arterial blood line filters(MOD)
なお,対応の程度を表す記号“MOD”は,ISO/IEC Guide 21-1に基づき,“修正している”
ことを示す。
2
引用規格
次に掲げる規格は,この規格に引用されることによって,この規格の規定の一部を構成する。これらの
引用規格は,その最新版(追補を含む。)を適用する。
JIS T 0993-1 医療機器の生物学的評価−第1部:リスクマネジメントプロセスにおける評価及び試験
注記 対応国際規格:ISO 10993-1:2009,Biological evaluation of medical devices−Part 1: Evaluation and
testing within a risk management process(MOD)
ISO 594-2,Conical fittings with 6 % (Luer) taper for syringes, needles and certain other medical equipment−
Part 2: Lock fittings
ISO 10993-11,Biological evaluation of medical devices−Part 11: Tests for systemic toxicity
3
用語及び定義
この規格で用いる主な用語及び定義は,次による。
3.1
血液フィルタ(arterial blood line filter)
凝血塊,血液の組織片,空気そく(塞)栓などの粒子をろ過するフィルタで,動脈血返血ラインで人工
心肺システムの一部として使われる医療機器。
2
T 3232:2016
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
3.1A
除泡器
気泡を取り除くために用いるもので,動脈血返血ラインで人工心肺システムの一部として使われる医療
機器。
3.2
血液経路(blood pathway)
血液フィルタ内又は除泡器内で血液が通過する部分。
3.3
血球損傷(blood cell damage)
血液構成要素である血球が損失又は破壊されること。
3.4
血小板減少(platelet reduction)
血液フィルタ又は除泡器を組み込んでいる回路に含まれている血小板の減少率から,血液フィルタ又は
除泡器を組み込んでいない同様の対照回路での減少率を引いた数値の経時変化。
3.5
血しょう(漿)遊離ヘモグロビン濃度(plasma-free-haemoglobin level)
血液フィルタ又は除泡器を組み込んでいる回路の血しょう(漿)遊離ヘモグロビン濃度と,血液フィル
タ又は除泡器を組み込んでいない同様の対照回路での血しょう(漿)遊離ヘモグロビン濃度との差異の経
時変化。
3.6
白血球減少(white blood cell reduction)
血液フィルタ又は除泡器を組み込んでいる回路の白血球の減少率から,血液フィルタ又は除泡器を組み
込んでいない同様の対照回路での減少率を引いた数値の経時変化。
3.7
ろ過効率(filtration efficiency)
血液模擬液から,粒子を除去する血液フィルタの性能。百分率(%)で示す。
3.7A
試験用血液
ヒト,ウシ又はブタから採取して,抗凝固処理した全血又はこれを生理食塩液で希釈したもの。
3.8
血液模擬液(blood analog)
血液を模擬するために粘度を調整して準備した試験液。
3.9
バブルトラップ(bubble eliminator)
気泡を除去することができる機器。
3A 構成及び各部の名称
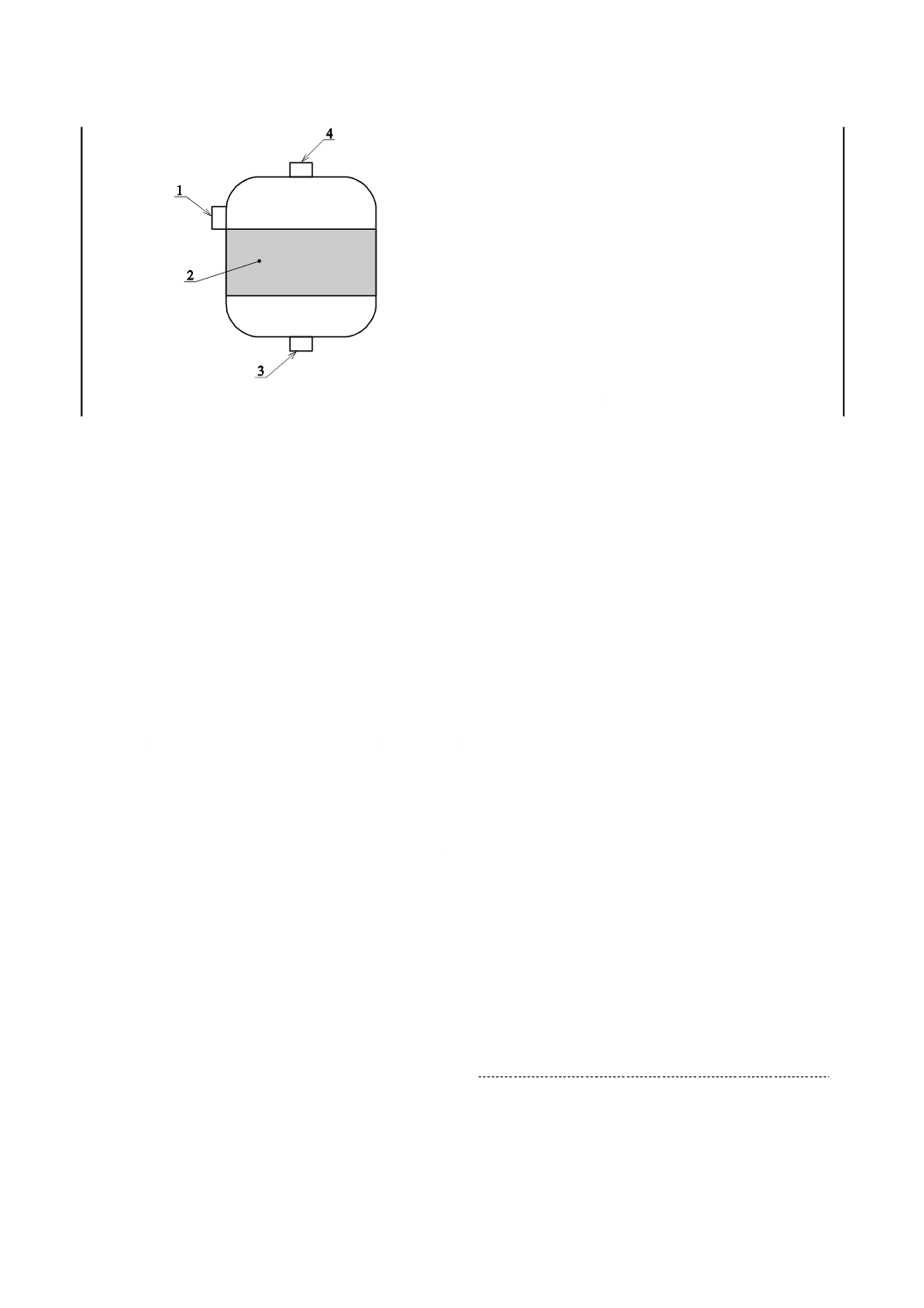
人工心肺回路用血液フィルタは,主として流入口,ろ過部,流出口及び附属ポート(ベントポート)か
らなる。除泡器は,ろ過部を含まず,気液分離部を含む場合がある。図1は,人工心肺回路用血液フィル
タ又は除泡器の構成及び各部の名称の例である。
3
T 3232:2016
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
1 流入口
2 ろ過部(除泡器の場合,気液分離部)
3 流出口
4 附属ポート(ベントポート)
図1−人工心肺回路用血液フィルタ又は除泡器の構成及び各部の名称の例
4
要求事項
4.1
生物学的特性
4.1.1
無菌性及び非発熱性
血液経路は滅菌済みで,かつ,非発熱性とする。この要求事項への適合は,5.2.1によって確認する。
4.1.2
生物学的安全性
血液経路の構成品は,使用目的に対して生物学的安全性がなければならない。この要求事項への適合は,
5.2.2によって確認する。
4.2
物理的特性
4.2.1
血液経路の耐圧性
5.3.1によって試験を行ったとき,血液経路に漏れがあってはならない。
4.2.2
血液容量
血液経路の容量は,血液容量と称し,製造販売業者の指定する許容差範囲内とする[6.3 l) 参照]。
4.2.3
コネクタ
血液経路に接続するコネクタは,5.3.3によって試験を行ったとき,確実に接続されるものとする。附属
ポートへの接続は,ISO 594-2の要求事項に適合するものを使用する。
注記 チューブ内径4.8 mm,6.3 mm,9.5 mm若しくは12.7 mmのチューブに接続が可能なコネクタ,
又はISO 7199に適合するコネクタは,上記要求事項に適合するものを使用する。
4.3
性能特性
4.3.1
血球損傷
5.4.1によって試験を行ったとき,血しょう(漿)遊離ヘモグロビン,血小板及び白血球の変化率(ポジ
ティブ又はネガティブ)は,製造販売業者の指定する範囲内とする。
4.3.2
ろ過効率
5.4.2によって試験を行ったとき,個々の試験フィルタのろ過効率は,フィルタの公称孔寸法よりも20 %
大きな粒子を用いて試験をしたとき,80 %以上とする。ただし,除泡器には,この要求事項は適用しない。
4.3.3
流量
5.4.3によって試験を行ったとき,試験結果は,製造販売業者が定めた安全性及び有効性が確保できるよ
うな流量及び圧力範囲を実証するものとする。
4.3.4
使用期限
4
T 3232:2016
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
5.4.4によって試験を行ったとき,試験結果は,製造販売業者が表示する使用期限を実証するものとする。
4.3.5
気泡除去性能
5.4.5によって試験を行ったとき,試験結果は,製造販売業者が定めた気泡除去性能を実証するものとす
る。
5
測定及び試験
5.1
一般事項
5.1.1
最終滅菌をした完成品で試験を行い,測定する。試験及び測定の準備は,臨床使用を目的として製
造販売業者が作成した添付文書又は取扱説明書による。
5.1.2
特に指示がない場合は,臨床使用を目的として,製造販売業者が指定した使用条件とする。
5.1.3
ほかに指示がない場合は,試験液の温度は37±1 ℃とする。
5.1.4
操作可変範囲が非線形の場合は,十分な測定を行い内挿する。
5.1.5
測定手順及び試験手順は,参照手順とみなす。精度が規定した手順と比較できることが実証されて
いる場合は,ほかの手順を使用してもよい。
5.2
生物学的特性
5.2.1
無菌性及び非発熱性
滅菌バリデーション基準又はこれと同等以上の基準に基づき,無菌性の担保を行う。また,ISO 10993-11
に基づき,非発熱性の評価を行う。
注記 滅菌バリデーション基準には,厚生労働省が定めた滅菌バリデーション基準がある。
5.2.2
生物学的安全性
JIS T 0993-1に規定する生物学的安全性の評価を行う。
5.3
物理的特性
5.3.1
血液経路の耐圧性
機器の血液経路に水を入れ,製造販売業者が指定する最大耐圧の1.5倍の陽圧をかける。製造販売業者
の指示がない場合は,152 kPa {22 psi} ゲージの圧力で6時間,又は製造販売業者が指定する使用時間の間
保持し,目視で検査したとき,水漏れがあってはならない。
5.3.2
血液容量
試験液は,試験用血液又は水とする。製造販売業者が定めたとおりに血液経路の容量を測定する。
5.3.3
コネクタ
製造販売業者の指示に従って,血液経路に接続するコネクタとチューブとの接続を行う。接続部は,15 N
の引張力で15秒間引っ張ったとき,外れてはならない。
5.4
性能特性
5.4.1
血球損傷
5.4.1.1
試験液
血液経路用の試験液は,試験用血液とする。
5.4.1.2
手順
ポンプ,接続配管,リザーバ(製造販売業者が指定する,試験品に適切な寸法のもの),及び熱交換器を
含めた適切で,同一の回路構成品を2セット組み立て,いずれか1セットに試験品を組み込む。2セット
間の血液経路試験液容量の差異は,試験開始時で1 %以下とする。表1の条件で,インビトロ試験を行う。
5
T 3232:2016
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
表1−血球損傷のインビトロ試験条件
項目
基準値
許容誤差
血液流量
意図した臨床使用目的で,製造販売業
者が指示する最大血液流量(6.3参照)
±5 %
血液グルコース
10 mmol/dL
±5 mmol/dL
ヘモグロビン
12 g/dL
±1 g/dL
サンプリングスケジュールは,表2に○印で示す。
表2−サンプリングスケジュール
パラメータ
経過時間(min)
試験前
30
180
360
血しょう(漿)遊離ヘモグロビン
○
○
○
○
白血球
○
○
○
○
血小板
○
○
○
○
ヘモグロビン
○
○
○
○
グルコース
○
活性化凝固時間
○
○
○
○
温度
○
○
○
○
流量
○
○
○
○
注記 測定は,○で示す経過時間で行う。
5.4.2
ろ過効率
5.4.2.1
試験液
試験液は,グリセリン液又は水とする。試験液は,1 mL当たりフィルタの公称孔寸法よりも15〜25 %
大きな範囲の粒子を350〜5 000粒子混ぜたものとする。
5.4.2.2
手順
試験液500 mLを室温(20〜22 ℃)で血液フィルタに100 mL/min以上の流量,及び152 kPa {22 psi} 以
下の圧力で流す。ろ過前及びろ過後の粒子数平均値を測定する。試験は,製造販売業者が推奨する流量で
実施する。各試験サンプルで用いた粒子の範囲を測定し,ろ過前の平均値からろ過後の平均値を引いた値
を,ろ過前の平均値で除し,100を乗じてろ過効率(%)を算出する。
5.4.3
フィルタの流量
5.4.3.1
試験液
試験液は,血液模擬液とする。
5.4.3.2
手順
適切な試験回路に試験品を接続する。流量は最大血液流量に設定し,フィルタの入口圧力及び出口圧力
を6時間モニターする。次に,校正した流量計で流量を測定し,試験時間中の圧力変化を記録する。
注記 この試験は,有形成分及びたんぱく凝集物の影響を考慮に入れていない。
5.4.4
使用期限
文書化された方法を用い,公称使用期限を決めるために,最終包装完成品を用いて加速試験を行う。統
計的に有効な平均使用期限とするために,1試験単位として完成品5本を用いて加速試験を行う。
5.4.5
気泡除去性能
6
T 3232:2016
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
5.4.5.1
試験液
試験液は,ヘモグロビン含有量が12±1 g/dLの抗凝固処理済みの試験用血液とする。
5.4.5.2
手順
1 mのベント配管(内径3.2 mm)をフィルタのベントポートに取り付け,ベント配管のもう一方の端は
周辺環境に開いておく。最大試験流量での背圧は,26.6 kPa {3.9 psi} ±5 %とする。二次側の流出口にバブ
ルトラップを取り付け,5分間累積された空気量を測定する。
最大血液流量の33 %,67 %及び100 %で,部屋の空気30 mL(小児用フィルタの場合は10 mL)を注入
する。
5.4.5.3
結果
結果は,除去された空気総量の効率(%)で表す。
6
製造販売業者から提供する情報
6.1
製品
血液フィルタ又は除泡器には,血液の流れ方向を表示する。
6.2
包装
6.2.1
一次包装
一次包装には,次の事項を表示する。
a) 製造販売業者の氏名又は名称,及び住所
b) 内容物の記載
c) 販売名
d) 滅菌に関する記載(例えば,滅菌方法及び非発熱性)
e) 使用期限
f)
製造番号又は製造記号
g) “使用前に添付文書を読む”旨の記載,又は同等の内容の記載
h) 特別の取扱い方法又は保管条件
i)
再使用禁止の旨(“ディスポーザブル”の表現を除く。)
6.2.2
二次包装
二次包装には,次の事項を表示する。ただし,二次包装を用いず,一次包装を最小販売単位の包装とし
て用いる場合は,次の事項を一次包装に表示する。
a) 製造販売業者の氏名又は名称,及び住所
b) 内容物の記載(入数を含む。)
c) 販売名
d) 使用期限
e) 特別の取扱い方法,保管又は開こん(梱)についての指示
6.3
添付文書
最小販売単位ごとに,次の情報を記載した文書を添付する。
a) 製造販売業者の氏名又は名称,住所及び電話番号又はファックス番号
b) 販売名
c) 必要な附属品
d) 必要な特別又は独特の手順についての指示(該当する場合)
7
T 3232:2016
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
e) フィルタのサポート又は取付けについての記載
f)
チューブ接続の設置,種類及び確保
g) 充塡操作
h) 血液の流れ方向
i)
通常使用時の一般的な操作手順
j)
気泡除去性能
k) 最大推奨血液流量及び最小推奨血液流量
l)
充塡量(血液容量)及びその許容差
m) 使用者の要望によって,次を提供できる旨の記載
1) 血液経路の材料リスト
2) 製造販売業者が指定する意図した臨床用途の最大血液流量での血液経路圧力損失
3) 血球損傷に関するデータ
4) 提示したデータの許容差
n) 滅菌に関する記載,滅菌方法及び非発熱性
6.4
添付文書に記載する重要情報
次の情報は,添付文書で,目立つように記載する。
a) 流量範囲
b) 他の用具との使用制限(例えば,既知の揮発性麻酔剤,溶剤,消毒剤などと構成材質との非適合性)
7
包装
7.1
一次包装
一次包装は,微生物の侵入を防止することができ,通常の取扱い,輸送及び保管中に,内容製品を適切
に保護できるものでなければならない。一次包装は,一度開封したら簡単に再シールできず,開封された
ことが明確に分からなければならない。
7.2
二次包装
二次包装は,通常の取扱い,輸送及び保管中に,内容製品を保護できる強度をもつものとする。
参考文献
[1] ISO 7199,Cardiovascular implants and artificial organs−Blood-gas exchangers (oxygenators)
[2] ISO 10993-10,Biological evaluation of medical devices−Part 10: Tests for irritation and skin sensitization
[3] ISO 13485,Medical devices−Quality management systems−Requirements for regulatory purposes
[4] ISO 14971,Medical devices−Application of risk management to medical devices
[5] ISO 15223 (all parts),Medical devices−Symbols to be used with medical device labels, labelling and
information to be supplied
[6] ISO/TS 23810,Cardiovascular implants and artificial organs−Checklist for preoperative extracorporeal
circulation equipment setup
8
T 3232:2016
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書JA
(参考)
JISと対応国際規格との対比表
JIS T 3232:2016 人工心肺回路用血液フィルタ
ISO 15675:2009,Cardiovascular implants and artificial organs−Cardiopulmonary bypass
systems−Arterial blood line filters
(I)JISの規定
(II)国際
規格番号
(III)国際規格の規定
(IV)JISと国際規格との技術的差異の箇条ごと
の評価及びその内容
(V)JISと国際規格との技術的差
異の理由及び今後の対策
箇条番号
及び題名
内容
箇条
番号
内容
箇条ごと
の評価
技術的差異の内容
1 適用範囲 人工心肺回路用血
液フィルタ及び除
泡器について規定
1
人工心肺回路用血液フ
ィルタについて規定
追加
除泡器を追加
フィルタと同様に用いるので除泡
器も適用する。
ISO規格の見直し時に提案を検討
2 引用規格
3 用語及び
定義
11項目の用語の定
義を規定
3
JISとほぼ同じ
追加
除泡器及び試験用血液を追加
“除泡器”は,この規格の適用範
囲に従い明確に定義
“試験用血液”は,理解を容易に
したものであり実質的差異はな
い。
3A 構成及
び各部の名
称
人工心肺回路用血
液フィルタ又は除
泡器の構成及び各
部の名称を概略図
で記載
−
−
追加
構成及び各部の名称例の図を追加
理解を容易にしたものであり,実
質的差異はない。
4 要求事項 4.3.2 ろ過効率
4.3.2
JISとほぼ同じ
追加
除泡器は適用外とする旨の記載を
追加
除泡器は気泡の除去だけで,粒子
の除去機能はもっていないため。
実質的差異はない。
5 測定及び
試験
5.2.1 無菌性及び非
発熱性
5.2.1
JISとほぼ同じ
変更
国内基準を優先し,同等のISO規
格を削除
内容的には同等で,記載表現を変
更した。
実質的差異はない。
5.2.2 生物学的安全
性
5.2.2
JISとほぼ同じ
変更
ISO 10993-7の削除
内容的には同等で,記載表現を変
更した。
実質的差異はない。
2
T
3
2
3
2
:
2
0
1
6
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
9
T 3232:2016
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
(I)JISの規定
(II)国際
規格番号
(III)国際規格の規定
(IV)JISと国際規格との技術的差異の箇条ごと
の評価及びその内容
(V)JISと国際規格との技術的差
異の理由及び今後の対策
箇条番号
及び題名
内容
箇条
番号
内容
箇条ごと
の評価
技術的差異の内容
5 測定及び
試験
(続き)
5.3.2 血液容量
5.3.2
試験液
変更
細分箇条名を“試験液”から要求事
項項目である“血液容量”へ変更
ISO規格の見直し時に提案を検討
変更
“血液”を“試験用血液”に変更
理解を容易にしたものであり,実
質的差異はない。
5.4.1.1 試験液
5.4.1.1 JISとほぼ同じ
変更
“血液”を“試験用血液”に変更
理解を容易にしたものであり,実
質的差異はない。
5.4.5.1 試験液
5.4.5.1 JISとほぼ同じ
変更
“血液”を“試験用血液”に変更
理解を容易にしたものであり,実
質的差異はない。
6 製造販売
業者から提
供する情報
6.1 製品
6.1
JISとほぼ同じ
追加
除泡器を追加
この規格の適用範囲に従い明確に
記載
実質的差異はない。
削除
製造販売元及び販売名を削除
製品本体への表示が必須である項
目だけ当該欄に記載
実質的差異はない。
6.3 添付文書
6.3
JISとほぼ同じ
削除
“追加の流入口及び流出口の位置
及び目的”を削除
フィルタ及び除泡器とも該当する
ものはないため。
ISO規格の見直し時に提案を検討
7 包装
7.1 一次包装
7.2 二次包装
7
ISO 11607-1及びISO
11607-2の該当する要
求事項
変更
一次包装と二次包装とを区別し,明
確に規定
理解を容易にしたものであり,実
質的差異はない。
JISと国際規格との対応の程度の全体評価:ISO 15675:2009,MOD
注記1 箇条ごとの評価欄の用語の意味は,次による。
− 削除 ················ 国際規格の規定項目又は規定内容を削除している。
− 追加 ················ 国際規格にない規定項目又は規定内容を追加している。
− 変更 ················ 国際規格の規定内容を変更している。
注記2 JISと国際規格との対応の程度の全体評価欄の記号の意味は,次による。
− MOD ··············· 国際規格を修正している。
2
T
3
2
3
2
:
2
0
1
6
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。