T 3228:2018
(1)
目 次
ページ
序文 ··································································································································· 1
1 適用範囲························································································································· 1
2 引用規格························································································································· 1
3 用語及び定義 ··················································································································· 2
4 構成及び各部の名称 ·········································································································· 2
5 要求事項························································································································· 4
5.1 針管の組合せ ················································································································ 4
5.2 針管の材料 ··················································································································· 4
5.3 寸法の許容差 ················································································································ 4
5.4 外観及び清浄度 ············································································································· 4
5.5 針先 ···························································································································· 4
5.6 性能 ···························································································································· 4
5.7 引張強さ ······················································································································ 5
5.8 弾性 ···························································································································· 5
5.9 曲げ強さ ······················································································································ 6
5.10 針基のテーパの合致 ······································································································ 6
5.11 無菌性の保証 ··············································································································· 6
5.12 生物学的安全性 ············································································································ 6
6 包装······························································································································· 6
6.1 一次包装 ······················································································································ 6
6.2 二次包装 ······················································································································ 7
7 表示······························································································································· 7
7.1 一次包装 ······················································································································ 7
7.2 二次包装 ······················································································································ 7
7.3 図記号の使用 ················································································································ 7
附属書A(参考)針の剛性の考え方の指針 ················································································ 8
T 3228:2018
(2)
まえがき
この規格は,工業標準化法第14条によって準用する第12条第1項の規定に基づき,一般社団法人日本
医療機器テクノロジー協会(MTJAPAN)及び一般財団法人日本規格協会(JSA)から,工業標準原案を具
して日本工業規格を改正すべきとの申出があり,日本工業標準調査会の審議を経て,厚生労働大臣が改正
した日本工業規格である。
これによって,JIS T 3228:2011は改正され,この規格に置き換えられた。
この規格は,著作権法で保護対象となっている著作物である。
この規格の一部が,特許権,出願公開後の特許出願又は実用新案権に抵触する可能性があることに注意
を喚起する。厚生労働大臣及び日本工業標準調査会は,このような特許権,出願公開後の特許出願及び実
用新案権に関わる確認について,責任はもたない。
日本工業規格 JIS
T 3228:2018
生体組織採取用生検針
Biopsy needles for single use
序文
この規格は,2005年に制定され,2011年の改正を経て,今日に至っている。その後,この規格で引用し
ているコネクタ規格(ISO 594-1:1986及びISO 594-2:1998)に関して,新たにISO 80369-6及びISO 80369-7
が制定されたため,この規格においても引用規格として追加するよう改正をした。
1
適用範囲
この規格は,組織診用の検体を採取する単回使用の生体組織採取用生検針(以下,生検針という。)につ
いて規定する。また,医薬品を投与するように意図した場合は,使用法によっては危険性がある場合を除
き,薬液などを注入できるものにも適用できる。
注記 2021年1月31日までJIS T 3228:2011を適用することができる。
2
引用規格
次に掲げる規格は,この規格に引用されることによって,この規格の規定の一部を構成する。これらの
引用規格のうちで,西暦年を付記してあるものは,記載の年の版を適用し,その後の改正版(追補を含む。)
は適用しない。西暦年の付記がない引用規格は,その最新版(追補を含む。)を適用する。
JIS G 4305 冷間圧延ステンレス鋼板及び鋼帯
JIS H 4650 チタン及びチタン合金−棒
JIS T 0307 医療機器−医療機器のラベル,ラベリング及び供給される情報に用いる図記号
JIS T 0993-1 医療機器の生物学的評価−第1部:リスクマネジメントプロセスにおける評価及び試験
ISO 594-1:1986,Conical fittings with a 6 % (Luer) taper for syringes, needles and certain other medical
equipment−Part 1: General requirements
ISO 594-2:1998,Conical fittings with 6 % (Luer) taper for syringes, needles and certain other medical
equipment−Part 2: Lock fittings
ISO 9626:2016,Stainless steel needle tubing for the manufacture of medical devices−Requirements and test
methods
ISO 80369-6:2016,Small bore connectors for liquids and gases in healthcare applications−Part 6: Connectors
for neuraxial applications
ISO 80369-7:2016,Small-bore connectors for liquids and gases in healthcare applications−Part 7: Connectors
for intravascular or hypodermic applications
2
T 3228:2018
3
用語及び定義
この規格で用いる主な用語及び定義は,次による。
3.1
生検針
針管及び針基(以下,針という。)並びに生検用器具又は吸引用器具からなるもの。針管には,筒だけの
もの,外筒及び内筒からなるもの,又は外筒及び内針からなるものがあり,先端が鋭利で組織採取機能を
もつ部位がある。筒だけのものは,せん(穿)刺用に内針を使用したり,薬液処置用などの筒を組み合わ
せるものもある。
3.2
吸引形
吸引用器具を使用又は併用して,組織診用の検体を採取できるよう設計した医療機器。また,吸引用器
具は,吸引装置又は吸引用装着器具,延長チューブなどで構成される。針にはカット形仕様のものもあり,
骨用生検又は内視鏡用として,内視鏡を通して又は内視鏡と一緒に体内に挿入するものもある。
3.3
カット形
針を目的部位にせん(穿)刺後,組織診用の検体を採取できるよう設計した医療機器。種類は針だけで
使用できるもの,針と生検用器具とを装着できるもの,あらかじめ針と生検用器具とが一体形のものなど
がある。骨用生検など,吸引用器具と併用して使用するものもあり,内視鏡用は,内視鏡を通して又は内
視鏡と一緒に体内に挿入するよう設計されている。
3.4
公称外径
生検針の包装又は容器に表示した針管の外径。
3.5
公称長さ
生検針の包装又は容器に表示した針管の長さ。
3.6
一次包装
生検針を直接に覆う包装で,生検針の無菌性を保持するためのもの。さらに,これを二次包装する場合
には,“内袋”に該当する。
3.7
二次包装
一次包装を直接に覆う包装。通常,複数の一次包装された生検針を入れた包装。
4
構成及び各部の名称
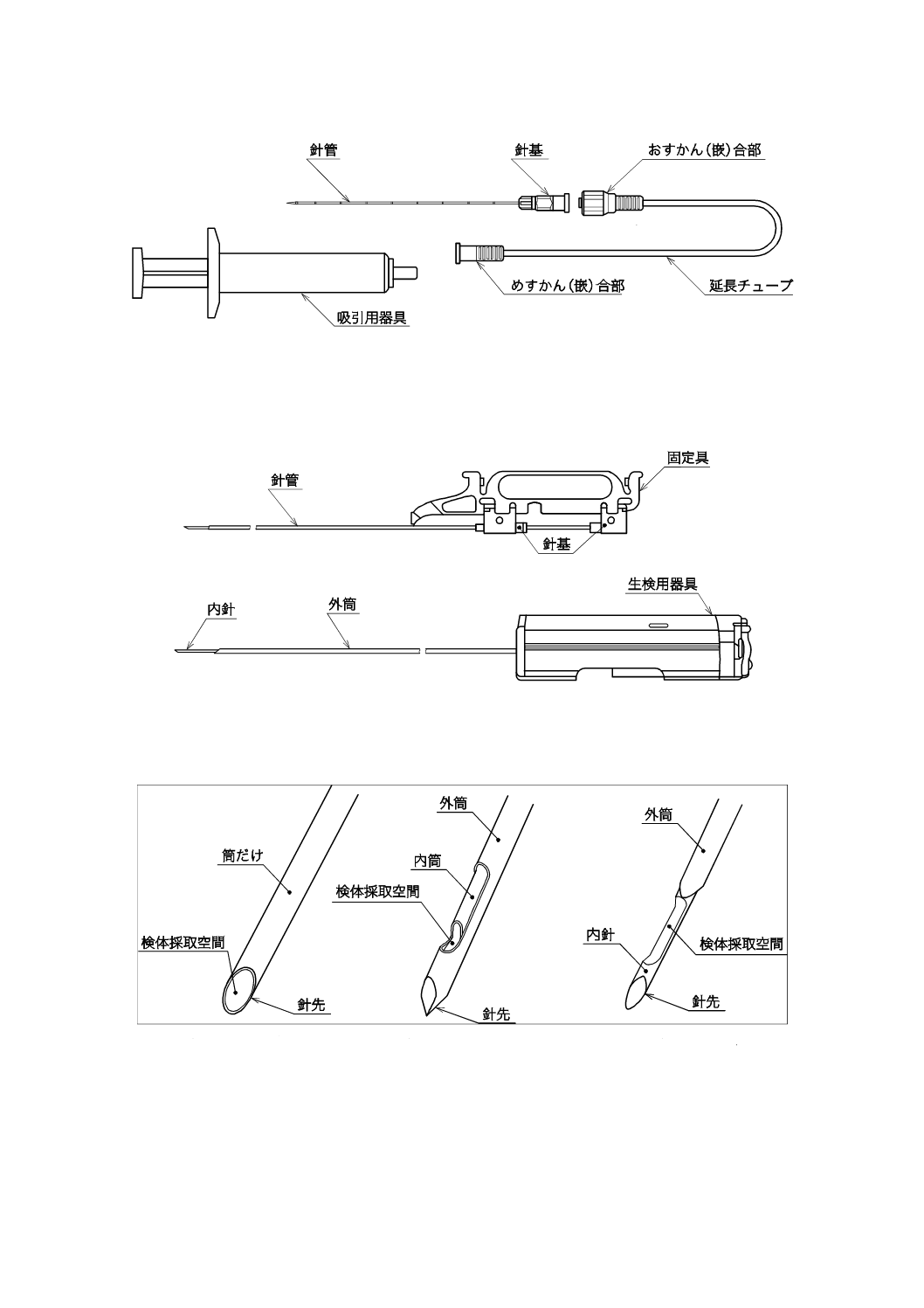
生検針は,吸引形とカット形とに区分する(図1及び図2参照)。生検針には,これらに生検用器具,吸
引用器具,採取組織固定用具,針の目的部位へのせん(穿)刺用具,薬液注入用具(麻酔薬は除く。),止
血用具などを構成品又は附属品として含む場合がある。また,針には,使用前後に術者が針管の針先を身
体に誤刺しないように保護する針さや(鞘)が付いているものもある。
なお,図1及び図2は,一般的な構造及び各部の名称を示した例である。また,図3は,針先の組織診
用検体採取空間を示した例である。
3
T 3228:2018
注記1 延長チューブは,使用するものと使用しないものとがある。
注記2 吸引用器具には,吸引装置又は吸引用装着器具がある。
図1−吸引形の構造及び各部の名称例
注記 針には,固定具を装着し供する。
図2−カット形の構造及び各部の名称例
a) 吸引形及び骨用形
b) 吸引形(カット形仕様)
c) カット形
注記1 筒だけのものには,先端部を組織採取用に加工しているもの,せん(穿)刺用に加工しているものがある。
また,組織を採取する根詰りストッパをもつものがある。
注記2 外筒及び内筒からなるものは,スライド方式によって,内筒の検体採取空間が外筒に収納できる。
注記3 外筒及び内針からなるものの検体採取空間は,外筒によって調整できる。
図3−針先の組織診用検体採取空間の例

4
T 3228:2018
5
要求事項
5.1
針管の組合せ
針管の組合せは,次のいずれかに適合しなければならない。
a) 筒だけからなる。せん(穿)刺用などに内針及び/又は薬液処置用などの筒を組み合わせる場合があ
る。
b) 外筒及び内筒からなる。
c) 外筒及び検体採取空間部をもつ内針からなる。
5.2
針管の材料
針管は,次のいずれかの材質でなければならない。
a) JIS G 4305に規定するSUS304,SUS304L,SUS321若しくは同等のステンレス鋼,又はISO 9626の
材料の項に適合するステンレス鋼。
5.1 b) 及び5.1 c) 並びに内視鏡用及び骨用の針の剛性は,附属書Aによるとよい。
b) JIS H 4650に規定するチタン。
c) ニッケルクロム合金,ニッケルチタン合金,チタン合金などの合金。
a)〜c) の材質に適合する針管の潤滑剤としてシリコーン油を用いる場合,シリコーン油は,シリコーン
油基準又はこれと同等以上の基準に適合しなければならない。
注記 シリコーン油基準には,厚生労働省が定めたシリコーン油基準がある。
5.3
寸法の許容差
寸法の許容差は,次による。
a) 公称外径を表示し供給するものについて,針管の外径の許容差は,公称外径の−3 %〜+8 %でなけれ
ばならない。
なお,筒,外筒及び内針の外径は,附属書Aによるとよい。
b) 公称長さを表示し供給するものについて,針管の長さの許容差は,公称長さに対して,表1による。
表1−寸法の許容差
針管公称長さ
mm
許容差
%
20以上40未満
±7
40以上60未満
±5
60以上
±3
5.4
外観及び清浄度
目視で検査したとき,きず,ばり又は異物の付着があってはならない。また,潤滑剤を使用しているも
のは,潤滑剤の量が,針管の表面に液滴を認めたり,内面にたまりを認める量であってはならない。
5.5
針先
針先は,鋭利に研磨し,目視検査で分かるようなばりなどの欠点があってはならない。
5.6
性能
次のいずれかの性能がなければならない。
a) 5.1 a) に適合する場合は,組織診用の検体を採取できる空間を保持しなければならない。また,せん
(穿)刺用などに内針及び/又は薬液処置用などの筒を組み合わせる場合は,筒に適切に挿入及び抜
5
T 3228:2018
去できなければならない。
b) 5.1 b) に適合する場合は,組織診用の検体を採取できる空間があり,添付文書の操作方法を行ったと
き,正常に機能しなければならない。
c) 5.1 c) に適合する場合は,組織診用の検体を採取できる空間があり,添付文書の操作方法を行ったと
き,外筒及び内針が正常に機能しなければならない。また,組織診用の検体採取空間部をもつ内針の
厚さ(肉厚)の最小値は,附属書Aによるとよい。
5.7
引張強さ
引張強さは,用途によって,次のいずれかに適合しなければならない。
a) 一般用(内視鏡用又は骨用以外に使用するもの)の針管の公称外径又は断面図の最小寸法に応じて,
針管の中心軸方向に表2の力を加えたとき,針基から引き抜けてはならない。
表2−引張強さ
針管の公称外径
又は断面図の最小寸法
mm
力
N
0.55未満
0.55以上 〜 0.7未満
0.7以上 〜 0.8未満
0.8以上 〜 0.9未満
0.9以上 〜 1.1未満
1.1以上
22
34
40
44
54
69
b) 内視鏡用の針管の公称外径又は断面図の最小寸法に応じて,針管の中心軸方向に7.84 Nの力を加えた
とき,針基から引き抜けてはならない。
c) 骨用の針管の公称外径又は断面図の最小寸法に応じて,針管の中心軸方向に69 Nの力を加えたとき,
針基から引き抜けてはならない。
5.8
弾性
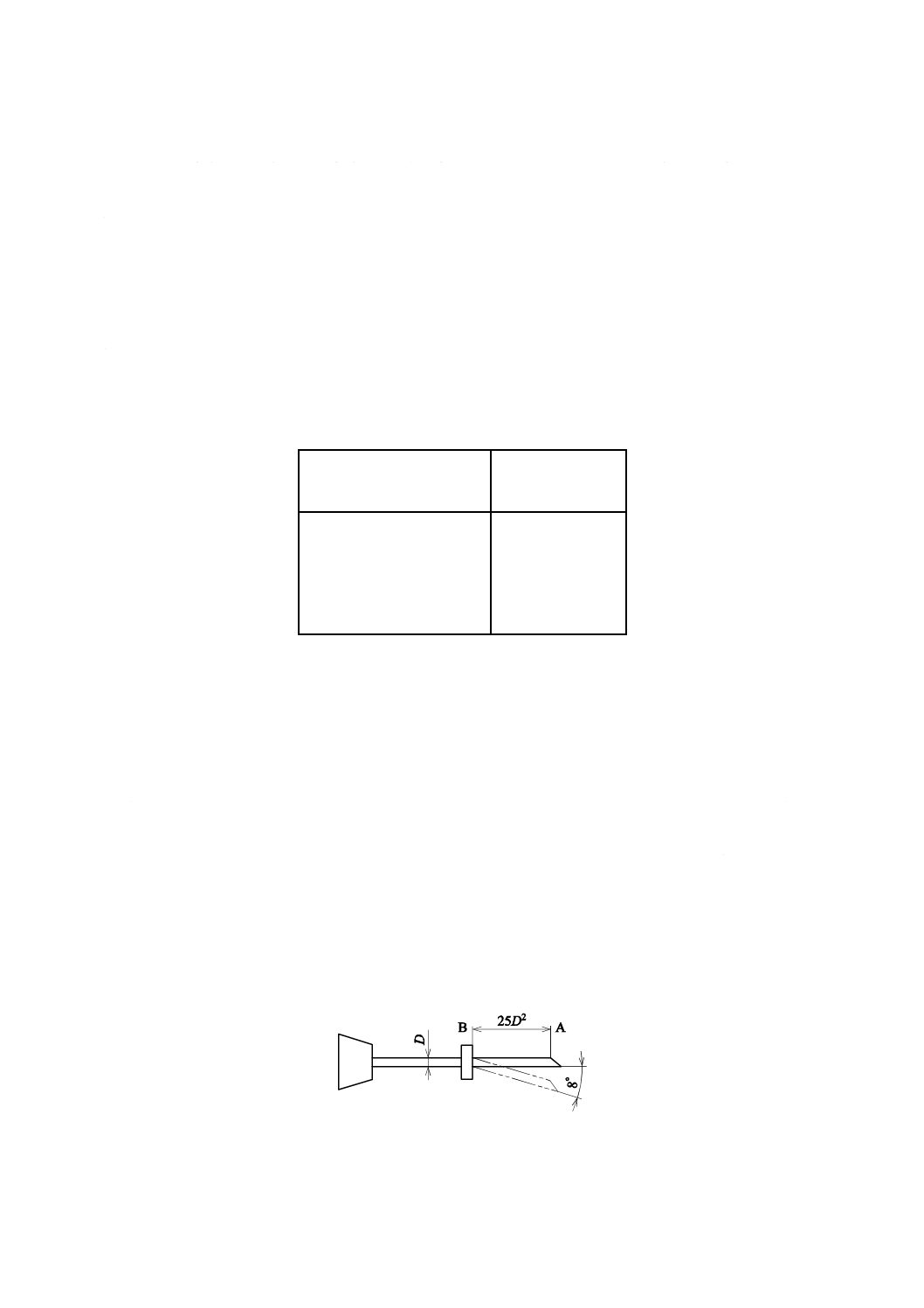
針管の公称外径又は断面図の最小外径(図4のD)が1.0 mm以下のものは,図4のように,針管の先
端の一点Aから25D2離れた針管上の点Bを固定し,Aに力を加え,8度曲げて1分間保った後,放して
目視したとき,針管は,元の位置に復するものでなければならない。5.1 a) 及び5.2 a) に相当するもので
ある場合は,この規定に適合しなければならない。ただし,ISO 9626の硬さの要求事項に適合するステン
レス鋼は,この規定を要求しない。
なお,5.2 c) に適合する場合は,公称外径及び公称長さによらず,5.1 b) の内筒を含む外筒又は5.1 c) の
内針は,この細分箇条の規定にも適合しなければならない。
図4−弾性
6
T 3228:2018
5.9
曲げ強さ
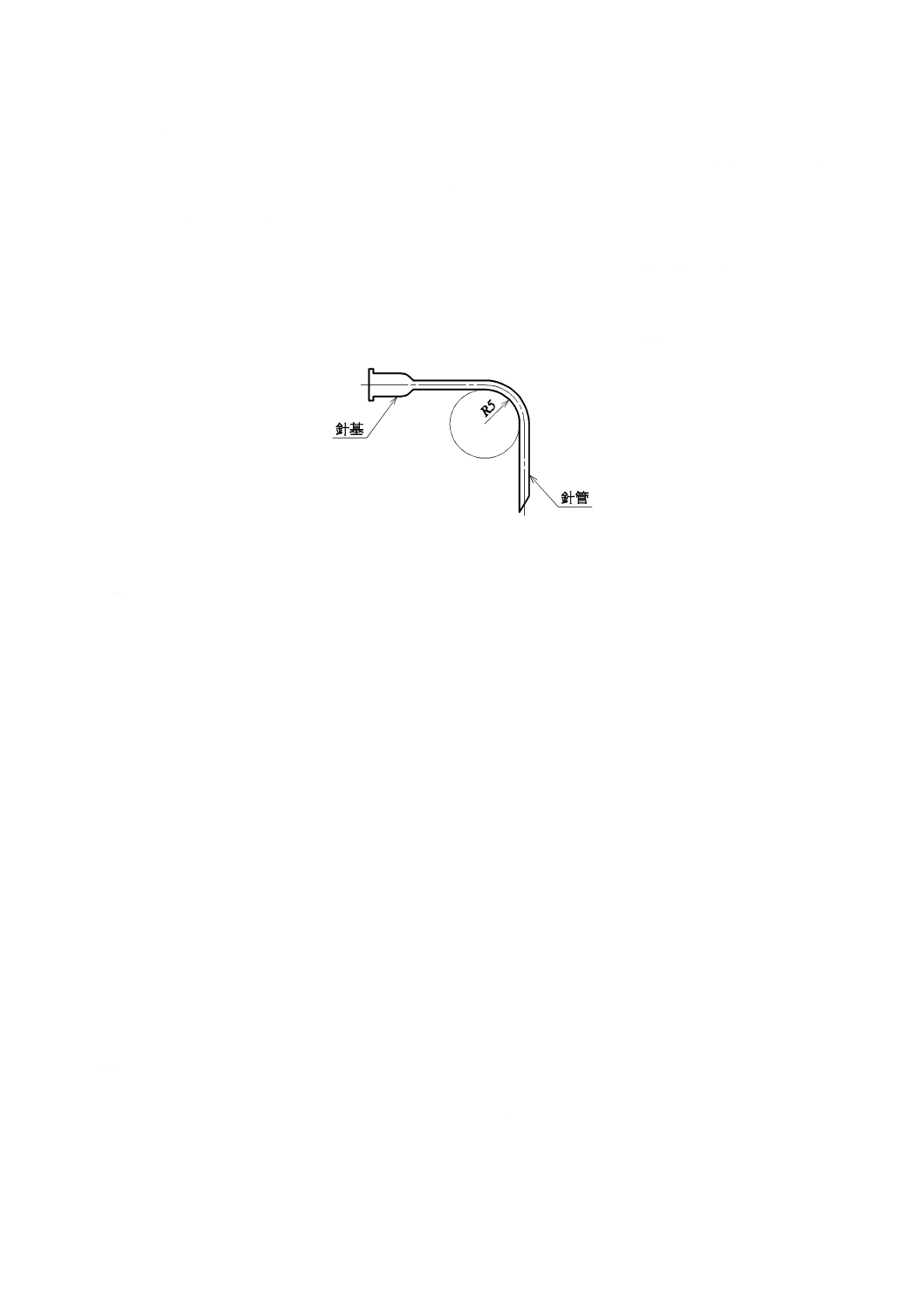
組合せを指定しているそれぞれの針管は,公称外径又は断面図の最小外径が1.0 mm以下で,かつ,公
称長さが12 mm以上のものは,図5のように,針管を5 mmの曲率半径で90度曲げたとき,折れてはな
らない。5.1 a) 及び5.2 a) に適合する場合は,この規定にも適合しなければならない。ただし,ISO 9626
の硬さの要求事項に適合するステンレス鋼は,この規定を要求しない。
なお,5.2 c) に適合する場合は,公称外径及び公称長さによらず,5.1 b) の内筒を含む外筒又は5.1 c) の
内針は,この細分箇条の規定にも適合しなければならない。
単位 mm
図5−曲げ強さ
5.10
針基のテーパの合致
注射筒を接続して組織を採取する生検針で,おすめす(雄雌)かん(嵌)合部は,ISO 594-1:1986及び
ISO 594-2:1998,又はISO 80369-6若しくはISO 80369-7に適合したものでなければならない。ただし,ISO
80369-6又はISO 80369-7を適用する場合には,それぞれの規格の適用範囲に該当する製品でなければなら
ない。
注記 ISO 80369-6の適用範囲に該当する製品がISO 594-1:1986及びISO 594-2:1998を適用できる期
間については,“神経麻酔分野の小口径コネクタ製品の切替えについて”(平成29年12月27
日付け医政総発1227第1号,薬生薬審発1227第1号,薬生機審発1227第1号,薬生安発1227
第1号厚生労働省医政局総務課長,医薬・生活衛生局医薬品審査管理課長,同医療機器審査管
理課長,同医薬安全対策課長連名通知)に示されている。
5.11
無菌性の保証
“滅菌済み”の旨を表示し供給する生検針の無菌性の保証は,滅菌バリデーション基準又はこれと同等
以上の基準に基づき,無菌性の担保を行う。
注記 滅菌バリデーション基準には,厚生労働省が定めた滅菌バリデーション基準がある。
5.12
生物学的安全性
JIS T 0993-1に規定する生物学的安全性の評価を行う。
6
包装
6.1
一次包装
一次包装は,微生物の侵入を防止することができ,かつ,通常の取扱い,輸送及び保管中に,内容製品
を適切に保護できるものでなければならない。また,一次包装は,一度開封したならば,簡単に再シール
できず,開封したことが明確に分からなければならない。

7
T 3228:2018
6.2
二次包装
二次包装は,通常の取扱い,輸送及び保管中に,内容製品を保護できる強度をもたなければならない。
7
表示
7.1
一次包装
一次包装には,次の事項を表示する。
a) 公称外径及び公称長さを表示し供給するものは,針管の外径(mm又はゲージ)及び長さ(mm)
b) “滅菌済み”又は“未滅菌”の旨
c) 製造番号又は製造記号
7.2
二次包装
二次包装には,次の事項を表示する。ただし,二次包装を用いないで,一次包装を最小販売単位の包装
として用いる場合には,次の事項を一次包装に表示する。
なお,製造番号又は製造記号が滅菌年月を表している場合は,改めて滅菌年月の表示をする必要はない。
また,滅菌年月の代わりに使用期限を表示してもよい。
a) 製造販売業者の氏名又は名称,及び住所
b) 医療機器の認証番号
c) 販売名
d) 公称外径及び公称長さを表示し供給するものは,針管の外径(mm又はゲージ)及び長さ(mm)
e) 数量(入り数)
f)
“滅菌済み”又は“未滅菌”の旨
g) “再使用禁止”の旨(“ディスポーザブル”の表現は使用しない。)
h) 製造番号又は製造記号
i)
滅菌年月(滅菌製品の場合だけ)
j)
ISO 80369-6をかん(嵌)合部に用いた場合には,識別表示を行う。識別は“ISO 80369-6”の文字又
はISO 80369-6に適合した製品であること等を表示する。
7.3
図記号の使用
7.1及び7.2は,JIS T 0307に規定する適切な図記号を使用することによって,これに替えてもよい。
注記 JIS T 0307に規定する主な図記号の例を,表3に示す。
表3−JIS T 0307に規定する主な図記号の例
8
T 3228:2018
附属書A
(参考)
針の剛性の考え方の指針
A.1 針の剛性の考え方の指針
A.1.1 外径
生検針の剛性は,針管の組合せ,材料,用途及び組織採取空間の形状によって異なってくる。しかし,
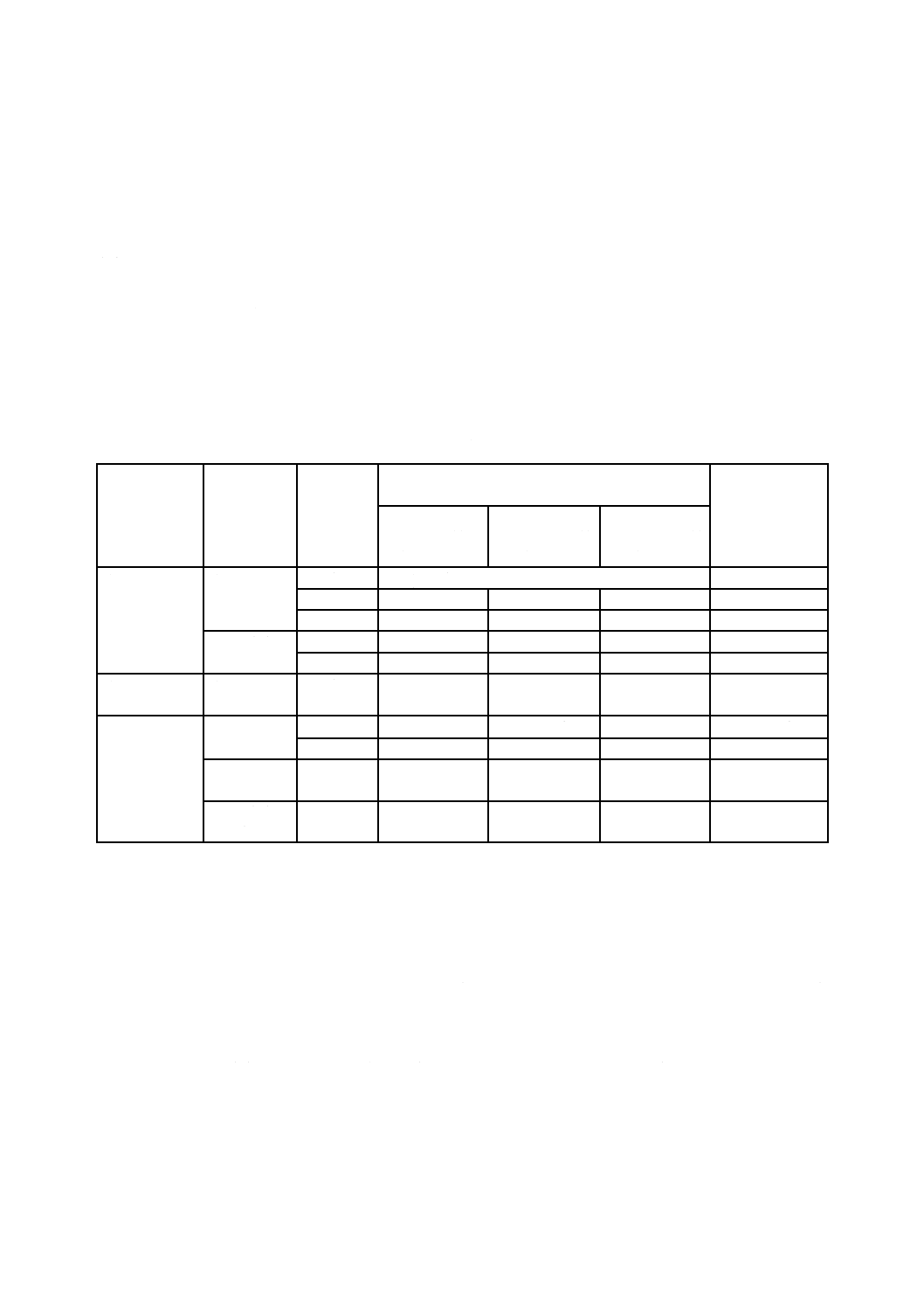
2004年8月現在,既承認品に対するこの要求事項は統一されていない。そのため,表A.1のとおり,剛性
を担保する情報として,針管の組合せ,針管の材料及び用途によって,既承認品の外径の規格値を示した
(2004年8月23日現在)。針の外径については,この既承認品と同等以上であることが望ましい。
表A.1−外径評価表
5.1
(針管の組合せ)
5.2
(針管の材料)
用途
参考値
mm
組織診用の検体
採取空間部をも
つ内針の厚さ
(肉厚)の参考値
mm
筒の外径又は
断面図の最小
外径
外筒の外径又
は断面図の最
小外径
内針の外径又
は断面図の最
小外径
a) に適合する
場合
a) に適合す
る場合
一般用
5.2 a) を確認する。
−
骨用
1.25以上
−
−
−
内視鏡用
0.70以上
−
−
−
b) に適合す
る場合
一般用
0.51以上
−
−
−
骨用
2.31以上
−
−
−
b) に適合する
場合
a) に適合す
る場合
一般用
−
1.49以上
−
−
c) に適合する
場合
a) に適合す
る場合
一般用
−
0.78以上
0.53以上
0.24以上
内視鏡用
−
1.00以上
0.8以上
0.55以上
b) に適合す
る場合
一般用
−
1.21以上
0.97以上
0.49以上
c) に適合す
る場合
一般用
−
1.20以上
0.89以上
0.35以上
A.1.2 組織診用の検体採取空間部をもつ内針の厚さ(肉厚)
組織診用の検体採取空間をもつ内針に対しても,その材料及び厚さが剛性に関係してくる。しかし,2004
年8月現在のところ,既承認品に対するこの要求事項は統一されていない。そのため,表A.1のとおり,
剛性を担保する情報として,針管の材料及び組織診用の検体採取空間部をもつ内針の厚さ(肉厚)につい
て,既承認品の規格値を示した(2004年8月23日現在)。組織診用の検体採取空間部をもつ内針の厚さ(肉
厚)について,この既承認品と同等以上の厚さ(肉厚)又は強度をもつことが望ましい。
A.1.3 A.1.1と同等でないステンレス製の剛性についての試験
材料が5.2 a) に適合するステンレス鋼の場合,A.1.1と同等でないステンレス製の剛性に関わる試験規
格として,公称外径及び公称長さによらず,5.8,5.9又はISO 9626の硬さの項に適合することが望ましい。





