R 1752:2020
(1)
目 次
ページ
序文 ··································································································································· 1
1 適用範囲························································································································· 1
2 引用規格························································································································· 1
3 用語及び定義 ··················································································································· 2
4 記号及び単位 ··················································································································· 4
5 測定原理························································································································· 4
6 材料······························································································································· 5
6.1 試験に用いる細菌株及び試験の準備··················································································· 5
6.2 試薬及び材料 ················································································································ 5
6.3 殺菌方法 ······················································································································ 5
7 装置及び機器 ··················································································································· 6
8 試験片···························································································································· 7
8.1 フィルム密着法 ············································································································· 7
8.2 ガラス密着法 ················································································································ 7
9 試験方法························································································································· 8
9.1 一般事項 ······················································································································ 8
9.2 フィルム密着法 ············································································································· 9
9.3 ガラス密着法 ··············································································································· 11
9.4 可視光照射条件 ············································································································ 13
9.5 生菌数の測定 ··············································································································· 13
10 試験結果の計算 ············································································································· 14
10.1 一般事項 ···················································································································· 14
10.2 フィルム密着法 ··········································································································· 14
10.3 ガラス密着法 ·············································································································· 15
11 抗菌効果の判定 ············································································································· 16
12 試験結果の報告 ············································································································· 16
附属書JA(規定)平板状の可視光応答形ハイブリッド光触媒抗菌加工材料の
光が当たらない環境での抗菌性試験方法及び抗菌効果 ·························································· 18
附属書JB(参考)JISと対応国際規格との対比表 ······································································ 22
R 1752:2020
(2)
まえがき
この規格は,産業標準化法第16条において準用する同法第12条第1項の規定に基づき,一般社団法人
日本ファインセラミックス協会(JFCA)及び一般財団法人日本規格協会(JSA)から,産業標準原案を添
えて日本産業規格を改正すべきとの申出があり,日本産業標準調査会の審議を経て,経済産業大臣が改正
した日本産業規格である。これによって,JIS R 1752:2013は改正され,この規格に置き換えられた。
この規格は,著作権法で保護対象となっている著作物である。
この規格の一部が,特許権,出願公開後の特許出願又は実用新案権に抵触する可能性があることに注意
を喚起する。経済産業大臣及び日本産業標準調査会は,このような特許権,出願公開後の特許出願及び実
用新案権に関わる確認について,責任はもたない。
日本産業規格 JIS
R 1752:2020
ファインセラミックス−可視光応答形光触媒
抗菌加工材料の抗菌性試験方法及び抗菌効果
Fine ceramics (advanced ceramics, advanced technical ceramics)-
Test method for antibacterial activity of photocatalytic materials and
efficacy under indoor lighting environment
序文
この規格は,2014年に第1版として発行されたISO 17094を基とし,技術的内容を変更して作成した日
本産業規格である。
なお,この規格で側線又は点線の下線を施してある箇所は,対応国際規格を変更している事項である。
変更の一覧表にその説明を付けて,附属書JBに示す。
1
適用範囲
この規格は,可視光照射後の細菌の生存数を計測することによる,可視光応答形光触媒を含有する加工
材料及び表面に可視光応答形光触媒加工フィルムを含む材料(以下,光触媒抗菌加工材料という。)の抗菌
性試験方法及びその結果による抗菌効果の判定について規定する。
この規格は,抗菌用途をもつ可視光応答形光触媒材料に適用する。可視光応答形光触媒材料の他の種類
の機能,例えば,抗かび性,抗ウイルス性,水浄化,セルフクリーニング,防曇及び空気浄化には適用で
きない。
この規格は,粉体,粒状及び多孔質な可視光応答形光触媒材料は含まないが,主に塗布するなどの作業
によって,平板状及び繊維状に加工した可視光応答形光触媒材料に対しては適用できる。
紫外光領域での抗菌性を試験する場合は,この規格ではなく,JIS R 1702を適用する。
警告 この規格に基づいて試験を行う者は,微生物学技術を習得していることを前提とする。
注記 この規格の対応国際規格及びその対応の程度を表す記号を,次に示す。
ISO 17094:2014,Fine ceramics (advanced ceramics, advanced technical ceramics)−Test method for
antibacterial activity of semiconducting photocatalytic materials under indoor lighting environment
(MOD)
なお,対応の程度を表す記号“MOD”は,ISO/IEC Guide 21-1に基づき,“修正している”
ことを示す。
2
引用規格
次に掲げる規格は,この規格に引用されることによって,この規格の規定の一部を構成する。これらの
引用規格は,その最新版(追補を含む。)を適用する。

2
R 1752:2020
JIS C 1609-1 照度計 第1部:一般計量器
JIS K 0950 プラスチック製滅菌シャーレ
JIS K 0970 ピストン式ピペット
JIS K 3800 バイオハザード対策用クラスIIキャビネット
JIS K 8101 エタノール(99.5)(試薬)
JIS L 0803 染色堅ろう度試験用添付白布
JIS L 1902 繊維製品の抗菌性試験方法及び抗菌効果
JIS P 3801 ろ紙(化学分析用)
JIS R 1600 ファインセラミックス関連用語
JIS R 1702 ファインセラミックス−光触媒抗菌加工材料の抗菌性試験方法及び抗菌効果
注記 対応国際規格 ISO 27447,Fine ceramics (advanced ceramics, advanced technical ceramics)−Test
method for antibacterial activity of semiconducting photocatalytic materials
JIS R 1709 ファインセラミックス−紫外線励起形光触媒試験用光源
JIS R 1750 ファインセラミックス−屋内照明環境で用いる光触媒試験用光源
JIS R 3505 ガラス製体積計
JIS R 3644 ガラス管類
JIS R 3645 ガラス棒
JIS Z 2801 抗菌加工製品−抗菌性試験方法・抗菌効果
3
用語及び定義
この規格で用いる主な用語及び定義は,次によるほか,JIS R 1600,JIS R 1702,JIS Z 2801及びJIS L 1902
による。
3.1
可視光応答形光触媒(indoor-light-active photocatalyst)
一般的な照明器具(室内照明環境など)の人工的な光源(可視光)の照射下において光触媒の諸機能を
発現する物質。
3.2
室内照明環境(可視光)(indoor light environment)
一般的な照明器具による人工的な光源(可視光)による照明環境。太陽光を含まず,波長が380 nm以
上780 nm未満の範囲の光である。
3.3
可視光応答形光触媒材料(indoor-light-active photocatalytic material)
コーティング,含侵,練り込みなどによって,可視光応答形光触媒物質を加えた材料。
3.4
可視光応答形光触媒抗菌加工(indoor-light-active photocatalytic antibacterial treatment)
可視光応答形光触媒の抗菌機能を利用するために,可視光応答形光触媒で抗菌加工すること。可視光応
答形単味光触媒抗菌加工及び可視光応答形ハイブリッド光触媒抗菌加工に分類される。
3.5
可視光応答形単味光触媒抗菌加工(indoor-light-active simplex photocatalytic antibacterial treatment)
可視光応答形光触媒抗菌加工のうち,塗布,含浸,練り込みなど種々の方法によって可視光応答形光触
3
R 1752:2020
媒を担持すること。また,可視光照射下での可視光応答形光触媒の抗菌性を増強するために,可視光応答
形光触媒と抗菌性のない他の機能性物質とを組み合わせた材料を担持することも含む。
3.6
可視光応答形ハイブリッド光触媒抗菌加工(indoor-light-active hybrid photocatalytic antibacterial treatment)
可視光応答形光触媒抗菌加工のうち,可視光が当たらない環境においても抗菌機能を発現させるために,
可視光応答形光触媒と抗菌性のある他の機能性物質とを組み合わせた材料を塗布,含浸,練り込みなど種々
の方法によって担持すること。
3.7
可視光応答形光触媒抗菌加工材料(indoor-light-active photocatalytic antibacterial treated material)
可視光応答形光触媒抗菌加工した膜状,平板状,繊維状などの材料。可視光応答形単味光触媒抗菌加工,
可視光応答形ハイブリッド光触媒抗菌加工及び可視光応答形光触媒抗菌加工した製品を含む。
3.8
フィルム密着法(film cover method)
可視光応答形光触媒抗菌加工した平板状材料の光照射条件下での抗菌性を評価する試験方法。
注記 平板状の可視光応答形ハイブリッド光触媒抗菌加工材料の光が当たらない環境での抗菌性を評
価する試験方法を,附属書JAに示す。
3.9
ガラス密着法(glass cover method)
可視光応答形光触媒抗菌加工した繊維状材料の光照射条件下での抗菌性を評価する試験方法。
注記 繊維状の可視光応答形ハイブリッド光触媒抗菌加工材料の光が当たらない環境での抗菌性を評
価する試験方法は,JIS L 1902の8.1(菌液吸収法)参照。
3.10
平板状の可視光応答形光触媒抗菌加工材料の抗菌活性値(antibacterial activity value of indoor-light-active
photocatalytic treated flat surface material)
可視光照射後の可視光応答形光触媒抗菌加工した平板状材料と無加工材料との生菌数の対数値の差。こ
の値には,可視光照射しない条件で得られる生菌数の減少分も含む。
3.11
繊維状の可視光応答形光触媒抗菌加工材料の抗菌活性値(antibacterial activity value of indoor-light-active
photocatalytic treated cloth)
可視光照射後の可視光応答形光触媒抗菌加工した繊維状材料と未加工布との生菌数の対数値の差。この
値には,可視光照射しない条件で得られる生菌数の減少分も含む。
3.12
平板状の可視光応答形光触媒抗菌加工材料の光照射による抗菌活性値(antibacterial activity value with
indoor light illumination of indoor-light-active photocatalytic treated flat surface material)
可視光照射後と暗所に保存した後との可視光応答形光触媒抗菌加工した平板状材料の生菌数の対数値の
差。
3.13
繊維状の可視光応答形光触媒抗菌加工材料の光照射による抗菌活性値(antibacterial activity value with
indoor light illumination of indoor-light-active photocatalytic treated cloth)
可視光照射後と暗所に保存した後との可視光応答形光触媒抗菌加工した繊維状材料の生菌数の対数値の
4
R 1752:2020
差。
3.14
抗菌効果(antibacterial efficacy)
抗菌活性値によって判定される可視光応答形光触媒抗菌加工による効果。
4
記号及び単位
この規格で用いる主な記号及び単位は,次による。
A:
無加工試験片の接種直後の3個の試験片の生菌数の平均値(個)
BD:
無加工試験片を暗所に保存した後の3個の試験片の生菌数の平均値(個)
BF-L:
無加工試験片を可視光照射条件F-Lで光照射した後の3個の試験片の生菌数の平均値(個)
CD:
可視光応答形光触媒抗菌加工した試験片を暗所に保存した後の3個の試験片の生菌数の平均値
(個)
CF-L:
可視光応答形光触媒抗菌加工した試験片を可視光照射条件F-Lで光照射した後の3個の試験片
の生菌数の平均値(個)
F:
試験で用いたシャープカットフィルタの種類(A又はB)
HD:
暗所で試験した増殖値
HF-L:
可視光照射条件F-Lで試験した増殖値
L:
試験で用いた照度(lx)
Logmax: 3個の試験片の生菌数の常用対数値の最大値
Logmean :3個の試験片の生菌数の常用対数値の平均値
Logmin: 3個の試験片の生菌数の常用対数値の最小値
M:
ガラス密着法による生菌数(個)
MB A: 無加工試験片の接種直後の3個の試験片の生菌数の算術平均値の常用対数値
MB D: 無加工試験片を暗所で保存した後の3個の試験片の生菌数の算術平均値の常用対数値
MB F-L: 無加工試験片を可視光照射条件F-Lで光照射した後の3個の試験片の生菌数の算術平均値の常
用対数値
MD:
可視光応答形光触媒抗菌加工した試験片を暗所に保存した後の3個の試験片の生菌数の算術平
均値の常用対数値
MF-L: 可視光応答形光触媒抗菌加工した試験片を可視光照射条件F-Lで光照射した後の3個の試験片
の生菌数の算術平均値の常用対数値
N:
フィルム密着法による生菌数(個)
P:
菌濃度(個/ml)
RF-L:
可視光照射条件F-Lで光照射した平板状の可視光応答形光触媒抗菌加工材料による抗菌活性値
ΔR:
平板状の可視光応答形光触媒抗菌加工材料の光照射による抗菌活性値
SF-L:
可視光照射条件F-Lで光照射した繊維状の可視光応答形光触媒抗菌加工材料による抗菌活性値
ΔS:
繊維状の可視光応答形光触媒抗菌加工材料の光照射による抗菌活性値
V:
洗い出しに用いたSCDLP培地の液量(ml)
5
測定原理
この試験方法は,光触媒材料の開発,性能比較,品質管理,特徴付け,信頼性及び設計データの取得に
5
R 1752:2020
適している。この試験方法は,可視光照射下において,細菌と試験片とが接触することによる可視光応答
形光触媒材料の抗菌性を得るために適用する。フィルム密着法は,平板状の材料に適用できる。ガラス密
着法は,繊維状の材料に適用できる。
試験片をシャーレに置き,試験菌液を試験片に滴下する。次に,密着フィルム又は密着ガラスによって
試験菌液を覆い,保湿ガラスをシャーレの上にかぶせる。試験片を入れたシャーレに可視光を照射する。
照射後,試験片,及び密着フィルム又は密着ガラスから試験菌を洗い出す。この洗い出された試験菌液の
生菌数を生菌数測定法によって測定する。得られた結果は,光触媒抗菌加工した試験片と同様の条件で紫
外光照射をした無加工試験片,暗所に置いた光触媒抗菌加工した試験片及び無加工試験片の測定結果と比
較する。
6
材料
6.1
試験に用いる細菌株及び試験の準備
6.1.1
フィルム密着法に用いる細菌の種類
JIS R 1702の6.1.1(フィルム密着法に用いる細菌の種類)に規定するものとする。
6.1.2
ガラス密着法に用いる細菌の種類
JIS R 1702の6.1.2(ガラス密着法に用いる細菌の種類)に規定するものとする。
6.1.3
細菌株の準備
JIS R 1702の6.1.3(細菌株の準備)に規定する方法による。
6.1.4
細菌株の保存
JIS R 1702の6.1.4(細菌株の保存)に規定する方法による。
6.2
試薬及び材料
試験に用いる試薬及び材料は,6.2.1〜6.2.6による。
なお,培地は,同一成分の場合は,市販のものを用いることができ,また,作成する培地量は,試験片
の数に合わせて変更することが望ましい。
6.2.1
SCDLP培地 JIS Z 2801の5.4 e)(SCDLP培地)に規定する方法による。
6.2.2
生理食塩水 生理食塩水の調製は,JIS L 1902の6.7(生理食塩水)に規定する方法による。調製
後,直ちに使用しないものは,5 ℃〜10 ℃の温度で保存する。調製後,1か月以上過ぎた生理食塩水は,
用いてはならない。
6.2.3
洗い出し用生理食塩水 洗い出し用生理食塩水の調製は,JIS L 1902の6.20(洗い出し用生理食塩
水)に規定する方法による。調製後,直ちに使用しないものは5 ℃〜10 ℃の温度で保存する。調製後,1
か月以上過ぎた洗い出し用生理食塩水は用いてはならない。
6.2.4
エタノール(C2H5OH) JIS K 8101に規定する特級を用いる。
6.2.5
非イオン界面活性剤 JIS R 1702の6.2.16(非イオン界面活性剤)に規定するものを用いる。
6.2.6
綿標準布 JIS L 0803に規定する染色堅ろう度試験用添付白布を,洗剤及び漂白剤を使用せず,
60 ℃の水温で10分間水洗い後,すすぎ5分を2回繰り返し,この一連の処理を10回繰り返し,風乾した
ものを用いる。
6.3
殺菌方法
殺菌方法は,高圧蒸気殺菌とし,JIS Z 2801の5.3 b)(高圧蒸気殺菌)による。
6
R 1752:2020
7
装置及び機器
装置及び機器は,次による。
7.1
試験装置 試験装置は,7.8に規定する光源,7.9に規定する光照射装置,7.10に規定するシャープ
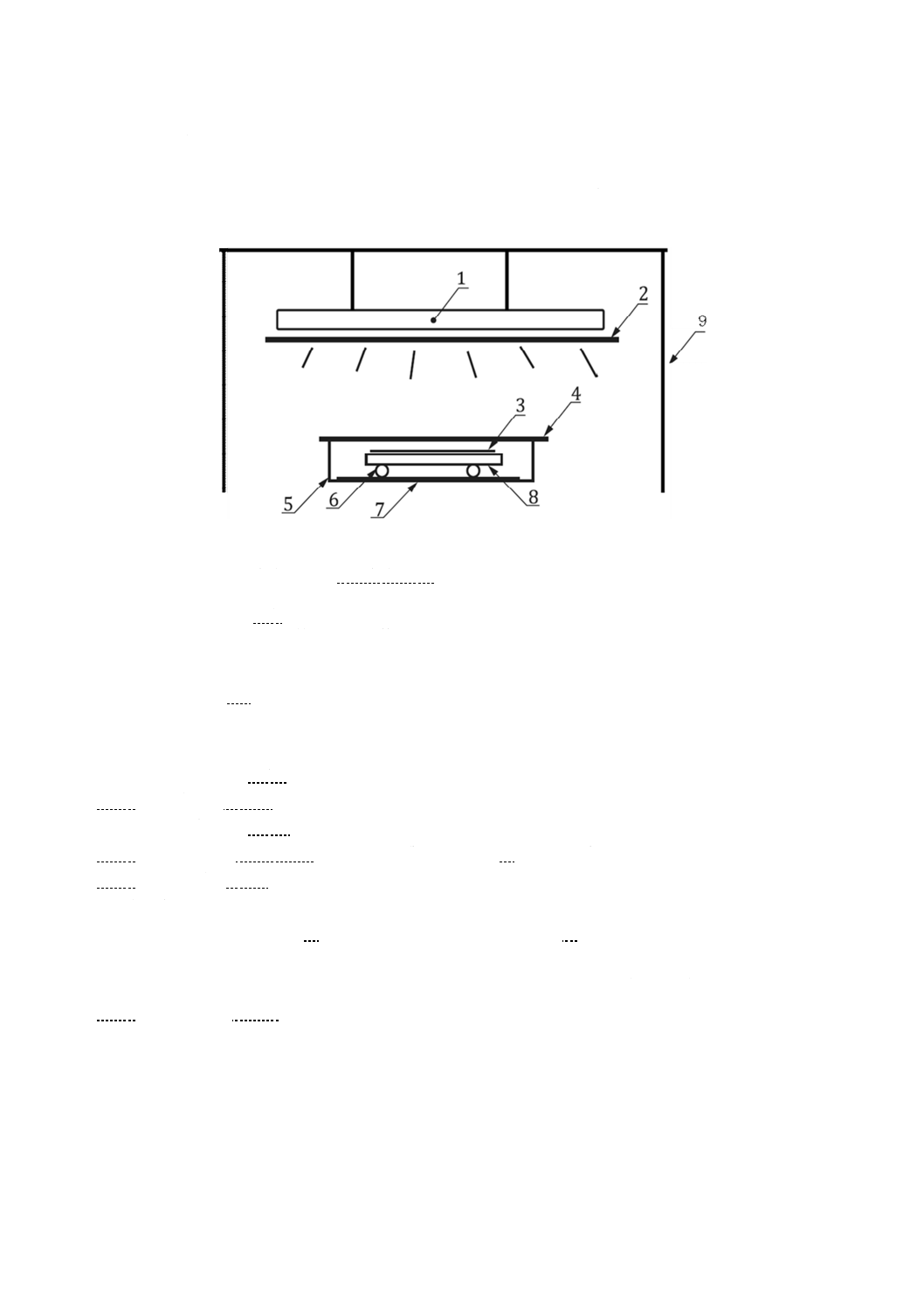
カットフィルタ及び箇条8に規定する試験片を備えたチャンバから成る。試験装置の概略を,図1に示す。
1
光源
2
シャープカットフィルタ
3
密着フィルム又は密着ガラス
4
保湿用ガラス
5
保存シャーレ
6
ガラス管又はガラス棒
7
調湿用ろ紙
8
試験片
9
光照射装置
図1−試験装置の概略
7.2
密着フィルム JIS R 1702の7.2(密着フィルム)に規定するもの。
7.3
密着ガラス JIS R 1702の7.3(密着ガラス)に規定するもの。
7.4
保湿用ガラス JIS R 1702の7.4(保湿用ガラス)に規定するもの。
7.5
保存シャーレ 内径約90 mmのガラス製,又はJIS K 0950に規定する90A号若しくは90B号。
7.6
調湿用ろ紙 JIS P 3801に規定する微生物の発育に影響を及ぼさないろ紙で,試験片を置く容器に入
るよう切断したもの。
7.7
ガラス管・ガラス棒 JIS R 3644に規定するガラス管又はJIS R 3645に規定するガラス棒を試験片
を置く容器に入るように切断したもの。
7.8
光源 JIS R 1750に規定する光源のうち,広帯域発光形蛍光ランプの普通形白色(W形)のもの。
7.9
光照射装置 JIS R 1702の7.9(光照射装置)による。
7.10 シャープカットフィルタ JIS R 1750の4.4(シャープカットフィルタ)に規定するType A又はType
Bのシャープカットフィルタ。製品が使用される状況によって,使用するフィルタ(試験条件)を選択す
る。シャープカットフィルタは,光源の直下に取り付ける。
なお,シャープカットフィルタを用いずに試験する場合は,次のa)又はb)に規定する条件と組み合わせ
て試験しなければならない。
a) 条件A(400 nm以下をカットする条件) JIS R 1750の4.4に規定するType Aのシャープカットフィ

7
R 1752:2020
ルタを用いた条件
b) 条件B(380 nm以下をカットする条件) JIS R 1750の4.4に規定するType Bのシャープカットフィ
ルタを用いた条件
7.11 照度計 JIS C 1609-1に規定するもののうち,一般形A級以上のもの。
7.12 紫外放射照度計 JIS R 1709に規定するもので,0.001 mW/cm2まで計測できるもの。
7.13 暗箱 容器内の照度が10 lx未満の蓋の付いたもの。
7.14 シャーレ 内径約90 mmのガラス製,又はJIS K 0950に規定する90A号若しくは90B号に適合す
るもの。
7.15 安全キャビネット JIS K 3800に適合するもの又は同等の性能をもつもの。
7.16 ピペット JIS K 0970若しくはJIS R 3505のクラスAに適合するもの又は同等の精度をもつもの。
8
試験片
8.1
フィルム密着法
フィルム密着法で用いる試験片は,次による。
a) 平板状の材料の平らな部分を50 mm±2 mm角(厚さ10 mm以内)の正方形に切り取り,これを標準
の大きさの試験片とする。
平板状の材料を50 mm±2 mm角(厚さ10 mm以内)にカットすることが難しい,又は不可能な場
合には,1/2のサイズ(厚さ10 mm以内)にした試験片を使用してもよい。試験片の大きさを小さく
した場合,密着フィルムの大きさも小さくする。表面積800 mm2〜1 600 mm2の密着フィルムをかぶせ
ることが可能な試験片の大きさの場合は,ここに規定する形状及び大きさ以外の試験片を使用しても
よい。
b) これらの試験片を,無加工試験片は9個,可視光応答形光触媒抗菌加工した試験片は6個準備する。
無加工試験片が準備できない場合は,ガラス板を使用する。微生物汚染,試験片間の相互汚染及び汚
れに十分注意する。
試験片表面が有機物で汚染されている場合は,JIS R 1702の8.1(フィルム密着法)に従い,有機物
を除去する予備作業をしてもよい。必要に応じて,試験片は試験前に無菌化処理を行うことができる
(例参照)。
例 エタノール,又は水で70 %に調整したエタノールを用いて拭き取る。
8.2
ガラス密着法
ガラス密着法で用いる試験片は,次による。
a) 繊維状の材料を50 mm±2 mm角の正方形に切り取り,これを標準の大きさの試験片とする。
b) これらの試験片を,無加工試験片は9個,可視光応答形光触媒抗菌加工した試験片は6個準備する。
微生物汚染,試験片間の相互汚染及び汚れに十分注意する。
c) 無加工試験片が準備できない場合は,6.2.6に規定の綿標準布を使用してもよい。
綿標準布を無加工試験片として使用する場合,照度条件によっては,試験成立条件を満足しない場
合があるので注意する。
d) 試験片ごとにガラス製シャーレに入れる。これらを金網かごに入れ,金網かごの上部全体をアルミニ
ウムはくで覆い,オートクレーブに入れ高圧蒸気殺菌する。オートクレーブから取り出した後,安全
キャビネット内でアルミニウムはくを外し,試験片を乾燥させるためにガラス製シャーレの蓋をずら
して60分程度乾燥後,ガラス製シャーレの蓋をする。
8
R 1752:2020
試験片表面が有機物で汚染されている場合は,1.0 mW/cm2程度の光源を24時間を上限として照射
し,有機物を除去する予備作業をしてもよい。必要に応じて,試験片は試験前に高圧蒸気殺菌などの
無菌化処理を行うことができる。
9
試験方法
9.1
一般事項
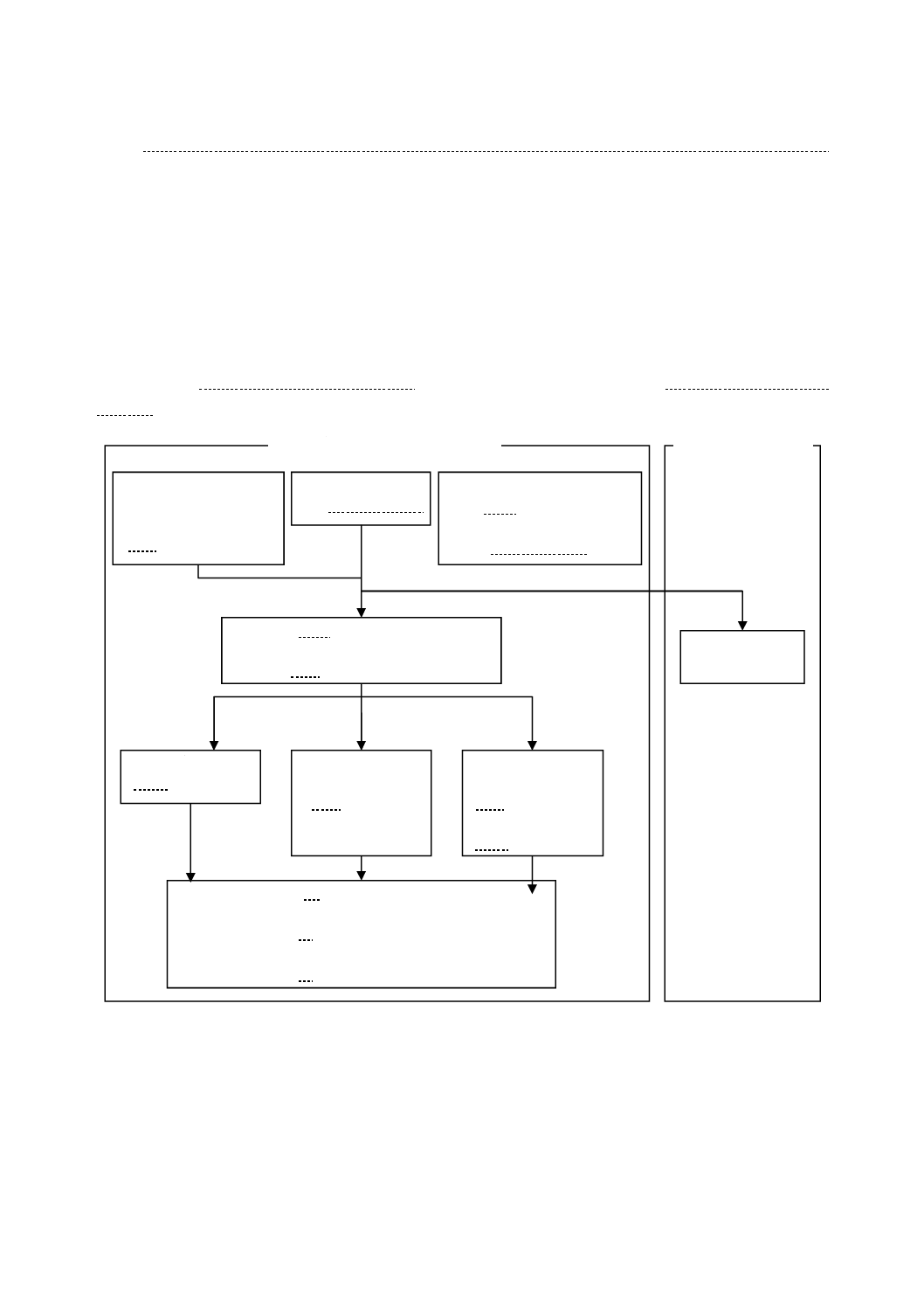
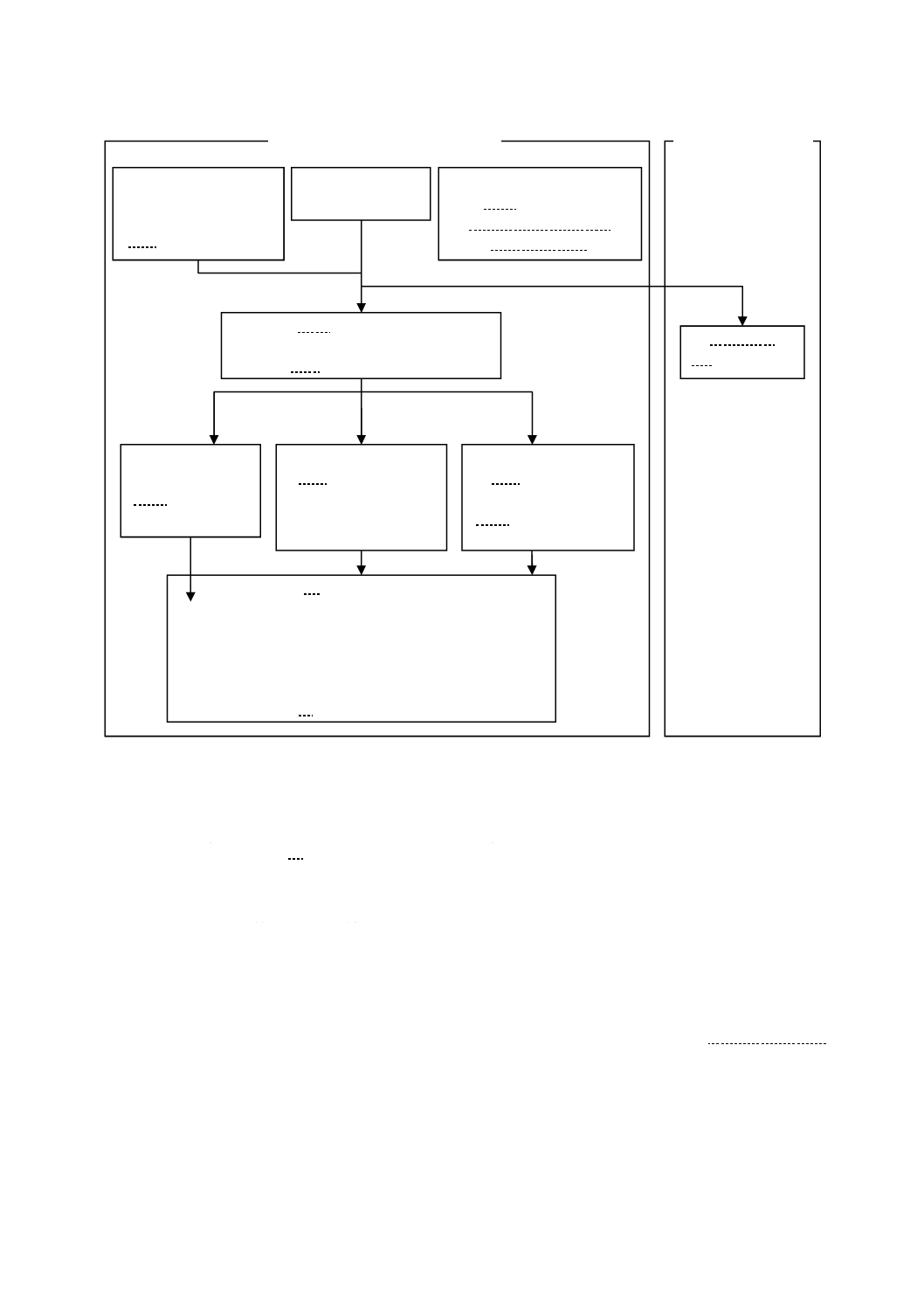
試験方法のフローチャートを図2及び図3に示す。試験片を取り扱う作業でSCDLP培地を加えるまで
の作業を行うときに,安全キャビネット内に漏れる光によって光触媒作用が働かないことを確実にするた
め,照度計及び紫外放射照度計を用いて,安全キャビネットの作業台上の照度及び紫外放射照度を測定す
る。照度が200 lx以上で紫外放射照度が0.001 mW/cm2以上の場合は,照度が200 lx未満で紫外放射照度
が0.001 mW/cm2未満になるよう,要因を取り除いてから試験する。
図2−フィルム密着法のフロート
光照射条件下でのフィルム密着法
試験片
8.1 フィルム密着法
可視光照射条件
9.4.1 照度の測定
試験片設置位置の準備
及び光照射条件
9.2.2 試験片の設置
↓
9.2.3 試験菌液の接種
9.5 生菌数の測定
↓
10 試験結果の計算
↓
12 試験結果の報告
光が当たらない
環境での
フィルム密着法
附属書JA
3個の加工試験片
3個の無加工試験片
3個の
無加工試験片
3個の加工試験片
3個の無加工試験片
試験菌を接種した
試験片
9.4.3 暗所保存
↓
9.2.4 b) 洗い出し
試験菌を接種した
試験片
9.4.2 紫外光照射
↓
9.2.4 b) 洗い出し
接種直後の試験片
9.2.4 a) 洗い出し
細菌
6.1.1 試験に用いる細菌
↓
9.2.1 試験菌液の調製
9
R 1752:2020
図3−ガラス密着法のフローチャート
9.2
フィルム密着法
9.2.1
試験菌液の調製
試験菌液の調製は,JIS R 1702の9.2.1(試験菌液の調製)による。
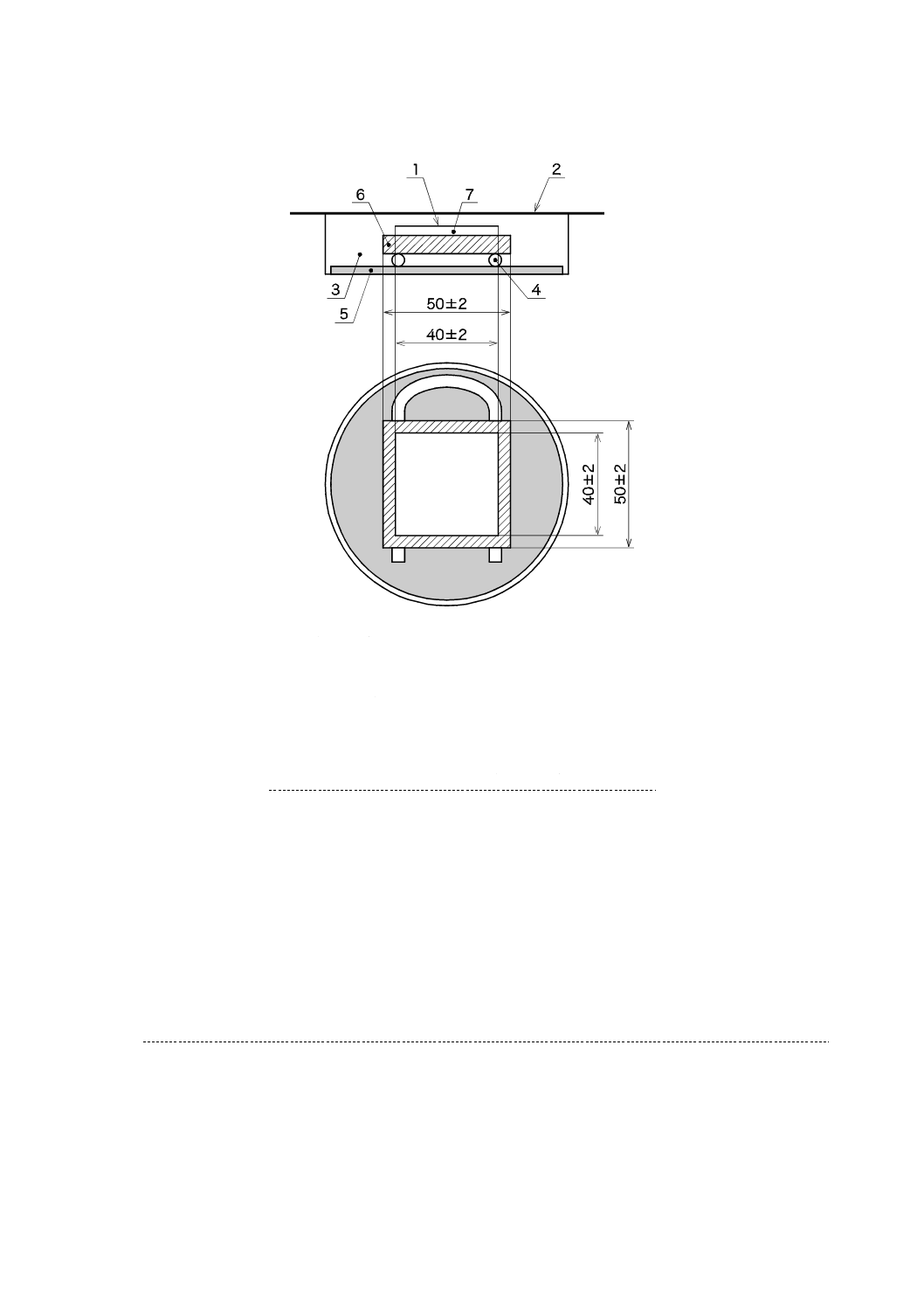
9.2.2
試験片の設置
滅菌済み保存シャーレの底に,滅菌した調湿用ろ紙を置き,滅菌水を適量入れ,試験片と調湿用ろ紙と
が触れないようガラス管又はガラス棒(7.7参照)を置き,その上に可視光応答形光触媒抗菌加工した面を
上にして試験片を置く(図4参照)。試験面は,可視光応答形光触媒抗菌加工した試験片の表面とする。
内部まで可視光応答形光触媒抗菌加工した試験片であっても,切断面は試験面としない。また,高圧蒸気
殺菌によってろ紙が湿った場合は,乾燥させてから使用する。
滅菌水を入れすぎると,保湿用ガラスが曇り,試験に影響するため,滅菌水の量は,4 ml〜6 mlが適切
である。
光照射条件下でのガラス密着法
試験片
8.2 ガラス密着法
可視光照射条件
9.4.1 照度の測定
試験片設置位置の準備
及び光照射条件
9.5 生菌数の測定
↓
10.3.1 生菌数の計算
↓
10.3.2 試験結果の計算
↓
12 試験結果の報告
光が当たらない
環境での
ガラス密着法
JIS L 1902
8.1 菌液吸収法
3個の加工した試験片
3個の無加工試験片
3個の
無加工試験片
3個の加工した試験片
3個の無加工試験片
試験菌接種直後の
試験片
9.3.5 a) 試験菌の
洗い出し
細菌
6.1.2 試験に用いる細菌
↓
9.3.2 試験菌液の調製
9.3.3 試験片の設置
↓
9.3.4 試験菌液の接種
試験菌を接種した試験片
9.4.3 暗所での保存
↓
9.3.5 b) 試験菌の洗い
出し
試験菌を接種した試験片
9.4.2 紫外光照射
↓
9.3.5 b) 試験菌の洗い
出し
10
R 1752:2020
単位 mm
1
密着フィルム
2
保湿用ガラス
3
保存シャーレ
4
ガラス棒・ガラス管
5
調湿用ろ紙
6
試験片
7
試験菌液
図4−フィルム密着法試験片及び保湿用ガラスの組立て
9.2.3
試験菌液の接種
試験菌液の接種は,次による。
a) 9.2.1に規定する試験菌液をピペットで0.15 ml採取し,これを試験菌液として,9.2.2に規定する各試
験片に滴下する。滴下した試験菌液の上に密着フィルムをかぶせ,試験菌液が密着フィルムの端から
こぼれないように注意しながら試験菌液が密着フィルム全体に行き渡るように軽く押さえ付けた後,
保湿用ガラスを載せる(図4参照)。標準の大きさ以外の試験片の場合,試験菌液の接種量は,被覆す
る密着フィルムに合わせて調整する。この手順を試験に使用する試験片(可視光応答形光触媒抗菌加
工した試験片は6個,無加工試験片は9個)全てに行う。
密着フィルムは,あらかじめ裁断したものをエタノールを吸収させた局方ガーゼ,又は脱脂綿を用
いて両面を拭くか,エタノールで両面を拭いた密着フィルムを無菌的に裁断したものを使用すること
が望ましい。また,保湿用ガラスはエタノールを吸収させた局方ガーゼ又は脱脂綿で両面を拭いた後,
十分に乾燥してから使用することが望ましい。
規定に基づく試験菌液量を接種したとき,密着フィルム全体に行き渡らなかったり,密着フィルム
の端から試験菌液が漏れ出す場合がある。このような場合は,接種試験菌液量を規定量の2倍から1/2
11
R 1752:2020
を限度に調整してもよい。ただし,試験片に接種する試験菌液は接種試験菌液量を変更した場合にお
いても,1試験片当たり1.0×105個〜4.0×105個とする。この場合,試験菌液の菌数は,9.2.1 b)の規
定によらず,接種試験菌液量から換算して調整する。
b) 試験菌液接種直後の生菌数測定用の3個の無加工試験片を除いて,試験菌液を接種した後,速やかに,
9.4に規定する光照射試験に進む。
9.2.4
試験菌の洗い出し
試験菌液の洗い出しは,次による。
a) 試験菌液接種直後の試験片 試験菌液接種直後の生菌数測定用の3個の無加工試験片については,密
着フィルム及び無加工試験片を滅菌ピンセットを用い,試験菌液が漏れないように注意しながら,ス
トマッカー袋に入れる。10 mlのSCDLP培地を加え,ストマッカー袋の外側から試験片とフィルムを
手でよくもんで,試験菌を洗い出す。この洗い出し液は速やかに9.5に規定する測定を行う。同等の
結果が得られる場合は,ストマッカー袋に代わるものを用いてもよい。
試験片の大きさによって,SCDLP培地10 mlで洗い出しが困難な場合は,液量を増やしてもよい。
b) 試験後の試験片 9.4.2及び9.4.3に規定する試験片について,a)と同様に試験菌を洗い出す。この洗
い出し液は,速やかに9.5に規定する測定を行う。
9.3
ガラス密着法
9.3.1
試験菌の培養
試験菌の培養は,JIS R 1702の9.3.1(試験菌の培養)による。
9.3.2
試験菌液の調製
試験菌液の調製は,JIS R 1702の9.3.2(試験菌液の調製)による。
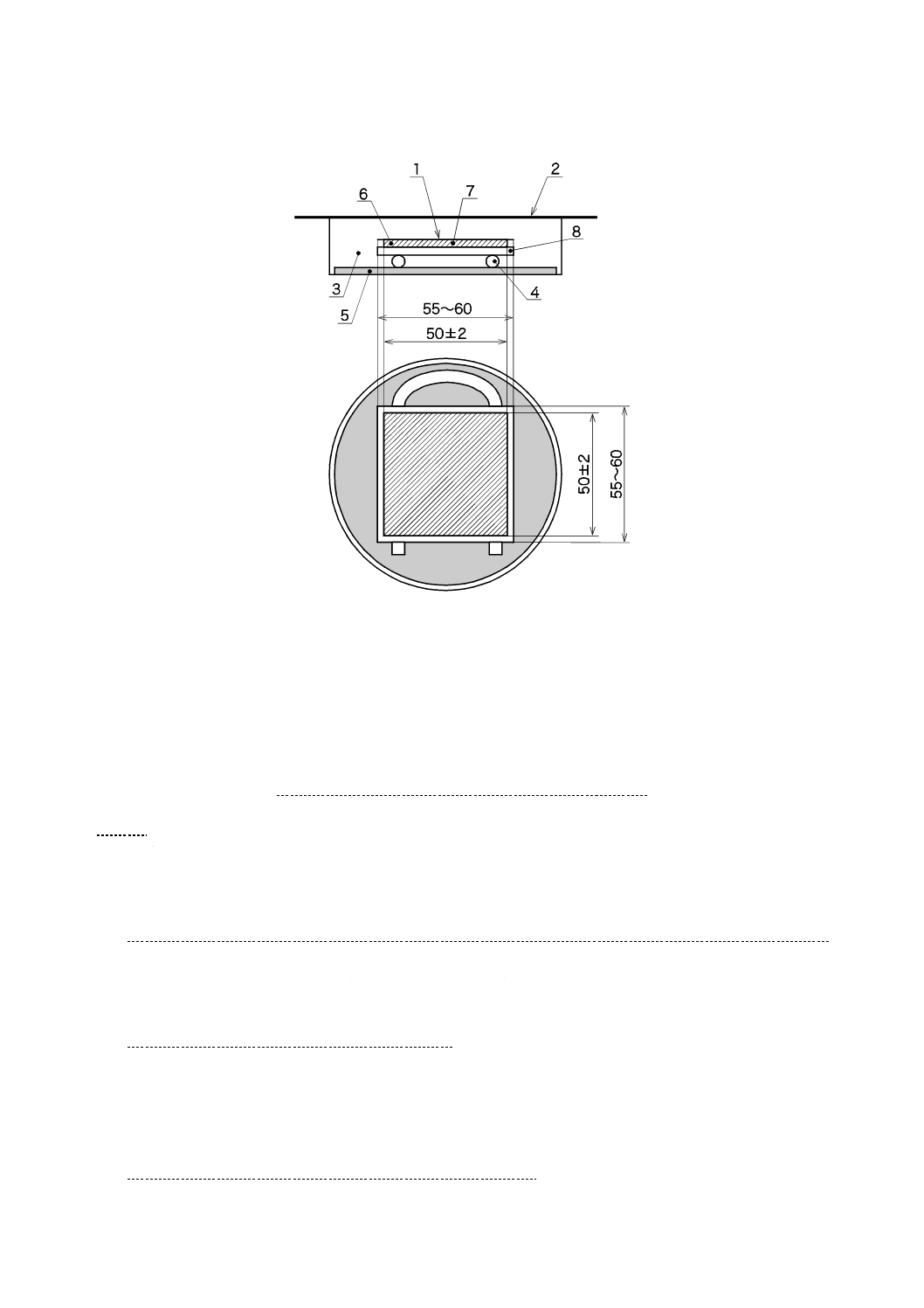
9.3.3
試験片の設置
滅菌済保存シャーレの底に,滅菌した調湿用ろ紙を置き,滅菌水を適量入れ,試験片と調湿用ろ紙とが
触れないようガラス管又はガラス棒を置き,その上に一辺が55 mm〜60 mmの正方形の殺菌したガラス板
を置く。その上に可視光応答形光触媒抗菌加工した面を上にして試験片を置く(図5参照)。高圧蒸気殺
菌によってろ紙が湿った場合は,乾燥させてから使用する。
滅菌水を入れすぎると,保湿用ガラスが曇り,試験に影響するため,滅菌水の量は,4 ml〜6 mlが適切
である。
12
R 1752:2020
単位 mm
1
密着ガラス
2
保湿用ガラス
3
保存シャーレ
4
ガラス棒・ガラス管
5
調湿用ろ紙
6
試験片
7
試験菌液
8
ガラス板
図5−ガラス密着法試験片及び保湿用ガラスの組立て
9.3.4
試験菌液の接種
試験菌液の接種は,次による。
a) 9.3.2に規定する試験菌液をピペットで0.2 ml採取し,これを試験菌液として,9.3.3に規定する各試
験片の数箇所に滴下接種する。滴下した試験菌液の上に滅菌した密着ガラスをかぶせ,試験菌液が密
着ガラスの端からこぼれないように注意しながら試験菌液が密着ガラス全体に行き渡るように軽く押
さえ付けた後,保湿用ガラスを載せる(図5参照)。この手順を試験に使用する試験片(可視光応答形
光触媒抗菌加工した試験片は6個,無加工試験片は9個)全てに行う。
密着ガラス及び保湿用ガラスは,エタノールを吸収させた局方ガーゼ又は脱脂綿で両面を拭いて,
十分に乾燥してから使用することが望ましい。
規定に基づく試験液量を接種したとき,試験片全体に行き渡らなかったり,試験片の端から試験液
が漏れ出したりする場合がある。このような場合は,接種菌液量を規定量の2倍から1/2を限度に調
整してもよい。ただし,試験片に接種する試験菌液は接種菌液量を変更した場合においても,標準の
液量の場合と同様に1試験片当たり1.4×104個〜2.6×104個とする。この場合,試験菌液の菌数は,
9.3.2の規定によらず,接種菌液量から換算して調整する。
13
R 1752:2020
試験片に試験菌液を十分に浸透させるため,非イオン界面活性剤0.05 %を含む試験菌液を用いても
よい。試験菌液に非イオン界面活性剤を使用した場合は,その記録を試験報告書に記載する。
b) 試験菌液接種直後の生菌数測定用の3個の無加工試験片を除いて,試験菌液を接種した後,速やかに,
9.4に規定する光照射試験に進む。
9.3.5
試験菌の洗い出し
試験菌液の洗い出しは,次による。
a) 試験菌液接種直後の試験片 試験菌液接種直後の3個の無加工試験片については,密着ガラス,無加
工試験片及びガラス板を滅菌ピンセットを用いて試験菌液が漏れないように注意しながら,ストマッ
カー袋に入れる。20 mlの洗い出し用生理食塩水又はSCDLP培地のいずれか1種類だけを加え,スト
マッカー袋の外側から試験片,ガラス板及び密着ガラスを手で十分にもみ,試験菌を洗い出す。この
洗い出し液は,速やかに9.5に規定する測定を行う。また,試験菌の洗い出しについては,この方法
と同等の結果が得られる場合は,ストマッカー袋に代わるものを用いてもよい。
b) 試験後の試験片 9.4.2及び9.4.3に規定する試験片について,a)と同様に試験菌を洗い出す。この洗
い出し液は,速やかに9.5に規定する測定を行う。
9.4
可視光照射条件
9.4.1
照度の測定,試験片設置位置及び光照射条件
可視光応答形光触媒材料を使用する状況に応じて,7.10に規定するシャープカットフィルタを選択する。
試験装置の試験片表面と同じ高さに照度計の受光部基準面を据え付ける。受光部の上に試験に使用する
密着フィルム及び保湿用ガラス板を置く。指示値を読み取りながら,試験片の表面で,500 lx±25 lxの照
度が得られる位置を決め,試験片設置位置とする。照度を測定する場合は,照度を安定化させるため,試
験装置の蛍光ランプを30分以上予備点灯しておく。蛍光ランプから発生する熱による影響を避けるために,
3 000 lxを上限とする。
照度は,可視光応答形光触媒を効果的に使用される場所を考慮して,100 lx±5 lx〜3 000 lx±150 lxの範
囲で変更してもよい。
なお,照度の設定については,JIS Z 9110,JIS Z 9125,社団法人照明学会編 住宅照明設計技術指針
(JIEG-009)及び社団法人照明学会編 オフィス照明設計技術指針(JIEG-008)を参照するのがよい。
9.4.2
試験菌液を接種した試験片の光照射
試験菌液を接種した試験片を入れた保存シャーレ(無加工試験片3個及び可視光応答形光触媒抗菌加工
した試験片3個)を,9.4.1で準備した試験片設置位置へ置き,8時間光照射する。この操作の間は,試験
片周囲の温度を25 ℃±3 ℃を保つようにする。
可視光応答形光触媒抗菌加工材料の用いられる場所の実情を考慮して,光照射時間を4時間を下限とし
て短くしてもよい。
9.4.3
試験菌液を接種した試験片の暗所での保存
試験菌液を接種した試験片を入れた保存シャーレ(無加工試験片3個及び可視光応答形光触媒抗菌加工
した試験片3個)を9.4.2に規定する試験と同じ時間,7.13に規定する暗箱の中に保存する。この操作の
間は,試験片周囲の温度を25 ℃±3 ℃に保つ。
保存シャーレを覆う保湿用ガラスの代わりに,保存シャーレの蓋を用いてもよい。
9.5
生菌数の測定
生菌数の測定は,JIS R 1702の9.5による。
14
R 1752:2020
10 試験結果の計算
10.1 一般事項
試験結果は,次のように計算する。
a) 3個の試験片の生菌数の平均値は,10.2.1及び10.3.1に規定する方法で求めた数値を用いて計算し,抗
菌活性値の計算時には四捨五入しない数値を用いる。
b) 得られた抗菌活性値は,小数点2桁目を四捨五入する。
c) 報告書に記載する平均値は,有効数字3桁目を四捨五入して有効数字2桁とした数値を用いる。
10.2 フィルム密着法
10.2.1 生菌数の計算
9.5によって求めた菌濃度を用い,式(1)によって生菌数を求める。
N=P×V ·················································································· (1)
ここに,
N: フィルム密着法による生菌数(個)
P: 9.5によって求めた菌濃度(個/ml)
V: 洗い出しに用いたSCDLP培地の液量(ml)
洗い出し液1.0 mlを用いたシャーレによって生残菌が認められない場合は,生菌数は“<10”と表示し
(Vが10 mlの場合),10.2.2では,“10”を用いて計算する。
10.2.2 試験結果の計算
試験結果は,次による。
a) 試験成立条件 次の4項目の試験成立条件を全て満たすとき,その試験は有効と判定する。1項目で
も条件を満足しない場合は,試験不成立と判定し,再度試験を実施する。
1) 無加工試験片の接種直後の生菌数の対数値について,次の式(2)が成立する。
(Logmax−Logmin)/(Logmean)≦0.2 ······················································· (2)
ここに,
Logmax: 3個の試験片の生菌数の常用対数値の最大値
Logmin: 3個の試験片の生菌数の常用対数値の最小値
Logmean: 3個の試験片の生菌数の常用対数値の平均値
2) 無加工試験片の接種直後の生菌数の平均値は,1.0×105個〜4.0×105個である。
3) 無加工試験片の光照射後の生菌数は,3個の値が全て1.0×103個以上である。ただし,無加工試験
片にガラス板を用いた場合は,光照射後の生菌数の値が全て1.0×104個以上とする。
4) 無加工試験片の暗所に保存した後の生菌数は,3個の値が全て1.0×103個以上である。ただし,無
加工試験片にガラス板を用いた場合は,暗所に保存した後の生菌数の値が全て1.0×104個以上とす
る。
b) 平板状の可視光応答形光触媒抗菌加工材料の抗菌活性値の計算 試験成立時の平板状の可視光応答
形光触媒抗菌加工材料の抗菌活性値の計算は,式(3)による。
RF-L=log(BF-L/A)−log(CF-L/A)=log(BF-L/CF-L) ····································· (3)
ここに, RF-L: 可視光照射条件F-Lで光照射した平板状の可視光応答形光触
媒抗菌加工材料による抗菌活性値
A: 無加工試験片の接種直後の3個の試験片の生菌数の平均値
(個)
BF-L: 無加工試験片を可視光照射条件F-Lで光照射した後の3個の
試験片の生菌数の平均値(個)。Fはシャープカットフィルタ
の種類(A又はB)。Lは照度(lx)。
CF-L: 可視光応答形光触媒抗菌加工した試験片を可視光照射条件
F-Lで光照射した後の3個の試験片の生菌数の平均値(個)

15
R 1752:2020
c) 平板状の可視光応答形光触媒抗菌加工材料の光照射による抗菌活性値の計算 平板状の可視光応答
形光触媒抗菌加工材料の光照射による抗菌活性値ΔRの計算式は,式(4)による。
ΔR=log(BF-L/CF-L)−[log(BD/A)−log(CD/A)]=log(BF-L/CF-L)−log(BD/CD) ··· (4)
ここに, ΔR: 平板状の可視光応答形光触媒抗菌加工材料の光照射による抗
菌活性値
BD: 無加工試験片を暗所に保存した後の3個の試験片の生菌数の
平均値(個)
CD: 可視光応答形光触媒抗菌加工した試験片を暗所に保存した後
の3個の試験片の生菌数の平均値(個)
10.3 ガラス密着法
10.3.1 生菌数の計算
9.5で求めた菌濃度を用いて,次の式(5)によって生菌数を求める。
M=P×20 ················································································ (5)
ここに,
M: ガラス密着法による生菌数(個)
P: 9.5によって求めた菌濃度(個/ml)
20: 洗い出しに用いた生理食塩水の量(ml)
洗い出し液1.0 mlを用いたシャーレから生残菌が認められない場合は,洗い出し液に20 mlを用いてい
ることから生菌数は“<20”と表示し,10.3.2では,“20”を用いて計算する。
10.3.2 試験結果の計算
試験結果は,次による。
a) 試験成立条件 試験成立の判定は,増殖値によって行う。増殖値を式(6)及び式(7)によって求め,小数
点2桁目を四捨五入する。増殖値が0を超える場合は,試験成立と判定し,増殖値が0以下の場合は,
試験不成立と判定し,再度試験を実施する。
HF-L=MB F-L−MB A ······································································ (6)
ここに,
HF-L: 可視光照射条件F-Lで試験した増殖値
MB F-L: 無加工試験片を可視光照射条件F-Lで光照射した後の3個の
試験片の生菌数の算術平均値の常用対数値。
Fは試験で用いたシャープカットフィルタの種類(A又はB)。
Lは試験で用いた照度(lx)。
MB A: 無加工試験片の接種直後の3個の試験片の生菌数の算術平均
値の常用対数値
HD=MB D−MB A ········································································· (7)
ここに,
HD: 暗所で試験した増殖値
MB D: 無加工試験片を暗所で保存した後の3個の試験片の生菌数の
算術平均値の常用対数値
b) 繊維状の可視光応答形光触媒抗菌加工材料の試験成立の判定及び抗菌活性値の計算 試験成立時の
繊維状の可視光応答形光触媒抗菌加工材料の抗菌活性値の計算は,式(8)による。
SF-L=MB F-L−MF-L ······································································· (8)
ここに, SF-L: 可視光照射条件F-Lで光照射した繊維状の可視光応答形光触
媒抗菌加工材料による抗菌活性値
MF-L: 可視光応答形光触媒抗菌加工した試験片を可視光照射条件
F-Lで光照射した後の3個の試験片の生菌数の算術平均値の常
用対数値
c) 繊維状の可視光応答形光触媒抗菌加工材料の光照射による抗菌活性値の計算 繊維状の可視光応答
形光触媒抗菌加工材料の光照射による抗菌活性値ΔSの計算は,式(9)による。

16
R 1752:2020
ΔS=(MB F-L−MF-L)−(MBD−MD) ····················································· (9)
ここに,
ΔS: 繊維状の可視光応答形光触媒抗菌加工材料の光照射による抗
菌活性値
MD: 可視光応答形光触媒抗菌加工した試験片を暗所に保存した後
の3個の試験片の生菌数の算術平均値の常用対数値
11 抗菌効果の判定
抗菌効果の有無の判定は,試験方法によって区分し,次による。
a) 光照射条件下でのフィルム密着法による判定 10.2.2 b) の式(3)によって算出した平板状の可視光応
答形光触媒抗菌加工材料の抗菌活性値が2.0以上のとき,平板状の可視光応答形光触媒抗菌加工材料
は抗菌効果があるものと判定する。受渡当事者間の協定によって,2.0を上回る数値をもって抗菌効果
の有無を判定してもよい。
なお,平板状の可視光応答形光触媒抗菌加工材料の光照射による抗菌活性値は,10.2.2 c) の式(4)に
よって算出する。
b) 光が当たらない環境でのフィルム密着法による判定 附属書JAによって算出した平板状の可視光応
答形ハイブリッド光触媒抗菌加工材料の抗菌活性値が2.0以上のとき,平板状の可視光応答形ハイブ
リッド光触媒抗菌加工材料は,光が当たらない環境においても抗菌効果があるものと判定する。受渡
当事者間の協定によって,2.0を上回る数値をもって抗菌効果の有無を判定してもよい。
c) 光照射条件下でのガラス密着法による判定 10.3.2 b) の式(8)によって算出した繊維状の可視光応答
形光触媒抗菌加工材料の抗菌活性値が2.0以上のとき,繊維状の可視光応答形光触媒抗菌加工材料は
抗菌効果があるものと判定する。受渡当事者間の協定によって,2.0を上回る数値をもって抗菌効果の
有無を判定してもよい。
なお,繊維状の可視光応答形光触媒抗菌加工材料の光照射による抗菌活性値は,10.3.2 c) の式(9)に
よって算出する。
d) 光が当たらない環境でのガラス密着法による判定 JIS L 1902の8.1.5.2(試験試料での試験成立の判
定及び抗菌活性値の計算)によって算出した繊維状の可視光応答形ハイブリッド光触媒抗菌加工材料
の抗菌活性値が2.0以上のとき,繊維状の可視光応答形ハイブリッド光触媒抗菌加工材料は,光が当
たらない環境においても抗菌効果があるものと判定する。受渡当事者間の協定によって,2.0を上回る
数値をもって抗菌効果の有無を判定してもよい。
12 試験結果の報告
試験結果の報告には,次の項目について記載する(表1参照)。
a) 規格番号及び試験方法の種類
b) 可視光応答形光触媒抗菌加工した試験片及び無加工試験片の種類・大きさ・形状・厚さ
c) 光源の種類,製造業者名及び品番
d) シャープカットフィルタの種類(製造業者名及び品番)
e) 照度計及び紫外放射照度計の製造業者名及び品番
f)
有機物を除去した場合の光源の情報(種類,製造業者名及び品番,照射時間など)
g) 光照射条件(照度,光照射時間)
h) 試験に用いた細菌の種類及び細菌の保存番号
17
R 1752:2020
i)
フィルム密着法の場合 密着フィルム・保湿用ガラスの種類及び大きさ,試験に用いた細菌の種類及
び細菌の保存番号,試験菌液の接種量,試験菌液の生菌数,並びに試験値(A,BL,CL,RL,BD,CD,
ΔR,並びに可視光応答形ハイブリッド光触媒抗菌加工した試験片の場合は,附属書JAによって算出
した抗菌活性値)
j)
ガラス密着法の場合 密着ガラス・保湿用ガラスの種類及び大きさ,試験に用いた細菌の種類及び細
菌の保存番号,試験菌液の接種量,試験菌液の濃度,並びに試験値(SL及びΔS)
k) ガラス密着法の場合 試験菌液に非イオン界面活性剤を添加した場合の情報(名称及び濃度)
l)
その他の必要事項
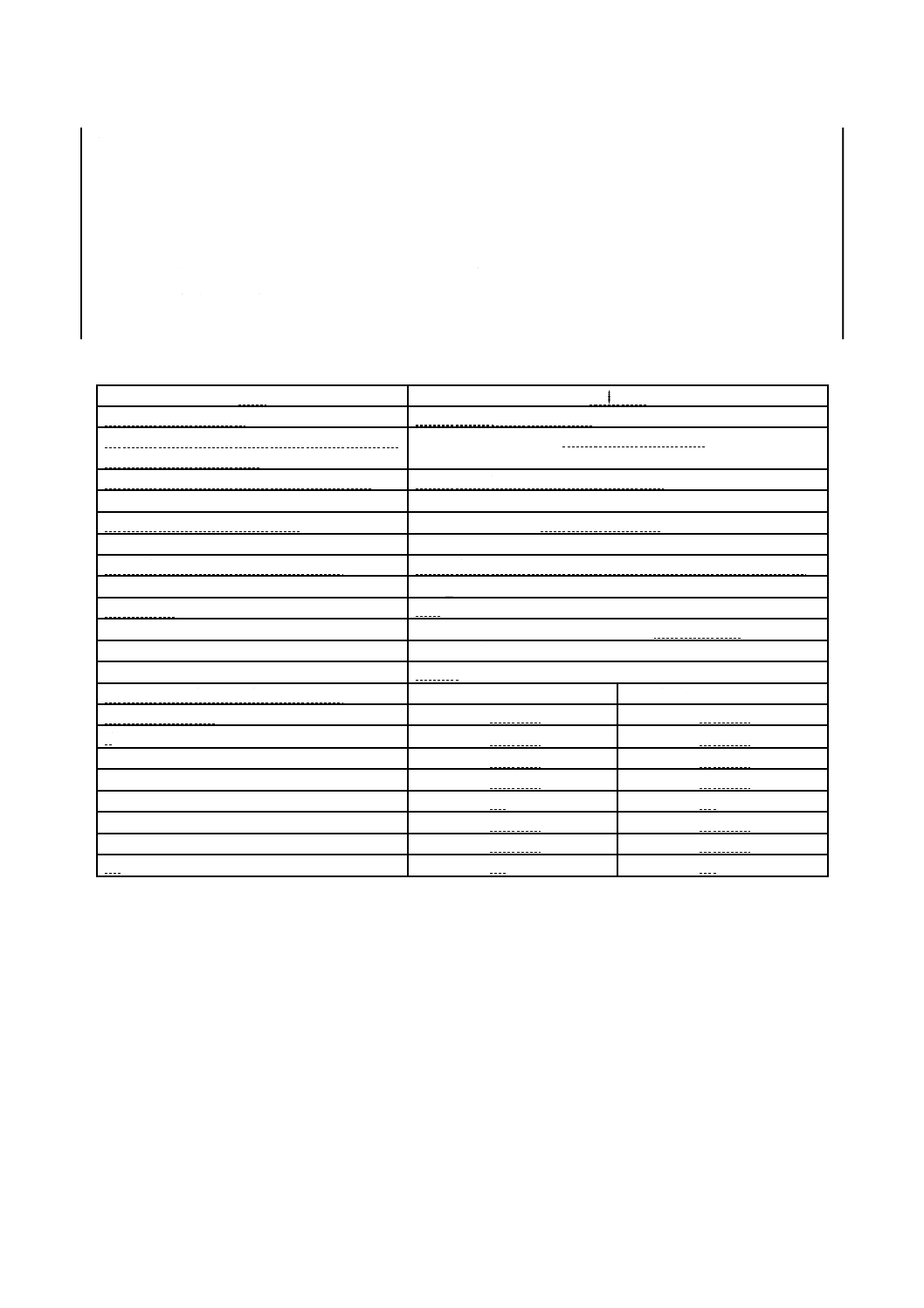
表1−試験結果の報告例
項目
記載内容
規格番号及び試験方法
JIS R 1752 フィルム密着法
可視光応答形光触媒抗菌加工した試験片の種
類・大きさ・形状・厚さ
単味光触媒フィルム,50 mm×50 mm×0.2 mm
無加工試験片の種類・大きさ・形状・厚さ
PETフィルム,50 mm×50 mm×0.2 mm
光源の種類,製造業者名及び品番
白色蛍光灯(○○電機,FL20S・W)
シャープカットフィルタの種類
タイプA(波長400 nm以下をカット)
照度計の製造業者名及び品番
照度計(△△製作所,本体:FL-X,受光部:FL-Y)
紫外放射照度計の製造業者名及び品番
紫外放射測定器(△△製作所,本体:UV-X,受光部:UV-Y)
有機物の除去方法
FL20̲BLB,1.0 mW/cm2で24時間予備照射
光照射条件
500 lxで,8時間
密着フィルムの種類,又は密着ガラスの種類
ポリプロピレンフィルム(□□商会),40 mm×40 mm
保湿用ガラスの種類
ほうけい酸ガラス
菌液接種量
0.10 ml
試験に用いた菌種(細菌の保存番号)
黄色ぶどう球菌(NBRC 12732) 大腸菌(NBRC 3972)
試験菌液の生菌数
2.0×106
3.2×106
A
2.0×105
3.2×105
BA-1000
3.2×105
2.0×106
CA-1000
5.0×102
3.1×103
RA-1000
2.8
2.8
BD
3.5×105
2.2×106
CD
2.8×105
1.8×106
ΔR
2.7
2.7
18
R 1752:2020
附属書JA
(規定)
平板状の可視光応答形ハイブリッド光触媒抗菌加工材料の
光が当たらない環境での抗菌性試験方法及び抗菌効果
JA.1 一般
この附属書は,平板状の可視光応答形ハイブリッド光触媒抗菌加工平板状材料及び製品の可視光が当た
らない環境での抗菌性を測定する手順について,JIS Z 2801の5.6(試験操作)に規定する操作に代わる試
験操作を規定する。
なお,ここに規定していない項目,箇条3(用語及び定義),5.7(生菌数の計算),5.8(試験結果)及び
箇条6(試験結果の記録)については,JIS Z 2801による。また,抗菌効果については,JIS Z 2801の箇条
4(抗菌効果)に従う。
JA.2 概要
JIS Z 2801では,抗菌加工製品の抗菌性試験法及び抗菌効果について規定しているが,可視光の影響を
考慮していない。平板状の可視光応答形ハイブリッド光触媒抗菌加工材料及び製品の可視光が当たらない
環境での抗菌性を測定するためには,光(可視光及び波長300 nm〜380 nmの光)の影響を排除しないと,
可視光応答形光触媒による抗菌性も含めて評価することになる。そこで,JIS Z 2801に記載されている試
験方法に,光の影響を排除した試験条件で抗菌性を評価するために必要な手順を追加する。
JA.3 試験操作
JA.3.1 一般事項
一般事項は,JIS R 1702のJA.3.1(一般事項)による。
JA.3.2 細菌株の保存
細菌株の保管及び継代は,JIS R 1702のJA.3.2(細菌株の保存)による。
JA.3.3 試験菌の前培養
試験菌の前培養は,JIS R 1702のJA.3.3(試験菌の前培養)による。
JA.3.4 試験に用いる安全キャビネット,容器及び培養器の評価(照度及び紫外放射照度の測定)
試験に用いる安全キャビネット,容器及び培養器の評価は,次による。
a) 試験片を取り扱うJA.3.6,JA.3.8及びJA.3.10の作業を行う場合に,安全キャビネット内に漏れる光
によって可視光応答形光触媒作用が働かないことを確実にするため,照度計及び紫外放射照度計を用
いて,安全キャビネットの作業台上の照度及び紫外放射照度を測定する。照度が200 lx以上で紫外放
射照度が0.001 mW/cm2以上の場合は,照度が200 lx未満で紫外放射照度が0.001 mW/cm2未満になる
よう,要因を取り除いてから試験する。
b) 試験片を取り扱うJA.3.6の作業を行うときに,試験片を保管する容器内に漏れる光によって可視光応
答形光触媒作用が働かないことを確実にするため,照度計及び紫外放射照度計を用いて,容器内の照
度及び紫外放射照度を測定する。照度が10 lx以上で紫外放射照度が0.001 mW/cm2以上の場合は,照
度が10 lx未満で紫外放射照度が0.001 mW/cm2未満になるよう,要因を取り除いてから試験する。
c) 試験片を培養する培養器内に漏れる紫外線によって光触媒作用が働かないことを確実にするため,照
19
R 1752:2020
度計及び紫外放射照度計を用いて,培養器内の照度及び紫外放射照度を測定する。照度が10 lx以上
で紫外放射照度が0.001 mW/cm2以上の場合は,照度が10 lx未満で紫外放射照度が0.001 mW/cm2未満
になるよう,窓を覆い隠すなど,要因を取り除いてから試験する。
JA.3.5 試験片の調製
試験片の調製は,次による。
a) 可視光応答形ハイブリッド光触媒抗菌加工平板状材料及び無加工材料の平らな部分を50 mm±2 mm
角(厚さ10 mm以内)の正方形に切り取り,これを標準の大きさの試験片とする。
材料を50 mm±2 mm角(厚さ10 mm以内)の正方形に切り取ることが困難又は不可能な場合,表
面積800 mm2〜1 600 mm2の密着フィルムをかぶせることが可能な試験片の形状及び大きさのときは,
ここに規定する形状及び大きさ以外の試験片を使用してもよい。
b) これらの試験片を,無加工試験片は6個,可視光応答形ハイブリッド光触媒抗菌加工した試験片は3
個準備する。
c) 無加工材料から無加工試験片が準備できない場合は,8.1 b)のガラス板を使用してもよい。試験片の調
製に当たっては,微生物汚染,試験片間の相互汚染及び汚れに十分注意する。
JA.3.6 試験片の清浄化及び保管
試験片に紫外線が作用しないようにするため,次によってJA.3.4 a) に規定する状態に保った安全キャ
ビネット内で作業する。
a) JA.3.5の試験片の全面を,エタノールを吸収させた局方ガーゼ又は脱脂綿で軽く2〜3回拭いた後,十
分に乾燥する。
b) JA.3.5に規定する各試験片を試験面を上にして滅菌済みシャーレ内に置く。ただし,直ちにJA.3.7に
規定する手順に移らない場合には,JA.3.7に規定する作業を始めるまでの間,JA.3.4 b) に規定する容
器内で保管する。試験面は,可視光応答形ハイブリッド光触媒抗菌加工が施されている試験片の表面
とし,内部まで可視光応答形ハイブリッド光触媒抗菌加工されている試験片であっても,切断面は試
験面としない。
JA.3.7 試験菌液の調製
試験菌液の調製は,JIS R 1702のJA.3.7(試験菌液の調製)による。
JA.3.8 試験菌液の接種
試験片に紫外線が作用しないようにするため,次によってJA.3.4 a)の状態に保った安全キャビネット内
で作業する。このとき,試験片に光が当たる時間は10分以内とし,直ちに作業に移れない場合は,試験片
に光が当たらないよう7.13の暗箱などを使って,光を遮る。
a) JA.3.7の試験菌液をピペットで0.4 ml採取し,これをシャーレ内の各試験片に滴下する。標準の大き
さ以外の試験片の接種菌液量は,被覆した密着フィルムに合わせて調整する。また,標準の大きさの
試験片であっても,規定に基づく菌液量を接種したとき,陶磁器,タイル,ほうろう,ガラスなどの
ぬれ性が極めてよい試験片では,僅かな傾斜で密着フィルムが移動したり,密着フィルムの端から菌
液が漏れ出す場合がある。このような場合は,接種菌液の液量を規定量の1/4を限度に減じてもよい。
ただし,試験片に接種する菌数は接種菌液量を少なくした場合においても,標準の大きさの試験片の
場合と同様に1試験片当たり1.0×105個〜4.0×105個(6.2×103個/cm2〜2.5×104個/cm2)とする。
b) 滴下した試験菌液の上に密着フィルムをかぶせ,菌液が密着フィルムの端からこぼれないように注意
しながら,試験菌液が密着フィルム全体に行き渡るように軽く押さえ付けた後,シャーレの蓋をする
(図JA.1参照)。密着フィルムの大きさは,40 mm±2 mm角の正方形を標準とする。試験片が標準の
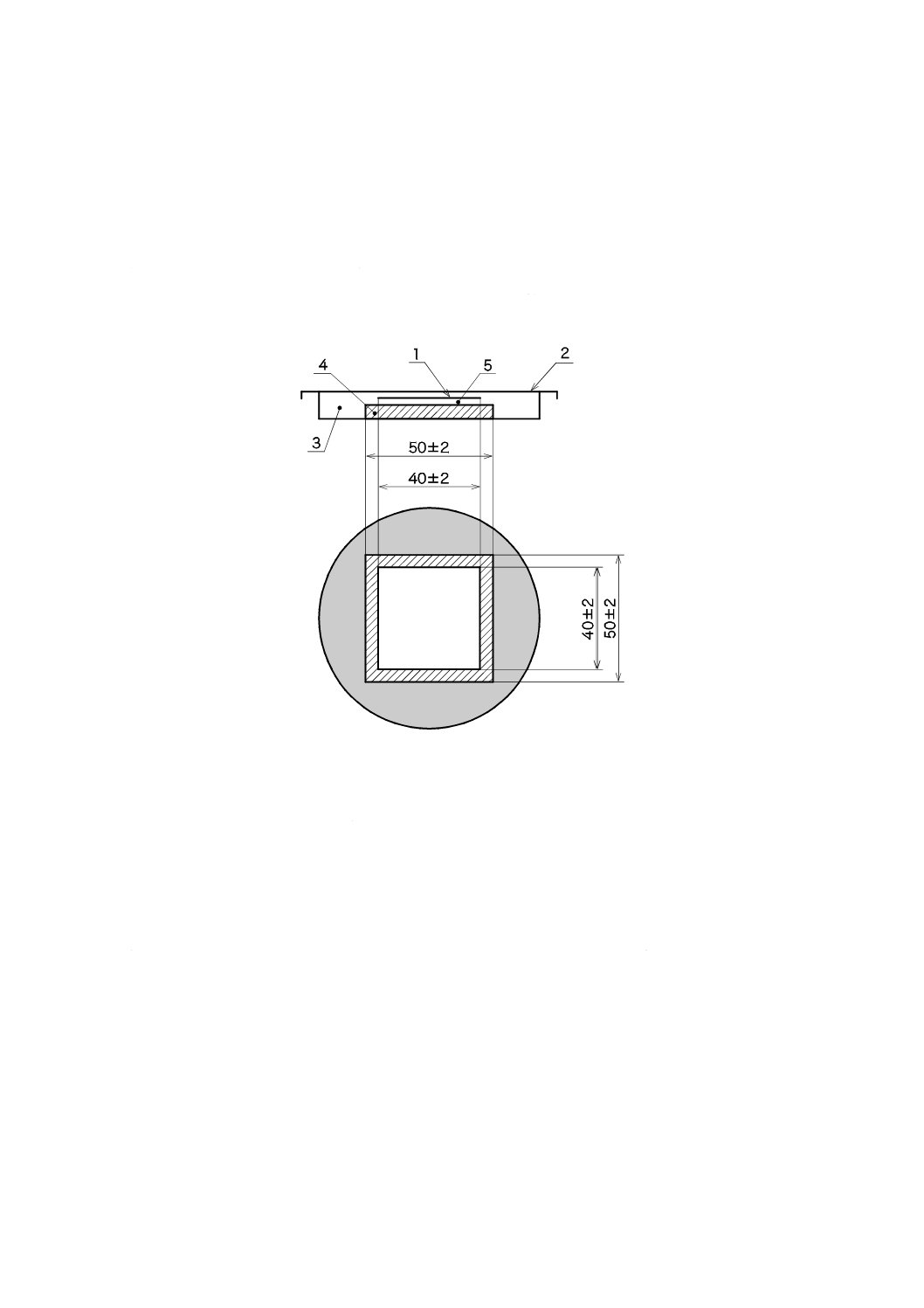
20
R 1752:2020
大きさ以外の場合は,密着フィルムが試験片より内側となるように大きさを調整する。ただし,密着
フィルムの面積は,800 mm2より大きくする。
c) 例えば,試験片の大きさが標準の3/4の大きさの場合には,1試験片当たり7.5×104個〜3.0×105個の
試験菌液を接種する。このとき,ぬれ性がよく,標準の大きさの試験片で1試験片当たり0.15 ml接
種する場合で想定すると,試験片の大きさが標準の3/4の大きさの場合には,6.7×105個/ml〜2.6×106
個/mlとなるように試験菌液を調製し,試験片には0.11 ml接種する。
d) 直ちにb)のシャーレを相対湿度90 %以上になるように調整した蓋の付いた容器に入れる。
単位 mm
1
密着フィルム
2
シャーレ蓋
3
シャーレ
4
試験片
5
試験菌液
図JA.1−試験片の組立て
JA.3.9 試験菌液を接種した試験片の培養
試験菌液を接種した試験片(無加工試験片3個及び可視光応答形ハイブリッド光触媒抗菌加工した試験
片3個)を入れたシャーレが入った容器を直ちにJA.3.4 c)の培養器に入れ,温度35 ℃±1 ℃で24時間±
1時間培養する。
JA.3.10 接種した試験菌の洗い出し
JA.3.10.1 試験菌液接種直後の試験片
JA.3.8の試験菌液を接種した直後の無加工試験片3個について,密着フィルム及び試験片をそれぞれ菌
液がこぼれないように注意しながらそれぞれ別のシャーレに置く。シャーレ内に6.2.1に規定するSCDLP
培地10 mlを加え,ピペットで無加工試験片上の試験菌を最低4回洗い出し,菌液を完全に回収する。こ
の洗い出し液は,速やかにJA.3.11に規定する測定を行う。また,試験菌の洗い出しについては,この方
法と同等又はそれ以上の回収率が認められる他の方法を用いてもよい。
21
R 1752:2020
なお,試験片に光が作用しないようにするため,SCDLP培地を加えるまでは,JA.3.4 a)の状態に保った
安全キャビネット内で作業する。このとき,SCDLP培地を加えるまでに試験片に光が当たる時間は,10
分以内とし,直ちに作業に移れない場合は,試験片に光が当たらないよう7.13に規定する暗箱などを使っ
て光を遮る。
試験片の大きさ又は特性上,SCDLP培地10 mlで洗い出しが困難な場合は,液量を増やしてもよい。
JA.3.10.2 培養後の試験片
JA.3.9の培養後の試験片について,JA.3.10.1と同様に試験菌を洗い出す。この洗い出し液は,速やかに
生菌数測定に供する。また,試験菌の洗い出しについては,この方法と同等又はそれ以上の回収率が認め
られる他の方法を用いてもよい。
なお,試験片に紫外線が作用しないようにするため,SCDLP培地を加えるまでは,JA.3.4 a)の状態に保
った安全キャビネット内で作業する。このとき,SCDLP培地を加えるまでに試験片に光が当たる時間は
10分以内とし,直ちに作業に移れない場合は,試験片に光が当たらないよう7.13に規定する暗箱などを使
って光を遮る。
試験片の大きさ又は特性上,SCDLP培地10 mlで洗い出しが困難な場合は,液量を増やしてもよい。
JA.3.11 寒天平板培養法による生菌数の測定
寒天平板培養法による生菌数の測定は,JIS R 1702のJA.3.11(寒天平板培養法による生菌数の測定)に
よる。
参考文献
[1] JIS Z 9110 照明基準総則
[2] JIS Z 9125 屋内作業場の照明基準
注記 対応国際規格:ISO 8995,Lighting of indoor work places
[3] 抗菌加工製品ガイドライン,通商産業省生活産業局編,(1998)
[4] 公益社団法人日本薬学会編 衛生試験法・注解(2015)
[5] 厚生労働省監修 食品衛生検査指針微生物編(2015)
[6] 住宅照明設計技術指針(JIEG-009),社団法人照明学会
[7] オフィス照明設計技術指針(JIEG-008),社団法人照明学会
[8] JIS Z 9110 照明基準総則
22
R 1752:2020
附属書JB
(参考)
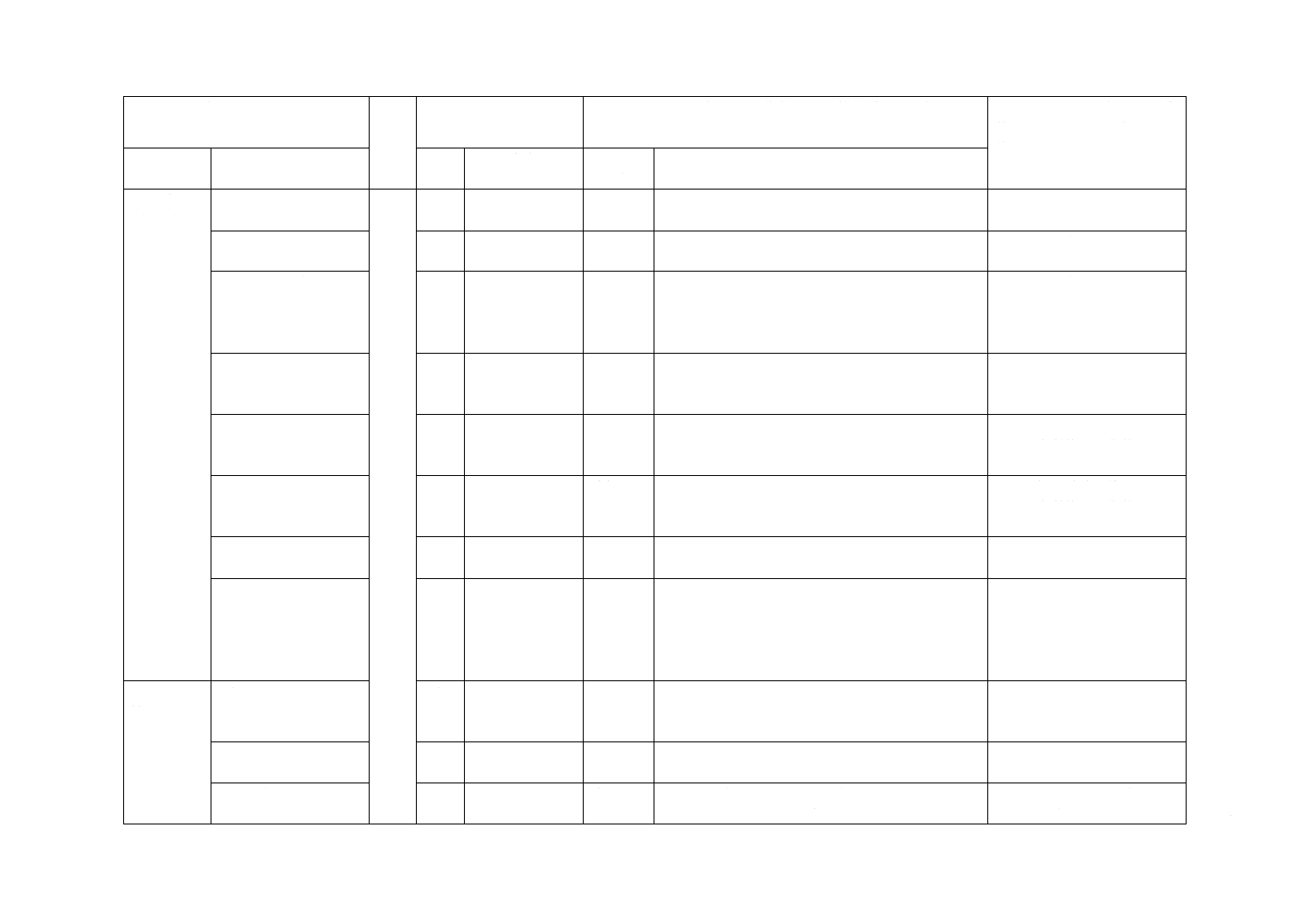
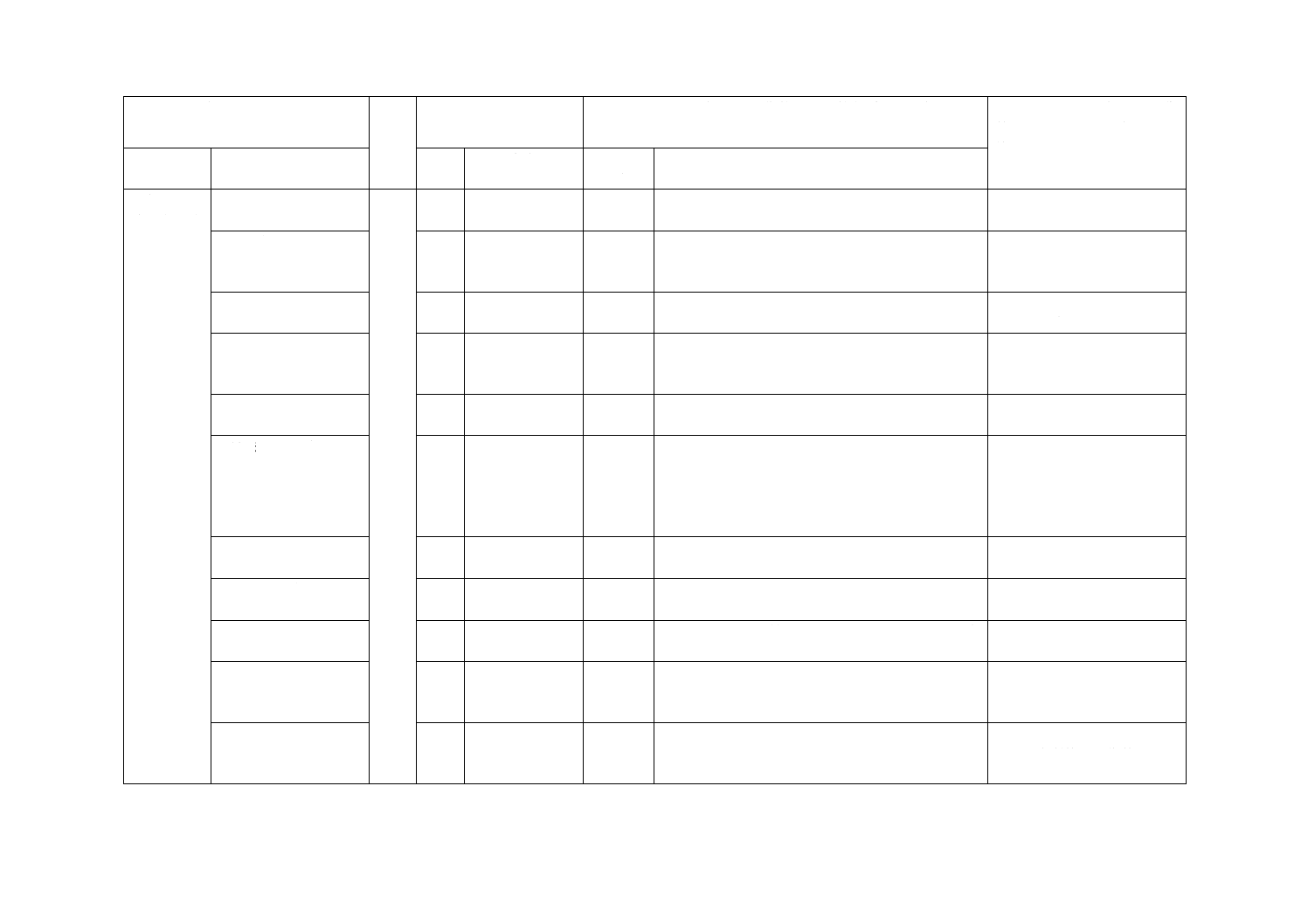
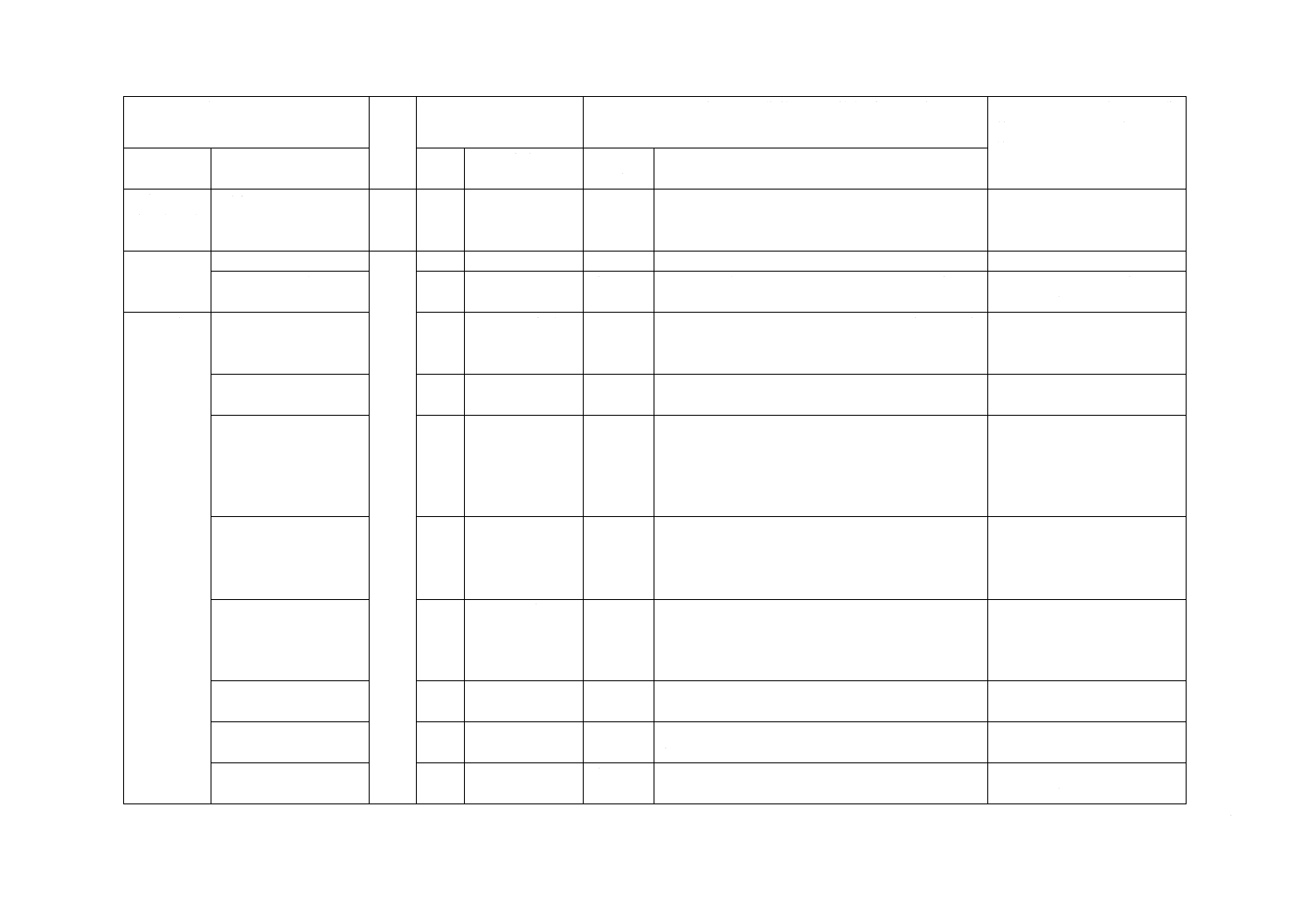
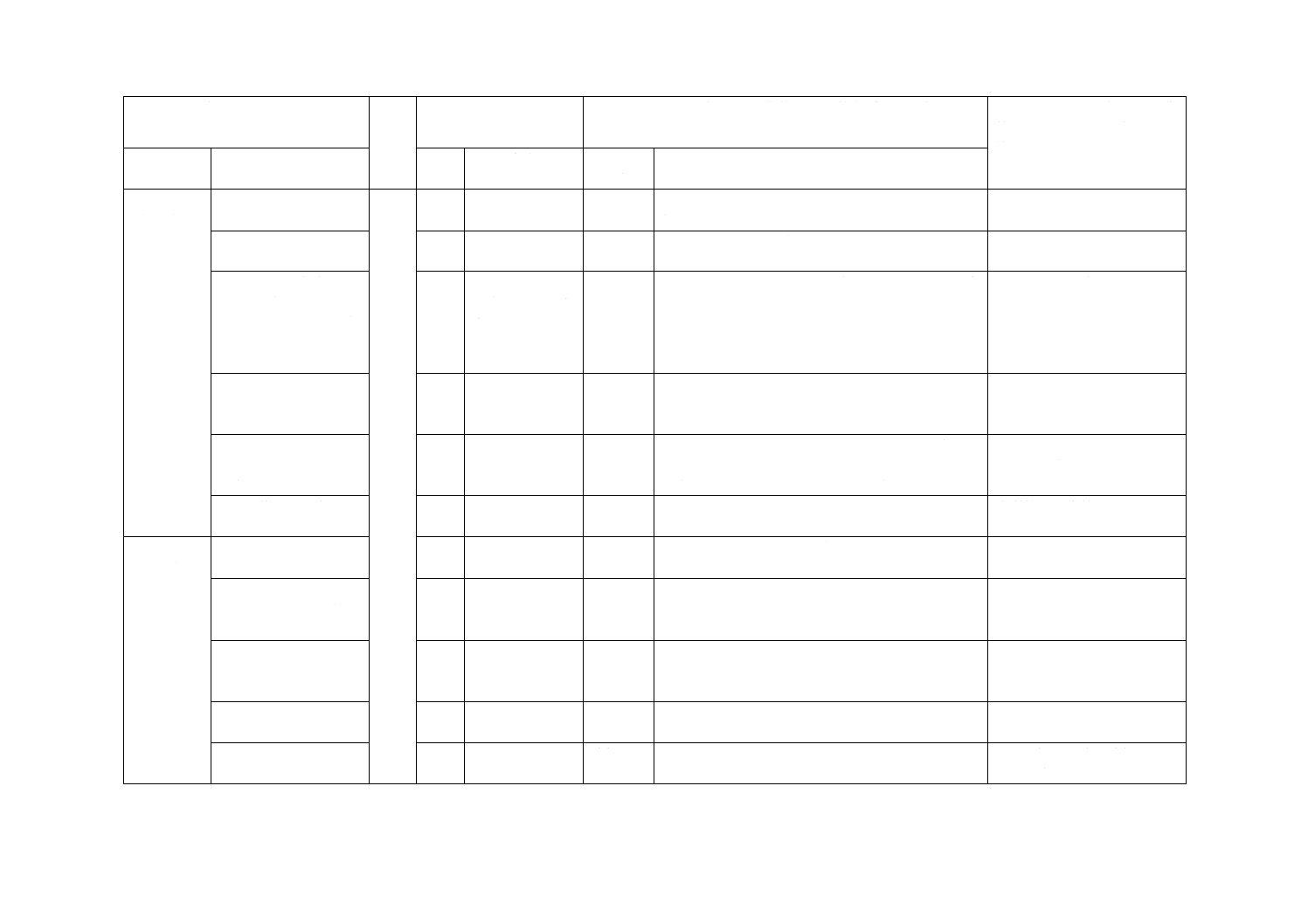
JISと対応国際規格との対比表
JIS R 1752:2020 ファインセラミックス−可視光応答形光触媒抗菌加工材料の
抗菌性試験方法及び抗菌効果
ISO 17094:2014,Fine ceramics (advanced ceramics, advanced technical ceramics)−Test
method for antibacterial activity of semiconducting photocatalytic materials under indoor
lighting environment
(I)JISの規定
(II)
国際
規格
番号
(III)国際規格の規定
(IV)JISと国際規格との技術的差異の箇条ごとの評価及びそ
の内容
(V)JISと国際規格との技術
的差異の理由及び今後の対
策
箇条番号
及び題名
内容
箇条
番号
内容
箇条ごと
の評価
技術的差異の内容
1 適用範囲 可視光応答形光触媒を
含有する加工材料及び
表面に光触媒加工フィ
ルムを含む材料の抗菌
性試験方法及び抗菌効
果を規定。
1
JISとほぼ同じ
変更
JISでは試験方法だけでなく抗菌効果も規定した。
また,ISO規格では繊維状の材料は適用外である
が,JISでは繊維状の材料の試験方法を追加し,繊
維状の材料も適用範囲に追加した。
適用外に抗ウイルス性,抗かび性を追加した。紫
外光応答形光触媒の抗菌性を試験する場合には
JIS R 1702を用いることを追加した。
ISO規格改正時に,適用外機
能の追加について提案を検
討する。
3 用語及び
定義
3.1
3.5
光触媒
抗菌
削除
JISでは,引用規格JIS R 1702,JIS Z 2801で定義
されているため削除した。
実質的な技術的な差異はな
い。
3.2 室内照明環境(可
視光)
3.3
JISとほぼ同じ
追加
JISでは,波長が380 nm以上780 nm未満の範囲の
光であることを追加した。
ISO規格改正時に,波長領域
の追加について提案を検討
する。
3.4 可視光応答形光触
媒抗菌加工
−
−
追加
光触媒の抗菌機能を利用するために,可視光応答
形光触媒で抗菌加工することを追加した。
規格使用者の理解のため,
JISに追加した。実質的な技
術的な差異はない。
3.5 可視光応答形単味
光触媒抗菌加工
−
−
追加
可視光応答形光触媒抗菌加工のうち,塗布,含浸,
練り込みなど種々の方法によって可視光応答形光
触媒を担持することを追加した。
規格使用者の理解のため,
JISに追加した。実質的な技
術的な差異はない。
3
R
1
7
5
2
:
2
0
2
0
23
R 1752:2020
(I)JISの規定
(II)
国際
規格
番号
(III)国際規格の規定
(IV)JISと国際規格との技術的差異の箇条ごとの評価及びそ
の内容
(V)JISと国際規格との技術
的差異の理由及び今後の対
策
箇条番号
及び題名
内容
箇条
番号
内容
箇条ごと
の評価
技術的差異の内容
3 用語及び
定義(続き)
3.6 可視光応答形ハイ
ブリッド光触媒抗菌加
工
−
−
追加
可視光応答形光触媒抗菌加工のうち,可視光が当
たらない環境においても抗菌機能を発現させるた
めに,可視光応答形光触媒と抗菌性のある他の機
能性物質とを組み合わせた材料を用いて,塗布,
含浸,練り込みなど種々の方法によって担持する
ことを追加した。
規格使用者の理解のため,
JISに追加した。実質的な技
術的な差異はない。
3.7 可視光応答形光触
媒抗菌加工材料
−
−
追加
可視光応答形光触媒抗菌加工した膜状,平板状,
繊維状などの材料であることを追加した。
規格使用者の理解のため,
JISに追加した。実質的な技
術的な差異はない。
3.8 フィルム密着法
−
−
追加
ISO規格の試験方法をフィルム密着法として,名
称を追加した。
ISO規格改正時に,改正提案
を検討する。
3.9 ガラス密着法
−
−
追加
繊維状の可視光応答形光触媒抗菌加工材料の試験
方法として,ガラス密着法を規定するために,従
来のISO規格試験をフィルム密着法とし,試験方
法を区別するために追加した。
ISO規格改正時に,改正提案
を検討する。
3.10 平板状の可視光
応答形光触媒抗菌加工
材料の抗菌活性値
3.6
可視光応答形光
触媒抗菌活性値
を規定
変更
ISO規格では,可視光応答形光触媒抗菌活性値と
しているが,JISでは可視光応答形光触媒抗菌加工
材料による抗菌活性値と変更した。ISO規格では,
生菌数の差としているが,対数値の差をみている
ので生菌数の対数値の差と変更した。
ISO規格改正時に,変更する
ことの提案を検討する。
3.11 繊維状の可視光
応答形光触媒抗菌加工
材料の抗菌活性値
−
−
追加
JISでは,ガラス密着法における可視光応答形光触
媒抗菌加工材料による抗菌活性値を追加した。
ISO規格改正時に,改正提案
を検討する。
3.12 平板状の可視光
応答形光触媒抗菌加工
材料の光照射による抗
菌活性値
3.7
可視光応答形光
触媒の光照射に
よる抗菌活性値
を規定
変更
ISO規格では,可視光応答形光触媒の光照射によ
る抗菌活性値としているが,JISでは可視光応答形
光触媒抗菌加工材料の光照射による抗菌活性値と
変更した。ISO規格では,生菌数の差としている
が,対数値の差をみているので生菌数の対数値の
差と変更した。
ISO規格改正時に,変更する
ことの提案を検討する。
3
R
1
7
5
2
:
2
0
2
0
24
R 1752:2020
(I)JISの規定
(II)
国際
規格
番号
(III)国際規格の規定
(IV)JISと国際規格との技術的差異の箇条ごとの評価及びそ
の内容
(V)JISと国際規格との技術
的差異の理由及び今後の対
策
箇条番号
及び題名
内容
箇条
番号
内容
箇条ごと
の評価
技術的差異の内容
3 用語及び
定義(続き)
3.13 繊維状の可視光
応答形光触媒抗菌加工
材料の光照射による抗
菌活性値
−
−
追加
JISでは,ガラス密着法における可視光応答形光触
媒抗菌加工材料による抗菌活性値を追加した。
ISO規格改正時に,改正提案
を検討する。
3.14 抗菌効果
−
−
追加
JISでは,抗菌活性値によって判定される可視光応
答形光触媒抗菌加工による効果であることを追加
した。
各国又は製品によって判定
基準は変わる可能性があり,
そのためJISには追加した。
4 記号及び
単位
4
フィルム密着法
の記号及び単位
だけ定義。
追加
ガラス密着法で使用する記号を追加した。(HD,
HF-L,MB A,MB D,MB F-L,MD,MF-L,SF-L,ΔS)
JISでは,F:試験で用いたシャープカットフィル
タの種類(A又はB)を追加した。それに伴い,
光照射を含む記号には添え字にフィルタの種類を
記載することを追加した。
ISO規格では,BD,BF-L,CF-L,CDには3個の試験
片の平均値との記載ないため,JISでは,3個の試
験片の平均値であることを追加した。記号Lmax,
Lmean,LminをLogmax,Logmean,Logminに変更した。
規格使用者が分かりやすく
するために記載・変更した。
ISO規格改正時に,ガラス密
着法に関わる追加部分を含
め,改正提案を検討する。
5 測定原理
5
フィルム密着法
の記載だけ定
義。
追加
JISでは,布又は織物は,材料の反りを避けるため
に,ガラス密着法を適用可能であること,その場
合には密着ガラスで細菌懸濁液を覆うことを追加
した。
得られた結果についての説明を追加した。
ISO規格改正時に,ガラス密
着法に関わる追加部分を含
む追加の改正提案を検討す
る。
6 材料
6.1 試験に用いる細菌
株及び試験の準備
6.1.1 フィルム密着法
に用いる細菌の種類
6.1.1
JISとほぼ同じ
変更
ISO規格の記載に変えて,JIS R 1702を引用する
よう変更した。
実質的な技術的差異はない。
6.1.2 ガラス密着法に
用いる細菌の種類
−
−
追加
ガラス密着法に用いる細菌の種類を追加し,JIS R
1702を引用するよう追加した。
ISO規格の改正時に,改正提
案を検討する。
6.1.3 細菌株の準備
6.1.2
JISとほぼ同じ
変更
ISO規格の記載に変えて,JIS R 1702を引用する
よう変更した。
実質的な技術的差異はない。
3
R
1
7
5
2
:
2
0
2
0
25
R 1752:2020
(I)JISの規定
(II)
国際
規格
番号
(III)国際規格の規定
(IV)JISと国際規格との技術的差異の箇条ごとの評価及びそ
の内容
(V)JISと国際規格との技術
的差異の理由及び今後の対
策
箇条番号
及び題名
内容
箇条
番号
内容
箇条ごと
の評価
技術的差異の内容
6 材料
(続き)
6.1.4 細菌株の保存
6.1.2
JISとほぼ同じ
変更
ISO規格の記載に変えて,JIS R 1702を引用する
よう変更した。
実質的な技術的差異はない。
6.2 試薬及び材料
6.2.1 SCDLP培地
6.2.4
JISとほぼ同じ
変更
ISO規格の記載に変えて,JIS Z 2801を引用する
よう変更した。
実質的な技術的差異はない。
6.2.2 生理食塩水
6.2.5
JISとほぼ同じ
変更
ISO規格の記載に変えて,生理食塩水の調製方法
は,JIS L 1902を引用するよう変更した。また,調
製後に直ちに使用しないものは5 ℃〜10 ℃の温
度で保存することを追加した。
実質的な技術的差異はない。
6.2.3 洗い出し用生理
食塩水
−
−
追加
JISでは,調製方法はJIS L 1902を引用すること,
調製後,直ちに使用しないものは5 ℃〜10 ℃の温
度で保存することを追加した。
実質的な技術的差異はない。
6.2.4 エタノール
−
−
追加
引用しているJISと試薬の説明を追加した。
ISO規格の試験で使用されて
おり,実質的な技術的な差異
はない。
6.2.5 非イオン界面活
性剤
−
−
追加
引用しているJISと試薬の説明を追加した。
ISO規格の試験で使用されて
おり,実質的な技術的な差異
はない。
6.2.6 綿標準布
−
−
追加
ガラス密着法で使用する綿標準布を規定し,JIS L
0803を引用するよう追加した。
ISO規格改正時に,改正提案
を検討する。
6.3 殺菌方法
−
−
追加
JIS Z 2801を引用するよう追加した。
規格使用者が分かりやすく
するために記載した。ISO規
格の試験では通常使われる
方法であり,技術的差異はな
い。
7 装置及び
機器
7.1 試験装置
7.1
JISとほぼ同じ
追加
JISでは,試験装置として光照射装置を追加した。 ISO規格改正時に,光照射装
置の追加について提案を検
討する。
7.2 密着フィルム
7.2
JISとほぼ同じ
変更
ISO規格の記載に変えて,JIS R 1702を引用する
よう変更した。
実質的な技術的差異はない。
7.3 密着ガラス
−
−
追加
ガラス密着法で使用する密着ガラスを規定し,JIS
R 1702を引用するよう変更した。
ISO規格改正時に,追加部分
の改正提案を検討する。
3
R
1
7
5
2
:
2
0
2
0
26
R 1752:2020
(I)JISの規定
(II)
国際
規格
番号
(III)国際規格の規定
(IV)JISと国際規格との技術的差異の箇条ごとの評価及びそ
の内容
(V)JISと国際規格との技術
的差異の理由及び今後の対
策
箇条番号
及び題名
内容
箇条
番号
内容
箇条ごと
の評価
技術的差異の内容
7 装置及び
機器(続き)
7.4 保湿用ガラス
7.3
JISとほぼ同じ
変更
ISO規格の記載に変えて,JIS R 1702を引用する
よう変更した。
実質的な技術的差異はない。
7.5 保存シャーレ
−
−
追加
試験片を設置するシャーレについてJIS K 0950を
引用するよう追加した。
ISO規格の試験で使用されて
おり,実質的な技術的な差異
はない。
7.6 調湿用ろ紙
−
−
追加
調湿用ろ紙について規格を引用して追加した。
ISO規格改正時に,追加部分
の改正提案を検討する。
7.7 ガラス管・ガラス
棒
7.4
JISとほぼ同じ
変更
JISでは,JIS R 3644又はJIS R 3645を引用するよ
う変更し,加えて長さと形状に関する規定を変更
した。
実質的な技術的差異はない。
7.9 光照射装置
−
−
追加
JISでは,JIS R 1702を引用するよう規定した。
ISO規格改正時に,追加部分
の改正提案を検討する。
7.10 シャープカット
フィルタ
7.6
追加
JISでは,製品が使用される状況を想定して,使用
するフィルタを選択すること,及びシャープカッ
トフィルタを用いずに試験する場合は,7.10 a)又は
7.10 b)の条件と組み合わせて試験しなければなら
ないことを追加した。
実質的な技術的差異はない。
7.11 照度計
7.7
ISO 14605で規
定。
変更
ISO規格の記述に変えて,JIS C 1609-1を引用する
よう変更した。
実質的な技術的差異はない。
7.12 紫外放射照度計
−
−
追加
JIS R 1709を引用するよう追加した。また,計測
下限値を規定した。
実質的な技術的差異はない。
7.13 暗箱
−
−
追加
JISでは,暗所保管用の箱を規定し,容器内の照度
に関する規定を追加した。
ISO規格改正時に,追加部分
の改正提案を検討する。
7.14 シャーレ
−
−
追加
JIS K 0950を引用するよう追加した。
ISO規格の試験で使用されて
おり,実質的な技術的な差異
はない。
7.15 安全キャビネッ
ト
−
−
追加
JIS K 3800を引用するよう追加した。
ISO規格の試験で使用されて
おり,実質的な技術的な差異
はない。
3
R
1
7
5
2
:
2
0
2
0
27
R 1752:2020
(I)JISの規定
(II)
国際
規格
番号
(III)国際規格の規定
(IV)JISと国際規格との技術的差異の箇条ごとの評価及びそ
の内容
(V)JISと国際規格との技術
的差異の理由及び今後の対
策
箇条番号
及び題名
内容
箇条
番号
内容
箇条ごと
の評価
技術的差異の内容
7 装置及び
機器(続き)
7.16 ピペット
−
−
追加
JIS K 0970又はJIS R 3505を引用するよう追加し
た。
ISO規格の試験で使用されて
おり,実質的な技術的な差異
はない。
8 試験片
8.1 フィルム密着法
8.1
JISとほぼ同じ
変更
試験片についての注記をJISでは本文に記載した。 実質的な技術的差異はない。
8.2 ガラス密着法
−
−
追加
ガラス密着法で使用する試験片について追加し
た。
ISO規格改正時に,追加部分
の改正提案を検討する。
9 試験方法 9.1 一般事項
9.1
フィルム密着法
のフローチャー
トを規定。
変更
追加
JISでは,光の当たらない場所での試験方法を規定
しているため,フローチャートを変更した。ガラ
ス密着法のフローチャートを図3として追加した。
ISO規格改正時に,追加部分
の改正提案を検討する。
9.2 フィルム密着法
9.2.1 試験菌液の調製
9.2.1
JISとほぼ同じ
変更
ISO規格の記載に変えて,JIS R 1702を引用する
よう変更した。
実質的な技術的差異はない。
9.2.2 試験片の設置
9.2.2
JISとほぼ同じ
追加
JISでは,試験面の規定及び高圧蒸気殺菌によって
ろ紙が湿った場合の対応を追加した。図を追加し,
試験片の設置について説明を追加した。
滅菌水量についての注記をJISでは本文に記載し
た。
ISO規格改正時に,追加部分
の改正提案を検討する。
9.2.3 試験菌液の接種
9.2.2
9.2.3
JISとほぼ同じ
追加
JISでは,標準の大きさ以外の試験片の接種菌液量
について規定した。
試験菌液量についての注記をJISでは本文に記載
した。
実質的な技術的差異はない。
9.2.4 試験菌の洗い出
し
9.2.3
9.3.6
JISとほぼ同じ
追加
JISでは,同様の結果が得られる場合は,ストマッ
カー袋に代わるものを用いてもよいことを追加し
た。また,洗い出し液を速やかに測定に用いるこ
とを追記した。
ISO規格改正時に,追加部分
の改正提案を検討する。
9.3 ガラス密着法
9.3.1 試験菌の培養
−
−
追加
JISでは,ガラス密着法の試験菌の培養を規定し,
JIS R 1702を引用するよう追加した。
ISO規格改正時に,追加部分
の改正提案を検討する。
9.3.2 試験菌液の調製
−
−
追加
JISでは,ガラス密着法の試験菌液の調製を規定
し,JIS R 1702を引用するよう追加した。
ISO規格改正時に,追加部分
の改正提案を検討する。
9.3.3 試験片の設置
−
−
追加
JISでは,ガラス密着法の試験片の設置方法を追加
した。
ISO規格改正時に,追加部分
の改正提案を検討する。
3
R
1
7
5
2
:
2
0
2
0
28
R 1752:2020
(I)JISの規定
(II)
国際
規格
番号
(III)国際規格の規定
(IV)JISと国際規格との技術的差異の箇条ごとの評価及びそ
の内容
(V)JISと国際規格との技術
的差異の理由及び今後の対
策
箇条番号
及び題名
内容
箇条
番号
内容
箇条ごと
の評価
技術的差異の内容
9 試験方法
(続き)
9.3.4 試験菌液の接種
−
−
追加
JISでは,ガラス密着法の試験菌液の接種方法を追
加した。
ISO規格改正時に,追加部分
の改正提案を検討する。
9.3.5 試験菌の洗い出
し
−
−
追加
JISでは,ガラス密着法の試験菌の洗い出し方法を
追加した。
ISO規格改正時に,追加部分
の改正提案を検討する。
9.4 可視光照射条件
9.4.1 照度の測定,試験
片設置位置及び光照射
条件
9.3.1
9.3.2
9.3.3
9.3.4
試験片表面での
照度は1 000 lx
±50 lxと規定
変更
追加
JISでは,試験片表面での照度を500 lx±25 lxに変
更した。
JISでは,蛍光ランプを安定化させるため,30分
以上の予備点灯を追加した。
照度に関する注記をJISでは本文に記載した。
国内の運用に合わせた。ISO
規格改正時に,変更部分の改
正提案を検討する。
9.4.2 試験菌液を接種
した試験片の光照射
9.3.1
試験片周辺温度
を25 ℃±5 ℃
と規定
変更
JISでは,試験片周辺温度を25 ℃±3 ℃に変更し
た。
照射に関する注記をJISでは本文に記載した。
ISO規格改正時に,変更部分
の改正提案を検討する。
9.4.3 試験菌液を接種
した試験片の暗所での
保存
9.3.1
試験片周辺温度
を25 ℃±5 ℃
と規定
変更
JISでは,試験片周辺温度を25 ℃±3 ℃に変更し
た。
保存シャーレの蓋に関する記載を追加した。
ISO規格改正時に,変更部分
の改正提案を検討する。
9.5 生菌数の測定
9.4
JISとほぼ同じ
変更
ISO規格の記載に変えて,JIS R 1702を引用する
よう変更した。
実質的な技術的差異はない。
10 試験結
果の計算
10.1 一般事項
10.1
JISとほぼ同じ
追加
JISでは,抗菌活性値の計算時及び報告書に記載す
る平均値の取扱いについて追加した。
実質的な技術的差異はない。
10.2 フィルム密着法
10.2.1 生菌数の計算
10.2
JISとほぼ同じ
追加
JISでは,洗い出し液1 mlを用いたシャーレから
生残菌が認められない場合,<10と表示すること
を追加した。
実質的な技術的差異はない。
10.2.2 試験結果の計算
10.2
10.3
JISとほぼ同じ
変更
JISでは,記号及び記号の添え字を変更した
(Logmax,Logmean,Logmin,RF-L,BF-L,CF-L)。
規格使用者が分かりやすく
するために変更した。実質的
な技術的な差異はない。
10.3 ガラス密着法
10.3.1 生菌数の計算
−
−
追加
JISでは,ガラス密着法の生菌数の計算方法を規定
し追加した。
ISO規格改正時に,追加部分
の改正提案を検討する。
10.3.2 試験結果の計算
−
−
追加
JISでは,ガラス密着法の試験結果の計算方法を追
加した。
ISO規格改正時に追加部分の
改正提案を検討する。
3
R
1
7
5
2
:
2
0
2
0
29
R 1752:2020
(I)JISの規定
(II)
国際
規格
番号
(III)国際規格の規定
(IV)JISと国際規格との技術的差異の箇条ごとの評価及びそ
の内容
(V)JISと国際規格との技術
的差異の理由及び今後の対
策
箇条番号
及び題名
内容
箇条
番号
内容
箇条ごと
の評価
技術的差異の内容
11 抗菌効
果の判定
a) 光照射条件下での
フィルム密着法による
判定
−
−
追加
平板状の可視光応答形光触媒抗菌加工材料の抗菌
活性値が2.0以上で抗菌効果があると判定するこ
とを追加とした。
JISとして規定した。
各国又は製品によって判定
基準は変わる可能性があり,
そのためJISには追加した。
b) 光が当たらない環
境でのフィルム密着法
による判定
−
−
追加
附属書JAによって算出した抗菌活性値が2.0以上
で抗菌効果があると判定することを追加とした。
JISとして規定した。
各国又は製品によって判定
基準は変わる可能性があり,
そのためJISには追加した。
c) 光照射条件下での
ガラス密着法による判
定
−
−
追加
繊維状の可視光応答形光触媒抗菌加工材料の抗菌
活性値が2.0以上で抗菌効果があると判定するこ
とを追加とした。
ISO規格の改正時に,改正提
案を検討する。
d) 光が当たらない環
境でのガラス密着法に
よる判定
−
−
追加
JIS L 1902の8.1.5.2によって算出した抗菌活性値
が2.0以上で抗菌効果があると判定することを追
加とした。
ISO規格の改正時に,改正提
案を検討する。
12 試験結
果の報告
11
JISとほぼ同じ
追加
JISでは,項目の構成を変更した。可視光応答形ハ
イブリッド光触媒抗菌加工した試験片を用いて附
属書JAの試験を実施した場合の記載について追
加した。また,ガラス密着法の場合の必要事項を
追加した。加えて,その他の必要事項及び結果の
表示例を追記した。
ISO規格改正時に,追加部分
の改正提案を検討する。
3
R
1
7
5
2
:
2
0
2
0
30
R 1752:2020
(I)JISの規定
(II)
国際
規格
番号
(III)国際規格の規定
(IV)JISと国際規格との技術的差異の箇条ごとの評価及びそ
の内容
(V)JISと国際規格との技術
的差異の理由及び今後の対
策
箇条番号
及び題名
内容
箇条
番号
内容
箇条ごと
の評価
技術的差異の内容
附属書JA
(規定)
平板状の可
視光応答形
ハイブリッ
ド光触媒抗
菌加工材料
の光が当た
らない環境
での抗菌性
試験方法及
び抗菌効果
−
−
追加
平板状の可視光応答形ハイブリッド光触媒抗菌加
工材料の光が当たらない環境での抗菌性試験方法
及び抗菌効果の詳細を追記した。
国内での製品認証に必要な
項目のため追加した。
JISと国際規格との対応の程度の全体評価:ISO 17094:2014,MOD
注記1 箇条ごとの評価欄の用語の意味は,次による。
− 削除 ················ 国際規格の規定項目又は規定内容を削除している。
− 追加 ················ 国際規格にない規定項目又は規定内容を追加している。
− 変更 ················ 国際規格の規定内容を変更している。
注記2 JISと国際規格との対応の程度の全体評価欄の記号の意味は,次による。
− MOD ··············· 国際規格を修正している。
3
R
1
7
5
2
:
2
0
2
0