25
Q 17025:2018 (ISO/IEC 17025:2017)
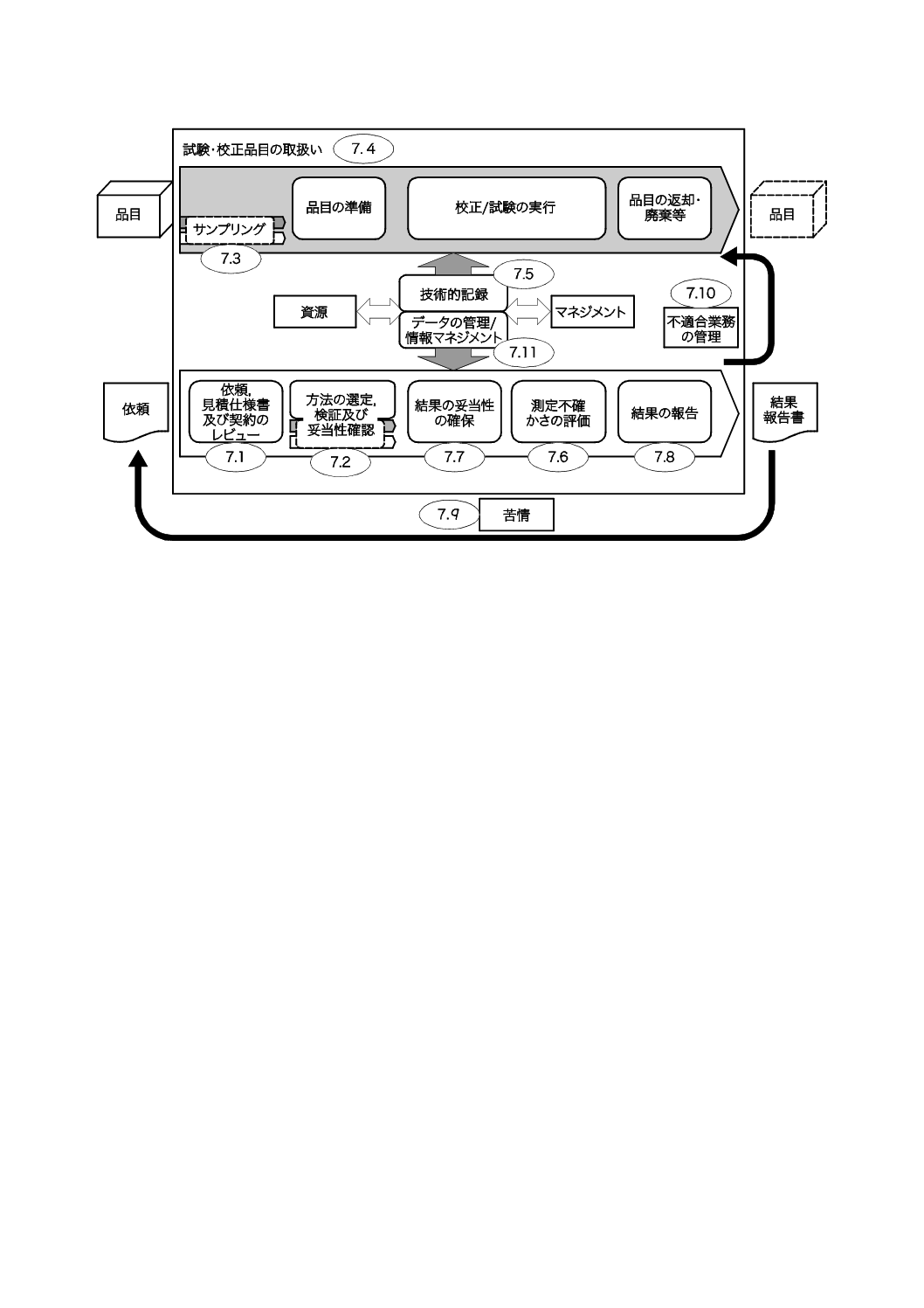
図B.1−ラボラトリの運用プロセスの図解
Q 17025:2018 (ISO/IEC 17025:2017)
(1)
目 次
ページ
序文 ··································································································································· 1
1 適用範囲························································································································· 1
2 引用規格························································································································· 1
3 用語及び定義 ··················································································································· 2
4 一般要求事項 ··················································································································· 3
4.1 公平性 ························································································································· 3
4.2 機密保持 ······················································································································ 4
5 組織構成に関する要求事項 ································································································· 4
6 資源に関する要求事項 ······································································································· 5
6.1 一般 ···························································································································· 5
6.2 要員 ···························································································································· 5
6.3 施設及び環境条件 ·········································································································· 5
6.4 設備 ···························································································································· 6
6.5 計量トレーサビリティ ···································································································· 7
6.6 外部から提供される製品及びサービス················································································ 8
7 プロセスに関する要求事項 ································································································· 8
7.1 依頼,見積仕様書及び契約のレビュー················································································ 8
7.2 方法の選定,検証及び妥当性確認······················································································ 9
7.3 サンプリング ··············································································································· 11
7.4 試験・校正品目の取扱い ································································································ 11
7.5 技術的記録 ·················································································································· 12
7.6 測定不確かさの評価 ······································································································ 12
7.7 結果の妥当性の確保 ······································································································ 13
7.8 結果の報告 ·················································································································· 13
7.9 苦情 ··························································································································· 16
7.10 不適合業務 ················································································································· 17
7.11 データの管理及び情報マネジメント ················································································ 17
8 マネジメントシステムに関する要求事項 ·············································································· 18
8.1 選択肢 ························································································································ 18
8.2 マネジメントシステムの文書化(選択肢A) ······································································ 18
8.3 マネジメントシステム文書の管理(選択肢A) ··································································· 19
8.4 記録の管理(選択肢A)································································································· 19
8.5 リスク及び機会への取組み(選択肢A) ············································································ 19
8.6 改善(選択肢A) ········································································································· 20
8.7 是正処置(選択肢A)···································································································· 20
Q 17025:2018 (ISO/IEC 17025:2017) 目次
(2)
ページ
8.8 内部監査(選択肢A)···································································································· 20
8.9 マネジメントレビュー(選択肢A) ·················································································· 21
附属書A(参考)計量トレーサビリティ ·················································································· 22
附属書B(参考)マネジメントシステムに関する選択肢 ······························································ 24
参考文献 ···························································································································· 26
Q 17025:2018 (ISO/IEC 17025:2017)
(3)
まえがき
この規格は,工業標準化法に基づき,日本工業標準調査会の審議を経て,経済産業大臣が改正した日本
工業規格である。
これによって,JIS Q 17025:2005は改正され,この規格に置き換えられた。
この規格は,著作権法で保護対象となっている著作物である。
この規格の一部が,特許権,出願公開後の特許出願又は実用新案権に抵触する可能性があることに注意
を喚起する。経済産業大臣及び日本工業標準調査会は,このような特許権,出願公開後の特許出願及び実
用新案権に関わる確認について,責任はもたない。
日本工業規格 JIS
Q 17025:2018
(ISO/IEC 17025:2017)
試験所及び校正機関の能力に関する一般要求事項
General requirements for the competence of testing and
calibration laboratories
序文
この規格は,2017年に第3版として発行されたISO/IEC 17025を基に,技術的内容及び構成を変更する
ことなく作成した日本工業規格である。
なお,この規格で点線の下線を施してある参考事項は,対応国際規格にはない事項である。
この規格は,ラボラトリの運営の信頼性を高めるという目的をもって作成された。
この規格は,ラボラトリが適格な運営を行い,かつ,妥当な結果を出す能力があることを実証できるよ
うにするための要求事項を含んでいる。
この規格に適合するラボラトリは,一般にJIS Q 9001の原則にも従った運営をすることになる。
この規格は,リスク及び機会に取り組むための処置を計画し,実施することをラボラトリに要求してい
る。リスク及び機会の双方に取り組むことによって,マネジメントシステムの有効性の向上,改善された
結果の達成及び好ましくない影響の防止のための基礎が確立される。ラボラトリは,どのリスク及び機会
に取り組む必要があるかを決定する責任をもつ。
この規格の使用は,ラボラトリとその他の機関との間の協力を容易にし,情報及び経験の交換並びに規
格及び手順の整合化を支援するであろう。ラボラトリがこの規格に適合している場合には,国家間での結
果の受入れが容易になる。
1
適用範囲
この規格は,ラボラトリの能力,公平性及び一貫した運営に関する一般要求事項を規定する。
この規格は,要員の数に関係なく,ラボラトリ活動を行う全ての組織に適用できる。
ラボラトリの顧客,規制当局,相互評価を使用する組織及びスキーム並びに認定機関及びその他の組織
が,ラボラトリの能力を確認又は承認するに当たってこの規格を使用する。
注記 この規格の対応国際規格及びその対応の程度を表す記号を,次に示す。
ISO/IEC 17025:2017,General requirements for the competence of testing and calibration laboratories
(IDT)
なお,対応の程度を表す記号“IDT”は,ISO/IEC Guide 21-1に基づき,“一致している”こ
とを示す。
2
引用規格
次に掲げる規格は,この規格に引用されることによって,この規格の規定の一部を構成する。これらの
引用規格は,その最新版(追補を含む。)を適用する。
2
Q 17025:2018 (ISO/IEC 17025:2017)
JIS Q 17000 適合性評価−用語及び一般原則
注記 対応国際規格:ISO/IEC 17000,Conformity assessment−Vocabulary and general principles(IDT)
ISO/IEC Guide 99,International vocabulary of metrology−Basic and general concepts and associated terms
(VIM) 1)
注1) JCGM 200としても知られている。
3
用語及び定義
この規格で用いる主な用語及び定義は,ISO/IEC Guide 99及びJIS Q 17000によるほか,次による。
3.1
公平性(impartiality)
客観性があること。
注記1 客観性とは,利害抵触がないか,又はラボラトリの事後の活動に悪影響を及ぼすことがない
よう,利害抵触が解決されていることを意味する。
注記2 公平性の要素を伝えるのに有用なその他の用語には,利害抵触がないこと,偏見がないこと,
先入観がないこと,中立,公正,心が広いこと,公明正大,利害との分離,及び均衡が含ま
れる。
(出典:JIS Q 17021-1:2015,3.2の注記1にある“認証機関”を“ラボラトリ”に置き換え及び“独立
性”を注記2から削除した。)
3.2
苦情(complaint)
ラボラトリの活動又は結果に関し,人又は組織が回答を期待して行う当該ラボラトリへの不満の表明。
(出典:JIS Q 17000:2005の6.5を修正。“適合性評価機関又は認定機関”を“ラボラトリ”に置き換え
た。また,“結果”を追加し,“異議申立て”を削除した。)
3.3
試験所間比較(interlaboratory comparison)
事前に定めた条件に従って,二つ以上のラボラトリが,同一品目又は類似品目で行う,測定又は試験の
企画,実施及び評価。
(出典:JIS Q 17043:2011の3.4)
3.4
試験所内比較(intralaboratory comparison)
事前に定めた条件に従って,同一のラボラトリ内で,同一品目又は類似品目で行う,測定又は試験の企
画,実施及び評価。
3.5
技能試験(proficiency testing)
試験所間比較による,事前に決めた基準に照らしての参加者のパフォーマンスの評価。
(出典:JIS Q 17043:2011の3.7を修正。注記を削除した。)
3.6
ラボラトリ(laboratory)
次の一つ以上の活動を実行する機関。
− 試験
3
Q 17025:2018 (ISO/IEC 17025:2017)
− 校正
− 後の試験又は校正に付随するサンプリング
注記 現在の規格の枠組みにおいて,“ラボラトリ活動”という用語は,上記三つの活動のことをいう。
3.7
判定ルール(decision rule)
特定の要求事項への適合性を表明する際に,測定不確かさをどのように考慮するかを記述した取決め。
3.8
検証(verification)
与えられたアイテムが規定された要求事項を満たしているという客観的証拠の提示。
例1 対象とする任意の標準物質が,当該の量の値及び測定手順に対して,質量10 mgの測定試料ま
で均質であることの確認。
例2 測定システムが性能特性又は法的要求事項を満たしていることの確認。
例3 目標測定不確かさを満たすことができることの確認。
注記1 適用可能な場合は,測定不確かさを考慮することが望ましい。
注記2 アイテムとは,例えば,プロセス,測定手順,材料,化合物又は測定システムのいずれであ
ってもよい。
注記3 規定された要求事項とは,例えば,製造業者の仕様を満たしていることである。
注記4 VIML及び一般に適合性評価で定義しているように,法定計量でいう検証は,評価及び表示,
及び/又は測定システムに対する検定証明書の発行を含む。
注記5 検証と校正とを混同しないようにすることが望ましい。全ての検証が妥当性確認であるとは
限らない。
注記6 化学の分野では,関連する実在物又は活性の同一性の検証には,その実在物若しくは活性の
構造又は性質の記述が必要となる。
(出典:ISO/IEC Guide 99の2.44)
3.9
妥当性確認(validation)
規定された要求事項が意図した用途に十分であることの検証。
例 水中の窒素の質量濃度の測定に通常用いる測定手順は,ヒトの血清中の窒素の質量濃度の測定に
対しても妥当である場合がある。
(出典:ISO/IEC Guide 99の2.45)
4
一般要求事項
4.1
公平性
4.1.1
ラボラトリ活動は,公平に実行され,公平性を確保するように編成及び運営されなければならない。
4.1.2
ラボラトリマネジメントは,公平性を確約しなければならない。
4.1.3
ラボラトリは,ラボラトリ活動の公平性に対して責任をもたなければならず,公平性を損なう商業
的,財務的,又はその他の圧力を容認してはならない。
4.1.4
ラボラトリは,公平性に対するリスクを継続的に特定しなければならない。ラボラトリの活動若し
くは他との関係,又はその要員の他との関係をもつことから生じるリスクもこれに含めなければならない。
ただし,そのような関係が,ラボラトリにとって必ずしも公平性に対するリスクになるとは限らない。
4
Q 17025:2018 (ISO/IEC 17025:2017)
注記 ラボラトリの公平性に対する脅威となる関係としては,所有,統治,マネジメント,要員,共
有資源,財務,契約,マーケティング(ブランド設定を含む。),及び新規顧客の紹介に関わる
売上手数料の支払い又はその他の誘引条件に基づくものが挙げられる。
4.1.5
公平性に対するリスクが特定された場合,ラボラトリは,そのリスクをどのように排除又は最小化
するかを実証できなければならない。
4.2
機密保持
4.2.1
ラボラトリは,法的に強制力のあるコミットメントによって,ラボラトリ活動を実行する過程で得
られた又は作成された全ての情報の管理について責任をもたなければならない。ラボラトリは,公開対象
にしようとしている情報を,事前に顧客に通知しなければならない。顧客が公開している情報,又はラボ
ラトリと顧客とが合意している場合(例えば,苦情への対応の目的のため)を除き,その他全ての情報は
占有情報とみなし,機密としなければならない。
4.2.2
ラボラトリが機密情報を公開することを,法律で要求されるか又は契約上の取決めで認められた場
合,顧客又は関係する個人は,法律によって禁止されない限り,当該情報の提供について知らされなけれ
ばならない。
4.2.3
当該顧客以外の情報源(例えば,苦情申立者,規制当局)から得られた顧客に関する情報は,顧客
とラボラトリとの間で機密としなければならない。この情報の提供者(情報源)は,ラボラトリの機密と
し,情報源が同意した場合を除き,顧客と共有してはならない。
4.2.4
委員会のメンバー,契約人,外部機関の要員又はラボラトリの代理人として活動する個人は,法律
で要求される場合を除き,ラボラトリ活動を遂行する間に得られた,又は生じた全ての情報について機密
保持しなければならない。
5
組織構成に関する要求事項
5.1
ラボラトリは,そのラボラトリ活動に法的責任をもつ法人であるか,又は法人の一部として明確に
位置付けられていなければならない。
注記 この規格の目的において,政府のラボラトリは,政府機関としての地位に基づき法人とみなす。
5.2
ラボラトリは,そのラボラトリについて総合的な責任をもつラボラトリマネジメントを特定しなけ
ればならない。
5.3
ラボラトリは,この規格に適合するラボラトリ活動の範囲を明確化し,文書化しなければならない。
ラボラトリは,継続的に外部から提供されるラボラトリ活動を除いた当該ラボラトリ活動の範囲に関して
だけ,この規格への適合を主張しなければならない。
5.4
ラボラトリ活動は,この規格,ラボラトリの顧客,規制当局及び認可を与える機関の要求事項を満
足するように実施されなければならない。このことには,その全ての恒久的施設で実施されるラボラトリ
活動,その恒久的施設から離れた場所で実施されるラボラトリ活動,関連する一時施設若しくは移動施設
で実施されるラボラトリ活動,又は顧客の施設で実施されるラボラトリ活動が含まれなければならない。
5.5
ラボラトリは,次の事項を行わなければならない。
a) ラボラトリの組織及び管理構造,親組織における位置付け,並びに管理,技術的業務及び支援サービ
スの間の関係を明確にする。
b) ラボラトリ活動の結果に影響する業務を管理,実施又は検証する全ての要員の責任,権限及び相互関
係を規定する。
c) ラボラトリ活動の一貫した適用及び結果の妥当性を確実にするために必要な程度まで手順を文書化す
5
Q 17025:2018 (ISO/IEC 17025:2017)
る。
5.6
ラボラトリは,他の責任のいかんにかかわらず,次の事項を含む責務を果たすために必要な権限及
び資源をもつ要員をもたなければならない。
a) マネジメントシステムの実施,維持及び改善
b) マネジメントシステムからの逸脱,又はラボラトリ活動の実施手順からの逸脱の特定
c) それらの逸脱を防止又は最小化する処置の開始
d) マネジメントシステムの実施状況及び改善の必要性に関するラボラトリマネジメントへの報告
e) ラボラトリ活動の有効性の確保
5.7
ラボラトリマネジメントは,次の事項を確実にしなければならない。
a) コミュニケーションが,マネジメントシステムの有効性,並びに顧客要求事項及びその他の要求事項
を満たすことの重要性に関して行われている。
b) マネジメントシステムに対する変更が計画され実施された場合,マネジメントシステムの“全体とし
て整っている状態”(integrity)が維持されている。
6
資源に関する要求事項
6.1
一般
ラボラトリは,ラボラトリ活動の管理及び実施に必要な要員,施設,設備,システム及び支援サービス
を利用できるようにしなければならない。
6.2
要員
6.2.1
ラボラトリ活動に影響を与え得る,ラボラトリの内部又は外部の全ての要員は,公平に行動し,力
量をもち,ラボラトリのマネジメントシステムに従って業務を行わなければならない。
6.2.2
ラボラトリは,学歴,資格,教育・訓練,技術的知識,技能及び経験に関する要求事項を含め,ラ
ボラトリ活動の結果に影響を与える各職務に関する力量要求事項を文書化しなければならない。
6.2.3
ラボラトリは,その要員が,責任をもつラボラトリ活動を実施し,かつ,逸脱の重大性を評価する
力量をもつことを確実にしなければならない。
6.2.4
ラボラトリの管理要員は,要員に責務,責任及び権限を伝達しなければならない。
6.2.5
ラボラトリは,次の事項に関する手順をもち,記録を保持しなければならない。
a) 力量要求事項の決定
b) 要員の選定
c) 要員の教育・訓練
d) 要員の監督
e) 要員への権限付与
f)
要員の力量の監視
6.2.6
ラボラトリは,特定のラボラトリ活動(次を含むが,これらに限定されない)を実施する権限を,
要員に与えなければならない。
a) 方法の開発,変更,検証及び妥当性確認
b) 適合性の表明又は意見及び解釈を含めた結果の分析
c) 結果の報告,レビュー及び承認
6.3
施設及び環境条件
6.3.1
施設及び環境条件は,ラボラトリ活動に適するものでなければならない。また,結果の妥当性に悪
6
Q 17025:2018 (ISO/IEC 17025:2017)
影響を及ぼしてはならない。
注記 結果の妥当性に悪影響を及ぼし得る影響には,微生物学的汚染,ほこり,電磁障害,放射線,
湿度,電力供給,温度,騒音及び振動が含まれるが,これらに限定されない。
6.3.2
ラボラトリ活動の実施に必要な施設及び環境条件に関する要求事項を文書化しなければならない。
6.3.3
ラボラトリは,該当する仕様書,方法若しくは手順書に従い,又は環境条件が結果の妥当性に影響
を及ぼす場合には,環境条件を監視し,制御し記録しなければならない。
6.3.4
施設を管理するための手段を実施し,監視し,定期的に見直さなければならない。これらの手段に
は,次の事項が含まれなければならないが,これらに限定されない。
a) ラボラトリ活動に影響を及ぼす区域への立入り及びこれらの区域の使用
b) 汚染,干渉又はラボラトリ活動への悪影響の防止
c) 両立不可能なラボラトリ活動が行われる区域間の効果的な分離
6.3.5
ラボラトリが自身の恒久的な管理下にない場所又は施設でラボラトリ活動を実施する場合は,この
規格の施設及び環境条件に関する要求事項が満たされることを確実にしなければならない。
6.4
設備
6.4.1
ラボラトリは,ラボラトリ活動の適正な実施に必要で,かつ,結果に影響を与え得る設備(これに
は測定装置,ソフトウェア,測定標準,標準物質,参照データ,試薬及び消耗品又は補助的器具を含むが,
これらに限定されない)が利用可能でなければならない。
注記1 標準物質及び認証標準物質(CRM)には,参照標準,校正用標準物質,参照標準物質(SRM),
品質管理用物質を含め,多数の名称が存在する。JIS Q 17034は,標準物質生産者(RMP)
に関する追加情報を含んでいる。JIS Q 17034の要求事項を満たすRMPは,能力があるとみ
なされる。JIS Q 17034の要求事項を満たす生産者から入手した標準物質には,製品情報シー
ト/認証書が添えられている。そこには,その他の特性とともに,規定特性の均質性及び安
定性が記載されており,認証標準物質については,更に認証値及び付随する測定不確かさ並
びに計量トレーサビリティをもつ規定特性が記載されている。
注記2 JIS Q 0033は,標準物質の選択及び使用に関する手引を提供する。ISO Guide 80は,内部で
品質管理用物質を生産するための手引を提供する。
6.4.2
ラボラトリが自身の恒久的な管理下にない設備を使用する場合は,この規格の設備に関する要求事
項が満たされることを確実にしなければならない。
6.4.3
ラボラトリは,設備が適正に機能することを確実にするため及び汚染又は劣化を防止するために,
設備の取扱い,輸送,保管,使用及び計画的保守の手順をもたなければならない。
6.4.4
ラボラトリは,設備を業務使用に導入する前又は業務使用に復帰させる前に,規定された要求事項
への適合を検証しなければならない。
6.4.5
測定に使用される設備は,妥当な結果を得るために必要な測定の精確さ及び/又は測定不確かさを
達成する能力をもたなければならない。
6.4.6
測定設備は,次の場合に校正されなければならない。
− 測定の精確さ又は測定不確かさが,報告された結果の妥当性に影響を与える。
− その設備の校正が,報告された結果の計量トレーサビリティを確立するために要求される。
注記 報告された結果の妥当性に影響を及ぼす設備には,次が含まれ得る。
− 測定対象量の直接測定に使用される設備。例えば,質量の測定を行うために,はかりを使
用する場合。
7
Q 17025:2018 (ISO/IEC 17025:2017)
− 測定値の補正に使用される設備。例えば,温度測定。
− 複数の量から計算された測定結果を得るために使用される設備。
6.4.7
ラボラトリは,校正プログラムを確立しなければならない。その校正プログラムは,校正状態につ
いての信頼を維持するため,見直され,必要に応じて調整されなければならない。
6.4.8
校正が必要な全ての設備又は有効期間が定められた全ての設備は,設備の使用者が校正状態又は有
効期間を容易に識別できるように,ラベル付けを行うか,コード化するか,又はその他の方法で識別しな
ければならない。
6.4.9
過負荷又は誤った取扱いを受けた設備,疑わしい結果を生じる設備,又は欠陥をもつ若しくは規定
の要求事項を満たさないことが認められた設備は,業務使用を停止しなければならない。その設備は,そ
れが正常に機能することが検証されるまで,使用を防止するため隔離するか,又は業務使用停止中である
ことを示す明瞭なラベル付け若しくはマーク付けを行わなければならない。ラボラトリは,不具合又は規
定された要求事項からの逸脱の影響を調査し,不適合業務の管理の手順を開始しなければならない(7.10
参照)。
6.4.10 設備の機能についての信頼を維持するために中間チェックが必要な場合には,これらのチェック
は,手順に従って実施しなければならない。
6.4.11 校正及び標準物質データに参照値又は補正因子が含まれる場合,ラボラトリは,規定された要求事
項を満たすために,必要に応じて,参照値及び補正因子が更新され,有効に使用されることを確実にしな
ければならない。
6.4.12 ラボラトリは,意図しない設備の調整によって結果が無効となることを防ぐために,実行可能な手
段を講じなければならない。
6.4.13 ラボラトリ活動に影響を与え得る設備の記録を保持しなければならない。記録には,適用可能な場
合,次の事項を含めなければならない。
a) ソフトウェア及びファームウェアのバージョンを含む,設備の識別。
b) 製造業者の名称,型式の識別及びシリアル番号又はその他の固有の識別。
c) 設備が規定された要求事項に適合していることの検証の証拠。
d) 現在の所在場所。
e) 校正の日付,校正結果,調整,受入基準及び次回校正の期日又は校正周期。
f)
標準物質の文書,結果,受入基準,関連する日付及び有効期間。
g) 設備の機能に関連する場合は,保守計画及びこれまでに実施された保守。
h) 設備の損傷,機能不良,改造又は修理の詳細。
6.5
計量トレーサビリティ
6.5.1
ラボラトリは,測定結果を適切な計量参照に結び付けるよう,それぞれの校正が測定不確かさに寄
与している,文書化された切れ目のない校正の連鎖によって,測定結果の計量トレーサビリティを確立し,
維持しなければならない。
注記1 ISO/IEC Guide 99には,計量トレーサビリティは,“それぞれが測定不確かさに寄与してい
る,文書化された切れ目のない校正の連鎖によって計量参照に測定結果を関係付けることが
できるという測定結果の性質”として定義されている。
注記2 計量トレーサビリティに関する追加の情報については,附属書Aを参照。
6.5.2
ラボラトリは,次のいずれかを通じて,測定結果が国際単位系(SI)にトレーサブルであることを
確実にしなければならない。
8
Q 17025:2018 (ISO/IEC 17025:2017)
a) 能力のあるラボラトリから提供される校正。
注記1 この規格の要求事項を満たすラボラトリは,能力があるとみなされる。
b) 能力のある生産者から提供された,表明されたSIへの計量トレーサビリティを伴った認証標準物質の
認証値。
注記2 JIS Q 17034の要求事項を満たす標準物質生産者は,能力があるとみなされる。
c) 直接的に又は間接的に,国家標準又は国際標準との比較によって確認がなされたSI単位の直接的実現。
注記3 幾つかの重要な単位の定義の現実的な実現方法の詳細は,SI文書に記載されている。
6.5.3
SI単位に対する計量トレーサビリティが技術的に不可能である場合,ラボラトリは,例えば,次
のような適切な計量参照への計量トレーサビリティを実証しなければならない。
a) 能力のある生産者から提供された認証標準物質の認証値。
b) 明確に記述され,意図した用途に合致した測定結果を提供するものとして受け入れられており,適切
な比較によって確認がなされた参照測定手順,規定された方法又は合意標準の結果。
6.6
外部から提供される製品及びサービス
6.6.1
ラボラトリは,ラボラトリ活動に影響を及ぼす,外部から提供される製品及びサービスが次の事項
に該当する場合には,適切なものだけが使用されることを確実にしなければならない。
a) 製品及びサービスがラボラトリ自体の活動に組み込まれることを意図したものである場合。
b) 製品及びサービスの一部又は全てが,外部提供者から受領したままの状態でラボラトリから顧客に直
接提供される場合。
c) 製品及びサービスが,ラボラトリの業務を支援するために使用される場合。
注記 製品には,例えば,測定標準並びに設備,補助設備,消耗品及び標準物質が含まれ得る。サー
ビスには,例えば,校正サービス,サンプリングサービス,試験サービス,施設及び設備保守
サービス,技能試験サービス並びに評価及び監査サービスが含まれ得る。
6.6.2
ラボラトリは,次の事項に関する手順をもち記録を保持しなければならない。
a) 外部から提供される製品及びサービスに関するラボラトリの要求事項を,明確にし,レビューし,承
認する。
b) 外部提供者の評価,選定,パフォーマンスの監視及び再評価に関する基準を明確にする。
c) 外部から提供される製品及びサービスが,使用される前又は顧客に直接提供される前に,ラボラトリ
の設定した要求事項,又は適用可能な場合,この規格の関連する要求事項への適合を確実にする。
d) 外部提供者の評価,パフォーマンスの監視及び再評価から生じた処置をとる。
6.6.3
ラボラトリは,次の事項に関して,外部提供者に要求事項を伝達しなければならない。
a) 提供される製品及びサービス。
b) 受入基準。
c) 必要とされる要員資格を含む,力量。
d) ラボラトリ又はその顧客が外部提供者先での実施を意図している活動。
7
プロセスに関する要求事項
7.1
依頼,見積仕様書及び契約のレビュー
7.1.1
ラボラトリは,依頼,見積仕様書及び契約のレビューに関する手順をもたなければならない。この
手順は,次の事項を確実にしなければならない。
a) 要求事項が十分に明確化され,文書化され,理解されている。
9
Q 17025:2018 (ISO/IEC 17025:2017)
b) ラボラトリが,要求事項を満たすための業務能力及び資源を備えている。
c) 外部提供者を利用する場合は,6.6の要求事項が適用され,ラボラトリが顧客に対して,外部提供者に
よって実施される特定のラボラトリ活動に関して通知し,顧客の承認を得る。
注記1 外部から提供されるラボラトリ活動は,次の場合に起こり得ることが認識されている。
− ラボラトリが,そのラボラトリ活動を実施する資源及び能力をもっているが,予期し
なかった理由によって,その一部又は全てを実行できない場合。
− ラボラトリが,そのラボラトリ活動を実施する資源又は能力をもっていない場合。
d) 適切な方法又は手順が選択され,顧客の要求事項を満たすことができる。
注記2 内部の顧客又は定期の顧客に対しては,依頼,見積仕様書及び契約のレビューは簡素化され
た方法で実施することができる。
7.1.2
ラボラトリは,顧客の依頼した方法が不適切又は旧式であると考えられる場合,顧客にその旨を通
知しなければならない。
7.1.3
顧客が,試験又は校正に関して,仕様又は規格への適合性の表明(例えば,合格/不合格,許容の
範囲内/範囲外)を要請する場合は,その仕様又は規格及び判定ルールを明確にしなければならない。要
請された仕様又は規格に当該取決めが内在する場合を除き,選択した判定ルールを顧客に伝達し合意を得
なければならない。
注記 適合性の表明に関する更なる手引について,ISO/IEC Guide 98-4を参照。
7.1.4
依頼又は見積仕様書と契約との間での何らかの相違は,ラボラトリ活動が開始される前に解決しな
ければならない。個々の契約は,ラボラトリ及び顧客の双方にとって受入れ可能でなければならない。顧
客から要請された逸脱が,ラボラトリの誠実さ(integrity)又は結果の妥当性に影響を及ぼしてはならない。
7.1.5
契約からのいかなる逸脱をも,顧客に知らせなければならない。
7.1.6
業務開始後に契約が変更される場合は,契約のレビューを繰り返さなければならない。また,全て
の変更を,影響を受ける全ての要員に伝達しなければならない。
7.1.7
ラボラトリは,顧客の依頼の明確化,及び実施される業務に関連したラボラトリのパフォーマンス
の監視に関して,顧客又は顧客の代理人と協力しなければならない。
注記 このような協力には,次の事項が含まれ得る。
a) 顧客固有のラボラトリ活動に立ち会うために,ラボラトリの関連する区域に正当に立ち入
れるようにする。
b) 検証の目的で顧客が必要とする品目の,準備,こん(梱)包及び発送。
7.1.8
重要な変更を含め,レビューの記録を保持しなければならない。顧客の要求事項,又はラボラトリ
活動の結果に関して顧客と交わした,関連する議論の記録も保持しなければならない。
7.2
方法の選定,検証及び妥当性確認
7.2.1
方法の選定及び検証
7.2.1.1
ラボラトリは,全てのラボラトリ活動に関して適切な方法及び手順を用いなければならず,また,
適切な場合,測定不確かさの評価及びデータ分析のための統計的手法に関しても同様である。
注記 この規格で使用される“方法”は,ISO/IEC Guide 99において定義される“測定手順”と同義
と考えられる。
7.2.1.2
全ての方法,手順,並びにラボラトリ活動に関連する指示書,規格,マニュアル及び参照データ
などの支援文書は,最新の状態で維持し,要員がいつでも利用できるようにしなければならない(8.3参照)。
7.2.1.3
ラボラトリは,有効な最新版の方法を用いることが不適切又は不可能でない限り,それを確実に
10
Q 17025:2018 (ISO/IEC 17025:2017)
しなければならない。必要な場合には,矛盾のない適用を確実にするため,詳細事項の追加によって方法
の適用を補足しなければならない。
注記 ラボラトリ活動の実施方法について,国際規格,地域規格若しくは国家規格又は十分で簡潔な
情報を含むその他の広く認められている仕様書が,そのままラボラトリの実施要員が使用でき
るように書かれている場合には,内部手順書として補足したり,書き直したりする必要はない。
その方法の中での操作の選択又は詳細な補足のために,追加の文書を用意する必要があり得る。
7.2.1.4
顧客が,使用する方法を指定しない場合,ラボラトリは適切な方法を選定し,選定した方法を顧
客に通知しなければならない。国際規格,地域規格若しくは国家規格のいずれかにおいて公表された方法,
定評ある技術機関が公表した方法,関連する科学文献若しくは定期刊行物において公表された方法,又は
設備の製造業者が指定する方法が推奨される。ラボラトリが開発又は修正した方法も用いることができる。
7.2.1.5
ラボラトリは,必要なパフォーマンスを達成できることを確実にすることによって,選定した方
法を導入する前にその方法を適切に実施できることを検証しなければならない。検証の記録を保持しなけ
ればならない。その方法がそれを発行する機関によって改訂される場合,ラボラトリは,必要な程度まで
検証を繰り返さなければならない。
7.2.1.6
方法の開発が必要な場合,これは計画的な活動でなければならず,十分な資質を備えた,力量を
もつ要員に割り当てなければならない。方法の開発の進行につれて,顧客のニーズが依然として満たされ
ていることを確認するため,定期的な見直しを行わなければならない。開発計画の変更は,承認され,許
可されなければならない。
7.2.1.7
全てのラボラトリ活動に関する方法からの逸脱は,その逸脱があらかじめ文書化され,技術的に
正しいと証明され,正式に許可され,かつ,顧客によって受け入れられている場合に限らなければならな
い。
注記 逸脱に対する顧客の受入れは,契約書において事前に合意されていることもあり得る。
7.2.2
方法の妥当性確認
7.2.2.1
ラボラトリは,規格外の方法,ラボラトリが開発した方法,及び規格に規定された方法であって
意図された適用範囲外で使用するもの又はその他の変更がなされたものについて,妥当性確認を行わなけ
ればならない。妥当性確認は,特定の適用対象又は適用分野のニーズを満たすために必要な程度まで幅広
く行わなければならない。
注記1 妥当性確認には,試験又は校正品目のサンプリング,取扱い及び輸送の手順が含まれ得る。
注記2 方法の妥当性確認に用いる手法は,次の事項のうちの一つ又はそれらの組合せであり得る。
a) 参照標準又は標準物質を用いた,校正又は偏り及び精度の評価。
b) 結果に影響する要因の系統的な評価。
c) 培養器の温度,分注量などの管理されたパラメータの変化を通じた,方法の頑健性の試
験。
d) 妥当性が確認された他の方法で得られた結果との比較。
e) 試験所間比較。
f)
方法の原理の理解及びサンプリング又は試験方法のパフォーマンスの実際の経験に基づ
いた,結果の測定不確かさの評価。
7.2.2.2
妥当性が確認された方法を変更する場合は,そのような変更の影響を確定しなければならず,そ
れらが元の妥当性確認に影響を与えることが判明した場合,新たに方法の妥当性確認を行わなければなら
ない。
11
Q 17025:2018 (ISO/IEC 17025:2017)
7.2.2.3
妥当性が確認された方法のパフォーマンス特性は,意図する用途に対する評価において顧客のニ
ーズに適し,規定された要求事項に整合していなければならない。
注記 パフォーマンス特性の例には,測定範囲,精確さ,結果の測定不確かさ,検出限界,定量限界,
方法の選択性,直線性,繰返し性又は再現性,外部影響に対する頑健性,又は試料若しくは試
験対象のマトリックスからの干渉に対する共相関感度,及び偏りが含まれ得るが,これらに限
定されない。
7.2.2.4
ラボラトリは,次の妥当性確認の記録を保持しなければならない。
a) 使用した妥当性確認の手順。
b) 要求事項の詳述。
c) 方法のパフォーマンス特性の確定。
d) 得られた結果。
e) 意図した用途に対する方法の適切性を詳述した,方法の妥当性に関する表明。
7.3
サンプリング
7.3.1
ラボラトリは,後の試験又は校正のための物質,材料又は製品のサンプリングを実施する場合,サ
ンプリングの計画及び方法をもたなければならない。サンプリング方法は,後の試験又は校正結果の妥当
性を確実にするために管理すべき要因を考慮しなければならない。サンプリングの計画及び方法は,サン
プリングが行われる場所で利用できなければならない。サンプリング計画は,合理的である限り,適切な
統計的方法に基づかなければならない。
7.3.2
サンプリング方法は,次の事項を記述しなければならない。
a) サンプル又はサンプリング場所の選択
b) サンプリング計画
c) 後の試験又は校正のために必要な品目を得るための,物質,材料又は製品からのサンプルの準備及び
処理
注記 ラボラトリに受領された際に,7.4に規定された更なる取扱いが必要とされる場合がある。
7.3.3
ラボラトリは,請け負った試験・校正の一部を構成する該当サンプリングデータの記録を保持しな
ければならない。これらの記録には,該当する場合,次の事項を含めなければならない。
a) 用いたサンプリング手順の参照。
b) サンプリングの日付及び時刻。
c) 試料を特定し記述するためのデータ(例えば,数,量,名称)。
d) サンプリングを実施した要員の識別。
e) 使用された設備の識別。
f)
環境条件又は輸送条件。
g) 適切な場合,サンプリング場所を特定するための図面又はその他の同等な手段。
h) サンプリング方法及びサンプリング計画からの逸脱,追加又は除外。
7.4
試験・校正品目の取扱い
7.4.1
ラボラトリは,試験・校正品目の完全性並びにラボラトリ及び顧客の利益を保護するために必要な
全ての規定を含め,試験・校正品目の輸送,受領,取扱い,保護,保管,保留及び処分又は返却のための
手順をもたなければならない。ラボラトリは,試験又は校正のための取扱い,輸送,保管/待機及び準備
の間に品目が劣化,汚染,損失又は損傷を受けることを防止するための予防策をとらなければならない。
試験・校正品目に添えられた取扱いの指示に従わなければならない。
12
Q 17025:2018 (ISO/IEC 17025:2017)
7.4.2
ラボラトリは,試験・校正品目の明確な識別のためのシステムをもたなければならない。この識別
は,当該品目がラボラトリの責任下にある間,保持されなければならない。識別システムは,品目の物理
的な混同又は記録若しくはその他の文書で引用する際の混同が起こらないことを確実にしなければならな
い。識別システムは,適切ならば品目又は品目のグループの小分け及び品目の移送に対応しなければなら
ない。
7.4.3
試験・校正品目を受領した際,規定された状態からの逸脱を記録しなければならない。品目の試験・
校正に対する適性に何らかの疑義がある場合,又は品目が添えられた記述に適合しない場合,ラボラトリ
は,業務を進める前に更なる指示を求めて顧客に相談し,この相談の結果を記録しなければならない。顧
客が,規定された状態からの逸脱を認めながらその品目の試験又は校正を要求する場合,ラボラトリは,
その逸脱によってどの結果が影響を受けるおそれがあるのかを示した免責条項を報告書に含めなければな
らない。
7.4.4
規定された環境条件下で品目を保管又は調整する必要がある場合は,これらの条件を維持し,監視
し,記録しなければならない。
7.5
技術的記録
7.5.1
ラボラトリは,個々のラボラトリ活動の技術的記録には,結果,報告並びに可能であれば測定結果
及び付随する測定不確かさに影響を与える要因の特定を容易にし,元の条件にできるだけ近い条件でラボ
ラトリ活動の反復を可能とする十分な情報が含まれることを確実にしなければならない。その技術的記録
には,日付並びに個々のラボラトリ活動及びデータ・結果の確認に責任をもつ要員の識別を含めなければ
ならない。観測原本,データ及び計算は,それらが作成される時点において記録され,特定の業務におい
て識別可能でなければならない。
7.5.2
ラボラトリは,技術的記録の変更について,以前の版又は観測原本に遡って追跡できることを確実
にしなければならない。変更の日付,変更点の表示及び変更に責任をもつ要員を含め,元のデータ及び変
更されたデータ並びにそれらのファイルの両方を保持しなければならない。
7.6
測定不確かさの評価
7.6.1
ラボラトリは,測定不確かさへの寄与成分を特定しなければならない。測定不確かさを評価する際,
サンプリングから生じるものを含み,重大な全ての寄与成分を,適切な分析方法を用いて考慮しなければ
ならない。
7.6.2
校正を実施するラボラトリは,所有する設備を含め,全ての校正に関する測定不確かさを評価しな
ければならない。
7.6.3
試験を実施するラボラトリは,測定不確かさを評価しなければならない。試験方法によって,厳密
な測定不確かさの評価ができない場合,原理の理解又は試験方法の実施に関する実際の経験に基づいて推
定しなければならない。
注記1 広く認められた試験方法が,測定不確かさの主な要因の値に限界を定め,計算結果の表現形
式を規定している場合には,ラボラトリは,試験方法及び報告方法の指示に従うことによっ
て,7.6.3を満足しているとみなされる。
注記2 結果の測定不確かさが確立され,検証されている特定の方法に関して特定された重大な影響
因子が制御されていることをラボラトリが実証できる場合,個々の結果について測定不確か
さを評価する必要はない。
注記3 さらに詳しい情報については,ISO/IEC Guide 98-3,JIS Z 8404-1及びJIS Z 8402規格群を参
照。
13
Q 17025:2018 (ISO/IEC 17025:2017)
7.7
結果の妥当性の確保
7.7.1
ラボラトリは,結果の妥当性を監視するための手順をもたなければならない。結果として得られる
データは,傾向が検出できるような方法で記録し,実行可能な場合,結果のレビューに統計的手法を適用
しなければならない。この監視は,計画し,見直さなければならない。また,適切な場合,次の事項を含
めなければならないが,これらに限定されない。
a) 標準物質又は品質管理物質の使用
b) トレーサブルな結果を得るために校正された代替の計測機器の使用
c) 測定設備及び試験設備の機能チェック
d) 適用可能な場合,チェック標準又は実用標準の管理図を伴う使用
e) 測定設備の中間チェック
f)
同じ方法又は異なる方法を用いた試験又は校正の反復
g) 保留された品目の再試験又は再校正
h) 一つの品目の異なる特性に関する結果の相関
i)
報告された結果のレビュー
j)
試験所内比較
k) ブラインドサンプルの試験
7.7.2
ラボラトリは,利用可能で適切な場合,他のラボラトリの結果との比較によって,そのパフォーマ
ンスを監視しなければならない。この監視は,計画し,見直さなければならない。また,次のいずれか,
又は両方を含まなければならないが,これらに限定されない。
a) 技能試験への参加
注記 JIS Q 17043は,技能試験及び技能試験提供者に関する追加情報を含んでいる。JIS Q 17043
の要求事項を満たす技能試験提供者は,能力があるとみなされる。
b) 技能試験以外の試験所間比較への参加
7.7.3
ラボラトリは,監視活動で得られたデータを分析し,ラボラトリ活動の管理に使用し,適用可能で
あれば,改善に使用しなければならない。監視活動で得られたデータの分析結果が,事前に規定した処置
基準を外れることが判明した場合は,不正確な結果が報告されることを防止するため,適切な処置を講じ
なければならない。
7.8
結果の報告
7.8.1
一般
7.8.1.1
結果は,開示する前に,レビューされ,承認されなければならない。
7.8.1.2
結果は,通常,報告書(例えば,試験報告書,校正証明書又はサンプリング報告書)の形で,正
確に,明瞭に,曖昧でなく,客観的に提供されなければならない。また,結果には,顧客と合意し,かつ,
結果の解釈に必要な全ての情報及び用いた方法が要求する全ての情報を含めなければならない。発行され
た全ての報告書は,技術的記録として保持しなければならない。
注記1 この規格の目的において,試験報告書及び校正証明書は,それぞれ試験証明書及び校正報告
書と呼ばれることがある。
注記2 この規格の要求事項が満たされている限り,報告書はハードコピー又は電子的手段によって
発行することができる。
7.8.1.3
顧客との合意がある場合には,簡略化した方法で結果を報告してもよい。7.8.2〜7.8.7に規定され
ているが,顧客に報告されなかったいかなる情報も,すぐに利用できるようにしておかなければならない。
14
Q 17025:2018 (ISO/IEC 17025:2017)
7.8.2
報告書(試験,校正又はサンプリング)に関する共通の要求事項
7.8.2.1
個々の報告書は,少なくとも次の情報を含まなければならない。ただし,ラボラトリが正当な除
外の理由をもち,それによって誤解又は誤用の可能性が最小化される場合はこの限りでない。
a) タイトル(例えば,“試験報告書”,“校正証明書”又は“サンプリング報告書”)
b) ラボラトリの名称及び住所
c) 顧客の施設若しくはラボラトリの恒久的施設から離れた場所,又は関連する一時施設若しくは移動施
設で実施された場合を含め,ラボラトリ活動が実施された場所
d) 全ての構成要素が完全な報告書の一部であることが分かる固有の識別,及び報告書の終わりを示す明
瞭な識別
e) 顧客の名称及び連絡先情報
f)
用いた方法の識別
g) 品目の記述,明確な識別,及び必要な場合,品目の状態
h) 結果の妥当性及び適用に重大な意味をもつ場合は,試験・校正品目の受領日,及びサンプリングの実
施日
i)
ラボラトリ活動の実施日(期間)
j)
報告書の発行日
k) サンプリング計画及びサンプリング方法が結果の妥当性又は適用に関連する場合には,ラボラトリ又
はその他の機関が用いたサンプリング計画及びサンプリング方法の参照
l)
結果が,その試験,校正又はサンプリングされた品目だけに関するものであるという旨の表明
m) 結果。適切な場合,測定単位を伴う。
n) 方法への追加又は方法からの逸脱若しくは除外
o) 報告書の承認権限者の識別
p) 結果が外部提供者から出されたものである場合は,明確な識別
注記 ラボラトリの承認なく報告書の一部分だけを複製してはならないことを規定する表明を含める
ことによって,報告書の一部が前後関係から切り離されないことを保証することができる。
7.8.2.2
ラボラトリは,その情報が顧客から提供されたものである場合を除き,報告書に記載された全て
の情報について責任をもたなければならない。顧客によって提供されたデータは,明確に識別されなけれ
ばならない。さらに,その情報が顧客から提供されたもので,結果の妥当性に影響する可能性がある場合
には,免責条項を報告書に記載しなければならない。ラボラトリがサンプリング段階に責任をもたない場
合(例えば,試料が顧客から提供された場合)には,結果は受領した試料に適用される旨を報告書に記載
しなければならない。
7.8.3
試験報告書に関する特定要求事項
7.8.3.1
7.8.2の要求事項に加え,試験結果の解釈に必要な場合,試験報告書は次の事項を含まなければな
らない。
a) 特定の試験条件に関する情報,例えば,環境条件
b) 該当する場合,要求事項又は仕様に対する適合性の表明(7.8.6参照)
c) 適用可能な場合であって,次のいずれかの条件を満たす場合には,測定対象量と同じ単位で表示され
た,又は測定対象量に対する相対値(例えば,パーセント)で表示された測定不確かさ
− 測定不確かさが,試験結果の妥当性又は適用に関連している。
− 顧客の指示が,測定不確かさを要求している。
15
Q 17025:2018 (ISO/IEC 17025:2017)
− 測定不確かさが,仕様の限界への適合性に影響を与える。
d) 適切な場合,意見及び解釈(7.8.7参照)
e) 特定の方法,規制当局,顧客又は顧客のグループによって要求されることがある追加の情報
7.8.3.2
ラボラトリがサンプリング活動に責任をもつ場合,試験結果の解釈に必要であれば,試験報告書
は,7.8.5の要求事項を満たさなければならない。
7.8.4
校正証明書に関する特定要求事項
7.8.4.1
7.8.2の要求事項に加え,校正証明書は,次の事項を含まなければならない。
a) 測定対象量と同じ単位で表示された,又は測定対象量に対する相対値(例えば,パーセント)で表示
された測定結果についての測定不確かさ
注記 ISO/IEC Guide 99によれば,測定結果は一般に,測定の単位及び測定不確かさを含む,単一
の測定された量の値で表される。
b) 測定結果に影響をもつ,校正が実施された際の条件(例えば,環境条件)
c) 測定値がどのように計量トレーサビリティをもつのかを明確化した表明(附属書Aを参照)
d) 利用可能な場合,調整又は修理の前後の結果
e) 該当する場合,要求事項又は仕様への適合性の表明(7.8.6参照)
f)
適切な場合,意見及び解釈(7.8.7参照)
7.8.4.2
ラボラトリがサンプリング活動に責任をもつ場合,校正結果の解釈に必要であれば,校正証明書
は,7.8.5の要求事項を満たさなければならない。
7.8.4.3
顧客との合意がある場合を除き,校正証明書又は校正ラベルのいずれも,校正周期に関する推奨
を含んではならない。
7.8.5
サンプリングの報告−特定要求事項
ラボラトリがサンプリング活動に責任をもつ場合,7.8.2に列挙する要求事項に加え,結果の解釈に必要
な場合には,報告書は次の事項を含まなければならない。
a) サンプリングの日付
b) サンプリングされた品目又は材料の固有の識別(適切な場合,製造業者の名称,指定されたモデル又
は型式,及びシリアル番号を含む。)
c) 図面,スケッチ又は写真を含む,サンプリングの場所
d) サンプリングの計画及び方法の参照
e) 結果の解釈に影響する,サンプリング中の環境条件の詳細
f)
後の試験又は校正の測定不確かさを評価するために必要な情報
7.8.6
適合性の表明の報告
7.8.6.1
ラボラトリは,仕様又は規格への適合性を表明する場合,採用した判定ルールに付随する,(誤
判定による合格及び誤判定による不合格,並びに統計的仮定などの)リスクのレベルを考慮に入れた上で
採用した判定ルールを文書化し,それを適用しなければならない。
注記 その判定ルールが,顧客,規制又は規範文書によって規定されている場合,リスクのレベルの
更なる検討は不要である。
7.8.6.2
ラボラトリは,次の事項を明示して,適合性の表明に関する報告を行わなければならない。
a) どの結果に対して適合性の表明が適用されるのか。
b) どの仕様,規格又はそれらの一部に適合又は不適合なのか。
c) 適用された判定ルール(要求された仕様又は規格に既に含まれている場合を除く。)。
16
Q 17025:2018 (ISO/IEC 17025:2017)
注記 さらに詳しい情報については,ISO/IEC Guide 98-4を参照。
7.8.7
意見及び解釈の報告
7.8.7.1
ラボラトリは,意見及び解釈を表明する場合,それらを表明する権限を与えられた要員だけがそ
れぞれの表明を提示することを確実にしなければならない。ラボラトリは,意見及び解釈が形成された根
拠を文書化しなければならない。
注記 意見及び解釈は,JIS Q 17020及びJIS Q 17065が意図している検査及び製品認証の表明,並び
に7.8.6の適合性の表明と区別することが重要である。
7.8.7.2
報告書に表明する意見及び解釈は,試験又は校正した品目から得られた結果に基づかなければな
らず,意見及び解釈である旨を明示しなければならない。
7.8.7.3 意見及び解釈が顧客との対話で直接伝達される場合,その対話の記録を保持しなければならない。
7.8.8
報告書の修正
7.8.8.1
発行済みの報告書を変更,修正又は再発行する必要がある場合は,いかなる情報の変更も明確に
識別し,適切な場合,変更の理由を報告書に含めなければならない。
7.8.8.2
発行後の報告書の修正は,“報告書,シリアル番号...(又は他の識別)の修正”という表明若しく
は同等の文言を含めた,追加文書又はデータ転送という形態だけによって行わなければならない。
そのような修正は,この規格の全ての要求事項を満たさなければならない。
7.8.8.3
完全な新規の報告書を発行することが必要な場合には,この新規の報告書に固有の識別を与え,
それが置き換わる元の報告書の引用を含めなければならない。
7.9
苦情
7.9.1
ラボラトリは,苦情を受領し,評価し,決定を下すための文書化したプロセスをもたなければなら
ない。
7.9.2
苦情処理プロセスの記述は,いかなる利害関係者にも,要請に応じて入手可能にしなければならな
い。苦情を受領した時点で,ラボラトリは,その苦情が,自らが責任をもつラボラトリ活動に関係するか
どうかを確認し,関係があればその苦情を処理しなければならない。ラボラトリは,苦情処理プロセスの
全ての階層において,全ての決定について責任をもたなければならない。
7.9.3
苦情処理プロセスは,少なくとも次の要素及び方法を含まなければならない。
a) 苦情を受領し,妥当性を確認し,調査を行い,それに対応してとるべき処置を決定するためのプロセ
スを記述する。
b) 苦情を解決するためにとられる処置を含め,苦情を追跡し,記録する。
c) 適切な処置がとられることを確実にする。
7.9.4
苦情を受領するラボラトリは,その苦情の妥当性を確認するために必要な全ての情報の収集及び検
証に責任をもたなければならない。
7.9.5
ラボラトリは,可能な場合には,苦情申立者に対して苦情の受領を通知し,進捗状況及び結果を提
示しなければならない。
7.9.6
苦情申立者に伝達される結果は,問題となっている元のラボラトリ活動に関与していなかった者が
作成するか,又はレビューし承認しなければならない。
注記 これは,外部の要員によって実施することができる。
7.9.7
ラボラトリは,可能な場合には,苦情処理の終了を苦情申立者に対して正式に通知しなければなら
ない。
17
Q 17025:2018 (ISO/IEC 17025:2017)
7.10 不適合業務
7.10.1 ラボラトリは,そのラボラトリ活動の何らかの業務の側面,又はその結果が,ラボラトリの手順又
は顧客との間で合意された要求事項に適合しない場合(例えば,設備又は環境条件が規定の限界を外れて
いる場合,監視の結果が規定の基準を満たさない場合)に実施しなければならない手順をもたなければな
らない。この手順は,次の事項を確実にしなければならない。
a) 不適合業務の管理に関する責任及び権限を定める。
b) 処置(必要に応じて,業務を停止する又は繰り返すこと,及び報告書を保留することを含む。)を,ラ
ボラトリの設定したリスクレベルに基づいて定める。
c) 以前の結果に関する影響分析を含め,不適合業務の重大さを評価する。
d) 不適合業務の容認の可否を決定する。
e) 必要な場合,顧客に通知して業務結果を回収する。
f)
業務の再開を承認する責任を定める。
7.10.2 ラボラトリは,不適合業務及び7.10.1のb)〜f)に規定する処置の記録を保持しなければならない。
7.10.3 ラボラトリは,評価によって,不適合業務が再発し得ること又はラボラトリ自身のマネジメントシ
ステムに対する運営の適合性に疑いがあることが示された場合には,是正処置を実施しなければならない。
7.11 データの管理及び情報マネジメント
7.11.1 ラボラトリは,ラボラトリ活動を行うために必要なデータ及び情報を利用できなければならない。
7.11.2 データの収集,処理,記録,報告,保管又は検索に使用されるラボラトリ情報マネジメントシステ
ムは,導入の前に,ラボラトリによって,ラボラトリ情報マネジメントシステム内のインタフェースが適
正に機能していることを含め,機能性の妥当性を確認しなければならない。ラボラトリ情報マネジメント
システムは,ラボラトリによるソフトウェアの設定変更又は市販の既製ソフトウェアの変更を含め,変更
が行われる場合には,使用前に承認し,文書化し,妥当性を確認しなければならない。
注記1 この規格において,“ラボラトリ情報マネジメントシステム”には,電子化されたシステム及
び電子化されていないシステムの両方に含まれるデータ並びに情報の管理が含まれる。要求
事項によっては,電子化されていないシステムより電子化されているシステムに適用しやす
くなる。
注記2 一般的に使用されている市販の既製ソフトウェアは,設計上の適用範囲において十分に妥当
性が確認されているとみなすことができる。
7.11.3 ラボラトリ情報マネジメントシステムは,次の事項を満たさなければならない。
a) 無許可のアクセスから保護されている。
b) 不正な書き換え及び損失から防護されている。
c) 提供者若しくはラボラトリの仕様に適合する環境の中で運用されているか,又は電子化されていない
システムの場合は,手書きの記録及び転記の正確さを確保する条件を備える環境の中で運用されてい
る。
d) データ及び情報の完全性を確実にする方法で維持されている。
e) システム障害及びそれに対する適切な応急処置及び是正処置を記録することを含む。
7.11.4 ラボラトリ情報マネジメントシステムが,異なる場所(off-site)で管理及び保守されているか,又
は外部提供者を通じて管理及び保守されている場合,ラボラトリは,システムの提供者又は操作者が,こ
の規格の適用される全ての要求事項に適合することを確実にしなければならない。
7.11.5 ラボラトリは,ラボラトリ情報マネジメントシステムに関連する指示書,マニュアル及び参照デー
18
Q 17025:2018 (ISO/IEC 17025:2017)
タを要員がいつでも利用できることを確実にしなければならない。
7.11.6 計算及びデータ転送は,適切かつ系統的な方法でチェックを行わなければならない。
8
マネジメントシステムに関する要求事項
8.1
選択肢
8.1.1
一般
ラボラトリは,この規格の要求事項の一貫した達成を支援し,実証するとともに,試験・校正結果の品
質を保証することを可能にするマネジメントシステムを構築し,文書化し,実施し,維持しなければなら
ない。この規格の箇条4〜箇条7の要求事項に適合することに加え,ラボラトリは,選択肢A又は選択肢
Bに基づくマネジメントシステムを実施しなければならない。
注記 詳しくは,附属書Bを参照。
8.1.2
選択肢A
ラボラトリのマネジメントシステムは,少なくとも次の事項に取り組まなければならない。
− マネジメントシステムの文書化(8.2参照)
− マネジメントシステム文書の管理(8.3参照)
− 記録の管理(8.4参照)
− リスク及び機会への取組み(8.5参照)
− 改善(8.6参照)
− 是正処置(8.7参照)
− 内部監査(8.8参照)
− マネジメントレビュー(8.9参照)
8.1.3
選択肢B
JIS Q 9001の要求事項に従ってマネジメントシステムを確立し,維持しており,この規格の箇条4〜箇
条7の要求事項を一貫して満たすことを裏付け,実証することが可能なラボラトリは,少なくとも8.2〜8.9
に規定するマネジメントシステム要求事項の意図をも満たしている。
8.2
マネジメントシステムの文書化(選択肢A)
8.2.1
ラボラトリマネジメントは,この規格の目的を果たすための方針及び目標を,確立し,文書化し,
維持し,ラボラトリの組織の全ての階層で,この方針及び目標が周知され,実施されることを確実にしな
ければならない。
8.2.2
この方針及び目標は,ラボラトリの能力,公平性及び一貫性のある運営を取り上げていなければな
らない。
8.2.3
ラボラトリマネジメントは,マネジメントシステムの開発及び実施,並びにマネジメントシステム
の有効性の継続的改善に対するコミットメントの証拠を提示しなければならない。
8.2.4
この規格の要求事項を満たすことに関係する全ての文書,プロセス,システム,記録をマネジメン
トシステムに含めるか,マネジメントシステムから引用するか,又はマネジメントシステムに関連付けな
ければならない。
8.2.5
ラボラトリ活動に関与する全ての要員は,それらの要員の職責に適用されるマネジメントシステム
文書及び関連情報の該当部分を利用できなければならない。
19
Q 17025:2018 (ISO/IEC 17025:2017)
8.3
マネジメントシステム文書の管理(選択肢A)
8.3.1
ラボラトリは,この規格を満たすことに関係する(内部及び外部の)文書を管理しなければならな
い。
注記 ここでいう“文書”とは,方針表明文,手順書,仕様書,製造業者の指示書,校正値表,チャ
ート,教科書,ポスター,通知,覚書,図面,図解などであり得る。それらは,ハードコピー
か,又はデジタル形式のような様々な媒体で作成できる。
8.3.2
ラボラトリは,次の事項を確実にしなければならない。
a) 文書の発行に先立って,権限をもった要員がその文書の妥当性について承認を与える。
b) 文書を定期的に見直し,必要に応じて更新する。
c) 文書の変更及び最新の改訂の状況が識別される。
d) 適用される文書の適切な版が使用に際して入手でき,必要に応じてそれらの文書の配布が管理される。
e) 文書に固有の識別を付す。
f)
廃止文書の意図しない使用を防止する。目的を問わず,廃止文書を保持する場合は,それらに適切な
識別を付す。
8.4
記録の管理(選択肢A)
8.4.1
ラボラトリは,この規格の要求事項を満たすことを実証するための読みやすい記録を確立し,保持
しなければならない。
8.4.2
ラボラトリは,記録の識別,保管,保護,バックアップ,アーカイブ,検索,保持期間及び廃棄の
ために必要な管理を実施しなければならない。ラボラトリは,契約上の義務に準じた期間にわたって記録
を保持しなければならない。これらの記録へのアクセスは,機密保持のコミットメントに準じなければな
らない。また,記録は直ちに利用できなければならない。
注記 技術的記録に関する追加的な要求事項は,7.5に記載されている。
8.5
リスク及び機会への取組み(選択肢A)
8.5.1
ラボラトリは,次の事項を目的として,ラボラトリ活動に付随するリスク及び機会を考慮しなけれ
ばならない。
a) マネジメントシステムが,その意図した結果を達成できるという確信を与える。
b) ラボラトリの目的及び目標を達成する機会を広げる。
c) ラボラトリ活動における望ましくない影響及び潜在的障害を防止又は低減する。
d) 改善を達成する。
8.5.2
ラボラトリは,次の事項を計画しなければならない。
a) これらのリスク及び機会への取組み。
b) 次の事項を行う方法。
− これらの取組みのマネジメントシステムへの統合及び実施。
− これらの取組みの有効性の評価。
注記 この規格は,ラボラトリのリスクへの取組みの計画について規定するが,リスクマネジメント
の正式な方法又は文書化されたリスクマネジメントプロセスの要求事項は規定していない。ラ
ボラトリは,例えば,他の手引又は規格の適用を通じて,この規格によって要求されるリスク
マネジメント手法よりも広範な手法を開発するか否かを決定できる。
8.5.3
リスク及び機会への取組みは,ラボラトリが出す結果の妥当性に与える潜在的影響に釣り合ったも
のでなければならない。
20
Q 17025:2018 (ISO/IEC 17025:2017)
注記1 リスクへの取組みの選択肢には,脅威の特定及び回避,機会を追求するためのリスク負担,
リスク源の除去,可能性若しくは結果の変更,リスクの共有,又は情報に基づく決定による
リスク保持が含まれ得る。
注記2 機会は,ラボラトリ活動の範囲拡大,新たな顧客への取組み,新技術の使用及び顧客のニー
ズに取り組むその他の可能性につながり得る。
8.6
改善(選択肢A)
8.6.1
ラボラトリは,改善の機会を特定し,選択して,必要な処置を実施しなければならない。
注記 改善の機会は,業務手順のレビュー,方針の使用,全体の目標,監査結果,是正処置,マネジ
メントレビュー,要員からの提案,リスクアセスメント,データの分析,技能試験の結果を通
じて特定することができる。
8.6.2
ラボラトリは,顧客からの肯定的なフィードバック及び否定的なフィードバックの両方を求めなけ
ればならない。マネジメントシステム,ラボラトリ活動及び顧客へのサービスの改善のためにフィードバ
ックを分析し,利用しなければならない。
注記 フィードバックの種類の例には,顧客満足の調査,コミュニケーションの記録及び顧客と共同
での報告書のレビューが含まれる。
8.7
是正処置(選択肢A)
8.7.1
不適合が発生した場合,ラボラトリは,次の事項を行わなければならない。
a) その不適合に対処し,該当する場合には,必ず,次の事項を行う。
− その不適合を管理し,修正するための処置をとる。
− その不適合の結果に対処する。
b) その不適合が再発又は他のところで発生しないようにするため,次の事項によって,その不適合の原
因を除去するための処置をとる必要性を評価する。
− 不適合をレビューし,分析する。
− その不適合の原因を明確にする。
− 類似の不適合の有無,又はそれらが発生する可能性を明確にする。
c) 必要な処置を実施する。
d) とった全ての是正処置の有効性をレビューする。
e) 必要な場合には,計画の過程で明確になったリスク及び機会を更新する。
f)
必要な場合には,マネジメントシステムの変更を行う。
8.7.2
是正処置は,検出された不適合のもつ影響に応じたものでなければならない。
8.7.3
ラボラトリは,次の事項の証拠として記録を保持しなければならない。
a) 不適合の性質,原因及びそれに対してとったあらゆる処置
b) 是正処置の結果
8.8
内部監査(選択肢A)
8.8.1
ラボラトリは,マネジメントシステムが次の状況にあるか否かに関する情報を提供するために,あ
らかじめ定めた間隔で内部監査を実施しなければならない。
a) 次の事項に適合している。
− ラボラトリ活動を含めた,ラボラトリ自体のマネジメントシステムに関する要求事項
− この規格の要求事項
b) 有効に実施され,維持されている。
21
Q 17025:2018 (ISO/IEC 17025:2017)
8.8.2
ラボラトリは,次の事項を行わなければならない。
a) 頻度,方法,責任,要求事項の立案,及び報告を含む,監査プログラムを計画し,確立し,実施し,
維持する。監査プログラムは,関連するラボラトリ活動の重要性,ラボラトリに影響を及ぼす変更及
び前回までの監査の結果を考慮に入れなければならない。
b) 各監査について,監査基準及び監査範囲を定める。
c) 監査の結果を関連する管理要員に報告することを確実にする。
d) 遅滞なく,適切な修正及び是正処置を実施する。
e) 監査プログラムの実施及び監査結果の証拠として,記録を保持する。
注記 JIS Q 19011は,内部監査に関する指針を示している。
8.9
マネジメントレビュー(選択肢A)
8.9.1
ラボラトリマネジメントは,マネジメントシステムが引き続き,適切,妥当かつ有効であることを
確実にするために,この規格を満たすことに関係する明示された方針及び目標を含め,あらかじめ定めた
間隔でマネジメントシステムをレビューしなければならない。
8.9.2
マネジメントレビューへのインプットは,記録しなければならない。また,マネジメントレビュー
へのインプットには,次の事項に関係する情報を含めなければならない。
a) ラボラトリに関連する,内部及び外部の課題の変化
b) 目標の達成
c) 方針及び手順の適切さ
d) 前回までのマネジメントレビューの結果とった処置の状況
e) 最近の内部監査の結果
f)
是正処置
g) 外部機関による評価
h) 業務の量及び種類の変化,又はラボラトリ活動の範囲の変更
i)
顧客及び要員からのフィードバック
j)
苦情
k) 実施された改善の有効性
l)
資源の適切性
m) リスク特定の結果
n) 結果の妥当性の保証の成果
o) 監視活動及び教育訓練などのその他の関連因子
8.9.3
マネジメントレビューからのアウトプットは,少なくとも次の事項に関係する全ての決定及び処置
を記録しなければならない。
a) マネジメントシステム及びそのプロセスの有効性
b) この規格の要求事項を満たすことに関係するラボラトリ活動の改善
c) 必要とされる資源の提供
d) あらゆる変更の必要性
22
Q 17025:2018 (ISO/IEC 17025:2017)
附属書A
(参考)
計量トレーサビリティ
A.1 一般
計量トレーサビリティは,国内的にも国際的にも,測定結果の比較可能性を確実にするために重要な概
念であり,この附属書では計量トレーサビリティに関する追加的情報を記載する。
A.2 計量トレーサビリティの確立
A.2.1 計量トレーサビリティは,次の事項を検討し,確実にすることによって確立される。
a) 測定対象量の詳述。
b) 定められた,適切な計量参照(適切な計量参照には,国家標準又は国際標準,及び固有標準が含まれ
る。)まで遡る,文書化された,切れ目のない校正の連鎖。
c) トレーサビリティの連鎖の各段階の測定不確かさは,合意された方法に従って評価される。
d) 連鎖の各段階は,適切な方法で実施されており,測定結果及び付随し記録された測定不確かさを伴う。
e) 連鎖の一段階以上を実施するラボラトリは,技術的能力に関する証拠を提示する。
A.2.2 ラボラトリにおける測定結果に計量トレーサビリティを与えるために,校正された設備の系統測定
誤差(“偏り”と呼ばれることがある。)を考慮に入れる。計量トレーサビリティの供給において系統測定
誤差を考慮に入れる幾つかの方法がある。
A.2.3 ある仕様に対する適合性の表明(測定結果と付随する不確かさを省略)だけを含む,能力のあるラ
ボラトリから報告された情報をもった測定標準が,計量トレーサビリティを与えるものとして用いられる
ことがある。仕様限界が不確かさ要因として組み入れられているこのアプローチは,次の事項に依存する。
− 適合性を確立するための適切な判定ルールの使用
− 仕様限界が不確かさバジェットにおいて,技術的に適切なアプローチで取り扱われる事項
このアプローチの技術的根拠は,仕様に対して宣言された適合性が測定値の範囲を明確にしており,そ
こでは,ある指定された信頼の水準において,真値がその範囲内にあると期待され,真値からの偏りも,
測定不確かさも考慮していることである。
例 はかりを校正するために用いられるOIML R 111に等級が規定された分銅の使用
A.3 計量トレーサビリティの実証
A.3.1 ラボラトリは,この規格に基づいて計量トレーサビリティを確立する責任をもつ。この規格に適合
するラボラトリの校正結果は,計量トレーサビリティを提供する。JIS Q 17034に適合する標準物質生産者
からの認証標準物質の認証値は,計量トレーサビリティを提供する。第三者による承認(認定機関等),顧
客による外部評価,自己評価といった,この規格への適合を実証する様々な方法がある。国際的に受け入
れられる方法には次のものが含まれるが,これらに限定されない。
a) CIPM MRA(国際度量衡委員会相互承認取決め)等の国際的取決めの下でピアレビュー・プロセスを
経た校正測定能力。CIPM MRAの対象となるサービスは,BIPM(国際度量衡局)KCDB(基幹比較デ
ータベース)の附属書Cで見ることができる。このデータベースには,一覧に記載された各サービス
の範囲及び不確かさが含まれる。
23
Q 17025:2018 (ISO/IEC 17025:2017)
b) ILAC(国際試験所認定協力機構)取決め,又はILACが承認した地域取決めに基づく認定機関によっ
て認定を受けた校正測定能力は,計量トレーサビリティを実証している。認定された校正機関の範囲
は,それぞれの認定機関から公に入手できる。
A.3.2 計量トレーサビリティに関するBIPM,OIML(国際法定計量機関),ILAC及びISOの共同宣言は,
計量トレーサビリティの連鎖が国際的に受け入れられることを実証することが必要な場合の明確な指針を
定めている。
24
Q 17025:2018 (ISO/IEC 17025:2017)
附属書B
(参考)
マネジメントシステムに関する選択肢
B.1
マネジメントシステムの利用が増加したことによって,ラボラトリが,この規格に加えてJIS Q 9001
にも適合するとみなされるマネジメントシステムを運用できることを確実にする必要性が,一般的に高ま
った。その結果,この規格では,マネジメントシステムの実施に関係する要求事項について,二つの選択
肢を示すことになった。
B.2
選択肢A(8.1.2参照)は,ラボラトリにおけるマネジメントシステムの実施に関する最小限の要求
事項を列挙したものである。マネジメントシステムが対象とする,ラボラトリ活動の範囲に該当するJIS Q
9001の全ての要求事項を取り入れるよう注意が払われた。したがって,箇条4〜箇条7に適合し,かつ,
箇条8の選択肢Aを実施するラボラトリは,一般にJIS Q 9001の原則にも従って運営されていることにな
る。
B.3
選択肢B(8.1.3参照)によって,この規格の箇条4〜箇条7を一貫して満たしていることを裏付け,
実証するという形をとることで,ラボラトリは,JIS Q 9001の要求事項に従ってマネジメントシステムを
確立し,維持することが可能となる。したがって,箇条8の選択肢Bを実施するラボラトリは,JIS Q 9001
にも従って運営されていることになる。ラボラトリが運営しているマネジメントシステムがJIS Q 9001の
要求事項に適合していることは,それ自体ではそのラボラトリが技術的に有効なデータ及び結果を生成す
る能力をもつことを実証するわけではない。これは,この規格の箇条4〜箇条7の順守を通じて実現され
る。
B.4
いずれの選択肢も,マネジメントシステムのパフォーマンス及び箇条4〜箇条7の順守において,同
じ結果を達成することを意図している。
注記 文書,データ及び記録は,JIS Q 9001及びその他のマネジメントシステム規格で用いられてい
る,文書化された情報の構成要素である。文書の管理については,8.3に記載している。記録の
管理については,8.4及び7.5に記載している。ラボラトリ活動に関係するデータの管理につい
ては,7.11に記載している。
B.5
図B.1は,箇条7に記載しているような,ラボラトリの運用プロセスの図解の例を示す。

25
Q 17025:2018 (ISO/IEC 17025:2017)
図B.1−ラボラトリの運用プロセスの図解
26
Q 17025:2018 (ISO/IEC 17025:2017)
参考文献
[1]
JIS Z 8402-1 測定方法及び測定結果の精確さ(真度及び精度)−第1部:一般的な原理及び定義
注記 対応国際規格:ISO 5725-1,Accuracy (trueness and precision) of measurement methods and results
−Part 1: General principles and definitions
[2]
JIS Z 8402-2 測定方法及び測定結果の精確さ(真度及び精度)−第2部:標準測定方法の併行精度
及び再現精度を求めるための基本的方法
注記 対応国際規格:ISO 5725-2,Accuracy (trueness and precision) of measurement methods and results
−Part 2: Basic method for the determination of repeatability and reproducibility of a standard
measurement method
[3]
JIS Z 8402-3 測定方法及び測定結果の精確さ(真度及び精度)−第3部:標準測定方法の中間精度
注記 対応国際規格:ISO 5725-3,Accuracy (trueness and precision) of measurement methods and results
−Part 3: Intermediate measures of the precision of a standard measurement method
[4]
JIS Z 8402-4 測定方法及び測定結果の精確さ(真度及び精度)−第4部:標準測定方法の真度を求
めるための基本的方法
注記 対応国際規格:ISO 5725-4,Accuracy (trueness and precision) of measurement methods and results
−Part 4: Basic methods for the determination of the trueness of a standard measurement method
[5]
JIS Z 8402-6 測定方法及び測定結果の精確さ(真度及び精度)−第6部:精確さに関する値の実用
的な使い方
注記 対応国際規格:ISO 5725-6,Accuracy (trueness and precision) of measurement methods and results
−Part 6: Use in practice of accuracy values
[6]
JIS Q 9000 品質マネジメントシステム−基本及び用語
注記 対応国際規格:ISO 9000,Quality management systems−Fundamentals and vocabulary
[7]
JIS Q 9001 品質マネジメントシステム−要求事項
注記 対応国際規格:ISO 9001,Quality management systems−Requirements
[8]
JIS Q 10012 計測マネジメントシステム−測定プロセス及び測定機器に関する要求事項
注記 対応国際規格:ISO 10012,Measurement management systems−Requirements for measurement
processes and measuring equipment
[9]
JIS X 0160 ソフトウェアライフサイクルプロセス
注記1 対応国際規格:ISO/IEC 12207,Systems and software engineering−Software life cycle
processes
注記2 ISO/IEC 12207は,ISO/IEC/IEEE 12207:2017へ改訂されている。
[10] ISO 15189,Medical laboratories−Requirements for quality and competence
[11] ISO 15194,In vitro diagnostic medical devices−Measurement of quantities in samples of biological origin−
Requirements for certified reference materials and the content of supporting documentation
[12] JIS Q 17011 適合性評価−適合性評価機関の認定を行う機関に対する要求事項
注記 対応国際規格:ISO/IEC 17011,Conformity assessment−Requirements for accreditation bodies
accrediting conformity assessment bodies
[13] JIS Q 17020 適合性評価−検査を実施する各種機関の運営に関する要求事項
27
Q 17025:2018 (ISO/IEC 17025:2017)
注記 対応国際規格:ISO/IEC 17020,Conformity assessment−Requirements for the operation of
various types of bodies performing inspection
[14] JIS Q 17021-1 適合性評価−マネジメントシステムの審査及び認証を行う機関に対する要求事項−
第1部:要求事項
注記 対応国際規格:ISO/IEC 17021-1,Conformity assessment−Requirements for bodies providing
audit and certification of management systems−Part 1: Requirements
[15] JIS Q 17034 標準物質生産者の能力に関する一般要求事項
注記 対応国際規格:ISO 17034,General requirements for the competence of reference material
producers
[16] JIS Q 17043 適合性評価−技能試験に対する一般要求事項
注記 対応国際規格:ISO/IEC 17043,Conformity assessment−General requirements for proficiency
testing
[17] JIS Q 17065 適合性評価−製品,プロセス及びサービスの認証を行う機関に対する要求事項
注記 対応国際規格:ISO/IEC 17065,Conformity assessment−Requirements for bodies certifying
products, processes and services
[18] ISO 17511,In vitro diagnostic medical devices−Measurement of quantities in biological samples−
Metrological traceability of values assigned to calibrators and control materials
[19] JIS Q 19011 マネジメントシステム監査のための指針
注記 対応国際規格:ISO 19011,Guidelines for auditing management systems
[20] JIS Z 8404-1 測定の不確かさ−第1部:測定の不確かさの評価における併行精度,再現精度及び真
度の推定値の利用の指針
注記 対応国際規格:ISO 21748,Guidance for the use of repeatability, reproducibility and trueness
estimates in measurement uncertainty evaluation
[21] JIS Q 31000 リスクマネジメント−原則及び指針
注記 対応国際規格:ISO 31000,Risk management−Principles and guidelines
[22] JIS Q 0030 標準物質に関連して用いられる用語及び定義
注記 対応国際規格:ISO Guide 30,Reference materials−Selected terms and definitions
[23] JIS Q 0031 標準物質−認証書,ラベル及び附属文書の内容
注記 対応国際規格:ISO Guide 31,Reference materials−Contents of certificates, labels and
accompanying documentation
[24] JIS Q 0033 認証標準物質の使い方
注記 対応国際規格:ISO Guide 33,Reference materials−Good practice in using reference materials
[25] JIS Q 0035 標準物質−認証のための一般的及び統計的な原則
注記 対応国際規格:ISO Guide 35,Reference materials−Guidance for characterization and assessment
of homogeneity and stability
[26] ISO Guide 80,Guidance for the in-house preparation of quality control materials (QCMs)
[27] ISO/IEC Guide 98-3,Uncertainty of measurement−Part 3: Guide to the expression of uncertainty in
measurement (GUM:1995)
[28] ISO/IEC Guide 98-4,Uncertainty of measurement−Part 4: Role of measurement uncertainty in conformity
assessment
28
Q 17025:2018 (ISO/IEC 17025:2017)
[29] IEC Guide 115,Application of uncertainty of measurement to conformity assessment activities in the
electrotechnical sector
[30] Joint BIPM, OIML, ILAC and ISO declaration on metrological traceability, 2011 2)
[31] International Laboratory Accreditation Cooperation (ILAC) 3)
[32] International vocabulary of terms in legal metrology (VIML), OIML V1:2013
[33] JCGM 106:2012,Evaluation of measurement data−The role of measurement uncertainty in conformity
assessment
[34] The Selection and Use of Reference Materials, EEE/RM/062rev3, Eurachem 4)
[35] SI Brochure: The International System of Units (SI), BIPM 5)
注2) http://www.bipm.org/utils/common/pdf/BIPM-OIML-ILAC-ISO̲joint̲declaration̲2011.pdf
3) http://ilac.org/
4) https://www.eurachem.org/images/stories/Guides/pdf/EEE-RM-062rev3.pdf
5) http://www.bipm.org/en/publications/si-brochure/