K 3701:2008
(1)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
まえがき
この規格は,工業標準化法第12条第1項の規定に基づき,財団法人バイオインダストリー協会(JBA)及
び財団法人日本規格協会(JSA)から,工業標準原案を具して日本工業規格を制定すべきとの申出があり,日
本工業標準調査会の審議を経て,経済産業大臣が制定した日本工業規格である。
この規格は,著作権法で保護対象となっている著作物である。
この規格の一部が,特許権,出願公開後の特許出願,実用新案権又は出願公開後の実用新案登録出願に
抵触する可能性があることに注意を喚起する。経済産業大臣及び日本工業標準調査会は,このような特許
権,出願公開後の特許出願,実用新案権又は出願公開後の実用新案登録出願に係る確認について,責任は
もたない。
K 3701:2008
(2)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
目 次
ページ
序文 ··································································································································· 1
1. 適用範囲 ························································································································ 1
2. 引用規格 ························································································································ 1
3. 定義 ······························································································································ 2
4. 試験施設 ························································································································ 2
4.1 試験区域 ······················································································································ 2
4.2 その他の区域 ················································································································ 2
4.3 施設の位置 ··················································································································· 3
4.4 施設の準備 ··················································································································· 3
4.5 保守点検 ······················································································································ 3
5. 設備及び機器 ·················································································································· 4
5.1 培地操作用キャビネット ································································································· 4
5.2 はかり ························································································································· 4
5.3 ホモジナイザー ············································································································· 4
5.4 pH計··························································································································· 5
5.5 オートクレーブ ············································································································· 5
5.6 インキュベーター ·········································································································· 5
5.7 冷蔵庫 ························································································································· 6
5.8 冷凍庫 ························································································································· 6
5.9 恒温水槽 ······················································································································ 6
5.10 オーブン ····················································································································· 7
5.11 電子レンジ ·················································································································· 7
5.12 光学顕微鏡 ·················································································································· 7
5.13 ガスバーナー又は白金線滅菌器 ······················································································· 7
5.14 培地及び試薬分注器 ······································································································ 7
5.15 かき混ぜ機 ·················································································································· 7
5.16 コロニー計数器 ············································································································ 8
5.17 環境を変えて培養する装置 ····························································································· 8
5.18 その他の器具 ··············································································································· 8
6. 作業者 ··························································································································· 8
6.1 適格性 ························································································································· 8
6.2 衛生 ···························································································································· 8
7. 器具の準備 ····················································································································· 8
7.1 滅菌 ···························································································································· 9
7.2 使い捨て器具 ················································································································ 9
K 3701:2008 目次
(3)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
ページ
7.3 清浄な器具の管理 ·········································································································· 9
7.4 滅菌済みの器具の管理 ···································································································· 9
7.5 汚染除去 ······················································································································ 9
7.6 洗浄 ···························································································································· 9
8. 培地の調製及び滅菌 ········································································································· 9
8.1 培地の調製 ·················································································································· 10
8.2 試薬及び培地の滅菌 ······································································································ 10
8.3 保存 ··························································································································· 10
8.4 寒天培地の融解 ············································································································ 11
8.5 培地の脱気 ·················································································································· 11
8.6 シャーレにおける寒天平板培地の調製 ············································································ 11
9. 試料 ····························································································································· 11
9.1 試料の採取 ·················································································································· 11
9.2 輸送 ··························································································································· 11
9.3 受領及び保存 ··············································································································· 11
9.4 試験試料 ····················································································································· 12
9.5 試料の保存及び廃棄 ······································································································ 12
10. 試験方法及び試験結果の表記··························································································· 12
10.1 予防措置 ···················································································································· 12
10.2 試料懸濁液及び希釈系列の調製 ······················································································ 13
10.3 固形培地の試験 ··········································································································· 13
10.4 液体培地の試験(最確数法) ························································································· 19
10.5 検出試験法 ················································································································· 21
10.6 基本的な同定法 ··········································································································· 22
附属書A(規定)推定数の信頼区間 ························································································ 25
附属書B(規定)最確数(MPN)表 ························································································ 27
附属書1(参考)JISと対応する国際規格との対比表 ·································································· 30
K 3701:2008
(4)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
白 紙
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
日本工業規格 JIS
K 3701:2008
培地の試験方法−通則
Culture media-General rules for microbiological examinations
序文 この規格は,1996年に第1版として発行されたISO 7218:1996,Microbiology of food and animal feeding
stuffs−General rules for microbiological examinations及びAMENDMENT 1(2001)を翻訳し,技術的内容を変
更して作成した日本工業規格である。ただし,追補(AMENDMENT)については,編集し,一体とした。
なお,この規格で点線の下線を施してある箇所は,原国際規格を変更している事項である。変更の一覧
表をその説明を付けて,附属書1(参考)に示す。
1. 適用範囲 この規格は,微生物の検出を目的とする培地試験の通則について規定する。
備考 この規格の対応国際規格を,次に示す。
なお,対応の程度を表す記号は,ISO/IEC Guide 21に基づき,IDT(一致している),MOD
(修正している),NEQ(同等でない)とする。
ISO 7218:1996,Microbiology of food and animal feeding stuffs−General rules for microbiological
examinations,and AMENDMENT 1(MOD)
2. 引用規格 次に掲げる規格は,この規格に引用されることによって,この規格の規定の一部を構成す
る。これらの引用規格は,その最新版(追補を含む。)を適用する。
JIS B 9922 クリーンベンチ
JIS K 3702 培地の試験方法−試料懸濁液及び希釈系列の調製方法
備考 ISO 6887-1:1999,Microbiology of food and animal feeding stuffs−Preparation of test samples,
initial suspension and decimal dilutions for microbiological examination−Part 1: General rules for
the preparation of the initial suspension and decimal dilutionsからの引用事項は,この規格の該当
事項と同等である。
JIS K 3703-1 コアグラーゼ陽性ブドウ球菌(黄色ブドウ球菌など)の菌数測定方法−第1部:ベアー
ド・パーカー寒天培地
JIS K 3703-2 コアグラーゼ陽性ブドウ球菌(黄色ブドウ球菌など)の菌数測定方法−第2部:ウサギ
血しょう(漿)フィブリノーゲン寒天培地
JIS K 3703-3 コアグラーゼ陽性ブドウ球菌(黄色ブドウ球菌など)の菌数測定方法−第3部:低菌数
の検出法及び最確数(MPN)法による生菌数測定法
JIS K 3704 培地の試験方法−大腸菌用検出培地
JIS K 3705 培地の試験方法−サルモネラ属菌用培地−サルモネラ属菌の検出
JIS K 3706-1 培地の試験方法−リステリア・モノサイトゲネス用培地−第1部:リステリア・モノサ
イトゲネスの検出
2
K 3701:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
JIS K 3706-2 培地の試験方法−リステリア・モノサイトゲネス用培地−第2部:リステリア・モノサ
イトゲネスの生菌数測定
JIS K 3800 バイオハザード対策用クラスⅡキャビネット
JIS K 8008 生化学試薬通則
JIS K 8102 エタノール(95) (試薬)
JIS K 8180 塩酸 (試薬)
JIS K 8230 過酸化水素 (試薬)
JIS K 8294 クリスタルバイオレット (試薬)
JIS K 8521 しゅう酸アンモニウム一水和物 (試薬)
JIS K 8576 水酸化ナトリウム (試薬)
JIS K 8913 よう化カリウム (試薬)
JIS K 8920 よう素 (試薬)
JIS T 7322 医療用高圧蒸気滅菌器
JIS T 7324 医療用小型高圧蒸気滅菌器
JIS Z 8802 pH測定方法
3. 定義 この規格で用いる主な用語の定義は,次による。
3.1
精製水 JIS K 8008の3.2(水)に規定するA2の水。
備考 これを超える精製度のものを使用することに関しては制限しない。
3.2
エタノール(95) JIS K 8102に規定するもの。
3.3
塩酸 JIS K 8180に規定するもの。
3.4
過酸化水素 JIS K 8230に規定するもの。
3.5
クリスタルバイオレット JIS K 8294に規定するもの。
3.6
しゅう酸アンモニウム一水和物 JIS K 8521に規定するもの。
3.7
水酸化ナトリウム JIS K 8576に規定するもの。
3.8
よう化カリウム JIS K 8913に規定するもの。
3.9
よう素 JIS K 8920に規定するもの。
4. 試験施設
4.1
試験区域 培地試験施設において特定の操作に必要な区域を,次に示す。
− 試料の搬入,保存,調製及び処理
− 培地の調製及び器具の準備,並びに滅菌
− 分析操作:ひょう量,希釈,接種,継代培養,培養,菌株の保存など
− 器具の汚染除去及び洗浄,並びに分析廃棄物の処理
4.2
その他の区域 次に例示する。
− 入り口,廊下,階段,業務用リフト又はエレベーター
− 業務管理区域(秘書室,事務室,資料作成室など)
− 更衣室及びトイレ
− 資料保管室
− 物品庫
3
K 3701:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
4.3
施設の位置 微生物学的分析を行う施設の環境によって,試験の信頼性が影響されてはならない。
交差汚染の危険性の回避に留意して,施設を配置する。施設内部は,一方通行とする。過度の温度,粉じ
ん,湿度,蒸気,騒音,振動,直射日光など,極端な状態にならないように保護する。作業区域は,十分
な広さの面積とし,清潔,かつ,整とんされた状態とする。すべての試験施設は,分析者1人当たり約20
m2の作業場を確保することが望ましい。試験中の試験区域への立ち入りは,試験実施担当者だけに制限す
る。
次の操作に対しては,隔離した部屋及び/又は区域を設けるか,若しくは特定の囲いを設置する。
− 試料の搬入及び保存
− 試料の調製,特に原材料を扱う場合(多数の微生物を含む粉末試料など)
− 病原菌の取り扱い(サルモネラ,リステリア・モノサイトゲネスなど)
− 培地の調製及び器具の準備,並びに滅菌
− ガラス器具及び他の器具の洗浄,並びに器具及び汚染した培地の汚染除去
− 食品の無菌試験
次の区域も隔離する。
− 培地の調製に用いる区域,培地及び器具の滅菌に用いる部屋
− 汚染除去区域及び洗浄区域
インキュベーター,冷蔵庫及び冷凍庫は,特にその用途に適した専用の部屋に設置する。
4.4
施設の準備
4.4.1
試験施設は,粉じん及び粉じんが介する微生物による汚染の危険性を軽減するため,次のように整
備する。
− 壁,天井及び床は,平たんで清掃が容易であり,試験施設で用いる洗浄剤及び消毒剤に対して耐久
性があるもの。
− 頭上に設置する送液管が,施設間をまたがる場合は,(管と壁とのすき間を)密封しなければなら
ない。
− 窓の外側に,特別な場合を除き,直射日光に対する保護システムを取り付ける。
− 通風しないように,窓及び扉は試験実施時に密閉する。窓及び扉は,ほこりだまりを形成しないよ
うな構造とし,容易に清掃できるように設計する。
4.4.2
周囲温度及び空気の清浄度(微生物含有量,湿度,粉じん拡散率など)が試験に適合していなけれ
ばならない。フィルター換気システムを用いて,空気は取り込むことが望ましい。低汚染環境で試験する
場合は,JIS B 9922に規定するクリーンベンチ及び/又はJIS K 3800に規定するバイオハザード対策用ク
ラスⅡキャビネットを設置する。
4.4.3
試験作業台の上面及び備品は,洗浄及び消毒が容易な,平たんで不浸透性の材質で製作する。粉じ
んの蓄積を防止するため,戸棚は天井に届いているのが望ましい。試験室の備品は可動式とし,床は容易
に洗浄できなければならない。試料,培地,試薬などの文書を保管する密閉式の設備を備える。
備考 使用頻度の低い文書又は書物は,試験区域外に置くことが望ましい。
4.4.4
試験施設の照明は,障害となる反射光を排するように設置する。作業場及び影響を受けやすい装置
(特に,インキュベーター)は,直射日光を避けることが望ましい。
4.5
保守点検 床,壁,天井,試験作業台上及び備品は,汚物が蓄積して汚染源となるようなき裂の発
生を避けるため,定期的に保守点検し修復する。試験に適した状態に施設を維持するために,定期的に洗
浄及び消毒を行う。空調設備とそのフィルターは定期的に保守管理し,必要に応じてフィルターを交換す
4
K 3701:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
る。各設備の表面及び空気は微生物学的に定期的にモニターする。表面汚染は,適切な不活化剤を含む接
触板を直接接触させることによって点検する。空気は,標準寒天培地などの非選択寒天培地を入れたシャ
ーレを,ふたを開けたまま15分間放置して点検する。
備考 表面汚染及び空気汚染を点検するために他の方法を用いてもよい。
5. 設備及び機器 設備及び機器は,すべて清潔にして良好な作動状態とする。保守作業はモニターし,
監視機器は定期的に点検する。
5.1
培地操作用キャビネット 培地操作用キャビネットは,水平又は垂直層流式の粉じん除去作業台で
構成する。安全キャビネットでは,粒径0.5 μmを超える粒子数が1 m3当たり4 000個を超えてはならない。
病原菌の培地試験は,JIS K 3800に規定するバイオハザード対策用クラスⅡキャビネットを用いて実施し
なければならない。
5.1.1
保守点検 バイオハザード対策用クラスⅡキャビネットは,搬入時及び設置後,有資格者が点検す
る。毎年点検することが望ましい。プレフィルターを備えたキャビネットの場合は,プレフィルターを定
期的に交換する。キャビネットは使用後に洗浄消毒する。キャビネットの作業面及び壁面を点検し,定期
的に微生物汚染の有無を確認する。通常の試験器具を用いて,存在する微生物の割合を定期的に確認する。
例えば,標準寒天培地などの非選択寒天培地を入れたシャーレ数枚を,各キャビネットの中でふたを開け
たまま30分間放置して点検する。このほかの方法を用いてもよい。
5.2
はかり
5.2.1
用途及び使用法 試験施設には,試料,培地成分及び試薬をひょう量するために用いるはかりを設
置する。はかりのひょう量精度は±0.01 g及び±0.000 1 gの2種類とする。はかりは,希釈液の体積を質
量によって測定する場合に用いてもよい。
5.2.2
保守点検 はかりは,安定した水平な台の上に置き,防振措置を施す。標準分銅を用いて校正する
(各作業日に実施することが望ましい。)。年1回以上,有資格者が全ひょう量範囲を試験する。はかり皿
は,必要に応じて使用の都度,また,使用後少なくとも1日1回は清掃する。また,年1回以上,有資格
者が機械部分を清掃し点検する。
5.3
ホモジナイザー 液状以外の試料から試料懸濁液(1次希釈試料液)を調製するために用いる機器。
機器は,次による。
− 無菌のプラスチック袋を備えたぜん(蠕)動式で,可能であれば速度及び時間を調節できるもの。
− 回転式で回転速度が8 000から45 000 rpmであり,ふた付きで,滅菌可能なガラス製又は金属製容
器を備えているもの。
適切な外径の滅菌可能なガラスビーズ(直径約6 mm,個別の規格参照)を用いて均質化してもよい。
5.3.1
用途及び使用法 ぜん動式ホモジナイザーの通常の運転時間は1〜2分間である。この種類のホモ
ジナイザーは,次のような試料には用いない。
− 鋭利な小片,硬質な小片又は乾燥した小片を含み,袋を破損させるおそれのあるもの。
− サラミソーセージなど生地のために均質化が困難なもの。
回転式ホモジナイザーは,回転数(の累計)が15 000〜20 000 回となるまで運転を継続しなければなら
ない。最低速のホモジナイザーを用いる場合でも運転時間は,2.5分間を超えてはならない。
粘性のある製品又は濃厚な製品,特にある種の乳製品(個別の規格を参照)を振とう(盪)によって一
次懸濁して調製する場合には,ガラスビーズを用いてもよい。
5.3.2
保守点検 個々の機器は,その製造業者の取扱説明書に従って保守点検する。
5
K 3701:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
5.4
pH計 JIS Z 8802に規定するpH計の形式Ⅲによる。測定電極と参照電極とを試料の中に入れ,規
定温度で両電極間の電位差を測定するもの。精度±0.1 pH,分解能0.01 pHで,手動又は自動温度平衡機能
を備えたものでなければならない。
5.4.1
用途及び使用法 pH計は,各バッチの培地などのpHを測定し,調節が必要であるかを調べるた
めに用いる。試料又は試料原液のpHを測定し,調節するためにも用いる。
5.4.2
保守点検 pH計は,製造業者の取扱説明書に従い,2種類以上のpH標準緩衝液を用いて,使用前
に1日1回以上,校正する。pH標準液のpHは測定温度で小数第2位まで既知とする(通常は20 ℃でpH
4.00及び7.00。)。試料のpHは,pH標準液のpHの範囲内でなければならない。
pH計の電極は,製造業者の取扱説明書に従って保守点検を行う。次の点について定期的にモニターする。
− 電極の劣化及び汚れの状態
− 応答時間及び安定性
使用前に電極のガラス測定端は,精製水又は製造業者が推奨する他の液体に完全に浸っていることを確
認する。そうでない場合は,測定前に24時間浸す。使用後,必ず精製水又は製造業者が推奨する他の液体
で電極を洗浄する。電極の汚れ及び劣化を考慮し,定期的に製造業者の取扱説明書に従って十分に精製水
又は製造業者が推奨する他の液体で洗浄する。製造業者の取扱説明書に従って電極を保管する。
5.5
オートクレーブ JIS T 7322(又はJIS T 7324)に規定するもの。微生物を殺菌するために必要な
121 ℃以上の飽和蒸気温度が得られる機器。
5.5.1
用途・使用法 清浄な器具・培地の滅菌と使用済みの器具・培地の汚染除去を,同じ滅菌工程で同
時に高圧蒸気滅菌してはならない。これらの二つの処理には,別のオートクレーブを用いることが望まし
い。オートクレーブは,次の部品を備える。
− 一つ以上の安全弁
− 圧力計
− 排水弁
− 設定値の±1 ℃以内に温度を維持する制御装置
− 温度計又は熱電対
時間表示器又はプログラムタイマーを備えていることが望ましい。蒸気滅菌では,圧力が上昇する前に
すべての空気が排出されなければならない。オートクレーブに自動排気装置が取り付けられていない場合
には,蒸気噴流が連続的に排出されるまで空気を除去する。
5.5.2
保守点検 オートクレーブは,完全な稼動状態に維持し,製造業者の取扱説明書に従って定期的に
点検する。すべての監視装置を完全な作動状態に維持し,定期的に確認する。必要に応じて湯あか(垢)
を落とし,定期的に排液を処理する。
5.6
インキュベーター インキュベーターは,温度を安定に維持し,全体を±1 ℃以内に均一に保つこと
が可能なものとする。
5.6.1
用途及び使用法 インキュベーターは,使用容積全体にわたり温度を均一,かつ,安定に維持する
調節装置を備えていなければならない。周囲温度がインキュベーターの温度と同等又はそれ以上である場
合には,冷却装置を取り付ける。インキュベーターの壁面は直射日光から保護する。インキュベーターは,
単一の操作において一杯にして使用しない方がよい。どのようなタイプのインキュベーター(強制対流形
など)を用いても,培地の温度が平衡になるまで時間がかかるためである。インキュベーター使用中は,
インキュベーター内部の空気の循環に注意する。インキュベーターの内壁から25 mm以内にシャーレ又は
試験管を置いてはならない。シャーレは6枚以上積み重ねない。重ねたシャーレは互いに,25 mm以上離
6
K 3701:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
さなければならない。
5.6.2
保守点検 数個の温度計又は熱電対を用いて,使用容積内の温度が均一であることを点検する。測
定器の測定精度は,要求される精度の4倍以上とする(要求される精度が±2 ℃であれば,測定精度は
±0.5 ℃以上とする。)。一つ以上の最高最低温度計を用いて,温度の安定性を点検する。インキュベーター
の温度は,作業日ごとに点検する。インキュベーターの内壁及び外壁は定期的に洗浄及び消毒し,換気装
置のじんあいを除去する。
5.7
冷蔵庫 確実に低温保存できる装置又は設備。温度は3±2 ℃とする。分析用試料の保存に用いる場
合は,2±2 ℃に維持できなければならない。
5.7.1 用途及び使用法 次の保存には,それぞれ特定の冷蔵庫又は低温保存室を用意する。
− 菌を接種していない培地及び試薬
− 分析用試料
− 菌株及び菌を接種した培地
冷蔵庫及び低温保存室を置く場所は,適切な空気循環が維持されなければならない。
5.7.2
保守点検 冷蔵庫及び低温保存室の温度は,作業日ごとに点検する。
次の保守作業を定期的に実施する。
− 回転翼又は外部熱交換板に付着したじんあいの除去
− 霜取り
− 庫内及び保存室内の洗浄及び消毒
5.8
冷凍庫 確実に凍結保存できる装置又は設備。温度は−18 ℃以下でなければならない。−24±2 ℃
に維持できることが望ましい。
5.8.1
用途及び使用法 次の保存には,それぞれ特定の冷凍庫を用意する。
− 菌を接種していない培地及び試薬
− 分析用試料
− 菌株
凍結していない試料を冷凍庫に入れる場合には,事前に庫内の温度を十分低温に維持する。
5.8.2
保守点検 各冷凍庫の温度は,作業日ごとに点検する。
次の保守作業を定期的に実施する。
− 回転翼又は外部熱交換板に付着したじんあいの除去
− 霜取り
− 庫内の洗浄及び消毒
5.9
恒温水槽 規定温度に維持することが可能な水槽。精度は±0.5 ℃でなければならない。
5.9.1
用途及び使用法 主な用途は,次のとおりである。
− 滅菌済みの融解した寒天培地を用途に適した温度に保温する。
− 菌を接種した培地を一定温度で培養する。
− 試料原液を制御温度で調製する。例えば,カゼイン塩を加えた試料原液の調製では,最後に37 ℃
の恒温水槽で15分間保温する。
− 試料原液を制御温度で加熱処理する。
正確な温度制御のためには,循環水流ポンプ及び自動加熱制御装置が恒温水槽に装備されていなければ
ならない。液体のかき混ぜによって液滴を飛散させてはならない。
5.9.2
保守点検 各恒温水槽には,それぞれ専用の温度計又は熱電対を取り付ける。恒温水槽の温度は,
7
K 3701:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
使用時ごとに点検する。毎日実施することが望ましい。恒温水槽内の水又は1,2−エタンジオール(エチ
レングリコール)などの液量は,定期的に点検する。微生物の増殖を防ぐため,恒温水槽内の液体は頻繁
に交換する。
5.10 オーブン 170〜180 ℃の乾燥空気で微生物を滅菌する装置。
5.10.1 用途及び使用法 オーブンで滅菌するものは,金属製の器具又はガラス器具に限定する。設定温度
に達した後,1時間以上その温度に維持する。
警告 体積の測定に用いるガラス器具はオーブンで滅菌してはならない。
オーブンは内部の温度は均一で,次のものを備えている。
− サーモスタット
− 温度計又は熱電対
時間表示器又はプログラム・タイマを備えていることが望ましい。
5.10.2 保守点検 内部の温度が均一であることを点検する。オーブンを完全な稼動状態に維持し,定期的
に監視装置を点検する。定期的に洗浄することが望ましい。
5.11 電子レンジ マイクロ波を用いて試料を加熱する装置。
5.11.1 用途及び使用法 寒天培地の融解に用いる。マイクロ波を試料に対して均一に照射し,試料の部分
過熱を防止する。試料を均一に加熱するためには,試料を回転させる仕組みを備えた装置を用いるとよい。
警告 電子レンジで加熱した寒天培地は,加熱操作終了後,しばらくしてから突然,沸騰することが
あるため,取り扱いに注意する。
備考 電子レンジによる培地の滅菌は,マイクロ波の有効性が十分確認されていないため,この規格
では適用しない。
5.12 光学顕微鏡
5.12.1 用途及び使用法 高倍率の油浸対物レンズを用いると,水性懸濁液中又は染色後の微生物の形態を
観察できる。位相差対物レンズ及び集光器付きであることが望ましい。
備考 寒天培地の表面又は培地中に存在する細菌のコロニー試験には,低倍率の顕微鏡の実体顕微鏡
(培養顕微鏡)を用いることが望ましい。
5.12.2 保守点検 油浸レンズの使用後は,光学的特性に影響を及ぼさないように,レンズを清掃する。年
1回以上,責任者が清掃作業を実施し,機械系及び光学系を点検する。
5.13 ガスバーナー又は白金線滅菌器 ガスバーナーは,火炎周囲に無菌空間をつくり出し,維持するた
めに用いる。白金線滅菌器は白金線及びループを赤熱させて滅菌するために用いる。病原菌を扱った後に
白金線又はループを滅菌する場合には,白金線滅菌器の使用が望ましい。
5.14 培地及び試薬分注器 メスシリンダー,手動注射器,自動注射器,ぜん動ポンプなど,培地及び試
薬を試験管,瓶又はシャーレに分注するために用いる器具又は装置をいう。
5.14.1 用途及び使用法 滅菌した培地及び試薬を無菌的に分注する場合には,分注するものと接する器具
又は装置の全部分を滅菌する(7.1参照)。
器具又は装置の精度は,分注する容量の精度に適したものでなければならない。10倍段階希釈系列の調
製(JIS K 3702参照)に用いる希釈液の分注精度は±2 %とする。
5.14.2 保守点検 これらの器具は,製造業者の取扱説明書に従って良好な状態に維持する。分注量は定期
的に確認する。
5.15 かき混ぜ機 液体を偏心回転運動させて,10倍段階希釈系列及び液体試料など種々の液体又は細菌
細胞の一次懸濁液を均一に混合する装置。
8
K 3701:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
5.16 コロニー計数器 背景が黒い照明装置,拡大率が1.5倍以上の拡大鏡及び機械式又は電子式のデジタ
ルカウンタを備えていることが望ましい。レーザーカウンターなど,同等の効率であれば他の自動計数装
置を用いてもよい。
5.17 環境を変えて培養する装置 嫌気性の条件下など通常と異なる環境を,全培養期間を通して維持で
きる密閉可能な容器又は他の適切な装置。同等の性能であれば,他の装置を用いてもよい。取り付け及び
保守は製造業者の取扱説明書に従う。
5.17.1 用途及び使用法 ガスボンベなどから供給される混合ガス又は市販のガスパックなど他の適切な
方法で得られる環境雰囲気の組成については,それを規定した規格による。
5.17.2 保守点検 使用時には,雰囲気の性質を監視する表示器を各容器内に設置する。触媒を用いる場合
には,製造業者の取扱説明書に従って定期的に触媒を再生する。定期的に洗浄及び消毒する。
5.18 その他の器具 日常的に用いるその他の器具及び装置には,ろ過器,ガラス製又はプラスチック製
の容器(試験管,フラスコ及び瓶),ガラス製又はプラスチック製のシャーレ(外径90〜100 mm),ガ
ラス製又はプラスチック製のパスツールピペット(10 mL,2 mL及び1 mL),試料採取装置,白金線及び
ニッケルクロム製ループ,白金イリジウム製ループ,使い捨てのプラスチック製ループなどがある。
6. 作業者
6.1
適格性 培地試験を実施する施設で働く作業者は,適切な教育訓練を受けることが望ましい。培地
試験の担当者は,培地試験方法及び微生物自体について,豊富な知識及び十分な実務経験がなければなら
ない。
6.2
衛生 試料及び培地の汚染,作業者の感染の危険性を回避するため,次の予防措置を講じる。
− 淡色,かつ,清潔で ほころびがなく,引火の危険性を抑えた布地で製造した試験作業着を着用する。
この作業着は作業区域外では着用しない。更衣室でも着用しない。
− 頭髪及びあごひげに対しても保護具を着用する。
− つめ(爪)は完全に清潔にして十分に整え,短くしておくことが望ましい。
− 培地試験の前後及び用便直後は,液状石けん又は粉石けんを用いて30〜40 ℃の温水で十分に手を
洗う。適切な清浄度に維持されたディスペンサーから供給される消毒剤を用いることが望ましい。
手を使わない自動感知式の蛇口から給水することが望ましい。手をふ(拭)く場合には,使い捨て
の紙又は布タオルを用いる。
− 菌の接種時には,会話及びせき(咳)などをしない。
− 試験区域では喫煙及び飲食をしない。
− 感染症[ひょうそ(疽)]又は微生物が試料を汚染し試験結果を無効にする可能性がある疾患にり
(罹)患している作業者は,特別な予防措置を講じる。
− 試験室の冷蔵庫には,作業者の飲食に供する食品を置かない。
7. 器具の準備 培地試験で用いる器具は,使用時までにその清浄度及び/又は無菌性を保証するような
方法で準備しなければならない。器具は,新品であっても使用前に洗浄する。試験管及び瓶は,滅菌前に,
綿栓,金属栓,プラスチック栓など適切な方法で施栓しておく。パスツールピペットは,綿栓又は他の適
切な材料で施栓する。滅菌する器具は必要に応じて特殊容器に入れるか,専用紙,アルミニウムはくなど
適切な材料で包む。培地又は他の水溶液を入れずに空のままで容器を高圧蒸気滅菌する場合には,蒸気を
均一に接触させる。
9
K 3701:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
7.1
滅菌
7.1.1
乾熱滅菌 乾熱滅菌は,5.10に規定するオーブンを用いて,170〜180 ℃で1時間以上加熱する。
7.1.2
湿熱滅菌 湿熱滅菌は,5.5に規定するオートクレーブを用いて,121 ℃以上で少なくとも15分間
加熱する。真空乾燥装置を備えたものが望ましい。設定温度に達したことを確認するため,温度表示ラベ
ルなどを用いる。
7.2
使い捨て器具 使い捨て器具を用いてもよい。この場合は,製造業者に照会し,培地試験,特に無
菌性での使用に適しており,その材料に微生物の発育を阻止する物質が含まれていないことを確認する。
使い捨て器具は,廃棄する前に汚染を除去する。
7.3
清浄な器具の管理 清浄な器具を保管する場合には,その清浄度が維持される条件でじんあいから
保護する。
7.4
滅菌済みの器具の管理 滅菌済みの器具は,使用するまで無菌性が維持される条件で保管する。使
い捨て器具は,製造業者の仕様書に従って,包装が劣化しないように保管する。試験室で作製した器具は,
清浄な容器に保管する。培地試験に用いる器具を滅菌する場合には,各包装の上に使用期限又は製造年月
日を表示する。密閉した器具は,使用まで最長3か月間保管できる。密閉包装していない器具の保管期間
は,より短期間(例えば8日間)とする。
7.5
汚染除去 微生物の培養器具又は微生物と接触した器具類を用いた後は,微生物の種類に関係なく,
洗浄又は廃棄する前に器具及びその内容物の汚染を除去する。例えば,綿栓は,パスツールピペットの汚
染を除去した後,取り外す。液体培地を入れた試験管は,洗浄前に汚染を除去する。
汚染の除去は,次に示す二つの方法のいずれかによって実施する。
− 培養した固形培地又は液体培地,汚染した試薬及び器具類など,培養微生物と接触した物品はすべ
て,5.5に規定するオートクレーブを用いて121 ℃以上で30分間以上,湿熱滅菌する。
− パスツールピペットなど,小形で耐食性の器具は消毒剤に浸して汚染を除去する。パスツールピペ
ットは1回で使い切りとする。
7.6
洗浄 器具を洗浄する前に汚染を除去する。容器の内容物は空にする。洗浄前に栓又はふたからシ
ールをはがす。洗剤を用いて,栓,ふた及びガラス器具を温水で注意深く洗浄する。市販の洗剤がない場
合には,炭酸ナトリウム溶液(1.25 g/L)で処理した後,塩酸(0.1 mol/L)などの酸に浸す。洗浄操作を容易に
するため,パスツールピペット洗浄器,皿洗い機,超音波槽などの専用機器を用いてもよい。器具はすべ
て,精製水(3.1)ですすぐ。
8. 培地の調製及び滅菌 培地の調製は培地試験の重要な操作の一つである。特に注意して,調製しなけ
ればならない。
用いる水は,精製水(3.1)若しくは蒸留水又は蒸留水と同等の品質とする。試験条件下で,微生物の増
殖を抑制又は増殖に影響する物質を含まない水とする。蒸留水を塩素を含む水から調製する場合は,蒸留
の前に塩素を中和する必要がある。蒸留水は,不活性な材料(例えば,ガラス,ポリエチレンなど)から
なり,阻害性の物質を含まない容器に貯蔵する。
備考1. 溶解した二酸化炭素を含まない作りたての蒸留水をもちいなければならない場合がある。
3 000 000 Ω以上の電気抵抗の水は,高純水とみなせる。
2. イオン交換樹脂を通して金属を除いた水は,高濃度の微生物を含む場合がある。水中の微生
物含有量が少ないことが保証されない限り,イオン交換樹脂による金属の除去操作は行わな
い方がよい。微生物含有量を最少にする方法は,製造業者の指示による。フィルター滅菌の
10
K 3701:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
後で,微生物に汚染されたイオン除去水は,ある種の微生物の増殖を抑える物質を含むこと
がある。
8.1
培地の調製 次の2種類の調製方法による。
− 乾燥品か否かを問わず,基本成分から調製する。
− 粉末完全培地から調製する。
粉末基本成分又は粉末完全培地を入れた瓶は遮光し,乾燥した場所で製造業者が指定する温度で保存す
る。記載された保存期間を超えたものは用いない。粉末成分及び粉末培地は吸湿性があるため,使用後は,
直ちに密栓する。粘結又は凝固の徴候が認められ,吸水したと考えられる粉末培地は用いてはならない。
8.1.1
復水 復水は,個別の規格が存在しない場合,当事者間の合意による。
8.1.2
pH測定 pHは,5.4に規定するpH計を用いて測定し,必要に応じて調節する。滅菌して25 ℃に
冷却した後,所定のpHの±0.2以内になるように滅菌前にpH調節を行う。通常は,水酸化ナトリウム溶
液(1 mol/L)(95 %水酸化ナトリウム40 gを水に溶かして1 Lとする。)又は塩酸(1 mol/L)(35 %塩酸90 mL
を水に溶かして1 Lとする。)を用いて調節する。
8.1.3
分注 5.14で規定する手動又は自動装置を用いて,培地を適切な容器に分注する。分注量の1〜3
倍の容量をもつ容器を用いる(高圧蒸気滅菌中に培地が沸騰してあふれるのを防ぐ。)。
8.2
試薬及び培地の滅菌 次による。
− 水蒸気で加熱して滅菌する。
− ろ過して滅菌する。
当事者間の協定によって,その他の方法で滅菌してもよい。滅菌操作をしないで用いることができる培
地及び試薬もある。培地は,滅菌後,pH,色,無菌性及び細菌学的性能に関して監視する。
8.2.1
湿熱による滅菌 5.5に規定する専用のオートクレーブ又は培地調製器及び分注器の中で行う。オ
ートクレーブの場合は,水蒸気を用いて121 ℃で15分間必要である。容量が1 Lを超える場合には,必要
に応じて滅菌サイクルを調節する。いずれの場合も関連規格及び/又は製造業者の指示に従う。高圧蒸気
滅菌を行う前に,5.5に規定するオートクレーブの各段を代表する数の容器に,必要温度に達したことを示
す市販の滅菌テープをはる。
8.2.2
ろ過による滅菌 この操作は減圧又は加圧条件下で行う。孔径0.22 μmのメンブレンフィルター及
びろ過器を用いる。使用前に5.5に規定するオートクレーブで滅菌しておく。無菌状態で購入したろ過器
又はメンブレンフィルターの使用に関しては,製造業者の取扱説明書を参照する。組立式か否かに関係な
く,ろ過器の各部品は,5.5に規定するオートクレーブを用いて121 ℃で15分間滅菌する。必要に応じて,
蒸気滅菌後に安全キャビネット内で無菌的に組み立てる。
無菌状態で購入することができるろ過器又はメンブレンフィルターもある。
8.3
保存 瓶,試験管及びシャーレの各包装にラベルをはり,次の詳細事項を記載する。
− 培地の名称
− 調製日及び/又は使用期限
8.3.1
試験室で調製した培地及び試薬 試験管又は瓶に分注した培地,及びすぐには用いない試薬は遮光
して保存する。ゴム栓又はスクリューキャップなどを用いて,保存中の乾燥を防止する。5.7に規定する冷
蔵庫で保存する場合は3か月以内とする。成分の変性を防ぐ条件下で18〜23 ℃に維持して保存する場合は
1か月以内とし,乾燥した培地は用いない。使用前に,培地の温度を試験室の温度に保つことが望ましい。
8.3.2
既製の培地及び試薬 使用期限,保存温度,保存条件,pHなどの使用条件及び有効性は,製造業
者の取扱説明書に従う。
11
K 3701:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
8.4
寒天培地の融解 沸騰水浴中に入れるか,蒸気が流れ込む5.5に規定するオートクレーブ又は電子レ
ンジなど同じ結果が得られる他の操作によって培地を融解する。過熱を避け,融解後は直ちに培地を取り
出す。使用するまで,用途に適した温度に維持した5.9に規定する恒温水槽を用いて,培地を融解状態に
保つ。融解した状態で保持する時間は8時間を超えないことが望ましい。使用しなかった培地を再度固化
して用いてはならない。特に変性しやすい培地は,融解時間を短縮する。
8.5
培地の脱気 必要に応じて使用直前に,ふた又は栓を緩め,沸騰水浴中又は蒸気流の下で培地を15
分間加熱する。その後,ふたを締めて試験温度まで急冷する。
8.6
シャーレにおける寒天平板培地の調製 融解した寒天平板培地を4 mm以上の厚さになるようにシ
ャーレに注ぐ(外径90 mmのシャーレでは,通常寒天培地20 mLが必要である。)。水平な冷たい台の上に
シャーレを置き,寒天培地を冷却及び固化させる。調製した寒天平板培地は直ちに用いるか,組成変化を
防ぐために,5.7に規定する冷蔵庫の中で,1週間以内を目処に保存する。シャーレにラベルをはる。寒天
平板培地は,乾燥させた後に用いる。寒天培地の表面に接種する場合には寒天平板培地を,望ましくは,
25〜50 ℃に維持した乾燥機の中で,ふたを外して倒置し,培地表面の液滴が消えるまで乾燥させる。必要
以上に乾燥させない。寒天平板培地は,層流式安全キャビネットの中で乾燥させることも可能であり,ふ
たを半開した状態では30分間,ふたを閉じた状態では一夜置いて乾燥させる。既製の寒天平板培地も市販
されている。保存及び使用方法は製造業者の取扱説明書に従う。
9. 試料 試料の取り扱いは,次による。
9.1
試料の採取 試料採取は,この規格では規定しない。
個別の規格が存在しない場合には,当事者間で合意を得るものとする。
9.2
輸送 試料の輸送は,微生物の数が変化しない条件で実施する。試料は,次に示す温度で保存する。
− 常温で保存可能な試料:常温
− 新鮮な冷蔵試料:0〜4 ℃
− 冷凍試料:−18 ℃未満
− 低温殺菌及び同様の処理をした試料:0〜4 ℃
− 不良品となったが安定した状態の試料:0〜4 ℃
不良品となったが安定した状態の試料は,漏出しないように密閉包装で輸送する。
9.3
受領及び保存 試験担当者は,受領時に試料の状態を点検する。試料の状態に不備があるか,試料
が不十分である場合には,その試料の受領を拒否する。状況によっては,試験担当者がその試料を分析し
てもよいが,結果の保証については懸念があることを報告しなければならない。試験室が受領を許可した
試料については,試験報告書作成までの全過程が追跡できるように記録をする。
− 受領日
− 試料採取操作の詳細(試料採取日,採取条件など)
− 試験要請機関など名称及び所在地
− 試料の特徴
試験前の試料は,存在する微生物の数が変化しない条件で保存する。
次の試料は,保存温度(9.2参照)及び試験期限に注意する。
− 常温で保存可能な試料:保存期限内に試験する。
− 新鮮な冷蔵試料:24時間以内に試験する(長期保存がやむを得ない場合には,できる限り速やかに
−18 ℃未満で試料を凍結する。凍結によって細菌そう(叢)の構成状態が変化する試料があるため,
12
K 3701:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
試験報告書に凍結したことを記載する。)。
− 低温殺菌又は同様の処理をした試料:保存期限内に試験する。
− 不良品となったが,安定した試料:48時間以内に試験する。
9.4
試験試料 試料の試験は,環境汚染及び試験試料の汚染を避けるため,特殊施設又はクラスⅡ安全
キャビネット内で実施することが望ましい。微生物の含有量が極めて少ないことが明らかな試料を常に最
初に試験し,その後より高度に汚染されていることが明らかな試料を試験する。高度に汚染された粉末試
料の試料をひょう量し,採取する場合には,環境汚染の防止が特に重要である。これらの操作は安全キャ
ビネット内で実施する。試料を扱う場合には,次の操作を実施し,あらゆる汚染を防止する。
− バイオハザード対策用クラスⅡキャビネット内で作業しない場合には,火炎の周辺で作業する。
− 包装された試料は,開封する包装部分の外側をエタノール溶液(体積分率70 %)で消毒し,可能
であれば引火に注意して火炎にかざす。
− 缶切り及びはさみなど,開封の際に用いる器具を火炎滅菌する。
− さじ(匙),ピンセット及びパスツールピペットなど,試料採取に用いる器具を火炎滅菌する。
− 試験試料を入れた袋などの容器に,試料の詳細を記録する(9.3参照)。
9.5
試料の保存及び廃棄 すべての結果が得られるまで試料を保管し,必要に応じてさらに長期間保管
する。袋などの無菌容器に入れ,試料の保存温度に戻す。冷蔵した試料は凍結する。品質が劣化した試料
又は危険な試料は,廃棄する前に汚染除去をする。劣化していない試料は直接廃棄する。
10. 試験方法及び試験結果の表記
10.1 予防措置 次に示す予防措置を講じ,可能な限り無菌状態で作業する。
− 作業区域が清潔であり,扉及び窓を閉めてすき間風がないことを確認する。
− 作業前後には,適切な消毒剤を用いて作業台上の汚染を除去する。
− 作業開始前に必要なものがすべてそろっていることを確認する。
− クラスⅡ安全キャビネット内で作業する場合には,滅菌手袋を用いるか,エタノール溶液(体積分
率70 %)などを用いて作業開始前に両手の汚染を除去し,腕又は手を組まない。
− クラスⅡ安全キャビネット内で作業しない場合には,可能な限り試験管及び瓶を傾けて保持し,火
炎の近くで開栓する。
− 不要な動作を行わず,素早く作業する。
− パスツールピペット及びシャーレなど,袋入りの使い捨て器具を1回の試験中にすべて使い切れな
い場合には,適正な数の器具を取り出した後,袋が正しく閉じられていることを確認する。
− ループ及び接種用白金線などは,使用前後に火炎滅菌する。付着物及び微生物の飛散を避けるため,
5.13に規定する白金線滅菌器を用いることが望ましい。使い捨てで滅菌済みのループ及び白金線を
用いる。
− 使用済みのパスツールピペットなどは,7.5に規定する汚染除去前に消毒剤を入れた専用容器に入れ
る。パスツールピペットには,消毒剤として次亜塩素酸ナトリウム溶液(有効塩素濃度500〜1 000
ppm)を使用する。
− シャーレ及び培地のほか,微生物を含んでいる可能性がある器具はすべて,汚染除去前に専用容器
に入れた後,精製水で洗浄する。
− 使い捨て器具は,7.5に規定する汚染除去をする前に適切な容器に入れる。
− 汚染液などがこぼれた場合には,エタノール溶液(体積分率70 %)又は他の消毒剤に浸した脱脂
13
K 3701:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
綿又は他の適切な用具で直ちにふき取り,作業台上を洗浄消毒してから作業を続ける。
サルモネラ及びリステリア・モノサイトゲネスなどの病原菌又は毒素を含んでいる可能性がある試料の
操作には,次の措置を講じる。
− 分析に必要なあらゆる操作は,バイオハザード対策用クラスⅡキャビネット内で行う。
− 機械式吸引装置を利用し,パスツールピペットを口で吸わない。
エアロゾルの発生を防止する。
エアロゾルは,環境汚染及び感染の主原因である。次の操作で環境汚染及び感染を生じる可能性がある。
− シャーレ,試験管及び瓶の開放
− 振とう器,注射器,遠心分離機などの使用
− 吹き出しによってパスツールピペットを空にするとき
− 菌接種用のぬれたループ又は針の滅菌
− 凍結乾燥培地の入ったアンプルの開封
10.2 試料懸濁液及び希釈系列の調製
JIS K 3702による。試料懸濁液を調製する場合には,個別のISO規格又はJIS K 3703-1,JIS K 3703-2,
JIS K 3703-3,JIS K 3704,JIS K 3705,JIS K 3706-1及びJIS K 3706-2に規定がない限り,調製を終えて
から接種材料が培地に接触する瞬間まで,45分間を超えてはならない。
10.3 固形培地の試験 固形培地の試験は,次による。
10.3.1 平板混釈法 恒温水槽中で47 ℃に保って培地を融解後,実施する。ラベルを付けたシャーレに規
定量の接種材料の希釈系列を分注後,8.6で規定する量の培地を各シャーレに注ぐ。培地全体に微生物が均
一に分布するように,融解した培地と接種材料を直ちに混合する。水平の冷たい台上にシャーレを置いて
冷却し,速やかに固化させる。試験対象試料の中にプロテウス属など拡散コロニーを形成する菌が存在す
ると予想される場合には,滅菌した非栄養寒天培地又は試験に用いる培地と同じ寒天培地を,固化した固
形平板培地に重層する。
10.3.2 平板塗抹法 シャーレにラベルを付け,8.6に従って調製した寒天平板培地の中央に接種材料を落
とし,滅菌したガラス製又はプラスチック製のスプレッダーを用いて,寒天平板培地の表面に液体が見え
なくなるまで,接種材料を均一に塗抹する。塗抹は,手早く行う。
10.3.3 培養 接種した寒天平板培地を直ちに倒置し,適切な温度に設定したインキュベーターに素早く移
す。温度が55 ℃となったり,強度の空気循環が生じるなど,過乾燥が起きる場合には,培養前に袋で寒天
平板培地を軽く包むか,同等の効果が得られる同様の方法を用いる。
備考 計数するときに,試験試料の粒子と菌のコロニーとの混同を避けるため,場合によっては1試
料を寒天平板培地2枚に接種して1枚を2 ℃で保存し,接種し,培養した寒天平板培地と比較
するとよい。
培養後,すぐに各寒天平板培地を試験する。5.7に規定する冷蔵庫で最長24時間保管してもよい。
10.3.4 コロニーの計数 個別の規格に規定されている培養期間後,各寒天平板培地上のコロニー数(全コ
ロニー,定形コロニー又は疑わしいコロニー)を計数する。計数の対象となる寒天平板培地は,コロニー
数が300個未満のものとする。コロニー数が0個の寒天平板培地が得られた場合,10.3.5に規定された様々
な算定法を用いる。定形コロニー又は疑わしいコロニーを計数するとき,定形又は非定形コロニーの数は
合計で300個を超えてはならない。
備考1. 微生物が拡散するなど,コロニーの計数が困難である場合は,個別の規格の規定による。
2. 定形コロニー又は疑わしいコロニーを計数する場合は,コロニーを表す方法は,個別の規格によ
14
K 3701:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
る。
10.3.5 コロニー数の算定法 コロニー数の算定法は,次のとおり行う。
10.3.5.1 算定対象 算定対象は,次による。
− 各希釈率につき,外径90 mmのシャーレ2枚に接種した場合
− 全コロニーの最大数が一寒天平板培地当たり300個である場合
− 定形コロニー又は疑わしいコロニーの計測において,定形コロニー及び非定形コロニーの合計数が一
寒天平板培地当たり300個以下である場合
− 定形コロニー又は疑わしいコロニーが一寒天平板培地当たり150個以下である場合
− 各寒天平板培地から同定及び確認のために,接種した疑わしいコロニー(10.3.5.3)から採取した数が
5個である場合
− 少なくとも1枚の寒天平板培地にコロニー[全コロニー,定形コロニー,又は同定及び確認基準
(10.3.5.3)を満たしたコロニー]数が15個以上ある場合
シャーレの外径が90 mmでない場合,シャーレの表面積に比例してコロニーの最大数を増やす。
備考 希釈率が同一の試料を接種した寒天平板培地2枚のコロニー数に著しい差異が生じる場合,及
び連続する2段階の希釈率の比に対してコロニー数の比が大幅に異なる場合がまれに生じる。
そのような場合は,微生物の専門技術者の判断が必要である。
10.3.5.2 算定法:一般例(全コロニー数及び定形コロニー数の計測) 有効な結果を得るためには,寒天
平板培地上のコロニーを計数するとき,対象とする寒天平板培地のうち少なくとも1枚に,15個以上のコ
ロニー[全コロニー,定形コロニー,又は同定及び確認基準(10.3.5.3)を満たしたコロニー]が発生して
いなければならない。次の式を用いて連続する2段階の希釈試料液から加重平均として試験試料に存在す
る微生物数(N)を算定する。
(
)
[
]d
n
n
V
C
N
×
×
+
×
∑
=
2
1
1.0
ここに, ΣC: 連続する2段階の希釈試料液を入れた全寒天平板培地
に出現したコロニーの合計数(少なくとも1枚には15
個以上のコロニーが発生していなければならない。)
V: 各寒天平板培地への接種量(mL)
n1: 選定した希釈率の寒天平板培地数
n2: n1に続く希釈率の寒天平板培地数
d: 選定した試料希釈液(n1)の希釈率(希釈しない液体試
料を用いる場合は,d=1とする。)
算定結果を四捨五入して有効数字2けたとする。菌数は,1.0〜9.9の数値に10xを乗じた形で記述する。こ
こではxはゼロ又は整数を示す。結果は,次のように表記する。
− 1 mL(液体試料)又は1 g(その他の試料)当たりの微生物数N(個/mL)
例 コロニー数を計数したところ,次の結果が得られた。
− 選定した希釈試料液(10-2):コロニー数168個及び215個
− 選定した希釈試料液に続く10倍希釈液(10-3):コロニー数14個及び25個
(
)
[
]
(
)
182
19
022
.0
422
10
2
1.0
2
1
25
14
215
168
1.0
2
2
1
=
=
×
×
+
×
+
+
+
=
×
×
+
×
∑
=
−
d
n
n
V
C
N
よって,試料1 mL又は1 g当たりの微生物数は1.9×104(個/mL)となる。
15
K 3701:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
10.3.5.3 算定法(同定又は確認後の場合) 微生物の同定又は確認が必要とされる方法を用いる場合には,
コロニー数を計測した各寒天平板培地上から任意の数A(通常は5)個の疑わしいコロニーを接種し,微
生物を同定又は確認後,各寒天平板培地につき,次の式を用いて同定又は確認基準を満たしたコロニー数
aを算定する。
C
A
b
a
×
=
ここに,
b: 接種したコロニー数Aのうち,同定及び確認基準を
満たしたコロニー数
C: 寒天平板培地上で計数した疑わしいコロニーの合計
数
算定結果を四捨五入して近似する整数を求める。この場合,小数点第1位が5未満であれば1の位はそ
のままとし,小数点第1位が5以上であれば1の位を1増やす。10.3.5.2及び後記の10.3.5.4.1,10.3.5.5.3
にそれぞれ示した式のΣCをΣaに置き換えて,試験試料中に存在する同定及び確認された微生物数N,
NE及びN′を算定する。10.3.5.2によって,この結果を四捨五入する。結果の表記については,10.3.5.2,
10.3.5.4.1,10.3.5.5.3による。
例 コロニー数を計測したところ,次の結果が得られた。
− 選定した希釈試料液(10-3):コロニー数66個及び80個
− 選定した希釈試料液に続く10倍希釈液(10-4):コロニー数4個及び7個
選択したコロニーを試験した結果:
66個のうち8個を接種,6個が基準を満たした:a=50
80個のうち9個を接種,6個が基準を満たした:a=53
7個のうち5個を接種,4個が基準を満たした:a=6
4個のうち,4個すべてが基準を満たした:a=4
(
)
[
]
(
)
[
]
364
51
2
002
.0
113
10
2
1.0
2
1
4
6
53
50
1.0
3
2
1
=
=
×
×
+
×
+
+
+
=
×
+
×
∑
=
−
d
n
n
V
a
N
したがって,試料1 mL又は1 g当たりの微生物数は5.1×104(個/mL)となる。
10.3.5.4 算定法(推定数)
10.3.5.4.1 コロニー数15個未満の寒天平板培地(試験試料,試料原液又は選定した希釈液を接種)2枚の
場合 試験試料,試料原液又は選定した希釈試料液を接種した2枚の寒天平板培地上のコロニー数(全コ
ロニー,定形コロニー又は同定及び確認基準を満たしたコロニー)が15個未満である場合には,試験試料
中に存在する微生物の推定数NEを,次の式を用いて寒天平板培地2枚のコロニー数の算術平均として算定
する。
d
n
V
C
N
×
×∑
=
E
ここに,
ΣC: 寒天平板培地2枚のコロニーの合計数
V: 各寒天平板培地への接種量(mL)
n: 接種した寒天平板培地数(ここでは2とする。)
d: 接種した試料原液又は選定した希釈試料液の希
釈率[希釈しない液体試料(試験試料)を用いる
場合は,d=1とする。]
10.3.5.2によって,この結果を四捨五入する。結果は次のように表記する。
16
K 3701:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
− 1 mL(液体試料)又は1 g(その他の試料)当たりの微生物推定数NE(個/mL)
例 コロニー数を計測したところ,次の結果が得られた。
− 選定した希釈試料液(10-2)を接種:コロニー数12個及び13個
250
1
02
.0
25
10
2
1
13
12
2
=
=
×
×
+
=
−
E
N
したがって,試料1 mL又は1 g当たりの微生物の推定数は1.3×103(個/mL)となる。
10.3.5.4.2 コロニー数0個の寒天平板培地(試験試料,試料原液又は選定した希釈液を接種)2枚の場合。
試験試料,試料原液又は選定した希釈試料液を接種した2枚の平板上にコロニーが全く認められない場
合,次のように結果を表記する。
− 1 mL(液体試料)又は1 g(その他の試料)当たりの微生物は1/d未満
ここで,dは,接種した試料原液又は選定した希釈試料液の希釈率を示す。試験試料を希釈しないで用
いる場合は,d=1となる。
10.3.5.4.3 特殊例(定形コロニー又は疑わしいコロニーの計数)
10.3.5.4.3.1 選定した希釈試料液d1を接種した寒天平板培地2枚において,定形コロニー及び非定形コロ
ニー数が300個(又は個別規格に規定された数)を超え,明らかな定形コロニー又は確認されたコロニー
が認められる場合,又はd1に連続する希釈段階の試料液d2を接種した平板2枚においてはコロニー数が
300個(又は個別規格に規定された数)未満であり,定形コロニーも確認されたコロニーも認められない
場合,次のように結果を表記する。
− 1 mL(液体試料)又は1 g(その他の試料)当たりの微生物数:1/d1超,1/d2未満
ここでd1及びd2は,希釈試料液d1及びd2の希釈率を示す。
例 コロニー数を計数したところ,次の結果が得られた。
− 選定した希釈試料液(10-2)を接種:各寒天平板培地当たりのコロニー数が300個を超え,定形
コロニー,確認されたコロニーが認められた。
− 選定した希釈試料液に続く10倍希釈液(10-3)を接種:コロニー数は33個及び35個,定形コ
ロニー又は確認されたコロニーは認められない。
したがって,試料1 mL又は1 g当たりの微生物数は100より多く1 000未満である。
10.3.5.4.3.2 選定した希釈試料液d1を接種した寒天平板培地2枚において,定形コロニー及び非定形コロ
ニー数は300個(又は個別規格に規定された数)を超えるが,明らかな定形コロニー又は確認されたコロ
ニーは認められない場合,またd1に連続する希釈段階の試料液d2を接種した寒天平板培地2枚においては
コロニー数が300個(又は個別規格に規定された数)未満であり,定形コロニーも確認されたコロニーも
認められない場合,次のように結果を表記する。
− 1mL(液体試料)又は1 g(その他の試料)当たりの微生物数:1/d2未満
ここでd2は,希釈試料液d2の希釈率である。
例 コロニー数を計数したところ,次の結果が得られた。
− 選定した希釈試料液(10-2)を接種:各寒天平板培地当たりのコロニー数が300を超えるが,定
形コロニー又は確認されたコロニーは認められない。
− 選定した希釈試料液に続く10倍希釈液(10-3)を接種:コロニー数は33個及び35個,定形コ
ロニー又は確認されたコロニーは認められない。
したがって,試料1 mL又は1 g当たりの微生物数は1 000未満である。
10.3.5.5 算定法:特殊例
17
K 3701:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
10.3.5.5.1 選定した希釈試料液d1を接種した寒天平板培地2枚において,計数された全コロニー,定形コ
ロニー,又は疑わしいコロニー数が300個(又は個別規格に規定された数)を超え,また,d1に連続する
希釈段階の試料液d2を接種した寒天平板培地2枚においては,全コロニー,定形コロニー,又は同定及び
確認基準を満たしたコロニー数が15未満である場合:
− 選定した希釈試料液(10-2)を接種した各寒天平板培地のコロニー数が324個(加重平均300個の
信頼区間上限値)〜300個の範囲にある場合,10.3.5.2に示す一般例の算定法を適用する。
− 選定した希釈試料液(10-2)を接種した各寒天平板培地のコロニー数が324個(加重平均300個に
対する信頼区間の上限値)を超える場合,希釈試料液d2のコロニー数だけを考慮し,10.3.5.4に示
す推定数を算定する。ただし,コロニー数の最大値を300個に設定した場合,後者の結果が10個未
満(加重平均15個の信頼区間下限値)であれば,二つの希釈試料液の差が許容範囲を超えるため,
これを除く。
備考 信頼区間は,コロニー数の計数に規定される最大数に応じたものとする。
例1. コロニー数を計数したところ,次の結果が得られた。
− 選定した希釈試料液(10-2)を接種:コロニー数310個及び322個。
− 選定した希釈試料液に続く10倍希釈液(10-3)を接種:コロニー数8個及び12個。
一般例の算定方法を用いる。二つの希釈試料液を接種した全寒天平板培地を用いる。
例2. コロニー数を計数したところ,次の結果が得られた。
− 選定した希釈試料液(10-2)を接種:各寒天平板培地のコロニー数が324個を超えた。
− 選定した希釈試料液に続く10倍希釈液(10-3)を接種:コロニー数12個及び14個。
10-3の希釈試料液を接種した寒天平板培地2枚におけるコロニー数を基に,推定数を算定
する。
例3. コロニー数を計数したところ,次の結果が得られた(コロニー数の計数に当たり,最大数を300
個に設定する。)。
− 選定した希釈試料液(10-2)を接種:各寒天平板培地のコロニー数が324個を超えた。
− 選定した希釈試料液に続く10倍希釈液(10-3)を接種:コロニー数8個及び6個。
この結果は採用されない。
例4. コロニー数を計数したところ,次の結果が得られた(コロニー数の計数に当たり,最大数を150
個に設定する。)。
− 選定した希釈試料液(10-2)を接種:各寒天平板培地のコロニー数が167個を超えた(加重
平均の信頼区間上限値は150個)。
− 選定した希釈試料液に続く10倍希釈液(10-3)を接種:コロニー数8個及び6個。
10-3の希釈試料液を接種した寒天平板培地2枚におけるコロニー数を基に,推定数を算定
する。
10.3.5.5.2 各希釈試料液を接種したすべての寒天平板培地において,全コロニー,定形コロニー及び疑わ
しいコロニーの数を計数すると300個を超える場合,次のように結果を表記する。
− 試料1 mL(液体試料)又は1 g(その他の試料)当たりの微生物数は,全コロニー又は定形コロニ
ーの場合:300/dを超える。確認されたコロニーの場合:300×b/A×1/dを超える。
ここに,
d: 最終段階の希釈試料液の希釈率
b: 疑わしいコロニーA個のうち,同定及び確認基準を満
たしたコロニー数
18
K 3701:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
10.3.5.5.3 最終段階の希釈試料液が接種された寒天平板培地2枚だけにおいて,全コロニー,定形コロニ
ー,又は疑わしいコロニーの数が300個(又は個別規格に規定された数)未満である場合,試験試料中に
存在する微生物数N′を,寒天平板培地2枚のコロニー数の算術平均として,次の式を用いて算定する。
d
n
V
C
'
N
×
×∑
=
ここに, ΣC: 寒天平板培地2枚のコロニーの合計数(少なくとも
1枚はコロニー数が15個以上)
V: 各寒天平板培地への接種量(mL)
n: 接種した寒天平板培地数(ここでは2とする。)
d: 接種した希釈試料液の希釈率
10.3.5.2で推奨したように,この結果を四捨五入する。算定結果は,次のように表記する。
− 1 mL(液体試料)又は1 g(その他の試料)当たりの微生物数N′(個/mL)
例 コロニー数を計数したところ,次の結果が得られた。
− 最終段階の希釈試料液(10-4):コロニー数120個及び130個。
000
250
1
2
000
.0
250
10
2
1
130
120
4
=
=
×
×
+
=
−
'
N
したがって,試料1 mL又は1 g当たりの微生物数N′ は,1.3×106(個/mL)となる。
10.3.6 信頼区間 結果の有効性を評価し,過度に厳密な解釈を避けるため,試料中に存在する微生物の統
計分布を示す信頼区間を求める。
備考 希釈誤差に関連する変動に影響を及ぼしており,その程度は各試験室で異なる。
10.3.6.1 一般例 試料中に存在する微生物の分散度を表す信頼区間δ(確率95 %)は,次の式を用いて
算出する。
d
B
C
B
B
C
δ
1
96
.1
92
.1
×
∑
±
+
∑
=
ただし,B=V(n1+0.1×n2)である。
ここに, ΣC: 希釈試料液を入れた全寒天平板培地上に認められた
コロニーの合計数
n1: 選定した希釈試料液を入れた寒天平板培地数
n2: 選定した希釈試料液に続く10倍希釈液を入れた寒天
平板培地数
V: 各寒天平板培地への接種量(mL)
d: 選定した希釈試料液の希釈率
例1. 極端な例(表1参照)
19
K 3701:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
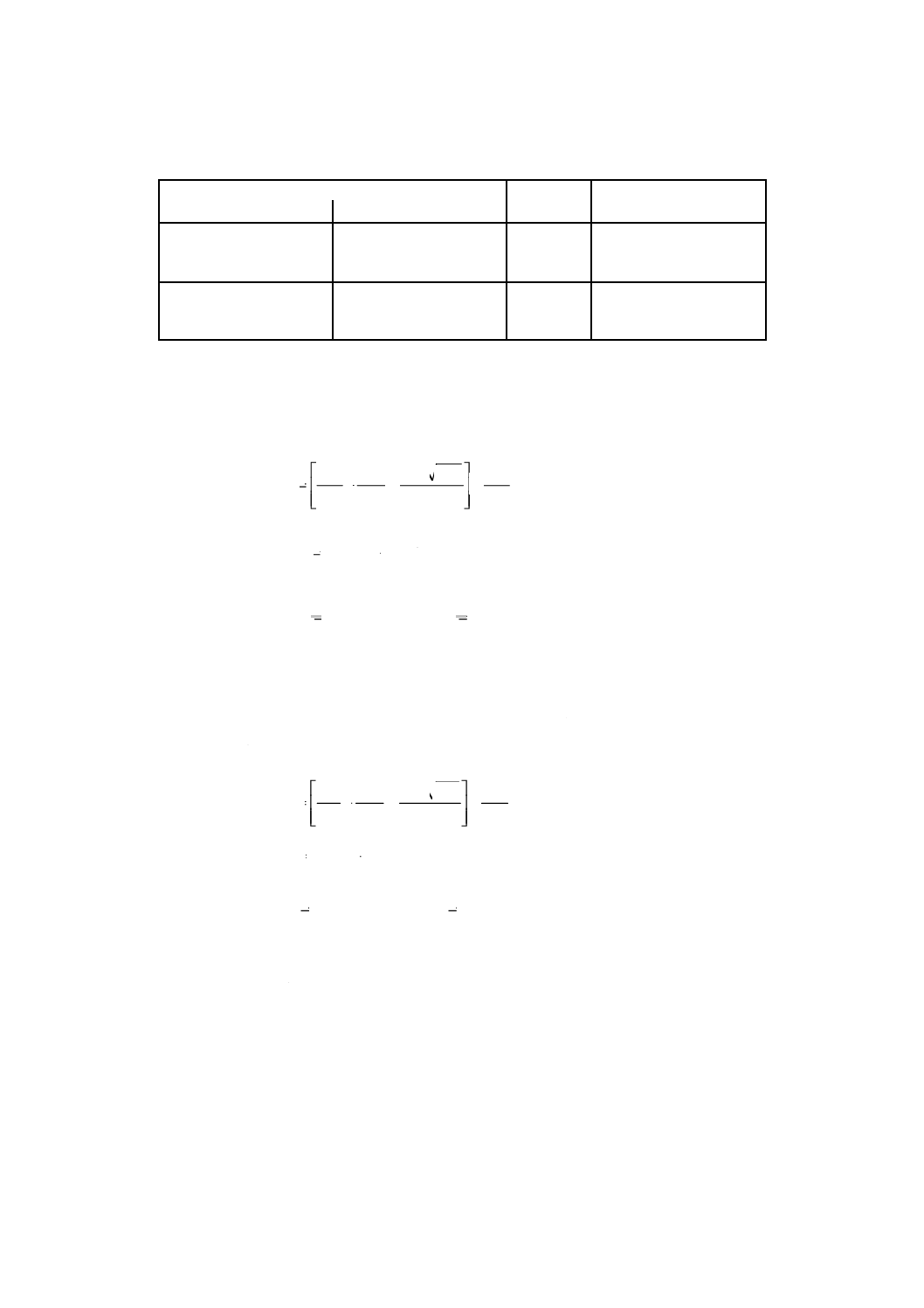
表 1 極端な例
単位 個
計測したコロニー数
加重平均
信頼区間
希釈試料液 n
希釈試料液 n+1
300
300
30
30
300
278〜324
−7 %〜+8 %
15
15
1
1
14
10〜20
−29 %〜+43 %
例2. 10.3.5.1に示した例の信頼区間
計測したコロニー数が422個で,N = 1.9×104 /gである場合の信頼区間δは,次のとおりであ
る。
2
10
1
2.2
422
96
.1
2.2
92
.1
2.2
422
−
×
±
+
=
δ
(
)
2
10
30
.
18
87
.0
82
.
191
×
±
+
=
δ
上記の結果から,信頼区間は,次のようになる。
4
1
10
7.1×
=
δ
4
2
10
1.2×
=
δ
この例では,四捨五入していないデータから算出した信頼区間は−9.1〜+10.0 %である。
10.3.6.2 同定後の場合 試料中に存在する微生物の分散度を表す信頼区間δ(確率95 %)は,10.3.6.1に
示した式のΣCをΣaに置き換えて求める。
例 10.3.5.2に示した例において,認められたコロニー数が113個で試験された微生物数Nが5.1×104
/mLであれば,次のようになる。
3
10
1
2.2
113
96
.1
2.2
92
.1
2.2
113
−
×
±
+
=
δ
(
)
3
10
47
.9
87
.0
36
.
51
×
±
+
=
δ
上記の結果から,信頼区間は,次のようになる。
4
1
10
3.4×
=
δ
4
2
10
6.2×
=
δ
この例では,信頼区間は−16.7〜+20.1 %である。
10.3.6.3 推定数 附属書A表1及び附属書A表2に信頼区間が示されている。
10.4 液体培地の試験(最確数法)
備考 接種方法には,対称システム法と非対称システム法がある。対称システム法は,各希釈段階に
同数の試験管を用いる。二つの希釈段階間の接種する希釈試料液の体積比は一般に1:10であ
る。この方法は,ある限界を超えていないかの確認及び微生物数を明らかにする試験に用いる。
希釈段階ごとに異なる数の試験管を用いる非対称システム法もある。この規格では,10倍段階
希釈系列による対称システム法だけを規定する。
10.4.1 接種 結果に要求される精度に基づいて,適切な数のフラスコ又は試験管に同一の希釈試料液を接
20
K 3701:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
種する(例えば,フラスコ又は試験管を3本,5本又は10本用いる。)。通常,この手法を実施する場合に
は,希釈段階ごとに3本のフラスコ又は試験管が必要である。パスツールピペットを用いて,対応するフ
ラスコ又は試験管に接種材料を移す。各希釈段階につき,新しい滅菌済みのパスツールピペットを用いる。
10.4.2 培養 培養は,接種したフラスコ又は試験管をインキュベーターに入れて行う。4.9に規定する恒
温水槽に入れることが望ましい。
10.4.3 結果の判定
10.4.3.1 希釈試料液の選択 各希釈段階に対して3個の試験管又はフラスコに接種する例では,各試験試
料について連続する3段階の希釈試料液を選択する。
備考 液体であれば,試料原液及び試験試料は,希釈試料液とみなす。
10.4.3.1.1 事例1:陽性を示した管数が3本である希釈段階が一つ以上ある場合(表2参照)
陽性を示した管数が3本であったもののうち,最高の希釈段階(試料濃度が最低の希釈試料液),及びそ
れよりも順次高い希釈段階二つ(最初に選択した希釈試料液の1/10及び1/100に相当する試料濃度をもつ
希釈試料液)を選択する(例1.及び10.4.3.1.2参照)。
陽性を示した管数が3本であったもののうち,最高の希釈段階よりも上に,十分な数の希釈段階が用意
されていない場合には,最高希釈段階を含んだ連続する三つの希釈段階(試料濃度が最低の希釈試料液3
段階)を選択する(例2.参照)。
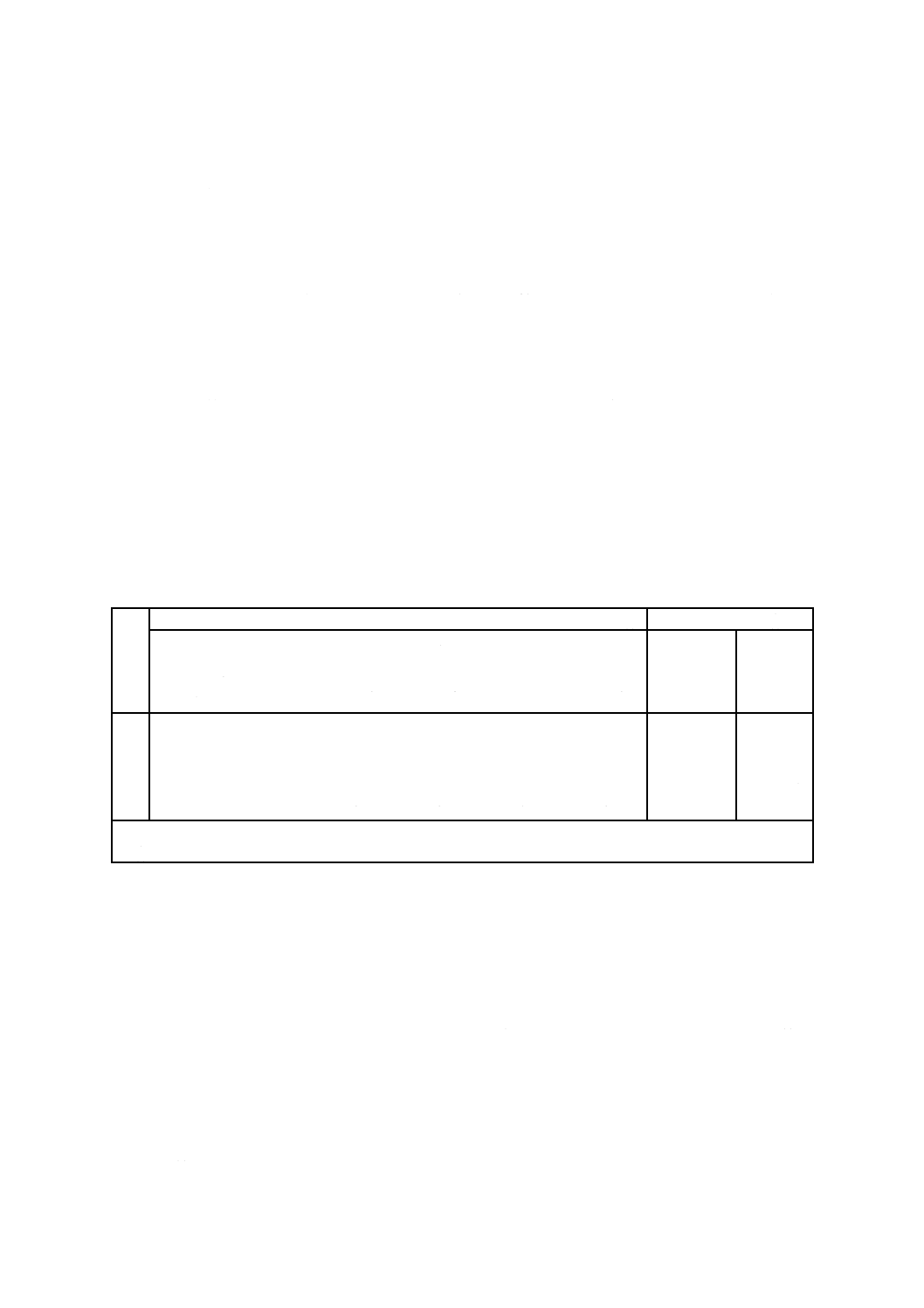
表 2 最確数(MPN)値算出のための陽性を示した管数の選択例
例
培養試験管3本から得られた陽性管数(試験管1本当たり次の量を接種)(1)
最確数MPN (2)
希釈試料液
10 mL
1 mL
10−1 mL
10−2 mL
10−3 mL
希釈試料液
その他の
試料
その他の試
料
1 g
10−1 g
10−2 g
10−3 g
10−4 g
mL−1
g−1
1
3
3
2
1
0
1.5×101
1.5×102
2
3
3
3
0
−
2.4×101
2.4×102
3
2
2
1
1
0
7.4
7.4×101
4
3
3
0
0
0
2.4
2.4×101
5
2
2
0
1
0
2.1×10−1
2.1
注(1) 太字:選択した組合せ
(2) 3本の試験管についてMPN指数から算出した値(附属書B表1)
10.4.3.1.2 事例2:陽性を示した管数が3本である希釈段階が存在しない場合 事例1を適用することは
できない場合は,少なくとも1本が陽性反応を示したもののうち,最高の希釈段階を含んだ連続する三つ
の希釈段階を選択する(例3.及び10.4.3.1.3参照)。
10.4.3.1.3 特殊例:10.4.3.1.1及び10.4.3.1.2に従って選択した三つの希釈段階のうち,2段階以上で陽性管
が1本も得られない場合は,陽性管を含まないもののうち最低の希釈段階(試料濃度が最高の希釈試料液)
及びそれよりも前の希釈段階二つ(最初に選択した希釈段階の10倍及び100倍に相当する試料濃度の希釈
試料液)(例4.及び例5.参照)を選択する。試験試料から調製した第1段階の希釈試料液にだけ陽性管が認
められる場合には,最初の三つの希釈段階に陽性管を全く含まない希釈段階が二つ含まれていても,最確
数の算出にはこの連続する希釈段階を選択する。
10.4.3.2 最確数(MPN指数)の算出
10.4.3.2.1 附属書B表1でまとめて試験した試料の数に基づき,10.4.3.1に従って選択した希釈段階に対
応する陽性管数の系列が,統計学的見地から許容できるか検討する。
21
K 3701:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
許容できるかどうかは,試験試料数に依存するほか,信頼度2及び3(附属書B表2参照)の結果を認
めるか棄却するかの判断にも左右される。
附属書B表1の陽性を示した試験管数の組合せが2-2-1の場合を例として考える。信頼度1の結果だけ
を受け入れる場合には,該当するバッチで10回試験した場合に限り,組合せ2-2-1を考慮に入れることが
できる。これより確率が低い信頼度2の結果まで受け入れる場合には,2,3又は5回の少ない回数の試験
まで,組合せ2-2-1を考慮することができる。陽性を示した組合せ2-2-1が1回の試験の結果であれば,ど
のような状況でも許容できない。
10.4.3.2.2 10.4.3.2.1に従って許容できると判断されたそれぞれの陽性を示した試験管数の組合せから,
附属書B表1を用いてMPN指数を求める。
10.4.4 結果の表記 附属書B表1から得たMPN指数(10.4.3.2参照)から,次の式を用いて基準容量に
存在する微生物の最確数を求める。
S
S
V
V
F
M
C
0
=
ここに, CS: 基準容量VSに存在する微生物の最確数
M: 基本希釈試料液V0(1mL)について附属書B表1から
得たMPN指数
F: 表1で用いる基本希釈試料液として選択した希釈試料
液の希釈率の逆数(一般に,Fは10又は100などの値
をとる。)
VS: 微生物の濃度を表すために選択した基準体積 (mL)
V0: 基本希釈試料液 (mL)
選択した最低の希釈段階が,2倍濃度の培地(10 mLの接種材料)から調製した試験管に相当する場合
には,あらかじめMPN指数を10で除する。
微生物の最確数が液体試料で0.3個/mL,その他の試料で0.3個/g未満であり,微生物数が少ない例に適
切な方法を用いた場合には,“試料1 mL(液体試料の場合)又は1 g(その他の試料の場合)中の微生物
数は1未満”のように結果を表記する。
例 固体試料において,MPN指数が24であり,最初に選択した試験管が 1 mLの試料原液(F = 10)
を接種した試験管であれば,1 g当たりのCsは次のとおりである。
2
S
10
4.2
10
24
×
=
×
=
C
10.4.5 信頼区間 MPN表(附属書B表1)に信頼区間を示す。
MPN法では,結果に大きなばらつきが生じることがある。このため,この方法によって得られた結果は
注意して用いる。
10.5 検出試験法 試料の一定量当たりの目的の微生物の有無を判定する方法。
10.5.1 概要 任意量pの試験試料にpの9倍量(mL又はg)の分離及び選択液体培地を加え,液体試料
であれば混和し液体以外の試料であればホモジナイザー(5.3)で懸濁する。恒温水槽(5.9)で培養した後,
培養試料をループに採取し,孤立したコロニーが得られるように選択寒天培地の表面に塗抹することが望
ましい。培養後に得られた任意数(一般には5)のコロニーを同定する。
ストレスを受けた微生物を回復させるため,栄養培地(普通ブロス)であらかじめ増菌した後,分離及
び選択液体培地で増菌する場合もある。2種以上の分離及び選択液体培地を用いると同時に,2種以上の選
択寒天培地を用いることが有用な場合もある。
10.5.2 結果の表記

22
K 3701:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
目的の微生物が確認された場合は,次の形式で結果を表記する。
“分析したp mL(液体試料)又はp g(その他の試料)中に存在する。”
目的の微生物が確認されない場合は,次の形式で結果を表記する。
“分析したp mL(液体試料)又はp g(その他の試料)中に存在しない。”
この量以上に大きな量に一般化してはならない。
10.6 基本的な同定法
10.6.1 純培養の調製
10.6.1.1 概要 試験試料の希釈液又は培養試料を接種した寒天培地の表面上又は培地中のコロニーを選
択し,純培養の調製を開始する。次に,選択したコロニーを非選択寒天培地の上に接種する。培養後,明
らかに孤立したコロニーを選択する。必要に応じてこの操作を繰り返す。10.6.1.2の寒天平板培地塗抹法を
用いる。特殊な例では,他の方法が必要となる。嫌気性微生物では,培養物を好気的条件下に置く時間を
可能な限り短くする。
10.6.1.2 寒天平板培地塗抹法 明らかに孤立したコロニーの表面から滅菌済みループの先に少量を釣菌
し,これを直接塗抹するか(10.6.1.2.1)又はこれらの細胞の懸濁液を調製した後に塗抹する(10.6.1.2.2)。
10.6.1.2.1 直接法:例 ループの先を利用して,寒天培地表面の約1/3の部分に,画線間隔を密にして接
種する。ループを滅菌及び冷却後,接種した部分の端から最初の部分に比べて画線間隔を広くして,まだ
接種していない部分の半分の領域に画線塗抹する。さらに間隔を広くして,残りの部分でこの操作を繰り
返す(図1参照)。
図 1 塗抹例:直接法
10.6.1.2.2 希釈液を用いる方法 選択した希釈液1〜2 mLの中に細胞を懸濁する。液表面で試験管の壁面
に接種用ループを擦り付け,よく混和する。ループを滅菌及び冷却後,ループに微生物の懸濁液を少量と
り,10.6.1.2.1によって接種する。
10.6.1.3 培養 個別の規格にない限り,接種したシャーレを倒置し,規定温度のインキュベーター内で規
定時間培養する。
10.6.1.4 選択 培養後,明らかに孤立したコロニーをシャーレから選択し,次の寒天平板培地培養及び試
験を実施する。可能であれば,単一コロニーに由来する細胞を用いて最終試験を実施する。単一コロニー
に十分な細胞が存在しない場合には,最初に液体培地又は斜面寒天培地で継代培養した後,その継代培養
を用いる。
10.6.2 グラム染色(Huckerの変法) 多くの方法が存在するが,いずれも次に示す手順に従う。
備考 この方法によって細菌細胞を染色すると,細菌形態が明らかとなるほか,試験条件下でクリス
タルバイオレットの染色性に基づいて微生物を2群に分類できる。この分類は主に両群の細胞
壁の構造に差があることに由来し,両群間の他の主な差と相関する。

23
K 3701:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
10.6.2.1 溶液及びキット 市販の溶液及びキットを用いてもよい。この場合は製造業者の推奨事項に従う。
10.6.2.1.1 クリスタルバイオレット溶液
10.6.2.1.1.1 組成 クリスタルバイオレット溶液(10.6.2.1.1)の組成は,表3による。
表 3 クリスタルバイオレット溶液の組成
クリスタルバイオレット
2.0 g
エタノール(95)
20 mL
しゅう酸アンモニウム一水和物
0.8 g
精製水
80 mL
10.6.2.1.1.2 調製 クリスタルバイオレットをエタノールに溶かし,しゅう酸アンモニウムは精製水に溶
かす。これら二つの液を混和し,用いるまで24時間静置する。
10.6.2.1.2 よう素溶液
10.6.2.1.2.1 組成 よう素溶液 (10.6.2.1.2) の組成は,表4による。
表 4 よう素溶液の組成
よう素
1.0 g
よう化カリウム
2.0 g
精製水
100 mL
10.6.2.1.2.2 調製 よう化カリウムをフラスコに入れ,精製水10 mLを加えて溶かし,よう素を少しずつ
加えて溶かし,精製水を加えて100 mLとする。
10.6.2.1.3 サフラニンO溶液
10.6.2.1.3.1 組成 サフラニンO溶液 (10.6.2.1.3) の組成は,表5による。
表 5 サフラニンO溶液の組成
サフラニン O(純度80 %以上のもの)
0.25 g
エタノール(95)
10 mL
精製水
100 mL
10.6.2.1.3.2 調製 サフラニンOをエタノール(95)に溶かした後,精製水と混合する。
10.6.2.2 染色方法 18〜24時間培養後又は液体培地が混濁した後,スライドガラス上に細菌塗抹標本を調
製し固定する。その後,クリスタルバイオレット溶液(10.6.2.1.1)で十分覆い,1分間反応させる。スラ
イドガラスを傾け,数秒間穏やかに水洗する。スライドガラスをよう素溶液(10.6.2.1.2)で覆い,1分間
反応させる。スライドガラスを傾け,数秒間穏やかに水洗する。傾けたスライドガラスの表面にエタノー
ル(95)を色素の流出が止まるまで途切れることなく穏やかに注ぐ(最長30秒間とする。)。スライドガラ
スを傾けて穏やかに水洗し,エタノールを除去する。スライドガラスをサフラニン溶液(10.6.2.1.3)で覆
い,10秒間保つ。スライドガラスを傾けて穏やかに水洗する。スライドガラスを乾燥する。
10.6.2.3 判定 高倍率の油浸対物レンズ(5.12参照)を用いてスライドガラスを鏡検する。紫〜青紫を表
した細菌細胞をグラム陽性(Gram+),暗いピンク〜赤を呈するものをグラム陰性(Gram−)とする。
ある種の細菌の純培養では,顕微鏡下の同一視野でグラム陽性菌及びグラム陰性菌の両方が得られる。
備考 胞密度が高いと,特徴が不明りょうな反応を生じることがある。また,生育状態によっても異
なる。
10.6.3 カタラーゼ試験 過酸化水素を水と酸素とに分解する酵素試験。液体培養,寒天培養,又は寒天培
地上の単一コロニーを用いて実施する。加熱処理していない血液が培地に含まれていてはならない。
24
K 3701:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
備考1. グルコース非存在下又は低グルコース濃度(質量分率0.1 %)の条件下で培養したある種の
乳酸菌には,ヘム部分を含まない“偽カタラーゼ様酵素”が存在する。
2. 嫌気性細菌の場合は,過酸化水素を加える前に30秒間空気にさらす。
10.6.3.1 液体培地を対象とする場合 培養液1 mLに過酸化水素水(1+9)(3.4の過酸化水素を水で10倍
に薄めたもの。)0.5 mLを加える。酸素の気泡が発生するか(カタラーゼ陽性)発生しないか(カタラー
ゼ陰性)を観察する。
10.6.3.2 寒天培地を対象とする場合 過酸化水素水(1+9)を培地のコロニー上に滴加する。その直後及
び5分間後に酸素の気泡が発生するか否かを観察する。
10.6.3.3 釣菌する場合 スライドガラスの上に過酸化水素水(1+9)2滴を,離して滴加する。滅菌した
ガラス製又はプラスチック製の棒(金属線を用いてはならない。)を用いて,あるコロニーを拾い上げ,2
滴の一方で穏やかに乳化させる。その直後から数分間(少なくとも1分間),酸素の気泡が発生するかを観
察する。疑わしい場合には,スライドガラスで各液滴を覆い,両方のスライドガラスの下で気泡の発生を
比較する。顕微鏡又は低倍率の拡大鏡を用いて観察してもよい。
10.6.4 オキシダーゼ試験 オキシダーゼは,この酵素の作用による酸化で化合物が青く着色することによ
って試験する。
10.6.4.1 N,N,Nʼ,Nʼ−テトラメチル-p-フェニレンジアミン二塩酸塩溶液
10.6.4.1.1 組成 N,N,Nʼ,Nʼ−テトラメチル-p-フェニレンジアミン二塩酸塩溶液(10.6.4.1)の組成は,表
6による。
表 6 N,N,Nʼ,Nʼ−テトラメチル-p-フェニレンジアミン二塩酸塩溶液の組成
N,N,Nʼ,Nʼ−テトラメチル-p-フェニレンジアミン二塩酸塩(純度98 %
以上のもの)
1.0 g
精製水
100 mL
10.6.4.1.2 調製 N,N,Nʼ,Nʼ−テトラメチル-p-フェニレンジアミン二塩酸塩1.0 gを精製水に溶かして
100 mlとする。使用時に調製する。市販の試験用ディスク又はスティックを用いてもよい。この場合は製
造業者の推奨事項に従う。
10.6.4.2 方法 1片のろ紙をこのN,N,Nʼ,Nʼ−テトラメチル-p-フェニレンジアミン二塩酸塩溶液で湿潤
させる。白金線,ガラス棒又はプラスチック棒(ニッケルクロム線では偽陽性となる。)を用いて寒天培地
上の菌をとり,湿らせたろ紙上に塗まつ(沫)する。
10.6.4.3 結果の判定 オキシダーゼが存在すると,5〜10秒間以内にピンク又は青〜青紫になる。10秒間
後に呈色しなければ陰性とする。
10.6.5 同定用生化学試験キットの使用 市販の生化学試験キットを同定に用いてもよい。ただし,すべて
の市販キットに同じ水準の信頼性があるわけではない。特に他の方法で検証されていない場合には,使用
前にその性能を確認する。
25
K 3701:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書A(規定)推定数の信頼区間
附属書A 表1及び表2で示した値は,[参考文献10)]に基づく。
附属書A表1 コロニー数から算出される信頼区間−シャーレ1枚から求める場合
コロニー数
95 %信頼区間
信頼区間誤差 %
下限
上限
下限
上限
1
<1
6
−97
+457
2
<1
7
−88
+261
3
<1
9
−79
+192
4
1
10
−73
+156
5
2
12
−68
+133
6
2
13
−63
+118
7
3
14
−60
+106
8
3
16
−57
+97
9
4
17
−54
+90
10
5
18
−52
+84
11
6
20
−50
+79
12
6
21
−48
+75
13
7
22
−47
+71
14
8
24
−45
+68
15
8
25
−44
+65
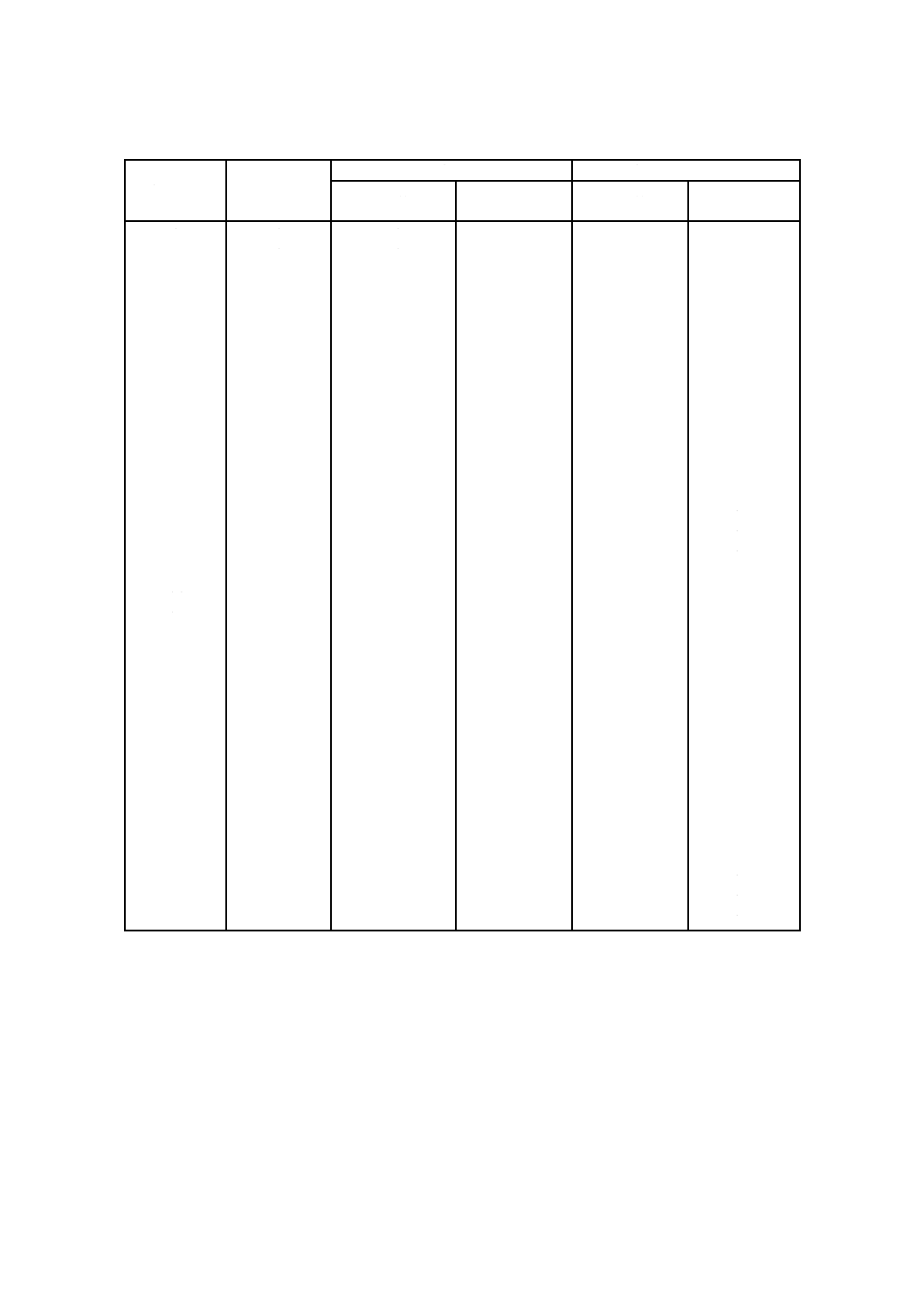
26
K 3701:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
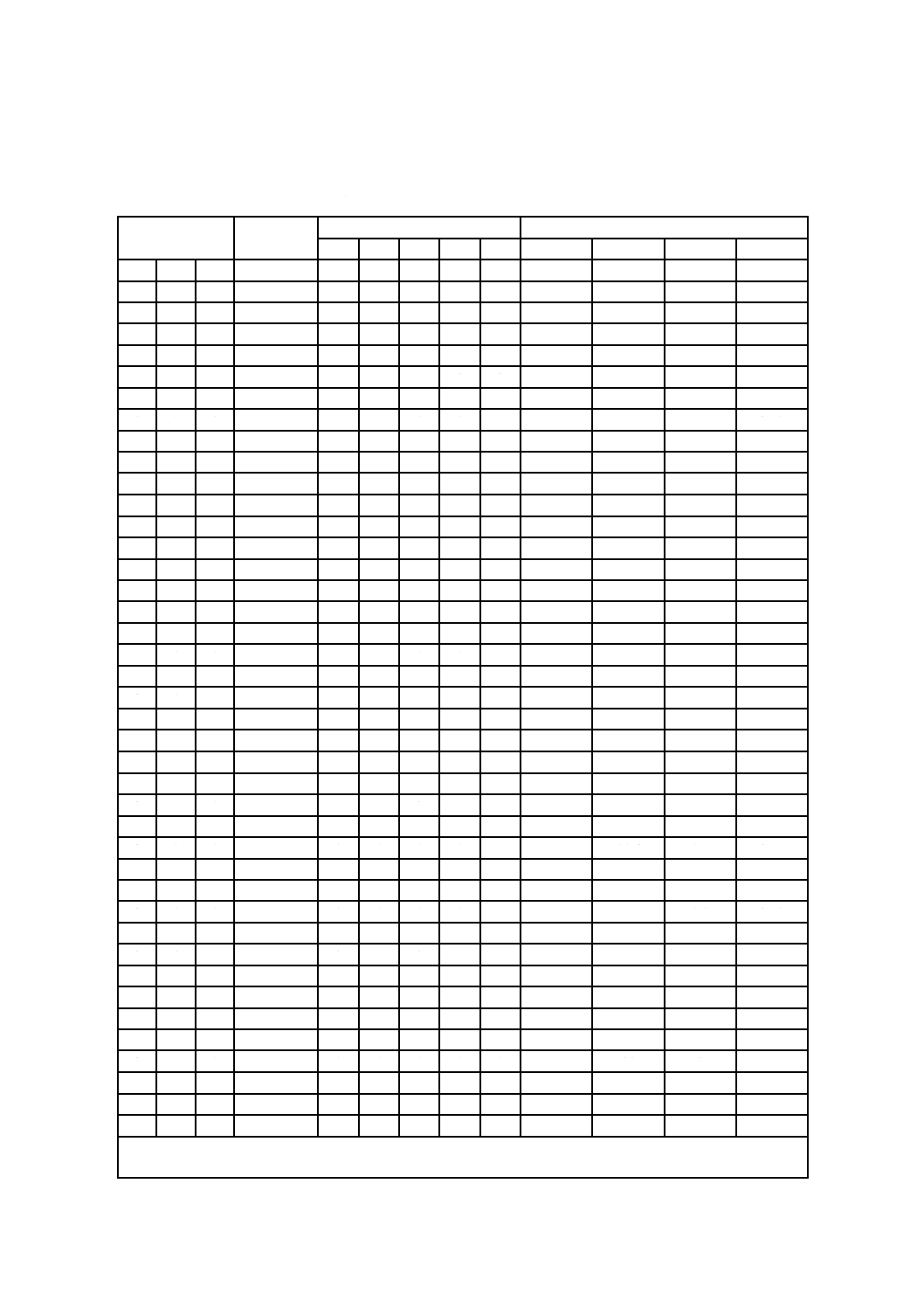
附属書A表2 コロニー数から算出される信頼区間−シャーレ2枚の合計から求める場合
シャーレ2枚
の合計コロニ
ー数
シャーレ2枚
の平均コロニ
ー数
95 %信頼区間
信頼区間誤差 %
下限
上限
下限
上限
1
1
<1
3
−97
+457
2
1
<1
4
−88
+261
3
2
<1
4
−79
+192
4
2
1
5
−73
+156
5
2
1
6
−68
+133
6
3
1
6
−63
+118
7
4
2
7
−60
+106
8
4
2
8
−57
+97
9
4
2
9
−54
+90
10
5
2
9
−52
+84
11
6
3
10
−50
+79
12
6
3
10
−48
+75
13
6
3
11
−47
+71
14
7
4
12
−45
+68
15
8
4
12
−44
+65
16
8
5
13
−43
+62
17
8
5
14
−42
+60
18
9
5
14
−41
+58
19
10
6
15
−40
+56
20
10
6
15
−39
+54
21
10
6
16
−38
+53
22
11
7
17
−37
+51
23
12
7
17
−36
+50
24
12
8
18
−36
+49
25
12
8
18
−35
+48
26
13
8
19
−35
+47
27
14
9
20
−34
+46
28
14
9
20
−34
+45
29
14
9
21
−33
+44
30
15
10
21
−32
+43
27
K 3701:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書B(規定)最確数(MPN)表
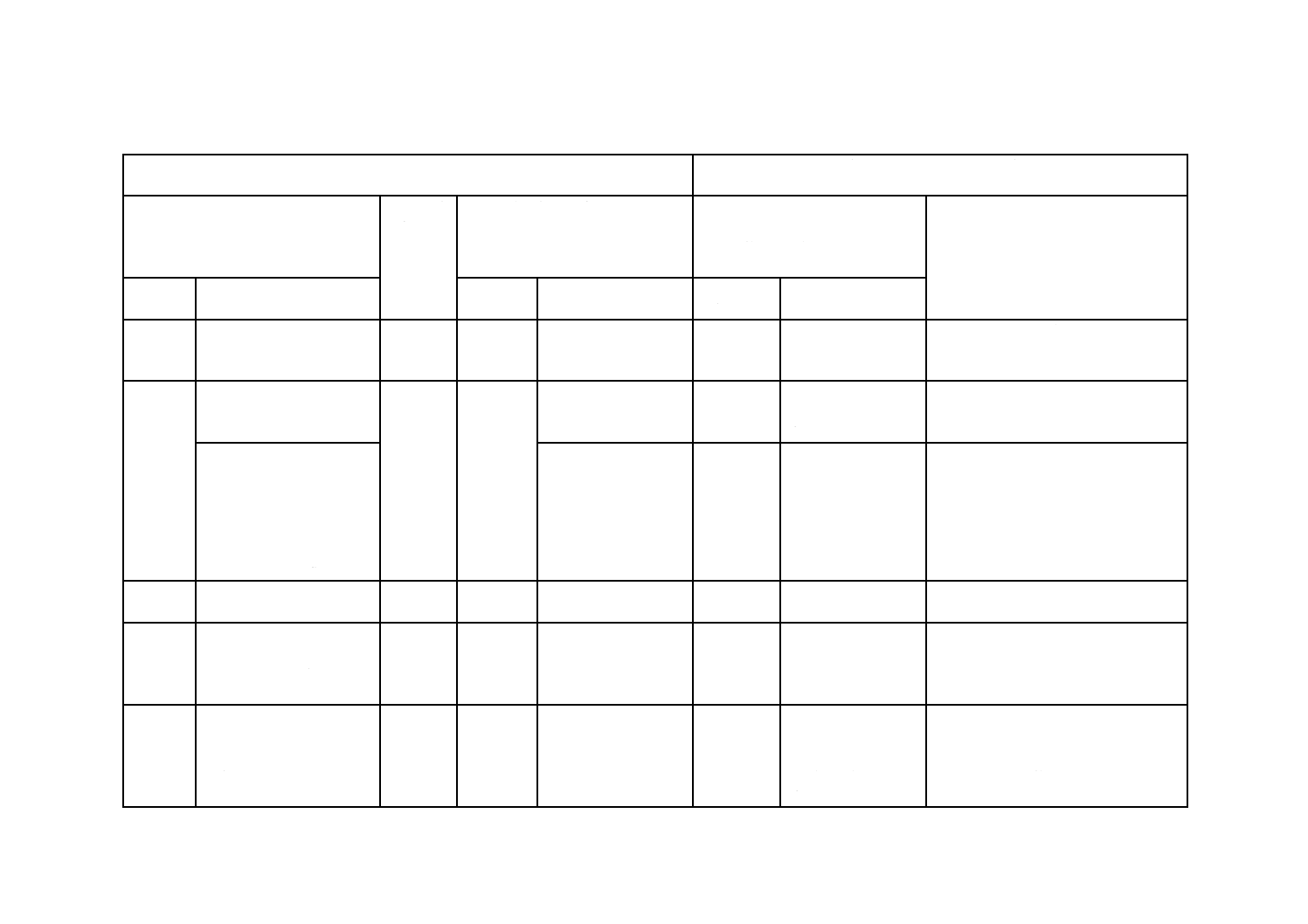
附属書B表1 3×1 g(ml),3×0.1 g(ml),及び3×0.01 g(ml)の最確数(MPN)
陽性を示した
試験管数
MPN値
試験回数別信頼度
95 %信頼区間
1
2
3
5
10
上限
下限
上限
下限
0
0
0
<0.30
0.00
0.94
0.00
1.40
0
0
0
0.30
3
2
2
2
1
0.01
0.95
0.00
1.40
0
1
0
0.30
2
1
1
1
1
0.01
1.00
0.00
1.60
0
1
1
0.61
0
3
3
3
3
0.12
1.70
0.05
2.50
0
2
0
0.62
3
2
2
2
1
0.12
1.70
0.05
2.50
0
3
0
0.94
0
0
0
0
0
0.65
3.50
0.18
4.60
1
0
0
0.36
1
1
1
1
1
0.02
1.70
0.01
2.50
1
0
1
0.72
2
2
1
1
1
0.12
1.70
0.05
2.50
1
0
2
1.1
0
0
0
3
3
0.4
3.5
0.2
4.6
1
1
0
0.74
1
1
1
1
1
0.13
2.00
0.06
2.70
1
1
1
1.1
3
3
2
2
2
0.4
3.5
0.2
4.6
1
2
0
1.1
2
2
1
1
1
0.4
3.5
0.2
4.6
1
2
1
1.5
3
3
3
3
2
0.5
3.8
0.2
5.2
1
3
0
1.6
3
3
3
3
2
0.5
3.8
0.2
5.2
2
0
0
0.92
1
1
1
1
1
0.15
3.50
0.07
4.60
2
0
1
1.4
2
1
1
1
1
0.4
3.5
0.2
4.6
2
0
2
2.0
0
3
3
3
3
0.5
3.8
0.2
5.2
2
1
0
1.5
1
1
1
1
1
0.4
3.8
0.2
5.2
2
1
1
2.0
2
2
1
1
1
0.5
3.8
0.2
5.2
2
1
1
2.0
2
2
1
1
1
0.5
3.8
0.2
5.2
2
1
2
2.7
0
3
3
3
3
0.9
9.4
0.5
14.2
2
2
0
2.1
1
1
1
1
1
0.5
4.0
0.2
5.6
2
2
1
2.8
3
2
2
2
1
0.9
9.4
0.5
14.2
2
2
2
3.5
0
0
0
0
3
0.9
9.4
0.5
14.2
2
3
0
2.9
3
2
2
2
1
0.9
9.4
0.5
14.2
2
3
1
3.6
0
3
3
3
3
0.9
9.4
0.5
14.2
3
0
0
2.3
1
1
1
1
1
0.5
9.4
0.3
14.2
3
0
1
3.8
1
1
1
1
1
0.9
10.4
0.5
15.7
3
0
2
6.4
3
3
2
2
2
1.6
18.1
1.0
25.0
3
1
0
4.3
1
1
1
1
1
0.9
18.1
0.5
25.0
3
1
1
7.5
1
1
1
1
1
1.7
19.9
1.1
27.0
3
1
2
12
3
2
2
2
1
3
36
2
44
3
1
3
16
0
0
0
3
3
3
38
2
52
3
2
0
1
1
1
1
1
1
1.8
36.0
1.2
43.0
3
2
1
15
1
1
1
1
1
3
38
2
52
3
2
2
21
2
1
1
1
1
3
40
2
56
3
2
3
29
3
3
3
2
2
9
99
5
152
3
3
0
24
1
1
1
1
1
4
99
3
152
3
3
1
46
1
1
1
1
1
9
198
5
283
3
3
2
110
1
1
1
1
1
20
400
10
570
3
3
3
>110
備考 附属書B表1の信頼区間は,統計的な変動要因の影響を記述する参考指標値である。有意な影響を及
ぼす要因がその他にも存在する場合がある。

28
K 3701:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書B表 2 結果説明
信頼度
定義
1
試料中の微生物数が表から算出したMPN値と等しい場合,その結果は,得られたもののう
ち,最も可能性が高いものである。得られた結果がこの信頼度における最も低い確率のもの
を下回るものである可能性は,最大でも5 %である。
2
試料中の微生物数が表から算出したMPN値と等しい場合,その結果は,得られたもののう
ち,信頼度1における最も低い確率のものを下回る可能性のあるものである。得られた結果
がこの信頼度における最も低い確率のものを下回るものである可能性は,最大でも1 %であ
る。
3
試料中の微生物数が表から算出したMPN値と等しい場合,その結果は,得られたもののう
ち信頼度2における最も低い確率のものを下回る可能性のあるものである。得られた結果が
この信頼度における最も低い確率のものを下回るものである可能性は,最大でも0.1 %であ
る。
0
試料中の微生物数が表から算出したMPN値と等しい場合,その結果は,得られたもののう
ち信頼度3における最も低い確率のものを下回る可能性のあるものである。この信頼度にお
いて得られた結果が何も問題点のないものである可能性は,0.1 %である。
試験を始めるに当たり,どの信頼度なら許容範囲内であるかを決める(例えば,信頼度1だけである。信頼度
1及び2である。信頼度1,2,及び3である。)(附属書B表1及び附属書B表2を参照)。その結果に基づく決
定が重要な場合は,信頼度1の結果又は信頼度1及び2の結果による。信頼度0の結果は,特に慎重に検討しな
ければならない。
29
K 3701:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
参考文献
1.
Australian Standard AS 1766,Australian Standard Methods for the Microbiological Examination of Food -
Part 1: General Techniques and Procedures.
2.
Australian Standard AS 2243,Safety in Laboratories - Part 3: Microbioology.
3.
Buttiaux,R.,Beerens,H.,and Tacquet,A. Manuel de techniques bactériologiques.
4.
Compendium of Methods for the Microbiological Examination of Foods. (Speek N.L.,ed.),APHA
Intersociety/Agency Committee on Microbiological Methods for Foods. American Public Health Association,
Washington,1976.
5.
Cruickshank et al. Medical Microbiology. Vol.2,12th edn. Churchill-Livingstone,Edinburgh,1975.
6.
Kenya Standard KS 05-176-1978,Methods for the Microbiological Examination of Foods - Part 1: General
Procedures and Techniques.
7.
Harrewijin, G.A.and Hartog,B.J. Guidelines to perform microbiological analyses of food and food products
(“Good laboratory practice”). De Ware - Chemicus,9,1979,pp. 1-11.
8.
Hazards in the chemical laboratory. (Muir G.D. ed.). Royal Institute of Chemistry,London,1971.
9.
Jarvis,B. Statistics of the microbiological analysis of foods. In: Progress in industorial Microbiology. Vol.21,
Elsevier,Amsterdam,1989.
10. Johonson,N.J and Kotz,S. Discrete distribution. Houfhon Mifflin Company,Boston,1969.
11. Laboratory Biosafety Manual. WHO,Geneva,1983.
12. Harrigan W.F. and McCance M.E. Laboratory Methods in Food and Dairy Microbiology. Academic Press,
London and New York,1976.
13. Laboratory Safety at the Center for Disease Control (CDC). NHEW Publication No. CDC 79-8118,Atlanta,
1979.
14. Laboratory Safety at the Center for Disease Control. U.S.D. for Health,Education and Welfare (Public Health
Service),Atlanta,1979.
15. Manual of Methods for General Bacteriology. (Gerhadt P.,Murray R.G.E.,Costillow R.N.,Nester E.W.,Kreig
N.R. and Phillips G.B. eds.). American Society for Microbiology,Washington,DC 20006,1981.
16. Methods in Microbiology. (Norris J.R. and Ribbons D.W. eds.). Vol. 1,Academic Press. London and New York,
1969.
17. Microbiological Testing Laboratory Accommodation Guidlines. National Association of Testing Authorities,
Australia.
18. Microorganisms in Foods: 1 - Their significance and methods of enumeration. ICMSF,University of Tronto
Press,1988.
19. Safety in Microbiology. Society for Applied Bacterioplogy. Technical Series No.1 and No.6. Shapton D.A. and
Board R.G. (Hauster W.J. ed.). Academic Press. London and New York,1972.
20. Standard Methods for the Examination of Dairy Products. (Hauster W.J. ed.),13th edn.,American Public
Health Association,Washington,1972.
21. De Man,J.C. MPN tables (corrected). Eur. J.Appl.Biotechnol.,17,1983,pp. 301-305.
30
K 3701:2008
3
0
K
3
7
0
1
:
2
0
0
8
3
0
K
3
7
0
1
:
2
0
0
8
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
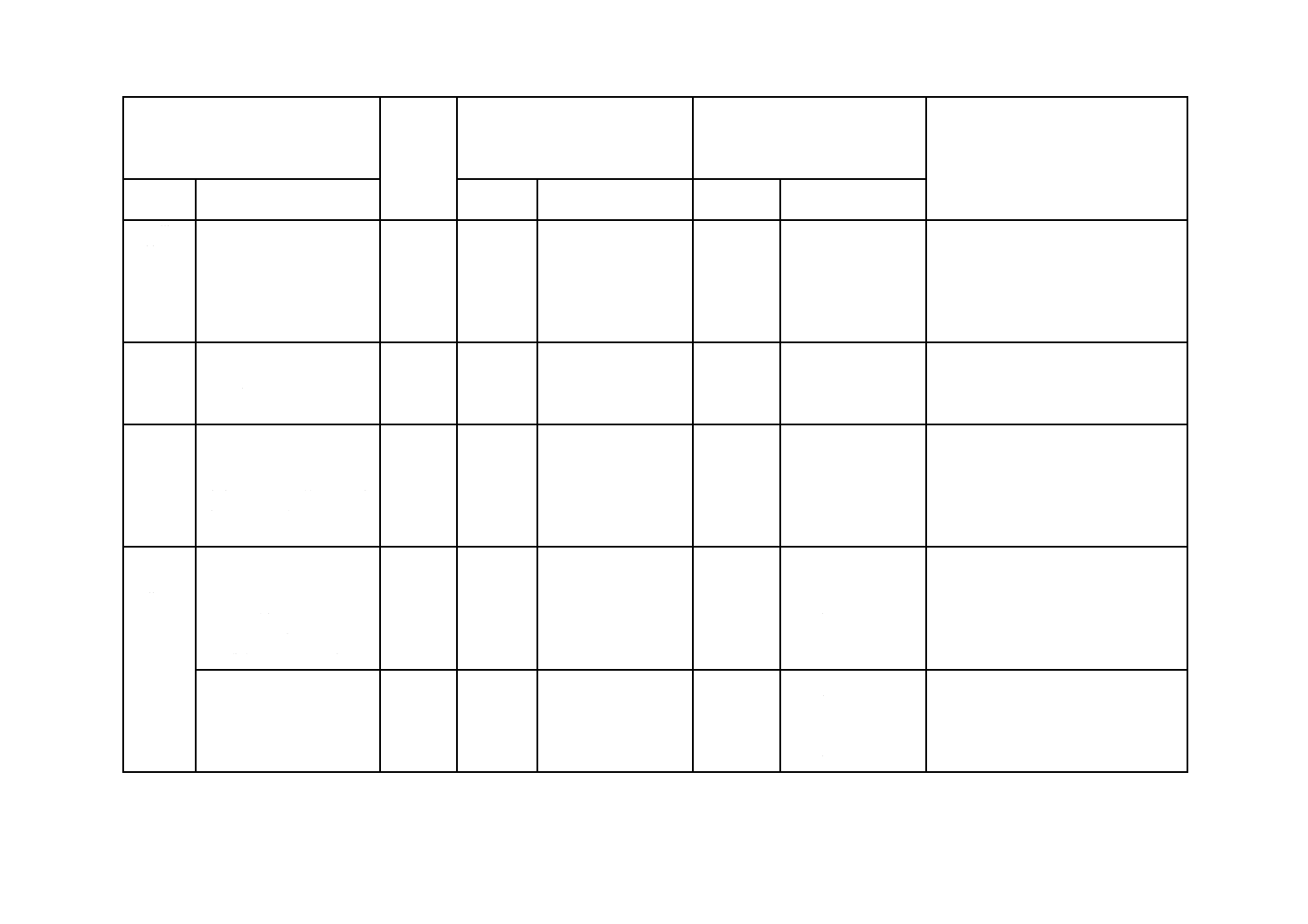
附属書1(参考)JISと対応する国際規格との対比表
JIS K 3701:2008 培地の試験方法−通則
ISO 7218:1996及び追補1:2001,食品及び動物用飼料の微生物試験−微生物
試験の一般規則
(Ⅰ) JISの規定
(Ⅱ) 国際
規格番号
(Ⅲ) 国際規格の規定
(Ⅳ) JISと国際規格との技術的差異
の項目ごとの評価及びその内容
表示箇所:本体
表示方法:点線の下線
(Ⅴ) JISと国際規格との技術的差異の理由
及び今後の対策
項目
番号
内容
項目
番号
内容
項目ごとの
評価
技術的差異の内容
1.適用範
囲
微生物の検出を目的とす
る培地試験の通則につい
て規定。
ISO 7218
1
微生物試験の通則に
ついて規定。
MOD/削除
培地試験に限定。
工業標準化法の対象とならない試験を
削除。
2.引用規
格
JIS K 3702
2
ISO 6887-1
MOD/変更
JISからの引用事項
は,ISO規格の該当
事項と同等である。
−
JIS B 9922, JIS K 3703-1, JIS K
3703-2, JIS K 3703-3, JIS K
3704, JIS K 3705, JIS K 3706-1,
JIS K 3706-2, JIS K 3800, JIS
K 8008, JIS K 8102, JIS K
8180, JIS K 8230, JIS K 8294,
JIS K 8521, JIS K 8576, JIS K
8913, JIS K 8920, JIS Z 8802
−
MOD/追加
−
用語を規定するため。
規定の適用範囲を明確にするため。
技術的差異はない。
3.定義
精製水及び試薬について
の用語を規定。
−
−
MOD/追加
−
実質的な技術的差異はない。
4.試験施
設
試験設備(試験区域,その
他の区域,施設の位置,設
備の準備及び保守点検)に
ついて規定。
3
JISとほぼ同じ。
MOD/変更
JISを追加した。
実質的な技術的差異はない。
5.設備及
び機器
設備及び機器(培地操作用
キャビネットなど18種類
の設備及び機器)について
規定。
4
JISとほぼ同じ。
MOD/変更
5.1(培地操作用キャ
ビネット)でJISを
追加。
5.4(pH計)でJISを
追加。
5.9.1の寒天の融点は,その精製度合い
などによって調節可能であるため。
ISO規格の次回改正時に提案を予定。
その他は,実質的な差異なし。
31
K 3701:2008
3
1
K
3
7
0
1
:
2
0
0
8
3
1
K
3
7
0
1
:
2
0
0
8
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
(Ⅰ) JISの規定
(Ⅱ) 国際
規格番号
(Ⅲ) 国際規格の規定
(Ⅳ) JISと国際規格との技術的差異
の項目ごとの評価及びその内容
表示箇所:本体
表示方法:点線の下線
(Ⅴ) JISと国際規格との技術的差異の理由
及び今後の対策
項目
番号
内容
項目
番号
内容
項目ごとの
評価
技術的差異の内容
5.設備及
び機器
(続き)
5.4.2(保守点検)で
洗浄の規定を追加。
5.9.1(用途及び使用
法)において、保温
温度の定量表示を定
性表示に変更。
6.作業者
作業者の適格性及び衛生
(感染リスク回避のため
の予防措置)について規
定。
5
JISと同じ。
IDT
−
−
7.器具の
準備
器具の準備(培地試験で用
いる器具の減菌,使い捨て
器具,清浄な器具の管理,
減菌済み器具の管理,汚染
除去及び洗浄)について規
定。
6
JISとほぼ同じ。
MOD/削除
7.5(汚染除去)にお
いて,プラスチックの
焼却規定を削除。
国内法で禁止されているため。
8.培地の
調製及び
滅菌
培地の調製及び減菌(培地
の調製,試薬及び培地の減
菌,保存,寒天培地の融解,
培地の脱気及びシャーレ
ーにおける寒天平板培地
の調製)について規定。
7
JISとほぼ同じ。
MOD/変更
8.4(寒天培地の融解)
において,保温温度
の定量表示を定性表
示に変更。
5.の(Ⅴ)と同じ。
MOD/変更
8.6(シャーレーにお
ける寒天平板培地の
調製)において,寒
天培地の厚さ及び容
量を変更。
ISO規定の寸法・容量では,寒天培地
が薄すぎて過度に乾燥しやすいため。
ISO規格の次回改正時に提案を予定。
32
K 3701:2008
3
2
K
3
7
0
1
:
2
0
0
8
3
2
K
3
7
0
1
:
2
0
0
8
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
(Ⅰ) JISの規定
(Ⅱ) 国際
規格番号
(Ⅲ) 国際規格の規定
(Ⅳ) JISと国際規格との技術的差異
の項目ごとの評価及びその内容
表示箇所:本体
表示方法:点線の下線
(Ⅴ) JISと国際規格との技術的差異の理由
及び今後の対策
項目
番号
内容
項目
番号
内容
項目ごとの
評価
技術的差異の内容
9.試料
試料の取扱い(採取,輸送,
受領及び保存,試験試料並
びに試料の保存と破棄)に
ついて規定。
8
JISとほぼ同じ。
MOD/変更
9.4(試験試料)にお
いて,バイオハザー
ド対策用クラスⅡキ
ャビネットを追加
し,試料を入れる“プ
ラスチック袋”を単
に“袋”に変更。
プラスチック袋の材質及び包装構成が
規定されていないため。
ISO規格の次回改正時に提案を予定。
10.試験
方法及び
試験結果
の表記
試験方法及び試験結果の
表記(予防措置,試料原液
及び希釈液の調製,固形培
地の試験,液体培地の試
験,無菌試験方法及び基本
的な同定法)について規
定。
9
JISとほぼ同じ。
MOD/変更
10.1(予防措置)でバ
イオハザード対策用
クラスⅡを追加し,
10.3.1(平板混釈法)
において,冷却時間
の長さの変更(10 min
を“速やかに”)。
時間を限定する根拠がないため。
ISO規格の次回改正時に提案を予定。
附属書A 推定数の信頼区間
附属書A
JISと同じ。
IDT
−
−
附属書B 最確数(MPN)表
附属書B
JISと同じ。
IDT
−
−
JISと国際規格との対応の程度の全体評価:MOD
備考1. 項目ごとの評価欄の記号の意味は,次のとおりである。
― IDT……………… 技術的差異がない。
― MOD/削除……… 国際規格の規定項目又は規定内容を削除している。
― MOD/追加……… 国際規格にない規定項目又は規定内容を追加している。
― MOD/変更……… 国際規格の規定内容を変更している。
2. JISと国際規格との対応の程度の全体評価欄の記号の意味は,次のとおりである。
― MOD…………… 国際規格を修正している。
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。