2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
日本工業規格 JIS
K 3603-1990
細胞凍結保存用プラスチック製容器
Plastic Vials for Frozen Storage and Ultra Low−Temperature Preservation
1. 適用範囲 この規格は,バイオテクノロジー関連分野において,細胞をその性質を変化させることな
く,−80℃以下で凍結保存するために用いるプラスチック製(1)容器(以下,容器という。)について規定す
る。
注(1) ポリエチレン,ポリプロピレンなど。
備考 この規格の中で { } を付けて示してある単位及び数値は,従来単位によるものであって参考
として併記したものである。
引用規格:
JIS K 0114 ガスクロマトグラフ分析のための通則
JIS K 0211 分析化学用語(基礎部門)
JIS K 0512 水素
JIS K 1107 高純度窒素
JIS K 3600 バイオテクノロジー用語
JIS K 8101 エタノール (99.5) [エチルアルコール (99.5) ](試薬)
JIS Z 9031 ランダム抜取方法
2. 用語の意味 この規格に用いる用語の意味は,JIS K 0114(ガスクロマトグラフ分析のための通則),
JIS K 0211[分析化学用語(基礎部門)]及びJIS K 3600(バイオテクノロジー用語)によるほか,次によ
る。
(1) 滅菌 微生物を殺滅又は除去すること。
(2) 放射線滅菌法 放射性同位元素を含む線源からのガンマ線などの放射線照射によって行う滅菌。
(3) エチレンオキシド滅菌法 エチレンオキシドを含むガスによって行う滅菌。
(4) 電子線滅菌法 電子線照射によって行う滅菌。
3. 種類 容器の種類は,滅菌製品及び未滅菌製品とし,滅菌製品は滅菌法によって3種類とする。
(1) 滅菌製品
(a) 放射線滅菌法によるもの。
(b) エチレンオキシド滅菌法によるもの。
(c) 電子線滅菌法によるもの。
(2) 未滅菌製品
4. 品質 容器の性質は,次のとおりとする。
2
K 3603-1990
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
(1) 外観 肉まわりが平均しており,きず,ひび割れが認められないこと。
(2) 耐低温性 6.2によって試験を行い,異常が認められないこと。
(3) 無菌性 滅菌製品については6.3によって試験を行い,無菌であること。
(4) 残留エチレンオキシド 6.4によって試験を行い,残留エチレンオキシドの値は,受渡当事者間の協定
によること。
(5) 耐放射線 ガンマ線など放射線照射製品については,品質に著しい経時変化が認められないこと。
(6) 密封性 密封性がよいこと。
5. 構造及び寸法
5.1
構造 有栓で,円筒形又はアンプル状で溶封できる構造であること。
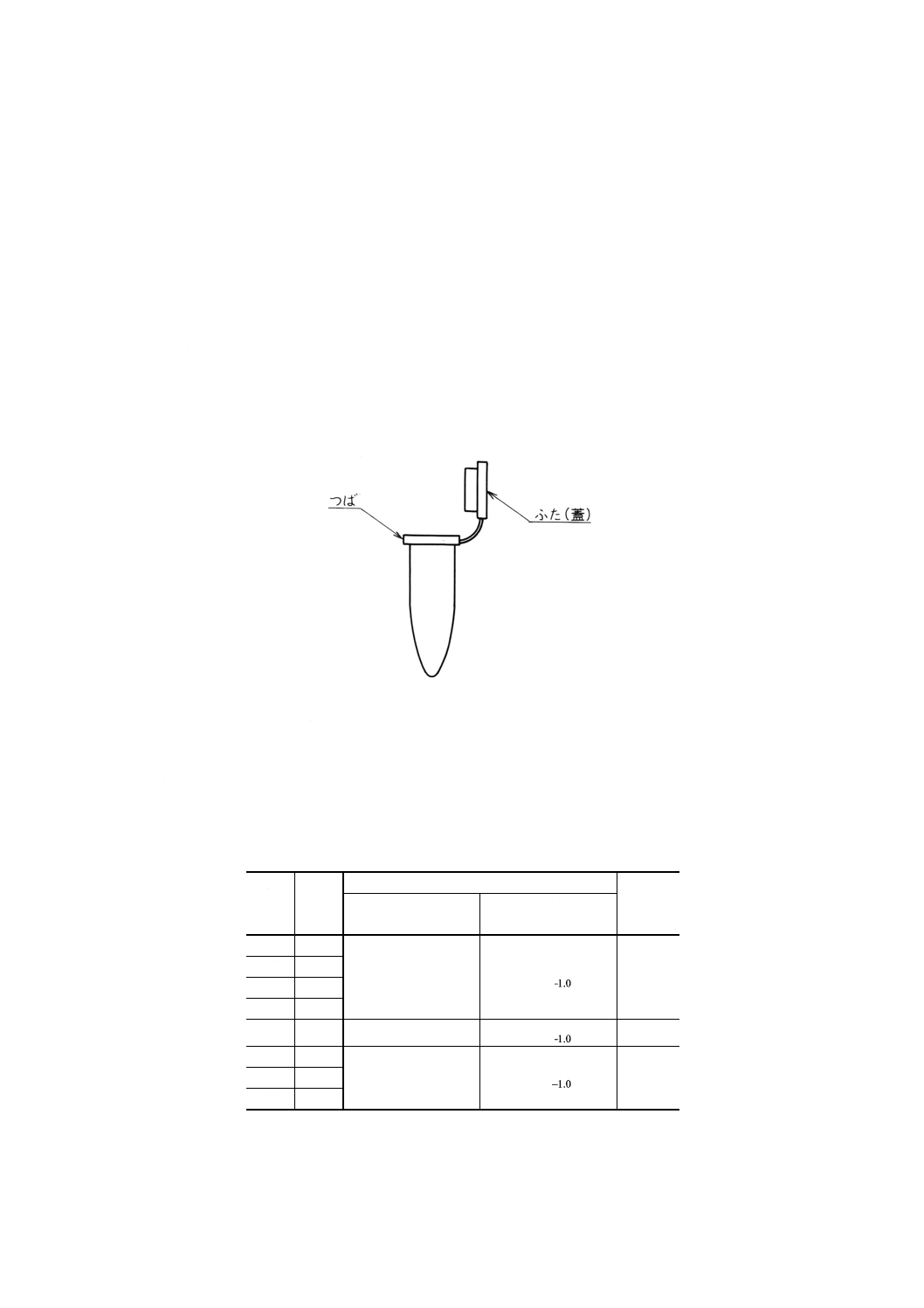
備考1. “つば”付きのものでもよい。“つば”付き容器の例を図1に示す。
図1 “つば”付き容器の一例
2. 密封方式による構造の分類は,次のとおりである。
(a) パッキン,リングなどを用いた構造のもの。
(b) パッキン,リングなどを用いない構造のもの。
(c) 溶封できる構造のもの。
5.2
寸法 容器の寸法は表による。
表 寸法
単位 mm
呼び
記号
呼び
容量
(ml)
外径
高さ
A形
(“つば”付きのもの)
B形
(“つば”なしのもの)
1号
0.5
10.5±0.5
5.00.1
5.
12
+−
25〜50
2号
1.0
3号
1.2
4号
1.5
5号
2.0
10.5±0.5
5.00.1
5.
12
+−
38〜63
6号
3.5
10.5±0.5
5.00.1
5.
12
+−
63〜100
7号
4.0
8号
5.0
6. 試験方法
3
K 3603-1990
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
6.1
試料の採取 試料の採取は,JIS Z 9031(ランダム抜取方法)によって行う。
6.2
耐低温性試験方法 耐低温性試験方法は,次のとおりとする。
(1) 試料容器に容量の21の水を入れる。
(2) その容器を液化窒素が入ったジュワ−瓶(2)の気相中に72時間放置する。
(3) その後,容器を取り出し,直ちに37℃の水(3)に浸せき(漬)する。
(4) 容器内の氷が完全に解凍したら取り出し,容器の異常の有無を観察する。
注(2) 熱の遮断を有効に行える保存容器であること。ガラス製でなくてもよい。
(3) 容器の大きさに対して,十分な量の水であること。
6.3
無菌性試験方法 日本薬局方の無菌試験法に準じる(参考参照)。
6.3.1
培地及びその調製法
(1) 培地の組成(4) 日本薬局方に規定するもの。
注(4) 調製後の培地は必ず密閉状態に保ち,調製後3週間以上経過したものは用いない。
なお,無菌試験用チオグリコール酸培地I,ぶどう糖・ペプトン培地には,市販品がある。た
だし,これを用いるときは毎回性能試験を行わなければらない。
(2) 調製法
(a) 細菌試験用 日本薬局方の規定による。
(b) 真菌試験用 日本薬局方の規定による。
6.3.2
操作 試料容器に6.2.1で調製した無菌試験用培地を容量の21程度加え容器にふたをした後,細菌
の場合には30〜32℃で少なくとも7日間,真菌の場合には20〜25℃で少なくとも10日間ふ卵器中で培養
する。
6.3.3
判定 日本薬局方の規定による。
6.4
残留エチレンオキシド試験方法
6.4.1
概要 試料を細断し抽出容器に入れ,プロピレンオキシドエタノールを加え振り混ぜ,残留エチレ
ンオキシドを抽出し,抽出液についてガスクロマトグラフによって定量を行う。
6.4.2
測定装置・器具及び試薬
(1) 測定装置・器具
(a) ガスクロマトグラフ 水素炎イオン化検出器 (FID) 付きのもの。
(b) 抽出容器 気密性ガラス容器で容量100ml(5)のもの。
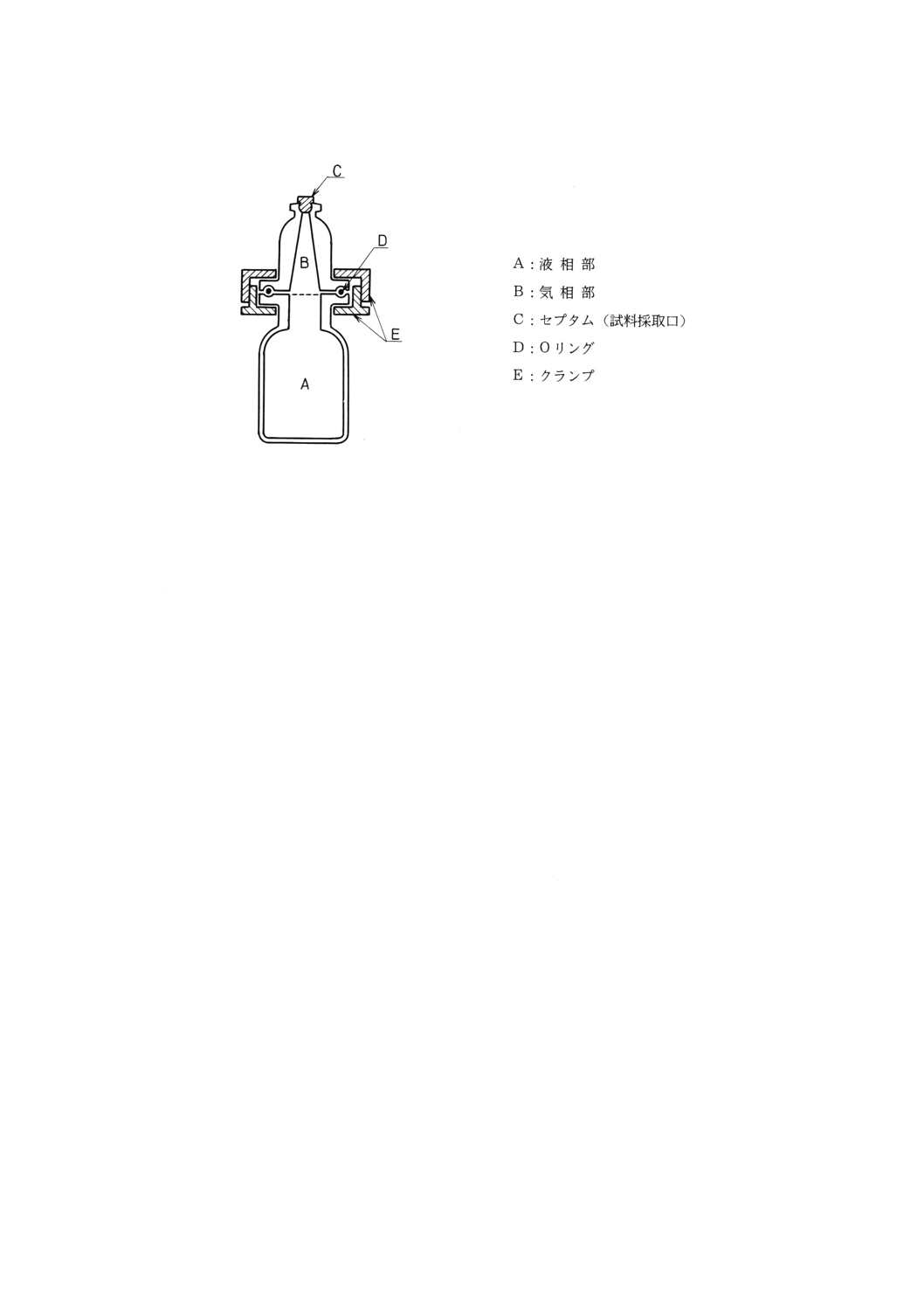
注(5) 例えば,図2に示すようなヘッドスペースボトルが用いられる。
4
K 3603-1990
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
図2 ヘッドスペースボトル(一例)
(2) 試薬
(a) エタノール JIS K 8101〔エタノール (99.5) [エチルアルコール (99.5) ](試薬)〕に規定するも
の。
(b) エチレンオキシドエタノール溶液(100μg/ml) 低温室でエチレンオキシド(6)約1gを1mgのけた
まではかりとり,全量フラスコ100mlに入れ,エタノールを加えて100mlにする。この溶液10ml
を全量フラスコ1 000mlにとり,エタノールで1 000mlにする。
(c) プロピレンオキシドエタノール溶液(200μg/ml) 低温室でプロピレンオキシド(7)約2gを1mgの
けたまではかりとり,全量フラスコ100mlに入れ,エタノールを加えて100mlにする。この溶液10ml
を全量フラスコ1 000mlにとり,エタノールで1 000mlにする。
注(6) エチレンオキシドは沸点10.7℃の低沸点化合物であるから,エチレンオキシドの揮散を防ぐた
め,雰囲気温度を5℃以下に保ち操作を行う。エチレンオキシドエタノール溶液は,市販品のも
のを用いることもできる。
(7) プロピレンオキシドの沸点は35℃であるから,低温室で操作することが望ましい。プロピレン
オキシドエタノール溶液は,市販品を用いてもよい。
6.4.3
分析方法
(1) 試料の調製方法 容器を包装から取り出し5mm角くらいの大きさに切り,その約5gを1mgのけたま
ではかりとり,内標準物質として,6.4.3(3)(b)で作成した検量線の範囲に入るような濃度のプロピレン
オキシドエタノール溶液(200μg/ml) (8)50mlを加えた抽出容器に入れ,70℃で少なくとも6時間恒温振
とう機で振とう後(9),冷蔵庫内(10)に放置する。
注(8) プロピレンオキシドエタノール溶液(200μg/ml)をエタノールで適宜希釈して用いる。
(9) 材質,厚さ,残存量によって抽出時間は異なるので,予備実験によって,6時間振とうで十分
抽出が行われているかを確認する。
(10) 検量線の作成の場合と同一温度を保つ。
(2) 分析条件 分析条件は機器によって異なるので,最適となる分析条件を選び定量を行う。一例を次に
示す。
分析条件の一例
(a) カラム用管 内径3〜4mm,長さ3mのガラス管又はステンレス鋼管
5
K 3603-1990
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
(b) カラム充てん剤 酸洗浄した白色けい藻土担体(粒径177〜250μm)にポリエチレングリコール20M
を約20%被覆したもの。
参考 白色けい藻土担体は,クロモソルブWなどの名で市販されている。
(c) カラム槽温度 40℃
(d) 試料注入口温度 120℃
(e) 検出器 水素炎イオン化検出器
(f) キャリヤーガス JIS K 1107(高純度窒素)に規定する特級の窒素で,流量40ml/min
(g) 燃料ガス JIS K 0512(水素)に規定する1級の水素で,58.8kPa {0.6kgf/cm2}
(h) 助燃ガス 空気で98.1kPa {1.0kgf/cm2}
(3) 操作
(a) 定量 (1)で調製した抽出容器中の気相部分のガス1〜0.5mlを(2)で最適の条件に設定したガスクロ
マトグラフに導入し,得られたクロマトグラムからエチレンオキシドのピーク面積とプロピレンオ
キシドのピーク面積の比を求め,検量線からエチレンオキシド濃度(μg/g)を求める。
(b) 検量線の作成 抽出容器に6.4.2(2) (b)のエチレンオキシドエタノール溶液5mlをとり,プロピレン
オキシドエタノール溶液を,混合液中のエチレンオキシド (EO) とプロピレンオキシド (PO) の濃
度比 (EO/PO) が1.0, 0.8, 0.5, 0.2, 0.1になるように加えた後,全量が50mlになるようにエタノール
を加える。この抽出容器を70℃,6時間加温し冷蔵庫に放置した後,抽出容器の気相部分のガス1ml
を(2)で最適条件に設定したガスクロマトグラフに導入し,得られたクロマトグラムから横軸にエチ
レンオキシド濃度とプロピレンオキシド濃度比 (EO/PO) とを,縦軸にエチレンオキシドのピーク
面積とプロピレンオキシドのピーク面積の比をとって検量線を作成する。
7. 包装 最小包装単位の容器の包装材料には,取扱い中又は輸送中に破れない材質のものを用いる。
8. 表示 容器の外箱又は内包装に,次の事項を表示しなければならない。
(1) 名称及び呼び記号
(2) 材質
(3) 種類
(4) 滅菌法(滅菌製品の場合)
(5) 製造業者名又はその略号
(6) ロット番号
(7) 滅菌年月
9. 取扱い上の注意 容器の取扱いに当たっては,次の事項に注意する。
(1) オートクレーブで滅菌する場合は,変形を防ぐため,キャップを緩めて,121℃で行う。この際荷重が
かからないよう注意する。
(2) エチレンオキシド滅菌をした容器を使用する場合は,エチレンオキシドの残存量を減少させるため,
包装したまま箱から出して2週間ほど放置して使用することが望ましい。
(3) 細胞保存に使用した容器及び内容物の廃棄に当たっては,環境汚染のないよう注意して処理する。
(4) 容器を液化窒素に浸せきすると,内容物へのコンタミネーションのおそれがあり,また容器内に侵入・
残存した液化窒素が急速解凍時に急膨張して爆発するおそれがあるので注意する。
6
K 3603-1990
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
参考
無菌性試験方法[日本薬局方(第十一改正)39無菌試験法]
1. 培地及びその調製法
(1) 培地の組成
(a) 細菌試験用培地(チオグリコール酸培地Ⅰ)
L−シスチン
0.5g
カゼイン製ペプトン
15.0g
カンテン
0.8g
チオグリコール酸ナトリウム
0.5g
塩化ナトリウム
2.5g
レザズリン溶液 (1→1 000)
1.0ml
ぶどう糖
5.0g
水
1 000ml
酵母エキス
5.0g
滅菌後のpHを7.0〜7.2に調整する。
(b) 真菌試験用培地(ぶどう糖,ペプトン培地)
りん酸二水素カリウム
1.0g
硫酸マグネシウム
0.5g
カゼイン製ペプトン
5.0g
酵母エキス
2.0g
ぶどう糖
20.0g
水
1 000ml
滅菌後のpHを5.6〜5.8に調整する。
(2) 調製法
(a) 細菌試験用 水1 000mlにL−シスチン,カンテン,塩化ナトリウム,ぶどう糖,酵母エキス及び
カゼイン製ペプトンを加え,水浴上で加温して溶かし,次にチオグリコール酸ナトリウムを加えて
溶かした後,必要ならば水酸化ナトリウム試液を加え,滅菌後のpHが7.0〜7.2になるように調整
する。必要ならば加温した後,水で潤したろ紙を用いてろ過する。次にレザズリン溶液 (1→1 000) を
加え,よく混和し高圧蒸気滅菌器を用いて121℃で20分間加熱して滅菌した後,直ちに常温に冷却
し,遮光して常温で保存する。保存中に水分が蒸発して流動性に変化が認められたもの,又は上部31
以上が赤色に変わった培地は使用できない。ただし,このように変色した培地でも,水浴上で加温
して赤色部分が31以下になったときは使用して差し支えないが,その後再び31以上が赤色に変わっ
たものは使用してはならない。
(b) 真菌試験用 水1 000mlにりん酸二水素カリウム,硫酸マグネシウム,カゼイン製ペプトン,酵母
エキス及びぶどう糖を加え,水浴上で加温して溶かす。必要ならば水酸化ナトリウム試液を加え,
滅菌後のpHが5.6〜5.8になるように調整する。必要ならば水で潤したろ紙を用いてろ過し,高圧
蒸気滅菌器を用いて121℃で20分間加熱して滅菌する。
2. 判定 試料溶液を培養したものについて肉眼的に菌の発育を認めたときは,不適であると判定する。
ただし,判定が困難なときは,次の方法によって判定する。
(1) 培養したものの内容の一部をとり,直接又は染色して鏡検する。
7
K 3603-1990
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
(2) 培養したものの内容の一部を新たな同種の培地又は適当な培地に移植し,細菌試験にあっては30〜
32℃で少なくとも3日間,真菌試験にあっては20〜25℃で少なくとも7日間培養する。
原案作成委員会の構成
氏名
所属
(委員長)
川 瀬 晃
工業技術院化学技術研究所
寺 西 大三郎*1 通商産業省基礎産業局
増 田 優
通商産業省基礎産業局
細 川 幹 夫*2 工業技術院標準部
海老原 成 圭
工業技術院繊維高分子材料研究所
杉 浦 巳代治
農林水産省農業生物資源研究所
大 野 忠 夫
理化学研究所ライフサイエンスつくば研究センター
赤 木 秀 人*3 財団法人バイオインダストリー協会
笹 川 滋
日本赤十字社中央血液センター
大 場 健 吉
ライオン株式会社生物科学研究所
河 野 源
東レ株式会社基礎研究所
池 永 裕
キリンビール株式会社研究開発部
日 暮 喜八郎
第一化学薬品株式会社
佐 藤 利 男
ラジエ工業株式会社
倉 林 肇
住友ベークライト株式会社医療機器事業部
山 崎 一 也
日本インターメツド株式会社営業部
滝 沢 鼎
株式会社アシスト
田 村 恭 一
岩城硝子株式会社企画室
谷 幸 一
家田貿易株式会社
栗 原 力
財団法人化学品検査協会
(関係者)
浦 野 四 郎
工業技術院標準部繊維化学規格課
飯 嶋 啓 子
工業技術院標準部繊維化学規格課
小 島 益 生
財団法人化学品検査協会
小 林 昭
財団法人化学品検査協会
佐 野 裕 之
日本インターメツド株式会社
伊 藤 登
第一化学薬品株式会社
工 藤 俊 博
ライオン株式会社
荒 谷 靖 博
家田貿易株式会社
鈴 木 克 則
家田貿易株式会社
発足当初の委員は,次のとおり。
*1 阿 部 巳喜雄
*2 桜 井 俊 彦
*3 篠 田 和 男

