K 1200-2 : 2000
(1)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
まえがき
この規格は,工業標準化法に基づいて,日本工業標準調査会の審議を経て,通商産業大臣が制定した日
本工業規格である。
今回の制定は,対応する国際規格に整合させるために,ISO 979 : 1974及びISO 3196 : 1975を基礎とし
て用いた。
これによってJIS K 1200 : 1968は廃止され,JIS K 1200-1〜JIS K 1200-10に置き換えられる。
JIS K 1200-2には,次に示す附属書がある。
附属書1(規定) 中和滴定法
附属書2(規定) 電位差滴定法
附属書3(参考) 注意事項
JIS K 1200は,一般名称を“工業用水酸化ナトリウム”として,次の各部によって構成する。
第1部:比重又は密度の求め方
第2部:全アルカリ,水酸化ナトリウム及び炭酸ナトリウム含有量の求め方
第3部:塩化ナトリウム含有量の求め方−第1節:チオシアン酸水銀 (II) 吸光光度分析方法
第3部:塩化ナトリウム含有量の求め方−第2節:ホルハルト改良法,イオンクロマトグラフ分析方
法
第4部:硫酸ナトリウム含有量の求め方
第5部:けい素含有量の求め方−高周波誘導結合プラズマ発光分光分析方法
第6部:鉄含有量の求め方−原子吸光分析方法,高周波誘導結合プラズマ発光分光分析方法
第7部:アルミニウム含有量の求め方
第8部:カルシウム含有量の求め方−第1節:原子吸光分析方法
第8部:カルシウム含有量の求め方−第2節:高周波誘導結合プラズマ発光分光分析方法
第9部:マグネシウム含有量の求め方−第1節:原子吸光分析方法
第9部:マグネシウム含有量の求め方−第2節:高周波誘導結合プラズマ発光分光分析方法
第10部:マンガン含有量の求め方
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
日本工業規格 JIS
K 1200-2 : 2000
工業用水酸化ナトリウム−
第2部:全アルカリ,水酸化ナトリウム
及び炭酸ナトリウム含有量の求め方
Sodium hydroxide for industrial use−Part 2 :
Determination of total alkalinity, sodium hydroxide and sodium carbonate
序文 この規格は,1974年に第1版として発行されたISO 979 Sodium hydroxide for industrial use−Method of
assay及び1975年に第1版として発行されたISO 3196 Sodium hydroxide for industrial use−Determination of
carbonates content−Titrimetric methodを元に,技術的内容を変更することなく作成した日本工業規格である
が,対応国際規格には規定されていない規定内容(水酸化ナトリウムと炭酸ナトリウムを一度に連続で分
析する方法)を附属書1(規定)として追加した。また,対応国際規格に規定されていない規定項目(電
位差滴定法)を附属書2(規定)として追加した。
なお,この規格で点線の下線を施した箇所は,対応国際規格にはない事項である。
1. 適用範囲 この規格は,工業薬品として用いる水酸化ナトリウムの全アルカリ,水酸化ナトリウム及
び炭酸ナトリウム含有量の求め方について規定する。
備考1. 水酸化ナトリウム及び水酸化ナトリウム液の取扱い上の注意については,附属書3(参考)を
参照する。
2. この規格の対応国際規格を,次に示す。
ISO 979 : 1974 Sodium hydroxide for industrial use−Method of assay
ISO 3196 : 1975 Sodium hydroxide for industrial use−Determination of carbonates content−
Titrimetric method
2. 引用規格 次に掲げる規格は,この規格に引用されることによって,この規格の規定の一部を構成す
る。これらの引用規格は,その最新版(追補を含む。)を適用する。
JIS K 0113 電位差・電流・電量・カールフィッシャー滴定方法通則
JIS K 8001 試薬試験方法通則
JIS Z 8401 数値の丸め方
3. 試験方法 全アルカリ,水酸化ナトリウム及び炭酸ナトリウムの測定法は次の4種とし,そのいずれ
か又は組合せによる。
a) 全アルカリ−中和滴定法(4.による。)
2
K 1200-2 : 2000
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
b) 炭酸ナトリウム−滴定法(5.による。)
c) 水酸化ナトリウム及び炭酸ナトリウム−中和滴定法(附属書1による。)
d) 水酸化ナトリウム及び炭酸ナトリウム−電位差滴定法(附属書2による。)
4. 全アルカリ−中和滴定法
4.1
要旨 指示薬としてメチルオレンジを使用し,塩酸で定量して全アルカリを測定する。
4.2
試料(以下,原液Aという。)の調製
4.2.1
試料の採取 すり合せのふたの付いたガラスひょう量瓶に,NaOHとして40gよりわずかに少ない
量に相当する固形又は液体の分析用試料を0.01gまでひょう量する。
4.2.2
希釈用の水 蒸留した炭酸塩を含まない水又はこれと同等の純度の水を使用する。
4.2.3
調製操作
a) 固形試料 4.2.1の試料を水200mlに溶かす。室温に冷却し,1000ml全量フラスコに移し,標線近く
まで希釈し,再び室温に冷却し,標線に完全に合うまで希釈して混合する。
b) 液体試料 4.2.1の試料を直接1000ml全量フラスコに移し,標線近くまで希釈し,再び室温に冷却し,
標線に完全に合うまで希釈して混合する。
4.3
試薬 試薬は,次による。
a) 1mol/l塩酸 JIS K 8001の4.5(5.1)(1mol/l塩酸)に規定するもの。
b) メチルオレンジ溶液 (0.5g/l) JIS K 8001の4.4(指示薬)に規定するものの2倍希釈液。
4.4
器具 通常の実験室用器具及び次のもの。
a) ピペット50ml ±0.05mlまで正確なもの。
b) ビュレット50ml ml当たり約30滴の滴下が可能な傾斜を備えた液出口をもつもの。
4.5
操作 操作は,次による。
4.5.1
試料採取 原液A50.0mlをピペット4.4 a)によって500mlのコニカルフラスコに採取する。
4.5.2
滴定 これに,50mlの水と,メチルオレンジ溶液を加え,上記ビュレット中の1mol/l塩酸で黄色
からオレンジ色に変色するまで滴定する。
4.6
計算
a) 全アルカリ 水酸化ナトリウムに換算した全アルカリ (%) は,次の式によって計算する。
m
V
m
V
A
80
00
040
.0
100
50
000
1
=
×
×
×
=
ここに, A: 水酸化ナトリウムに換算した全アルカリ(重量%)
V: 滴定に要した1mol/l塩酸の量 (ml)
m: 原液 (A) の質量 (g)
結果は,JIS Z 8401によって小数点以下1けたまで表示する。
b) 水酸化ナトリウム 水酸化ナトリウム(重量%)は,次の式によって計算する。
B=A−1.818b
ここに,
B: 水酸化ナトリウム(重量%)
A: 水酸化ナトリウムに換算した全アルカリ(重量%)
b: 下記の炭酸ナトリウム−滴定法で測定される,炭酸ガス
(CO2) に換算した炭酸塩含有量(重量%)
1.818: CO2を2NaOHに置き換えるためのファクター
結果は,JIS Z 8401によって小数点以下1けたまで表示する。

3
K 1200-2 : 2000
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
5. 炭酸ナトリウム−滴定法
5.1
要旨 試料を塩酸酸性にした後,加熱して炭酸塩を炭酸ガスとして追い出し水酸化バリウム溶液に
吸収させ,過剰の水酸化バリウムを塩酸で逆滴定し定量する。この方法は,炭酸塩含有量が炭酸ガスに換
算して0.01重量%以上のサンプルに適用できる。
次の予備試験によって三つのケースに分類される。
a) 硫化物や塩素酸塩のいずれも含まない水酸化ナトリウム
b) 硫化物を含む水酸化ナトリウム
c) 塩素酸塩を含む水酸化ナトリウム
5.2
予備試験
5.2.1
原理 メチルオレンジを含む試料酸性液を煮沸する。その蒸気に酢酸鉛試験紙片をさらす。硫化物
が存在すると試験紙は黒変し,塩素酸塩が存在するとメチルオレンジの着色が消える。
5.2.2
試薬 試薬は次による。ただし,試薬は分析試薬を使用し,蒸留水又は蒸留水と同等の純度で炭酸
ガスを含まない水を使用する。
a) 6mol/l塩酸 JIS K 8001の4.5(5.1)(6mol/l塩酸)に規定するもの。
b) メチルオレンジ溶液 (0.5g/l) JIS K 8001の4.4(指示薬)に規定するものの2倍希釈液。
c) 酢酸鉛試験紙 約15×80mmの小片に切断する。
5.2.3
操作 20gの試料を300mlのコニカルフラスコに採取する。150mlの水とメチルオレンジ溶液を3
滴添加する。塩酸溶液で中和し,5mlを過剰に添加する。酢酸鉛試験紙片をコニカルフラスコの首の内側
に,フラスコの外側へ曲がって出るように固定する。
溶液を5分間煮沸し,次の表に従って取るべき操作手順を選択する。
外観
ケース
操作手順
溶液
試験紙
赤
白
a
5.3
赤
黒色化
b
5.4
無色
白
c
5.5
5.3
硫化物や塩素酸塩のいずれも含まない水酸化ナトリウム
5.3.1
原理 試料酸性液を加熱し炭酸ガスを遊離させ,ガスの流れに同伴して過剰の水酸化バリウム溶液
に吸収させる。過剰の水酸化バリウムを指示薬チモールフタレインの存在化に標準塩酸溶液で滴定する。
5.3.2
試薬 5.2.2に挙げた試薬及び次に示す試薬とする。
a) 窒素又は炭酸ガスを含まない空気
b) 水酸化バリウム 約0.1mol/l溶液
約15.0gの水酸化バリウム8水塩をひょう量し,水に溶かし,溶液を1000mlの全量フラスコへ移し,
標線まで希釈し混合する。
c) 塩酸 0.1mol/l溶液
d) チモールフタレイン 5g/lの95容量%エチルアルコール溶液
5.3.3
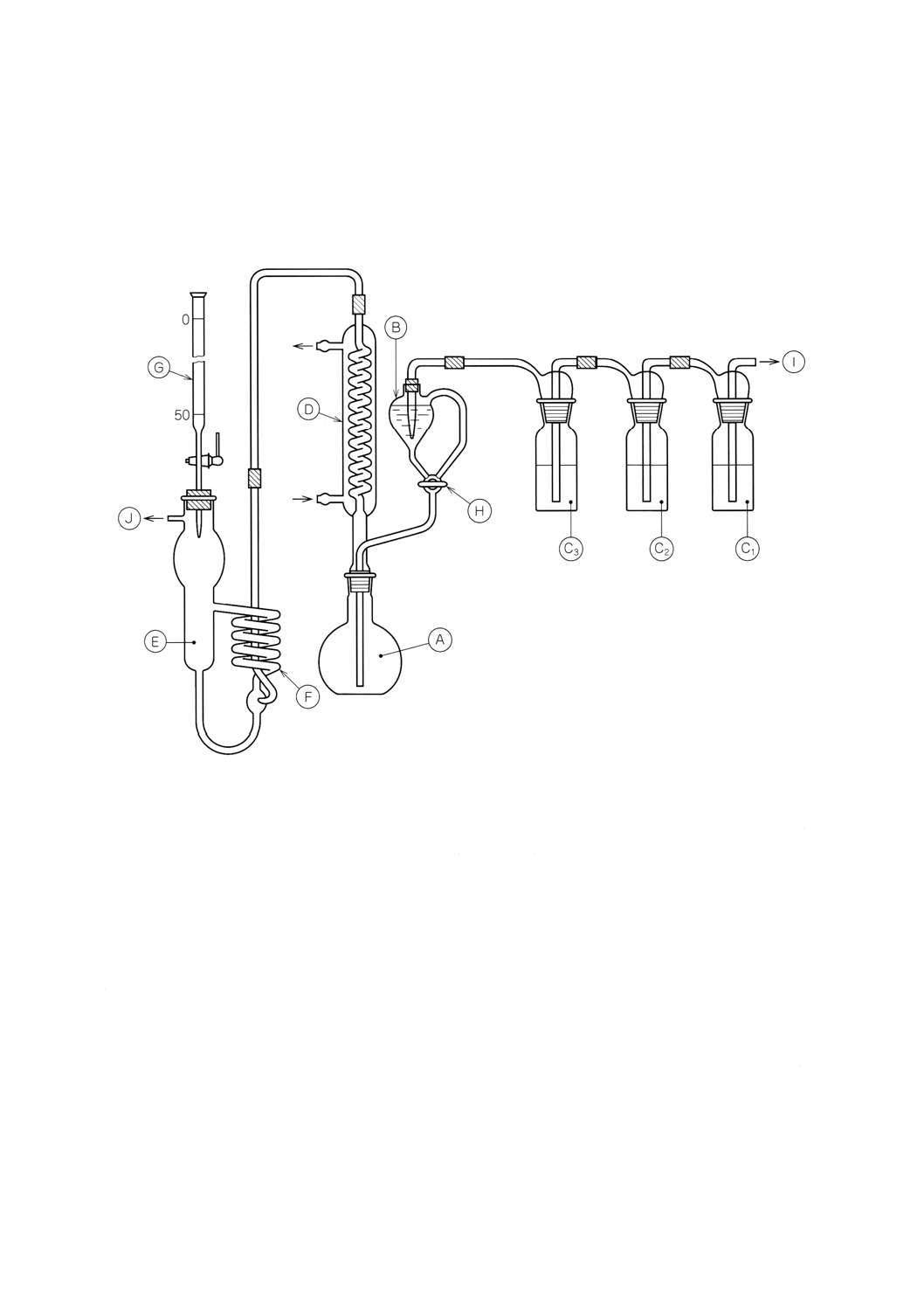
装置 炭酸ガスの遊離,吸収,滴定装置。典型的な装置の例を図1に示す。図の記号を次に示す。
A
フラスコ 500ml容量
B
分液ロート 100ml
C1, C2,C3 ガス洗浄瓶(Drechselタイプ),20重量%の水酸化ナトリウム入り
D
スパイラルコンデンサ
4
K 1200-2 : 2000
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
E
吸収管
F
吸収コイル 最短長さ70cm
G
ビュレット 50ml 0.1mlきざみの目盛付き
H
V字形に穴のあいたストップコック
I及びJ 窒素又は空気の入口と出口
図1 炭酸ナトリウム−滴定法で使用する装置
5.3.4
操作手順
5.3.4.1
試料採取 ふた付きひょう量瓶に試料25gを超えない量の固形又は液体の試料を0.01gの精度で
ひょう量する。このサンプル量からは50mg以上の炭酸ガスは遊離しない。
5.3.4.2
空試験 測定が終わった後に,5.3.4.3に記載の手順に従って空試験を実施する。
5.3.4.3
測定操作
5.3.4.3.1
窒素又は空気を毎秒約5気泡の速度で10分間装置内に流す。
5.3.4.3.2
ガスの流れを停止し,それぞれ次のように添加する。
a) 分液ロート (B) に5.2.2 a)の塩酸溶液90ml
b) フラスコ (A) に5.3.4.1の採取試料,水150ml及び5.2.2 b)のメチルオレンジ溶液3滴
c) 吸収管 (E) に50.00mlの水酸化バリウム溶液とチモールフタレイン溶液を3滴
5.3.4.3.3
装置を閉じ,コンデンサ (D) に水を流し,酸を分液ロート (B) からフラスコ (A) の中へ極め
てゆっくりと指示薬が赤に変わるまで流し込む。
それから更に約5mlの塩酸をストップコック (H) の上に少なくとも数ml残るように注意しながら添加
する。
5
K 1200-2 : 2000
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
5.3.4.3.4
ガスを調節して毎秒2気泡流す。次にこのガスを中断することなく,フラスコ (A) の内容物が
沸騰するまで加熱し,20分間煮沸状態を保つ。熱源を遠ざけ,ガスの流れを毎秒5気泡に増加し,吸収管
(E) の中に入っている過剰の水酸化バリウムをビュレット (G) から標準塩酸溶液を指不薬が青から無色
になるまで落として滴定する。
5.3.5
計算 炭酸ガスの重量%として表示される炭酸塩の含有量は,次の式で示される。
C= (V0−V1) ×T×100/m×0.022=2.2 (V0−V1) Tm
ここに,
C: 炭酸塩の含有量
V0: 空試験に使用した標準塩酸溶液の容積 (ml)
V1: 測定に使用した標準塩酸溶液の容積 (ml)
T: 標準塩酸溶液の規程度で表した実際の濃度
m: 採取試料の重量 (mg)
0.022: 正確に1mol/lの標準塩酸溶液の1mlに相当する炭酸ガス
の重量 (g)
5.4
硫化物を含む水酸化ナトリウム 硫化物を含む水酸化ナトリウムの場合,試料を酸性にすると硫化
水索を遊離し,炭酸ガスと同時に水酸化バリウム溶液に吸収されるので実際の値を上回る結果を与える。
したがって,採取試料の前処理が必要である。
この方法は,kg当たり硫化ソーダ (Na2S) に換算して1g以下の硫化物を含む試料に適用できる。
5.4.1
原理 過酸化水素による硫化物の酸化と試料酸性液の煮沸による。5.3に規定した方法に従い分析
する。
5.4.2
試薬 5.2.2及び5.3.2に挙げた試薬と次に示す試薬とする。
a) 過酸化水素30% (m/m) 溶液
5.4.3
装置 5.3.3参照
5.4.4
操作 次の修正を加えながら,5.3.4.3に規定された操作手順に従う。
5.4.4.1
5.3.4.3.2において採取試料をフラスコ (A) に入れる。次に水150mlと5.4.2 a)の過酸化水素30%
(m/m) 溶液5滴を添加する。
5.4.4.2
5.3.4.3.2において採取試料をフラスコ (A) に酸を添加する前にフラスコの内容物をガスを流し
ながら5分間煮沸し,ついで冷却しメチルオレンジ3滴を添加する。
5.4.5
計算 5.3.5参照
5.5
塩素酸塩を含む水酸化ナトリウム 塩素酸塩を含む水酸化ナトリウムの場合は,試料の酸性化は塩
素ガスの遊離を引き起こし,炭酸ガスと同時に水酸化バリウム溶液に吸収されるので真の値を上回る結果
を与える。したがって,採取試料の前処理が必要である。
5.5.1
原理 硫酸第一鉄溶液添加による塩素酸塩の塩化物への事前還元を行う。
次に5.3に規定した方法に従って測定する。
5.5.2
試薬 5.2.2及び5.3.2に挙げた試薬と次に示す試薬とする。
a) 硫酸第一鉄溶液 100ml中に硫酸第一鉄7水塩28gと塩酸溶液5.2.2 a)4滴を含む。
5.5.3
装置 5.3.3参照
5.5.4
操作 次の修正を加えながら,5.3.4.3に規定された操作手順に従う。
5.5.4.1
5.3.4.3.2においてフラスコ (A) に5.3.4.1の採取試料,水150ml,5.2.2 b)のメチルオレンジ溶液3
滴及び5.5.2 a)の硫酸第一鉄溶液を加え,混合する。
5.5.5
計算 5.3.5参照
6
K 1200-2 : 2000
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書1(規定) 中和滴定法
1. 要旨 試料に塩化バリウムを加え,炭酸塩を炭酸バリウムとして沈殿させた後,両者を分別定量する。
2. 試料溶液の調製 水酸化ナトリウムの一定量を量り取り,水で500mlとし試料溶液を調製する。
水酸化ナトリウム液の場合は,試料を直接量り取る方法によってもよい。
参考 水酸化ナトリウム及び水酸化ナトリウム液の取扱上の注意については附属書3(参考)を参照
する。
2.1
操作 操作は,次のとおり行う。
a) 水酸化ナトリウム約40gを,筒形はかり瓶 (50×70mm) を用いて1mgまで量り取る。
b) 全量フラスコ500mlに,二酸化炭素を含まない水で洗い移し,標線の近くまで薄めて,振り混ぜた後,
室温まで冷却する。
c) 水で標線を合わせ,よく振り混ぜる。
3. 試薬 試薬は,次による。
a) 塩化バリウム溶液 (100g/l) JIS K 8001の4.2(試薬溶液)に規定するもの。
b) フェノールフタレイン溶液 (10g/l) JIS K 8001の4.4(指示薬)に規定するもの。
c) 1mol/l塩酸 JIS K 8001の4.5(5.1)(1mol/l塩酸)に規定するもの。
d) 0.1mol/l塩酸 JIS K 8001の4.5(5.5)(0.1mol/l塩酸)に規定するもの。
e) 0.1mol/l水酸化ナトリウム溶液 JIS K 8001の4.5(19.4)(0.1mol/l水酸化ナトリウム溶液)に規定する
もの。
4. 器具
a) 共栓付き三角フラスコ,300ml
5. 操作
5.1
二酸化炭素を含まない水約50mlを加えた共栓付き三角フラスコ300mlに,試料の適量(1)を0.1mgま
ではかり取り(2),共栓をする。
注(1) 水酸化ナトリウムの場合は,2.の試料溶液の20mlを全量ピペットを用いてはかり取る。水酸化
ナトリウム液の場合は,洗浄乾燥したプラスチック製注射筒2.5mlを用いて2.1mlを採取して
0.1mgまで量り,共栓付き三角フラスコ300mlに注入後,再び注射筒をはかりその質量差を,試
料の質量とする。
(2) 大気中の二酸化炭素を吸収しないように速やかに操作を行う。
5.2
塩化バリウム溶液 (100g/l) 10mlを加え,共栓をし,静かに振り混ぜる。
5.3
指示薬としてフェノールフタレイン溶液 (10g/l) 数滴を加え,静かに振りながら1mol/l塩酸で,微
紅色が消失する少し前まで滴定し,その所要量を読み取る。
5.4
引き続き,0.1mol/l塩酸で滴定し,微紅色が消失した点を終点とする。
5.5
次に,0.1mol/l塩酸10〜15mlを正しく加えた後,沸石を入れて,約5分間静かに煮沸する。
7
K 1200-2 : 2000
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
5.6
室温に冷却した後,0.1mol/l水酸化ナトリウム溶液で,微紅色になるまで滴定する。
6. 計算 水酸化ナトリウム及び炭酸ナトリウムは,次の式によって算出する。
100
0400
.0
)
10
/
(
2
2
1
1
×
×
×
+
=
W
f
V
f
V
A
ここに,
A: 水酸化ナトリウム (NaOH) %
V1: 滴定に要した1mol/l塩酸の量 (ml)
f1: 1mol/l塩酸のファクター
V2: 滴定に用いた0.1mol/l塩酸の量 (ml)
f2: 0.1mol/l塩酸のファクター
W: 試料の質量 (g)
100
00530
.0
)
(
3
4
2
3
×
×
×
−
×
=
W
f
V
f
V
B
ここに,
B: 炭酸ナトリウム (Na2CO3) %
V3: 0.1mol/l塩酸の添加量 (ml)
f2: 0.1mol/l塩酸のファクター
V4: 逆滴定に要した0.1mol/l水酸化ナトリウム溶液の量 (ml)
f3: 0.1mol/l水酸化ナトリウム溶液のファクター
W: 試料の質量 (g) (3)
注(3) 水酸化ナトリウム(固形かせいソーダ)の場合
2.1 a)において量り取った,試料の質量 (g) ×500
20
8
K 1200-2 : 2000
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書2(規定) 電位差滴定法
1. 要旨 試料を水に溶解した後,塩酸を用いて電位差滴定を行い,水酸化ナトリウムと炭酸ナトリウム
を定量する。
2. 試薬 試薬は,次による。
a) 1mol/l塩酸 JIS K 8001の4.5(5.1)(1mol/l塩酸)に規定するもの。
b) 0.02mol/l塩酸 JIS K 8001の4.5(5.7)(0.02mol/l塩酸)に規定するもの。
3. 装置及び器具 電位差滴定装置は,JIS K 0113の5.1(装置)に規定するものとし,滴定槽は,窒素ガ
スシールができるものとする。
4. 操作 操作は,次のとおり行う。
4.1
試料の適量(水酸化ナトリウムの場合は約1.6g,水酸化ナトリウム液の場合は約3.2g)を0.1mgまで
はかり取り,二酸化炭素を含まない水で滴定槽200mlに洗い移す。
4.2
電極が液に浸り,回転子に支障のない程度に二酸化炭素を含まない水を加えて溶解希釈し,スター
ラー上にセットする。
4.3
滴定条件を設定し(1),1mol/lの塩酸を設定した電位まで定量注入した後,0.02mol/lの塩酸で滴定を
行い,電位差の変化率が最大となる2点の変曲点を求め,水酸化ナトリウムと炭酸ナトリウムの滴定量を
求める。
注(1) この滴定は,変曲点が2点必要なため滴定曲線によって検討を行い,適切な滴定条件を決めるか,
又はおおまかな滴定(予備滴定)を行って滴定条件の特性を知り,適切な滴定条件を自動的に
算出し,メモリーさせる方法などによって決定する。
5. 計算 水酸化ナトリウム,炭酸ナトリウムは,次の式によって算出する。
100
0400
.0
)
02
.0
02
.0
3
2
2
2
1
1
×
×
×
−
×
+
=
W
V
f
V
f
V
f
A
ここに,
A: 水酸化ナトリウム (NaOH) (%)
f1: 1mol/l塩酸のファクター
V1: 定量注入に要した1mol/l塩酸の量 (ml)
f2: 0.02mol/l塩酸のファクター
V2: 第1変曲点までに要した0.02mol/l塩酸の量 (ml)
V3: 第1変曲点から第2変曲点までに要した0.02mol/l塩酸の量 (ml)
W: 試料の質量 (g)
100
1060
.0
02
.0
3
2
×
×
×
=
W
V
f
B
ここに,
B: 炭酸ナトリウム(Na2CO3) (%)
f2: 0.02mol/l塩酸のファクター
V3: 第1変曲点から第2変曲点までに要した0.02mol/l塩酸の量 (ml)
W: 試料の質量 (g)
9
K 1200-2 : 2000
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書3(参考) 注意事項
この附属書(参考)は,本体及び附属書の規定に関連する事柄を補足するもので,規定の一部ではない。
1. 一般的注意事項
a) 水酸化ナトリウム及び水酸化ナトリウム液は,毒物及び劇物取締法によって劇物として規定されてい
るので法規に従い,取扱いには十分な注意が必要である。
b) 試料容器は,運搬に適するもので,かつ,容器の破損が起きにくい構造,材質のものとする。
c) 試料採取作業員には,あらかじめ水酸化ナトリウム及び水酸化ナトリウム液取扱い時の危険性を十分
に教育し,危険に対する注意を指示しておく。
d) 試料採取は危険を伴うから,必要な保安上の知識をもつ者によって,又はその監督下に行わなければ
ならない。
e) 試料採取作業に当たっては,保護眼鏡,ゴム手袋,ゴム靴,ビニル衣などの保護具を着装すること。
また,ミストや粉じんが飛散する所では,防じんマスクを着用する。
2. 試料採取上の注意事項
a) パイプラインから試料を採取する場合は,水酸化ナトリウム液が漏えい及び飛散するおそれがあるた
め,採取量を明確にし,かつ,流量を適切に調整できるようにしておくこと。
b) 事故の際,試料採取場所の安全を確保するため,バルブなどによる流量の調整ができるように配慮し
ておくことが望ましい。
c) 漏えいした水酸化ナトリウム液を安全に集めることのできる容器(砂,炭酸水素ナトリウムなどを一
緒に回収が可能なもの)を用意し,かつ,試料採取作業員を保護するため,水酸化ナトリウム液の飛
散を防ぐような配慮が望ましい。
d) 水酸化ナトリウム及び水酸化ナトリウム液には,爆発性及び引火性はないが,両性金属などと反応す
ると水素を発生し爆発するおそれがあるので,万一容器の破損に備え,酸,金属,爆発,有機過酸化
物などからは離しておくことが望ましい。
10
K 1200-2 : 2000
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
解説表2 ソーダ関係製品JIS原案作成委員会 構成表
氏名
所属
(委員長)
松 野 武 雄
横浜国立大学名誉教授
(委員)
西 出 徹 雄
通商産業省基礎産業局化学課
大 嶋 清 治
通商産業省工業技術院標準部
高 橋 和 夫
通商産業省製品評価技術センター
中 村 進
物質工学工業技術研究所
橋 本 繁 晴
財団法人日本規格協会
神 代 啓
社団法人日本化学工業協会
並 木 昭
財団法人化学品検査協会
吉 田 儀 章
化成品工業協会
渡 辺 浄 光
日本石鹼洗剤工業会
堀 定 男
日本製紙連合会
佐 藤 邦 弘
日本化学工業株式会社
湯 村 崇 男
日本化学繊維協会
一 戸 正 憲
社団法人日本水道協会
橋 本 俊 夫
旭硝子株式会社
小 野 宏
旭化成工業株式会社
安 食 亮 伍
旭化成工業株式会社
西 尾 圭 司
日本曹達株式会社
片 岡 基
株式会社トクヤマ
藤 井 昇
鶴見曹達株式会社
須 永 忠 典
日本ソーダ工業会
(事務局)
三 須 武
社団法人日本化学工業協会
内 田 幹 雄
社団法人日本化学工業協会
ソーダ関連製品JIS分科会 構成表
氏名
所属
(主査)
小 野 宏
旭化成工業株式会社
橋 本 俊 夫
旭硝子株式会社
安 食 亮 伍
旭化成工業株式会社
大 津 健 治
ダイソー株式会社
親宮領 宏
鐘淵化学工業株式会社
西 尾 圭 司
日本曹達株式会社
鈴 木 邦 彦
東亜合成株式会社
片 岡 基
株式会社トクヤマ
武 居 弘 記
東ソー株式会社
藤 井 昇
鶴見曹達株式会社
(事務局)
須 永 忠 典
日本ソーダ工業会
三 須 武
社団法人日本化学工業協会
宮 越 正 行
日本ソーダ工業会
(文責 西尾圭司)

