K 0463:2009
(1)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
目 次
ページ
1 適用範囲························································································································· 1
2 引用規格························································································································· 1
3 用語及び定義 ··················································································································· 1
4 原理······························································································································· 3
5 組換え培養細胞 ················································································································ 3
6 試薬······························································································································· 3
7 器具及び機器 ··················································································································· 4
8 サンプリング,前処理及び試料調製 ····················································································· 4
8.1 サンプリング ················································································································ 4
8.2 前処理 ························································································································· 4
8.3 標準液の調製 ················································································································ 4
8.4 試料調製 ······················································································································ 4
9 細胞の管理 ······················································································································ 5
9.1 一般 ···························································································································· 5
9.2 細胞の起眠 ··················································································································· 5
9.3 細胞の継代培養 ············································································································· 5
9.4 細胞の保存 ··················································································································· 5
10 測定操作 ······················································································································· 5
10.1 一般 ··························································································································· 5
10.2 は(播)種操作 ············································································································ 6
10.3 暴露操作 ····················································································································· 6
10.4 洗浄操作 ····················································································································· 6
10.5 検出操作 ····················································································································· 6
11 分析方法のバリデーション(妥当性確認) ·········································································· 6
11.1 一般 ··························································································································· 6
11.2 精度プロファイル ········································································································· 6
11.3 検出下限 ····················································································································· 7
11.4 定量範囲 ····················································································································· 7
12 計算 ····························································································································· 8
12.1 検量線 ························································································································ 8
12.2 測定試料の定量 ············································································································ 8
13 日常精度管理 ················································································································· 9
14 検査報告書 ···················································································································· 9
附属書A(参考)サンプリング及び前処理 ··············································································· 11
附属書B(参考)細胞培養のフローチャート············································································· 13
K 0463:2009 目次
(2)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
ページ
附属書C(参考)測定操作例 ································································································· 14
附属書D(参考)誤差要因及び妨害要因並びにその対策 ····························································· 15
附属書E(参考)レセプターアッセイの分類············································································· 17
K 0463:2009
(3)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
まえがき
この規格は,工業標準化法に基づき,日本工業標準調査会の審議を経て,経済産業大臣が制定した日本
工業規格である。
この規格は,著作権法で保護対象となっている著作物である。
この規格の一部が,特許権,出願公開後の特許出願,実用新案権又は出願公開後の実用新案登録出願に
抵触する可能性があることに注意を喚起する。経済産業大臣及び日本工業標準調査会は,このような特許
権,出願公開後の特許出願,実用新案権及び出願公開後の実用新案登録出願にかかわる確認について,責
任はもたない。
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
日本工業規格
JIS
K 0463:2009
アリル炭化水素受容体結合レポーター遺伝子アッセ
イ通則−ダイオキシン類のAhRアッセイ
Guidelines for reporter gene assay binding on arylhydrocarbon
receptor-Assay of Dioxins in an Ah Receptor
1
適用範囲
この規格は,工業用水,工場敷地,産業活動によって生じる排ガス,ばいじん,燃え殻,工場排水,汚
染土壌及び汚染底質中のダイオキシン類及びその類縁化合物を,ほ乳類由来の組換え培養細胞を用いたア
リル炭化水素受容体結合レポーター遺伝子アッセイによって定量分析する場合の通則について規定する。
2
引用規格
次に掲げる規格は,この規格に引用されることによって,この規格の規定の一部を構成する。これらの
引用規格は,その最新版(追補を含む。)を適用する。
JIS K 0461 競合免疫測定方法通則
JIS K 0557 用水・排水の試験に用いる水
JIS K 1106 液化二酸化炭素(液化炭酸ガス)
JIS K 3600 バイオテクノロジー用語
JIS K 3603 細胞凍結保存用プラスチック製容器
JIS K 3800 バイオハザード対策用クラスⅡキャビネット
JIS K 3801 除菌用HEPAフィルタの性能試験方法
JIS K 3802 膜用語
JIS Z 8122 コンタミネーションコントロール用語
JIS Z 9021 シューハート管理図
3
用語及び定義
この規格で用いる主な用語及び定義は,JIS K 0461,JIS K 3600,JIS K 3802及びJIS Z 8122によるほ
か,次による。
3.1
ダイオキシン類及びその類縁化合物
アリル炭化水素受容体に結合することのできるPCDDs (polychlorodibenzo-p-dioxins),PCDFs
(polychlorodibenzofurans),ダイオキシン様(よう)PCB (dioxin-like PCB) 及びその他のハロゲン化芳香族
炭化水素類。
3.2
アリル炭化水素受容体 (arylhydrocarbon receptor)
2
K 0463:2009
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
ダイオキシン類などの多環芳香族炭化水素をリガンドとする受容体。芳香族炭化水素受容体
(aromatichydrocarbon receptor)ともいい,Ah受容体やAhRと略すこともある。
注記1 通常細胞質にhsp90複合体として存在し,リガンドの結合によってhsp90が離れ,核内に移
行し,ARNT (arylhydrocarbon receptor nuclear translocator) というたん白質と複合体を形成して,
ダイオキシン応答配列 (DRE) に結合する。この結合によって下流にあるCYP1A1遺伝子な
どの転写活性化が誘導される。
注記2 ダイオキシン類の生体影響の多くは,この受容体とリガンドとが結合することによって引き
起こされる。
3.3
レポーター遺伝子 (reporter gene)
遺伝子産物又はその反応物を検出・定量するため,プロモーター下流に配置された遺伝子。通常ルシフ
ェラーゼなどの酵素遺伝子が用いられる。
3.4
相対発光量 (RLU : relative light unit)
発光光度計によって検出・測定された光子の量を示す値。
注記 測定機器の特性からサンプル由来の光子の絶対量を測定することは困難であるため,一般には
検出器によって測定された光子の量を示す値を相対値 (RLU) として用いる。
3.5
ダイオキシン応答配列 (DRE : dioxin responsive element)
アリル炭化水素受容体とリガンドとの結合体及びARNTから成る複合体が特異的に結合する遺伝子の塩
基配列部分。
3.6
ルシフェラーゼ (luciferase)
ホタル,ウミシイタケなどから得られる生物発光反応を触媒する酵素の総称。ルシフェラーゼの基質と
なり,酸化分解によって光を発する化学物質を総称してルシフェリンという。
3.7
継代培養 (subculture)
凍結保存した細胞又は培養した細胞の一部を分取して,別の新鮮な培地に移植して培養を繰り返す操作。
用いる細胞は,無限又は有限の細胞分裂能があるが,継代 (Passage) していくうちに細胞の性質が変化し
ていくことがある。このため,安定した結果を得るために継代回数が一定数以下の細胞だけを用いる。
3.8
起眠 (initial culture)
凍結保存しておいた細胞を用いて培養を開始する操作。
3.9
EC50 (50 % effective concentration)
化学物質の生物学的影響,例えば,レポーター遺伝子アッセイにおけるルシフェラーゼ由来の発光量を
測定した場合に,その化学物質によって生じる最大の影響を100 %としたとき,50 %の影響を与える濃度。
3.10
試料における定量下限 (minimum limit of determination in samples)
定量が可能な試料中の分析対象成分の最小濃度。用いた試料の量及び標準物質(6.3参照)における検出
3
K 0463:2009
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
下限から理論的に算出する。
3.11
相対活性 (relative potency)
標準物質のアッセイ応答に対する,分析対象成分の個々の物質(異性体)のアッセイ応答の度合い。
4
原理
分析対象成分による生体内でのAh受容体結合を介した遺伝子発現誘導メカニズムを活用し,組換え細
胞を用いて,試料中の分析対象成分に応答した遺伝子によって生成されるルシフェラーゼなどの活性(発
光量)を測定することによって,分析対象成分の濃度を定量する方法である。
この方法では,外来レポーター遺伝子であるルシフェラーゼ遺伝子に,ダイオキシン応答配列 (DRE) を
つないだDNAを細胞内に安定的に挿入した組換え培養細胞を用いる。分析対象物質がAh受容体と結合し,
生じた複合体がDREに結合し,下流の遺伝子を転写活性化した結果,発現するルシフェラーゼの活性に基
づく発光量を発光光度計によって測定する。検量は,標準物質(6.3参照)の溶液を用いて行う。
5
組換え培養細胞
アッセイに使用するほ乳類由来の組換え培養細胞には,ヒト,マウス,ラット,モルモットなどのほ乳
類由来の培養細胞に,ヒト,マウス,ラット,モルモットなどのほ乳類由来のダイオキシン応答配列 (DRE)
を含むプロモーターにルシフェラーゼレポーター遺伝子を融合したプラスミドを導入したものを用いる。
注記 使用する組換え細胞の作製例を次に示す。
a) 組換え培養細胞H1L6.1c2:ホタルのルシフェラーゼ遺伝子の上流域に4個のダイオキシン
応答配列DREを含むシトクロムP450 (CYP1A1) プロモーターをもつプラスミド
pGudLuc6.1をマウス肝ガン細胞 (Hepa1c1c7) に導入した組換え細胞。
b) 組換え培養細胞101L:3個のダイオキシン応答配列DREを含むヒトのシトクロムP450
(CYP1A1) プロモーターにホタルのルシフェラーゼ遺伝子と融合した5' 隣接配列が安定的
に統合されたプラスミドpL1A1Nを,ヒト肝細胞由来HepG2に導入した組換え細胞。
c) 組換え培養細胞HeB5:ラットグルタチオンS-トランスフェラーゼYaサブユニット遺伝子
の転写調節領域にあるダイオキシン応答配列をプラスミドpGL3のホタルのルシフェラー
ゼ遺伝子上流域に含むプラスミドpGL3-chTATA-YaXRE×5-bsdを,マウス肝由来Hepa-1
細胞に導入した組換え細胞。
d) 組換え培養細胞H4IIE-luc:ホタルのルシフェラーゼ遺伝子の上流域に4個のダイオキシン
応答配列DREを含むシトクロムP450 (CYP1A1) プロモーターをもつプラスミド
pGudLuc1.1を,ラット肝ガン細胞 (H4IIE) に導入した組換え細胞。
6
試薬
測定に用いる試薬は,次による。ただし,これ以外に前処理で必要となる試薬は,空試験などによって
測定に支障のないことを,また,培養に用いる試薬は細胞に影響を与えないことを確認してから用いる。
6.1
培地 基礎培地に,別途ウシ胎児血清,抗生物質などを添加したもの。使用時に微生物の増殖,マ
イコプラズマなどによる汚染がないことを確認して用いる。
6.2
トリプシン 細胞培養用又は同等の品質のものを用いる。細胞培養用として市販されているトリプ
シン溶液を用いてもよい。
4
K 0463:2009
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
6.3
標準物質 標準物質は,市販されている2,3,7,8-TeCDD (2,3,7,8-tetrachlorodibenzo-p-dioxin) のうち,
可能な限りトレーサビリティが保証され,純度の高いものを用いる。
6.4
水 JIS K 0557に規定するA4若しくはA3の水又はこれらと同等の品質のもの。細胞培養に用いる
場合は,必要に応じて,孔径0.22 μmのメンブランフィルタなどを通すろ過滅菌又は高圧蒸気滅菌を行っ
て用いる。
6.5
二酸化炭素 JIS K 1106に規定する3種のもの,又はこれと同等の品質のもの。
6.6
緩衝液 緩衝液にはJIS K 0461に規定するりん酸緩衝生理食塩水 (PBS:pH7.6),又はこれと同等の
品質のものを用いる。細胞培養に用いる場合には,必要に応じて,孔径0.22 μmのメンブランフィルタな
どを通すろ過滅菌又は高圧蒸気滅菌を行って用いる。
6.7
細胞凍結保存液 凍結による細胞障害を防ぐ目的で添加する。ジメチルスルホキシド (DMSO) を主
成分とする滅菌した溶液。細胞を凍結保存する目的で開発された市販の細胞凍結保存液を用いてもよい。
6.8
細胞溶解液 細胞溶解作用によって,細胞内の成分を溶液中に放出させる目的で添加する。界面活
性剤を主成分とすることが多い。ルシフェラーゼ活性を阻害する成分を含んではならない。市販されてい
るルシフェラーゼ活性測定キットを用いてもよい。
7
器具及び機器
測定に用いる器具及び機器は,次による。
7.1
CO2インキュベーター 飽和湿度及び二酸化炭素の濃度5 %(体積分率)で,37±1 ℃に調節でき
るもの。
7.2
安全キャビネット JIS K 3800に規定するもの,又は同等以上の性能をもつもの。
7.3
クリーンベンチ JIS K 3801によって試験を行ったとき,粒径0.3 μm以上のジオクチルフタレート
(DOP) 粒子の最大透過率が0.01 %以下のHEPAフィルタを備えたもの。
7.4
血球計算盤 プラスチック製又はガラス製で,赤血球数の算定に用いられるもの。
7.5
細胞凍結保存用プラスチック製容器 JIS K 3603に規定するもの,又はこれと同等のもの。
7.6
細胞培養容器 細胞培養が可能なことを確認済みの滅菌したフラスコ又はペトリ皿。
7.7
液体窒素保存容器 細胞の長期凍結保存ができるもの。
7.8
超低温フリーザー 機器仕様で,−80 ℃以下,−150 ℃以下などの超低温が保てるもの。
8
サンプリング,前処理及び試料調製
8.1
サンプリング
サンプリングを行う試料媒体並びに目的に応じた採取量及び採取時間を十分に考慮して代表試料を採取
する。その例を附属書Aに示す。
8.2
前処理
採取した試料は,抽出及びクリーンアップによって,分析対象成分の定量に影響を及ぼす物質を除去す
る。その例を附属書Aに示す。
8.3
標準液の調製
標準物質を,細胞培養培地と均一な混合が可能で,ジメチルスルホキシド (DMSO) など細胞に対する
毒性の少ない適切な溶媒に溶かして標準液列を調製する。
8.4
試料調製
試料の前処理によって得られた分析対象成分を含む溶液は,標準液調製と同一の溶媒に転溶する。
5
K 0463:2009
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
9
細胞の管理
9.1
一般
細胞の管理を行うには,専門家(又は教育及び訓練を受けたもの)及び専門施設が必要である。
細胞の取扱い方法を9.2〜9.4に示すが,これに限定されるものではなく,使用細胞に最適な方法によっ
て実施すべきである。細胞を取り扱うすべての作業は,雑菌汚染が生じないよう,クリーンベンチ又は安
全キャビネット内で,無菌的に行う。例として一般的な細胞培養のフローチャートを附属書Bに示す。
9.2
細胞の起眠
9.2.1
細胞の解凍
液体窒素保存容器又は超低温フリーザーから取り出した細胞凍結保存用プラスチック製容器中の凍結細
胞を,37 ℃で急速に解凍し,培地を加えて細胞懸濁液を調製する。37 ℃に温めた培地を凍結細胞に加え
て解凍し,細胞懸濁液を調製してもよい。
9.2.2
細胞の培養
細胞懸濁液を細胞培養容器に入れ,細胞を拡散させた後,CO2インキュベーターに入れて培養する。使
用細胞に最適な期間培養し,細胞を増殖させる。
9.2.3
細胞の品質確認
継代培養によって細胞が安定した増殖を示すことを確認した後,培地の濁り,細胞はく離などの雑菌汚
染による異常がないことを確認した後,標準物質への応答能を評価し,適切な応答性を示した細胞を実試
料の測定に用いる。
9.3
細胞の継代培養
9.3.1
細胞のはく離
CO2インキュベーターから細胞培養容器を取り出し,培地を吸引除去する。容器壁面を緩衝液で洗浄し,
吸引除去後,トリプシンを加え細胞となじませる。トリプシンで1〜10分間処理した後,容器壁面の細胞
を容器からはく離させる。適切な量の培地をはく離させた細胞に加えて,細胞懸濁液を調製する。
9.3.2
細胞の培養
細胞懸濁液の細胞数を血球計算盤で計測した後,新しい培地と適切な細胞数の細胞懸濁液とを混合し,
新しい細胞培養容器に加える。細胞培養容器をCO2インキュベーターに入れ,使用細胞に最適な期間培養
し増殖させる。
細胞の継代回数は,細胞の起眠後使用細胞ごとに定められた上限回数までとし,上限に達した場合は,
凍結細胞を新しく解凍して,9.2から実施する。
9.4
細胞の保存
9.4.1
細胞凍結保存用細胞懸濁液の調製
9.3.1の方法で細胞培養容器からはく離した細胞に,使用細胞に最適な方法で細胞凍結保存液を添加して,
細胞凍結保存用細胞懸濁液を調製する。
9.4.2
細胞の凍結保存
調製した細胞凍結保存用細胞懸濁液を,細胞凍結保存用プラスチック製容器に分注し,使用細胞に最適
な条件で凍結する。凍結した細胞は,液体窒素保存容器又は超低温フリーザー中で保存する。
10 測定操作
10.1 一般
この操作を行うには,専門家(又は教育及び訓練を受けたもの)及び専門施設が必要である。
6
K 0463:2009
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
測定操作方法を,10.2〜10.5に示すが,これに限定されるものではなく,使用細胞に最適な方法によっ
て実施すべきである。10.2〜10.4の操作は,クリーンベンチ又は安全キャビネット内で行う(特に10.3〜
10.4の操作は,安全キャビネット内で行う。)。
10.2 は(播)種操作
細胞培養容器から細胞をはく離し,血球計算盤で細胞数を計測し,適正な細胞数になるように培地を用
いて調節する。細胞培養容器に,使用細胞に応じた適切量の細胞懸濁液を分注し,培養する。
10.3 暴露操作
検量線作成用標準物質及び測定用試料をそれぞれ培地と混合し,細胞培養容器に添加する。その後,CO2
インキュベーターに入れ,使用細胞に応じた適切な時間暴露を行う。
10.4 洗浄操作
暴露後,培地を除去し,使用細胞に応じた適切な緩衝液で細胞培養容器を洗浄する。
10.5 検出操作
使用細胞に応じた適切な量の細胞溶解液及びルシフェリンを細胞培養容器に加え,発光量を測定する。
具体的手順は,使用細胞に応じて,技術提供元の指示に従って実施する。
注記 アリル炭化水素受容体結合レポーター遺伝子アッセイの測定操作の例を,フローチャートで附
属書Cに示す。
11 分析方法のバリデーション(妥当性確認)
11.1 一般
データの質を保証するために,新たに導入したレポーター遺伝子アッセイでは,分析方法のバリデーシ
ョン(妥当性確認)を実施し,箇条13において使用する工程平均及び定量値の標準偏差を求める。さらに,
11.2〜11.4に示した方法によって,精度プロファイル,検出下限及び定量範囲を求める。
11.2 精度プロファイル
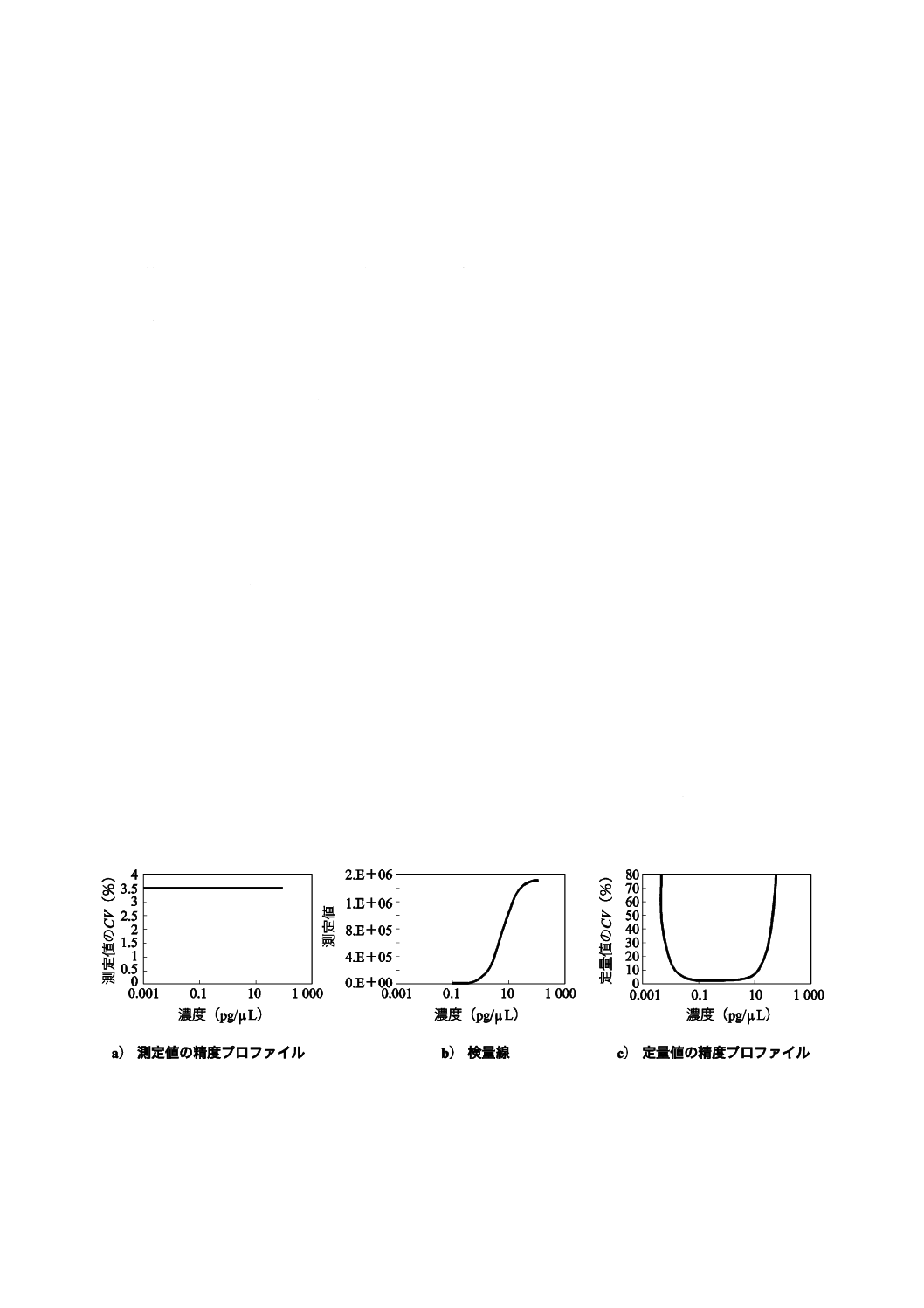
分析値の変動係数 (CV) を分析対象成分の濃度に対して図示した図を,精度プロファイルと定義する
([1]参照)。精度プロファイルには,測定値の精度プロファイル及び定量値の精度プロファイルの2種類
がある。レポーター遺伝子アッセイの精度プロファイル及び標準物質に対する検量線の一例を,図1に示
す。
図1−精度プロファイル及び検量線(レポーター遺伝子アッセイ)
測定値のCVから定量値のCVへの変換は,検量線の微分係数(
dX
dY/
)を用いて,標準偏差 (SD) 間の
変換を,図2に示すように行う。
7
K 0463:2009
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
図2−測定値のCVから定量値のCVへの変換
この変換は,次の式による。
X
dX
dY
Y
r
r
)
/
(
m
c=
ここに,
X: 定量値
Y: 測定値
rc: 定量値のCV
rm: 測定値のCV
11.3 検出下限
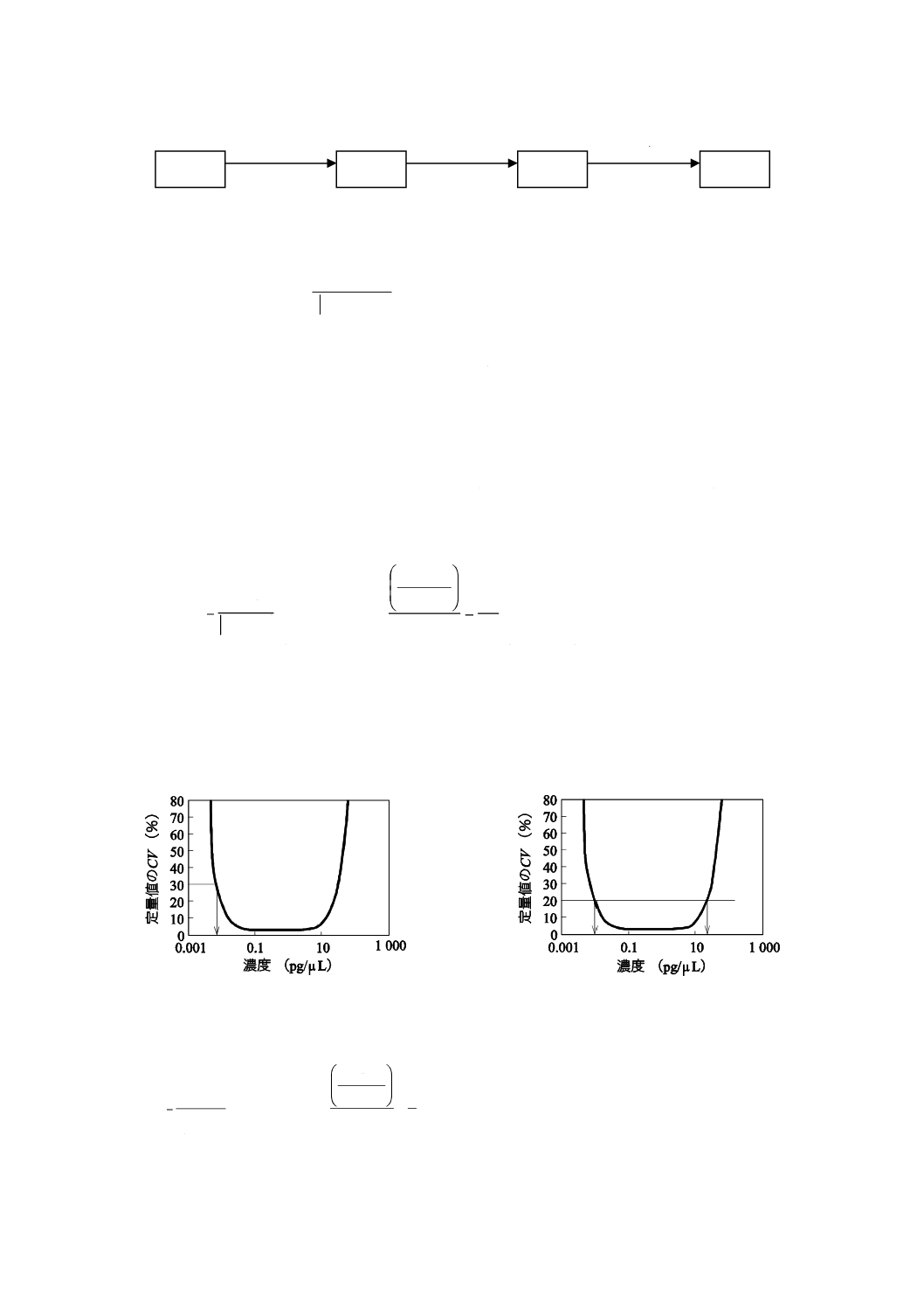
定量値の精度プロファイルのCVが30 %を示す濃度を検出下限とする。図3は,図1に示した定量値の
精度プロファイルから求めた検出下限である。
注記 JIS K 0127に示す定量値の標準偏差と検量線との傾きに基づく方法は,検量線が原点を通る直
線となる場合に用いる。この定義では,検出下限Lを測定値の標準偏差sの3.3倍とし,これ
を検量線で換算した濃度と定義している。したがって,検出下限は
dX
dY
s
L
/
3.3
=
となる。これを
3.3
1
/
=
L
dX
dY
s
と書き直すと,左辺は検出限界濃度での定量値
のCVを示し,右辺は30 %を示し,この規格の定義と一致する。
11.4 定量範囲
定量値の精度プロファイルにおけるCVが20 %以下となる濃度範囲を定量範囲とし,最小濃度を定量下
限,最大濃度を定量上限とする。図4は,図1に示した定量値の精度プロファイルから求めた定量下限及
び定量上限である。
図3−検出下限の求め方
図4−定量下限及び定量上限の求め方
注記 検量線が原点を通る直線となる場合は,定量下限及び定量上限 (L) を測定値の標準偏差sの5倍とし,これを
換算した濃度と定義すると,定量下限及び定量上限は
dX
dY
s
L
/
5
=
となる。これを
5
1
/
=
L
dX
dY
s
と書き直すと,左辺は定量下限又は定量上限での定量値のCVを
示し,右辺は20 %を示す。
測定値の
CV
定量値の
SD
測定値の
SD
定量値の
CV
×Y
÷X
÷|dY/dX|
8
K 0463:2009
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
12 計算
12.1 検量線
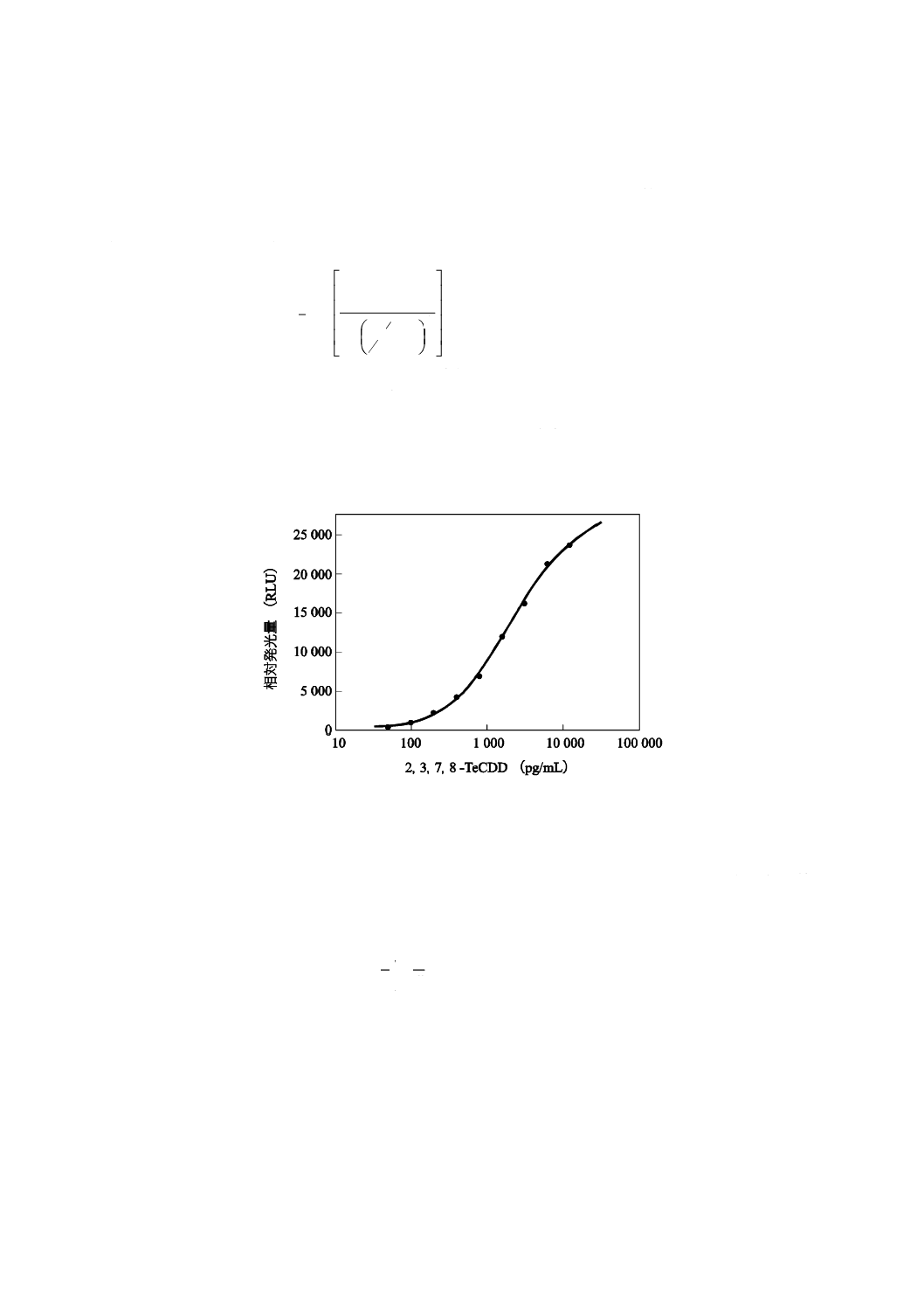
通常,それぞれのレポーター遺伝子アッセイには,技術提供元が指示した計算方法(4-parameter logistic
回帰,直線回帰など)が示されているので,その方法による。検量線の関数を得るのによく用いられる例
(4-parameter logistic回帰)を図5に示す。
+
−
+
=
b
d
a
d
y
50
EC
1
ρ
ρ
ここに,
y: 測定値
d: 曲線における上方漸近値
a: 曲線における下方漸近値
ρ: 標準物質の質量濃度
ρEC50: EC50における標準物質の質量濃度
b: EC50における曲線の傾き
図5−検量線の例
12.2 測定試料の定量
通常,測定試料は希釈系列を作製し測定する。各々の測定試料から得られた相対発光量 (RLU) を検量
線の回帰式に代入し,測定試料の濃度C (ng/mL) を算出する。試料中の濃度Cs(ng/m3,ng/gなど)は,
次の式によって求める。濃度は,通常,3けた目を四捨五入し,有効数字2けたで表す。
S
V
V
v
n
C
C
1
E
E
s
×
′
×
×
×
=
ここに,
Cs: 試料中の濃度(ng/m3,ng/gなど)
C: 測定試料液の濃度 (ng/mL)
n: 希釈倍数
v: 測定試料液の液量 (mL)
VE: 抽出液量 (mL)
V'E: 抽出液分取量 (mL)
S: 試料の採取量(m3,gなど)
9
K 0463:2009
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
試料における定量下限は,上記の式の濃度Cに標準物質における定量下限の濃度を代入し計算する。試
料における定量下限は,測定試料液の希釈倍数,分析に供した抽出液の割合,試料の採取量によって異な
ってくるため,試料ごとに求める。
13 日常精度管理
分析対象成分の測定にかかわる精度が確保されていることの確認などを行うため,適切な頻度で,箇条
11で求めた値で管理し,併せて次のa)及びb)の試料について必要な前処理,試料調製を行い,測定を行う。
また,適切な頻度で,c)の二重測定を行い,d)の管理図を作成し,記録する。このアッセイの誤差要因及
び妨害要因並びにその対策の例を,附属書Dに示す。
a) 操作ブランク試料 操作ブランク試料の調製は,測定用試料の調製などに起因する汚染を確認し,試
料の測定に支障のない測定環境を確認するために行うものであり,試料のサンプリング及び前処理に
用いるのと同じ試薬などを用いて試料と同様に行う。試薬,資材の変更など前処理操作に大きな変更
があった場合及び試料間汚染(クロスコンタミネーション)が予想されるような高濃度試料の前処理
を行う場合にも,操作ブランク試料を調製する。操作ブランク試料測定値(以下,操作ブランク測定
値という。)が高い場合は,試料測定値の補正に操作ブランク測定値を用いる必要があるが,操作ブラ
ンク測定値が大きいと,試料測定値の信頼性が低下するため,操作ブランク測定値は,極力低減を図
らなければならない。
b) 濃度既知試料 標準的な濃度既知の試料(標準物質溶液,濃度既知の環境試料など)であり,適切な
頻度(例えば,一連の分析操作ごと)で,前処理から測定までの工程に精度管理上の問題が発生して
いないことを,定期的に確認するために用いる試料である。抽出及び前処理操作において十分な回収
率が得られているかを確認する目的では,通常,濃度既知の試料を用いる。また,細胞を用いた測定
系(測定,定量操作)に異常がないか否かを確認する目的では,通常,標準物質溶液又は濃度既知の
前処理済み試料を用いる。
c) 二重測定 同一試料から二つ以上の測定試料を採取し,採取した試料について前処理操作,測定操作
を行う。測定試料数の10 %程度の頻度で二重測定を行い,定量下限以上の測定量について,±30 %以
内であることを確認する。
d) 管理図 測定,定量操作が適切に行われているかを確認するため,検量線作成用標準液及び濃度既知
試料の測定値について,JIS Z 9021に規定した管理図に測定値を記録し,保存する。管理図による処
置基準は,警戒限界(μ±2σ)からの逸脱状況及び管理図の傾向に応じて適切に定める(μ:工程平
均,σ:定量値の標準偏差)。
なお,警戒限界は十分なサンプル数から導出する。
1点でも警戒限界を超えた場合は,原因の究明及び対策を行うとともに,再測定する。対策のため
に講じた措置及び再測定の結果について,記録を行う。また,警戒限界内であっても基準値に対して,
一定の傾向で外れていくような状態又は偏った定量値が続くような状態においても原因の究明を行い,
必要に応じ対策を講じるとともに,再測定する。
14 検査報告書
検査報告書には,次の事項を詳細に明記する。
a) この規格の番号
b) 試料を特定するために必要な情報
10
K 0463:2009
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
c) 試料のサンプリング及び前処理方法(必要な場合)
d) 12.1に規定する標準溶液の検量線
e) 12.2の計算方法
f)
箇条13に規定する精度データ
g) 箇条11に規定する妥当性の確認にて求めた精度プロファイル,検出下限及び定量範囲
h) 検査に用いたアリル炭化水素受容体結合レポーター遺伝子アッセイの分析対象成分に対する相対活性
i)
この手順からの逸脱及び結果に影響を及ぼす可能性のあるすべての状況の記載
11
K 0463:2009
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書A
(参考)
サンプリング及び前処理
A.1 サンプリング及び前処理
アリル炭化水素受容体結合レポーター遺伝子アッセイを実試料に適用する場合は,試料媒体ごとに適し
たサンプリング及び前処理を行うことが必要である。
例えば,次のJIS,公的な分析マニュアルなどに従い,サンプリング及び前処理を行うが,サンプリン
グスパイク,クリーンアップスパイクなどの内標準物質については,この方法では分析対象成分との識別
が不可能であるため使用することはできない。しかし,分析対象成分の回収性について濃度既知試料(12.2
参照)を用いるなどによって確認を行う。
排ガス:JIS K 0095,JIS K 0311,
ダイオキシン類に係る生物検定法マニュアル(環境省 平成18年3月改訂)
燃え殻及びばいじん:環境省告示第80号(平成16年12月27日),
ダイオキシン類に係る生物検定法マニュアル(環境省 平成18年3月改訂)
水質:JIS K 0312
大気:ダイオキシン類に係る大気環境測定マニュアル(環境省 平成18年2月改訂)
底質:ダイオキシン類に係る底質調査測定マニュアル(環境省 平成12年3月),
河川・沼底質中のダイオキシン類簡易測定マニュアル(案)(国土交通省 平成16年7月)
土壌:ダイオキシン類に係る土壌調査測定マニュアル(環境省 平成12年1月)
A.2 排ガスサンプリング方法の概要
A.2.1 一般
試料ガス採取の一般的事項は,JIS K 0095による。また,ダイオキシン類測定のための試料ガス採取方
法は,JIS K 0311の5.(試料ガスの採取)による。
A.2.2 試薬
JIS K 0311の5.3(試薬)に規定したものを使用する。
A.2.3 試料採取装置
JIS K 0311の5.2(試料ガス採取装置)に規定したもの。通常は,JIS K 0311の附属書1のJIS I形採取
装置を用いることとし,JIS II形採取装置又はJIS III形採取装置を用いる場合は,JIS K 0311の5.2に従っ
て採取装置の妥当性を確認する。
A.2.4 試料ガスの採取の準備
JIS K 0311の5.4(試料ガスの採取の準備)に規定した方法。ただし,5.4.3の内標準物質(サンプリン
グスパイク)の添加は通常行わない。
A.2.5 試料ガスの採取量
試料ガスの採取量は,例えば,次の式によって決定する。排出ガスの採取に当たっては,通常の操業状
態において(燃焼状態が安定した時点から約1時間以上経過した後をめどとする),採取する。
なお,採取時間については,その目的に応じて試料ガスの発生状況などを十分考慮して代表試料が採取
できるようにしなければならない。
12
K 0463:2009
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
DL
E
E
DL
1
000
1
C
V
V
v
Q
V
×
′
×
×
=
ここに,
V: 測定に必要な最小の試料ガスの量 (m3) (0 ℃,
101.325 kPa)
QDL: 標準物質における検出下限 (pg /mL)
v: 測定用試料の液量 (mL)
VE: 抽出液量 (mL)
V'E: 抽出液分取量 (mL)
CDL: 必要となる試料ガスにおける標準物質相当の検
出下限 (ng /m3) (0 ℃,101.325 kPa)
A.2.6 採取操作
JIS K 0311の5.6(採取操作)に規定した方法による。
A.2.7 試料の回収及び保存
JIS K 0311の5.7(試料の回収及び保存)に規定した方法による。
A.2.8 試料採取量の算出
JIS K 0311の5.8(試料ガスの採取量の算出)に規定した方法による。
A.2.9 試料ガスの採取の記録
JIS K 0311の5.9(試料ガスの採取の記録)に規定した方法による。
A.3 試料の前処理の概要
A.3.1 一般
採取した試料は,ろ紙,樹脂,吸収液などの形態ごとに抽出する。これらの抽出液を合わせた後,必要
に応じて分取する。その後,硫酸処理−シリカゲルカラムクロマトグラフ操作,多層シリカゲルクロマト
グラフ操作又は硫酸処理−多層シリカゲルカラムクロマトグラフ操作を行い,必要に応じてアルミナカラ
ムクロマトグラフ操作,高速液体クロマトグラフ操作,活性炭クロマトグラフ操作などのいずれか又はこ
れらを組み合わせた精製操作を行う。
A.3.2 試薬
JIS K 0311の6.2(試薬)に規定したものを使用する。
A.3.3 器具及び装置
JIS K 0311の6.3(器具及び装置)に規定したものを使用する。
A.3.4 前処理操作
JIS K 0311の6.4(前処理操作)に従って実施する。ただし,JIS K 0311の6.4.1に規定する内標準物質
(クリーンアップスパイク)及びJIS K 0311 の6.4.6(測定用試料の調製)に規定する内標準物質(シリ
ンジスパイク)の添加は行わない。また,JIS K 0311の6.4.6において測定用試料の調製溶媒として,ノナ
ン,トルエン,デカンなどが用いられているが,アリル炭化水素受容体結合レポーター遺伝子アッセイの
場合は,精製操作によって得られた濃縮液をDMSOなど,細胞培養培地と均一な混合が可能で細胞に対す
る毒性の少ない適切な溶媒の一定量に置換して用いる。
13
K 0463:2009
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書B
(参考)
細胞培養のフローチャート
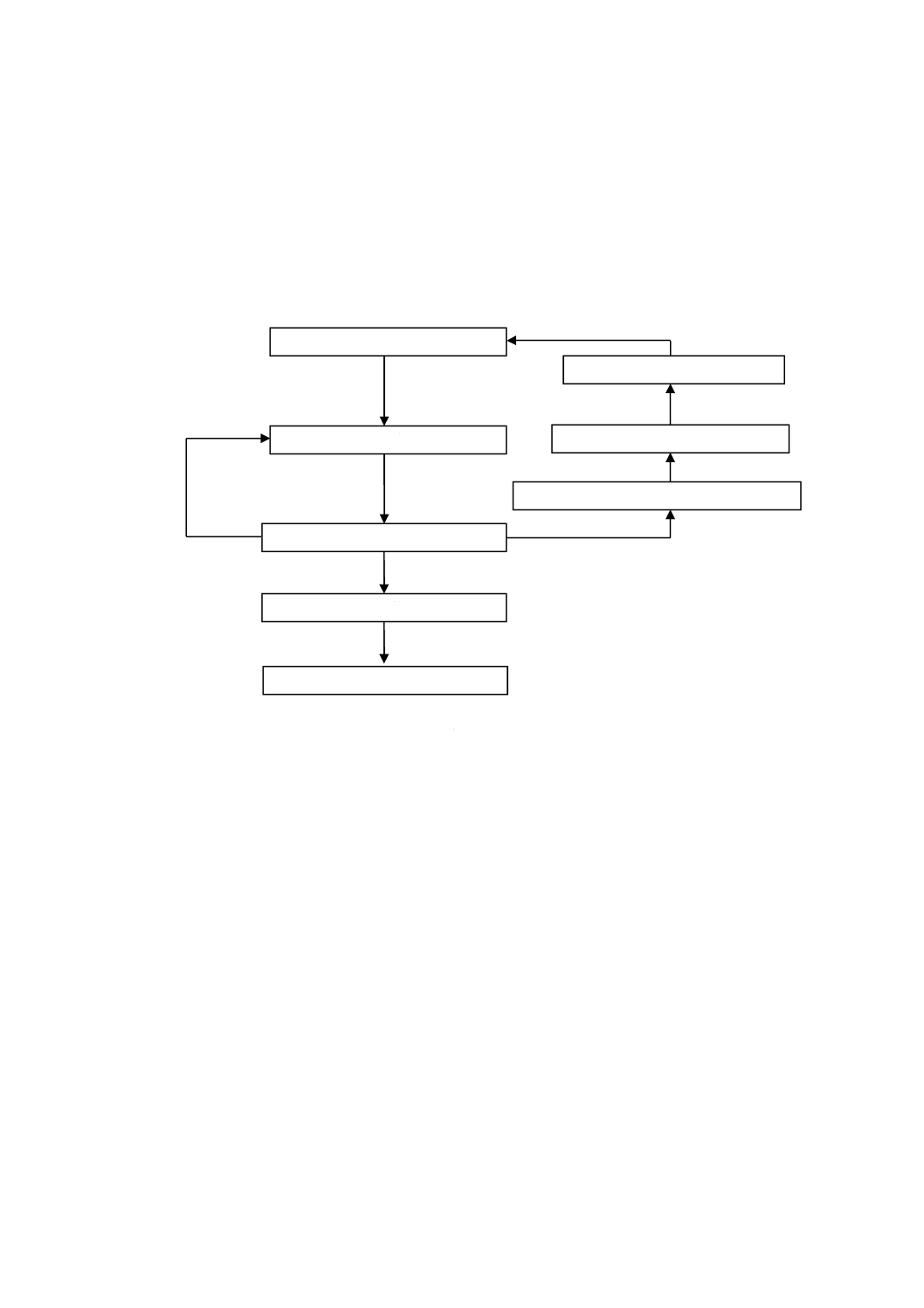
細胞培養のフローチャート
細胞培養のフローチャートを,図B.1に示す。
図B.1−細胞培養のフローチャート
細胞の継代培養
細胞の保存
細胞のはく離を行う
凍結細胞を解凍する
細胞を培養する
凍結細胞を保存する
細胞を培養する
細胞凍結保存用細胞懸濁液を調製する
細胞を凍結する
測定に使用する
細胞の起眠

14
K 0463:2009
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書C
(参考)
測定操作例
アリル炭化水素受容体結合レポーター遺伝子アッセイの測定操作例
マウス組換え肝ガン細胞 (H1L6.1c2) を用いたアリル炭化水素受容体結合レポーター遺伝子アッセイに
おけるフローチャート例を図C.1に示す。
細胞培養容器に細胞をは(播)種する
↓
CO2インキュベーター内で培養する(14〜24時間)
↓
細胞培養容器から培地を除去する
↓
測定試料及び標準物質をそれぞれ培地と混合し,
細胞培養容器に添加する
↓
CO2インキュベーター内で培養する(20〜24時間)
↓
細胞培養容器から培地を除去し,緩衝液で洗浄する
↓
細胞溶解液を加える
↓
基質を加える
↓
発光量を測定する
↓
結果を計算する
図C.1−アリル炭化水素受容体結合レポーター遺伝子アッセイのフローチャート
[マウス組換え肝ガン細胞 (H1L6.1c2) の例]

15
K 0463:2009
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書D
(参考)
誤差要因及び妨害要因並びにその対策
誤差要因及び妨害要因並びにその対策
アリル炭化水素受容体結合レポーター遺伝子アッセイの誤差要因及び妨害要因並びにその対策について,
表D.1に例示する。
表D.1−アリル炭化水素受容体結合レポーター遺伝子アッセイの誤差要因及び
妨害要因並びにその対策(例)
工程
誤差要因・妨害要因
対策例
サンプリング
代表試料の採取に問題があ
る。
十分な捕集率があり,操作中に分析対象成分の損失,分解又
は二次汚染などの起こり得る可能性のない採取器具及び機
器を用いる。
試料の均一化がなされるよう適切な採取方法(採取量,採
取時間,採取頻度など)に基づいて実施する。
試料回収及び保存時におけ
る汚染,損失など
試料採取終了後,密閉性,遮光,温度管理などに留意し,適
切な手立てを講じて試験室に運搬し,保存する。速やかに前
処理以降の操作を行う。
前処理及び試料調製
不適切な前処理方法の選択
新たな試料媒体又は特殊な性状の試料を取り扱うときは,十
分な前処理方法のバリデーションを行い,分析対象成分の測
定に支障が生じないように,きょう雑物質及びマトリクス成
分の除去についてあらかじめ検討を行う。
試料間汚染(クロスコンタミ
ネーション)
前処理及び試料調製並びに測定操作を実施する施設内環境
からの化学汚染がないよう留意し,必要に応じて対策を実施
する。
使用試薬,器具の変更による
前処理条件の変化
使用試薬などのロット変更があった場合には,前処理条件の
変化(分析対象成分の回収率の低下など)について確認を行
い,必要に応じて対策を実施する。また,操作ブランク試料
の調製及び濃度確認を実施する。
最終検液の調製に問題があ
る。
前処理によって得られた分析対象成分を含む溶液をDMSO
などの少量の溶媒に転溶するときは,分析対象成分の損失,
回収性及び最終検液の定量性に十分留意する。
細胞の管理
細胞の雑菌汚染
クリーンベンチ及び安全キャビネット内の清浄環境の維持
に努める。
細胞の起眠,継代培養,凍結保存作業のときは,上記の設
備を使用するとともに,エタノール消毒及び火炎滅菌操作の
励行に努める。
日常的に細胞の状態観察を行い,培地の濁り及び細胞はく
離の生じたものは直ちに廃棄する。
細胞品質の劣化
日常精度管理を実施し,標準物質だけを実際の測定に用い
る。
培養試薬品質の変更又は劣
化
使用試薬などのロット変更があった場合には,細胞が適切な
増殖性又は応答性を示すか確認を行い,適切な試薬を用い
る。
開封日及び調製日について記録を行い,有効期限を定めて
用いる。
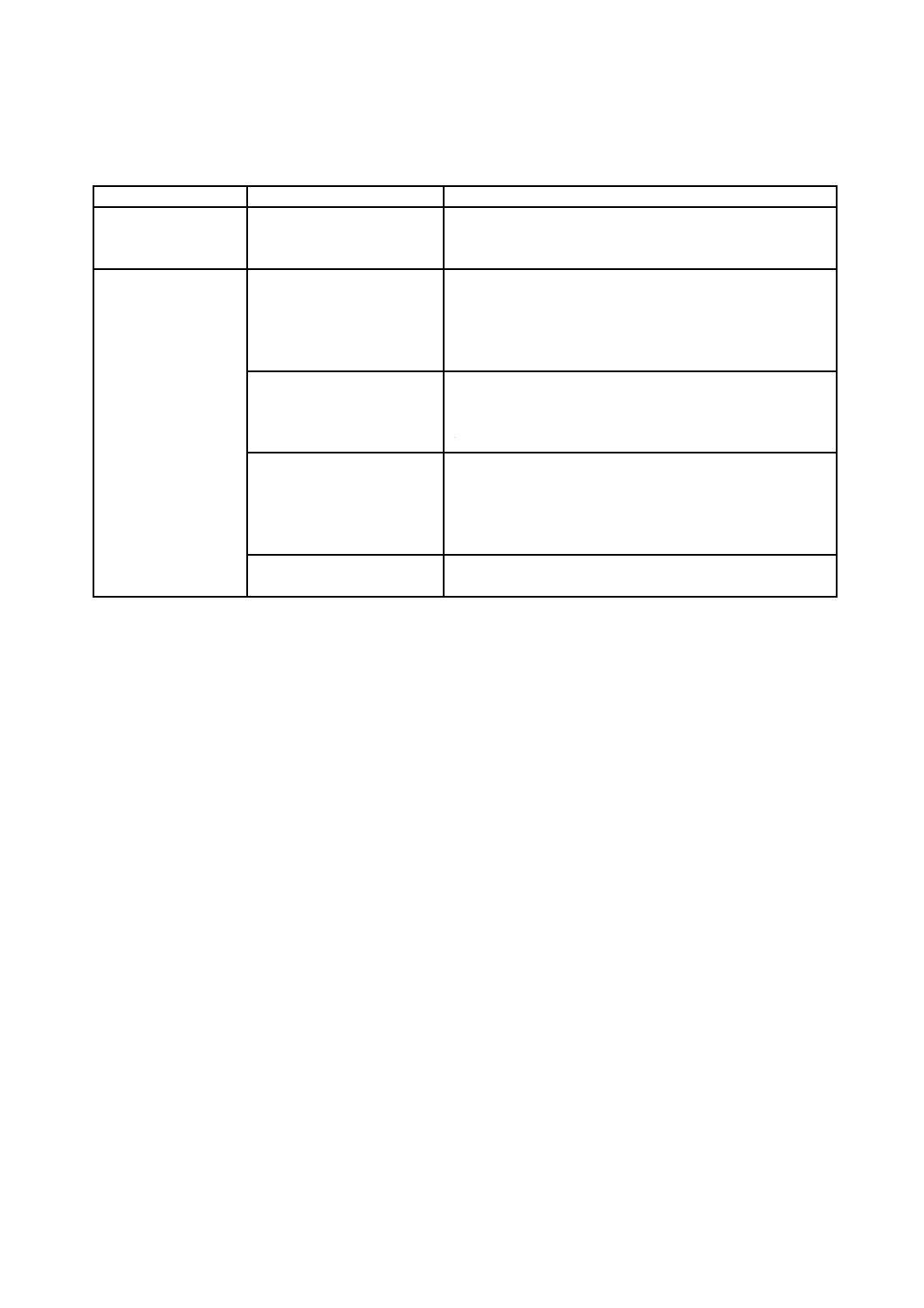
16
K 0463:2009
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
表D.1−アリル炭化水素受容体結合レポーター遺伝子アッセイの誤差要因及び
妨害要因並びにその対策(例)(続き)
工程
誤差要因・妨害要因
対策例
細胞の管理
細胞培養装置,細胞保存装置
及び使用器具類の不具合
日常点検及び校正を実施し,管理状態を確認する。雑菌汚染
及び故障などのトラブルに備えて定期清掃及び定期点検を
行う。
測定操作
細胞の雑菌汚染
クリーンベンチ及び安全キャビネット内の清浄環境の維持
に努める。
細胞のは(播)種操作及び暴露操作をするときは,それら
の設備を使用するとともに,エタノール消毒及び火炎滅菌操
作の励行に努める。
測定関連試薬品質の変更又
は劣化
使用試薬などのロット変更があった場合には,細胞が適切な
応答性を示すか確認を行い,適切な試薬を用いる。
開封日及び調製日について記録を行い,有効期限を定めて
用いる。
細胞培養装置,発光光度計及
び使用器具類の不具合
日常点検及び校正を実施し,管理状態を確認する。雑菌汚染
及び故障などのトラブルに備えて定期清掃及び定期点検を
行う。
マイクロピペットによる分注量の誤差について留意し,必
要に応じて対策を実施する。
暴露操作における暴露時間
の長短
用いる細胞の種類に応じて設けられている暴露時間を遵守
する。
17
K 0463:2009
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書E
(参考)
レセプターアッセイの分類
E.1
レセプターアッセイの分類
レセプターアッセイの分類を,図E.1に示す。
A. 標識リガンドを用いる方法
結合を直接検出
B. 分子量の変化を検出する方法
レセプターアッセイ
C. 抗体を用いる方法
複合体形成を検出
(非細胞法)
D. DNAの量をはかる方法
転写活性化能を検出
E. 遺伝子発現誘導をはかる方法
(細胞法)
(レポーター遺伝子アッセイ)
図E.1−レセプターアッセイの分類
リガンド(測定対象成分を含む。)と受容体との結合を測定するレセプターアッセイは,受容体とリガン
ドとの結合を直接観測する方法,受容体とリガンドとの結合によって他の生体分子(たん白質又はDNA)
との新たな結合が起こる場合においてはその結合した生体分子を観測する方法,受容体とリガンドとの結
合によって転写活性化能を獲得する場合には遺伝子発現の変化として観察する方法の3種類に大きく分類
される。
このほかにも,生細胞に細胞膜受容体を発現させ,リガンドの結合によって引き起こされる一連のシグ
ナルを細胞の増殖などとして検出する方法もレセプターアッセイに含まれるが,ここでは,主として用い
られている最初に述べた三つの検出方法についてE.2〜E.4に記載する。
E.2
結合を直接検出する方法
受容体とリガンドとの結合を直接観測する方法の代表としては,標識したトレーサーを用いて,このト
レーサーと測定対象成分とを受容体への結合において競合させる測定法であるラジオレセプターアッセイ
がある。
一方,非標識検出としては,例えば,受容体を金属薄膜表面に固定化し,リガンドが受容体に結合する
ことによる分子量の変化に依存した表面プラズモン共鳴の変化を観察する方法がある。
E.3
複合体形成を検出する方法
受容体とリガンドとの結合によって,複合体を形成する組合せは多く知られている。例えば,アリル炭
化水素受容体の場合,リガンド非存在下においてはアリル炭化水素受容体は熱ショックたん白質の一種
(hsp90) と結合しているが,リガンドとの結合によってhsp90が離れ,代わりにARNTというたん白質が
結合し,この複合体のターゲット配列であるDREをもつDNAに対して結合する能力を獲得する。このよ
うな場合には,受容体とリガンドとが結合した量を,この複合体に含まれる成分を検出することで観察す
18
K 0463:2009
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
ることが可能である。
上記のアリル炭化水素受容体の場合には,DREを含むDNAに結合したアリル炭化水素受容体複合体(ア
リル炭化水素受容体−リガンド−ARNT−DREを含むDNAから成る)を抗ARNT抗体で免疫測定方法
(JIS K 0461) によって検出する方法と,アリル炭化水素受容体複合体に結合したDREを含むDNA量をリ
アルタイムPCRで測定する方法とがある。
E.4
転写活性化能を検出する方法(レポーター遺伝子アッセイ)
生細胞内において受容体とリガンドとの結合によって,転写活性化を引き起こす組合せは核内受容体で
多数知られている。例えば,アリル炭化水素受容体の場合には,リガンドとの結合によってARNTとの複
合体を形成することによって,転写調節配列であるDREを含むさまざまな遺伝子に関して転写活性化を引
き起こす。
この場合には,レセプターとリガンドとが結合した量を,当該遺伝子の転写量として推定することが可
能であり,特にレポーター遺伝子アッセイと呼ばれ,前述の方法とは,生細胞を用いるという点で大きく
異なる。
レポーター遺伝子アッセイにおいては,転写量をより簡便に測定するために,転写活性化によって発現
するたん白質として,ホタルのルシフェラーゼ,ガラクトシダーゼなどの酵素遺伝子を用いることが多く,
この場合は生成酵素の酵素活性によって転写活性化の程度,更には転写活性化を引き起こした受容体及び
リガンドの相互作用の程度(リガンドの量及び受容体との親和性に依存する)を,簡便に評価することが
可能となる。ホタルのルシフェラーゼの場合には,基質であるルシフェリンを加えることによって起こる
発光量を,発光光度計で測定する。
参考文献 [1] Y. Hayashi, R. Matsuda, T. Maitani, K. Ito, W. Nishimura, K. Imai and M. Maeda ; An expression of
within-plate uncertainty in sandwich ELISA., J. Pharm. Biomed. Anal., 36 (2004) 225-229.
[2] JIS K 0094 工業用水・工場排水の試料採取方法
[3] JIS K 0095 排ガス試料採取方法
[4] JIS K 0127 イオンクロマトグラフ分析通則
[5] JIS K 0211 分析化学用語(基礎部門)
[6] JIS K 0216 分析化学用語(環境部門)
[7] JIS K 0311 排ガス中のダイオキシン類の測定方法
[8] JIS K 0312 工業用水・工場排水中のダイオキシン類の測定方法
[9] JIS K 0950 プラスチック製滅菌シャーレ
[10] JIS K 0970 プッシュボタン式液体用微量体積計
[11] JIS K 3605 高圧蒸気滅菌操作通則
[12] JIS R 3503 化学分析用ガラス器具
[13] JIS R 3505 ガラス製体積計
[14] JIS T 7322 医療用高圧蒸気滅菌器
[15] JIS T 7324 医療用小型高圧蒸気滅菌器