K 0462:2008
(1)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
目 次
ページ
1 適用範囲 ························································································································· 1
2 引用規格 ························································································································· 1
3 用語及び定義 ··················································································································· 1
4 妨害······························································································································· 2
5 原理······························································································································· 2
6 試薬······························································································································· 3
7 器具及び機器 ··················································································································· 3
8 サンプリング及び試料調製 ································································································· 3
8.1 サンプリング ················································································································ 3
8.2 固相のコーティング ······································································································· 3
8.3 標識抗体 ······················································································································ 4
8.4 溶液 ···························································································································· 4
8.5 標準溶液の調製 ············································································································· 4
8.6 試料の調製 ··················································································································· 4
9 操作方法 ························································································································· 4
9.1 注意事項 ······················································································································ 4
9.2 固相化抗体結合反応 ······································································································· 4
9.3 標識抗体結合反応 ·········································································································· 4
9.4 洗浄操作 ······················································································································ 4
9.5 分析対象成分の検出 ······································································································· 4
9.6 反応生成物の測定 ·········································································································· 5
9.7 非競合免疫測定方法(サンドイッチ法)(2ステップ法)の例 ················································· 5
9.8 ゼロ標準の測定 ············································································································· 5
9.9 校正 ···························································································································· 5
10 分析方法バリデーション(妥当性確認) ············································································· 5
10.1 一般 ··························································································································· 5
10.2 精度プロファイル ········································································································· 6
10.3 定量下限及び定量上限 ··································································································· 6
10.4 検出下限 ····················································································································· 7
10.5 他の分析方法との比較 ··································································································· 7
11 計算 ····························································································································· 8
11.1 繰返し ························································································································ 8
11.2 検量線 ························································································································ 8
12 精度 ····························································································································· 8
13 検査報告書 ···················································································································· 8
K 0462:2008 目次
(2)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
ページ
附属書A(参考)フローチャート ··························································································· 10
附属書B(参考)試験室間試験から得られた精度データの例 ························································ 12
K 0462:2008
(3)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
まえがき
この規格は,工業標準化法に基づき,日本工業標準調査会の審議を経て,経済産業大臣が制定した日本
工業規格である。
この規格は,著作権法で保護対象となっている著作物である。
この規格の一部が,特許権,出願公開後の特許出願,実用新案権又は出願公開後の実用新案登録出願に
抵触する可能性があることに注意を喚起する。経済産業大臣及び日本工業標準調査会は,このような特許
権,出願公開後の特許出願,実用新案権又は出願公開後の実用新案登録出願に係る確認について,責任は
もたない。
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
日本工業規格 JIS
K 0462:2008
非競合免疫測定方法(サンドイッチ法)通則
Guidelines for non-competitive immunoassay (Sandwitch method)
1
適用範囲
この規格は,工業用水,工場排水及び工場敷地の汚染の指標となる高分子バイオマーカー,微生物など
を,非競合免疫測定方法(サンドイッチ法)を用いて分析する場合の通則について規定する。
2
引用規格
次に掲げる規格は,この規格に引用されることによって,この規格の規定の一部を構成する。これらの
引用規格は,その最新版(追補を含む。)を適用する。
JIS K 0094 工業用水・工場排水の試料採取方法
JIS K 0410-3-1 水質−サンプリング−第1部:サンプリング計画策定の指針
JIS K 0410-3-2 水質−サンプリング−第2部:サンプリング技術の指針
JIS K 0410-3-3 水質−サンプリング−第3部:試料の保存及び取扱いの指針
JIS K 0461 競合免疫測定方法通則
JIS K 0557 用水・排水の試験に用いる水
JIS K 0970 プッシュボタン式液体用微量体積計
JIS K 3600 バイオテクノロジー用語
JIS K 8150 塩化ナトリウム(試薬)
JIS K 8576 水酸化ナトリウム(試薬)
JIS K 8622 炭酸水素ナトリウム(試薬)
JIS K 8625 炭酸ナトリウム(試薬)
JIS K 8951 硫酸(試薬)
JIS K 9009 りん酸二水素ナトリウム二水和物(試薬)
JIS K 9020 りん酸水素二ナトリウム(試薬)
3
用語及び定義
この規格で用いる主な用語及び定義は,JIS K 0461及びJIS K 3600によるほか,次による。
3.1
親和性 (affinity)
分析対象成分への抗体の結合の強さ(JIS K 0461参照)。
注記 結合の強さは,Ab+Ag=AbAgで表す反応の平衡定数(K)によって定義する。ここで,Ab は抗体の
結合部位,Agは抗原である。 K は,質量作用式K=cAbAg/(cAb×cAg)で示す。
3.2
2
K 0462:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
分析対象成分 (analyte)
非競合免疫測定方法の対象となる,水・土壌中の測定成分。
3.3
固相化抗体 (coating antibody)
固相に固定化した抗体。
3.4
非競合免疫測定方法(サンドイッチ法)[non-competitive immunoassay (sandwitch method)]
固相化抗体と標識抗体とによって試料中の分析対象成分を挟み込み,定量する試験方法。
3.5
交差反応性 (cross-reactivity)
抗体又は抗血清が,分析対象成分とは構造的に異なる物質に対して反応する度合い(JIS K 0461参照)。
注記1 このような物質に対する抗体又は抗血清の交差反応性は,各検量線の比較によって求められ
る。抗体又は抗血清の選択性(いわゆる特異性)は,交差反応性と逆の関係にある。抗体又
は抗血清は,異なる物質に対して異なる親和性を示す。ある特定の物質に対する抗血清の交
差反応性は,その測定濃度範囲内でも変化することがある。大抵の場合,免疫原の構造が抗
血清の選択性(いわゆる特異性)を本質的に決定する。抗血清でよく見られるように,種々
の抗体が集合体として存在していることによって交差反応が生じている場合,望ましくない
抗体は,交差吸収によって取り除くことができる。
注記2 検出可能な濃度で存在している交差反応性を示すすべての物質は,より高濃度値として又は
偽陽性としての結果をもたらす。
3.6
標識抗体 (antibody conjugate)
酸素,蛍光色素などで標識された抗体。トレーサーともいう(JIS K 0461参照)。
4
妨害
測定への妨害は,不適切な試料採取(例えば,分析対象成分を吸着又は溶出するような用具),又は材料
を選択したことによって起こる。測定条件,例えば,pH,試料に含まれる金属イオン,フミン酸,防せい
(錆)剤,試験成分に影響する溶媒(例えば,マトリックス効果)などは分析に影響する。マトリックス
効果の影響は,分析対象成分の一定量を試料に添加することによって推定できる。
5
原理
免疫測定方法は,分析対象成分の濃度を定量するために,分析対象成分又はその集団に対して調製した
抗体を,生化学的センサーとして使用する方法である。免疫測定方法は,スクリーニング用の分析手法と
して特に有用である。
分析対象成分に同時に2分子の抗体が結合できる場合の測定方法として,非競合免疫測定方法(サンド
イッチ法)を用いる。非競合免疫測定方法(サンドイッチ法)では,固相化抗体と標識抗体との2種類の
抗体を用いる。一定量の固相化抗体で分析対象成分を固相に捕らえ,一定量の標識抗体を作用させること
によって,2種類の抗体で分析対象成分を挟み込む。抗原抗体反応に関与しない成分は洗浄によって取り
除く。妨害的なマトリックス効果の大部分もこれによって除去される。より多くの分析対象成分が存在す
る場合,2種類の抗体に挟み込まれる分析対象成分も多くなり,標識抗体の濃度も高くなる。
3
K 0462:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
6
試薬
試薬は,高純度のもので試験に支障のないもので,次による。
なお,サンドイッチ法分析結果には,抗体及び抗血清のタイプ,由来(例えば,動物種,細胞などを例
示する。)及び交差反応性を記載する。使用した試薬の保存条件及び安定性に関する情報を,供給元に要求
する。抗体及び抗血清の特異性が低い場合,化学的又は物理的手法によって,試料から測定に干渉する物
質を取り除く。抗血清中の交差反応を示す抗体は,吸収によって取り除く。
6.1 水 JIS K 0557に規定するA4又はA3の水。
6.2 りん酸二水素ナトリウム二水和物 JIS K 9009に規定するもの。
6.3 りん酸水素二ナトリウム JIS K 9020に規定するもの。
6.4 塩化ナトリウム JIS K 8150に規定するもの。
6.5 硫酸 JIS K 8951に規定するもの。
6.6 水酸化ナトリウム JIS K 8576に規定するもの。
6.7 緩衝液 洗浄には緩衝液を用いる。例えば,JIS K 9009に規定するりん酸二水素ナトリウム二水和物
12.48 g,JIS K 9020に規定するりん酸水素二ナトリウム11.36 g及びJIS K 8150に規定する塩化ナトリウ
ム8.5 gを水に溶かし,水を加えて1 000 mLにしたりん酸緩衝生理食塩水(PBS:pH 7.6)を用いる。市販の
PBSを使用してもよい。
注記 PBS: Phosphate buffered saline
6.8 酸 pH調節及び酵素反応の停止のために用いる。例えば,硫酸 (1 g/L)など。
6.9 塩基 pH調節及び酵素反応の停止のために用いる。例えば,水酸化ナトリウム溶液 (4 g/L) など。
6.10 標準物質 分析対象となる物質の標準物質は,日本工業規格(以下,JISという。)の規定によるも
の又は市販の標準物質があればそれを用いる。JISに規定がなく,又はJISの規定に合致する市販の標準
物質がない場合には,市販されている分析対象成分のうち,できるだけ純度の高いものを用いる。
7
器具及び機器
器具及び機器は,次による。
7.1 固相 免疫測定方法に使用する,プラスチック,ガラス,又は磁性粒子製の固相。例えば,96穴1)
マイクロプレート,試験管,ビーズ,磁性粒子,薄膜など。
注1) 穴をウェルという。
7.2 マイクロピペット JIS K 0970に規定するもの(例えば,10〜500 μLの可変式ピペット,10 μL,100
μL及び200 μLの容量固定ピペット,300 μLなどのマルチチャンネルピペット,ディスペンサーなど)。
7.3 磁気ラック 磁性の基盤付きのもの。磁性粒子に結合した抗体を用いる免疫測定方法における洗浄工
程で使用する。
8
サンプリング及び試料調製
8.1
サンプリング
サンプリングは,受渡当事者間の協定による。一般的な方法を,次に示す。
“非競合免疫測定方法通則”を実試料に適用する場合には,サンプリング方法及び前処理方法について
規定する次のJISに従って,サンプリング及び前処理を行う。
JIS K 0094,JIS K 0410-3-1,JIS K 0410-3-2及びJIS K 0410-3-3
8.2
固相のコーティング
4
K 0462:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
免疫測定用の固相を,次のようにコーティングする。市販品の固相を用いてもよい。
a) 抗体又は抗血清の希釈溶液を,適切な緩衝液,例えば,JIS K 8625に規定する炭酸ナトリウム5.3 g
及びJIS K 8622に規定する炭酸水素ナトリウム4.2 gを水に溶かし,硫酸(1 g/L)又は水酸化ナトリウ
ム(4 g/L)を用いてpH 9.6に調整した50 mmol/L炭酸塩緩衝液(pH 9.6)中で固相化する。
b) 測定を始める前に抗体を固相化する。コーティング及びそれに続く洗浄段階の後に,非特異的吸着が
高い場合はブロッキングが必要である。
8.3
標識抗体
免疫測定方法に使用する標識抗体は,使用直前に6.7のりん酸緩衝生理食塩水などの緩衝液で適切に希
釈若しくは溶解するか,又はすぐに使用できるように安定化した状態で製造業者から供給されたものを使
用する。
8.4
溶液
固相を洗浄する緩衝液(6.7参照),及び酵素反応を終了させる酸(6.8参照)又は塩基(6.9参照)は,
測定前に調製するか,又は緩衝液で適切に希釈するか,若しくは直ちに使用できるように安定化した状態
で製造業者から供給されたものを使用する。
8.5
標準溶液の調製
標準物質又は抗体が分析対象成分と同等の反応性をもつ物質を,6.7のりん酸緩衝生理食塩水などの適切
な緩衝液を用いて溶解希釈し,所定の標準溶液を調製する。
8.6
試料の調製
測定前に,すべての試料,前処理した試料,試薬,溶液,装置及び固相化物を,規定した温度に調節す
る。酵素反応は一定の温度で行う。試料のpHが測定に最適な範囲にない場合は,pH調節(例えば,水酸
化ナトリウム,硫酸などで行う。)が必要である。測定結果から分析対象成分の濃度を計算する場合には,
希釈倍率を考慮する。
9
操作方法
9.1
注意事項
この規格に従って操作を行う場合には,専門施設が必要である。
9.2
固相化抗体結合反応
標準液,試料又は前処理した試料を固相化抗体と所定の時間反応させる。
9.3
標識抗体結合反応
希釈した標識抗体(8.3参照)を,標準液,試料又は前処理した試料と所定の時間反応させる。
固相化抗体結合反応と標識抗体結合反応とは,別途実施しても(2ステップ法及び洗浄操作2回),同時
に実施しても(1ステップ法及び洗浄操作1回),どちらでもよい。
9.4
洗浄操作
反応終了後に固相を洗浄する。緩衝液(PBSなど,6.7参照)で数回洗浄して,結合反応中に結合しな
かった標準品及び試料を除去する。
9.5
分析対象成分の検出
分析対象物に結合した標識抗体を適切な方法(例えば,酵素反応,蛍光強度)で検出する。使用した標
識抗体の濃度で,基質が完全に変換されないよう,反応時間及び基質の濃度を選択する。終末点測定では,
反応時間が終わった後に,酸(6.8参照)又は塩基(6.9参照)を添加して反応を停止させる。連続測定で
は連続的に測定を行う。
5
K 0462:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
9.6
反応生成物の測定
適切な機器(例えば,可視比色計)を用いた分析によって,反応生成物量を測定する。
注記 市販の免疫測定用キットには,通常,機器選択の指針が付いている。
9.7
非競合免疫測定方法(サンドイッチ法)(2ステップ法)の例
注記 非競合免疫測定方法(サンドイッチ法)は,例えば,附属書Aに示すフローチャートに従って
実施する。2ステップ法の作業方法の例を9.7.1〜9.7.6に示すが,具体的手順は,分析対象成分
定量キットの製造業者から供給された添付文書の指示に従い実施する。
9.7.1
固相化抗体結合反応
ピペットを用いて標準液又は試料を,添付文書で指示された量ずつ固相に添加し,所定の時間反応させ
る。
9.7.2
洗浄操作1
反応後,プレートの穴1)ごとに十分な量の洗浄液(穴当たり300 μL程度)を用い,マイクロプレート洗
浄機(又は手作業)によって,固相(穴)を洗浄する。この操作は,通常3回程度行えば十分である。最
後の洗浄の後,必要であれば,プレートをきれいな柔い紙(綿)上にたたき付けて(タッピング),残った
緩衝液を除く。
9.7.3
標識抗体結合反応
固相化抗体結合反応を終了した固相に,例えば,標識抗体原液を6.7のりん酸緩衝生理食塩水で希釈し
た標識抗体(8.3参照)を製造業者から供給された添付文書で指示された量ずつ添加し,所定の時間反応さ
せる。
9.7.4
洗浄操作2
洗浄操作1と同様に操作して固相(穴)を洗浄する。
9.7.5
酵素反応
酵素基質を準備した後,一定間隔で反応固相に一定量の酵素基質を注入して酵素反応を開始し,一定時
間酵素反応を行った後,反応停止液を加えて酵素反応を止める。
9.7.6
活性測定
適切な機器(例えば,可視比色計)を用いた分析によって,反応生成物量を測定する。
注記 市販の免疫測定用キットには,通常,機器選択の指針が付いている。
9.8
ゼロ標準の測定
装置及び試薬の妥当性の最終確認のために,一連の測定ごとにゼロ標準(空試験用試料)を測定する。
試料調製方法の妥当性は,実試料と同じ方法で調製した空試験用試料の分析を,ゼロ標準測定として行う
ことによって確認する。ゼロ標準が検出下限を超えた場合は,このゼロ標準を含む一連の測定から得られ
た結果は,破棄するとともに,汚染源を除くために系統的に調査を行い,問題点を特定する。
9.9
校正
標準液を用いて,免疫測定ごとに検量線を作成する。標準液の濃度が対応する検量線の値に一致してい
ることを,定期的に確認する。ただし,検量線の濃度の差が20 %を超えてはならない。
10 分析方法バリデーション(妥当性確認)
10.1 一般
データの質を保証するために,新たに導入した免疫測定方法については,分析方法バリデーション(妥
当性確認)を実施する。
6
K 0462:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
免疫測定方法は,10.2〜10.5に示す管理基準を適切に満たしていれば,日常分析として用いることがで
き,統計的に妥当性があるといえる。統計的に管理するには,その方法を実験室で初めて行う前に,十分
な性能評価(パーフォーマンスバリデーション)をすべての分析対象成分に対して行う。この性能評価か
ら,日常の“品質保証及び品質管理”の基準のパラメータを決め,管理図を作成しておく。
一連の測定ごとに,既知濃度の分析対象成分を加えたゼロ試料を少なくとも一つ分析する。この既知濃
度の対象化合物を添加した空試験の結果を,一つの管理図として使うことが望ましい。
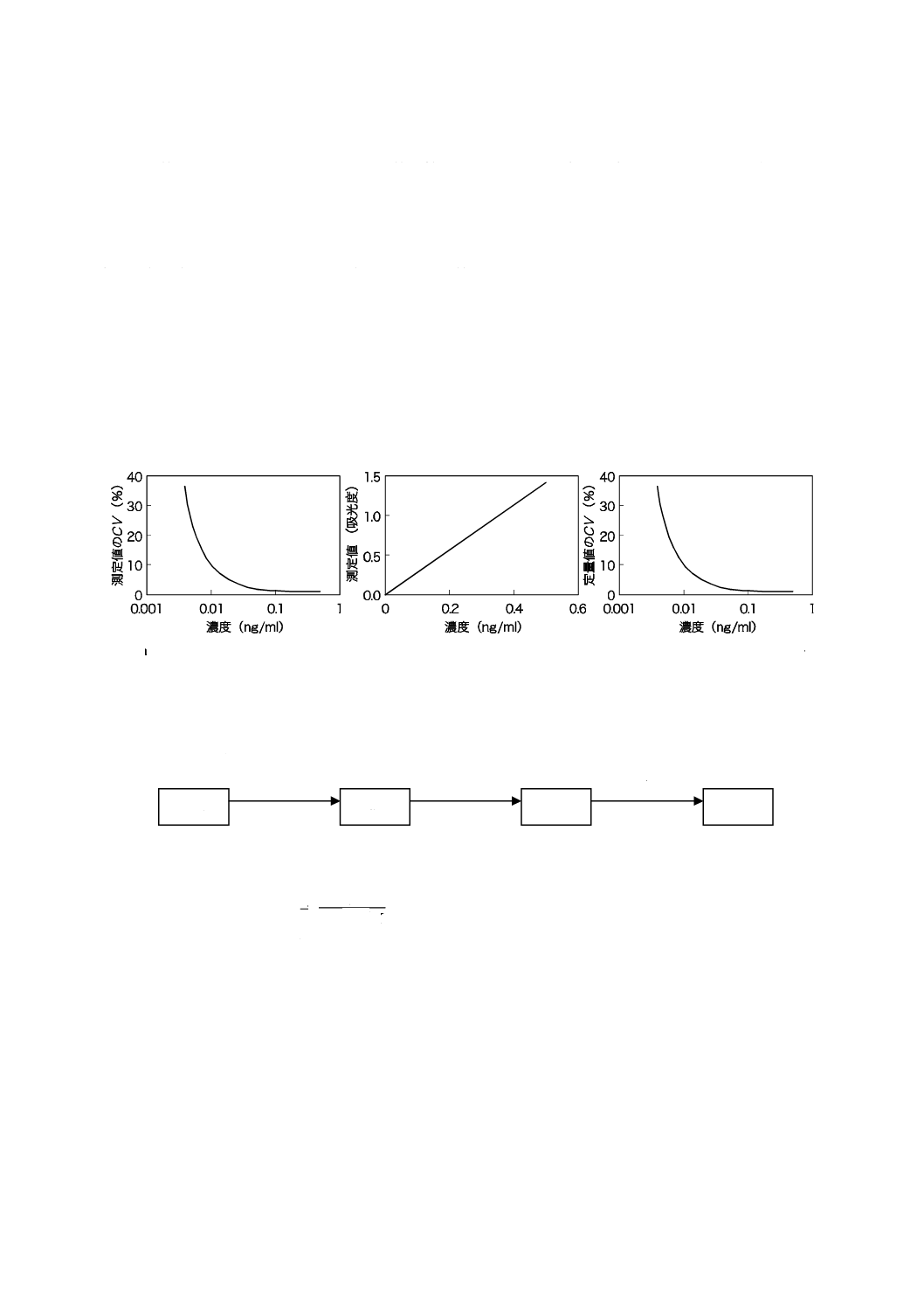
10.2 精度プロファイル
分析値の変動係数を分析対象成分の濃度に対してプロットした図を,精度プロファイルと定義する(参
考文献[1]参照)。精度プロファイルには,測定値の変動係数(CV)のプロット及び定量値の(CV)のプロ
ットの2種類がある。図1に,非競合免疫測定方法の典型的な精度プロファイルを示す。図1の場合は,
検量線が原点を通る直線であり,測定値の精度プロットと定量値の精度プロットとは同じである。
なお,精度プロットは,見やすくするために,横軸を対数目盛にしている。
a) 測定値の精度プロファイル b) 検量線 c) 定量値の精度プロファイル
図 1−非競合免疫測定方法(サンドイッチ法)の精度プロファイル
測定値のCVから定量値のCVへの変換は,検量線の微分係数を用いて,標準偏差(SD)間の変換を行い,
図2に示すように行う。
図 2−測定値のCVから定量値のCVへの変換
この変換は,次の式による。
(
)X
dX
dY
Y
r
r
m
c
/
=
ここに,
X: 定量値
Y: 測定値
rc: 定量値のCV
rm: 測定値のCV
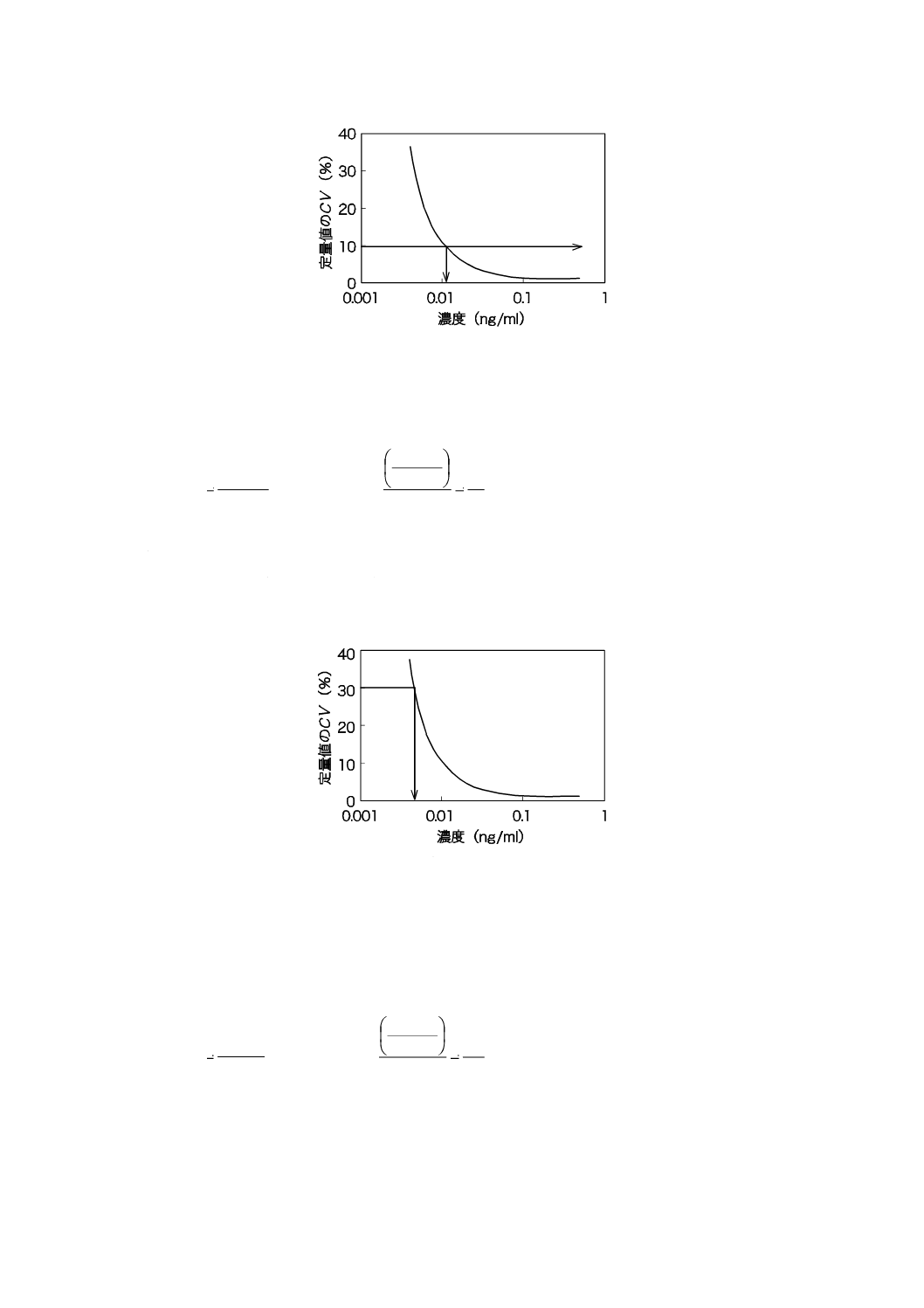
10.3 定量下限及び定量上限
定量下限とは,試料に含まれる分析対象成分の定量が可能な最小量又は最小濃度であり,定量上限とは,
定量が可能な最大量又は最大濃度である。定量値のCVが10 %を示す分析対象成分の量又は濃度を,そ
れぞれ定量下限及び定量上限とする。図3は,図1で示した精度プロファイルから求めた定量下限であり,
この場合,定量上限は濃度レンジの最高値となる。
測定値の
CV
定量値の
SD
測定値の
SD
定量値の
CV
×Y
÷X
÷dY/dX
7
K 0462:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
図 3−定量下限の求め方
注記 検量線が原点を通る直線となる場合は,定量下限及び定量上限(L)を測定値の標準偏差 sの10
倍とし,これを換算した濃度と定義すると,定量下限は,
dX
dY
s
L
/
10
=
となる。これを
10
1
/
=
L
dX
dY
s
と書き直すと,左辺は,定量下限又は定量上限の
濃度での定量値のCVを示し,右辺は10 %を示す。
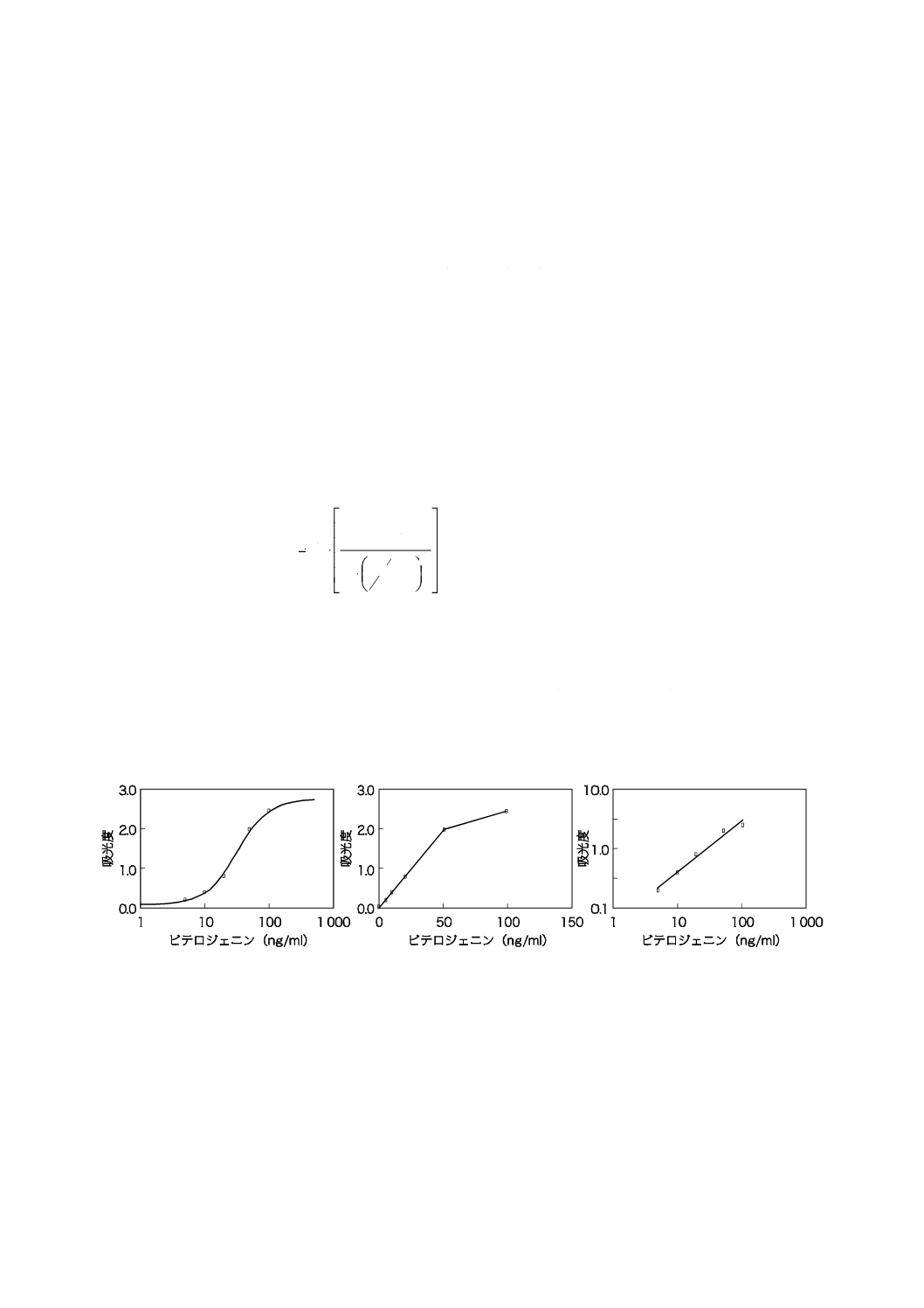
10.4 検出下限
検出下限とは,試料に含まれる分析対象成分の検出可能な最低の量又は濃度である。図4に示すように,
定量値のCVが30 %を示す目的値の量又は濃度を検出下限とする。
図 4−検出下限の求め方
もしも,定量値の精度プロファイルがU字曲線である場合には,検出下限は低濃度側とする。
注記 JIS K 0127に示す定量値の標準偏差と検量線の傾きとに基づく方法は,検量線が原点を通る直
線となる場合に用いられる。この定義では,検出下限Lを測定値の標準偏差 s の3.3倍とし,
これを検量線で換算した濃度と定義しており,検出下限は,
dX
dY
s
L
3.3
=
となる。これを
3.3
1
/
=
L
dX
dY
s
と書き直すと,左辺は検出限界濃度での定量値の
CVを示し,右辺は30 %を示し,この規格の定義と一致する。
10.5 他の分析方法との比較
既に他のJISに分析方法の規定がある場合には,それらの試験方法との比較を行うとよい。具体的には,
8
K 0462:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
既存測定系による同一の標準品を用いて得られた標準曲線,又は値の異なる幾つかの試料体(通常,3試
料体程度)の既存測定系での測定結果との比較を行い,その相関性を明らかにしておくことが望ましい。
11 計算
11.1 繰返し
測定の目的によって異なるが,繰返し測定を実施する場合,変動係数(CV)が10 %以下となるように行
うのがよい。望ましいCVによって繰返し数も規定される。各濃度のCVは,図3の精度プロファイルか
ら求め,これから繰返し数を決定する。
11.2 検量線
通常,4-パラメーターロジステイック(4-parameter logistic)回帰を使用するが,市販のキットには計算方
法の選択の指針が付いているのでその方法に従う。
次の式は,検量線の関数を得るのによく用いられ,4-parameter logistic回帰といわれる(参考文献[2]参照)。
また,その他の方法も利用可能である。例を,図5に示す。
+
−
+
=
b
d
a
d
y
50
IC
1
ρ
ρ
ここに,
y: 測定値
d: 曲線における下方漸近値
a: 曲線における上方漸近値
ρ: 分析対象成分の質量濃度
50
IC
ρ
: IC50における分析対象成分の質量濃度
b: IC50における曲線の傾き
図5−検量線の例
12 精度
免疫測定方法の性能の例を,附属書Bに示す。これは,異なった試料における試験室間の実験結果であ
る。
13 検査報告書
検査報告書には,次の事項を詳細に記載する。
9
K 0462:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
a) この規格の規格番号
b) 試料を特定するために必要な情報
c) 試料の前処理方法(必要な場合)
d) 9.8に規定する標準溶液(ゼロ標準を含む。)の検量線
e) 11.2の計算方法
f)
箇条10に規定する妥当性確認の表明
g) この手順からの逸脱及び結果に影響を及ぼし得るすべての状況の記述
h) 検査に用いた抗体の交差反応性
i)
JISなどで既に定められた分析方法がある場合は,その分析方法との比較結果

10
K 0462:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書A
(参考)
フローチャート
序文
この附属書は,非競合免疫測定方法(サンドイッチ法)におけるフローチャートを示すものであって,
規定の一部ではない。
A.1 フローチャート
非競合免疫測定方法(サンドイッチ法)におけるフローチャートを,図A.1及び図A.2に例示する。
抗体固相化担体(例 マイクロプレート)
↓
固相化抗体結合反応:試料(又は標準物質)を加え一定時間反応させる
↓
洗浄1:結合していない試料(又は標準物質)を除去する
↓
標識抗体結合反応:標識抗体を加え一定時間反応させる
↓
洗浄2:結合していない標識抗体を除去する
↓
酵素反応:酵素基質を加え一定時間反応させる
↓
(終末点法の場合)停止液を加える
↓
検出:シグナル強度を読み取る
↓
結果を計算する
図A.1−非競合免疫測定方法(サンドイッチ法)(2ステップ法)のフローチャートの例

11
K 0462:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
抗体固相化担体(例 磁性ビーズ)及び酵素標識抗体
↓
固相化抗体結合反応:試料(又は標準物質)及び標識抗体を加え一定時間反応させる
↓
洗浄:結合していない試料(又は標準物質),標識抗体を除去する
↓
酵素反応:酵素基質を加え一定時間反応させる
↓
(終末点法の場合)停止液を加える
↓
検出:シグナル強度を読み取る
↓
結果を計算する
図A.2−非競合免疫測定方法(サンドイッチ法)(1ステップ法)のフローチャートの例
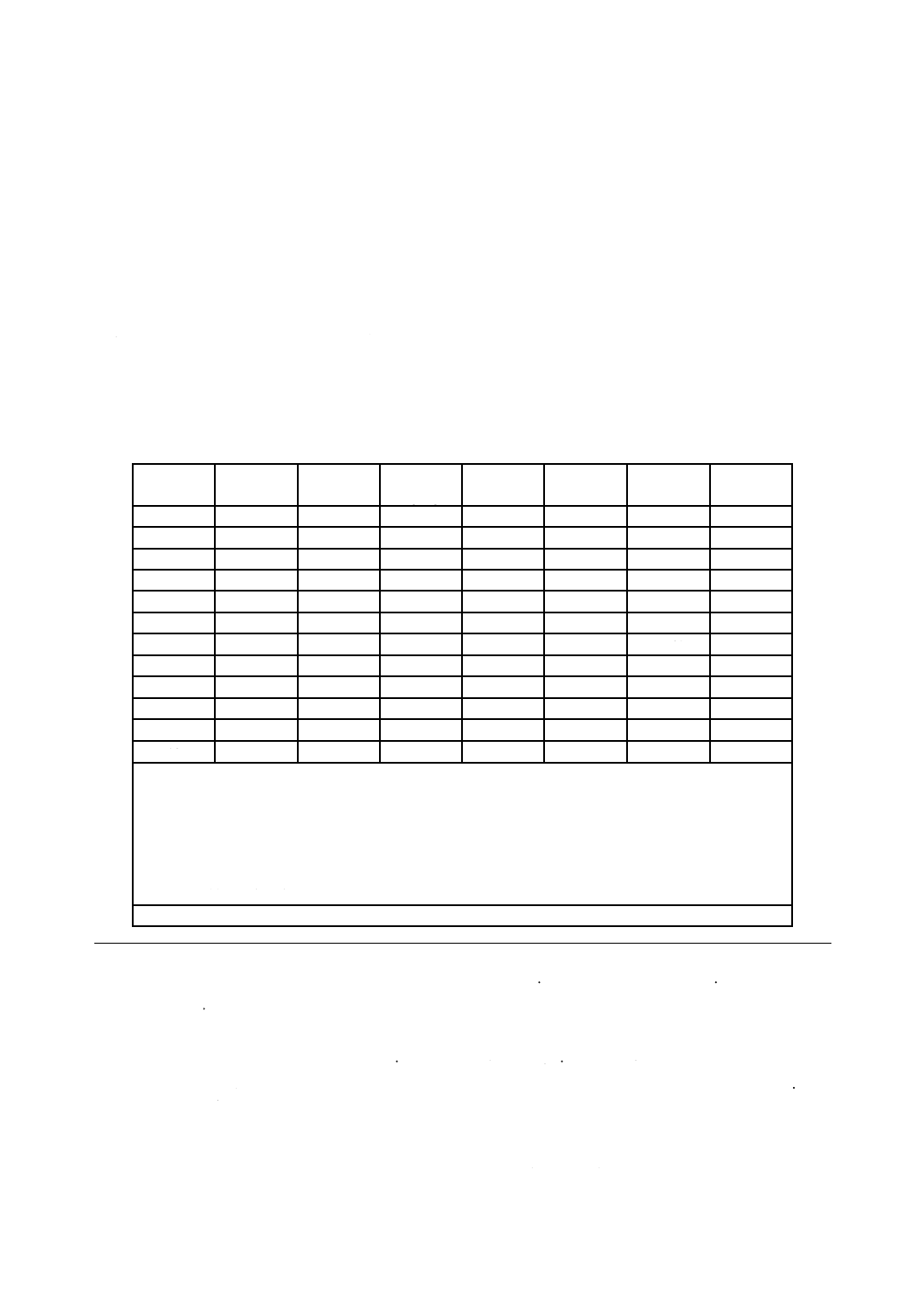
12
K 0462:2008
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書B
(参考)
試験室間試験から得られた精度データの例
序文
この附属書は,異なった試料における試験室間の実験結果を示すものであって,規定の一部ではない。
B.1
試験室間試験から得られた精度データ
表B.1に,めだか12個体からそれぞれ肝臓ホモジネートを調製し,非競合免疫測定方法を用いてビテロ
ジェニンの濃度を測定した試験室間試験から得られた精度データを示す(参考文献[3]参照)。
表B.1−試験室間試験から得られた精度データ
試料
l
n
X
ng/mg
σR
CVR
%
σr
CVr
%
1
5
10
0.57
0.12
21.1
0.069
12.1
2
5
10
3.3
1.24
37.7
0.094
2.8
3
5
10
3.3
1.29
38.6
0.15
4.6
4
5
10
15
2.32
15.8
1.00
6.8
5
5
10
19
3.04
16.0
0.85
4.5
6
5
10
55
15.5
28.2
5.85
10.6
7
5
10
69
22.9
33.2
5.41
7.8
8
5
10
111
24.6
22.2
6.88
6.2
9
5
10
125
14.4
11.5
15.3
12.2
10
5
10
180
45.1
25.1
9.37
5.2
11
5
10
210
25.6
12.5
26.5
12.9
12
5
10
810
229
28.3
45.5
5.6
l
試験室数
n
測定値の数
X
全平均値
σR
室間再現精度の標準偏差
CVR
室間再現精度の変動係数
σr
併行精度の標準偏差
CVr
併行精度の変動係数
試料:メダカ肝臓ホモジネート
参考文献
[1] Y. Hayashi, R. Matsuda, T. Maitani, K. Ito, W. Nishimura, K. Imai and M. Maeda; An expression of within-plate
uncertainty in sandwich ELISA., J. Pharm. Biomed. Anal., 36 (2004) 225-229.
[2] DUDLEY R.A.,EDWARDS P.,EKINS R.P.,FINNEY D.J., MCKENZIE I.G.M., RAAB G.M., RODBARD
D. and RODGERS R.P.C. ; Guidelines for immunoassay data processing. Clin. Chem., 31, 1995, pp. 1264-1271
[3] Tatarazako N., et al. Validation of an Enzyme-Linked Immunosorbent Assay Method for Vitellogenin in the
Medaka., Journal of Health Science., 50 (3), 2004, pp. 301-308
[4] JIS K 0127 イオンクロマトグラフ分析通則
[5] ISO/TR 13530 Water quality−Guide to analytical quality control for water analysis